Академический Документы
Профессиональный Документы
Культура Документы
3 - Cristales 2013 1
Загружено:
Hanover Pedro0 оценок0% нашли этот документ полезным (0 голосов)
23 просмотров127 страницОригинальное название
3_Cristales-2013-1
Авторское право
© Attribution Non-Commercial (BY-NC)
Доступные форматы
PPT, PDF, TXT или читайте онлайн в Scribd
Поделиться этим документом
Поделиться или встроить документ
Этот документ был вам полезен?
Это неприемлемый материал?
Пожаловаться на этот документАвторское право:
Attribution Non-Commercial (BY-NC)
Доступные форматы
Скачайте в формате PPT, PDF, TXT или читайте онлайн в Scribd
0 оценок0% нашли этот документ полезным (0 голосов)
23 просмотров127 страниц3 - Cristales 2013 1
Загружено:
Hanover PedroАвторское право:
Attribution Non-Commercial (BY-NC)
Доступные форматы
Скачайте в формате PPT, PDF, TXT или читайте онлайн в Scribd
Вы находитесь на странице: 1из 127
Ing.
Luis Alberto Sampn Alquizar
A
1
OBJETIVOS
Comprender los diferentes tipos de enlaces
atmicos.
Reconocer los diferentes tipos de estructura
cristalina.
Determinar caractersticas en las estructuras
cristalinas: cubica centrada en las caras y
cbica centrada en el cuerpo y hexagonal
compacta.
Distinguir los principales defectos cristalinos
y su influencia en los materiales.
Comprender como ocurre la deformacin
plstica en los metales.
2
1. Los enlaces interatmicos
2. La estructura cristalina
3. Estructuras cristalinas compactas
4. Direcciones y planos cristalogrficos
5. Difraccin de rayos X
6. Monocristales y policristales
3
1 Los enlaces interatmicos
Generalidades
- Para entender las propiedades
macroscpicas de los materiales es
necesario en muchas ocasiones saber
como estn los tomos unidos entre s
Por un lado hay que saber que fuerzas los unen
Y por otro lado como estn dispuestos entre s
4
1 Los enlaces interatmicos
Enlaces primarios
- Son enlaces bastante fuertes
- Se rompen a temperaturas de entre 1000 y 5000 K
- A esta categora pertenecen los enlaces
inicos, covalentes y metlicos
- Las cermicas y los metales estn
unidos exclusivamente por este tipo de
enlaces
5
1 Los enlaces interatmicos
Enlaces primarios / Enlace Inico
- Los xidos(Al
2
O
3
, MgO) y los
compuestos inicos (NaCl, LiF) estn
unidos mediante este tipo de enlace
- El caso ms tpico es el del Cloruro
Sdico (Sal comn)
6
1 Los enlaces interatmicos
Enlaces primarios / Enlace Inico
- Cloruro Sdico (NaCl)
Sodio (Na): 11 electrones
Cloro (Cl): 17 electrones
7
1 Los enlaces interatmicos
Enlaces primarios / Enlace Inico
- Energa de un enlace inico
TOTAL
Ionizacin
Atractivo
Repulsivo
8
Enlaces primarios / Enlace Inico
- Pese a que los electrones de los iones se
colocan en regiones de formas complejas
(orbitales) se puede considerar que el
enlace inico no es direccional
Geometra de algunos tipos de orbitales
1 Los enlaces interatmicos
9
Enlaces primarios / Enlace Covalente
- Aparece en diversos materiales:
Materiales puros con alto mdulo elstico (Diamante, Si, Ge)
Silicatos y vidrios (Rocas, ladrillos, cemento, ...)
Metales de alto punto de fusin (W, Mo, Ta)
Uniendo los tomos de Carbono de los polmeros
1 Los enlaces interatmicos
10
Enlaces primarios / Enlace Covalente
- El ejemplo ms sencillo corresponde al hidrgeno
- La proximidad de los tomos hacen que se
solapen los orbitales electrnicos reduciendo
la energa
1 Los enlaces interatmicos
11
- Energa de un enlace covalente (emprico)
TOTAL
Atractivo
Repulsivo
1 Los enlaces interatmicos
Enlaces primarios / Enlace Covalente
12
- El ejemplo ms relevante de enlace
covalente es el diamante (C)
- Enlaces fuertemente orientados
1 Los enlaces interatmicos
Enlaces primarios / Enlace Covalente
13
- Otros ejemplos de enlaces covalentes
Propano (C
3
H
8
) Agua (H
2
0) cido Actico
(CH3COOH)
1 Los enlaces interatmicos
Enlaces primarios / Enlace Covalente
14
- Es el principal (pero no el nico) enlace
presente en los metales
- Los electrones ms energticos abandonan
los tomos ionizndolos
- Estos electrones libres forman un nube que
rodea a los tomos
1 Los enlaces interatmicos
Enlaces primarios / Enlace Metlico
15
Enlaces primarios / Enlace Metlico
- La facilidad de movimiento del mar de
electrones facilita notablemente la
conductividad elctrica
- La curva de la energa del enlace es muy
similar a la mostrada para el enlace
covalente
- Los enlaces metlicos no son direccionales
- Al no tener enlaces direccionales los
tomos tienden a empaquetarse formando
estructuras de alta densidad
1 Los enlaces interatmicos
16
Enlaces secundarios
- Son enlaces dbiles
- Se disocian a temperaturas de entre 100 y 500 K
- A esta categora pertenecen las uniones de
Van der Waals y los puentes de hidrgeno
- Estos enlaces aparecen principalmente
en los polmeros y en los lquidos
1 Los enlaces interatmicos
17
- Estos enlaces, que unen las cadenas
polimricas entre s, hacen que el
polietileno(y otros polmeros) sean
slidos
- As mismo si este tipo de enlaces no
existiera el agua hervira a -80
0
C
1 Los enlaces interatmicos
Enlaces secundarios
18
Enlaces secundarios / Van der Waals
- Describe la atraccin que sufren los tomos
no cargados a causa de los dipolos que
aparecen espordicamente en su interior
1 Los enlaces interatmicos
19
- Energa de un enlace de Van der Waals es
TOTAL
Atractivo
Repulsivo
1 Los enlaces interatmicos
Enlaces secundarios / Van der Waals
20
- El nitrgeno lquido se mantiene en ese
estado a -198
0
C a causa de los enlaces de
Van der Waals
- Sin estos enlaces, la mayora de los gases
no se podran licuar y por lo tanto no se
podran separa industrialmente
1 Los enlaces interatmicos
Enlaces secundarios / Van der Waals
21
Enlaces secundarios / Puente de hidrgeno
- El enlace por puente de hidrgeno es el
encargado de mantener el agua lquida a
temperatura ambiente y de unir las
cadenas polimricas entre s
- La atraccin entre molculas se produce
cuando estas son dipolares
1 Los enlaces interatmicos
22
- Un ejemplo donde este tipo de enlace
es especialmente importante es el Hielo I
1 Los enlaces interatmicos
Enlaces secundarios / Puente de hidrgeno
23
Fuerzas interatmicas
- Conociendo el
potencial del enlace es
posible calcular la fuerza
asociada a este
mediante la expresin:
1 Los enlaces interatmicos
24
- Si se separan los tomos una pequea
distancia r-r
0
, la fuerza que aparece entre
ellos es proporcional a dicha distancia
- La rigidez del enlace se expresa como:
1 Los enlaces interatmicos
Fuerzas interatmicas
25
2 La estructura cristalina
Distribucin peridica de los tomos
Simetras
Los sistemas cristalinos
26
Distribucin peridica de los tomos
- Un cristal ideal se construye mediante la
infinita repeticin de unidades estructurales
idnticas
- En los cristales ms sencillos la
unidad
estructural es un solo tomo (Cu, Ag, Au,...)
- En muchos casos la unidad estructural
puede contener muchos tomos o molculas
2 La estructura cristalina
27
- Para una estructura cristalina fija es
posible escoger distintas celdas
primitivas, pero todas ellas contendrn el
mismo nmero de tomos
- La celda unidad convencional se elige de
forma que refleje la simetra del cristal
Distribucin peridica de los tomos
2 La estructura cristalina
28
- Como ejemplo; una celda que posea un tomo
en cada vrtice (cada uno compartido con 8
vecinos) tendr:
Distribucin peridica de los tomos
2 La estructura cristalina
29
- Un sistema cristalino puede presentar tres
tipos de simetra:
Simetras
2 La estructura cristalina
30
- La simetra traslacional se da en
estructuras peridicas
Simetras
2 La estructura cristalina
31
- La simetra rotacional se da cuando un
objeto coincide consigo mismo tras rotarlo
un ngulo de 360/n
Simetras
2 La estructura cristalina
32
- La simetra especular se da si existe un
plano imaginario que divide al cristal en dos
mitades simtricas
Simetras
2 La estructura cristalina
33
- Los sistemas cristalinos vienen definidos
por la simetra; no la forma de la celda
unidad.
- La forma de la celda unidad es una
consecuencia de la simetra.
Los sistemas cristalinos
2 La estructura cristalina
34
Los sistemas cristalinos
2 La estructura cristalina
35
- Todas estas redes pueden ser
combinadas con cuatro tipos de celdas
primitivas
Los sistemas cristalinos
2 La estructura cristalina
36
- Las combinaciones resultantes dan las 14
redes de Bravais
Los sistemas cristalinos
2 La estructura cristalina
37
3 Estructuras cristalinas compactas
Factor de empaquetamiento atmico
Cbica centrada en las caras (FCC)
Cbica centrada en el cuerpo (BCC)
Hexagonal compacto (HCP)
38
Factor de empaquetamiento atmico (APF)
- El APF es la fraccin volumtrica de una
estructura cristalina ocupada por los
tomos
- Es adimensional y menor de uno
- De forma prctica, el APF de una
estructura cristalina, se determina
suponiendo que los tomos son esferas
rgidas
3 Estructuras cristalinas compactas
39
- Factor de empaquetamiento atmico: 0.74
- Ejemplos: Al, Ag, Cu,
Cbica centrada en las caras (FCC)
3 Estructuras cristalinas compactas
40
- Factor de empaquetamiento atmico: 0.68
- Ejemplos: Na, Fe,
Cbica centrada en el cuerpo (BCC)
3 Estructuras cristalinas compactas
41
- Factor de empaquetamiento atmico: 0.74
- Ejemplos: Mg, C, Ti,
Hexagonal compacto (HCP)
3 Estructuras cristalinas compactas
42
3 Estructuras cristalinas compactas
Hexagonal compacto (HCP)
43
4 Direcciones y planos cristalogrficos
ndices de Miller
Direcciones cristalogrficas
Planos cristalogrficos
Aspectos grficos
Planos compactos
44
- Es un sistema de notacin cristalogrfica
para definir planos y direcciones en redes
cristalinas
- Direcciones y planos se representan por
grupos de tres nmeros enteros
4 Direcciones y planos cristalogrficos
ndices de Miller
45
- Una direccin cristalogrfica es una lnea
imaginaria que une nodos(tomos, iones o
molculas) de un cristal
- Notacin: [i j k] nica direccin
i j k Familia de direcciones
4 Direcciones y planos cristalogrficos
Direcciones cristalogrficas
46
- Planos cristalogrficos son planos ficticios que
unen nodos de la red
- Notacin:
(h k l) nico plano
{h k l} Familia de planos
4 Direcciones y planos cristalogrficos
Planos Cristalogrficos
47
- El plano (h k l) corta a los vectores primitivos
en a
1
/h, a
2
/k y a
3
/l, o algn mltiplo
4 Direcciones y planos cristalogrficos
Planos Cristalogrficos
48
- Ejemplos 3D
4 Direcciones y planos cristalogrficos
Planos Cristalogrficos
49
4 Direcciones y planos cristalogrficos
Planos Cristalogrficos
- Ejemplos 3D
50
- Para redes cbicas, la distancia entre dos
planos paralelos (h k l) es:
4 Direcciones y planos cristalogrficos
Planos Cristalogrficos
51
- Algunas propiedades de los materiales estn
directamente relacionadas con los planos y
direcciones cristalogrficas
Propiedades pticas
Adsorcin y reactividad
Tensin superficial
Dislocaciones y comportamiento plstico
4 Direcciones y planos cristalogrficos
Aspectos grficos
52
- Ciertos planos presentan un elevado grado
de empaquetamiento de tomos
- Estos planos tienen una gran importancia
para el fenmeno de la deformacin plstica
Cbica centrada en el cuerpo: {111}
Hexagonal compacta: {001} Plano basal
4 Direcciones y planos cristalogrficos
Planos compactos
53
5 Difraccin de Rayos X
Introduccin
Ley de Bragg
Condiciones de difraccin
Mtodos experimentales de
difraccin
Aplicaciones
54
- Es una tcnica para determinar el
ordenamiento de los tomos en el interior de
un cristal
- Esta informacin se obtiene a partir del modo
en que un haz de rayos X es dispersado por el
cristal
- Esta dispersin es consecuencia directa de la
disposicin peridica de los tomos
5 Difraccin de Rayos X
Introduccin
55
- Es una condicin necesaria para tener difraccin
5 Difraccin de Rayos X
Ley de Bragg
56
- Cbica simple:
Todos los planos (hkl) existentes
Planos (hkl) con h, k y l pares
Planos (hkl) con h, k y l impares
- Cbica centrada en el cuerpo (BCC):
Planos (hkl) que satisfagan que h+k+l par
5 Difraccin de Rayos X
Condiciones de difraccin
- Cbica centrada en las caras (FCC):
57
- Mtodo de Laue
La muestra ha de ser monocristalina y con espesor
menor de 1 mm
Emplea radiacin X policromtica
El cristal solo difractar longitudes de onda que
satisfagan la ley de Bragg para algn plano y ngulo
concretos
El patrn de difraccin se registra en una pelcula
colocada en frente (o detrs) de la muestra
5 Difraccin de Rayos X
Mtodos experimentales de difraccin
58
5 Difraccin de Rayos X
Mtodos experimentales de difraccin
- Mtodo de Laue
59
- Mtodo del cristal giratorio
La muestra es monocristalina menor de 1 mm
3
Se emplea un fuente de rayos X monocromtica
El monocristal solo difractara en los ngulo
que satisfagan la ley de Bragg para un cierto plano
La muestra se gira para obtener todos los
ngulos difractados
5 Difraccin de Rayos X
Mtodos experimentales de difraccin
60
5 Difraccin de Rayos X
Mtodos experimentales de difraccin
- Mtodo del cristal giratorio
61
- Mtodo de Debye-Scherrer
La muestra es policristalina (tpicamente polvo)
Se emplea una fuente de rayos X monocromtica
La muestra difractar todos los ngulos que
satisfagan la ley de Bragg
Solo se emplea en elementos con muy alta simetra
Muy til para identificar y analizar compuestos
5 Difraccin de Rayos X
Mtodos experimentales de difraccin
62
5 Difraccin de Rayos X
Mtodos experimentales de difraccin
- Mtodo de Debye-Scherrer
63
5 Difraccin de Rayos X
Mtodos experimentales de difraccin
- Mtodo de Debye-Scherrer (Cmara cilndrica)
64
5 Difraccin de Rayos X
Mtodos experimentales de difraccin
- Mtodo de Debye-Scherrer
65
- Determinacin de estructuras/redes cristalinas
- Determinacin de orientaciones cristalogrficas
- Determinacin de parmetro de red
- Identificacin y anlisis de compuestos
- Determinacin de tensiones en materiales
5 Difraccin de Rayos X
Aplicaciones
66
6 Monocristales y policristales
Ordenamientos atmicos
Monocristales
Policristales
67
Ordenamientos atmicos
- En los slidos es energticamente ms
estable disponer los tomos en redes
regulares que no guardar ningn orden
6 Monocristales y policristales
68
- El ordenamiento atmico es perfecto
- No hay interrupciones a lo largo de
todo el material
- No hay cambios en la orientacin de la red
- La forma macroscpica de un
monocristal puede reflejar o no la
simetra de la estructura cristalina
Monocristales
6 Monocristales y policristales
69
- Los monocristales son muy anistropos:
La anisotropa depender de la simetra
del cristal
- Ejemplo: El mdulo elstico del Cu es 66.7
GPa en la direccin [100], 130.3 GPa en la
direccin [110] y 191.1 GPa en la [111]
Monocristales
6 Monocristales y policristales
70
- Mtodos de produccin
Mtodo de Czochralsky
Monocristales
6 Monocristales y policristales
71
Monocristales
6 Monocristales y policristales
- Mtodos de produccin
Tcnica de Bridgeman
72
- Ejemplos de monocristales naturales
Monocristales
6 Monocristales y policristales
73
- Ejemplos de monocristales artificiales
Monocristales
6 Monocristales y policristales
74
- Aplicaciones tecnolgicas
Monocristales de Si en microelectrnica
Monocristales de Zafiro (Al2O3) para la industria del
lser
Monocristales de Fluorita (CaF2) para objetivos de
telescopios
Monocristales de superaleaciones de Ni para labes de
turbinas
Monocristales de Cu para cables de altas prestaciones
Monocristales
6 Monocristales y policristales
75
- La mayora de los slidos cristalinos
estn formados por pequeas
cristalitas
- La estructura del cristal es la misma en
cada una de las cristalitas, pero la
orientacin de la red vara de unas a
otras
- Estas cristalitas se denominan granos
Policristales
6 Monocristales y policristales
76
Policristales
6 Monocristales y policristales
77
Policristales
6 Monocristales y policristales
78
- Si todos los granos estn orientados
aleatoriamente los policristales se
comportan de forma istropa
- Muchas propiedades dependen del
tamao de grano
Policristales
6 Monocristales y policristales
79
7 Deformacin plstica
Metales Resistencia y ductilidad son
fuertemente controladas por la estructura
atmica y microestructura
Por ello es importante estudiar y entender con
claridad el mecanismo de control de estas
propiedades
Inicialmente deformacin de monocristales
Luego deformacin de policristales
Deformacin
Deformacin elstica completamente
recuperable al eliminarse el esfuerzo
Deformacin plstica no recuperable al
eliminarse el esfuerzo
7 Deformacin plstica
Desplazamiento atmico producido por un
esfuerzo cortante t :
c o E =
t G =
Mecanismos de deformacin plstica:
deslizamiento
maclado
deslizamiento en los lmites de grano
termofluencia difusional
Deslizamiento Movimiento paralelo de dos regiones
cristalinas adyacentes, una respecto a la otra, a travs
de algn plano (o planos)
Sistema de deslizamiento Es la combinacin de un
plano y una direccin que se halla sobre el plano, a lo
largo del cual se produce el deslizamiento
7 Deformacin plstica
Los planos compactos hacen
ms fcil el deslizamiento que
los planos alineados en otra
direccin respecto al esfuerzo
cortante
7 Deformacin plstica
Sistemas de deslizamiento ccc
a
Planos {111}
Direcciones <110>
7 Deformacin plstica
Sistemas de deslizamiento ccc
u
7 Deformacin plstica
Sistemas de deslizamiento
hc
7 Deformacin plstica
Deslizamiento ccc
a
7 Deformacin plstica
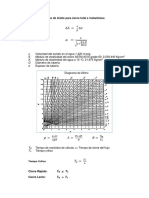
8 Resistencia de los metales
Esfuerzo cortante resuelto (factor de
Schmid)
Supngase un monocristal
cilndrico de un metal ccc
a
Tensin bajo una fuerza F
Deslizamiento
planos (111)
3 direcciones <110>
Resolver el esfuerzo
cortante sobre el plano
(111) y a lo largo de las
direcciones <110>
Cul es el esfuerzo cortante resuelto a lo largo de
una direccin
que hace un ngulo con el eje
de
tensin en el plano cuya normal
forma
un ngulo | con dicho eje?
A cos A
e
= |
2
a
4
A
t
=
b a
4
A
e
t
=
a cos b = |
cos F
8 Resistencia de los metales
Esfuerzo cortante resuelto (t
r
)
) cos (cos
A
F
r
| t =
e
r
A
cos F
t =
) FS (
r
o t =
o : esfuerzo de tensin y FS: factor de Schmid
8 Resistencia de los metales
Se ha encontrado que en un sistema de deslizamiento
se producir el deslizamiento cuando el esfuerzo
cortante resuelto en ese sistema alcance cierto valor
crtico
Al esfuerzo cortante resuelto requerido para iniciar el
deslizamiento sobre un sistema de deslizamiento
dado se le llama a menudo esfuerzo cortante crtico
resuelto (ECCR) y su valor depende en gran medida
de la pureza del metal (ver siguiente tabla)
8 Resistencia de los metales
Resistencia terica de los metales
8 Resistencia de los metales
Esfuerzo cortante terico
Es el esfuerzo cortante determinado
tericamente, capaz de producir el
deslizamiento de todos los tomos - de una
sola vez - que se hallan encima (o debajo)
del plano de deslizamiento, haciendo que se
desplacen permanentemente desde un
conjunto de sitios reticulares hasta otro
nuevo conjunto de sitios en la red
Cul es el esfuerzo cortante terico
necesario para producir un desplazamiento
permanente de los tomos?
8 Resistencia de los metales
a 2
b G
m
t
t =
Cul es la diferencia entre el esfuerzo cortante
crtico resuelto (ECCR) y el esfuerzo cortante de
terico (lmite elstico o lmite de fluencia) de los
metales? Porqu?
8 Resistencia de los metales
9 DEFECTOS CRISTALINOS
Una red cristalina ideal supone una posicin
tridimensional de repeticin perfecta
Los cristales de los metales reales tienen
varios defectos, stos se enlistan
sistemticamente como sigue:
1. Vacancias
2. tomos del metal (base) colocados en forma
intersticial
3. Un tomo extrao colocado en forma substitucional
4. Un tomo extrao colocado en forma intersticial
5. Dislocaciones
6. Maclas o fallas de apilamiento
7. Lmites de grano
8. Huecos o cavidades
9. Inclusiones
puntual
es
planare
s
de
volumen
lineales
Defectos puntuales
9 Defectos cristalinos
1. vacancia 4. tomo extrao intersticial
3. tomo extrao
pequeo sustitucional
3. tomo extrao
grande sustitucional
Dislocaciones de borde
9 Defectos cristalinos
9 Defectos cristalinos
9 Defectos cristalinos
9 Defectos cristalinos
Dislocacin de
tornillo o helicoidal
9 Defectos cristalinos
Dislocaciones
mixtas
Bandas y escalones de deslizamiento causadas
por el movimiento de dislocaciones (acero AISI
1010 - SEM)
9 Defectos cristalinos
10 Resistencia real de metales
Metales reales policristalinos
F
E
B
R
P
F
O
10 Resistencia real de los metales
Resistencia real f(densidad de
dislocaciones)
10 Resistencia real de los metales
Enmaraamiento de dislocaciones en lmites de
grano (TEM)
10 Resistencia real de los metales
11 Mecanismos de endurecimiento
Recuerdese que:
La deformacin plstica se debe al movimiento de
las dislocaciones
La resistencia a la fluencia de un metal (o
aleacin) usualmente se puede incrementar
mediante la introduccin de obstculos al
movimiento de dislocaciones
Tales obstculos pueden ser:
Enmaraamiento de dislocaciones
Lmites de grano
Estructuras cristalinas distorsionadas debido a
tomos de impureza
Pequeas partculas dispersas en la estructura
cristalina
11 Mecanismos de endurecimiento
Mtodos de endurecimiento de los metales
108
MTODO
CARACTERSTICA QUE IMPIDE EL
MOVIMIENTO DE DISLOCACIONES
Trabajo en fro
Elevadas densidades de dislocaciones producen
enmaraamientos
Afinamiento de grano
Cambios en la orientacin del cristal y otras
irregularidades en los lmites de grano
Fortalecimiento por
solucin slida
Impurezas intersticiales o substitucionales
distorsionan la estructura cristalina
Endurecimiento por
precipitacin
Partculas finas de un material duro precipitan fuera
de la solucin en el enfriamiento
Fases mltiples
Discontinuidades en los lmites de fase de una
estructura cristalina
Templado y revenido
Estructuras multifsicas de martensita y carburos
precipitados (Fe
3
C)
Trabajo en fro
Produce cambios en la microestructura y por
tanto en las propiedades:
cambio en la forma de grano
endurecimiento por deformacin y
un aumento en la densidad de dislocaciones
Una fraccin de la energa consumida en la
deformacin es almacenada en el metal como
energa de deformacin
la energa almacenada est asociada con las
concentraciones de tensiones (traccin,
compresin y cizalladura) alrededor de las
dislocaciones creadas
Adems, otras propiedades son modificadas
conductividad elctrica, resistencia a la corrosin,
etc.
11 Mecanismos de endurecimiento
comportamiento a traccin
11 Mecanismos de endurecimiento
Resistencia a la
traccin
11 Mecanismos de endurecimiento
Ductilidad Resistencia a la
fluencia
comportamiento a traccin
Recuperacin recristalizacin crecimiento
11 Mecanismos de endurecimiento
09/12/2013 jaasullcahuamn 113
NDICE > <
T recristalizacin
Trabajo en caliente
Trabajo en fro
+
recristalizacin
11 Mecanismos de endurecimiento
Afinamiento de grano
El tamao, o el dimetro medio, de los granos de un
metal policristalino afecta a las propiedades
mecnicas
El lmite de grano acta como barrera al movimiento
de dislocaciones por dos razones:
la posibilidad de que una dislocacin pase de un
grano a otro vecino se hace ms difcil a medida que
aumenta la diferencia en la orientacin (mayor
ngulo)
el desorden atmico en el lmite de grano producir
una discontinuidad de los planos de deslizamiento
de un grano a otro
Un material con grano fino es ms duro y resistente
que otro que tiene granos gruesos
material de grano fino tiene un rea total de lmite de
grano mayor para impedir el movimiento de las
dislocaciones
Control solidificacin, deformacin y
recristalizacin
11 Mecanismos de endurecimiento
115
12 Difusin en estado slido
La difusin es una forma de transporte de
masa
La difusin es la migracin de tomos a travs
de la red cristalina
no incluye los movimientos atmicos que se
producen en la deformacin plstica
Energa de activacin ( Q ). Generalmente un tomo
sustitucional requiere mayor energa que otro intersticial
12 Difusin en estado slido
Mecanismos de difusin
12 Difusin en estado slido
DIFUSIN SUBSTITUCIONAL
En el caso anterior no se mencion el
movimiento de difusin de los tomos de Fe , ya
que tal movimiento es insignificante comparado
con el de los tomos ms pequeos y ms
mviles del C .
Supngase, ahora, que el par de difusin est
formado por Cu y Ni (ver figura siguiente)
tomos casi del mismo tamao se disuelven
uno en otro como solutos substitucionales
Se espera que la movilidad de estos tomos
sea de casi el mismo orden de magnitud
Se debe considerar tanto la difusin del Cu
hacia la derecha como la del Ni hacia la
izquierda
12 Difusin en estado slido
Difusin substitucional
del par cobre-nquel. Al
final, los tomos de
cobre estn
uniformemente
distribuidos en todo el
nquel
12 Difusin en estado slido
CARBURIZACIN O CEMENTACIN
Supngase que una barra de Fe puro tiene
un extremo relleno con grafito y se calienta a
700C como se ilustra en la figura siguiente:
12 Difusin en estado slido
Considerando el elemento diferencial de volumen
para la difusin unidireccional del experimento
anterior:
Se puede demostrar la 2 ley de Fick :
t
C
]
Z
C
D [
Z
1 1
1
c
c
=
c
c
c
c
Es una ecuacin diferencial parcial de C
1
como variable
dependiente y Z y t como las dos variables
independientes C
1
= f(Z,t,D)
12 Difusin en estado slido
12 Difusin en estado slido
12 Difusin en estado slido
09/12/2013 jaasullcahuamn 124
NDICE > <
12 Difusin en estado slido
VARIABLES QUE INFLUYEN EN LA
DIFUSIN
Las variables que influyen en la difusin se
reflejan directamente en el coeficiente de
difusin D
El coeficiente de difusin D no es constante
D es una funcin de muchas variables, tales
como:
la temperatura
la concentracin
la estructura cristalina
las impurezas
el tamao de grano
Para un caso determinado se supone que estas
variables tienen valores especficos D es un
nmero
12 Difusin en estado slido
D es una funcin notable de la Temperatura
Donde D
o
, Q
y R son constantes
independientes de la temperatura
D
o
: factor de frecuencia frecuencia de
vibracin de los tomos que se difunden
Q : energa de activacin representa la medida
de la barrera de energa que tiende a impedir la
difusin
R : constante de los gases
T : temperatura absoluta (K)
RT
Q
e D D
o
=
12 Difusin en estado slido
Bibliografa
Lean, P. (2007). Introduccin a la ingeniera de
materiales. 1ra. Edi, Edit. PUCP, Lima, Per.
Smith, W. Hashemi, J. (2004). Fundamentos de
la ciencia e ingeniera de materiales. 4ta. Edi,
Edit. McGraw-Hill, Mxico D.F., Mxico.
Askeland, D. (2010). Fundamentos de ingeniera
y ciencia de materiales. 2da. Edi, Edit.
Cenagage Learning, Mxico D.F., Mxico.
Shackefolford, J. (1995). Ciencia de Materiales
para ingenieros. 3ra. Edi, Edit. Prentice Hill,
Mxico D.F., Mxico.
127
Вам также может понравиться
- Entregable 1 - Informe Mes 1Документ41 страницаEntregable 1 - Informe Mes 1Hanover PedroОценок пока нет
- Recibo Por HonorariosДокумент1 страницаRecibo Por HonorariosHanover PedroОценок пока нет
- Silabo 03Документ2 страницыSilabo 03Hanover PedroОценок пока нет
- RHE10471069090E0014Документ1 страницаRHE10471069090E0014Hanover PedroОценок пока нет
- CARTA N°01-2021 - O.S. SSJM210043Документ1 страницаCARTA N°01-2021 - O.S. SSJM210043Hanover PedroОценок пока нет
- Rendición de Cuentas Viaticos 1Документ29 страницRendición de Cuentas Viaticos 1Hanover PedroОценок пока нет
- Cuadro de Posiciones de Nuevas CámarasДокумент6 страницCuadro de Posiciones de Nuevas CámarasHanover PedroОценок пока нет
- Carta 1Документ1 страницаCarta 1Hanover PedroОценок пока нет
- Carta 7Документ1 страницаCarta 7Hanover PedroОценок пока нет
- Resumen de ViáticosДокумент3 страницыResumen de ViáticosHanover PedroОценок пока нет
- Factura Alimentación Oxxo1Документ1 страницаFactura Alimentación Oxxo1Hanover PedroОценок пока нет
- Factura Electrónica Restaurant CHEZ VictorДокумент1 страницаFactura Electrónica Restaurant CHEZ VictorHanover PedroОценок пока нет
- Teoría AllieviДокумент1 страницаTeoría AllieviHanover PedroОценок пока нет
- Grupo Termoelectrico TG5 Malacas PDFДокумент1 страницаGrupo Termoelectrico TG5 Malacas PDFHanover PedroОценок пока нет
- Factura Digital - Libre HotelДокумент1 страницаFactura Digital - Libre HotelHanover PedroОценок пока нет
- Carácterísticas de Cámaras Ip-Ptz RequeridasДокумент41 страницаCarácterísticas de Cámaras Ip-Ptz RequeridasHanover PedroОценок пока нет
- Embalse HuacracochaДокумент9 страницEmbalse HuacracochaHanover PedroОценок пока нет
- Grupo Termoelectrico TG6 MalacasДокумент1 страницаGrupo Termoelectrico TG6 MalacasHanover PedroОценок пока нет
- Toma de Decisiones Gerenciales Basadas en Contabilidad de CostosДокумент4 страницыToma de Decisiones Gerenciales Basadas en Contabilidad de CostosHanover PedroОценок пока нет
- Guía de Aprendizaje No. 7 de Química: Semana de Aplicación: Colegio Calendario Año Lectivo Grado Periodo DocenteДокумент6 страницGuía de Aprendizaje No. 7 de Química: Semana de Aplicación: Colegio Calendario Año Lectivo Grado Periodo DocenteSantiago GarciaОценок пока нет
- Examen de Admisión - 24-09Документ5 страницExamen de Admisión - 24-09Katherin MilagrosОценок пока нет
- Semana 01. TevДокумент66 страницSemana 01. TevEdwin CiriloОценок пока нет
- Las BiomoleculasДокумент3 страницыLas BiomoleculasDinelson Martínez TejadaОценок пока нет
- Electronica Orgánica.Документ154 страницыElectronica Orgánica.Luis Guillermo Durango100% (2)
- LECCIÓN 3 ActividadesДокумент6 страницLECCIÓN 3 Actividadesalba5ortiz0% (1)
- Serie 4 Problema Resuelto Lewis NomenclaturaДокумент9 страницSerie 4 Problema Resuelto Lewis NomenclaturaBts CoreaОценок пока нет
- Compuestos de Helio, Neón y Argón PDFДокумент13 страницCompuestos de Helio, Neón y Argón PDFRomario JulioОценок пока нет
- Word Agua (Clase 2)Документ30 страницWord Agua (Clase 2)Ulises Rosas GarcíaОценок пока нет
- Fundamentos de QuímicaДокумент111 страницFundamentos de QuímicaHaydelba D'Armas100% (2)
- (Química) .Doc Contenido CurricularДокумент13 страниц(Química) .Doc Contenido CurricularMara Campos FebresОценок пока нет
- Unidad I 2020Документ104 страницыUnidad I 2020MARCELO ORELLANA CARTAGENAОценок пока нет
- CERÁMICOSДокумент4 страницыCERÁMICOSjoshuaОценок пока нет
- Ejem 04 EnlacesДокумент7 страницEjem 04 EnlacesCatherine Magnolia Carrasco SuasacaОценок пока нет
- Tema 6 Química Del Carbono: Departamento F-Q IES Peset Aleixandre Mara Yuste VilaДокумент62 страницыTema 6 Química Del Carbono: Departamento F-Q IES Peset Aleixandre Mara Yuste VilaDaniela MártinaОценок пока нет
- Discusión N 1Документ5 страницDiscusión N 1nicОценок пока нет
- QUIMICA BASICA-para Fisicomecanicas-2k7-A-1 PDFДокумент3 страницыQUIMICA BASICA-para Fisicomecanicas-2k7-A-1 PDFJose Javier Marquez PradaОценок пока нет
- Anexo 2 - Tarea 3Документ20 страницAnexo 2 - Tarea 3Edgar PerezОценок пока нет
- Semana (6) - Geometria Molecular y Polaridad Molecular PDFДокумент17 страницSemana (6) - Geometria Molecular y Polaridad Molecular PDFNoelia Eva Castillo LlicaОценок пока нет
- Control de Lectura Grupo 13Документ6 страницControl de Lectura Grupo 13Tatiana AragónОценок пока нет
- Reporte 3 QIДокумент4 страницыReporte 3 QIFernando CanoОценок пока нет
- Química Del Carbono: Prof. Carla FavaloroДокумент12 страницQuímica Del Carbono: Prof. Carla Favaloromicaela carreraОценок пока нет
- Comportamiento de La Fuerza EléctricaДокумент4 страницыComportamiento de La Fuerza EléctricaIgnacio Fuentes100% (1)
- Guia QuímicaДокумент116 страницGuia Químicamaria jose murciaОценок пока нет
- 04 Enlace Quimico CuestionarioДокумент4 страницы04 Enlace Quimico CuestionarioAnonymous Azo0o0aoZОценок пока нет
- Parametros de EnlaceДокумент2 страницыParametros de EnlaceAngel MedranoОценок пока нет
- REFZ. 3°FGHI Sem.22 III BIM 2Документ2 страницыREFZ. 3°FGHI Sem.22 III BIM 2Trisoline Centeno EngilyОценок пока нет
- Conceptos Generales de QuímicaДокумент3 страницыConceptos Generales de QuímicaStephany BecerrilОценок пока нет
- Propiedades de Los Compuestos Ionicos Covalentes y MetalicosДокумент6 страницPropiedades de Los Compuestos Ionicos Covalentes y Metalicosjeremias33% (3)
- Cuestionario 2do Tema Juan RuizДокумент21 страницаCuestionario 2do Tema Juan Ruizvicente camacaroОценок пока нет