Академический Документы
Профессиональный Документы
Культура Документы
Diapositivas
Загружено:
Katherin P. Parra MercadoАвторское право
Доступные форматы
Поделиться этим документом
Поделиться или встроить документ
Этот документ был вам полезен?
Это неприемлемый материал?
Пожаловаться на этот документАвторское право:
Доступные форматы
Diapositivas
Загружено:
Katherin P. Parra MercadoАвторское право:
Доступные форматы
14
mayo 2015
Solubilidad
Universidad del Atln/co
PRODUCTO
DE
SOLUBILIDAD
Constante
del
producto
de
solubilidad,
(KPS)
Clculo
del
KPS
a
par/r
de
la
solubilidad
(s)
Clculo
de
s
a
par/r
del
KPS
Criterios
para
la
formacin
de
un
precipitado,
producto
inico
(P.I.)
Factores
que
afectan
la
solubilidad
y
KPS
de
sales
poco
solubles
Efecto
del
ion
comn,
del
ion
diverso,
del
pH
Titulaciones
con
formacin
de
precipitados
Curva
de
/tulacin
para
los
procesos
de
precipitacin
Determinacin
del
punto
nal.
evertmendozacolina@gmail.com
A+
(ac)
+
AB
(s)
Universidad
del
Atln/co
Producto de solubilidad
AB (s)
Ejemplo:
BaSO4
2+
2
+
SO4(ac)
Ba(ac)
BaSO4(s)
Universidad del Atln/co
En general, el producto de solubilidad de un compuesto es el
producto de las concentraciones molares de los iones
cons/tuyentes, cada una elevada a la potencia de su
coeciente en la ecuacin de equilibrio.
+ B (ac)
A+ (ac)
AB (s)
La constante del producto de solubilidad, kps, es la constante
de equilibrio, para el equilibrio que se establece entre un
soluto slido y sus iones en una disolucin saturada.
kps =
Lic. Evert Mendoza Colina Msc.
A+
(ac)
B
(ac)
Universidad del Atln/co
Lic. Evert Mendoza Colina Msc.
14 mayo 2015
Ejemplo
kps = s2
B
(ac)
0
s
s
=
kps
Lic.
Evert
Mendoza
Colina
Msc.
Escriba la expresin de la constante del producto de
solubilidad para el equilibrio de solubilidad del cloruro de
plata y bromuro cuproso.
kps = Ag+ Cl
kps = Cu+ Br
AgCl (s)
Ag+
(ac)
+
Cl (ac)
CuBr (s)
Cu+
(ac)
+
Br (ac)
CaCO3(s)
Ca2+
(ac)
+
CO2
3(ac)
Universidad del Atln/co
kps = Ca2+ CO3
Lic. Evert Mendoza Colina Msc.
PRODUCTO DE SOLUBILIDAD
A+
(ac)
0
s
PRODUCTO DE SOLUBILIDAD
Un electrolito es una sustancia que al disolverse en agua, da
lugar a la formacin de iones. Los electrolitos pueden ser
dbiles o fuertes, segn estn parcial o totalmente ionizados
o disociados en medio acuoso, dependiendo de la proporcin
en que se encuentren los componentes pueden ser /po AB,
A2B, AB2, A3B, AB3, etc.
1. En un electrolito del /po AB el equilibrio de solubilidad viene
determinado por:
Universidad del Atln/co
14 mayo 2015
Electrolitos
AB
(s)
c
I
E
c
kps
=
s
x
s
PRODUCTO DE SOLUBILIDAD
B (ac)
PRODUCTO DE SOLUBILIDAD
A idn/ca situacin de equilibrio, se llega si el compuesto AB
se forma al mezclar disoluciones inicas de compuestos
solubles que con/enen los iones A+ y B por separado:
+
14 mayo 2015
Equilibrios de precipitacin
A+
(ac)
B
(ac)
Lic.
Evert
Mendoza
Colina
Msc.
14 mayo 2015
PRODUCTO DE SOLUBILIDAD
Se dene la solubilidad (s) como la mxima can/dad de soluto
disuelto permi/da por litro de disolucin, a una temperatura
dada.
Hay dos formas de expresar la solubilidad de una sustancia:
como solubilidad molar, que es el nmero de moles de soluto
en un litro de disolucin saturada, y como solubilidad, que es
el nmero de gramos de soluto en un litro de disolucin.
Todas las sustancias en mayor o menor grado son solubles en
agua. Incluso las sustancias denominadas, insolubles,
experimentan el equilibrio de solubilidad:
14 mayo 2015
14 mayo 2015
2. En un electrolito del /po A2B el equilibrio de solubilidad
viene determinado por:
+ B 2
2A+ (ac)
A2B (s)
(ac)
Cul ser la solubilidad molar del fosfato de calcio?
kpsCa3(PO4)2 = 1,2x10-26.
I
E
c
c
kps
=
(2s)2
x
s
0
2s
kps
=
4s3
0
s
s
=
kps
4
3
La
misma
expresin
ser
para
el
/po
AB2
Universidad del Atln/co
I
E
Ca3(PO4)2 3Ca2+ + 2PO43
c
0
0
c
3s
2s
kps = (3s)3 x (2s)2
kps = 108s5
5 1,2x1026
s
=
Lic.
Evert
Mendoza
Colina
Msc.
108
s
=
5
kps
108
s = 2,56x106 M
Universidad del Atln/co
14 mayo 2015
Ejercicio
Ejercicio
Universidad del Atln/co
kps = Ca2+ SO4
AgBr(s)
Ag+
+
Br
c
c
I
E
kps
=
s
x
s
kps
=
7,7
x
1013
kps = s2
0
s
s
=
kps
s = 7,7x1013
s = 8,8 x 107
kps
=
2,4x105
Lic.
Evert
Mendoza
Colina
Msc.
Universidad del Atln/co
14 mayo 2015
Lic. Evert Mendoza Colina Msc.
10
14 mayo 2015
Precipitacin total
Ejemplo
11
Ba2+
+
SO4
2-
Ba(SO4)(s)
El
nmero
de
moles
de
Ba2+
presentes
en
los
200
mL
de
la
disolucin
inicial
es:
PRODUCTO DE SOLUBILIDAD
Lic. Evert Mendoza Colina Msc.
Exactamente 200 mL de BaCl2 0,0040 M se agregan a 600 mL
exactos de K2SO4 0,0080 M. Se formar algn precipitado?
PRODUCTO DE SOLUBILIDAD
Del conocimiento de las reglas de solubilidad y de los
productos de solubilidad, es fac/ble predecir si se formar un
precipitado cuando se mezclan dos disoluciones o se agregue
un compuesto soluble a una disolucin.
La prediccin de la formacin de precipitados son alta u/lidad
en la industria qumica, en los laboratorios qumicos e
inclusive en la medicina.
Al comparar el producto inico (Qps)de una disolucin, con el
producto de solubilidad (kps) de la misma, se pueden
presentar tres situaciones a tener en cuenta:
Si Qps > kps hay precipitado, si Qps = kps no hay precipitado y si
Qps < kps no hay precipitado.
Universidad del Atln/co
0
s
PRODUCTO DE SOLUBILIDAD
0,67 g CaSO4 x 1 mol CaSO4 = 4,9x103 mol/L CaSO
4
1 L
136,2 g CaSO4
El bromuro de plata se u/liza en emulsiones fotogrcas. Cul es
la solubilidad molar del AgBr?
PRODUCTO DE SOLUBILIDAD
El sulfato de calcio se emplea como agente desecante y para
fabricar pinturas, cermicas y papel. El yeso de paris es una
forma hidratada del sulfato de calcio que se u/liza para hacer la
frula para los huesos rotos.
De manera experimental se encontr que la solubilidad del
sulfato de calcio es de 0,67 g/L. Calcule el valor de la kps para
este compuesto.
3)
kps
=
(4,9x103)
(4,9x10
Lic. Evert Mendoza Colina Msc.
14 mayo 2015
2
CaSO4(s)
Ca2+
+
SO4(ac)
(ac)
PRODUCTO DE SOLUBILIDAD
Ejemplo
PRODUCTO DE SOLUBILIDAD
Producto de solubilidad
1
L
8,0x104
molBa2+
nBa2+
=
200
ml
x
x
0,0040
mol
Ba
=
1000
ml
1
L
El
volumen
total
despus
de
combinar
las
dos
disoluciones
es
de
800
mL,
y
la
concentracin
de
Ba2+
en
este
volumen
es:
8,0x104
molBa2+x
1000
ml
=
1,0x103
M
Ba2+
Ba2+
=
800
ml
1
L
Universidad
del
Atln/co
Lic. Evert Mendoza Colina Msc.
12
14 mayo 2015
14 mayo 2015
El nmero de moles de SO42 presentes en los 600 mL de la
disolucin inicial es:
2
1 L
nSO42 = 600 ml x
x 0,0080 mol SO4 = 4,8x103 mol SO42
1000 ml
1 L
Se aaden tres gotas de KI 0,20M a 100,0 mL de Pb(NO3)2 0,010
M. Se formar un precipitado de PbI2?
(suponga que 1 gota = 0,05 mL) kps= 7,1x10-9.
PbI2(s) Pb2+ + 2 I
Necesitamos encontrar la concentracin del I procedente del KI.
0,05 ml
1 molI
nI = 3
x 0,20 molKI x
gotas x
x 1 L
1 gota 1000 ml
1 molKI
1 L
3,0x105 mol I
5 mol I
I =
I = 3,0x104 M
nI = 3,0x10
0,10015 L
2
2
2+
x
Q =
Pb
I
Qps=
0,0099
x
3,0x104
Qps=
8,9x1010
ps
Como
Qps
<
kps
entonces
no
precipitar.
El volumen total despus de combinar las dos disoluciones es de
800 mL, y la concentracin de SO42- en este volumen es:
4,8x103 molSO42x
1000 ml = 6,0x103 M SO 2
SO42 = 800 mL
4
1 L
6 M
3) (6,0x10
3) =
6,0x10
Qps= Ba2+ x SO42 = (1,0x10
Ahora se deben comparar Qps y kps
Qps= 6,0x106 M kps= 1,1x1010 M Qps> kps Precipitar
Universidad del Atln/co
Lic. Evert Mendoza Colina Msc.
13
Universidad del Atln/co
14 mayo 2015
Lic. Evert Mendoza Colina Msc.
Se aade lentamente AgNO3 a una disolucin que con/ene iones
de Cl y Br en concentracin 0,020 M para cada ion. Calcule la
concentracin de los iones Ag+ necesarios para iniciar la
precipitacin del AgBr sin que precipite el AgCl.
kps(AgCl)= 1,6 x 10-10 y kps(AgBr)= 7,7 x 10-13
Dado que la kps del AgBr es menor que la del AgCl, el bromuro
precipitar primero.
Para el AgBr se escribe:
k
Ag+ = ps
kps= Ag+ x Br
Br
13
7,7
x
1
0
Ag+ = 0,020
Ag+ = 3,9 x 1011 M
15
Universidad del Atln/co
14 mayo 2015
Lic. Evert Mendoza Colina Msc.
Si a una disolucin saturada de un electrolito poco soluble
aadimos otra sustancia que aporta uno de los iones, la
concentracin de ste aumentar.
Lgicamente, la concentracin del otro ion deber disminuir
para que el producto de las concentraciones de ambos
permanezca constante.
Como el equilibrio se desplaza a la izquierda la solubilidad,
que mide la mxima concentracin de soluto disuelto,
disminuir en consecuencia.
Es decir, el efecto que /ene aadir un ion comn es,
entonces, una disminucin de la solubilidad de la sal en
disolucin.
Ag+
1,6
x
1010
=
0,020
kps
Cl
Ag+ = 8,0 x 109 M
Para
precipitar
el
AgBr
sin
que
precipiten
los
iones
Cl,
el
valor
de
Ag+
debe
ser
mayor
que
3,9x10-11
y
menor
que
8,0x10-9
M.
Universidad del Atln/co
Lic. Evert Mendoza Colina Msc.
17
Universidad del Atln/co
Lic. Evert Mendoza Colina Msc.
PRODUCTO DE SOLUBILIDAD
Para el AgCl se escribe:
PRODUCTO DE SOLUBILIDAD
Efecto del ion comn
Ag+ =
16
14 mayo 2015
Ejemplo
kps= Ag+ x Cl
PRODUCTO DE SOLUBILIDAD
Es una tcnica en la que dos o ms iones en disolucin, todos
ellos capaces de precipitar con un reac/vo comn, se separan
mediante ese reac/vo: un ion precipita mientras que el otro o
los otros permanecen en disolucin.
La condicin principal para una buena precipitacin
fraccionada es que haya una diferencia signica/va en las
solubilidades de las sustancias que se van a separar.
La clave de esta tcnica es la adicin lenta de una disolucin
concentrada del reac/vo precipitante a la disolucin donde
debe producirse la precipitacin.
PRODUCTO DE SOLUBILIDAD
Ejemplo
Lic. Evert Mendoza Colina Msc.
14
14 mayo 2015
Precipitacin fraccionada
Universidad del Atln/co
PRODUCTO DE SOLUBILIDAD
Ejemplo
PRODUCTO DE SOLUBILIDAD
Ejemplo
18
14 mayo 2015
14 mayo 2015
Cul es la solubilidad molar del PbI2 en KI(ac) 0,10 M?
Kps(PbI2) = 7,1 x 10-9.
PbI2(s) Pb2+ + 2I -
Cul ser la solubilidad del cloruro de plata si aadimos nitrato
de plata, sal soluble, hasta una concentracin nal 0,002 M?
AgCl(s) Ag+ + Cl-
I
c
0
0
E
c
s
s
I
C
E
c
c
c
0
s
s
2
0,10
2s
0,10+2s
2
kps= Pb2+ x I
7,1x109
=
s
x
0,10+2s
2
7,1x109
=
s
x
0,10
Universidad
del
Atln/co
s =
7,1x109
2
0,10
kps=
Ag+
x
Cl
1,7
x
1010
Cl
=
0,0020
s = 7,1x107 M
Lic. Evert Mendoza Colina Msc.
s = 1,7x1010
kps = 1,7 x 1010
19
s = 1,3 x 105 M
Cl =
kps
Ag+
Cl = 8,5 x 108 M
Universidad del Atln/co
Lic. Evert Mendoza Colina Msc.
14 mayo 2015
Demuestre por qu el Mg(OH)2 se disuelve cuando se mezcla
con una disolucin cida.
Los iones hidrxido procedentes del Mg(OH) 2 disuelto
reaccionan con los iones H3O+ para formar H2O.
Mg(OH)2(s) Mg2+ + 2 OH
2OH(ac) + 2 H3O+(ac) 4 H2O(l)
De acuerdo con el principio de Le Chtelier se espera que la
reaccin se desplace hacia la derecha, es decir, se disuelva ms
Mg(OH)2 para remplazar los iones OH eliminados por reaccin
de neutralizacin.
21
Universidad del Atln/co
Lic. Evert Mendoza Colina Msc.
14 mayo 2015
Ejemplo
kps=
1,8x1011
K = (1,8x1011) x (1,0x1028)
K
=
1,8x1017
El
valor
grande
de
K
para
la
reaccin
indica
que
la
reaccin
se
produce
prc/camente
por
completo
y
que
el
Mg(OH)2
es
muy
soluble
en
disolucin
cida.
Universidad
del
Atln/co
Lic.
Evert
Mendoza
Colina
Msc.
NH3(ac) + H2O NH42+(ac) + OH(ac)
E
kb =
0,10
NH4
OH
1,8x105 =
x
x
x
x
x
=
1,3x103
NH3
0,10
Ahora
podemos
plantear
de
nuevo
la
cues/n
original:
precipitar
el
Mg(OH)2
en
una
disolucin
en
la
que
Mg2+=0,010M
y
OH=1,3x10-3M?.
Debemos
comparar
Qps,
con
kps.
2
2
Qps=
Mg2+
x
OH
Qps=
0,010
x
1,3x103
Qps=
1,7x108
Qps=
1,7x108
M
kps=
1,8x1011
M
Qps>
kps
23
Universidad del Atln/co
PRODUCTO DE SOLUBILIDAD
kps= 1,0x1028
Mg(OH)2(s) + 2 H3O+ Mg2+(ac) + 4 H2O(l) K = ?
K = kpsx k
Precipitar el Mg(OH)2(s) en una disolucin que es 0,010 M en
MgCl2 y adems 0,10 M en NH3?
PRODUCTO DE SOLUBILIDAD
2OH(ac) + 2 H3O+(ac) 4 H2O(l)
22
14 mayo 2015
Ejemplo
El resultado que obtenemos es:
Mg(OH)2(s) Mg2+ + 2 OH
PRODUCTO DE SOLUBILIDAD
El pH de una disolucin puede afectar mucho la solubilidad de
una sal. Esto es especialmente acusado cuando el anin de la
sal es la base conjugada de un cido dbil o la misma base
OH.
Equilibrio solubilidad: AB(s) A(ac) + B+(ac)
Equilibrio acidez: HA(ac) A (ac) + H+(ac)
Si el anin A en que se disocia un electrolito poco soluble
forma un cido dbil HA, al aumentar la acidez o [H+] el
equilibrio de disociacin del cido se desplazar hacia la
izquierda.
En consecuencia, disminuir [A], con lo que se solubilizar
ms electrolito AB.
PRODUCTO DE SOLUBILIDAD
Ejemplo
Lic. Evert Mendoza Colina Msc.
20
14 mayo 2015
Solubilidad y pH
Universidad del Atln/co
PRODUCTO DE SOLUBILIDAD
Ejercicios
PRODUCTO DE SOLUBILIDAD
Ejemplo
Precipitar
Lic. Evert Mendoza Colina Msc.
24
14 mayo 2015
14 mayo 2015
Suele producirse a par/r de sales solubles que con/enen el
ca/n NH4+.
NH4Cl(s) Cl-(ac) + NH4+(ac)
Equil base: NH4OH(ac) NH4+ (ac) + OH(ac)
Los NH4+ reaccionan con los OH formndose NH4OH al
desplazar el equilibrio de la base hacia la izquierda.
Es el mtodo usual de disolver hidrxidos poco solubles tales
como el Mg(OH)2.
Equil. Solub.: Mg(OH)2(s) Mg2+(ac) + 2 OH(ac)
En consecuencia, disminuir [OH], con lo que se solubilizar
ms Mg(OH)2.
Un ion complejo es un ion formado por ms de un tomo o
grupo de tomos.
Ejemplos: [Al(OH)4],[Zn(CN)4]2,[AlF6]3,[Ag(NH3)2]+.
De esta manera, se pueden disolver precipitados aadiendo,
por ejemplo, cianuro de sodio a electrolitos insolubles de cinc
como el Zn(OH)2, ya que al formarse el ca/n [Zn(CN)4]2,que
es muy estable. As, disminuir drs/camente la
concentracin de Zn2+, con lo que se disolver ms Zn(OH)2.
Igualmente, pueden disolverse precipitados de AgCl
aadiendo amoniaco.
Universidad del Atln/co
Lic. Evert Mendoza Colina Msc.
25
Universidad del Atln/co
14 mayo 2015
Lic. Evert Mendoza Colina Msc.
Las reacciones usadas en volumetra deben ser
estequiomtricas; para que una reaccin de precipitacin sea
estequiomtrica no deben ocurrir fenmenos de
coprecipitacin en extensin apreciable.
Los hidrxidos y xidos metlicos recin precipitados suelen
adsorber can/dades variables de iones OH-, S=, HS-, y es
comn la precipitacin simultnea de xidos e hidrxidos o
sulfuro y sulfuro cido.
27
Universidad del Atln/co
14 mayo 2015
Curva de Titulacin
Calcular la curva terica de la siguiente /tulacin:
La curva de /tulacin es un grco de valores calculados de
pCl o de pAg en funcin del volumen de reac/vo (VAg) que se
ha adicionado. La /tulacin pasar por las siguientes etapas:
1) VAg = 0 : solucin original de NaCl
2) VAgCAg < VClCCl: precipitado de AgCl en equilibrio con una
solucin que con/ene un exceso de iones Cl-
3) VAgCAg = VClCCl : p.e., precipitado de AgCl en equilibrio con una
solucin en la que ambos iones estn a igual concentracin (el
precipitado es la nica fuente para ambos iones).
PRODUCTO DE SOLUBILIDAD
PRODUCTO DE SOLUBILIDAD
Como durante la /tulacin la concentracin de ambos iones
vara a lo largo de varios rdenes de magnitud, adoptaremos
una expresin similar al pH:
pCl = - log [Cl-] pAg = - log [Ag+]
28
14 mayo 2015
Clculo de la curva de /tulacin de NaCl
con AgNO3
VCl = 50.00 mL CCl = 0.1 M (en el Erlenmeyer)
VAg : variable CAg = 0.1 M (en la bureta)
Lic. Evert Mendoza Colina Msc.
PRODUCTO DE SOLUBILIDAD
En este curso se han visto numerosos ejemplos de reacciones
de precipitacin; muchas sirven para la iden/cacin o
separacin de iones metlicos y algunas son u/lizables en
mtodos gravimtricos; pero son muy escasas las reacciones
de precipitacin aptas para el desarrollo de mtodos
volumtricos.
Las reacciones usadas en volumetra deben ser rpidas,
alcanzando su equilibrio en forma casi instantnea; de otro
modo la /tulacin se torna excesivamente lenta. Las
reacciones de precipitacin suelen completarse lentamente.
PRODUCTO DE SOLUBILIDAD
Volumetra de precipitacin
Lic. Evert Mendoza Colina Msc.
26
14 mayo 2015
Volumetra de precipitacin
Universidad del Atln/co
PRODUCTO DE SOLUBILIDAD
Formacin de un complejo estable
PRODUCTO DE SOLUBILIDAD
Solubilidad y base dbil
4) VAgCAg > VClCCl : precipitado de AgCl en equilibrio con una
solucin que con/ene un exceso de iones Ag+.
Universidad del Atln/co
Lic. Evert Mendoza Colina Msc.
29
Universidad del Atln/co
Lic. Evert Mendoza Colina Msc.
30
14 mayo 2015
14 mayo 2015
Curva
de
Titulacin
Debemos
calcular
pCl
o
pAg
para
cada
etapa.
[Cl-] = CCl = 0.1 M. En este punto pCl = 1
Y si bien pAg no est vsicamente denido, a los efectos de
construir la curva podemos calcular pAg= 9.75 - 1
pAg = 8.75
Universidad del Atln/co
Lic. Evert Mendoza Colina Msc.
2) VAgCAg < VClCCl
En esta regin tenemos un precipitado de AgCl en equilibrio
con una solucin que con/ene al exceso de cloruro. La
concentracin de cloruro en solucin puede considerarse
como la suma del exceso ms el aporte de cloruro debido a la
solubilidad del AgCl:
[Cl-] = [Cl-]exceso + [Cl-]del precipitado
[Cl-]exceso = {(VClCCl - VAgCAg) / (VCl + VAg)}
31
Universidad del Atln/co
14 mayo 2015
33
Si
VAg
=
20
mL
[Cl-]=[(50x0.1-20x0.1)/(50+20)]+1.7810-10/[Cl-]
[Cl-]=
0.0429
+
1.78
10-10/[Cl-]
Si
despreciamos
el
segundo
sumando
el
resultado
es
0.0429;
si
lo
mantenemos
y
resolvemos
la
ecuacin
de
segundo
grado
[Cl-]2
-
0.0429
[Cl-]
-
1.78
10-10
=
0
el
resultado
es
tambin
0.0429.
O
sea,
pCl
=
1.37
pAg
=
9.75
-
1.37
=
8.38
Universidad del Atln/co
14 mayo 2015
Curva de Titulacin
Universidad del Atln/co
Lic. Evert Mendoza Colina Msc.
35
Si
VAg
=
40
mL
[Cl-]=[(50x0.1-40x0.1)/(50+40)]+1.7810-10/[Cl-]
[Cl-]=
0.011
+
1.78
10-10/[Cl-]
Si
despreciamos
el
segundo
sumando
el
resultado
es
0.011;
si
lo
mantenemos
y
resolvemos
la
ecuacin
de
segundo
grado
[Cl-]2
-
0.0250
[Cl-]
-
1.78
10-10
=
0
el
resultado
es
tambin
0.011.
O
sea,
pCl
=
1.95
pAg
=
9.75
1.95
=
8.00
Universidad del Atln/co
Lic. Evert Mendoza Colina Msc.
PRODUCTO DE SOLUBILIDAD
Si
VAg
=
30
mL
[Cl-]=[(50x0.1-30x0.1)/(50+30)]+1.7810-10/[Cl-]
[Cl-]=
0.0250
+
1.78
10-10/[Cl-]
Si
despreciamos
el
segundo
sumando
el
resultado
es
0.0250;
si
lo
mantenemos
y
resolvemos
la
ecuacin
de
segundo
grado
[Cl-]2
-
0.0250
[Cl-]
-
1.78
10-10
=
0
el
resultado
es
tambin
0.0250.
O
sea,
pCl
=
1.60
pAg
=
9.75
1.60
=
8.14
PRODUCTO DE SOLUBILIDAD
34
14 mayo 2015
Curva de Titulacin
Lic. Evert Mendoza Colina Msc.
PRODUCTO DE SOLUBILIDAD
Adems, como por cada mol de AgCl que se disuelve se
produce 1 mol de cada ion, y como la nica fuente de iones
Ag+ a la solucin es la disolucin del precipitado, ser
[Cl-]del precipitado = [Ag+] = Kps / [Cl-]
donde con [Cl-] volvemos a signicar la concentracin total de
cloruro, dado que es sta quien regula a la concentracin de
plata. Remplazando se ob/ene:
[Cl-] = {(VClCCl - VAgCAg) / (VCl + VAg)} + Kps /[Cl-]
PRODUCTO DE SOLUBILIDAD
Curva de Titulacin
Lic. Evert Mendoza Colina Msc.
32
14 mayo 2015
Curva de Titulacin
Universidad del Atln/co
Lic. Evert Mendoza Colina Msc.
PRODUCTO DE SOLUBILIDAD
1) VAg = 0 Cuando no se ha adicionado reac/vo ser:
PRODUCTO DE SOLUBILIDAD
Curva de Titulacin
36
14 mayo 2015
14 mayo 2015
Si
VAg
=
49.99
mL
[Cl-]=[(50x0.1-49.99x0.1)/(50+49.99)]+1.7810-10/[Cl-]
[Cl-]=
10-5
+
1.78
10-10/
[Cl-]
Si
despreciamos
el
segundo
sumando
el
resultado
sera
10-5;
pero
ahora
la
ecuacin
de
segundo
grado
es
[Cl-]2
-
10-5
[Cl-]
-
1.78
10-10
=
0
cuya
resolucin
resulta
en
[Cl-]
=
1.92
10-5.
O
sea
que
en
puntos
muy
cercanos
al
p.e.
la
ecuacin
que
slo
toma
en
cuenta
al
exceso
acarrea
serios
errores.
En
este
punto
ser
pCl
=
4.72
y
pAg
=
9.75
-
4.72
=
5.03.
3)
VAgCAg
=
VClCCl
En
el
p.e.
no
existe
exceso
de
reac/vo
ni
de
analito,
y
todo
el
cloruro
y
la
plata
(AgCl)
que
hay
en
solucin
proviene
exclusivamente
de
la
disolucin
del
precipitado;
como
ste
origina
igual
nmero
de
ambos
iones,
en
el
p.e.
ser
[Cl-]=[Ag+],
y
tendremos
Kps=[Cl-][Ag+]=[Cl-]2=
[Ag+]2
[Cl-]=[Ag+]=(Kps)1/2
=1.3310-5
pAg
=
pCl
=
4.87
Notar
que
el
valor
de
pCl
y
de
pAg
en
el
p.e.
es
independiente
de
la
concentracin
de
la
muestra
y
del
reac/vo.
Universidad del Atln/co
Lic. Evert Mendoza Colina Msc.
37
Universidad del Atln/co
14 mayo 2015
Lic. Evert Mendoza Colina Msc.
En analoga con lo ya visto, el segundo sumando slo deber
ser tomado en consideracin en la cercana inmediata del p.e.
(por ejemplo para VAg = 50.01 mL).
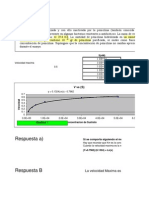
Los valores de pAg y de pCl fueron calculados para toda la
/tulacin en la forma descripta y se han gracado en la Figura
en funcin de Vag.
Interesa mencionar que la curva iden/cada como pCl
coincide con los valores de pAg que se calcularan para una
/tulacin de AgNO3 0.1 M contra NaCl 0.1 M.
39
14 mayo 2015
Curva de Titulacin
PRODUCTO DE SOLUBILIDAD
Universidad del Atln/co
Lic. Evert Mendoza Colina Msc.
41
Universidad del Atln/co
Lic. Evert Mendoza Colina Msc.
PRODUCTO DE SOLUBILIDAD
4) VAgCAg > VClCCl
Pasado el p.e. tendremos un precipitado en equilibrio con una
solucin que con/ene un exceso de Ag+.
La concentracin total de plata ahora ser:
[Ag+] = [Ag+]exceso + [Ag+]del precipitado
[Ag+]exceso = {(VAgCAg VClCCl)/(VCl + VAg)}
[Ag+]del precipitado = [Cl-] = Kps / [Ag+]
pues ahora la nica fuente para el cloruro en solucin es la
disolucin del precipitado.
[Ag+]={(VAgCAgVClCCl)/(VCl + VAg)} + Kps / [Ag+]
PRODUCTO DE SOLUBILIDAD
Curva de Titulacin
Lic. Evert Mendoza Colina Msc.
38
14 mayo 2015
Curva de Titulacin
Universidad del Atln/co
PRODUCTO DE SOLUBILIDAD
Curva de Titulacin
PRODUCTO DE SOLUBILIDAD
Curva de Titulacin
40
Вам также может понравиться
- Elaboracion de Mermelada de UvaДокумент9 страницElaboracion de Mermelada de UvaDante Fernandez GallardoОценок пока нет
- Practica 8 PDFДокумент4 страницыPractica 8 PDFArantxa EscobedoОценок пока нет
- Derecho Civil Obligaciones II Acción Pauliana y OblicuaДокумент9 страницDerecho Civil Obligaciones II Acción Pauliana y OblicuaKatherin P. Parra MercadoОценок пока нет
- Practica de Acidos Duros y BlandosДокумент8 страницPractica de Acidos Duros y BlandosLordvaako103Оценок пока нет
- S4 Reacciones Quimicas y EstequiometríaДокумент33 страницыS4 Reacciones Quimicas y EstequiometríaMarino GuerreroОценок пока нет
- VOLUMETRÍAДокумент8 страницVOLUMETRÍAKarl BeltranОценок пока нет
- Para BioquimicaДокумент7 страницPara Bioquimicacristhian10_00Оценок пока нет
- Guia de Moles 10Документ9 страницGuia de Moles 10RICARDO SUAREZ MEDINA100% (2)
- 02 - La Materia - RespuestasДокумент10 страниц02 - La Materia - RespuestasemiОценок пока нет
- Proyecto de Irrigacion-PonazaДокумент83 страницыProyecto de Irrigacion-Ponazavalles19100% (1)
- Qgii Tabla FC 1 PDFДокумент2 страницыQgii Tabla FC 1 PDFRonaldo BrionesОценок пока нет
- Lab N° 12 Propiedades de Los Là - QuidosДокумент11 страницLab N° 12 Propiedades de Los Là - Quidosjoel berrioОценок пока нет
- Informe Guía 1Документ19 страницInforme Guía 1Luis Carlos Bacca OcampoОценок пока нет
- Experimento No. 8Документ10 страницExperimento No. 8Maria MarcucciОценок пока нет
- Práctica 13 Reacciones Sucesivas de Cobre 2017 1Документ7 страницPráctica 13 Reacciones Sucesivas de Cobre 2017 1Erick Armando0% (1)
- Disoluciones Que Conducen ElectricidadДокумент11 страницDisoluciones Que Conducen ElectricidadGeancarlos Solis AlvaresОценок пока нет
- SensibilidadДокумент11 страницSensibilidadRoxii WojtuñОценок пока нет
- Reactivo LimitanteДокумент25 страницReactivo LimitanteClodoveo MartinezОценок пока нет
- Tipos de ReaccionesДокумент7 страницTipos de ReaccionesFabian Amed BeleñoОценок пока нет
- Historia Acidos y BasesДокумент30 страницHistoria Acidos y BasesOv Verónica100% (1)
- Lab 6Документ17 страницLab 6Ayrton Jimenez InfantesОценок пока нет
- Reporte de Practica # 8Документ4 страницыReporte de Practica # 8UnTipoRaroMas :0Оценок пока нет
- Informe Nº5 - Laboratorio #3 Disoluciones-1Документ26 страницInforme Nº5 - Laboratorio #3 Disoluciones-1Antonio Javier Pérez NavarroОценок пока нет
- Practica 5Документ7 страницPractica 5Eduardo TrejoОценок пока нет
- Determinacion de La Formula de Un Compuesto de Yoduro de CobreДокумент3 страницыDeterminacion de La Formula de Un Compuesto de Yoduro de CobreRoberto SánchezОценок пока нет
- Ejercicios Quimica 1,2 Y3Документ2 страницыEjercicios Quimica 1,2 Y3carolinaОценок пока нет
- Reactivo Limitante y en ExcesoДокумент33 страницыReactivo Limitante y en ExcesoAgu NunesОценок пока нет
- Laboratorio #5Документ10 страницLaboratorio #5Katherine Julissa Pabilo DavisОценок пока нет
- Transformaciones de CobreДокумент3 страницыTransformaciones de CobreCésar Flores RíosОценок пока нет
- Practica 13 Ley de La ConservacionДокумент3 страницыPractica 13 Ley de La ConservacionCristian ArámbulaОценок пока нет
- Taller de Enlaces Químicos Geometría Resonancia PolaridadДокумент2 страницыTaller de Enlaces Químicos Geometría Resonancia PolaridadLili OliverosОценок пока нет
- Uso y Manejo Del Mechero de Bunsen y La BalanzaДокумент4 страницыUso y Manejo Del Mechero de Bunsen y La Balanzalopez internetОценок пока нет
- Laboratorio de PHДокумент11 страницLaboratorio de PHMariaFrancisca Labbé AguileraОценок пока нет
- Ley de La Conservacion de La MateriaДокумент15 страницLey de La Conservacion de La MateriaDiego Alejandro Urbina MolinaОценок пока нет
- Nunero 4Документ7 страницNunero 4luceroОценок пока нет
- Práctica Reactivo LimitanteДокумент4 страницыPráctica Reactivo LimitanteGiuliana Orduña Amado0% (1)
- Tarea 1 Parcial 1 MauricioCruzДокумент3 страницыTarea 1 Parcial 1 MauricioCruzMauricio CruzОценок пока нет
- Tema 6. Ácidos y Bases PDFДокумент28 страницTema 6. Ácidos y Bases PDFsefogomezОценок пока нет
- Modelo Atómico de Bohr. Niveles de EnergíaДокумент5 страницModelo Atómico de Bohr. Niveles de EnergíalujulОценок пока нет
- Practica 6 Capacidad TérmicaДокумент4 страницыPractica 6 Capacidad TérmicaNorma Elena100% (3)
- Práctica 11 ReporteДокумент4 страницыPráctica 11 ReportePauLCОценок пока нет
- Informe SoluciónДокумент11 страницInforme SoluciónRafael Ricardo GarciaОценок пока нет
- Reporte Fuerzas Intermoleculares2Документ14 страницReporte Fuerzas Intermoleculares2Juana CruzОценок пока нет
- Titulacion Acido BaseДокумент3 страницыTitulacion Acido BaseAlexander MeraОценок пока нет
- Complejos Cu (II) - OxalatoДокумент6 страницComplejos Cu (II) - OxalatoAna Fernanda Leyva MinorОценок пока нет
- Reporte Práctica 12. Solubilidad de Sales en Agua.Документ9 страницReporte Práctica 12. Solubilidad de Sales en Agua.Allison VRОценок пока нет
- Inorganica 4Документ6 страницInorganica 4emilyОценок пока нет
- Pendu LoДокумент5 страницPendu LoAllenОценок пока нет
- Reporte Experimental QuelatoДокумент9 страницReporte Experimental QuelatoEdgar ArmandoОценок пока нет
- Práctica: Reacción Del Haloformo Sobre La AcetofenonaДокумент7 страницPráctica: Reacción Del Haloformo Sobre La AcetofenonaMaria Gabriela Martinez GonzalezОценок пока нет
- Estado GaseosoДокумент176 страницEstado GaseosoJesusAlejandroОценок пока нет
- Análisis de ResultadosДокумент3 страницыAnálisis de ResultadosChaampii Fernando Alderete Cruz100% (1)
- Reporte Practica 5Документ9 страницReporte Practica 5Ricardo CruzОценок пока нет
- Informe 7 InorganicaДокумент13 страницInforme 7 InorganicaYeniz Yanez Pantoja0% (1)
- Práctica 8 Reacción QuímicaДокумент13 страницPráctica 8 Reacción QuímicaIVANA SANJUAN SANJUANОценок пока нет
- Previo Practica 8Документ27 страницPrevio Practica 8JAMJ2001 Two TimerОценок пока нет
- Informe N 4 Quimica UnmsmДокумент7 страницInforme N 4 Quimica UnmsmJordy Ynquilla0% (1)
- Quimica 2001. Soluciones 6 ModelosДокумент25 страницQuimica 2001. Soluciones 6 ModelosfranjosevaОценок пока нет
- Laboratorio 2 Ley de Conservación de La Materia e Identificación de Sustancias Por Sus PropiedadesДокумент4 страницыLaboratorio 2 Ley de Conservación de La Materia e Identificación de Sustancias Por Sus Propiedadestaniarom14Оценок пока нет
- VELOCIDAD DE REACCIÓN ENZIMÁTICA Y DETERMINACIÓN DEL Pi DE UNA PROTEÍNAДокумент13 страницVELOCIDAD DE REACCIÓN ENZIMÁTICA Y DETERMINACIÓN DEL Pi DE UNA PROTEÍNAFernanda CarrilloОценок пока нет
- Tema 6, Tema 7 Alquinos SN1 y SN2 20 Mayo 2020Документ17 страницTema 6, Tema 7 Alquinos SN1 y SN2 20 Mayo 2020Alan YañezОценок пока нет
- Tabla Periódicas y Prop. (Fund. Teórico)Документ4 страницыTabla Periódicas y Prop. (Fund. Teórico)mariaОценок пока нет
- La nanotecnología: El mundo de las máquinas a escala nanométricaОт EverandLa nanotecnología: El mundo de las máquinas a escala nanométricaОценок пока нет
- KpsДокумент4 страницыKpssalvagriegoОценок пока нет
- Derecho Comercial Titulos ValoresДокумент4 страницыDerecho Comercial Titulos ValoresKatherin P. Parra MercadoОценок пока нет
- Diseño de Instrumentos de Evaluación Act 1Документ2 страницыDiseño de Instrumentos de Evaluación Act 1Katherin P. Parra MercadoОценок пока нет
- Interpretación Constitucional y Argumentación en La Decision JudicialДокумент2 страницыInterpretación Constitucional y Argumentación en La Decision JudicialKatherin P. Parra MercadoОценок пока нет
- Guias Tercer y Cuarto PeriodoДокумент4 страницыGuias Tercer y Cuarto PeriodoKatherin P. Parra MercadoОценок пока нет
- Determinación de Sulfatos en El AguaДокумент10 страницDeterminación de Sulfatos en El Agualb_BotsОценок пока нет
- Enalapril de Portugues TraducidoДокумент16 страницEnalapril de Portugues TraducidoMilagros CinthyaОценок пока нет
- Calculadora de CloraciónДокумент6 страницCalculadora de CloraciónAngel J. PanduroОценок пока нет
- FloculaciónДокумент18 страницFloculaciónEvelyn Carolina GavilanezОценок пока нет
- Marcha Analitica Determinacion de Proteinas Por Metodo BradforДокумент7 страницMarcha Analitica Determinacion de Proteinas Por Metodo BradforRober ParedesОценок пока нет
- Articul - Guia Clasificación Zonas Riesgo Por Gases Inflamables - 2Документ7 страницArticul - Guia Clasificación Zonas Riesgo Por Gases Inflamables - 2jaboneteОценок пока нет
- Actividad CamaroneraДокумент23 страницыActividad CamaroneraBecky Valencia Rivera100% (1)
- Ejercicios de Química General I (Oct 05)Документ16 страницEjercicios de Química General I (Oct 05)Jorman Medina100% (1)
- 04 - A Cálculo de Dosificación de Cloro - 2016Документ11 страниц04 - A Cálculo de Dosificación de Cloro - 2016Christian Alcántara HerediaОценок пока нет
- Apretam EMДокумент5 страницApretam EMarguijОценок пока нет
- Ac BaseДокумент3 страницыAc BaseFélix José Silva UrbanoОценок пока нет
- Fds g3 Fregasuelos HigienizanteДокумент9 страницFds g3 Fregasuelos HigienizantejesusОценок пока нет
- Banco de Preguntas de QuímicaДокумент91 страницаBanco de Preguntas de Químicaluisernestohernandezperez230% (1)
- Coleccion Ejercicios - AnaliticaДокумент19 страницColeccion Ejercicios - AnaliticamadecarupuОценок пока нет
- Deshidratación Gas NaturalДокумент15 страницDeshidratación Gas NaturalVanessa Sandoval AguileraОценок пока нет
- Detectores HPLCДокумент3 страницыDetectores HPLCAna Isabel Arias BarreraОценок пока нет
- Termo Met Extrac 1Документ33 страницыTermo Met Extrac 1Juan Alvarado ZegarraОценок пока нет
- Determinación de Magnesio y Sodio en Cerveza y Determinación de Hierro en Una Llave de Latón Por La Técnica de Absorción y Emisión Atómica A La LlamaДокумент8 страницDeterminación de Magnesio y Sodio en Cerveza y Determinación de Hierro en Una Llave de Latón Por La Técnica de Absorción y Emisión Atómica A La LlamaMiguelangelLeonОценок пока нет
- Clases y Formacion de MineralesДокумент31 страницаClases y Formacion de MineralesalexanderОценок пока нет
- Cómo Puedes Conocer La Concentración Del Ácido AcéticoДокумент2 страницыCómo Puedes Conocer La Concentración Del Ácido AcéticoDavid SorianoОценок пока нет
- Concentracion GravimetricaДокумент16 страницConcentracion GravimetricaMitch Laguna94% (17)
- Nuevos Tipos de Hidrociclones (18 Pag.)Документ18 страницNuevos Tipos de Hidrociclones (18 Pag.)mirtre9912Оценок пока нет
- Pickles Casero y Bajo Nivel ProductivoДокумент19 страницPickles Casero y Bajo Nivel Productivoyanina itati0% (1)
- 3 Disoluciones 1Документ47 страниц3 Disoluciones 1Juan Varg ReОценок пока нет
- Practica 8 Term oДокумент8 страницPractica 8 Term oJorge Moreno50% (2)
- Utilizacion de Pinturas y SolventesДокумент63 страницыUtilizacion de Pinturas y SolventesRodrigo Quispe SuneОценок пока нет
- El Solvente o Disolvente Es La Fase Dispersora y Constituye La Mayor Parte de La SoluciónДокумент3 страницыEl Solvente o Disolvente Es La Fase Dispersora y Constituye La Mayor Parte de La SoluciónIsabel GomeszОценок пока нет