Академический Документы
Профессиональный Документы
Культура Документы
Ecuaciones de Estado
Загружено:
Any SanchezИсходное описание:
Оригинальное название
Авторское право
Доступные форматы
Поделиться этим документом
Поделиться или встроить документ
Этот документ был вам полезен?
Это неприемлемый материал?
Пожаловаться на этот документАвторское право:
Доступные форматы
Ecuaciones de Estado
Загружено:
Any SanchezАвторское право:
Доступные форматы
ECUACIONES DE ESTADO
TERMODINAMICA I
“AÑO DE LA CONSOLIDACIÓN ECONÓMICA Y SOCIAL DEL PERÚ”
Universidad nacional
“SAN LUIS GONSAGA” DE ICA
FACULTAD DE INGENIERÍA QUÍMICA
ECUACIONES DE ESTADO
CURSO : TERMODINÁMICA I
DOCENTE : MAG. ROSALIO CUSI PALOMINO
ALUMNA : SANCHEZ ESCOBAR ANALY
AÑO : VI - CICLO
TURNO : TARDE
ICA – PERÚ
2010
SANCHEZ ESCOBAR ANALY FAC.
DE INGENIERIA QUIMICA
ECUACIONES DE ESTADO
TERMODINAMICA I
INTRODUCCIÓN
En física y química, una ecuación de estado es una ecuación constitutiva para
sistemas hidrostáticos que describe el estado de agregación de la materia
como una relación matemática entre la temperatura, la presión, el volumen, la
densidad, la energía interna y posiblemente otras funciones de estado
asociadas con la materia.
En sistemas de un componente y de una fase, una ecuación de estado es la
relación que existe entre dos o más propiedades termodinámica. la ecuación de
estado incluirá tres propiedades, dos de las cuales pueden ser consideradas
como independientes. Aunque en principio se podrían plantear relaciones
funcionales en que intervengan tres propiedades termodinámicas cualesquiera,
las expresiones analíticas de las relaciones entre propiedades han sido
limitadas casi completamente a la presión, volumen y temperatura. Debido a la
incompleta comprensión de las interacciones intermoleculares, especialmente
en los estados líquido y sólido, han sido utilizados métodos empíricos para
desarrollar muchas de las ecuaciones de estado de uso general. Dado que la
presión, temperatura y volumen pueden ser medidos directamente, los datos
necesarios para evaluar las constantes en tales ecuaciones pueden ser
obtenidos experimentalmente.
La elección de la ecuación a usar en una aplicación dada depende
principalmente de la exactitud deseada y de la capacidad del usuario. Como los
coeficientes de casi todas las ecuaciones de estado deben ser evaluados
ajustando o adaptando las ecuaciones a diversos datos experimentales de
presión, volumen y temperatura, estas ecuaciones nunca pueden representar
exactamente los datos experimentales; más aun, muchas veces estas
ecuaciones no representan los datos, limitando la exactitud. Esto es
particularmente cierto cuando las ecuaciones más sencillas son aplicadas en la
vecindad del punto crítico.
SANCHEZ ESCOBAR ANALY FAC.
DE INGENIERIA QUIMICA
ECUACIONES DE ESTADO
TERMODINAMICA I
ANTECEDENTES
1662. Boyle dio de manifiesto la ley de las isotermas.
1802. Gay-Lussac dio de manifiesto las leyes de las isobaras e isocoras.
1811. La Ley de Avogadro fue expuesta por Amedeo Avogadro y complementaba a
las de Boyle, Charles y Gay-Lussac. Asegura que en un proceso a presión y
temperatura constante (isobaro e isotermo), el volumen de cualquier gas es
proporcional al número de moles presente.
1883. Van Der Wals derivo una ecuación capaz de describir la continuidad entre las
fases líquido y vapor.
1940.Benedict-Webb-Rubin introduce una ecuación de estado especialmente para
hidrocarburos livianos y las mezclas de los mismos también es denominada
ecuación BWR.
1949.La ecuación de Redlich-Kwong fue una mejora considerable sobre las otras
ecuaciones de la época. La ecuación de Redlich-Kwong deriva de la ecuación de
estado térmico de Van Der Vaals.
1972. Soave reemplazó el término a/√(T) de la ecuación de Redlich-Kwong por una
expresión α(T,ω) función de la temperatura y del factor acéntrico.
1976. Fue desarrollada La ecuación de Peng-Robinson. Generalmente la ecuación
de Peng-Robinson da unos resultados similares a la de Soave, aunque es bastante
mejor para predecir las densidades de muchos compuestos en fase líquida,
especialmente los apolares.
1990. Fue propuesta la ecuación de estado de Elliott, Suresh, y Donohue (ESD).
Pretende corregir una desviación de la ecuación de estado de Peng-Robinson, en la
cual existe una imprecisión en el término de repulsión de Van Der Waals.
SANCHEZ ESCOBAR ANALY FAC.
DE INGENIERIA QUIMICA
ECUACIONES DE ESTADO
TERMODINAMICA I
ECUACIONES DE ESTADO
El estado de una cierta masa m de sustancia está determinado por su presión
p, su volumen V y su temperatura T. En general, estas cantidades no pueden
variar todas ellas independientemente.
Ecuación de estado:
V = f(p,T,m)
El término estado utilizado aquí implica un estado de equilibrio, lo que significa
que la temperatura y la presión son iguales en todos los puntos. Por
consiguiente, si se comunica calor a algún punto de un sistema en equilibrio,
hay que esperar hasta que el proceso de transferencia del calor dentro del
sistema haya producido una nueva temperatura uniforme, para que el sistema
se encuentre de nuevo en un estado de equilibrio.
Ley de los gases ideales
La teoría atómica de la materia define los estados, o fases, de acuerdo al orden
que implican. Las moléculas tienen una cierta libertad de movimientos en el
espacio. Estos grados de libertad microscópicos están asociados con el
concepto de orden macroscópico. Las moléculas de un sólido están colocadas
en una red, y su libertad está restringida a pequeñas vibraciones en torno a los
puntos de esa red. En cambio, un gas no tiene un orden espacial
macroscópico. Sus moléculas se mueven aleatoriamente, y sólo están limitadas
por las paredes del recipiente que lo contiene.
Se han desarrollado leyes empíricas que relacionan las variables
macroscópicas. En los gases ideales, estas variables incluyen la presión (p), el
volumen (V) y la temperatura (T). A bajas presiones,las ecuaciones de estado
de los gases son sencillas:
La ley de Boyle-Mariotte afirma que el volumen de un gas a temperatura
constante es inversamente proporcional a la presión.
p1.V1 = p2.V2
La ley de Charles y Gay Lussac afirma que el volumen de un gas a presión
constante es directamente proporcional a la temperatura absoluta.
SANCHEZ ESCOBAR ANALY FAC.
DE INGENIERIA QUIMICA
ECUACIONES DE ESTADO
TERMODINAMICA I
V1/T1 = V2/T2
Otra ley afirma que a volumen constante la presión es directamente
proporcional a la temperatura absoluta.
p1/T1 = p2/T2
Resumiendo:
p1.V1/T1 = p2.V2/T2 = constante
Definiendo las condiciones normales de presión y temperatura (CNPT) como, 1
atmósfera y 273 °K, para el volumen que ocupa un mol de cualquier gas (22,4
dm ³), esta constante se transforma en:
Constante = 1 atmósfera.22,4 dm ³/273 °K.mol = 0,08205 atmósferas.dm
³/°K.mol
Y se define R como la constante de los gases ideales:
R = 0,08205 atmósfera.dm ³/°K.mol
La combinación de estas leyes proporciona la ley de los gases ideales, también
llamada ecuación de estado del gas ideal:
p.V = n.R.T
Donde “n” es el número de moles.
Teoría cinética de los gases
Con la llegada de la teoría atómica de la materia, las leyes empíricas antes
mencionadas obtuvieron una base microscópica. El volumen de un gas refleja
simplemente la distribución de posiciones de las moléculas que lo componen.
Más exactamente, la variable macroscópica V representa el espacio disponible
para el movimiento de una molécula. La presión de un gas, que puede medirse
con manómetros situados en las paredes del recipiente, registra el cambio
medio de momento lineal que experimentan las moléculas al chocar contra las
paredes y rebotar en ellas. La temperatura del gas es proporcional a la energía
cinética media de las moléculas, por lo que depende del cuadrado de su
velocidad.
La reducción de las variables macroscópicas a variables físicas como la
posición, velocidad, momento lineal o energía cinética de las moléculas, que
pueden relacionarse a través de las leyes de la física de Newton, debería de
SANCHEZ ESCOBAR ANALY FAC.
DE INGENIERIA QUIMICA
ECUACIONES DE ESTADO
TERMODINAMICA I
proporcionar todas las leyes empíricas de los gases. En general, esto resulta
ser cierto.
La teoría física que relaciona las propiedades de los gases con la mecánica
clásica se denomina teoría cinética de los gases. Además de proporcionar una
base para la ecuación de estado del gas ideal.
La teoría cinética también puede emplearse para predecir muchas otras
propiedades de los gases, entre ellas la distribución estadística de las
velocidades moleculares y las propiedades de transporte como la conductividad
térmica, el coeficiente de difusión o la viscosidad.
Transiciones de fase
A temperaturas bajas (a las que el movimiento molecular se hace menor) y
presiones altas o volúmenes reducidos (que disminuyen el espacio entre las
moléculas), las moléculas de un gas pasan a ser influidas por la fuerza de
atracción de las otras moléculas. Bajo determinadas condiciones críticas, todo
el sistema entra en un estado ligado de alta densidad y adquiere una superficie
límite. Esto implica la entrada en el estado líquido. El proceso se conoce como
transición de fase o cambio de estado. La ecuación de Van der Waals permite
estas transiciones de fase, y también describe una región de coexistencia entre
ambas fases que termina en un punto crítico, por encima del cual no existen
diferencias físicas entre los estados gaseoso y líquido. Estos fenómenos
coinciden con las observaciones experimentales. En la práctica se emplean
ecuaciones más complejas que la ecuación de Van der Waals.
Punto crítico
En física, punto de temperatura o presión que corresponde a un cambio en el
estado físico de una sustancia. Durante el enfriamiento de una aleación
metálica, el punto crítico se alcanza a la temperatura en que se produce una
reorganización molecular que da lugar a una nueva forma de la sustancia;
generalmente, esta reorganización se ve acompañada por la absorción o
cesión de calor. La temperatura crítica de un gas es la temperatura máxima a la
que puede licuarse; la presión crítica es la presión necesaria para licuar el gas
a esa temperatura. Algunos gases, como el helio, el hidrógeno o el nitrógeno,
poseen temperaturas críticas muy bajas y tienen que ser enfriados
intensivamente antes de poder ser licuados. Otros, como el amoníaco o el
cloro, tienen temperaturas críticas elevadas y pueden licuarse a temperatura
ambiente aplicando suficiente presión. Una tercera característica del punto
crítico es el volumen crítico, que es el volumen que ocuparía un mol de gas a
su temperatura y presión críticas. Estas tres cantidades, la temperatura,
presión y volumen críticos, se denominan conjuntamente constantes críticas de
una sustancia.
SANCHEZ ESCOBAR ANALY FAC.
DE INGENIERIA QUIMICA
ECUACIONES DE ESTADO
TERMODINAMICA I
Presión de vapor
La presión de vapor en equilibrio con un líquido o un sólido a cualquier
temperatura se denomina presión de vapor de la sustancia a esa temperatura.
La presión de vapor de una sustancia es función de la temperatura solamente,
no del volumen.
En un recipiente que contenga líquido y vapor en equilibrio a temperatura
constante, la presión no depende de las cantidades relativas de vapor y líquido.
Si por algún motivo la cantidad de líquido disminuye, el vapor se condensa
(para compensar) y viceversa, pero si se suministra o sustrae calor a
temperatura constante, la presión no varía.
La temperatura del punto de ebullición de un líquido es la temperatura a la cual
su presión de vapor es igual a la presión exterior.
Humedad
Medida del contenido de agua en la atmósfera. La atmósfera contiene siempre
algo de agua en forma de vapor. La cantidad máxima depende de la
temperatura; crece al aumentar ésta:
a 4,4 °C, 1.000 kg. de aire húmedo contienen un máximo de 5 kg de vapor.
a 37,8 °C 1.000 kg. de aire húmedo contienen un máximo de 18 kg de vapor.
Cuando la atmósfera está saturada de agua, el nivel de incomodidad es alto ya
que la transpiración (evaporación de sudor corporal con resultado refrescante)
se hace imposible.
El masa de vapor de agua contenido en un volumen de aire se conoce como
humedad absoluta y se expresa en kg de agua por m ³ de aire seco.
Los científicos se refieren a estas medidas con gramos de vapor de agua por
metro cúbico.
La humedad relativa, es la razón entre el contenido efectivo de vapor en la
atmósfera y la cantidad de vapor que saturaría el aire a la misma temperatura.
100%.pp (vapor de agua)
HR (%) =
pv (a la misma temperatura)
SANCHEZ ESCOBAR ANALY FAC.
DE INGENIERIA QUIMICA
ECUACIONES DE ESTADO
TERMODINAMICA I
Si la temperatura atmosférica aumenta y no se producen cambios en el
contenido de vapor, la humedad absoluta no varía mientras que la relativa
disminuye. Una caída de la temperatura incrementa la humedad relativa
produciendo rocío.
La humedad se mide con un higrómetro. El índice de temperatura-humedad
(índice T-H, también llamado índice de incomodidad) expresa con un valor
numérico la relación entre la temperatura y la humedad como medida de la
comodidad o de la incomodidad. Se calcula sumando 40 al 72% de la suma de
las temperaturas en un termómetro seco y en otro húmedo. Por ejemplo, si la
temperatura en el termómetro seco es de 30 °C y en el húmedo es de 20 °C, el
índice T-H será de 76. Cuando el valor es 70, la mayoría de la gente está
cómoda, si el índice es de 75 el ambiente se hace más incómodo.
LEY DE GASES IDEALES
La ley de los gases ideales es la ecuación de estado del gas ideal, un gas
hipotético formado por partículas puntuales, sin atracción ni repulsión entre
ellas y cuyos choques son perfectamente elásticos (conservación de momento
y energía cinética). Los gases reales que más se aproximan al comportamiento
del gas ideal son los gases monoatómicos en condiciones de baja presión y
alta temperatura.
Empíricamente, se observan una serie de relaciones entre la temperatura, la
presión y el volumen que dan lugar a la ley de los gases ideales, deducida por
primera vez por Émile Clapeyron en 1834.
Ecuación de Van der Waals
La ecuación de estado del gas ideal no es del todo correcta: los gases reales
no se comportan exactamente así. En algunos casos, la desviación puede ser
muy grande. Por ejemplo, un gas ideal nunca podría convertirse en líquido o
sólido por mucho que se enfriara o comprimiera. Por eso se han propuesto
modificaciones de la ley de los gases ideales
P.V = n.R.T
Una de ellas, muy conocida y particularmente útil, es la ecuación de estado de
Van der Waals
(p + a/v ²).(v - b) = R.T
SANCHEZ ESCOBAR ANALY FAC.
DE INGENIERIA QUIMICA
ECUACIONES DE ESTADO
TERMODINAMICA I
Donde v = V/n
a y b son parámetros ajustables determinados a partir de medidas
experimentales en gases reales. Son parámetros de la sustancia y no
constantes universales, puesto que sus valores varían de un gas a otro.
La ecuación de Van der Waals también tiene una interpretación microscópica.
Las moléculas interaccionan entre sí. La interacción es muy repulsiva a corta
distancia, se hace ligeramente atractiva a distancias intermedias y desaparece
a distancias más grandes. La ley de los gases ideales debe corregirse para
considerar las fuerzas atractivas y repulsivas. Por ejemplo, la repulsión mutua
entre moléculas tiene el efecto de excluir a las moléculas vecinas de una cierta
zona alrededor de cada molécula. Así, una parte del espacio total deja de estar
disponible para las moléculas en su movimiento aleatorio. En la ecuación de
estado, se hace necesario restar este volumen de exclusión (b) del volumen del
recipiente (V); de ahí el término (V - b).
Ley de Boyle-Mariotte
La Ley de Boyle-Mariotte (o Ley de Boyle), formulada por Robert Boyle y Edme
Mariotte, es una de las leyes de los gases ideales que relaciona el volumen y la
presión de una cierta cantidad de gas mantenida a temperatura constante. La
ley dice que el volumen es inversamente proporcional a la presión:
Donde es constante si la temperatura y la masa del gas permanecen
constantes.
Cuando aumenta la presión, el volumen disminuye, mientras que si la presión
disminuye el volumen aumenta. El valor exacto de la constante k no es
necesario conocerlo para poder hacer uso de la Ley; si consideramos las dos
situaciones de la figura, manteniendo constante la cantidad de gas y la
temperatura, deberá cumplirse la relación:
Representación matemática:
Además se obtiene despejada que:
SANCHEZ ESCOBAR ANALY FAC.
DE INGENIERIA QUIMICA
ECUACIONES DE ESTADO
TERMODINAMICA I
Donde:
= Presión Inicial
= Presión Final
= Volumen Inicial
= Volumen Final
Esta Ley es una simplificación de la Ley de los gases ideales particularizada
para procesos isotermos.
Junto con la ley de Charles y Gay-Lussac y la ley de Graham, la ley de Boyle
forma las leyes de los gases, que describen la conducta de un gas ideal. Las
tres leyes pueden ser generalizadas en la ecuación universal de los gases.
Ley de Charles y Gay-Lussac
La Ley de Charles y Gay-Lussac, también llamada Ley de Charles explica las
leyes de los gases ideales. Relaciona el volumen y la temperatura de una cierta
cantidad de gas ideal, mantenido a una presión constante, mediante una
constante de proporcionalidad directa. En esta ley, Charles dice que a una
presión constante, al aumentar la temperatura, el volumen del gas aumenta y al
disminuir la temperatura el volumen del gas disminuye. Esto se debe a que
SANCHEZ ESCOBAR ANALY FAC.
DE INGENIERIA QUIMICA
ECUACIONES DE ESTADO
TERMODINAMICA I
"temperatura" significa movimiento de las partículas. Así que, a mayor
movimiento de las partículas (temperatura), mayor volumen del gas.
La ley fue publicada primero por Louis Joseph Gay-Lussac en 1802, pero hacía
referencia al trabajo no publicado de Jacques Charles, de alrededor de 1787, lo
que condujo a que la ley sea usualmente atribuida a Charles. La relación había
sido anticipada anteriormente en los trabajos de Guillaume Amontons en 1702.
Por otro lado, Gay Lussac relacionó la presión y la temperatura como unidades
directamente proporcionales y es llamada "La segunda ley de Gay-Lussac"
La ley de Charles es una de las más importantes leyes acerca del
comportamiento de los gases, y ha sido usada de muchas formas diferentes,
desde globos de aire caliente hasta acuarios. Se expresa por la fórmula; en
esta ley actúan la presión de un gas ideal así como la de un gas constante
Representación matemática:
Además puede expresarse como:
Despejando T1 se obtiene:
Despejando T2 se obtiene:
Despejando V1 se obtiene:
SANCHEZ ESCOBAR ANALY FAC.
DE INGENIERIA QUIMICA
ECUACIONES DE ESTADO
TERMODINAMICA I
Despejando V2 se obtiene:
Donde:
• V es el volumen
• T es la temperatura absoluta (es decir, medida en Kelvin)
• k es la constante de proporcionalidad
Ley de avogrado
La Ley de Avogadro fue expuesta por Amedeo Avogadro en 1811 y complementaba
a las de Boyle, Charles y Gay-Lussac. Asegura que en un proceso a presión y
temperatura constante (isobaro e isotermo), el volumen de cualquier gas es
proporcional al número de moles presente, de tal modo que: La Ley de Avogadro (a
veces llamada Hipótesis de Avogadro o Principio de Avogadro) es una de las leyes
de los gases ideales. Toma el nombre de Amedeo Avogadro, quien en 1811 afirmó
que:
"Volúmenes iguales de distintas sustancias gaseosas, medidos en las
mismas condiciones de presión y temperatura, contienen el mismo
número de partículas"
LEY GENERAL DE LOS GASES IDEALES:
Varía temperatura, presión y volumen; permanece constante la masa.
Deducción de la fórmula general:
SANCHEZ ESCOBAR ANALY FAC.
DE INGENIERIA QUIMICA
ECUACIONES DE ESTADO
TERMODINAMICA I
ECUACIÓN UNIVERSAL DE LOS GASES IDEALES:
PV= nRT
Donde:
P: presión absoluta: atm, torr, lb/pulg2
n: numero de mol-g o mol-lb.
T: temperatura absoluta: K, R
V: volumen: litros, ft3
R: constante universal de los gases.
Demostración: demostraremos de dos formas.
PRIMERA FORMA: de acuerdo a la ecuación general, se tiene:
PV = cte. Sea cte. = R luego:
SANCHEZ ESCOBAR ANALY FAC.
DE INGENIERIA QUIMICA
ECUACIONES DE ESTADO
TERMODINAMICA I
T
PV = RT para un mol
PV= nRT para n moles.
CONSTANTE UNIVERSAL DE LOS GASES IDEALES:
La constante universal de los gases ideales es una constante física que
relaciona entre sí diversas funciones de estado termodinámicas, estableciendo
esencialmente una relación entre la energía, la temperatura y la cantidad de
materia.
En su forma más particular la constante se emplea en la relación de la cantidad
de materia en un gas ideal, medida en número de moles (n), con la presión (P),
el volumen (V) y la temperatura (T), a través de la ecuación de estado de los
gases ideales.
El modelo del gas ideal asume que el volumen de la molécula es cero y las
partículas no interactúan entre sí. La mayor parte de los gases reales se
acercan a esta constante dentro de dos cifras significativas, en condiciones de
presión y temperatura suficientemente alejadas del punto de licuefacción o
sublimación. Las ecuaciones de estado de gases reales son, en mucho casos,
correcciones de la anterior.
GASES REALES
Se ha considerado que el gas ideal está constituido por partículas puntuales entre
las que no existen interacciones, que se mueven rápidamente, colisionando
elásticamente entre sí. Los gases reales están constituidos por moléculas o por
átomos, que poseen un volumen propio, y entre los que existen interacciones tanto
de tipo atractivo como repulsivo.
Por ello no debe extrañar que el comportamiento de los gases ideales (ley de Boyle,
ley de Gay Lusaac, y en general los gases perfectos), y que se desvíen tanto más
cuanto más elevada es la presión y menor la temperatura. La desviación cuantitativa
SANCHEZ ESCOBAR ANALY FAC.
DE INGENIERIA QUIMICA
ECUACIONES DE ESTADO
TERMODINAMICA I
del comportamiento de un gas real, a una temperatura dada, puede considerarse
dada por el factor de compresibilidad, a esa temperatura, referido a un mol de gas.
FACTOR DE COMPRESIBILIDAD Z
El factor de compresibilidad Z, es un factor de corrección, que se introduce en la
ecuación de estado de gas ideal para modelar el comportamiento de los gases
reales, los cuales se pueden comportar como gases ideales para condiciones de
baja presión y alta temperatura, tomando como referencia los valores del punto
crítico, es decir, si la temperatura es mucho más alta que la del punto crítico, el gas
puede tomarse como ideal, y si la presión es mucho más baja que la del punto crítico
el gas también se puede tomar como ideal.
La desviación de un gas respecto de su comportamiento ideal se hace mayor cerca
del punto crítico.
Remitiéndonos a la sección de gases ideales tenemos:
Introduciendo el factor de corrección Z:
Por lo tanto:
El factor Z también se puede entender como:
SANCHEZ ESCOBAR ANALY FAC.
DE INGENIERIA QUIMICA
ECUACIONES DE ESTADO
TERMODINAMICA I
Donde
V actual: volumen específico que se tiene del gas.
V ideal: volumen específico del gas tomado de la ecuación de gas ideal.
SIGNIFICADO DEL VALOR DE Z
Si el valor de Z es igual a 1 esto indica que el gas se comporta como ideal. Si el
valor de Z es mayor o menor que 1 el gas se comporta como un gas real.
Mientras más grande sea la desviación del valor de Z con respecto a 1, mayor
es la desviación del comportamiento respecto al comportamiento ideal del gas.
NORMALIZACIÓN DE LA TEMPERATURA Y LA PRESIÓN
Los gases se comportan de forma similar a temperaturas y presiones
normalizadas respecto a sus temperaturas y presiones críticas. Es decir, Z es
aproximadamente igual a la misma presión y temperatura reducidas para todos
los gases.
PRESIÓN REDUCIDA:
TEMPERATURA REDUCIDA:
PRINCIPALES ECUACIONES DE ESTADO PARA GASES IDEALES:
SANCHEZ ESCOBAR ANALY FAC.
DE INGENIERIA QUIMICA
ECUACIONES DE ESTADO
TERMODINAMICA I
Ecuación de Van der Waals
Esta ecuación es la más conocida y corrige las dos peores suposiciones de la
ecuación el gas ideal: tamaño molecular infinitesimal y ausencia de fuerzas
intermoleculares. La ecuación es:
El termino b es incluido para tener en cuenta el tamaño finito de las moléculas y
es llamado volumen molecular. El termino a/
2 es una corrección que fue incluida para considerar las fuerzas
intermoleculares. Estas dos constantes se escogen para que la ecuación se
adapte a los datos experimentales. Pero como sólo tiene dos constantes, no se
puede esperar que esta ecuación describa exactamente los datos PVT en un
intervalo amplio de presión y volumen.
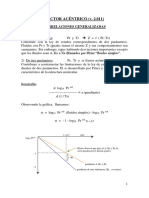
En la Figura Nº 3 se muestra las isotermas calculadas a partir de la ecuación
de Van der Walls. A la temperatura crítica Tc, la isoterma presenta un punto de
inflexión; a temperaturas más bajas se presenta un máximo y un mínimo y a
altas temperaturas las isotermas se asemejan a las del gas ideal. En la zona de
dos fases, esta gráfica predice tres valores para el volumen para una misma
presión, en cambio la Figura Nº 1 predice un número infinito de valores para el
volumen. Las secciones AB y CD se pueden lograr en forma experimental y
corresponden a estados de líquido sobrecalentado (AB) y de vapor
subenfriado(CD) y son estados metaestables. La sección BC es un estado
inestable.
SANCHEZ ESCOBAR ANALY FAC.
DE INGENIERIA QUIMICA
ECUACIONES DE ESTADO
TERMODINAMICA I
Figura Nº 3: Isotermas predecidas por la Ecuación de Van der Waals
Para obtener los valores de las constantes a y b, existen dos métodos que
llevan a similar resultado: aplicando la condición de inflexión en el punto crítico
y el otro es desarrollar la ecuación como una ecuación cúbica en volumen. El
desarrollo de ambos métodos se presenta en el ANEXO. Los valores obtenidos
son:
Como es difícil determinar experimentalmente el valor de
c, es recomendable que a y b se obtengan sólo a partir de Pc y Tc, por lo que
se obtiene:
Sin embargo al calcular
c y compararlo con los datos experimentales se observa que estos valores se
alejan apreciablemente, debido a que la ecuación de Van der Waals no es
precisa cerca del punto crítico. Esta ecuación pronostica un valor de Zc igual a
0,375, el cual se distancia notoriamente de los valores determinados
experimentalmente para éste parámetro. Además esta ecuación no es
satisfactoria a altas presiones.
SANCHEZ ESCOBAR ANALY FAC.
DE INGENIERIA QUIMICA
ECUACIONES DE ESTADO
TERMODINAMICA I
La virtud de la ecuación de Van der Waals es que se puede utilizar para
predecir el comportamiento PVT tanto de la región líquida como de la gaseosa,
así como también predecir transiciones de fase de líquido a vapor; además
predice la existencia de un estado crítico.
Ecuación de Redlich-Kwong
Esta ecuación de origen semiempírico, al igual que la ecuación de Van der
Waals, predice tres raíces para el volumen. La expresión de esta ecuación es:
Donde a y b son las constantes de Redlich-Kwong.
Al imponer la condición de que la isoterma presenta una inflexión en el punto
crítico, es posible expresar a y b en función de la presión y temperatura crítica
(similar a lo realizado con la ecuación de Van der Waals). Entonces los valores
de las constantes son [6]:
El factor de compresibilidad crítico para esta ecuación tiene un valor de 0,333 y
por lo tanto no es muy exacta cerca del punto crítico; además como sólo posee
dos parámetros no representa íntegramente la zona bifásica de la Figura Nº 1.
Sin embargo, es mucho más exacta que la ecuación de Van der Waals y da
buenos resultados a presiones altas y temperaturas sobre la temperatura
crítica, llegando a ser tan precisa como la ecuación de ocho parámetros. Por lo
tanto esta ecuación es muy útil, ya que combina la simplicidad de una ecuación
de dos parámetros con un alto grado de exactitud [7].
Ecuación de Soave
Esta ecuación es una modificación de la ecuación de Redlich-Kwong a la que
se le incluye el parámetro w, el cual es denominado factor acéntrico y es
característico de la estructura molecular del fluido. La expresión para esta
ecuación es:
SANCHEZ ESCOBAR ANALY FAC.
DE INGENIERIA QUIMICA
ECUACIONES DE ESTADO
TERMODINAMICA I
Los parámetros se determinan, al igual que la otras ecuaciones cúbicas,
aplicando la condición de inflexión en el punto crítico, obteniéndose las
siguientes expresiones para los parámetros.
Donde Tr =T/Tc temperatura reducida
Donde Prsat es la presión de vapor reducida.
Esta ecuación, al introducir otro parámetro más, permite mejorar aun más los
resultados entregados por la ecuación de Redlich-Kwong, sin embargo aún no
logra representar fielmente el comportamiento de un fluido para grandes
intervalos de presión y temperatura.
Ecuación Virial
Esta ecuación es la única que tiene una base teórica firme y se basa en el
comportamiento intermolecular previsto por la mecánica estadística. La
expresión para esta ecuación es:
en donde los coeficientes B, C, D, ... se llaman coeficientes viriales y dependen
de la temperatura y del compuesto. Estos coeficientes están relacionados
directamente con las fuerzas intermoleculares que existen entre grupos de
moléculas; por ejemplo el coeficiente B describe interacciones entre pares de
moléculas, C entre grupos de tres moléculas y así sucesivamente. Estas
interacciones se denominan viriales y pueden ser expresadas como
complicadas integrales de las fuerzas intermoleculares. Así, si se conocieran
las fuerzas intermoleculares entre cualquiera combinaciones de moléculas en
función de las separaciones moleculares, sería posible efectuar las
integraciones y obtener así las expresiones para los coeficientes sin necesidad
de ocupar datos experimentales; sin embargo estos cálculos son demasiados
SANCHEZ ESCOBAR ANALY FAC.
DE INGENIERIA QUIMICA
ECUACIONES DE ESTADO
TERMODINAMICA I
Complicados y aún no han sido completados, excepto para potenciales de
fuerzas simplificados (aún con esta simplificación los cálculos sólo han sido
factibles para el segundo y ocasionalmente el tercer coeficiente virial).
También la ecuación virial puede ser escrita de la siguiente manera (más fácil
de usar):
Donde los coeficientes B', C', D', .... también son llamados coeficientes viriales
y dependen de la temperatura y del compuesto.
Los coeficientes de ambas expresiones se pueden relacionar de la siguiente
manera.
Las dos formas de la ecuación virial son series infinitas; su uso práctico en
ingeniería resulta cuando converge rápidamente, es decir cuando no se
necesita más de dos o tres términos para que las series proporcionen valores
razonablemente aproximados. Esto es posible para gases y vapores a
presiones bajas o moderadas. Como en la zona de bajas presiones la gráfica Z
versus P (Figura Nº 2) es una recta, es posible truncar la ecuación virial
conservando dos términos:
Esta ecuación representa satisfactoriamente el comportamiento para muchos
vapores a temperatura subcrítica y hasta presiones de 15 bar. A temperaturas
mayores es apropiada para gases dentro de un intervalo de presiones creciente
a medida que aumenta la temperatura.
Para presiones sobre los 15 bar pero bajo los 50 bar la ecuación truncada en
tres términos da excelentes resultados:
SANCHEZ ESCOBAR ANALY FAC.
DE INGENIERIA QUIMICA
ECUACIONES DE ESTADO
TERMODINAMICA I
Esta ecuación es cúbica en volumen y la solución se obtiene con frecuencia por
iteraciones en un computador.
Las desventajas de usar la ecuación virial es la dificultad para calcular los
coeficientes sin recurrir a datos experimentales. Además por la forma que
presenta el ajuste a datos experimentales tampoco es tarea sencilla, por lo
tanto la ecuación virial es poco usada en ingeniería. Sin embargo, muchas de
las otras ecuaciones comúnmente utilizadas pueden ser reducidas a una forma
similar a la ecuación virial, ya que de esta forma las ecuaciones son más útiles
Ecuación de Clausius
Esta ecuación de tres parámetros fue propuesta poco después que la ecuación
de Van der Waals. La expresión para esta ecuación es:
donde las constantes b y c son las que describen el tamaño de las moléculas
del fluido.
Aplicando la condición de inflexión en el punto crítico y evaluando la ecuación
en las condiciones críticas (Pc, Tc y Vc), se obtiene los valores de los
parámetros
Al igual que la ecuación de Van der Waals, la constante b representa el mínimo
volumen molar de las moléculas y por lo tanto debe ser positivo. Al examinar la
expresión para b, se advierte que ésta es solo positiva si Zc>0,25; para muchos
fluidos el valor de Zc varía entre 0,25 a 0,31, pero para unos pocos como agua,
metanol, amonio, acetona, etc., Zc es menor que 0,25, lo que trae consigo un
valor de b negativo, lo cual es físicamente imposible.
Existe una modificación para superar este problema y consiste en reemplazar
la constante c por la b en la expresión original, dando:
SANCHEZ ESCOBAR ANALY FAC.
DE INGENIERIA QUIMICA
ECUACIONES DE ESTADO
TERMODINAMICA I
Y aplicando las condiciones del punto crítico se obtiene:
Esta modificación evita que el parámetro b sea negativo y predice un valor para
Zc igual a 0,3125.
Por lo tanto, la ecuación original de Clausius tiene la ventaja que al tener tres
parámetros se puede ajustar mucho mejor a los datos experimentales y predice
un valor de Zc apropiado; sin embargo, tiene la desventaja que predice valores
muy pequeños para el volumen molar. En cambio la ecuación modificada,
predice valores mucho más acertados para el volumen molar sin sacrificar
significativamente el valor de Zc.
Ecuación de Berthelot
La ecuación de estado de Berthelot es ligeramente más compleja que la
ecuación de Van der Waals. Esta ecuación incluye un término de atracción
intermolecular que depende tanto de la temperatura como del volumen. La
ecuación tiene la siguiente forma:
Aplicando las condiciones del punto crítico se determinan los parámetros a y b,
obteniéndose:
Esta ecuación al igual que la de Van der Waals predice un valor para Zc igual a
0,375, por lo que no es aconsejable utilizar cerca del punto crítico.
Para suplir esta deficiencia para utilizar la ecuación de Berthelot cerca del
punto crítico, se ha efectuado una modificación, la cual se presenta a
continuación:
SANCHEZ ESCOBAR ANALY FAC.
DE INGENIERIA QUIMICA
ECUACIONES DE ESTADO
TERMODINAMICA I
Donde: Tr = T/Tc temperatura reducida
Pr = P/Pc presión reducida
Para esta ecuación el factor de compresibilidad crítico tiene un valor de 0,28, el
cual se acerca bastante al valor promedio experimental de Zc para la gran
mayoría de los gases no polares.
Ecuación de Dieterici
La ecuación de Dieterici se desarrolló primordialmente para dar una mayor
coincidencia con el valor de Zc determinado experimentalmente. La expresión
para esta ecuación es:
El valor de Zc para esta ecuación es de 0,27 y por lo tanto esta ecuación se
puede usar cerca del punto crítico. Sin embargo es poco usada debido a la
función exponencial que presenta.
Ecuación de Peng-Robinson
Esta ecuación, al igual que la ecuación de Van der Waals, posee dos
parámetros, pero su forma es más complicada. La expresión de esta ecuación
es la siguiente:
Utilizando las condiciones de inflexión en el punto crítico, se obtiene los
parámetros:
Esta ecuación predice un valor para Zc igual a 0,3074, por lo que esta ecuación
es posible de aplicar cerca del punto crítico. Además permite predecir
densidades de líquidos levemente mejor que las otras ecuaciones cúbicas,
pero no es suficientemente exacta para diseños reales.
SANCHEZ ESCOBAR ANALY FAC.
DE INGENIERIA QUIMICA
ECUACIONES DE ESTADO
TERMODINAMICA I
Ecuación de Beattie-Bridgeman
Esta ecuación incluye cinco constantes, luego puede representar mucho mejor
el comportamiento de los fluidos en un amplio intervalo de presión y
temperatura. La expresión de esta ecuación es la siguiente:
Las constantes a', b', c',
y
para algunos gases se encuentran tablas en la literatura.
Esta ecuación es aplicable cuando la densidad promedio sea inferior a 0,8
veces la densidad crítica.
Ecuación de Benedict-Weeb-Rubin
Esta ecuación presenta ocho constantes y por lo tanto representa mucho mejor
el comportamiento de los fluidos que las ecuaciones anteriores. La expresión
para esta ecuación es:
Los parámetros a'', b'', c'',
,
,
, ð y γ para algunos fluidos se encuentran tabulados en la literatura .
Esta ecuación se puede utilizar cuando la densidad sea inferior a 1,2 veces la
densidad crítica.
La ecuación de Benedict-Weeb-Rubin a pesar de su complejidad tiene un gran
uso para determinar propiedades de hidrocarburos ligeros y otros componentes
gaseosos comúnmente encontrados tanto en la industria del petróleo como en
la del gas natural.
SANCHEZ ESCOBAR ANALY FAC.
DE INGENIERIA QUIMICA
ECUACIONES DE ESTADO
TERMODINAMICA I
USOS DE LAS ECUACIONES DE ESTADO
El diseño de equipos de procesos utilizados en la industria química requiere de
datos termodinámicos. Estos datos son entregados por las ecuaciones de
estados y se pueden aplicar al diseño de muchos tipos de equipos, como por
ejemplo: para intercambiadores de calor se debe determinar la entalpía a la
entrada y salida del equipo usando los datos de temperatura y presión;
determinar el volumen de un fluido a cierta temperatura y presión para el
diseño de recipientes, y generalmente para el diseño de rehervidores,
condensadores, bombas, compresores y expandidores.
En la industria petroquímica, especificamente en los procesos de liquefacción,
las ecuaciones de estados se utilizan entre muchas aplicaciones para: predecir
con alta precisión entalpías para así optimizar el diseño de intercambiadores de
calor; determinar datos de equilibrios vapor/líquido de los gases para los
procesos de separación; predicción precisa de la densidad de líquidos para
conocer la masa o volumen y calcular el calor total; determinar la potencia
requerida en los compresores, etc.
En los procesos de separación, como la destilación, para el diseño de equipos
se requiere de datos de equilibrios líquido/vapor. Estos datos pueden ser
obtenidos por correlaciones gráficas o analíticas. Ambas utilizan datos de
presión, volumen y temperatura, los cuales son proporcionados por las
ecuaciones de estado.
Para las correlaciones gráficas, la ecuación de estado más usada es la de
Benedict-Weeb-Rubin, la cual se utilizó para construir las gráficas de Kellogg,
las que incluyen los datos de equilibrios para los 12 principales hidrocarburos.
Para las correlaciones analíticas, las ecuaciones de estados más usadas son
las de Benedict-Weeb-Rubin y la de Redlich-Kwong o la de Soave.
En el diseño de reacciones heterogéneas, las ecuaciones de estado se utilizan
para determinar los valores de presión y temperatura que se utilizan para los
distintos modelos de adsorción. Con estos modelos se pueden diseñar los
reactores para reacciones heterogénea.
En general todos los procesos requieren de datos de equilibrios, entalpías,
presiones, volúmenes, y otras propiedades termodinámicas, las cuales son
derivadas de las ecuaciones de estado. La precisión y condiciones en las
cuales se quiera trabajar dependerá de la ecuación que se ocupe.
SANCHEZ ESCOBAR ANALY FAC.
DE INGENIERIA QUIMICA
ECUACIONES DE ESTADO
TERMODINAMICA I
CONCLUSIONES
Las ecuaciones de estado se utilizan para determinar datos de equilibrios,
entalpías, presiones, volúmenes, y otras propiedades termodinámicas. La
elección de la ecuación a utilizar dependerá de la precisión que se requiera y
de las condiciones de operación en las que se trabaje.
Las ecuaciones de estados cúbicas no pueden representar fielmente el
comportamiento de los gases, especificamente en la zona de dos fases, ya que
sólo poseen dos constantes.
La ecuación del virial, basada en la mecánica estadística, puede representar
fielmente el comportamiento. Sin embargo, es poco utilizada en ingeniería
debido a la complicación del cálculo de los coeficientes.
De las ecuaciones cúbicas, la más utilizada es la de Redlich-Kwong, la cual
combina la simplicidad de una ecuación de 2 parámetros con una alta precisión
similar a la ecuación de Benedict-Weeb-Rubin de ocho parámetros.
SANCHEZ ESCOBAR ANALY FAC.
DE INGENIERIA QUIMICA
ECUACIONES DE ESTADO
TERMODINAMICA I
BIBLIOGRAFÍA
1.- Kyle B.,1992,"Chemical and Process Thermodynamics", 2º Ed., Ed. Prentice
Hall, USA, Pág. 38-52.
2.- Castellan G., 1987, "Físico Química", 2º Ed., Ed. Addison-Wesley
Iberoamericana, México, Pág. 8-50.
3.- Balzhiser R., Samuels M., Eliassen J., 1974, "Termodinámica Química para
Ingenieros", Ed. Prentice Hall, España, Pág. 58-79.
4.- Levine I., 1991, "Físico-Química", 3º Edición, Ed. McGraw-Hill, Barcelona,
Pág. 243-257.
5.- Smith J., Van Ness H., 1989, "Introducción a la Termodinámica en
Ingeniería Química", 4º Ed., Ed. McGraw-Hill, México, Pág. 61-95, 485-497.
6.- Van Ness H., Abbott M., 1982, "Classical Thermodynamics of Nonelectrolyte
Solutions with Applications to Phase Equilibria", Ed. McGraw-Hill, USA, Pág.
114-169.
7.-Wark K., 1991, "Termodinámica", 5º Ed., Ed. McGraw-Hill, México, Pág. 457-
471.
8.- Eberhart J., 1992, "The Clausius Equation of State and a Two-Parameter
Modification", Journal of Chemical Education, Vol 68 (2): 113.
9.- Eberhart J., 1989, "Appliying the Critical Conditions to Equation of State",
Journal of Chemical Education, Vol 66 (12): 990-993.
10.- Perry R. and Green D., 1992, "Manual del Ingeniero Químico", 6º Ed., Ed.
McGraw-Hill, México, Cap 3, 4 y 13.
11.- Yaws C., Sachon D., Sheth M., 1996, "Thermodynamics Data for Process
Equipment Design", Chemical Engineering, Vol 103 (8): 110-111.
12.- Zudkevitch D. and Gray R., 1975, "Impact of Fluid Properties on the Design
of Equipment for Handling LNG", Pág. 103-121.
SANCHEZ ESCOBAR ANALY FAC.
DE INGENIERIA QUIMICA
Вам также может понравиться
- Problema BalanceДокумент4 страницыProblema BalanceGustavo DíazОценок пока нет
- Método de Dranchuk para Cálculo de Factor de Desviación "Z"Документ7 страницMétodo de Dranchuk para Cálculo de Factor de Desviación "Z"Marco ÁvalosОценок пока нет
- Ecuación de Estado de Redlich-KwongДокумент6 страницEcuación de Estado de Redlich-KwongAnonymous 6meMTlОценок пока нет
- 4 - Potenciales Termodinámicos. Relaciones de Maxwell (NXPowerLite)Документ23 страницы4 - Potenciales Termodinámicos. Relaciones de Maxwell (NXPowerLite)Daniel Sabino CampoОценок пока нет
- Teoría Del Gas Real: La Relación Exacta Para Gases RealesОт EverandTeoría Del Gas Real: La Relación Exacta Para Gases RealesОценок пока нет
- Practica Calificada EstadisticaДокумент8 страницPractica Calificada Estadisticasandra quispeОценок пока нет
- 8 - PP-412 Propiedades de Los Gases Reales PDFДокумент38 страниц8 - PP-412 Propiedades de Los Gases Reales PDFSusan Li HB100% (1)
- Repaso para LiquidosДокумент27 страницRepaso para LiquidosMelissa CarcacheОценок пока нет
- Clase 6 - Flujo Película DescendenteДокумент16 страницClase 6 - Flujo Película DescendenteThony Carrillo75% (4)
- Ecuacion de Estado Redlich Kwong Soave Boston Mathias APAДокумент14 страницEcuacion de Estado Redlich Kwong Soave Boston Mathias APAEdiie GO100% (1)
- Modelo Matemático de PengДокумент1 страницаModelo Matemático de PengPatricia BalcazarОценок пока нет
- Fisicoquimica Ecuación de Clausius ClapeyronДокумент4 страницыFisicoquimica Ecuación de Clausius ClapeyronMarc Muñoz100% (1)
- Equilibrio Quimic1Документ22 страницыEquilibrio Quimic1garracsoОценок пока нет
- Unidad 5. Ecuaciones de EstadoДокумент36 страницUnidad 5. Ecuaciones de EstadoJesús Daniel Villamizar QuinteroОценок пока нет
- Ecuaciones de EstadoДокумент17 страницEcuaciones de Estadoclarisapradorojas88% (8)
- Cap.5 Sistemas MulticomponenteДокумент62 страницыCap.5 Sistemas MulticomponenteestefaniaОценок пока нет
- Reservorio SubsaturadoДокумент3 страницыReservorio SubsaturadoSergio CAОценок пока нет
- Ecuación de Beattie-BridgemanДокумент1 страницаEcuación de Beattie-BridgemanCristhian Ricardo0% (1)
- Ecuaciones de EstadoДокумент30 страницEcuaciones de EstadoDarwinA.MillaОценок пока нет
- Taller Cálculos Con Ecuaciones Cúbicas de Estado para PetróleoДокумент16 страницTaller Cálculos Con Ecuaciones Cúbicas de Estado para PetróleoSantiagoVélezSОценок пока нет
- Ley de Los Estados CorrespondientesДокумент6 страницLey de Los Estados CorrespondientesLuis Oscar Lopez JuncoОценок пока нет
- I Parcial AB PDFДокумент1 страницаI Parcial AB PDFsantiago martinezОценок пока нет
- Determinacion Del Peso MolecularДокумент12 страницDeterminacion Del Peso MolecularJair AlterОценок пока нет
- Ecuación de Estados de Redlich-KwongДокумент26 страницEcuación de Estados de Redlich-KwongEmmanuel RamirezОценок пока нет
- Unidad 4-Presentacion Ecuaciones de EdoДокумент85 страницUnidad 4-Presentacion Ecuaciones de EdoIvan HdezОценок пока нет
- Libro de FicoДокумент1 374 страницыLibro de FicoSherlin Almanza ObregonОценок пока нет
- Factor de Compresibilidad y Ecuaciones de EstadoДокумент21 страницаFactor de Compresibilidad y Ecuaciones de Estadobarcelona_2092Оценок пока нет
- Ecuaciones de Estado para Gases Reales MДокумент9 страницEcuaciones de Estado para Gases Reales MSoltyrei95Оценок пока нет
- Redlich KwongДокумент4 страницыRedlich Kwongjhon0% (1)
- Analisis Dimensional y Teoria de ModelosДокумент33 страницыAnalisis Dimensional y Teoria de ModelosCarlos SmithОценок пока нет
- EJERCICIOS EN CLASE (Torres Contactora y de Amina)Документ8 страницEJERCICIOS EN CLASE (Torres Contactora y de Amina)Emili Vio KantutaОценок пока нет
- Unidad 6Документ59 страницUnidad 6Franklin SanchezОценок пока нет
- Revision de Algunas Ecuaciones de Estado PDFДокумент23 страницыRevision de Algunas Ecuaciones de Estado PDFKevin GonzalesОценок пока нет
- Resolucion de ProblemasДокумент14 страницResolucion de ProblemasFabrizzio_ValerОценок пока нет
- EVL Benceno-ToluenoДокумент10 страницEVL Benceno-ToluenoMiguel Jiménez FloresОценок пока нет
- Practica FenomenosДокумент8 страницPractica FenomenosAndrea Flores AcflОценок пока нет
- Calculos Practica 10Документ5 страницCalculos Practica 10Jordan UsiñaОценок пока нет
- Importancia Del Factor de Compresibilidad Del Gas PDFДокумент8 страницImportancia Del Factor de Compresibilidad Del Gas PDFMiguel Flores100% (1)
- Modelo de EyringДокумент5 страницModelo de EyringMarita M. OrbegosoОценок пока нет
- InformeДокумент24 страницыInformealexandraОценок пока нет
- Gases Reales y Ecuación de Van Der WaalsДокумент9 страницGases Reales y Ecuación de Van Der WaalsCamila PachecoОценок пока нет
- Métodos de Newton Raphson para El Equilibrio L-VДокумент4 страницыMétodos de Newton Raphson para El Equilibrio L-VTimoteo D. CastelazoОценок пока нет
- Fenómenos de Transporte 6Документ21 страницаFenómenos de Transporte 6Kevin MolinaОценок пока нет
- Ecuación de Estado de Van Der WaalsДокумент8 страницEcuación de Estado de Van Der Waalsgeorgemith100% (1)
- Método MargulesДокумент15 страницMétodo MargulesKaren Rocha0% (1)
- FugacidadДокумент4 страницыFugacidadRitch de la CalleОценок пока нет
- Diagrama de Flujo, Ley Del Enfriamiento de NewtonДокумент2 страницыDiagrama de Flujo, Ley Del Enfriamiento de NewtonLIDIA BRITNNY VALENCIA CÓRDOVAОценок пока нет
- Factor Acéntrico v. 2.011Документ3 страницыFactor Acéntrico v. 2.011Vanesa acostaОценок пока нет
- Asog Unifac UniquacДокумент3 страницыAsog Unifac UniquacCesar CaceresОценок пока нет
- Fundamentos de Ingeniería de YacimientosДокумент104 страницыFundamentos de Ingeniería de YacimientosCristhel Lisbeth Parrales LopezОценок пока нет
- Coeficientes Individuales y Globales de Crecimiento Masa 1Документ8 страницCoeficientes Individuales y Globales de Crecimiento Masa 1Jorge FrancoОценок пока нет
- Deber Teoria de JuegosДокумент10 страницDeber Teoria de JuegosGuadalupeSerranoОценок пока нет
- Ecuación de Estado de Peng-RobinsonДокумент3 страницыEcuación de Estado de Peng-RobinsonGustavo DíazОценок пока нет
- Análisis Factor de CompresibilidadДокумент3 страницыAnálisis Factor de CompresibilidadAndrés Felipe GuzmanОценок пока нет
- Termodinamica Del Equilibrio Entre FasesДокумент38 страницTermodinamica Del Equilibrio Entre FasesAlexis Maside100% (2)
- Sistemas MulticomponentesДокумент52 страницыSistemas MulticomponentesBENYОценок пока нет
- VAN Der Waals (Ing Industrial 3cer Ciclo)Документ8 страницVAN Der Waals (Ing Industrial 3cer Ciclo)Leonardo Rodriguez ChavezОценок пока нет
- GasesДокумент31 страницаGasesGivion WeaverОценок пока нет
- Ecuaciones de EstadoДокумент33 страницыEcuaciones de EstadoalexcornejosuniОценок пока нет
- Fisicoquimica Trabajo en Equipo PDFДокумент23 страницыFisicoquimica Trabajo en Equipo PDFRicardo TorresОценок пока нет
- Informe de Vander Walls 1Документ9 страницInforme de Vander Walls 1renataОценок пока нет
- Gas NaturalДокумент24 страницыGas NaturalAny Sanchez100% (1)
- Efecto Invernadero 2Документ22 страницыEfecto Invernadero 2richard2890Оценок пока нет
- Aplicacion de La Primera Ley de La Termodinamica A Equipos IndustrialesДокумент21 страницаAplicacion de La Primera Ley de La Termodinamica A Equipos IndustrialesAny Sanchez100% (22)
- Energia Libre de GibbsДокумент14 страницEnergia Libre de GibbsAny Sanchez83% (6)
- Energia Libre de GibbsДокумент14 страницEnergia Libre de GibbsAny Sanchez83% (6)
- Filosofar CientificamentДокумент3 страницыFilosofar CientificamentAny Sanchez100% (1)
- Diagrama de Fases Ternario 1.0Документ17 страницDiagrama de Fases Ternario 1.0JHON ALEX GONZALES QUISPEОценок пока нет
- AcuiferosДокумент57 страницAcuiferosDiego RangelОценок пока нет
- Quimica10ABC 02Документ32 страницыQuimica10ABC 02DIANA CAROLINA POSADA LINARESОценок пока нет
- Guia Taller Sobre Los Fluidos Grado 8Документ8 страницGuia Taller Sobre Los Fluidos Grado 8Alison RuizОценок пока нет
- Resumen CalorДокумент53 страницыResumen CalorKev LhuillierОценок пока нет
- PELZER Isocinetico 2014.5 MicroecolДокумент32 страницыPELZER Isocinetico 2014.5 Microecolrolando lainezОценок пока нет
- Yacimiento de GasДокумент33 страницыYacimiento de GasSalvador Ramirez EscalanteОценок пока нет
- Cap 2.marco TeoricoДокумент14 страницCap 2.marco TeoricoVicente JimenezОценок пока нет
- Docsity Viscocidad y Tension SuperficialДокумент38 страницDocsity Viscocidad y Tension SuperficialJhulisa Torrez CondoriОценок пока нет
- D Selección de Compresor 5.07 Rev 2019Документ60 страницD Selección de Compresor 5.07 Rev 2019jose2030621Оценок пока нет
- Unidad III GasesДокумент26 страницUnidad III GasesLionel Andrés Messi CuccittiniОценок пока нет
- PROBLEMAS RESUELTOS - Estado Gaseoso 21-21Документ6 страницPROBLEMAS RESUELTOS - Estado Gaseoso 21-21Jordy BolañosОценок пока нет
- Problemas Propuestos y Resueltos Primera Ley Termodinc3a1mica1Документ2 страницыProblemas Propuestos y Resueltos Primera Ley Termodinc3a1mica1Christhian Toranzo CalleОценок пока нет
- Repaso CEPREUNI Quimica Sist. DispersosДокумент15 страницRepaso CEPREUNI Quimica Sist. DispersosC D. MoriОценок пока нет
- Apuntes Mec. de Fluidos Univ. Polit. de Madrid PDFДокумент99 страницApuntes Mec. de Fluidos Univ. Polit. de Madrid PDFFabricioОценок пока нет
- (Oficial) Termo 3Документ8 страниц(Oficial) Termo 3Linette UbaldoОценок пока нет
- Estados de La Materia - TrabajoДокумент6 страницEstados de La Materia - TrabajoFrancisco PerezОценок пока нет
- Filtros de Gran Caudal MicroДокумент4 страницыFiltros de Gran Caudal MicroObed VargasОценок пока нет
- Metodo de Trekell-Campbell, Ecuacion de Clapeyron y Metodo Mcketta-Wehe para Gases DulcesДокумент15 страницMetodo de Trekell-Campbell, Ecuacion de Clapeyron y Metodo Mcketta-Wehe para Gases DulcesMaria Marcela GomezОценок пока нет
- Conceptos BásicosДокумент48 страницConceptos BásicosJona HernandezОценок пока нет
- Hexafluoruro de Azufre SF6Документ2 страницыHexafluoruro de Azufre SF6MaelypОценок пока нет
- Turbomaquinas TermicasДокумент68 страницTurbomaquinas Termicasjose reategui llempenОценок пока нет
- Texto de Neumática y ElectroneumáticaДокумент201 страницаTexto de Neumática y ElectroneumáticaGatico Salazar100% (1)
- Iiiex Parcial 092c 2019 IIДокумент2 страницыIiiex Parcial 092c 2019 IIMarco Antonio Pomahuali BravoОценок пока нет
- HumidificaciónДокумент21 страницаHumidificaciónJorge Eduardo MendezОценок пока нет
- GUIA No.3 QUIMICA SEPTIMOДокумент6 страницGUIA No.3 QUIMICA SEPTIMOAlex RosarioОценок пока нет
- Comparto 'Cuadro Comparativo de Las Leyes de Los Gases' Con UstedДокумент8 страницComparto 'Cuadro Comparativo de Las Leyes de Los Gases' Con UstedYossibel A. Ramos RОценок пока нет