Академический Документы
Профессиональный Документы
Культура Документы
Sifat Periodik Unsur
Загружено:
Occhi A CasperАвторское право
Доступные форматы
Поделиться этим документом
Поделиться или встроить документ
Этот документ был вам полезен?
Это неприемлемый материал?
Пожаловаться на этот документАвторское право:
Доступные форматы
Sifat Periodik Unsur
Загружено:
Occhi A CasperАвторское право:
Доступные форматы
SIFAT-SIFAT
PERIODIK UNSUR
Presented by: Mochamad Kodim, S.Pd
SIFAT-SIFAT PERIODIK UNSUR
STANDAR KOMPETENSI
Memahami sifat-sifat periodik unsur.
KOMPETENSI DASAR
Memahami sifat-sifat periodik unsur dalam tabel periodik serta menyadari keteraturannya, melalui pemahaman konfigurasi elektron.
INDIKATOR
Menganalisis tabel, grafik untuk menentukan keteraturan jari-jari atom, energi ionisasi, afinitas elektron dan keelektronegatifan.
Presented by: Mochamad Kodim, S.Pd
SIFAT-SIFAT PERIODIK UNSUR
JARI-JARI ATOM
ENERGI IONISASI
AFINITAS ELEKTRON
KEELEKTRONEGATIFAN
LOGAM DAN NON LOGAM
TITIK LEBUR DAN TITIK DIDIH OKSIDA ASAM BASA
Presented by: Mochamad Kodim, S.Pd
SIFAT-SIFAT PERIODIK UNSUR
1. JARI-JARI ATOM
Apa yang dimaksud dengan jari-jari atom..??
? ?
Presented by: Mochamad Kodim, S.Pd
SIFAT-SIFAT PERIODIK UNSUR
JARI-JARI ATOM
misalnya...
d = diameter bola r = jari-jari bola
r = jari-jari atom
JADI Jari-jari atom adalah jarak dari inti atom hingga elektron terluar. Presented by: Mochamad Kodim, S.Pd
SIFAT-SIFAT PERIODIK UNSUR
JARI-JARI ATOM Contoh 1
No. atom 11 19 Tingkat Energi 1 2 2 2 8 8 3 1 8 4 1
Unsur Na K
Konfigurasi elektron
Natrium (
11Na
Kalium (
19K)
Presented by: Mochamad Kodim, S.Pd
SIFAT-SIFAT PERIODIK UNSUR
JARI-JARI ATOM
JADI Dalam 1 golongan (dari atas ke bawah) jari-jari atom
semakin besar.
Presented by: Mochamad Kodim, S.Pd
SIFAT-SIFAT PERIODIK UNSUR
JARI-JARI ATOM Contoh 2
No. atom 11 12 Tingkat Energi 1 2 2 2 8 8 3 1 2 4 -
Unsur Na Mg
Konfigurasi elektron
Natrium (
11Na
Magnesium (
12Mg)
Presented by: Mochamad Kodim, S.Pd
SIFAT-SIFAT PERIODIK UNSUR
JARI-JARI ATOM Natrium (
11Na
Magnesium (
12Mg)
Tarikan muatan inti terhadap elektron
Jari-jari atom tetap
Jari-jari atom semakin kecil
Presented by: Mochamad Kodim, S.Pd
SIFAT-SIFAT PERIODIK UNSUR
JARI-JARI ATOM
JADI Dalam 1 periode (dari kiri ke kanan) jari-jari atom semakin kecil karena muatan inti bertambah yang menyebabkan tarikan elektron makin kuat. Presented by: Mochamad Kodim, S.Pd
SIFAT-SIFAT PERIODIK UNSUR
2. ENERGI IONISASI
Misalnya
en
g er
i
Energi + +e
Na (g)
Na+ (g)
Presented by: Mochamad Kodim, S.Pd
SIFAT-SIFAT PERIODIK UNSUR
ENERGI IONISASI
+ e
ne e gi r
Na (g)
Na+ (g)
INGAT Energi ionisasi adalah energi minimum yang diperlukan atom netral dalam bentuk gas untuk melepas satu elektron Membentuk ion bermuatan + Presented by: Mochamad Kodim, S.Pd
SIFAT-SIFAT PERIODIK UNSUR
ENERGI IONISASI
Tabel energi ionisasi unsur periode 2: Unsur
1 Li Be B C N O F 519 900 799 1088 1403 1314 1682 Energi Ionisasi (kj/mol) 2 7297 1757 2427 2351 2853 3393 3376 3 11811 14845 3661 4619 4577 5301 6046
Presented by: Mochamad Kodim, S.Pd
SIFAT-SIFAT PERIODIK UNSUR
ENERGI IONISASI
Tabel energi ionisasi beberapa unsur golongan 1: Energi Ionisasi (kj/mol) 1
3Li 11Na 19K
Unsur 519 496 419
2 7297 4563 3070
3 11811 6920 4439
Dari kedua tabel dapat disimpulkan:
Presented by: Mochamad Kodim, S.Pd
SIFAT-SIFAT PERIODIK UNSUR
ENERGI IONISASI Energi Ionisasi Pertama
- Unsur-unsur gas mulia (He, Ne, Ar, Kr) di puncak - Unsur-unsur alkali (Li, Na, K, Rb) di lembah
Presented by: Mochamad Kodim, S.Pd
SIFAT-SIFAT PERIODIK UNSUR
ENERGI IONISASI
Harga energi ionisasi dipengaruhi oleh jari-jari atom: Semakin besar jari-jari atom, tarikan inti semakin melemah dan mudah melepaskan elektron sehingga energi ionisasiya semakin kecil. Semakin kecil jari-jari atom, maka energi ionisasinya semakin besar karena atom sulit melepaskan elektron.
Presented by: Mochamad Kodim, S.Pd
SIFAT-SIFAT PERIODIK UNSUR
3. AFINITAS ELEKTRON
Misalnya
+ energi
e
INGAT
F (g)
F - (g)
Afinitas elektron adalah energi yang dilepas oleh atom netral dalam bentuk gas bila menerima elektron untuk membentuk ion negatif yang stabil.
Presented by: Mochamad Kodim, S.Pd
SIFAT-SIFAT PERIODIK UNSUR
AFINITAS ELEKTRON
Tabel afinitas elektron unsur-unsur golongan utama
IA Periode 1 Periode 2 Periode 3 Periode 4 Periode 5 Periode 6 H
-73
II A
III A
IV A
VA
VI A
VII A
VIII A He
21
Li
-60
Be
0
B
-27
C
-122
N
-7
O
-141
F
-328
Ne
29
Na
-53
Mg
0
Al
-44
Si
-134
P
-72
S
-200
Cl
-349
Ar
35
K
-48
Ca
-2.4
Ga
-30
Ge
-120
As
-77
Se
-195
Br
-325
Kr
39
Rb
-47
Sr
-4.7
In -30 Tl
-30
Sn
-121
Sb
-101
Te
-190
I
-295
Xe
41
Cs
-45
Ba
-15
Pb
-110
Bi
-110
Po
-180
At
-270
Rn
41
Ket: Tanda (-) menunjukkan pelepasan energi oleh atom.
SIFAT-SIFAT PERIODIK UNSUR
AFINITAS ELEKTRON
KESIMPULAN DARI TABEL
Presented by: Mochamad Kodim, S.Pd
SIFAT-SIFAT PERIODIK UNSUR
AFINITAS ELEKTRON
Harga afinitas elektron dipengaruhi oleh jari-jari atom: Jari-jari atom semakin kecil (dalam 1 periode), semakin mudah atom menerima elektron sehingga harga afinitas elektronnya cenderung semakin besar. Jika jari-jari atom semakin besar (dalam 1 golongan), harga afinitas elektronnya cenderung semakin kecil.
Presented by: Mochamad Kodim, S.Pd
SIFAT-SIFAT PERIODIK UNSUR
4. KEELEKTRONEGATIFAN
Misalnya
FA
FB
JIKA FB > FA maka A akan tertarik ke B
Presented by: Mochamad Kodim, S.Pd
SIFAT-SIFAT PERIODIK UNSUR
KEELEKTRONEGATIFAN
HF
Itu karena F lebih elektronegatif dari H
JADI
Keelektronegatifan adalah suatu bilangan yang menyatakan kecenderungan suatu unsur untuk menarik elektron ke pihaknya dalam suatu ikatan kimia.
Presented by: Mochamad Kodim, S.Pd
SIFAT-SIFAT PERIODIK UNSUR
KEELEKTRONEGATIFAN Keelektronegatifan dalam Skala Pauling
- Dalam 1 golongan, keelektronegatifan cenderung semakin berkurang - Dalam 1 periode, keelektronegatifan cenderung semakin bertambah sehingga membentuk ion negatif
Presented by: Mochamad Kodim, S.Pd
SIFAT-SIFAT PERIODIK UNSUR
KEELEKTRONEGATIFAN
Keelektronegatifan dapat dihubungkan dengan EI (energi ionisasi) dan AE (afinitas elektron). Misalnya - Fluor (F) : AE dan EI tinggi mempunyai harga keelektronegatifan besar - Natrium (Na) : AE dan EI rendah mempunyai harga keelektronegatifan kecil
Presented by: Mochamad Kodim, S.Pd
SIFAT-SIFAT PERIODIK UNSUR
KEELEKTRONEGATIFAN
PERTANYAAN :
Dari data keelektronegatifan dalam skala Pauling di atas, buatlah grafiknya dengan sumbu x untuk golongan/periode dan sumbu y untuk nilai: keelektronegatifannya untuk: a. Golongan 1 b. Periode 3 c. Golongan 17
JAWABAN :
Presented by: Mochamad Kodim, S.Pd
SIFAT-SIFAT PERIODIK UNSUR
5. LOGAM DAN NON LOGAM
Logam biasanya pada suhu kamar berwujud padat (kecuali Hg), mengkilap, konduktor yang baik, umumnya mempunyai densitas dan titik lebur yang tinggi. Misalnya:
Logam Emas
Logam Natrium
Presented by: Mochamad Kodim, S.Pd
SIFAT-SIFAT PERIODIK UNSUR
LOGAM DAN NON LOGAM
Non logam cirinya tidak mengkilap, umumnya mempunyai titik lebur dan densitas yang rendah, misalnya:
Gas Argon
Gas Neon
Metaloid memiliki sifat dari logam dan non logam, misalnya:
silicon
Presented by: Mochamad Kodim, S.Pd
SIFAT-SIFAT PERIODIK UNSUR
LOGAM DAN NON LOGAM
Tabel sifat logam dan non logam
Presented by: Mochamad Kodim, S.Pd
SIFAT-SIFAT PERIODIK UNSUR
LOGAM DAN NON LOGAM
KESIMPULAN DARI TABEL
SIFAT-SIFAT PERIODIK UNSUR
LOGAM DAN NON LOGAM
Sifat logam bergantung pada Energi Ionisasi Makin besar Energi ionisasi makin berkurang sifat logamnya.
Sifat non logam dihubungkan dengan keelektronegtifan Makin besar keelektronegatifan makin bertambah sifat non logamnya.
Presented by: Mochamad Kodim, S.Pd
SIFAT-SIFAT PERIODIK UNSUR
6. TITIK LEBUR DAN TITIK DIDIH
Misalnya: panas
panas
Air (berwujud cair)
Es (berwujud padat)
Uap Air (berwujud gas)
JADI Titik lebur adalah suhu suatu zat dimana fasa padatnya berkesetimbangan dengan fasa cairnya (rentang suhu dimana zat mulai melebur sampai melebur seluruhnya). Titik didih adalah suhu pada saat tekanan uap jenuh cairan sama dengan tekanan luar (tekanan pada permukaan cairan).
Presented by: Mochamad Kodim, S.Pd
SIFAT-SIFAT PERIODIK UNSUR
TITIK LEBUR DAN TITIK DIDIH
No Atom
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20
Unsur
H He Li Be B C N O F Ne Na Mg Al Si P S Cl Ar K Ca
Titik lebur (K)
13.8 3.3 453.5 1550 2030 4000 63 54.2 53.4 24 370.8 923 933 1683 317.2 392 172 83.6 336.7 1111
Titik didih (K)
2.3 4 163 3043 3658 5103 77 90 84.8 27 1165 1443 2723 2953 553 718 238.3 87.2 1033 1713
Presented by: Mochamad Kodim, S.Pd
SIFAT-SIFAT PERIODIK UNSUR
TITIK LEBUR DAN TITIK DIDIH
Presented by: Mochamad Kodim, S.Pd
SIFAT-SIFAT PERIODIK UNSUR
TITIK LEBUR DAN TITIK DIDIH
Dalam 1 periode (dari kiri ke kanan), titik lebur dan titik didih naik sampai golongan IV A (golongan 1, 2, 13 sampai 14), kemudian turun drastis. Dalam 1 golongan (dari atas ke bawah ), ada 2 kecenderungan: Titik lebur dan titik didih unsur golongan 1, 2, 13 sampai 14 semakin berkurang. Titik lebur dan titik didih unsur golongan 15 sampai golongan 18 semakin bertambah.
Presented by: Mochamad Kodim, S.Pd
SIFAT-SIFAT PERIODIK UNSUR
7. OKSIDA ASAM DAN BASA
Unsur-unsur dalam sistem periodik dapat bereaksi dengan oksigen membentuk senyawa oksida. Oksida dapat bersifat asam, basa, atau amfoter
1. Bersifat asam: bila bereaksi dengan air menghasilkan ion hidrogen. Misalnya: SO3(s) + H2O H+(aq) + HSO4-(aq) 4 H+(aq) + 4 H2PO4-(aq)
P4O10(s) + 6 H2O
Presented by: Mochamad Kodim, S.Pd
SIFAT-SIFAT PERIODIK UNSUR
OKSIDA ASAM DAN BASA
Bila tidak larut dalam air, tetapi bereaksi dengan basa membentuk garam. Misalnya: SiO2(s) + Na2O(s) Na2SiO3(s) + H2O Na2SiO3(s) 2Na+(aq) + SiO32-
2. Bersifat basa: bila bereaksi dengan air menghasilkan ion hidroksida. Misalnya: Na2O(s) + H2O BaO(s) + H2O 2Na+(aq) + 2OH-(aq) Ba2+ (aq) + 2OH-(aq)
Presented by: Mochamad Kodim, S.Pd
SIFAT-SIFAT PERIODIK UNSUR
OKSIDA ASAM DAN BASA
3. Bersifat amfoter (bersifat asam sekaligus basa): bila dapat bereaksi dengan asam dan basa. misalnya: Al2O3(s) + 6H+(aq) 2Al3+(aq) + 3H2O 2Al(OH)4-(aq)
Al2O3(s) + 2OH-(aq) + 3H2O
Tabel Oksida asam dan basa periode 3
Golongan Oksida sifat 1 Na2O basa 2 MgO basa 13 Al2O3 amfoter 14 SiO2 asam 15 P2O5 asam 16 SO3 asam 17 Cl2O7 asam 18 -
Presented by: Mochamad Kodim, S.Pd
SIFAT-SIFAT PERIODIK UNSUR
OKSIDA ASAM DAN BASA Tabel oksida asam dan basa
Golongan Periode 1 Periode 2 Periode 3 Periode 4 Periode 5 Keterangan: Merah: asam Hijau: amfoter Biru: basa 1 Li2O Na2O K2O Rb2O Cs2O 2 BeO MgO CaO SrO BaO 13 B2O3 Al2O3 Ga2O3 In2O3 Tl2O3 14 CO2 SiO2 GeO2 SnO2 PbO2 15 N2O5 P4O10 As4O6 Sb4O6 Bi2O3 16 O2 SO2 SeO2 TeO2 PoO2 17 F2 O Cl2O Br2O I2O5 -
Jadi
Presented by: Mochamad Kodim, S.Pd
SIFAT-SIFAT PERIODIK UNSUR
KESIMPULAN
Jari-jari atom adalah jarak dari inti atom hingga elektron terluar. - Dalam 1 golongan = semakin besar - Dalam 1 periode = semakin kecil Energi ionisasi adalah energi minimum yang diperlukan atom netral dalam bentuk untuk melepas satu elektron dan membentuk ion positif yang stabil. - Dalam 1 golongan = semakin kecil - Dalam 1 periode = cenderung semakin besar Afinitas elektron adalah energi yang dilepaskan oleh atom netral dalam bentuk gas bila menerima elektron untuk membentuk ion negatif yang stabil. - Dalam 1 golongan = cenderung semakin kecil - Dalam 1 periode = cenderung semakin besar
Presented by: Mochamad Kodim, S.Pd
SIFAT-SIFAT PERIODIK UNSUR
KESIMPULAN
Keelektronegatifan adalah suatu bilangan yang menyatakan kecenderungan suatu unsur untuk menarik elektron ke pihaknya dalam suatu ikata kimia. - Dalam 1 golongan = cenderung semakin kecil - Dalam 1 periode = cenderung semakin besar
Logam dan Non logam Dalam 1 periode (dari kiri ke kanan), sifat non logamnya makin bertambah. Dalam 1 golongan (dari atas ke bawah), sifat logamnya makin bertambah.
Presented by: Mochamad Kodim, S.Pd
SIFAT-SIFAT PERIODIK UNSUR
KESIMPULAN
Titik didih dan titik lebur. Dalam satu golongan, ada 2 jenis kecenderungan: - Unsur-unsur golongan 1, 2, 13, dan 14 dari atas ke bawah titik lebur dan titik didihnya makin rendah. - Unsur-unsur golongan 15, 16, 17, dan 18 dari atas ke bawah titik lebur dan titik didihnya makin tinggi. Dalam satu periode (dari kiri ke kanan), titik lebur dan titik didihnya semakin naik sampai golongan 14, kemudian turun drastis. Oksidasi Asam dan Basa Dalam 1 periode (dari kiri ke kanan), sifat asamnya makin bertambah. Dalam 1 golongan (dari atas ke bawah), sifat basanya makin bertambah
Presented by: Mochamad Kodim, S.Pd
SIFAT-SIFAT PERIODIK UNSUR
KESIMPULAN
Presented by: Mochamad Kodim, S.Pd
Terima
Kasih
Вам также может понравиться
- 45 Soal Kimia Kelas X Sma Bab Ikatan KimiaДокумент4 страницы45 Soal Kimia Kelas X Sma Bab Ikatan KimiarezazrОценок пока нет
- Tata Nama Senyawa KimiaДокумент7 страницTata Nama Senyawa KimiaFerri FerdiansyahОценок пока нет
- Vsepr 2Документ3 страницыVsepr 2Yemima100% (1)
- Reaksi Penggaraman 6 - 8Документ8 страницReaksi Penggaraman 6 - 8postingkimiaОценок пока нет
- 1 Bidang Datar LicinДокумент7 страниц1 Bidang Datar LicinLestariОценок пока нет
- Soal Latihan Ikatan Kimia Dan Bentuk MolekulДокумент4 страницыSoal Latihan Ikatan Kimia Dan Bentuk MolekulintanОценок пока нет
- Sejarah Perkembangan Tabel Periodik Unsur Dan Sifat-Sifat Yang Ada Pada Tabel Periodik UnsurДокумент6 страницSejarah Perkembangan Tabel Periodik Unsur Dan Sifat-Sifat Yang Ada Pada Tabel Periodik UnsurNuril idha0% (1)
- Soal Larutan Elektrolit Dan Non ElektrolitДокумент11 страницSoal Larutan Elektrolit Dan Non ElektrolitRetno Wulan Gayatri100% (2)
- Sifat Fisika Dan Kimia Unsur Transisi Periode Ke 4Документ14 страницSifat Fisika Dan Kimia Unsur Transisi Periode Ke 4ristaОценок пока нет
- Makalah Kimia Anorganik II - Kel 2 KalsiumДокумент26 страницMakalah Kimia Anorganik II - Kel 2 KalsiumMariati Batma A Silaban100% (1)
- H2OДокумент7 страницH2OAIfa MIzumortОценок пока нет
- Soal Laju ReaksiДокумент3 страницыSoal Laju ReaksiDian DamayantiОценок пока нет
- Latihan Ulangan SPUДокумент11 страницLatihan Ulangan SPUazfadamiaОценок пока нет
- SSP 3 LKPD Isomer HidrokarbonДокумент21 страницаSSP 3 LKPD Isomer HidrokarbonHaeruddin SalengОценок пока нет
- Laporan MagnesiumДокумент9 страницLaporan MagnesiumD NYОценок пока нет
- Bentuk MolekulДокумент6 страницBentuk MolekulekinooristiqomahОценок пока нет
- RPP 2Документ12 страницRPP 2Rahmadannor Pangeran TunggalОценок пока нет
- Materi Bentuk MolekulДокумент42 страницыMateri Bentuk Molekulayu hartatiОценок пока нет
- Soal Astra Babak III Gebyar AtomДокумент8 страницSoal Astra Babak III Gebyar AtomMuhammadRadhiSiriwaОценок пока нет
- Pertemuan 22. Contoh Soal Derajat IonisasiДокумент10 страницPertemuan 22. Contoh Soal Derajat IonisasiAziz ZakiОценок пока нет
- Bahan Ajar Stoikiometri (Kadar, Rm&Re, C Lar., P'RX PMBTS)Документ14 страницBahan Ajar Stoikiometri (Kadar, Rm&Re, C Lar., P'RX PMBTS)Mohamad NashirОценок пока нет
- Jawaban Latihan Soal Reaksi PenggaramanДокумент7 страницJawaban Latihan Soal Reaksi PenggaramanAtina Husnaqilati50% (2)
- Tes DiagnostikДокумент6 страницTes Diagnostikyurianti lamaya50% (2)
- Termokimia PDFДокумент3 страницыTermokimia PDFPujiОценок пока нет
- Soal Sifat-Sifat Unsur Alkali Tanah ZeniusДокумент4 страницыSoal Sifat-Sifat Unsur Alkali Tanah ZeniusLindawati SitorusОценок пока нет
- Soallatihan Termokimia Kelas 11 Ipa Sem 1 N JawabДокумент11 страницSoallatihan Termokimia Kelas 11 Ipa Sem 1 N JawabMuhammad Azhar HadiОценок пока нет
- Contoh Reaksi Eksoterm Dan EndotermДокумент1 страницаContoh Reaksi Eksoterm Dan EndotermTiara RamadhiantiОценок пока нет
- Soal Essay Kimia Kelas 10 Tentang Ikatan KimiaДокумент1 страницаSoal Essay Kimia Kelas 10 Tentang Ikatan KimiaMuhammad KhoirurrizqiОценок пока нет
- Gong LuangДокумент6 страницGong LuangAlya SyauqiОценок пока нет
- 3.10 Tata Nama SenyawaДокумент11 страниц3.10 Tata Nama Senyawawawat resnawatiОценок пока нет
- Ringkasan Olimpiade KimiaДокумент113 страницRingkasan Olimpiade Kimiahendra kusumaОценок пока нет
- Soal Bilangan KuantumДокумент3 страницыSoal Bilangan KuantumKhudrotunnada AdityaОценок пока нет
- Bentuk MolekulДокумент41 страницаBentuk Molekuljayadi haddadОценок пока нет
- Ringkasan Materi Elektrolit Dan Non ElektrolitДокумент7 страницRingkasan Materi Elektrolit Dan Non ElektrolitpuntadewaОценок пока нет
- Soal Dan Pembahasan Bab 6 Persamaan Kimia PDFДокумент3 страницыSoal Dan Pembahasan Bab 6 Persamaan Kimia PDFNaruto UzumakiОценок пока нет
- Penyimpangan Kaidah OktetДокумент30 страницPenyimpangan Kaidah Oktetaufa faraОценок пока нет
- Laporan Praktikum KimiaДокумент17 страницLaporan Praktikum KimiaMuhamad ZaenОценок пока нет
- PembahasanДокумент2 страницыPembahasanRichoco ChannelОценок пока нет
- Bab 1 - Pengenalan Ilmu KimiaДокумент27 страницBab 1 - Pengenalan Ilmu KimiaRestu Dwi AprianОценок пока нет
- Massa Atom Relatif Dan Massa Molekul RelatifДокумент6 страницMassa Atom Relatif Dan Massa Molekul Relatifsi penyuka musikОценок пока нет
- Uji Kepolaran Senyawa AДокумент17 страницUji Kepolaran Senyawa ALailatul_NurfadilaОценок пока нет
- Perkaratan BesiДокумент10 страницPerkaratan Besi'Anis' Cuuplizz Tosca Lapetitefilledesalazar100% (1)
- Soal Sifat Koligatif LarutanДокумент13 страницSoal Sifat Koligatif LarutanAstari WulandariОценок пока нет
- Perkembangan Model AtomДокумент17 страницPerkembangan Model AtomBun YaminОценок пока нет
- Soal Periode 3 Kimia PDFДокумент6 страницSoal Periode 3 Kimia PDFHizqiil NuryashinОценок пока нет
- Kesetimbangan Kimia Dalam MulutДокумент2 страницыKesetimbangan Kimia Dalam MulutAnonymous ySCZN5hwYОценок пока нет
- Rangkuman Kimia PDFДокумент46 страницRangkuman Kimia PDFHana Kiraina100% (3)
- Rumus Empiris Dan Rumus MolekulДокумент11 страницRumus Empiris Dan Rumus MolekulAeniОценок пока нет
- RPP 3Документ20 страницRPP 3anggelОценок пока нет
- Kelarutan Dan Hasil Kali KelarutanДокумент23 страницыKelarutan Dan Hasil Kali KelarutanDwiayuAdinda100% (2)
- Bank Soal UGMДокумент50 страницBank Soal UGMAndhi Putro100% (1)
- Ion KompleksДокумент43 страницыIon KompleksPutri AssalamОценок пока нет
- Kimia Reaksi RedoksДокумент32 страницыKimia Reaksi RedoksLynn WangОценок пока нет
- TERMOKIMIAДокумент17 страницTERMOKIMIASyafiqa50% (2)
- Soal Kimia Konfigurasi ElektronДокумент8 страницSoal Kimia Konfigurasi ElektronWardah FaizahОценок пока нет
- Logam TransisiДокумент7 страницLogam TransisiNuril AlamОценок пока нет
- Sifat Fisika Logam AlkaliДокумент30 страницSifat Fisika Logam AlkaliAnggi AngganaОценок пока нет
- Sifat Dan Reaksi Gol. AlkaliДокумент7 страницSifat Dan Reaksi Gol. AlkaliDefi ElfridaОценок пока нет
- Bab 23 Logam Transisi Dan Senyawa KoordinasiДокумент11 страницBab 23 Logam Transisi Dan Senyawa KoordinasiAnindita IndrianaОценок пока нет
- B. Sifat Fisis Dan Sifat Kimia Unsur-Unsur Gas Mulia, Halogen, Alkali, Alkali Tanah Periode 3 Dan Periode 4 Dewita Triani PutriДокумент32 страницыB. Sifat Fisis Dan Sifat Kimia Unsur-Unsur Gas Mulia, Halogen, Alkali, Alkali Tanah Periode 3 Dan Periode 4 Dewita Triani PutriArthur SanОценок пока нет
- Kimia: Stoikiometri 2Документ6 страницKimia: Stoikiometri 2Occhi A CasperОценок пока нет
- GamelanДокумент22 страницыGamelanOcchi A Casper100% (1)
- Kimia: Soal Minyak BumiДокумент17 страницKimia: Soal Minyak BumiOcchi A CasperОценок пока нет
- Retinopati Pada SLEДокумент10 страницRetinopati Pada SLEOcchi A CasperОценок пока нет
- KarawitanДокумент24 страницыKarawitanOcchi A CasperОценок пока нет
- Kimia: Minyak Bumi 2Документ11 страницKimia: Minyak Bumi 2Occhi A CasperОценок пока нет
- Kompos PDFДокумент26 страницKompos PDFIsroi.comОценок пока нет
- Matematika: Logika Matematika Soal UnДокумент2 страницыMatematika: Logika Matematika Soal UnOcchi A CasperОценок пока нет
- Kimia: Makalah Minyak BumiДокумент11 страницKimia: Makalah Minyak BumiOcchi A Casper50% (2)
- Kimia: Hukum Kekekalan MassaДокумент6 страницKimia: Hukum Kekekalan MassaOcchi A CasperОценок пока нет
- Kimia: StoikiometriДокумент37 страницKimia: StoikiometriOcchi A Casper100% (1)
- Fraksi Minyak BumiДокумент11 страницFraksi Minyak BumiFanny NoviaОценок пока нет
- MikroskopДокумент4 страницыMikroskopOcchi A CasperОценок пока нет
- Artikel Pencemaran Puisi AlamДокумент9 страницArtikel Pencemaran Puisi AlamOcchi A CasperОценок пока нет
- Klasifikasi PegaganДокумент2 страницыKlasifikasi PegaganOcchi A CasperОценок пока нет
- Kimia: Macam-Macam Ikatan KimiaДокумент10 страницKimia: Macam-Macam Ikatan KimiaOcchi A CasperОценок пока нет
- Matematika: Grafik Fungsi KuadratДокумент30 страницMatematika: Grafik Fungsi KuadratOcchi A Casper50% (2)
- Kimia: Kepolaran Senyawa KimiaДокумент2 страницыKimia: Kepolaran Senyawa KimiaOcchi A Casper100% (1)
- Fisika: Teropong Bintang, Panggung, & PantulДокумент11 страницFisika: Teropong Bintang, Panggung, & PantulOcchi A CasperОценок пока нет
- Kimia: Sistem Periodik UnsurДокумент23 страницыKimia: Sistem Periodik UnsurOcchi A CasperОценок пока нет
- Kimia: Ikatan KimiaДокумент42 страницыKimia: Ikatan KimiaOcchi A Casper100% (1)
- Mekanika GerakДокумент13 страницMekanika Geraktembokbatu20100% (1)
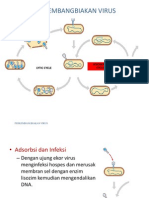
- Biologi: Reproduksi VirusДокумент12 страницBiologi: Reproduksi VirusOcchi A CasperОценок пока нет
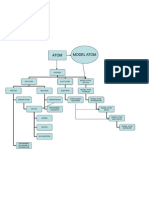
- Kimia: Peta Konsep Struktur AtomДокумент1 страницаKimia: Peta Konsep Struktur AtomOcchi A Casper67% (3)
- Kimia: Peta Konsep Sistem Periodik UnsurДокумент7 страницKimia: Peta Konsep Sistem Periodik UnsurOcchi A Casper75% (4)
- Biologi: ProtozoaДокумент17 страницBiologi: ProtozoaOcchi A CasperОценок пока нет