Академический Документы
Профессиональный Документы
Культура Документы
Exercices Ondes Electromagnetiques Web Corrige
Загружено:
Stéfan Ben RhoumaАвторское право
Доступные форматы
Поделиться этим документом
Поделиться или встроить документ
Этот документ был вам полезен?
Это неприемлемый материал?
Пожаловаться на этот документАвторское право:
Доступные форматы
Exercices Ondes Electromagnetiques Web Corrige
Загружено:
Stéfan Ben RhoumaАвторское право:
Доступные форматы
Les ondes lectromagntiques : Exercices - corrections
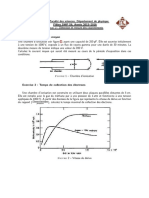
Exercice 1 Les micro-ondes, comme celles quutilisent les radars et les fours micro-ondes, ont des longueurs donde suprieures 3 mm. Quelle est leur frquence ? = c / = 3 . 108 m . s1 / (3 . 103 m) = 1 . 1011 Hz. Donc, < 1 . 1011 s1 .
Exercice 2 Lorsquun faisceau dlectrons frappe un bloc de cuivre, des rayons X de frquence 2.0 . 1018 Hz sont mis. Quelle est la longueur donde (en pm) de ces rayons X ? = c / = 3 . 108 m . s1 / (2.0 . 1018 s1) = 1.5 . 1010 m = 1.5 . 102 pm .
Exercice 3 Les ondes de votre station FM prfre sont produites 99.3 MHz. Quelle est la longueur donde de cette station ? = c / = 3 . 108 m . s1 / (99.3 . 106 s1) = 3.021148 m 3.02 m .
Exercice 4 Les lampes vapeur de sodium utilises pour lclairage public mettent une lumire jaune 589 nm. Quelle est lnergie vhicule par cette onde ? E = h . = h . c / = 6.62618 . 1034 J . s . 3 . 108 m . s1 / (589 . 109 m) = 3.3749644 . 1019 J 3.37 . 1019 J .
Exercice 5 Nommez les rgions du spectre lectromagntique voisines du spectre visible vers (a) les hautes nergies ; (b) les basses nergies. a) UV ( < 400 nm) b) IR ( > 730 nm)
Exercice 6 Lnergie pour rompre la liaison CC est 348 kJ/mol. Une lumire violette de longueur donde 420 nm peut-elle rompre une telle liaison ? Energie pour rompre une liaison : E = Etot / NA = 348 . 103 J . mol1 / (6.022 . 1023 mol1) = 5.7788 . 1019 J. Energie lumineuse : E = h . = h . c / = 6.62618 . 1034 J . s . 3 . 108 m . s1 / (420 . 109 m) = 4.7329857 . 1019 J. Non, la lumire violette de = 420 nm ne peut pas dtruire la liaison CC.
Exercice 7 Quelles sont la longueur donde et la frquence du rayonnement susceptibles de provoquer lionisation dun atome dhydrogne son tat fondamental ? Eionisation, (H, littrature) = 1.31 . 106 J . mol1. Pour un seul atome : E = Etot / NA = 2.1754 . 1018 J = E / h = 2.1754 . 1018 J / (6.62618 . 1034 J . s) = 3.282973 . 1015 s1 3.28 . 1015 s1 . = c / = 3 . 108 m . s1 / (3.282973 . 1015 s1) = 9.1381 . 108 m 91.4 nm .
Exercice 8 Vous voulez prendre le spectre UV-VIS dune substance dont la masse molaire vaut 738 g/mol. Dans les tables, vous avez trouv qu max = 298 nm, vaut 4870 L . mol1 . cm1. Quelle masse de cette substance devrez-vous dissoudre dans 10 mL de solvant pour que dans une cuvette de quartz de 1.000 cm, labsorbance maximale soit de 0.800 ? c = A / . d = 0.800 / (4870 L . mol1 . cm1 . 1.000 cm) = 1.6427 . 104 mol . L1. n = c . V = 1.6427 . 104 mol . L1 . 10 . 10-3 L = 1.6427 . 106 mol. m = n . M = 1.6427 . 106 mol . 738 g . mol1 = 1.2123 . 103 g 1.21 . 103 g .
Вам также может понравиться
- corrigeExoOndes 1415Документ3 страницыcorrigeExoOndes 1415khadijaОценок пока нет
- AthomistiqueДокумент32 страницыAthomistiqueMaria ShuckahoseeОценок пока нет
- Exercices RX CorrigésДокумент4 страницыExercices RX CorrigésablearnОценок пока нет
- SERIE2 CorrigeeДокумент7 страницSERIE2 CorrigeeAhmed Jebbouri100% (1)
- TD1 Et 2-IRM1Документ15 страницTD1 Et 2-IRM1مارية حسنينОценок пока нет
- MicrophonesДокумент53 страницыMicrophonesbetaОценок пока нет
- 2020 Cours TD Physiquenuclaire 2 PDFДокумент42 страницы2020 Cours TD Physiquenuclaire 2 PDFAyoub El Hasnaoui100% (1)
- L'optique GéométriqueДокумент18 страницL'optique GéométriqueZakari Yae100% (1)
- DS Sons1Документ7 страницDS Sons1Sié Jérémie KambiréОценок пока нет
- Theorie de La Fonctionnelle de DensiteДокумент15 страницTheorie de La Fonctionnelle de DensiteMouniaОценок пока нет
- Analyse Spectrale Rayonnement InfrarougeДокумент18 страницAnalyse Spectrale Rayonnement InfrarougeMohamed KouryaniОценок пока нет
- M14 - TD N°2: Spectrométrie Infra Rouge: Master (PACQ)Документ2 страницыM14 - TD N°2: Spectrométrie Infra Rouge: Master (PACQ)Imane MouamrОценок пока нет
- TP Étudier La Propagation D'une Onde UltrasonoreДокумент1 страницаTP Étudier La Propagation D'une Onde UltrasonoreMohieddine KhailiОценок пока нет
- SpectresДокумент43 страницыSpectresayman lamzouriОценок пока нет
- Interferences PCДокумент53 страницыInterferences PCDaboОценок пока нет
- Chap5 PHONON II Propriétés Thermiques - ENSTAB CoursewareДокумент17 страницChap5 PHONON II Propriétés Thermiques - ENSTAB CoursewareTunENSTAB100% (1)
- TD2 Tech T 2020Документ2 страницыTD2 Tech T 2020Elyes KОценок пока нет
- Cont 1 s1 PC 2 Bac Prof - Filali (WWW - Pc1.ma)Документ1 страницаCont 1 s1 PC 2 Bac Prof - Filali (WWW - Pc1.ma)said youssfiОценок пока нет
- 8 ExercicesДокумент3 страницы8 ExercicesSedraniaina Iavo100% (1)
- SERIE3 CorrigeeДокумент5 страницSERIE3 CorrigeeSaid MrfОценок пока нет
- Exposé SohaДокумент12 страницExposé Sohafati100% (1)
- TSP1SP2Ch6T4-Exo p177 n22 CorrectionДокумент2 страницыTSP1SP2Ch6T4-Exo p177 n22 Correctionsamibdz100% (1)
- Polarisation Du LumiereДокумент16 страницPolarisation Du Lumierevisual and outfits victizmed kim taehyungОценок пока нет
- Interferences Lumineuses CoursДокумент4 страницыInterferences Lumineuses CoursSami Khouja0% (1)
- FiltreДокумент19 страницFiltrelamilouch6498Оценок пока нет
- Exercices Corrigés Chimie QuantiqueДокумент4 страницыExercices Corrigés Chimie QuantiqueRottina Rossy100% (1)
- Chapitre 14 Diagramme e PHДокумент9 страницChapitre 14 Diagramme e PHAbdelhakim BailalОценок пока нет
- Ondes Et Transformations NucléairesДокумент73 страницыOndes Et Transformations NucléairesM U S I C100% (2)
- 03 Propagation Des Ondes ElectromagnetiquesДокумент5 страниц03 Propagation Des Ondes ElectromagnetiquesHamza BadrОценок пока нет
- Exercice PhysiquesДокумент6 страницExercice PhysiquesBenAngel NzóОценок пока нет
- Phenomenes Non Lineaires en ElectroniqueДокумент22 страницыPhenomenes Non Lineaires en ElectroniqueMohammed AlaouiОценок пока нет
- TD2 5ieme IGEДокумент2 страницыTD2 5ieme IGElahbak abderrahmeneОценок пока нет
- Nouha Ramadan Terminal S 2010-AmSud-Exo1-Correction-Lumiere-7ptsДокумент2 страницыNouha Ramadan Terminal S 2010-AmSud-Exo1-Correction-Lumiere-7ptsrihab100% (1)
- LICENCE PROFESSIONNELLE INDUSTRIES CHIMIQUES ET PHARMACEUTIQUES Option DM PDFДокумент9 страницLICENCE PROFESSIONNELLE INDUSTRIES CHIMIQUES ET PHARMACEUTIQUES Option DM PDFTaouil MohamedОценок пока нет
- TEP SubatomiqueДокумент56 страницTEP SubatomiqueKhalid GarbaОценок пока нет
- Le Radar de Recul PDFДокумент3 страницыLe Radar de Recul PDFanasОценок пока нет
- 7interference Par Division D'amplitudeДокумент20 страниц7interference Par Division D'amplitudeSedraniaina IavoОценок пока нет
- Quelques Gnralits Sur Les Plasmas - Exercice - PDFДокумент9 страницQuelques Gnralits Sur Les Plasmas - Exercice - PDFNadaОценок пока нет
- Corps NoirДокумент11 страницCorps NoirManuel ArzolaОценок пока нет
- Exos Corrigé El JadidaДокумент11 страницExos Corrigé El JadidaYoussef Taoufiki0% (1)
- Résume de Cristallo HC - CFC - CS - CC PDFДокумент47 страницRésume de Cristallo HC - CFC - CS - CC PDFØptímí Štã100% (1)
- Ondes StationnairesДокумент6 страницOndes StationnaireshammouОценок пока нет
- Chap. 1 - IntroductionДокумент40 страницChap. 1 - IntroductionRabah AmidiОценок пока нет
- ZZZ Palan Plan Incline TP 2Документ1 страницаZZZ Palan Plan Incline TP 2saidi chaoukiОценок пока нет
- SemiconducteursДокумент100 страницSemiconducteurssebastien100% (2)
- Exercice OndesДокумент2 страницыExercice OndesmohaaamedОценок пока нет
- Exercice Antenne PDFДокумент2 страницыExercice Antenne PDFHeather43% (7)
- TP 2 MNДокумент9 страницTP 2 MNAmir Na DzОценок пока нет
- Dossier #1 (Les Ondes)Документ17 страницDossier #1 (Les Ondes)amine boukhssibiОценок пока нет
- Applications de la spectrophotomérie en phytochimie: sciencesОт EverandApplications de la spectrophotomérie en phytochimie: sciencesОценок пока нет
- Physique ChimieДокумент8 страницPhysique Chimieabdellilah777hattabОценок пока нет
- Chimie TD 3 Cinétique Chimique PDFДокумент4 страницыChimie TD 3 Cinétique Chimique PDFOussama El BouadiОценок пока нет
- Le Spin Du Photon Et de L'électronДокумент3 страницыLe Spin Du Photon Et de L'électronBernard SCHAEFFERОценок пока нет
- TD A11 04 Adaptation ImpedanceДокумент2 страницыTD A11 04 Adaptation ImpedanceMariam Zouhair100% (1)
- MVT Force Centrale - ExosДокумент6 страницMVT Force Centrale - Exosabderrahim najim100% (1)
- TD Chromatographie en Phase Gazeuse de L3Документ6 страницTD Chromatographie en Phase Gazeuse de L3Kharoubi NassimaОценок пока нет
- Incertitude SДокумент16 страницIncertitude SSeif HabbachiОценок пока нет