Академический Документы
Профессиональный Документы
Культура Документы
Apostila de Termodinamica
Загружено:
Adriano RuizАвторское право
Доступные форматы
Поделиться этим документом
Поделиться или встроить документ
Этот документ был вам полезен?
Это неприемлемый материал?
Пожаловаться на этот документАвторское право:
Доступные форматы
Apostila de Termodinamica
Загружено:
Adriano RuizАвторское право:
Доступные форматы
Notas de Aula / Fenmenos de Transportes / Parte1 : Termodinmica Prof. Jorge M.
Moraes
1. Termodinmica
Os princpios bsicos das cincias trmicas esto includos na Termodinmica, Mecnica dos Fludos e Transferncia de Calor. Termodinmica (algumas definies): a) a cincia da energia e da entropia; b) a cincia que trata do calor e do trabalho, e daquelas propriedades das substncias relacionadas ao calor e ao trabalho; c) cincia que se preocupa com o estudo das transformaes da energia e o relacionamento entre as vrias grandezas fsicas de uma substncia afetadas por aquelas transformaes energticas. A base da termodinmica, como a de outras cincias a observao experimental. Mecnica dos Fludos: estudo do comportamento dos fludos em repouso ou em movimento. Transferncia de Calor: a energia em trnsito devido a uma diferena de temperatura.
Exemplos a serem ilustrados em aula : ciclo motor (pg. 247, Van Wylen et al.), ciclo de refrigerao (pg. 283, Van Wylen et al.) *****Energia: conceito de difcil definio, tecnicamente pode ser entendido como : capacidade de realizar trabalho ou ainda capacidade de realizaes.
1 .1. Conceitos e definies Sistema termodinmico: quantidade de massa e identidade fixas, sobre a qual nossa ateno dirigida para o estudo. Os limites (ou fronteiras) do sistema podem ser fixos ou mveis e o tudo o mais externo chamado vizinhana ou exterior. Calor e trabalho podem cruzar a fronteira do sistema.
fronteira do sistema sistema W (trabalho)
Q (calor)
g s
W (trabalho)
fronteira do Sistema
Q (calor)
Notas de Aula / Fenmenos de Transportes / Parte1 : Termodinmica Prof. Jorge M. Moraes
Volume de controle : um volume arbitrrio do espao no qual pode haver fluxo de massa, calor e trabalho.
volume de controle
calor Q descarga trabalho W
admisso
compressor
motorr
superfcie de controle
Propriedade : quantidade observvel (quantificvel) da substncia. extensiva : proporcional massa (volume, energia, etc.) intensiva : independe da massa (temperatura, presso, etc.) especfica : obtida dividindo-se uma propriedade extensiva pela massa da respectiva substncia. Uma propriedade especfica tambm uma propriedade intensiva do sistema. Ex.: volume especfico = Volume/Massa (do sistema)
Fase : quantidade de matria totalmente homognea Estado : diferentes propriedades (temperatura, presso, vol.especfico, etc.) em que a substncia pode estar em cada fase Processo : caminho definido pela sucesso de estados atravs dos quais o sistema passa. E podem ser : - isotrmico : temperatura constante - isobrico : presso constante - isomtrico : volume constante - isoentlpico: entalpia constante - adiabtico : sem transferncia de calor - isoentrpico: entropia constante
W (trabalho)
Desenho embolo :
fronteira do Sistema
Q (calor)
Notas de Aula / Fenmenos de Transportes / Parte1 : Termodinmica Prof. Jorge M. Moraes
O processo pode ser tambm : reversvel : o processo que pode retornar ao seu estado original simplesmente invertendo o caminho, ou a sequncia de estados aos quais ele foi submetido, sem deixar marcas nem no sistema nem na vizinhana. Irreversvel : processo onde ocorrem alteraes provocadas por diferena finita de potencial, e portanto no pode ser revertido de forma expontnea. Todos os fenmenos reais observveis no universo fsico apresentam esta caracterstica.
Ciclo : um sistema em um dado estado inicial, passa por certo nmero de mudanas de estado ou processos e finalmente retorna ao estado inicial (no final do ciclo todas as propriedades tem o mesmo valor inicial. - ciclo termodinmico: quando o fluido de trabalho percorre um ciclo dentro do motor. Ex : ciclo motor ou refrigerador - ciclo mecnico: quando o fluido de trabalho no percorre um ciclo. Ex. : motor de combusto o ar e o combustvel queimados e transformados nos produtos de combusto so descarregados pela atmosfera.
1.2. Unidades de massa, comprimento, tempo e fora. Essas grandezas esto relacionadas com a 2a lei de Newton: F=ma Onde: F fora; m massa; a acelerao
P F m g=9,81 m/s2 m
No Sistema Internacional (SI): Se m= 1kg e a=1m/s2 F=1 kgm/s2 = 1 N
Se m=10 kg e g=9,81 m/s2 P=98,1 kgm/s2 = 98,1 N
Distino entre massa e peso:
Notas de Aula / Fenmenos de Transportes / Parte1 : Termodinmica Prof. Jorge M. Moraes
Massa a propriedade de um corpo que a medida da sua inrcia ou resistncia uma mudana no movimento. E tambm uma medida da quantidade de substncia. Peso a fora com a qual um corpo atrado na direo da terra pela gravidade.
1.2.1. Sistemas de Unidade
1.2.1.1. Sistema Intenacional SI : unidades bsicas Grandeza Comprimento Tempo Massa Fora ou Peso Presso Energia Potncia Volume rea Vazo Fluxo de massa Densidade Peso especfico Definio bsica Unidade SI metro [m] segundos[s] kilogramas [kg] Newton [N] [N/m2] ou Pascal [Pa] N.m ou Joule [J] N.m/s ou J/s m3 m2 m3/s kg/s kg/m3 N/m3 Outras unidades usuais milmetro[mm];kilmetro[km] horas[h];minutos [min] N.s2/m kg.m/s2 kilopascal [kPa]; bar Kg.m2/s2 Watt [W]; kW litro[L] mm2 L/s ; L/min kg/h Ns2/m4 kg/m2.s2
quantidade da substncia puxa ou empurra um corpo Fora/rea Fora x distancia Energia/tempo (Comprimento)3 (Comprimento)2 Volume/tempo Massa/tempo Massa/volume Peso/volume
F = m a = kg.m/s2 = Newton (uma fora de 1 N aplicado a uma massa de 1 kg resultar numa acelerao de 1 m/ s2) 1.2.1.2. Sistema Gravitacional Ingls : unidades bsicas Grandeza Comprimento Tempo Massa Fora ou Peso Presso Energia Potncia Volume Definio bsica Unidade SI ps (foot) [ft] segundos[s] slug libra (pound) [lb] [lb/ft2] ou [psf] lb.ft lb.ft/s ou J/s ft3 Outras unidades usuais polegadas(inches)[in];milhas [mi] horas[h];minutos [min] [lb-s2/ft] kip [1000 lb] lb/in2[psi] lb.in cavalos (horsepower) [hp] gales (gallon)[gal]
quantidade da substncia puxa ou empurra um corpo Fora/rea Fora x distancia Energia/tempo (Comprimento)3
Notas de Aula / Fenmenos de Transportes / Parte1 : Termodinmica Prof. Jorge M. Moraes
rea Vazo Fluxo de massa Densidade Peso especfico
(Comprimento)2 Volume/tempo Massa/tempo Massa/volume Peso/volume
ft2 ft /s ou [cfs] slug/s slug/ft3 lb/ft3
3
in2 gal/min[gpm] ; ft3/min [cfm] lb/h; lb/min
Obs.: Slug difcil compreenso m = F/a = lb/ ft/ s2
Tabela de Prefixos : _________________________________________________ Prefixo Simbolo SI fator _________________________________________________ giga G 109 mega M 106 kilo k 103 milli m 10-3 micro 10-6 _________________________________________________ Ex.: 1kPa = 103 Pa = 1000 Pa (lembrando : Pascal, unidade de Presso = N/m2) g = 9,81 m/s2 (sistema internacional SI) g = 32.2 ft/s2 (sistema gravitacional Ingls ou sistema usual US )
1.3 - Lei Zero da Termodinmica
Quando dois corpos tem a mesma temperatura dizemos que esto em equilbrio trmico entre si. Podemos definir a lei zero da termodinmica como: " Se dois corpos esto em equilbrio trmico com um terceiro eles esto em equilibrio trmico entre si ". A lei zero da termodinmica define os medidores de temperatura, os TERMMETROS.
Notas de Aula / Fenmenos de Transportes / Parte1 : Termodinmica Prof. Jorge M. Moraes
1.4 - Escalas de Temperatura
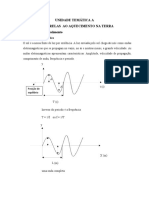
O funcionamento dos termmetros est baseada na lei zero da termodinmica pois so colocados em contato com um corpo ou fluido do qual se deseja conhecer a temperatura at que este entre em equilbrio trmico com o respectivo corpo. A escala do aparelho foi construda comparando-a com um termmetro padro ou com pontos fsicos fixos de determinadas substncias. Quatro escalas de temperatura so hoje usadas para se referir temperatura, duas escalas absolutas e duas escalas relativas; so elas respectivamente: Escala KELVIN (K) e RANKINE (oR) e escala Celsius (oC) e Fahrenheit (oF). A Fig. Abaixo mostra as quatro escalas de temperatura e a relao entre elas.
As escalas de temperatura e sua inter-relao Tipos de Termmetros - Termmetro de Mercrio em vidro - Termmetro de Alcool em vidro - Termmetro de Par Bimetlico - Termmetro de Termistores - Termmetro de Gs Perfeito - Termmetro de Termopar - Pirmetro tico - etc. Exemplo : Escreva a relao entre graus Celsius ( oC ) e Fahrenheit ( oF ) ( expanso volumtrica ) ( expanso volumtrica ) ( dilatao linear diferenciada ) ( variao da resistividade ) ( expanso volumtrica ) ( fora eletromotriz ) ( cor da chama )
Notas de Aula / Fenmenos de Transportes / Parte1 : Termodinmica Prof. Jorge M. Moraes
Soluo - Considere-se a escala dos dois Termmetros, Celsius e Fahrenheit como mostrado na figura Interpolando linearmente as escalas entre a referncia de gelo fundente e a referncia de vaporizao da gua temos:
C 0 O F 32 = 100 0 212 32
O
C=
5 O ( F 32) 9
1.5. O contnuo Na maioria das aplicaes da Engenharia interessa-se pela mdia ou os efeitos macroscpicos do conjunto de numerosas molculas, os quais podemos perceber e medir. O fluido portanto tratado como uma substncia que pode ser dividida ao infinito, num contnuo, sem se preocupar com o comportamento individual de suas molculas.
m V
V = lim V V m V
V valor mnimo que permite avaliar a densidade de um ponto
1.6. Presso
Definio : fora normal agindo sobre uma superfcie por unidade de rea desta superfcie. A presso num ponto a relao entre a fora normal e a rea quando esta tende a um valor limite sempre contendo um ponto.
Notas de Aula / Fenmenos de Transportes / Parte1 : Termodinmica Prof. Jorge M. Moraes
p =
F A
Dois princpios importantes sobre a presso foram descritos por Blaise Pascal (sculo 17): a presso age uiformemente em todas as direes numa pequena quantidade de fluido
em um fluido confinado por superfcies slidas a presso age perpendicular s superfcies
Fig.1.2 Mott Fig 1.3 Mott
Fig. :
Presso em um ponto
Fig. : circular
Presso agindo perpendicularmente s superfcies em : a) barragem e b) duto
1.6.1. Presso absoluta e presso medida
Po
Presso absoluta
Po Presso medida (manomtrica)
Presso atmosfrica
Presso medida negativa (vcuo)
Presso atmosfrica
Presso absoluta
Notas de Aula / Fenmenos de Transportes / Parte1 : Termodinmica Prof. Jorge M. Moraes
Fig. Diagrama de presses manomtricas e absoluta
Pabs = Pman + Patm Patm = 101,325 kPa = 2116 lb/ft2 = 14,7 psi (lb/in2) = 760 mm Hg = 10,34 m gua
Obs : Apesar da unidade do SGI ser lb/ft2 ela no comumente usada . Para o comprimento a unidade mais utilizada a polegada (in) assim como a unidade lb/in2 = psi (pound square inch) para a presso. psia = presso absoluta psig = presso manomtrica (g de gage) O bar = 105 Pa = 105 N/m2 outra unidade usual. **** Conveno : em termodinmica toda vez no dito a presso absoluta Ex.:2.10 Van Wylen. Cilindro vertical provido de pisto (diam=150 mm) contm leo hidrulico. A presso atmosfrica 1 bar . Qual a massa do pisto se a presso interna 125 kPa. (g=9.80665m/s2). Pleo = Patm + P pisto = 102 (kPa) + Ppisto = 125 kPa Ppisto = F/A = m.g/A = 25 kPa A= D2/4 = 0,15 2/4 = 0,01767 m2
pisto mvel Patm
lquido
m = 25 103 [Pa] . 0,01767 [m2] / 9,80665 [m/s2] = 45,0459 kg
1.7. Densidade, volume especfico, peso especfico e densidade especfica Devido s definies de contnuo mais conveniente telacionar a massa e o peso de um fluido em relao a um dado volume. Densidade (massa especfica) : quantidade de massa por unidade de volume :
m V
unidades : SI [Kg/m3 ] e SGI [ slug/ft3]
Notas de Aula / Fenmenos de Transportes / Parte1 : Termodinmica Prof. Jorge M. Moraes
10
Volume especfico : o inverso da densidade 1
v =
Peso especfico : peso por unidade de volume de uma substncia
Ps mg = V V
Unidades : SI [N/m3] SGI [lb/ft3]
Densidade especfica : a relao entre a densidade de uma substncia com a densidade da gua a 4 0C. esp = fluido gua 4oC = fluido gua 4oC
1.8. Propriedades de uma substncia pura
1.8.1. Substncia pura Definio: - tem composio qumica homognea e invarivel pode existir em mais de uma fase (estado homogneo de agregao das molculas) substncia pura compressvel simples: substncia pura na ausncia de efeitos de movimento, ao da gravidade e efeitos de superfcie, magnticos ou eltricos.
Notas de Aula / Fenmenos de Transportes / Parte1 : Termodinmica Prof. Jorge M. Moraes
11
equilbrio de fases de uma substncia pura :
Ex. : processo de vaporizao : presso mantida constante a 101,35 kPa = 0,10135 Mpa (Ver tabela A 1 pag. 517 Van Wylen et al.)
1 a b 2 c 3
vapor Q gua T1 = 20oC gua T2 = 100 C
o
vapor T2 = 100oC
vapor T3 > 100oC
gua T2 = 100oC
T aumenta bastante V aumenta ligeiramente
P e T constantes V aumenta bastante
T aumenta V aumenta
temperatura de saturao : temperatura na qual se d a vaporizao de uma substncia pura a uma dada presso (presso de saturao). Ex.: gua a 101325 Pa (presso atmosfrica) a temperatura de saturao 100o C. presso de saturao ou presso de vapor : para uma dada temperatura, a presso na qual ocorre a vaporizao chamada presso de saturao ou presso de vapor.
Curva de presso de vapor P
Lquido Vapo r
lquido saturado: lquido que se encontra temperatura e presso de saturao.(x=0) lquido sub-resfriado: lquido cuja temperatura menor que a de saturao para uma determinada presso.
Notas de Aula / Fenmenos de Transportes / Parte1 : Termodinmica Prof. Jorge M. Moraes
12
ttulo : quando uma substncia existe, parte lquida e parte vapor, na temperatura de saturao, seu ttulo definido como a relao entre a massa de vapor e a massa total : x=
m m
total
m +m
v
v l
T 374,14oC
vapor saturado: quando a substncia se encontra completamente como vapor a temperatura de saturao. (x=1) vapor superaquecido: quando o vapor est a uma temperatura maior que a temperatura de saturao. Diagrama temperatura-volume
40 MPa 22,09 MPa ponto crtico
linhas de presso constante
1 MPa
99,6oC
0,1 MPa 1 2a 2b linha de lquido saturado 2c linha de vapor saturado
1.lquido sub-resfriado (comprimido) 2a. lquido saturado (x=0) 2b. mudana de fase 2c. vapor saturado (x=1) 3.vapor superaquecido
V
ponto triplo : corresponde a uma combinao de presso e temperatura onde possvel haver equilbrio entre fases solida, lquida e gasosa
P 22,09 MPa Lquido linha de vaporizao 0,6113 kPa Slido linha de sublimao Vapo r -0,01oC 374,14o C T ponto triplo linha de fuso ponto crtico
Notas de Aula / Fenmenos de Transportes / Parte1 : Termodinmica Prof. Jorge M. Moraes
13
propriedades independentes : so propriedades nas quais no se pode determinar uma delas atravs do conhecimento da outra. Ex.: numa mudana de fase presso e temperatura no so independentes e portanto no so suficientes para determinar o estado. Ex.: de propriedades independentes : estado de saturao (Pxv ; Pxx, Txx ); fase vapor (PxT, Pxv, Txv)
1.8.2. Equao de estado para a fase vapor de uma substncia pura compressvel simples A partir de observaes experimentais estabeleceu-se que o comportamento P- v T dos gases a baixa massa especfica dado pela equao dos gases perfeitos : Pv =RT onde: P presso absoluta (manomtrica + atmosfrica) [Pa] v - volume molar especfico [ m3/kmol] R constante universal dos gases [8,3145 kJ/kmol-K] T temperatura absoluta [K]= oC + 273,15 Se dividirmos os dois lados pelo peso molecular M a equao de estado na base mssica fica : Pv=RT onde R = R/M que a constante para um gs particular.[J/kg-K] [N.m/kg-K] v= volume especfico [m3/kg] Ex.: Considere o ar atmosfrico como um gs ideal e determine o volume especfico e a densidade para a presso atmosfrica padro na temperatura de 20 oC. ( adote a massa molecular do ar = 28,97 kg/kmol , R = 8 314 J/ kmol-K ) Soluo Para a hiptese de gs ideal temos:
P v = RT
v=
RT P
A constante particular do gs dada por: 8314 R R= 28,97 M logo, o volume especfico ser
R=
Ra r 287
J kg K
** J=N.m
Notas de Aula / Fenmenos de Transportes / Parte1 : Termodinmica Prof. Jorge M. Moraes
14
a)
287 . (273,15 + 20) v= 101325
m3 0,8303 kg
A densidade o inverso do volume especfico, assim; b)
1 v
1 = 1,204 0,8303
kg m3
Lei de Boyle e Charles
P V1 = m R T1 1
P2 V2 = m R T2
P V1 P2 V2 1 = T1 T2
Gs real
z=
Pv RT
z fator de compressibilidade
Para um gs perfeito z=1 e o desvio de z em relao unidade uma medida do desvio da relao real comparada equao de estado dos gases perfeitos. z<1 - densidade real maior que a de um gs perfeito z>1 densidade real menor que a de um gs perfeito Do ponto de vista prtico : 1- para presses muito baixas P << Pcritica : comportamento de gs perfeito para qualquer temperatura; 2- para temperaturas elevadas T> 2Tcritica : comportamento de gs perfeito at da ordem de 4 a 5xPcritica; 3- T < Tcritica e P no muito baixa : vapor superaquecido desvio do comportamento do gs perfeito melhor usar tabelas. **** VER EXEMPLOS PAG 41 Van Wilen*****
Notas de Aula / Fenmenos de Transportes / Parte1 : Termodinmica Prof. Jorge M. Moraes
15
1.8.3. Tabelas de propriedades termodinmicas
ponto crtico
Lquido Sub-resfriado
Vapor superaquecido linha de presso constante
vl vlv
linha de lquido saturado
vv
linha de vapor saturado v (volume especfico)
vlv = v v vl v = x vv + (1 x)vl v = vl + x vlv
*****Essas equaes servem para outras propriedades (ex.: h e s ) Ex.: pg. 43 Van Wylen Calcular o volume especfico da gua (mistura de vapor e lquido) a T= 200 oC com um ttulo de 70 %. Tab. A1.1. pg 518 Ttulo : x = 0,7 v = 0,7 (0,12736) + 0,3 (0,001156) = 0,0895 [m3/kg] vl=0.001156 [m3/kg] vv= 0.12736 [m3/kg]
Exemplos : Ttulo : Ex pg 40 Schimidt.
Notas de Aula / Fenmenos de Transportes / Parte1 : Termodinmica Prof. Jorge M. Moraes
16
Encontre o ttulo de uma mistura lquido-vapor onde vl=0,00101[m3/kg] , vv=0,00526 [m3/kg] e uma massa total de 2,0 kg e volume 0,01 m3. v = V/m = 0,01/2 = 0,005 [m3/kg]
v = vl + x vlv
x=
v vl 0,005 0,00101 = 0,938 = 0,00526 0,00101 vlv
93,88% de vapor e 6,12% de lquido
*****VER EXEMPLOS PAG 46 VAN WYLEN*******
DIAGRAMAS MAIS UTILIZADOS
Notas de Aula / Fenmenos de Transportes / Parte1 : Termodinmica Prof. Jorge M. Moraes
17
2. Trabalho e Calor 2.1. Definio Trabalho Trabalho : usualmente definido como uma fora F agindo atravs de um deslocamento x (na direo da fora) :
W = F dx
1
[N.m = Joule]
Termodinamicamente um sistema realiza trabalho se o nico efeito sobre o meio for equivalente ao levantamento de um peso ou ainda toda a energia em transito, no associada transferncia de massa, que no seja calor.
ventilador
W
motor motor
polia
equivalente bateria
fronteira
bateria
fronteira
peso
a) W cruza a fronteira
motor
b) W no cruza a fronteira
bateria
fronteira
Notas de Aula / Fenmenos de Transportes / Parte1 : Termodinmica Prof. Jorge M. Moraes
18
W
motor
polia
bateria
peso
c) desprezando perdas eltricas e de atrito pode-se considerar como sendo o levantamento de um peso o nico efeito. Portanto : fluxo de eletricidade atravs da fronteira trata-se de trabalho
fronteira
Q >0 => +
Conveno de sinais :
Sistema W < 0 => W > 0 => +
Unidades : SI : 1J = 1 N.m Potncia : Trabalho por unidade de tempo
W=
.
Q < 0 => -
W dt
[Watts ( W ) = J / s]
** A diferencial de trabalho uma diferencial inexata ( ao invs de d), isto , so funo do processo ou de linha (dependem do caminho). As propriedades termodinmicas so diferenciais exatas (d) ou funo de ponto (independem do caminho). Outras unidades usuais :
Trabalho kJ kWh Hph CVh kcal BTU Potncia kJ/s = kW kW Hp CV kcal/h BTU/h
Notas de Aula / Fenmenos de Transportes / Parte1 : Termodinmica Prof. Jorge M. Moraes
19
2.2. Trabalho realizado devido ao movimento de fronteira de um sistema compressvel simples num processo quase esttico
dL gs 1 retirando o peso menor gs
W = F dx W = P A dL = P dV
1W2 = W = 1 2
P dV
1
Como P funo de V essa integrao somente pode ser efetuada se conhecermos a relao entre P e V
Ex: Movimento de um pisto
P 2
V2
V1
Soluo grfica :
W =
1
P dV
1
= rea sob a curva
Entretanto possvel ir do estado 1 ao estado 2 por vrios caminhos :
P 2 C
W A WB WC
B A
Notas de Aula / Fenmenos de Transportes / Parte1 : Termodinmica Prof. Jorge M. Moraes
20
Portanto : W depende do caminho => funo de linha => diferencial inexata (W) Duas classes de solues do problema : 1 relao entre P e V determinada experimentalmente ou em forma grfica; 2 relao entre P e V dada em forma de equao e essa integrada.
Ex.: Pg 57 do Van Wylen : Um exemplo comum desse segundo tipo de relao o caso de um processo chamado politrpico, no qual P V n = cons tan te , atravs de todo o processo. O expoente "n" pode tomar qualquer valor entre - e + dependendo do processo particular sob anlise.
PV = cons tan te = P1 V = P2 V
n n 1 n 2
cons tan te P1 V1n P2 V2n P= = = Vn Vn Vn
Para esse tipo de processo, podemos integrar a Eq. 3.1-3, resultando em:
PdV = cons tan te
2 1
dV V n +1 = cons tan te ( ) n +1 Vn
2 1
cons tan te 1 n ( V2 V11 n ) = 1 n P2 V2 P1 V1 1 n
1 P2 V2n V2 n P1 V1n V11 n 1 n
PdV =
Note-se que este resultado vlido para qualquer valor do expoente n, exceto n = 1. No caso onde n = 1, tem-se;
PV = Constante = P1V1 = P2V2 , e portanto,
PdV = P1V1
2 1
dV V
= P1 V1 ln
V2 V1
Exemplo 4.1 do Van Wylen pg. 58. 2.3. Calor Calor uma forma de energia transferida atravs da fronteira do sustema numa dada temperatura a um outro sistema (ou meio) numa temperatura inferior, em virtude da diferena de temperatura entre os dois sistemas.
Notas de Aula / Fenmenos de Transportes / Parte1 : Termodinmica Prof. Jorge M. Moraes
21
Unidade SI (J-Joule) Fluxo de calor :
Q [Watts ( W ) = J / s] dt Comparao entre trabalho e calor : Q=
.
a) so fenmenos transitrios (os sistemas nunca possuem calor ou trabalho) b) so fenmenos de fronteira c) ambas so funes de linha e tem diferenciais inexatas 3. 1a Lei da Termodinmica (Lei da Conservao da Energia) 3.1. 1a Lei para um sistema percorrendo um ciclo Para um sistema percorrendo um ciclo a integral cclica do trabalho proporcional a integral cclica do calor transferido
J Q = W
calor lquido transferido durante o ciclo = trabalho lquido durante o ciclo onde J uma constante de proporcionalidade que depende da unidade que as unidades para calor e trabalho so o JOULE. ****Experincia de Joule pg 73 Van Wylen. 3.2. A primeira lei da Termodinmica para mudana de estado de um sistema Def. Schmidt pg 62. A primeira lei da termodinmica um enunciado da conservao da energia aplicada para um sistema. Este princpio afirma que toda a energia que cruza a fronteira do sistema deve ser igual variao de energia do sistema. Como calor e trabalho so as nicas formas de energia que podem atravessar uma fronteira de sistema pode-se escrever a 1a lei na forma diferencial do seguinte modo : Q W = dE A equao acima define a propriedade E (ENERGIA DO SISTEMA). Energia : Conceito abstrato, associado de forma intuitiva capacidade de realizaes. Em Termodinmica diz-se que um sistema pode armazenar energia de vrias maneiras, sendo portanto conveniente decompor esta propriedade em 3 componentes : energia interna (U) : resulta do movimento molecular interno, da composio mssica, energia qumica, etc. no SI J = 1 j
Notas de Aula / Fenmenos de Transportes / Parte1 : Termodinmica Prof. Jorge M. Moraes
22
energia cintica (Ec) : resulta do movimento de um corpo ou fluido energia potencial (Ep) : resulta da posio de um corpo ou fluido
Equao da Energia total (E) : E = U + Ec + Ep = U + mV 2
2
+ mg z
[N.m = Joule]
Valores especficos, por unidade de massa (e = E/m) a equao fica :
e = u + ec + ep = u +
V
2
+ gz
N.m Joule = kg kg
A energia interna especfica (u) uma propriedade termodinmica extensiva (depende da massa) associada ao estado de agitao e vibrao molecular. dependente da presso e temperatura da substncia e pode ser determinada atravs de equaes ou tabelas. As equaes utilizadas para u so similares s utilizadas para o volume especfico, ou seja : U = Uliq + Uvap m u = mliq ul + mvap uv u = (1-x) ul + x uv Introduzindo esses conceitos de energia, pode-se escrever a equao da 1a Lei como :
Q = dE + W = dU + dEc + dEp + W
Ou ainda integrando essa equao fica:
1
Q2 = E 2 E1 + 1W2 = U 2 U 1 + Ec 2 Ec1 + Ep 2 Ep1 + 1W2
1 Q2 = U 2 U 1 +
m(V22 V12 ) + mg (Z 2 Z 1 ) + 1W2 2
***** VER EXERCCIOS 5.1 E 5.2 PAG 78
Notas de Aula / Fenmenos de Transportes / Parte1 : Termodinmica Prof. Jorge M. Moraes
23
Entalpia
Quando trabalhamos com volume de controle devemos considerar a energia associada ao fluxo de massa entrando ou saindo do volume de controle. Esta composta de duas parcelas :
a energia especfica da massa que cruza a fronteira do volume de controle
e = u + ec + ep = u +
V
2
+ gz
o trabalho de fluxo (trabalho necessrio para introduzir a massa no volume de controle)
w = P v (num processo a Presso constante)
A energia associada massa entrando ou saindo de um volume de controle portanto :
u+Pv+
V
2
+ gz = h +
V
2
+ gz
A combinao dos dois primeiros termos denomina-se entalpia, propriedade termodinmica (encontrado em tabelas). As equaes da entalpia total e especfica podem ser escritas :
H=U+PV
e
h=u+Pv
Como a entalpia uma propriedade uma funo de ponto ou estado e seu uso para os clculos em termodinmica no depende do processo, portanto podendo ser usado mesmo quando o processo no ocorre a presso constante.
Calores especficos a volume constante (cv) e a presso constante (cp)
definido como a quantidade de calor necessria para elevara temperatura de um grau por unidade de massa.
Q = dE + W = dU + dEc + dEp + W
Notas de Aula / Fenmenos de Transportes / Parte1 : Termodinmica Prof. Jorge M. Moraes
24
Desprezando as variaes dEc e dEp a equao fica:
Q = dE + W = dU + W = dU + pdV
1 se o volume constante pdV = 0, ento cv fica:
1 Q 1 U u = = m T v m T v T v
cv =
2 se a presso constante pode-se associar u e pV pela equao u + pV = h (nos estados iniciais e finais) e cp fica :
cp =
1 Q 1 H h = = m T p m T p T p
**Como cv e cp contm propriedades termodinmicas elas tambm o so. Exemplo 5.5 pg 85.
3.3 Conservao de massa para um Volume de Controle
taxa de variao de massa no V.C.
dm dt
taxa de massa (fluxo de massa) entrando no V.C.
taxa de massa (fluxo de massa) entrando no V.C.
me
ms
regime permanente (dm/dt = 0) :
.
me = ms
m e1
Volume de controle
m s1
m s2
(dm/dt)vc
. .
m e2
.
.
m s3
Ex:
m precipitao
lago
.
evap
m vazo sada
(dm/dt)vc
m vazo entrada m inf iltrao
Notas de Aula / Fenmenos de Transportes / Parte1 : Termodinmica Prof. Jorge M. Moraes
25
m = V A=
V A
. . . . . mprecipitao + mvazo entrada + (dm/dt)lago = mevaporao + minfiltrao + mvazo sada
3.4. Equao de Primeira Lei para um volume de controle (calor, trabalho e massa cruzam a fronteira).
taxa de variao = taxa de Energia - taxa de Energia + taxa de Energia - taxa de Energia da energia no entrando como saindo como entrando com saindo com a Sistema Calor Trabalho massa massa (potncia=W/t) . . . . dE = Q W + m e (ee + Pe ve ) m s (es + Ps v s ) dt ou ainda :
dE dt = Q W
. .
V2 m e (h + + gz ) e 2
.
V2 m s (h + + gz ) s 2
.
3.4.1. Regime Permanente
Hipteses para o regime permanente : 1- O volume de controle no se move em relao ao sistema de coordenadas; 2- O estado da substncia, em cada ponto do volume de controle, no varia com o tempo, ento : dmvc/dt = 0 e dEvc/dt=0 3- O fluxo de massa e o estado dessa massa em cada rea discreta de escoamento na superfcie de controle no varia com o tempo. Portanto, quando o regime permanente o termo de variao da energia no volume de controle se anula (dE/dt = 0) e todos os termos so constantes. A equao pode ser escrita :
.
m e (h +
V2 + gz ) e 2
m s (h +
V2 + gz ) s 2
Esta equao pode ser escrita por unidade de massa. A hiptese 3 acima, no caso de um fluxo entrando e um saindo pode-se escrever:
me = ms = m
. . .
Onde :
q
+
& Q q= & m
.
V he + e + gz e 2
V + hs + s + gz s 2
.
w=
& W & m
Вам также может понравиться
- Experiências de Física Sobre ConvecçãoДокумент4 страницыExperiências de Física Sobre Convecçãojoao gabrielОценок пока нет
- Carta Psicrometrica Temp. ElevadasДокумент18 страницCarta Psicrometrica Temp. ElevadasBernardo HuykeОценок пока нет
- Simulação Numérica de ReservatóriosДокумент75 страницSimulação Numérica de ReservatóriosgermangsilvaОценок пока нет
- Apostila 03 - Exigências Humanas e Índices de ConfortoДокумент11 страницApostila 03 - Exigências Humanas e Índices de ConfortoNayara CristinaОценок пока нет
- QFL1345 - Exercício de EMДокумент3 страницыQFL1345 - Exercício de EMSarah Barbosa VeigaОценок пока нет
- Manual Dominick RunterДокумент24 страницыManual Dominick RunterJulio Alves80% (10)
- 1 Lista de ExercíciosДокумент2 страницы1 Lista de ExercíciosFrancisco AlvesОценок пока нет
- 0 - II Seminário - CD6 - Dullness Wa WB WC WD WeДокумент128 страниц0 - II Seminário - CD6 - Dullness Wa WB WC WD Weedumm001Оценок пока нет
- Relatorio 3Документ3 страницыRelatorio 3Camila Nascimento100% (1)
- Resumo Aula TeóricaДокумент6 страницResumo Aula TeóricaPhellipe AraujoОценок пока нет
- Simuladores HYSYS Exercícios e GuiaДокумент4 страницыSimuladores HYSYS Exercícios e GuiaLarissa PinheiroОценок пока нет
- Fisica 2º Ano-Aula 4Документ11 страницFisica 2º Ano-Aula 4Davi MoraesОценок пока нет
- Espectrofotometria CEFET QuimicaДокумент25 страницEspectrofotometria CEFET QuimicaKakai XavierОценок пока нет
- Prática 10Документ12 страницPrática 10Maria Luiza de Abreu Alves100% (1)
- Texto - Segurança Na Operação de Geradores de Vapor PDFДокумент5 страницTexto - Segurança Na Operação de Geradores de Vapor PDFrita alaideОценок пока нет
- Manual de Instalação 8890 Com PAL 3 - SSP TO - 310943901Документ8 страницManual de Instalação 8890 Com PAL 3 - SSP TO - 310943901Pedro Fernando Veloso dos PassosОценок пока нет
- Astm A 249Документ1 страницаAstm A 249leonardoportocОценок пока нет
- Aula 4 Titulometria de Neutralização QUI094 2012.2Документ32 страницыAula 4 Titulometria de Neutralização QUI094 2012.2NAYARA DA SILVA PANTOJAОценок пока нет
- Homeschooling 10 - 9o AnoДокумент3 страницыHomeschooling 10 - 9o AnoCarminha Porto LombaОценок пока нет
- Operações Unitárias IVДокумент18 страницOperações Unitárias IVJuarez Hilleshein JuniorОценок пока нет
- Fispq346 - 000 RiodineДокумент7 страницFispq346 - 000 RiodinemarielsonОценок пока нет
- Materia Kelas 2Документ35 страницMateria Kelas 2Jose D CostaОценок пока нет
- Isolamentos TérmicosДокумент59 страницIsolamentos TérmicosPedro Malheiro100% (1)
- TEO MÓD6 LIG - QUÍMICAS CORPUSCULAR ExerciciosДокумент10 страницTEO MÓD6 LIG - QUÍMICAS CORPUSCULAR ExerciciosThiago SouzaОценок пока нет
- Lista de Exercícios 2Документ3 страницыLista de Exercícios 2Ricardo MatosОценок пока нет
- Lista 8 - Termodinamica IIДокумент2 страницыLista 8 - Termodinamica IILucas RenanОценок пока нет
- OD-QUA-194 (FISPQ VP 31 HI) Rev 05Документ6 страницOD-QUA-194 (FISPQ VP 31 HI) Rev 05Elton RicardoОценок пока нет
- Lista de Exercícios 01 - Introdução À Química OrgânicaДокумент2 страницыLista de Exercícios 01 - Introdução À Química OrgânicaLyndonJohnson0% (1)
- Apresentação Módulo 1 Combate A Incêndio 2018Документ75 страницApresentação Módulo 1 Combate A Incêndio 2018Dayvson FerreiraОценок пока нет
- Parte 2 - Valencia HibridaoДокумент19 страницParte 2 - Valencia HibridaoAnonymous UYDJtUnОценок пока нет