Академический Документы
Профессиональный Документы
Культура Документы
Ch4 Analyse Spectrale
Загружено:
الغزيزال الحسن EL GHZIZAL HassaneАвторское право
Доступные форматы
Поделиться этим документом
Поделиться или встроить документ
Этот документ был вам полезен?
Это неприемлемый материал?
Пожаловаться на этот документАвторское право:
Доступные форматы
Ch4 Analyse Spectrale
Загружено:
الغزيزال الحسن EL GHZIZAL HassaneАвторское право:
Доступные форматы
Observer: ondes et matire
Chapitre 4 : analyse spectrale
Animation: 1. reprsentation spatiale des molcules 2. animation wikipdia sur les diffrentes vibrations du groupe CH2. 3. animation du spectre infrarouge du mthanal (en anglais) 4. le spectrophotomtre (ostralo.net) Introduction: La matire interagit avec les ondes lectromagntiques. La spectroscopie est l'tude quantitative des interactions entre la lumire et la matire. Elle permet de dterminer la nature et la concentration d'espces chimiques prsentes dans un chantillon de matire. Table des matires
Chapitre 4 : analyse spectrale I) Spectroscopie UV-visible 1) principe de fonctionnement d'un spectroscope 2) loi de Beer Lambert 3) couleur et absorbance d'une solution colore II) Nomenclature des composs organiques 1) groupe caractristique et fonction 2) rappel sur le nom des 5 premiers alcanes chaine linaire 3) rgles de nomenclature a) acides carboxyliques b) alcools c) aldhydes et ctones d) alcnes e) les amines f) les amides III) spectroscopie infrarouge 1) dfinition 2) le spectre IR d'une molcule 3) Pourquoi l'espce chimique absorbe les IR? 4) Mthode pour analyser un spectre IR IV) quelques bandes d'absorption caractristiques 6) cas de la liaison O-H V) la rsonnance magntique nuclaire 1) Principe 2) le spectre RMN 3) le dplacement chimique (ppm) 4) les protons quivalents 5) multiplicit du signal: explication du nombre de pics dans un signal 6) intgration du signal: dterminer le nombre de protons quivalents Programme officiel
I) Spectroscopie UV-visible
1) principe de fonctionnement d'un spectroscope
Animation: Utiliser le spectrophotomtre en faisant varier les diffrents paramtres de l'animation. Comment volue l'absorbance en fonction de la longueur d'onde puis de la concentration pour une solution de permanganate de potassium?
Un spectrophotomtre UV-visible est constitu de: - une source de lumire blanche - un monochromateur permettant de slectionner une radiation monochromatique de longueur d'onde prcise (sur le schma la longueur d'onde vaut 551 nm) - un sparateur de faisceau. En sortie du sparateur, un faisceau traverse la cuve contenant le solvant (gnralement de l'eau distille), un second faisceau traverse la solution analyser.
- la comparaison des 2 faisceaux d'intensits respectives I (la solution) et Io (le solvant) permet de calculer l'absorbance A de l'chantillon. - la courbe qui reprsente l'absorbance en fonction de la longueur d'onde est appele le spectre de l'chantillon. Vido de TP au laboratoire: absorbance en fonction de la longueur d'onde
A = f()
Exemple: le spectre d'absorption du dichromate de potassium (compris entre 400 et 600 nm) est le suivant:
2) loi de Beer Lambert
A ( ) = ( ).L.C
Vido de TP au laboratoire: loi de Beer Lambert L'absorbance d'une solution colore A () est gale :
() : coefficient d'absorption molaire qui dpend du
solvant de la temprature et de la longueur d'onde Unit lgale: m-1. mol-1.L L(m): paisseur de solution traverse C (mol.m-3) : concentration de la solution. A est sans unit. Remarque : Si la concentration est trop grande l'absorbance est trop leve, cette loi n'est plus valable il faut diluer la solution. Une espce chimique est caractrise en spectroscopie UV-visible par la longueur d'onde (max) du maximum d'absorption et par la valeur du coefficient d'extinction molaire
Il absorbe les radiations violettes, bleues et une partie des radiations vertes. Sa couleur est donc la somme des couleurs complmentaires qui sont (d'aprs le cercle chromatique) le jaune orang, l'orange et le rouge. La solution en effet une couleur orange. Solution de dichromate de potassium (2K+,Cr2O72-):
II) Nomenclature des composs organiques
1) groupe caractristique et fonction
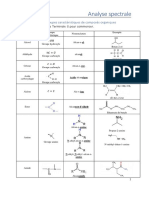
Un compos organique provient d'une espce vivante. Il contient une chaine carbone et un ou plusieurs groupes caractristiques. Les molcules possdant le mme groupe caractristique ont des proprits chimiques similaires Ces proprits dfinissent la fonction chimique. Animation: reprsentation spatiale des molcules Voici quelques composs organiques oxygns: fonction groupe caractristique groupe carboxyle exemple acide thanoque (prsent dans le vinaigre)
(max ) correspondante.
acide carboxyliq ue
3) couleur et absorbance d'une solution colore
alcool
groupe hydroxyle groupe carbonyle (encadr)
thanol (prsent dans le vin) thanal (produit par les plantes)
Une substance incolore, comme l'eau, n'absorbe aucune radiation visible: son absorbance est nulle quelque soit . La couleur d'une espce est la somme des couleurs complmentaires des radiations qu'elle absorbe. Le cercle chromatique reprsentent quelques couleurs ainsi que leur couleur complmentaire (au bout de la flche !)
aldhyde
groupe carbonyle ctone
propanone (produit par les
plantes) 2-mthylbut-2-ne alcne alcne
ester (encadre) mthanoate de mthyle Ester
amine Amine
la trimthylamine acide 3,3dimethylbutanoque
amide Amide
N-mthylpropanamide
2) rappel sur le nom des 5 premiers alcanes chaine linaire
Les alcanes chaine linaire sont constitus partir de carbone ttragonal (li 4 autres atomes) et d'atomes d'hydrogne. Leur formule brute gnrale est CnH2n+2. Leur nom doit tre connu car on va utiliser le prfixe pour nommer les composs oxygns. Maman est partie bb pleure Mthane thane propane butane pentane Nom Nombre datomes de carbone 1 2 3 4 5 Formule brute formule et nom du groupement alkyle correspondant CH3mthyl CH3-CH2thyl CH3-CH2-CH2propyl CH3-CH2-CH2-CH2butyl CH3-CH2-CH2-CH2-CH2penthyl
Les rgles sont identiques celles des acides carboxyliques. On remplace ensuite le "e" du nom de l'alcane correspondant par la terminaison 'ol'. Exemple: Nom thanol propan-2-ol Formule brute C2H6O C3H8O formule semidveloppe CH3-CH2-OH classe d'alcool primaire secondaire
b) alcools
2-mthylpropan-2ol
C4H10O
tertiaire
mthane thane propane butane pentane
CH4 C2H6 C3H8 C4H10 C5H12
c) aldhydes et ctones
Les rgles sont identiques celles des acides carboxyliques. On remplace ensuite le "e" du nom de l'alcane correspondant par la terminaison 'al' pour les aldhydes et 'one' pour les ctones. Exemples: formule semi-dveloppe
nom pentan-3-one
3) rgles de nomenclature a) acides carboxyliques
2-mthylbutanal
Pour tablir le nom des acides carboxyliques 1. on recherche la chane la plus longue comportant l'atome de carbone fonctionnel 2. on numrote les atomes de carbone en minimisant l'indice du carbone fonctionnel 3. on repre les ramifications alkyle sur la chane principale, on crit le numro du carbone portant la ramification, puis un tiret et enfin le nom de la ramification avant le nom de la chane principale. 4. Le nom du compos est prcd du mot acide. On remplace ensuite le 'e' du nom de l'alcane correspondant par la terminaison 'oque'. Exemple: nom acide mthanoque (prsent dans les venins de certains insectes, fourmi acide 3methylbutanoque (prsent dans l'urine de chat, qui sert de marqueur de territoire!) acide 2mthylpropanoque (prsent dans certains arbres comme le caroubier) formule dveloppe ou semi-dveloppe
3-mthylbutan-2-one
4,4-dimthylpentanal
Les rgles sont identiques celles des acides carboxyliques. On remplace ensuite le "e" du nom de l'alcane correspondant par la terminaison 'ne'. On rajoute (Z) ou (E) suivi d'un tiret lorsqu'une isomrie Z ou E existe dans la molcule
d) alcnes
Exemple: formule semi-dveloppe
nom
(Z)-pent-2-ne
(E)-but-2-ne
butanamide
prop-1-ne
III) spectroscopie infrarouge
2-mthylbut-1-ne Photo d'un spectroscope infrarouge
Les rgles sont identiques celles des acides carboxyliques. On remplace ensuite le "e" du nom de l'alcane correspondant par la terminaison 'amine'. Lorsque l'atome d'azote est li d'autres groupes alkyles, le nom de l'amine est prcd de la mention N-alkyl. S'il y a 2 groupes alkyles, le nom est prcd de la mention N,N-alkyl.
e) les amines
1) dfinition
Exemple: formule semidveloppe
La spectroscopie infrarouge (IR) est dans son principe identique la spectroscopie UV-visible. Le domaine de longueur d'onde utilis est (2500 nm, 25000 nm). Les OEM interagissent avec les liaisons covalentes de la molcule. Pour cette raison la spectroscopie IR permet de reprer la prsence de certaines liaisons et d'en dduire les groupes caractristiques prsents dans la molcule. nom 2-methylpropan-2-amine
2) le spectre IR d'une molcule
Le nombre d'onde d'une OEM est gal l'inverse de sa longueur d'onde :
CH3-NH-CH3
N-mthylmethanamine N-mthylpentan-3-amine
unit lgale : (m), (m-1 )
La transmittance T est gale au rapport de l'intensit transmise I travers la substance analyser sur l'intensit Io transmise par le solvant. La transmittance n'a pas d'unit, sa valeur est comprise entre 0 et 1 :
T= I Io
N,3-dimthylbutan-2-amine
Les rgles sont identiques celles des acides carboxyliques. On remplace ensuite le "e" du nom de l'alcane correspondant par la terminaison 'amide'. Lorsque l'atome d'azote est li d'autres groupes alkyles, le nom de l'amide est prcd de la mention N-alkyl. S'il y a 2 groupes alkyles, le nom est prcd de la mention N,N-alkyl.
f) les amides
Le spectre IR d'une espce chimique reprsente la transmittance T en ordonne en fonction du nombre d'onde en abscisse. Gnralement le nombre d'onde est exprim en cm-1. Une transmittance de 100 % indique que l'IR n'est pas absorb. Lorsqu'un IR ou une bande d'IR est absorb alors on observe un pic ou une bande d'absorption (transmittance faible) orient vers le bas. Exemple: animation du spectre infrarouge du mthanal (en anglais). Le spectre IR du mthanal possde plusieurs pics d'absorption: - 5 pics correspondant la liaison entre le carbone et les 2 hydrognes (note CH2 sur le spectre) - un pic correspondant la double liaison entre le carbone et l'oxygne. Ce spectre permet d'affirmer que l'espce analyse et le premier aldhyde : le mthanal. Sur le graphique sont indiqus les nombres d'onde correspondant aux absorptions les plus importantes donc aux transmittances les plus faibles.
Exemple: formule semi-dveloppe
nom
N-mthylthanamide
N,2-dimthylpropanamide
Plus la liaison est forte, plus le nombre d'onde d'absorption est lev
IV) quelques bandes d'absorption caractristiques
Les nombres d'ondes utiles la recherche des groupes caractristiques sont suprieurs 1500 cm-1 ( part quelques exceptions comme pour la liaison C-O, voir tableau ci dessous). Ceux infrieurs 1500 cm-1 ne sont utiles que pour comparer les spectres.
1) bandes C-H
Le nombre d'onde (C H) dpend de la nature du
3) Pourquoi l'espce chimique absorbe les IR?
Les atomes de la molcule peuvent se dplacer dans toutes les directions. Par exemple les atomes du groupe CH2 peuvent vibrer de 6 manires diffrentes : tirements (stretching), symtrique et anti symtrique, cisaillement (scissoring), bascule (rocking), agitation hors du plan (wagging) et torsion (twisting). Voir l'animation wikipdia.
carbone. Par exemple, le carbone ttragonal est prsent dans les alcanes comme l'thane H3Ctet-CtetH3. Le carbone trigonal est prsent dans les alcnes comme lthne H2Ctri=CtriH2. D'aprs le tableau ci dessus Un alcane prsentera deux bandes d'absorption due la liaison C-H: - entre 2800 et 3000 cm-1 d'intensit forte - entre 1415 et 1470 cm-1 (li la dformation angulaire des liaisons C-H) d'intensit forte Un alcne prsentera une bande d'absorption de moyenne intensit due la liaison C-H comprise entre 3000 et 3100 cm-1 .
A chaque vibration correspond une nergie En. Lorsque les IR correspondant cette nergie interagissent avec l'espce chimique, ils sont absorbs, leur transmittance est alors faible.
4) Mthode pour analyser un spectre IR
1) reprer les liaisons chimiques ( C-H, N-H, C=O etc..) grce leurs nombres d'onde. Attention une liaison peut correspondre plusieurs bandes d'absorption car la liaison peut vibrer de diffrentes faons (symtrique, cisaillement etc..) 2) rechercher les groupes caractristiques ( hydroxyle OH, carboxyle -COOH etc..) possdant ces liaisons. Attention certaines liaisons appartiennent plusieurs groupes. Par exemple la liaison C=O appartient aux groupes carboxyle et carbonyle. 3) vrifier que toutes les bandes caractristiques des groupes retenus se trouvent dans le spectre IR 4) utiliser ventuellement les valeurs prcises des nombres d'onde pour dpartager les groupes. Tableaux de quelques bandes d'absorption avec l'intensit correspondante de l'absorption (F: forte, M: moyen) nombre d'onde (cmliaison intensit 1) O-H libre 3580 3650 F, fine O-H li 3200 3400 F, large N-H 3100 3500 M Ctri-H (carbone 3000 3100 M trigonal) Ctet-H (carbone 2800 3000 F ttragonal) C=Oester 1700 1740 F C=C 1625 1685 m C=Oacide 1680 1710 F C-C 1625 1685 M Ctet-H 1415 1470 F C-O 1050 1450 F
2) bande C=C
Elle se retrouve dans les alcnes et galement dans les composs aromatiques comme le benzne ou elle est moins fortes car dlocalise (le nombre d'onde est alors plus
faible (Caromat = C) (compris entre 1450 et 1600 cm-1).
Voici un extrait des spectres IR de l'hexane et de l'alcne hexne.
3) bande C=O: la liaison C=O est prsente dans les aldhydes, ctones, esters, amides etc. ; La position de la bande d'absorption dpend du type de fonction (voir tableau). Elle se situe entre 1650 et 1740 cm-1 environ. 4) bande C-O: la liaison C-O est prsente dans les
acides carboxyliques, alcools etc. ; La position de la bande d'absorption dpend du type de fonction (voir tableau). Sa bande se situe entre 1050 et 1450 cm-1.
5) bande N-H: la liaison N-H est prsente dans les
amines et amides etc. ; La position de la bande d'absorption dpend du type de fonction (voir tableau). Sa
bande se situe entre 3100 et 3500 cm-1. Remarque, le spectre IR d'une amine RNH2 donne 2 bandes alors que celui d'une amine RNR'H ne donne qu'une bande (1 seule liaison N-H). Exemple: spectre IR de la N-mthylamine et du cyclohexylamine
Pour les acides carboxyliques sous forme liquide, l'largissement de la bande correspondant la liaison O-Hli provoque un chevauchement avec la bande d'absorption Ctet-H.
V) la rsonnance magntique nuclaire
6) cas de la liaison O-H 1) Principe
Rappel: une liaison hydrogne se forme lorsquun atome dhydrogne, li un atome A trs lectrongatif, interagit avec un atome B, galement trs lectrongatif et porteur dun doublet non liant (O, N, Cl, F). Cette liaison est note en pointill et les trois atomes concerns sont aligns. Ex : Liaison hydrogne entre deux molcules deau : La rsonance magntique nuclaire (RMN) est une technique qui permet d'identifier les atomes d'hydrogne d'une molcule ainsi que la nature et le nombre d atomes de leur environnement proche. L'appareil met une OEM qui interagit avec le noyau des atomes d'hydrogne donc avec le proton d'ou le nom de RMN du proton. On place un chantillon de matire dans un champ magntique Bo. On envoie une OEM qui fait entrer en rsonance le proton qui vibre une frquence f. En retournant son tat initial le proton met une OEM de frquence f qui est enregistre puis traite afin d'obtenir le spectre RMN. La RMN permet ainsi de distinguer dans la molcule d'thanol CH3-CH2-OH les protons du groupe CH3 ceux du groupe CH2 et celui du groupe OH.
La liaison hydrogne correspond une interaction lectrostatique entre latome dhydrogne, qui porte un excs de charge partielle positive, et le doublet non liant dun atome O,N ou F. Remarques : Les liaisons hydrognes sont plus intenses que les liaisons de Van der Walls mais beaucoup moins intense quune liaison covalente. La liaison O-H se trouve dans les alcools, les acides carboxyliques. Dans le cas des alcools, La liaison hydrogne affaiblie la liaison O-H. Elle a tendance la rompre. A l'tat gazeux il n'existe pas de liaison hydrogne entre les molcules car elles se trouvent de grandes distances les unes des autres. La liaison O-H est alors appele O-Hlibre. A l'tat gazeux la liaison O-Hlibre donne une bande d'absorption forte et fine vers 3620 cm-1. A l'tat liquide la liaison hydrogne existe, la liaison O-H est alors note O-Hli. Elle est affaiblie par consquent le ombre d'onde est plus faible et la bande plus large. Elle est comprise entre 3200 et 3400 cm-1.
2) le spectre RMN
Un spectre RMN est constitu d'un ensemble de signaux, constitus d'un ou plusieurs pics fins. Chaque signal correspond un atome ou groupe d'atomes d'hydrogne. L'environnement de l'atome ou du groupe d'atome influe sur: - la position du signal, repre en abscisse par une valeur appele le dplacement chimique Le dplacement chimique
d'un atome d'hydrogne dpend
des atomes prsents dans son environnement. Son unit est la ppm (partie par million). Il dpend de la frquence de rsonnance de l'atome d'hydrogne. - sa multiplicit (nombre de pics le composant) Une courbe d'intgration se superpose au spectre. Elle est constitue de paliers successifs (voir le 5 pour la signification de la hauteur des paliers).
3) le dplacement chimique
(ppm)
L'axe des dplacements chimique est orient de droite gauche, gnralement de 0 15 ppm. A un dplacement chimique nulle
(ppm) = 0 correspond les hydrognes du
ttramthylsilane (TMS):
Cette substance est ajoute la substance analyser. Chaque signal constitu d'un ou plusieurs pics traduit une absorption d'nergie par les protons. Ceux ci entre alors en rsonnance.
Exemple 2: dans la molcule de mthoxymthane CH3-O-CH3 il y a une symtrie tous les atomes d'hydrogne sont quivalents. Le spectre RMN ne sera constitu que d'un seul signal. - Dans la molcule de pentan-3-one CH3-CH2-COCH2-CH3, il y a une symtrie. Les 6 protons lis aux carbones situs aux extrmits sont quivalents. Les 4 protons lis aux carbones situs de part et d'autre de la liaison carbonyle sont quivalents. Le spectre RMN sera constitu de deux signaux.
5) multiplicit du signal: explication du nombre de pics dans un signal
Dans l'thanol CH3-CH2-OH les hydrognes du groupe CH3 rsonnent vers 1,2 ppm, ceux du groupe CH2 vers 3,6 ppm et celui du groupe OH vers 4,7 ppm. Le proton du groupe carboxyle -CO2H rsonne entre 8,5 et 13 ppm; celui du groupe carbonyle des aldhydes -COH rsonnent entre 9 et 10 ppm. Voir p 595 les dplacements chimiques des protons en RMN. Quelques dplacements chimiques de protons:
Dans une molcule les protons lis un atome de carbone interagissent avec les protons ports par les atomes de carbone voisins : il y a couplage entre les atomes (les protons quivalents ne se couplent pas). Un proton ou un groupe de protons quivalents ayant n protons quivalents voisins (port par des carbone voisins) donne un signal constitu de (n+1) pics appel multiplet. Exemple: spectre de l'thanol CH3-CH2-OH (voir figure ci dessus) - l'hydrogne li l'atome d'oxygne forme 1 seul pic c'est un singulet. En effet il n'est pas li un atome de carbone. - les protons du groupe CH3 sont quivalents (port par le mme atome de carbone). Ils ont n = 2 protons quivalents voisins, ils donnent un signal constitu de n+1 = 3 pics appel triplet. - les protons du groupe CH2 sont quivalents. Ils ont n = 3 protons quivalents voisins, ils donnent un signal constitu de n+1 =4 pics appel quadruplet. Les protons non lis des atomes de carbone ne donnent qu'un seul pic (1 singulet). Ils ne peuvent se coupler d'autres atomes d'hydrogne. Il s'agit des protons des groupes hydroxyle -OH, carboxyle -CO2H, amine -NH2 ou NH
4) les protons quivalents
Dans le cas des molcules simples les protons sont dit quivalents (ils ne donnent qu'un seul signal sur le spectre) dans les cas suivants: a) les protons sont ports par un mme atome de carbone. b) si la molcule prsente une symtrie, les protons qui se correspondent sont quivalents. Exemple 1 : Dans la molcule de propane CH3-CH2-CH3 sont quivalents : - les 3 atomes d'hydrogne du premier carbone car ils sont lis au mme atome de carbone - les 2 atomes du second - les 3 atomes du troisime - de plus il y a une symtrie par raport au carbone 2 par consquent les 3 protons du premier carbone sont quivalent aux trois protons du carbone 3. Le spectre RMN sera constitu de 2 signaux.
6) intgration du signal: dterminer le nombre de protons quivalents
On superpose parfois sur les spectres une courbe d'intgration. Elle est constitue de paliers successifs. La hauteur sparant deux paliers successifs est proportionnelle aux nombre de protons qui rsonnent.
Exemple : 2,2-dimthylpropanol. Dans le groupement OH il y a un proton h1 =1; dans le groupement CH2 il y a 2 protons quivalents qui rsonnent donc h2 = 2.h1 = 2; dans le groupement C(CH3) il y a 9 protons quivalents qui rsonnent donc h3 = 9.h1 = 9
(Z) Csp2-H aromatique monosubstitu Csp2-H aromatique o-disubstitu m-disubstitu p-disubstitu Csp2-H aromatique trisubstitu1,2,3 trisubstitu1,2,4 trisubstitu1,3,5
Dformation
730-770 et 690-770 735-770 750-810 et 680-725 800-860 770-800 et 685-720 860-900 et 800-860 810-865 et 675-730 700-800 600-750 500-600
F ;2 bandes F F et m; 2 bandes F F et m; 2 bandes F et m; 2 bandes F;2 bandes F F F
Dformation Dformation Dformation
Dformation Dformation Dformation
Annexe Spectroscopie infrarouge Table des nombres d'onde des vibrations de valence et de dformation. Nombre Liaison Nature Intensit d'onde(cm-1) O-H alcool libre Valence 3580-3670 F; large Csp-H Valence 3300-3310 m O-H alcool li Valence 3200-3400 F N-H Valence 3100-3500 m (amines+imines) N-H (amides) Valence 3100-3500 F Csp2-H Valence 3000-3100 m Csp2-H Valence 3030-3080 m aromatique Csp3-H Valence 2800-3000 F Csp2-H aldhyde Valence 2750-2900 m O-H acide F m; Valence 2500-3200 carboxylique large C=C Valence 2100-2250 f C=N Valence 2120-2160 F ou m F; 2 C=O anhydride Valence 1700-1840 bandes C=O chlorure Valence 1770-1820 F d'acyle C=O ester Valence 1700-1740 F 1650-1730 abaissement C=O aldhyde et Valence de 20 30 F ctone cm-1 si conjugaison C=O acide Valence 1680-1710 F C=O amide Valence 1650-1700 F C=C Valence 1625-1685 m variable;3 C=C aromatique Valence 1450-1600 ou 4 bandes 1510-1580 F; 2 N=O Valence 1325-1365 bandes C=N Valence 1600-1680 F N-H amine ou Dformation 1560-1640 F ou m amide Csp3-H Dformation 1415-1470 F F;2 Csp3-H(CH3) Dformation 1365-1385 bandes P=O Valence 1250_1310 F C-O Valence 1050-1450 F C-N Valence 1020-1220 m C-C Valence 1000-1250 F C-F Valence 1000-1040 F Csp2-H deDformation 950-1000 F CH=CHDformation 650-770 m (E)
C-Cl Valence C-Br Valence C-I Valence sp: carbone digonal sp2: carbone trigonal sp3: carbone ttragonal
Dplacements chimiques de protons en RMN
CH3 proton CH3 C d 0,9 CH2 proton C CH2 C (cyclique) CH3 C C= CH3 C O CH3 C=C CH3 Ar CH3 CO R CH3 CO Ar CH3 CO OR 1,1 1,4 1,6 2,3 2,2 2,6 2,0 C CH2COOR 2,3 CCH2 C C=C C CH2 C O C CH2 C=C C CH2 Ar C CH2 CO R d 1,3 1,5 1,7 1,9 2,3 2,7 C CH Ar 2,4 3 C CH C O 2 CH proton C CH C (en tte de pont) d 1,5 2,2
C CH CO 2,7 R
CH3 CO OAr 2,4 CH3 CO NR CH3 OR CH3 OH CH3 O Ar CH3 O CO R CH3 N CH3 N+ CH3 S CH3 C NO2 2,0 3,3 3,4 3,8 3,7 2,3 3,3 2,1 1,6 C CH2 S CCH2 NO2 CCH2 C NO2 CH3 C=C CO 2,0 C = C(CH3) CO 1,8 CCH2 C=CCO C=C(CH3) CO 2,4 4,4 2,1 2,4 2,4 CCH NO2 4,7 C CH2 OR C CH2 OH C CH2 O Ar CCH2 OCOR C CH2 N 3,4 C CH OR 3,7 3,6 C CH OH 3,9 4,3 4,1 CCH O CO R 4,8
2,5 C CH N 2,8
5,9
CH3 Cl CH3 C Cl CH3 Br CH3 C Br CH3 I CH3 C I CH3 CN
3,0 1,5 2,7 1,7 2,2 1,9 2,0
C CH2 Cl C CH2 C Cl C CH2 Br C CH2 C Br C CH2 I C CH2 C I C CH2 CN CO CH2 Ar
3,4 C CH Cl C CH C 1,7 Cl 3,3 C CH Br 1,7 3,1 C CH C Br C CH I
4,0 1,6 3,6 1,7 4,2 1,9
C CH C 1,8 I
2,3 C CH CN 2,7 3,8 0,3 0,7
2,6
3,1
Programme officiel
Observer Ondes et matire Les ondes et les particules sont supports dinformations. Comment les dtecte-t-on ? Quelles sont les caractristiques et les proprits des ondes ? Comment raliser et exploiter des spectres pour identifier des atomes et des molcules ? Notions et contenus Comptences exigibles
Spectres UV-visible Lien entre couleur perue et longueur donde au maximum dabsorption de substances organiques ou inorganiques Spectres IR Identification de liaisons laide du nombre donde correspondant ; dtermination de groupes caractristiques. Mise en vidence de la liaison hydrogne.
Spectres RMN du proton Identification de molcules organiques laide : - du dplacement chimique ; - de lintgration ; - de la multiplicit du signal : rgle des (n+1)-uplets.
Mettre en uvre un protocole exprimental pour caractriser une espce colore. Exploiter des spectres UVvisible Exploiter un spectre IR pour dterminer des groupes caractristiques laide de tables de donnes ou de logiciels. Associer un groupe caractristique une fonction dans le cas des alcools, aldhyde, ctone, acide carboxylique, ester, amine, amide. Connatre les rgles de nomenclature de ces composs ainsi que celles des alcanes et des alcnes. Relier un spectre RMN simple une molcule organique donne, laide de tables de donnes ou de logiciels. Identifier les protons quivalents. Relier la multiplicit du signal au nombre de voisins. Extraire et exploiter des informations sur diffrents types de spectres et sur leurs utilisations.
Вам также может понравиться
- Mémoire de Fin D'année - Google AnalyticsДокумент66 страницMémoire de Fin D'année - Google Analyticsjollet_pierre+scribd100% (1)
- Guide Installation RenolinkДокумент2 страницыGuide Installation Renolinklacan illisibleОценок пока нет
- Ch4 Analyse SpectraleДокумент7 страницCh4 Analyse SpectraleLahoucine GhourchaneОценок пока нет
- C1analyse SpectraleДокумент7 страницC1analyse SpectraleFranck EinsteinОценок пока нет
- Chorg Fmpos 1Документ8 страницChorg Fmpos 1André Kassogue100% (1)
- Chapitre-9-Réaction D'ésterificationДокумент11 страницChapitre-9-Réaction D'ésterificationa houssОценок пока нет
- Extrait de Cours Sciences Physiques TerminaleДокумент15 страницExtrait de Cours Sciences Physiques TerminaleAmine schoolОценок пока нет
- CHP 11 Molecules OrganiquesДокумент4 страницыCHP 11 Molecules Organiques9yn7wr899gОценок пока нет
- Chimie OrganiqueДокумент28 страницChimie OrganiqueNaru NamuОценок пока нет
- Pdf&rendition 1Документ60 страницPdf&rendition 1othmane boubarad100% (1)
- Chimie OrganiqueДокумент29 страницChimie OrganiqueRubyОценок пока нет
- Le Squelette Carboné Des Molécules OrganiquesДокумент4 страницыLe Squelette Carboné Des Molécules OrganiquesSonia Sadek100% (1)
- Chapitre 5 Nomenclature SystematiqueДокумент92 страницыChapitre 5 Nomenclature SystematiqueNatacha N'GUESSANОценок пока нет
- SVI (S2) 2019-2020 Chimie II Chimie Organique Pr. Oussaid Adyl1Документ80 страницSVI (S2) 2019-2020 Chimie II Chimie Organique Pr. Oussaid Adyl1abb32214Оценок пока нет
- Ifrt 3Документ8 страницIfrt 3Soulef ZemzoumОценок пока нет
- Chapitre 7 Suite Et FinДокумент5 страницChapitre 7 Suite Et Findjaelaudinet67Оценок пока нет
- Cours Chimie Organique 2009-2010Документ179 страницCours Chimie Organique 2009-2010AlvaroEnriqueQuinterosОценок пока нет
- Spectroscopie RMNДокумент5 страницSpectroscopie RMNernestrockwell40Оценок пока нет
- TP EsterificationДокумент10 страницTP EsterificationAnn Ouss100% (1)
- Molecules Organiques Et Squelettes Carbones Modification Du Squelette Carbone Cours 2 4Документ5 страницMolecules Organiques Et Squelettes Carbones Modification Du Squelette Carbone Cours 2 4Ossama SariaОценок пока нет
- COURS - Formules Et Nomenclature en Chimie OrganiqueДокумент5 страницCOURS - Formules Et Nomenclature en Chimie OrganiqueLucas Ric0% (1)
- Lycee Louis Payen ReunionДокумент12 страницLycee Louis Payen ReunionAnasОценок пока нет
- Extrait de Cours Tale Physique ChimieДокумент12 страницExtrait de Cours Tale Physique ChimiemarioagbozoОценок пока нет
- BBA - Chapitre 1 Et 2 Chimie Organique - Bahloul Ahmed - L2Документ16 страницBBA - Chapitre 1 Et 2 Chimie Organique - Bahloul Ahmed - L2Imene Aoun SeghirОценок пока нет
- Nomenclature PDFДокумент10 страницNomenclature PDFOudjoud KeddourОценок пока нет
- Cours 5 Nomenclature SNV L1 2020 2021Документ30 страницCours 5 Nomenclature SNV L1 2020 2021Mohamed DjaniОценок пока нет
- Nomenclature 1Документ14 страницNomenclature 1Stachis MadiambaОценок пока нет
- Travaux Diriges de Chimie Generale (Enstmo)Документ4 страницыTravaux Diriges de Chimie Generale (Enstmo)pierreboris123Оценок пока нет
- 05 Spectroscopie Dans UltravioletДокумент6 страниц05 Spectroscopie Dans UltravioletBibi BibaОценок пока нет
- Chimie RMN PDFДокумент15 страницChimie RMN PDFMajouri NajahОценок пока нет
- Cours Les AlcanesДокумент10 страницCours Les Alcanesstefan100% (1)
- Corrige EVAL2 2014-2015Документ5 страницCorrige EVAL2 2014-2015sou50% (2)
- TD1 UV Corrig PDFДокумент28 страницTD1 UV Corrig PDFoumayma oufir100% (1)
- Esbtp 2022 Cours NomenclatureДокумент45 страницEsbtp 2022 Cours Nomenclaturecynthia andrianantenainaОценок пока нет
- Examen Blanc PC Prof AitouarabДокумент8 страницExamen Blanc PC Prof Aitouarabmohamed laghribОценок пока нет
- TD SpectroДокумент6 страницTD SpectroHk Eh67% (3)
- Cours Chimie Organique-1Документ30 страницCours Chimie Organique-1Henri Cynthio RAZANADRAVELOSONОценок пока нет
- Chimie Organique Chap2Документ20 страницChimie Organique Chap2Mira MaroОценок пока нет
- Spectres UV RMNДокумент12 страницSpectres UV RMNGiovanni RaziqОценок пока нет
- Nomenclature OrganiqueДокумент10 страницNomenclature Organiqueshadowkyllers89% (9)
- Chapitre 2 Chimie Organique 2024Документ12 страницChapitre 2 Chimie Organique 2024anie KheliliОценок пока нет
- Travaux Dirigés de Chimie OrganiqueДокумент86 страницTravaux Dirigés de Chimie OrganiqueELGORMA HananeОценок пока нет
- Spectroscopie UV-VisibleДокумент40 страницSpectroscopie UV-VisibleGenie des procede Promotion 2022Оценок пока нет
- 2eme Cours de Chimie OrganiqueДокумент44 страницы2eme Cours de Chimie OrganiqueAnfel BouchairОценок пока нет
- C 05 Do 1 eДокумент15 страницC 05 Do 1 eMihnea GamanОценок пока нет
- EVALUATION PHYSIQUE 3 CHIMIE TS CorrigeДокумент5 страницEVALUATION PHYSIQUE 3 CHIMIE TS Corrigethefalseboy23Оценок пока нет
- Chimie Premiere CdeДокумент30 страницChimie Premiere CdeHans René Nkwinga NgokoОценок пока нет
- Chapitre I.2 - Alcènes-Alcynes - B. MESSAOUDI - 14-02-2022Документ50 страницChapitre I.2 - Alcènes-Alcynes - B. MESSAOUDI - 14-02-2022Abderrahmane AEОценок пока нет
- Concours 2012 (+sol.) Proposition EPST23Документ19 страницConcours 2012 (+sol.) Proposition EPST23Nidal BestОценок пока нет
- Chap 2Документ4 страницыChap 2Ouehnia tynaОценок пока нет
- Chapitre I - Chimie4Документ5 страницChapitre I - Chimie4evilievОценок пока нет
- Chap 2a Les Hydrocarbures Saturés Et InsaturésДокумент12 страницChap 2a Les Hydrocarbures Saturés Et InsaturésYves Patrick AngoОценок пока нет
- TD 1 - UV Vis 2020-ConvertiДокумент2 страницыTD 1 - UV Vis 2020-ConvertihadilОценок пока нет
- BTS Chimie 2 Chimie OrganiqueДокумент7 страницBTS Chimie 2 Chimie Organiquekarpla69Оценок пока нет
- 1ère A - APC - Les AlcanesДокумент5 страниц1ère A - APC - Les AlcanesLAWSON NICOLASОценок пока нет
- 1S Chimie ChapДокумент9 страниц1S Chimie ChapHadia DjeltiОценок пока нет
- Cours de Chimie Organique Chapitre IIДокумент15 страницCours de Chimie Organique Chapitre IIzahramathlouthi127Оценок пока нет
- PC 1ère CD-C6 Quelques Composés Oxygénés PDFДокумент11 страницPC 1ère CD-C6 Quelques Composés Oxygénés PDFZanaple CoulibalyОценок пока нет
- PRATIQДокумент29 страницPRATIQYavo Vivas AKEОценок пока нет
- Physique 1 Et 2-Fi12999646Документ58 страницPhysique 1 Et 2-Fi12999646الغزيزال الحسن EL GHZIZAL HassaneОценок пока нет
- Cours Chimie 1BACДокумент43 страницыCours Chimie 1BACالغزيزال الحسن EL GHZIZAL HassaneОценок пока нет
- Exos OMP CorrigesДокумент6 страницExos OMP Corrigesالغزيزال الحسن EL GHZIZAL HassaneОценок пока нет
- Cours Physique-Chimie 1bac BIOF .S1Документ47 страницCours Physique-Chimie 1bac BIOF .S1الغزيزال الحسن EL GHZIZAL Hassane100% (1)
- Alcootest Et Oxydoreduction, Exercice de Chimie - 232424Документ3 страницыAlcootest Et Oxydoreduction, Exercice de Chimie - 232424الغزيزال الحسن EL GHZIZAL HassaneОценок пока нет
- 2005 Antilles Spe Sujet Exo3 ModulationДокумент2 страницы2005 Antilles Spe Sujet Exo3 Modulationالغزيزال الحسن EL GHZIZAL HassaneОценок пока нет
- Mouvement Particule Chargée MagnétiqueДокумент6 страницMouvement Particule Chargée Magnétiqueالغزيزال الحسن EL GHZIZAL HassaneОценок пока нет
- Correction de Devoir SurveilléДокумент2 страницыCorrection de Devoir Surveilléالغزيزال الحسن EL GHZIZAL HassaneОценок пока нет
- Travail Et Energie Cinetique Cours 2Документ9 страницTravail Et Energie Cinetique Cours 2Smove Oner100% (1)
- Serie 10 Lois de Newton FBДокумент5 страницSerie 10 Lois de Newton FBالغزيزال الحسن EL GHZIZAL HassaneОценок пока нет
- C6 La Pile ElectrochimiqueДокумент7 страницC6 La Pile ElectrochimiquePecorellaОценок пока нет
- Devoir Surveillé de Physique NucléaireДокумент2 страницыDevoir Surveillé de Physique Nucléaireالغزيزال الحسن EL GHZIZAL HassaneОценок пока нет
- Devoir SurveilléДокумент3 страницыDevoir Surveilléالغزيزال الحسن EL GHZIZAL HassaneОценок пока нет
- Devoir N 1SII 2021 Bac BiofДокумент4 страницыDevoir N 1SII 2021 Bac Biofالغزيزال الحسن EL GHZIZAL Hassane100% (1)
- Chapitre3-Exercice Cinematique Dynamique NewtonДокумент8 страницChapitre3-Exercice Cinematique Dynamique Newtonالغزيزال الحسن EL GHZIZAL HassaneОценок пока нет
- Chapitre 11 Les Lois de NewtonДокумент12 страницChapitre 11 Les Lois de Newtonالغزيزال الحسن EL GHZIZAL Hassane100% (1)
- Exercices 2 Les Lois de NewtonДокумент1 страницаExercices 2 Les Lois de Newtonالغزيزال الحسن EL GHZIZAL Hassane100% (5)
- Question Discussion Réponse: LimiteДокумент19 страницQuestion Discussion Réponse: Limiteالغزيزال الحسن EL GHZIZAL HassaneОценок пока нет
- 2007 Reunion Exo2 Sujet Meca Trebuchet 5 5ptsДокумент3 страницы2007 Reunion Exo2 Sujet Meca Trebuchet 5 5ptsالغزيزال الحسن EL GHZIZAL Hassane100% (1)
- Exercice Détermination de La Viscosité D'une Huile MoteurДокумент3 страницыExercice Détermination de La Viscosité D'une Huile Moteurالغزيزال الحسن EL GHZIZAL HassaneОценок пока нет
- 2006 11 NelleCaledonie Exo3 Correction RLC 4ptsДокумент3 страницы2006 11 NelleCaledonie Exo3 Correction RLC 4ptsالغزيزال الحسن EL GHZIZAL HassaneОценок пока нет
- Terminales S Devoir Surveillé de Physique Chimie N°1 2h 22 09 2015Документ3 страницыTerminales S Devoir Surveillé de Physique Chimie N°1 2h 22 09 2015الغزيزال الحسن EL GHZIZAL Hassane100% (1)
- Audit - Integrité Et DimensionДокумент18 страницAudit - Integrité Et DimensionB.I94% (16)
- Cours - HADERBACHE Bachir - Théories Des OrganisationsДокумент94 страницыCours - HADERBACHE Bachir - Théories Des OrganisationsEsma BelguithОценок пока нет
- Enercoop FactureДокумент2 страницыEnercoop Facturearthur.smolinskiОценок пока нет
- 2014 Liban Exo1 Sujet LaitYaourt 6ptsДокумент4 страницы2014 Liban Exo1 Sujet LaitYaourt 6ptsAlicherif BenaissaОценок пока нет
- Luxembourg ChiffresДокумент56 страницLuxembourg ChiffresyeuminhОценок пока нет
- Exposé Microbiologie AlimentaireДокумент15 страницExposé Microbiologie AlimentaireMohamed HamelОценок пока нет
- Fonds Mohammed VI Pour L'investissementДокумент5 страницFonds Mohammed VI Pour L'investissementasma asmaОценок пока нет
- 11 GranulatДокумент32 страницы11 GranulatFatre 1980Оценок пока нет
- Ankylostomose L3Документ52 страницыAnkylostomose L3Sahouin Claude Medard100% (2)
- Le Travail SaisonnierДокумент3 страницыLe Travail SaisonnierMohamed LaarjОценок пока нет
- Chap2 - CollecteDeDonnéesДокумент2 страницыChap2 - CollecteDeDonnéesوليد بن عمرОценок пока нет
- Manuel Utilisateur Configuration, Test Et Exécution de Programmes CNДокумент348 страницManuel Utilisateur Configuration, Test Et Exécution de Programmes CNetudes ameurplasticsОценок пока нет
- 1.SHP IntroДокумент26 страниц1.SHP Introfranck nzauОценок пока нет
- CourДокумент84 страницыCourKim Jae-hwaОценок пока нет
- 2016 04 16 Exercices Partage EquitableДокумент4 страницы2016 04 16 Exercices Partage EquitablemarwaОценок пока нет
- Activite TP05 Composition de L Atmosphere Fiche - EleveДокумент3 страницыActivite TP05 Composition de L Atmosphere Fiche - EleveEmma RoemerОценок пока нет
- Droit de La RetractationДокумент4 страницыDroit de La RetractationKarima KhribchiОценок пока нет
- Lettre de MotivationДокумент2 страницыLettre de MotivationbhhbsckОценок пока нет
- Mémoire - Solidarité Et Intéret Mutuel - OS - Charles WAUBANTДокумент91 страницаMémoire - Solidarité Et Intéret Mutuel - OS - Charles WAUBANTCharles WaubantОценок пока нет
- Côte D'ivoire TEMPLATE - Bassam 30juinДокумент2 страницыCôte D'ivoire TEMPLATE - Bassam 30juinDeloumeauxОценок пока нет
- COURS Excel 2007 GraphiqueДокумент15 страницCOURS Excel 2007 GraphiqueDje RachidОценок пока нет
- Mob Chop 5Документ56 страницMob Chop 5Gérald LagnesОценок пока нет
- Tenda ModemДокумент2 страницыTenda Modemtighrine faredjОценок пока нет
- Guide Santé SONEPAR ActifsДокумент36 страницGuide Santé SONEPAR ActifsmarcotkОценок пока нет
- PFE Covid 19 Et Le SIДокумент21 страницаPFE Covid 19 Et Le SIHamza KaimaОценок пока нет
- CALCUL GicleursДокумент2 страницыCALCUL GicleursHvacdm CesОценок пока нет
- Bribes Du TempsДокумент2 страницыBribes Du TempspatriceleblanОценок пока нет
- Liason ChimiqueДокумент7 страницLiason Chimiquesalah mebrouk100% (1)