Академический Документы
Профессиональный Документы
Культура Документы
Ecuaciones D Estado
Загружено:
Erick ChavezОригинальное название
Авторское право
Доступные форматы
Поделиться этим документом
Поделиться или встроить документ
Этот документ был вам полезен?
Это неприемлемый материал?
Пожаловаться на этот документАвторское право:
Доступные форматы
Ecuaciones D Estado
Загружено:
Erick ChavezАвторское право:
Доступные форматы
FACULTAD DE INGENIERIA QUIMICA Y METALURGIA ESCUELA ACADEMICO PROFESIONAL DE INGENIERIA QUIMICA
TERMODINAMICA PARA INGENIEROS QUIMICOS II
PROFESOR ALUMNOS
: Dr. Segundo Albertano Parrera Espinoza. : Chvez Aguirre, Erick ngel Enrique Ramrez Pulache, Geraldine.
CICLO
: VII
FECHA DE ENTREGA: 03 de Mayo del 2012
Huacho Per 2012
Ecuaciones 2
de
Estado
TRABAJO N1:
TEMA: LAS ECUACIONES DE ESTADO
Virial Redlich Peng
Kwong
Robinson
Ingeniera Qumica
Ecuaciones 3
de
Estado
INDICE
ndice2 ndice de Figuras3 ndice de Anexos4 Introduccin.5 Fundamento Terico..6
I.
LA ECUACION VIRIAL DE ESTADO6
I.1. I.2. I.3. I.4.
Generalidades......6 Formulacin Matemtica6 Aplicacin de las Ecuaciones Viriales..8 Relacin entre las ecuaciones de Van Der Walls y del Virial.10
I.5. I.6. II.
Importancia del segundo coeficiente de Virial..12 Ejercicio de Aplicacin..13
LA ECUACION DE REDLICH KWONG..15
II.1. II.2. II.3.
Generalidades15 Formulacin Matemtica..18 Ejercicio de Aplicacin..20
III.
LA ECUACION DE PENG-ROBINSON.22
III.1. Generalidades22 III.2. Formulacin Matemtica..23 III.3. Ejercicio de Aplicacin..24
Ingeniera Qumica
Ecuaciones 4
de
Estado
Conclusiones30 Recomendaciones..30 Bibliografa31 Anexos..32
INDICE DE FIGURAS.
FIGURA N01: Grafica del factor de compresibilidad por el metano.8 FIGURA N02: Grafica de B vs T12 FIGURA N03: Jose Neng Shun Kwong..18 FIGURA N04: Isoterma que relaciona la presin y el volumen...19 FIGURA N05: Ding Yu Peng.22 FIGURA N06: Sistema Cilndrico Pistn.24
Ingeniera Qumica
Ecuaciones 5
de
Estado
INDICE DE ANEXOS.
ANEXO N01:Cosntantes Criticas.32 ANEXO N02: Tabla de Constantes de la Ecuacin de Redlich Kwong32 ANEXO N03: Carta Generalizada de Compresibilidad.33
Ingeniera Qumica
Ecuaciones 6
de
Estado
INTRODUCCION
Una ecuacin de estado es la relacin que existe entre dos o ms propiedades termodinmica. En sistemas de un componente y de una fase, la ecuacin de estado incluir tres propiedades, dos de las cuales pueden ser consideradas como independientes. Aunque en principio se podran plantear relaciones funcionales en que intervengan tres propiedades termodinmica cualesquiera, las expresiones analticas de las relaciones entre propiedades han sido limitadas casi completamente a la presin, volumen y temperatura. Debido a la incompleta comprensin de las interacciones intermoleculares, especialmente en el estado lquido y solido, han sido utilizados mtodos empricos para desarrollar muchas de las ecuaciones de estado de uso general. Dado que la presin, temperatura y volumen pueden ser medidos directamente, los datos necesarios para evaluar las constantes en tales ecuaciones pueden ser obtenidos experimentalmente. La eleccin de la ecuacin a usar en una aplicacin dada depende principalmente de la exactitud deseada y de la capacidad del usuario. Como los coeficientes de casi todas las ecuaciones de estado deben ser evaluados adaptando las ecuaciones a diversos datos experimentales de presin, volumen y temperatura, estas ecuaciones nunca pueden representar exactamente los datos experimentales; mas aun; muchas veces estas ecuaciones no representan los datos, limitando la exactitud. Esto es
Ingeniera Qumica
Ecuaciones 7
de
Estado
particularmente cierto cuando las ecuaciones ms sencillas son aplicadas en la vecindad del punto crtico. En el siguiente trabajo se har el desarrollo de tres ecuaciones de estado (Virial, Redlich Kwong, Peng Robinson), buscando el entendimiento de sus aplicaciones en nuestro quehacer profesional.
FUNDAMENTO TEORICO
I. LA ECUACION VIRIAL DE ESTADO.
I.1.
Generalidades:
Heyke Kamerlingh Onnes un fsico Holands, descubridor del fenmeno del a superconductividad. Kamerlingh Onnes contaba con una solida educacin en matemticas y estaba profundamente inspirado por tericos holandeses como Lorentz y Johannes Van Der Walls. Antes de iniciar su gran programa en criogenia, haba trabajado en termodinmica y fsica molecular, y estaba especialmente interesado en comprobar las consecuencias de la teora molecular de Van Der Walls. En 1880 Van der Walls haba formulado la ley de estados correspondientes, que Kamerlingh Onnes desarroll independientemente al ao siguiente. De acuerdo con esta Ley, todas las sustancias obedecen a la misma ecuacin de estado cuando su presin, temperatura y volumen se expresan como mltiplo de los valores que estas variables tienen en el punto critico. En 1894 Kamerlingh Onnes formul de manera clara la base terica para embarcarse en un programa de licuefaccin de gases: Me vi encaminado a trabajar con gases condensados debido al estudio de la ley de estados correspondientes de Van der Walls.
I.2.
Formulacin Matemtica
Ingeniera Qumica
Ecuaciones 8
de
Estado
Esta ecuacin es la nica que tiene una base terica firme y se basa en el comportamiento intermolecular previsto por la mecnica estadstica. Es otra forma de representar a los gases no ideales, en esta relacin, el factor de compresibilidad (Z) se expresa como una expansin en serie de potencias inversas del volumen molar V :
Z=
PV B C D =1+ + 2 + 3 + V RT V V
(1)
Donde:
Z: Factor de comprensibilidad. B, C y D se conocen como segundo, tercero, cuarto,coeficientes viriales. El primer coeficiente virial es 1.
V
: Volumen Molar.
Una forma alterna de la ecuacin virial es la que proporciona una expansin en serie del factor de comprensibilidad, en trminos de la presin (P):
Z = 1 + B ' P + C ' P 2 + D ' P 3 +
(2)
En principio, el lado derecho de la ecuacin (2) es una serie infinita. De cualquier modo, en la prctica se emplea un nmero finito de trmino. A presiones bajas el truncamiento despus de dos trminos con frecuencia proporciona resultados satisfactorios. Ambas ecuaciones se conocen como expansiones viriales, y los parmetros B, C, D, etc., y B, C, D, etc., se llaman coeficientes viriales. Los parmetros B y
Ingeniera Qumica
Ecuaciones 9
de
Estado
B son segundos coeficientes viriales; viriales, etc.
C y C son los terceros coeficientes
Para cierto gas los coeficientes viriales son funciones nicamente de la temperatura. Debido a que P y V estn relacionados, no es sorprendente que existan relaciones entre los dos conjuntos de coeficientes en las ecuaciones (1) y (2); estas relaciones estn dadas de la manera siguiente:
B'=
B RT
C B2 ( RT )2
(3)
C=
'
(4)
D=
'
D 3 BC + 2 B3 ( RT )3
(5)
En las ecuaciones (1) y (2), los valores de los coeficientes disminuyen rpidamente. Por ejemplo, en la ecuacin (2), la magnitud de los coeficientes es tal que B`>>C`>>D`.
I.3.
Aplicacin de las ecuaciones Viriales.
Las dos formas de la expresin virial conocidas como las ecuaciones (1) y (2), son series infinitas. Para propsitos tcnicos, su uso es prctico solo cuando la convergencia es muy rpida, esto es, cuando dos o tres trminos son suficientes para una aproximacin razonable a los valores de las series. Esto ocurre para gases y vapores de presiones bajas a moderadas.
Ingeniera Qumica
Ecuaciones 10
de
Estado
Figura 1: Grafica del factor de compresibilidad para el metano.
La figura 1 muestra la grafica del factor de compresibilidad para el metano. Los valores del factor de compresibilidad Z (como se calculan a partir de la informacin PVT del metano mediante la ecuacin que la define Z = PV/RT) estn graficados en funcin de la presin para varias temperaturas constantes. Las isotermas resultantes muestran de manera grafica lo que se intenta representar en forma analtica con la expansin virial en P. Todas las isotermas se originan en el valor Z = 1 para P = 0, y a bajas presiones las isotermas son lneas casi rectas. As, la tangente a una isoterma en P = 0 es una buena aproximacin de la isoterma.
Al derivar la ecuacin (2) con respecto a P para una T constante:
Ingeniera Qumica
Ecuaciones 11
de
Estado
Z = 1 + B ' P + C ' P 2 + D ' P 3 + Se obtiene:
( )
Luego, para P = 0:
Z = B' + 2 C' P + 3 D ' P2+ P T
(6)
( Z P)
= B'
T , P =0
(7)
As, la ecuacin de la recta tangente es: Z = 1 + BP (siendo B la pendiente de la recta), que tambin es un resultado que se obtiene al truncar la ecuacin (2) a dos trminos. Una forma mas comn de expresar esta ecuacin es sustituyendo B por la ecuacin (3).
Z=
PV BP =1+ RT RT
(8)
Esta ecuacin expresa una proporcionalidad directa entre Z y P, y con frecuencia se aplica a vapores a temperaturas subcriticas hasta sus presiones de saturacin. A temperaturas altas se proporciona una aproximacin razonable
Ingeniera Qumica
Ecuaciones 12
de
Estado
para los gases hasta una presin de varios bar, incrementndose el intervalo de presin a medida que aumenta la temperatura. La ecuacin (1) tambin es posible truncarse a dos trminos para su aplicacin a bajas presiones.
Z=
PV B = 1+ RT V
(9)
De cualquier modo, la ecuacin (8) es ms conveniente y su aplicacin es tan exacta como la ecuacin (9). De este modo, cuando la ecuacin virial se trunca a dos trminos se prefiere la ecuacin (8). El segundo coeficiente virial B depende de la sustancia y es funcin de la temperatura. Los valores experimentales estn disponibles para varios gases. Adems, es posible calcular el segundo coeficiente virial cuando no hay informacin disponible. Los coeficientes viriales pueden ser determinados a partir de datos experimentales, mediante la mecnica estadstica o a partir de expresiones analtica. Para presiones que estn arriba del intervalo de aplicabilidad de la ecuacin (8), pero debajo de la presin critica, la ecuacin virial truncada a tres trminos con frecuencia proporciona excelentes resultados. En este caso, en la ecuacin (1) la expansin en 1 V es muy superior que la
ecuacin (2). As, cuando la ecuacin virial se trunca a tres trminos, la forma apropiada es: Z= PV B C =1+ + 2 RT V V (10)
Ingeniera Qumica
Ecuaciones 13
de
Estado
Esta ecuacin se puede resolver directamente para la presin, pero es cubica en el volumen. La solucin para V se obtiene fcilmente usando clculos numricos.
I.4.
Relacin entre las ecuaciones de Van Der Walls y del Virial.
Ecuacin del Virial: De la ecuacin (1) PV B C D =1 + + 2 + 3 + V RT V V
Ecuacin de Van der Waals:
RT a P= 2 ( V b) V
(11)
En forma del Virial, remplazando (11) en (1):
PV V RT a V a = 2 = = RT RT (V b ) V V b RT V
1 b 1 V
a RT V
(12)
Si
b =x V
, y matemticamente se cumple que:
1
( 1 x ) =1 + x + x 2 + x 3 +
Ingeniera Qumica
Ecuaciones 14
de
Estado
Entonces, la ecuacin (12) queda expresada por:
PV b b2 b3 a 1 = 1+ + 2 + 3 + RT V V V RT V
(13)
Luego:
PV a 1 b2 b3 =1 + b + 3 + +V 2 V RT RT V
(14)
Comparando (1) con la ecuacin (14) B=b a RT
C =b2
D = b 3 ..etc.
I.5.
Importancia del segundo coeficiente del Virial.
Si graficamos: B=b a RT (15)
Ingeniera Qumica
Ecuaciones 15
de
Estado
Figura 2: Grafica de B vs T La grafica de la figura 2 nos ilustra el efecto de la temperatura sobre el segundo coeficiente del virial, en ella podemos observar que: Cuando T es elevada, B > 0
Cuando T es baja, B < 0 Tambin, cuando B = 0, T= T (boyle)
La temperatura de Boyle es aquella temperatura en la cual un gas cumple con la ecuacin de los gases ideales. La temperatura de Boyle se puede evaluar a partir de la ecuacin (15), con la condicin de que en la ecuacin del virial expresada 1/V los terceros y dems coeficientes viriales se hacen nulos, y luego haciendo a B = 0; se obtiene: 0= b a RT
T Boyle =
a Rb
(16)
I.6.
Ejercicios de Aplicacin:
Ingeniera Qumica
Ecuaciones 16
de
Estado
Los valores conocidos para los coeficientes viriales del vapor de isopropanol a 200C son: B =388 cm 3 mol1
C = 26000 cm6 mol2
Calclese V y Z para el vapor de isopropanol a 200C y 10 bar por: PV BP Z= =1 + a) La ecuacin RT RT ...
b) La ecuacin
Z=
PV B C =1 + + 2 RT V V ..
Solucin: La temperatura absoluta es T = 473.15 K y el valor apropiado de la constante de los gases es R = 83.14 cm3 bar mol-1K-1 a) Resolviendo la ecuacin para V se encuentra. V= RT + B =3934 388= 3456 cm3 mol 1 P
De donde: PV V 3546 Z= = = = 0.9014 RT RT / P 3934
b) Para facilitar la iteracin, se escribe la ecuacin () en la forma:
V i +1=
RT B C 1+ + 2 P Vi Vi
Donde le subndice i denota el numero de iteracin; para la primera, i=0
V 1= RT B C 1+ + 2 P V0 V0
)
)
Donde Vo es una primera aproximacin del volumen molar; para esto se usa el valor del volumen del gas ideal, con el que se obtiene. V 1= 3934 1
388 26000 = 3539 3934 39342
Ingeniera Qumica
Ecuaciones 17
de
Estado
La segunda iteracin depende del resultado.
V 2= RT B C 1+ + 2 P V1 V1
)
)
Por tanto V 2 =3934 1
388 26000 = 3495 3539 3539 2
La iteracin contina hasta que la diferencia V i+1 Vi es insignificante, y despus de cinco iteraciones el valor final es: V = 3488 c m 3 mol1
De donde: Z = 0.8866
II. LA ECUACION DE REDLICH KWONG.
II.1.
Generalidades:
Quin fue Otto Redlich? Otto Redlich (4 de noviembre de 1986 al 14 de agosto de 1978) fue un qumico austriaco fsico e ingeniero qumico que es mejor conocido por su desarrollo de las ecuaciones de estado, como la ecuacin de Redlich Kwong. Redlich naci en 1896 en Viena, Austria. Fue a la escuela en el distrito de Dobling de Viena. Despus de terminar la escuela en 1915 se uni al ejrcito hngaro de Austria y se desempeo como oficial de artillera, principalmente en el frente italiano en la primera guerra mundial. l fue herido y se convirti en un prisionero de guerra en agosto de 1918. Regres a Viena despus de la guerra en 1919. Estudio qumica y recibi su PhD. en 1922 por el trabajo sobre el
Ingeniera Qumica
Ecuaciones 18
de
Estado
equilibrio de Acido Ntrico, oxido nitroso y ntrico. l public su trabajo sobre la mejora de la ecuacin del gas ideal, en 1949, hoy conocida como la ecuacin de Redlich-Kwong de Estado. Redlich muri en California en 1978. Quin fue Jos N. Shun Kwong? Jos Neng Shun Kwong naci en Chung Won, China, el 28 de octubre de 1916, el mayor de los siete hermanos (uno de los nios y las hermanas de 6) que sobrevivieron a la edad adulta. Cuando tena unos 7 aos, la familia se mud a los Estados Unidos, donde su padre estudiaba optometra. Cuando su padre regres a China despus de completar su formacin, Kwong permaneci en Sacramento, California, con su abuelo, que haba emigrado a los EE.UU. en 1888 y construy un almacn de frutas y verduras. Kwong comenz su educacin en la Escuela Superior de Sacramento, y continu en el Junior College de Sacramento para los prximos dos aos, y ms en la Universidad de California en un ao. Kwong recibi su Bachillerato en Artes (BA) de la Universidad de Stanford en 1937 en Qumica y Ciencias Mdicas Bsicas, situndose entre los cinco primeros de su clase. Se le concedi su Maestra en Ciencias en Ingeniera Qumica y Metalrgica, con nfasis en las operaciones de la unidad, en la Universidad de Michigan, en octubre de 1939 y obtuvo su doctorado en Ingeniera Qumica, con especialidad en Qumica Fsica en la Universidad de Minnesota en el ao 1942. Su tesis doctoral vers sobre "La relacin de la superficie y la energa en el aplastamiento de los minerales", con el profesor Edgar Piret Lambert (1910-1987) como su asesor principal. El propsito de esta investigacin fue para confirmar la relacin de proporcionalidad directa entre la superficie de la nueva forma con el aplastamiento de algunos materiales slidos y la entrada de la energa, y tratando de desarrollar a continuacin la informacin bsica requerida en este campo. Los resultados de esta investigacin fueron presentados en un artculo publicado slo unos aos despus. Se convirti en un ingeniero profesional con licencia en California y las Universidades de Minnesota (1952). La Primera experiencia profesional de Kwong fue en Minnesota Mining and Manufacturing Co. (ms tarde 3M), donde se desempe como ingeniero qumico en productos adhesivos entre 1942 y 1944. Este fue un perodo en la historia de la empresa, cuando los intereses principales son el desarrollo de diferentes aplicaciones de las cintas de celofn (sensible a la presin, material transparente, a prueba de humedad con el pegamento) se complementan con la produccin de material de defensa de la Segunda Guerra Mundial, y otros tipos de cintas para diferentes usos. Kwong se encontraba en el rea de proceso, principalmente en relacin a la esterificacin, emulsificacin, y la sntesis de monmeros y la purificacin. Kwong fue el primer no-blanco profesional contratado por la empresa. Es muy probable que el conocimiento
Ingeniera Qumica
Ecuaciones 19
de
Estado
de que Jos Kugler, su primer gerente de 3M, tena de l desde sus das universitarios, y la alta reputacin cientfica de su asesor y sus servicios como consultor para la empresa ms de dos dcadas, tuviera cierta influencia en la contratacin de Kwong. En 1944, un ao antes de su naturalizacin como ciudadano estadounidense, Kwong se uni a Shell Cooperacin al Desarrollo, en Emeryville, California. All tuvo la oportunidad de trabajar en diferentes reas profesionales. Durante los primeros cinco aos, su investigacin ha sido como un qumico, as como fsico-qumico, siendo lder del proyecto para un grupo de hasta ocho personas. Ellos trabajaron en el desarrollo, construccin y operacin de unidades de plantas piloto para la esterificacin continua, la extraccin de prepolmero, monmero y la purificacin. Fue durante este perodo que Kwong conoci al qumico austraco Otto Redlich (1896-1978). Redlich haba emigrado a los Estados Unidos en 1938 despus de perder su trabajo en la Universidad Tecnolgica de Viena debido a la aplicacin en su pas de algunas leyes que restringan las actividades acadmicas para el pueblo judo, y se uni a Shell 7 aos ms tarde, despus de salir de Washington State College (donde fue Investigador Asociado). Adems de otros temas, Redlich mostro gran inters en llevar a cabo la investigacin sobre la termodinmica de las soluciones. Aunque no parece haber evidencia de las inclinaciones profesionales Kwong en esta rea de la ciencia, lo cierto es que en septiembre de 1948 presentaron un documento conjunto sobre una nueva ecuacin de estado en el Simposio sobre Termodinmica y la estructura molecular de las soluciones, que se celebr como parte de la 14 reunin de la American Chemical Society en Portland, Oregon, la cual fue publicada en febrero de 1949. La investigacin fue muy probablemente relacionada con sus actividades habituales de Shell, y la necesidad de la creacin de una expresin algebraica simple respecto a la representacin precisa de los datos experimentales volumtricas de los compuestos, principalmente hidrocarburos, que intervienen en los procesos de la empresa, lo que permiti el clculo de las fugacidades respectivas. La nueva ecuacin, RT a P= (V + b ) T 1/ 2 V b V donde P, v, y T, representan la presin, volumen molar y la temperatura, respectivamente, mientras que a y b son los parmetros especficos para cada fluido, no respondi de inmediato al reconocimiento que mereca. Slo casi dos dcadas despus empieza a ser apreciado ya que era lo suficientemente preciso para usarse en relacin con otras ecuaciones que tenan un mayor nmero de constantes. Incluso teniendo en cuenta sus limitaciones (que son principalmente debido a su carcter emprico que, en consecuencia, no le permite ofrecer resultados rigurosos y la consistencia termodinmica) y su
Ingeniera Qumica
Ecuaciones 20
de
Estado
derivacin propia de no polares (o ligeramente polares) las sustancias y sus mezclas (no es recomendable usarlo para los compuestos que forman enlaces de hidrgeno), todava se considera una de los dos mejores ecuaciones de dos constantes que se haya sido publicada. Junto con la ecuacin desarrollada por DY Peng y Robinson DB en 1976, la ecuacin de estado de Redlich-Kwong ofrece la mejor expresin de tercer grado y es una de las ecuaciones ms utilizadas de Estado en la industria para correlacionar equilibrio lquido-vapor y propiedades volumtricas y termodinmicas de sustancias puras y sus mezclas en la fase gaseosa. La ecuacin es integrada en el software y utilizada por los investigadores y estudiantes para la prediccin de propiedades volumtricas y termodinmicas, diseo y optimizacin de equipos de proceso y simulacin numrica de yacimientos. Parece que Kwong no retom los aspectos tericos de la termodinmica. Sus actividades en el ltimo ao en la Shell fueron, en cambio, sobre todo en las reas de las evaluaciones econmicas y el proceso de diseo y de ingeniera. En 1951 regres a 3M, en San Pablo, como un ingeniero qumico en la Divisin de Productos Qumicos. l fue asignado inicialmente a un proyecto para evaluar econmicamente la ruta del cido propinico con cido acrlico. Kwong lleg a la conclusin que la mejor alternativa era la ruta de acrilonitrilo, una sugerencia que una vez, que se llev a cabo por la Compaa, se tradujo en un ahorro de varios millones de dlares y utilidades por 16 aos. Este no fue el nico momento en que sus investigaciones contribuyeron a las ganancias de la compaa 3M. Su trabajo de investigacin sobre las resinas epoxi y materiales fluorados, que comenzaron en los aos 50 y continu todo el tiempo que trabaj all, trajo importantes beneficios a 3M tambin. En 1956, Kwong fue promovido a la posicin de Especialista de Ingeniero Qumico. Sus habilidades fueron reconocidas por lo que en la Compaa, que comenz sus contribuciones para cubrir los campos tcnicos diferentes a aquellos en los que estuvo involucrado oficialmente. Este era el caso, por ejemplo, cuando no haba una necesidad de nuevos alambiques grandes con estrictas especificaciones de presin y temperatura para la purificacin de monmero acrilato. A lo largo de su vida continu su desarrollo profesional en muchas reas, incluyendo cursos en programacin informtica, la qumica avanzada de polmero, y la financiacin de las empresas.
Ingeniera Qumica
Ecuaciones 21
de
Estado
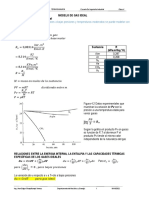
Figura N03: Jos Neng Shun Kwong II.2. Formulacin Matemtica. Introducida en 1949, la ecuacin de Redlich Kwong fue una mejora considerable sobre las otras ecuaciones de la poca. Aun goza de bastante inters debido a su expresin relativamente simple. Aunque es mejor que la ecuacin de Van Der Walls no da buenos resultados sobre la fase liquida y por ello no puede usarse para calcular precisamente los equilibrios liquido vapor. Sin embargo, puede usarse conjuntamente con expresiones concretas para la fase liquida en tal caso. La ecuacin de Redlich Kwong es adecuada para calcular las propiedades de la fase gaseosa cuando el cociente entre la presin y la presin crtica es menor que la mitad del cociente entre la temperatura y la temperatura critica. La ecuacin de estado de Redlich Kwong es muy utilizada para calcular propiedades termodinmicas para la fase vapor en combinacin con modelos termodinmicos ms complejos. Es adecuado para sistemas prximos al comportamiento ideal. La ecuacin de Redlich Kwong deriva de la ecuacin de estado trmico de Van Der Walls. La ecuacin del modelo es: RT a P= (V + b ) T 1/ 2 V b V
(17)
Esta ecuacin, al igual que otras ecuaciones cubicas de estado, tiene tres races para el volumen, de las cuales es posible que dos sean complejas. Los valores de V que tienen un significado fsico son siempre reales, positivos y mayores que la constante b.
Ingeniera Qumica
Ecuaciones 22
de
Estado
Figura 04: Isoterma que relaciona la presin y el volumen. En la figura 4 se observa que cuando T >Tc la solucin de
V
para cualquier
valor positivo de P proporciona solo una raz positiva real. Cuando T=Tc, esto tambin es cierto, excepto a la presin critica, donde existen tres races, todas iguales a V c. Para T < Tc, se tiene nicamente una raz real positiva cuando la presin es alta, pero para un intervalo de presiones menores existen tres races reales positivas. En este caso, la raz intermedia no tiene significado; la raz mas pequea es un liquido o un volumen similar al de un liquido, y la raz mas grande es un vapor o un volumen parecido a un vapor. Los volmenes de lquido y vapor saturados estn dados por las races ms pequeas y ms grande cuando P es la presin de saturacin o de vapor. Las constantes para la ecuacin (17) son:
/2 0.42748 R 2 T 5 C a= PC
(18)
b=
0.08664R T C PC
(19)
Ingeniera Qumica
Ecuaciones 23
de
Estado
Al tratarse de una ecuacin cubica de estado, no proporciona los mejores valores posibles, pero ellos son razonables y casi siempre pueden determinarse. II.3. Ejercicio de Aplicacin. Dado que la presin de vapor del cloruro de metilo a 60C es de 13.76 Bar, emplee la ecuacin de Redlich Kwong para calcular los volmenes molares del vapor y del lquido saturado a esas condiciones. Nota: Tc = 416.13 y Pc = 66.8 Solucin: /2 0.08664R T C 0.42748 R 2 T 5 C b = a = Mediante las ecuaciones: y se PC PC evalan las constantes a y b tomando los valores de la T c y Pc.
0.42748 (83.14 ) 2 ( 416.3 )2.5 a =
b=
( 0.08664 )(83.14 )( 416.3 ) = 44.891 cm3 mol1 66.8
El volumen molar del vapor saturado se obtiene sustituyendo los valores conocidos en la ecuacin: a (V i b ) RT + b 0.5 P T P V i ( V i + b)
V i + 1=
V i +1= 2057.83
622784 V i 44.891 Vi V i + 44.891
)
RT = 201294 cm 3 mol1 P y contina hasta
La iteracin comienza con converger en el Valor:
V i= V 0 =
V = 1712 cm3mol-1
Ingeniera Qumica
Ecuaciones 24
de
Estado
III. LA ECUACION DE PENG ROBINSON.
III.1.
Generalidades:
Qu Relacin hubo entre Peng y Robinson? Robinson tuvo una larga y distinguida carrera y una vida maravillosa, estaba muy interesado en la investigacin experimental y terica sobre los hidratos de gas, compuestos solidos, que se forman a partir de hidrocarburos en la presencia de agua, y que causan problemas de funcionamiento en la produccin de gas natural. En 1976, en colaboracin con su recin graduado estudiante de Doctorado Ding Yu Peng, desarroll la ecuacin de Peng Robinson. La ecuacin se aplica al calculo de equilibrio liquido-vapor de mezclas de hidrocarburos y gases como el sulfuro de hidrogeno y dixido de carbono a temperaturas elevadas. Robinson naci en Calgary, 3 de abril de 1922. Su familia se mudo al valle de Okanagan, donde la familia se ganaba la vida en un rancho de fruta. Se gradu de la escuela secundaria local en 1940, obtuvo su BASc de la universidad de Columbia Britnica en 1945, se gradu con una maestra al ao siguiente de la UBC, y pas a ganar su doctorado en la Universidad de Michigan en 1949. Despus de su distinguida carrera en la universidad de Alberta, donde finalmente se levanto para asumir la catedra del departamento de Ingeniera qumica y de Petrleo de 1958 a 1971.
Ingeniera Qumica
Ecuaciones 25
de
Estado
Figura N05: Ding Yu Peng
Formulacin Matemtica. La ecuacin de Peng Robinson fue desarrollada en 1976 para cumplir los siguientes objetivos: 1. Los parmetros haban de poder ser expresados en funcin de las propiedades crticas y el factora acntrico.
III.2. 2. El modelo deba ser razonablemente preciso cerca del punto critico,
particularmente para clculos del factor de compresibilidad y la densidad liquida.
3. Las reglas de mezclado no deban emplear ms que un parmetro sobre
las interacciones binarias, que deba ser independiente de la presin, temperatura y composicin. 4. La ecuacin deba ser aplicable a todos los clculos de todas las propiedades de los fluidos en procesos naturales de gases. RT a P= 2 + 2b V b2 ) V b (V
(20)
0.45723553 R2 T 2 c a= Pc
(21)
Ingeniera Qumica
Ecuaciones 26
de
Estado
b=
0.07779607 R T c Pc T Tc
(22)
T r=
(23)
=[ 1 + ( 0.37464 + 1.54226 0.26992 2 ) ( 1 T 0.5 r )]
(24)
Donde: R = Constante de los gases (8.31451 J/mol K)
= Factor Acntrico
III.3.
Ejercicios de Aplicacin.
Se tiene el sistema cilndrico pistn mostrado en la Figura N06, que contiene inicialmente una mezcla liquido-vapor de agua con una calidad de 0.6.El sistema se calienta hasta que el pistn apenas toca los topes. Luego se introduce 1kg de agua, momento en el cual la temperatura alcanza los 200C. Hallar la masa inicial del agua:
Figura N06: Sistema Cilndrico Pistn
Ingeniera Qumica
Ecuaciones 27
de
Estado
Propiedades para el agua: Tc=647.1 K Pc=22048.32KPa =0.345 Kg M=18.015 Kmol RU=8.31451
KJ Kmol.K RU =0.46153 M A2 = 3985.439 A3 =
La constante especfica del agua es:
R=
Las constantes de Antoine son: A1 = 6.532470 -38.9974 Solucin:
P1 = 100 KPa (el sistema se encuentra a presin atmosfrica) x1 = 0.6 Estamos en saturacin lquido vapor, se debe aplicar el criterio de Maxwell para determinar los volmenes especficos de las fases lquido y vapor, adems de la temperatura de saturacin. Se plantea el procedimiento iterativo:
1. Suponer Tsat, para lo cual se emplea la ecuacin de Antoine:
ln
=A ( Psat P ) T +A
c 1
A2
Donde T va en Kelvin
Despejando:
Ingeniera Qumica
Ecuaciones 28
de
Estado
T=
A2 Psat A1 ln ( ) PC
A3
As, el primer estimado es:
T 1=
A2 P A1 ln ( 1 ) PC
A3
T1 = 373.1139 K
T1 -
273.15=99.9639
2. Se resuelve la ecuacin cubica (Ecuacin Peng-Robinson):
RT a P= 2 + 2b V b2 ) V b (V Donde: R2 T 2 C a = 0.45724 PC
RT C b = 0.07780. P C
= 1.84976
=1.05385x10-3
En forma cubica: 3 + c2 . V 2 + c1 . V + c0 =0 V Con:
Ingeniera Qumica
Ecuaciones 29
de
Estado
c0 =b +
R.T. b 2 ab P a 2bRT 3 b 2 P
c1 =
c 2= b
RT P
2
=[ 1 + ( 0.37464 + 1.54226 0.26992 2 ) ( 1 T 0.5 r )]
Para la primera iteracin: 1 T 0.5 r 1 + ( 0.37464 + 1.54226 . w 0.2699 . w 2 ) . 1 =
R. T 1 . b 2 a. 1 . b c 0 =( b + )=2.66498x 105 P1
3
c 1 =(
a. 1 2bR T 1 3 b 2 )= 0.02347 P1
R T1 =1.72099 P1
c 2= b
Las races de la ecuacin cubica son: Coeficientes: Races
Ingeniera Qumica
Ecuaciones 30
de
Estado
Coef=
[]
c0 c1 c2 1
3
Liquido
vv: =polyroots (coef)
vv=
Gas
1.2499 10 0.01249 1.70725
]
vf1=1.2499 x10-3
vg1=vv2
vf1=vv0
vg1=1.70725
3. Comprobamos con el criterio de Maxwell:
1 Psat = . Pd V V gV f v
f
vg
En este caso: R.T. ln
V g b [ V + ( 1 2 ) . b ][ V f + ( 1 + 2 ) . b ] a. . ln [ g ] V f b 2. 2 . b [ V g + ( 1 + 2 ) . b ][ V f +( 1 2 ) . b ] 1 Psat = . V gV f
Comprobamos: R. T 1 . ln
V g1 b [ V + ( 1 2 ) . b ][ V f1+ ( 1 + 2 ) . b ] a.1 . ln [ g1 ] V f1 b 2. 2 . b [ V g1 + ( 1 + 2 ) . b ][ V f1 + ( 1 2 ) . b ] 1 Psat1= . V g1 V f1
Psat1 = 95.77063
diferente de P1=100
Para la segunda iteracin:
Ingeniera Qumica
Ecuaciones 31
de
Estado
Suponiendo una nueva temperatura (debe ser mayor, puesto quedamos por debajo de la presin) T2 = 101 + 273.15
2 1 + ( 0.37464 + 1.54226 . w 0.26992 . w 2 ) . ( 1 T 0.5 r ) = 1.46304 2=
C 0= b +
(
(
R. T 2 . b a.2.b 5 = 2.6601 10 P1
C1=
a. 2 2.b.R. T 2 3. b 2 = 0.02342 P1
C 2= b
R.T 2 =1.7257 7 P1
Recalculemos las races del polinomio cubico: Coeficientes: Races
Liquido
Coef =
[]
c0 c1 c2 1
3
vv=polyroots (coef)
vv=
gas
1.25109 x 10 0.01242 1.7121
]
vg2=vv2 vg2=1.7121
vf2=vv0
vf2=1.25109 x 10-3
Ingeniera Qumica
Ecuaciones 32
de
Estado
Comprobemos: V b [ V g2 + ( 1 2) . b ][ V f2+ ( 1+ 2) . b ] ] 1 a . 2 . [ R.T. ln g2 . ln V g2 V f2 V f2 b 2. 2 . b [ V g2 + ( 1+ 2 ) . b ][ V f2 + ( 1 2) . b ]
Psat2 =
Psat2 = 99.56147 El error es esa por debajo del 1%, podramos quedarnos con este valor, sin embargo, realicemos una iteracin adicional: Extrapolemos a P=100 T 3= inter Psat1 , T1 , 100 Psat2 T2
[( ) ( ) ]
T3 = 374.26986 K o
T3 - 273.15 =101.11986
Comprobamos nuevamente:
2 1 + ( 0.37464 + 1.54226 . w 0.26992 . w 2 ) . ( 1 T 0.5 r ) = 1.46304 3=
C 0= b +
R. T 3 . b a . 3.b 5 = 2.65954x 10 P1
C1=
(
(
a . 3 2.b.R. T 3 3. b 2 = 0.02341 P1
C 2= b
R.T 3 =1.72632 P1
Recalculemos las races del polinomio cubico: Coeficientes Races
Ingeniera Qumica
Ecuaciones 33
de
Estado
Coef=
[]
c0 c1 c2 1
3
Liquido
vv =polyroots (coef)
vv=
Gas
1.25123 10 0.01241 1.71266 vf3=vv0
]
vf3=1.25123*10-3 vg3=vv2 vg3=1.71266
Comprobemos:
Psat3=
[ V g3+ ( 1 2 ) . b ] [ V f3+ ( 1+ 2) . b ] V b a . 3 1 R. T 2 . ln g3 ln V g3 V f3 V f3 b 2 2 . b [ V g3 + ( 1+ 2 ) . b ][ V f3 + ( 1 2) . b ]
Psat3=99.70522 nos quedamos con esta temperatura. As: T1=T3 T1=374.26986
El volumen especfico de la mezcla es: v1=vf3+x1. (vg3-vf3) v1=1.0281m3/Kg
La masa viene dada por: El volumen total en el estado 1es: V1=1m3 m 1= V1 v1
m1=0.97267Kg
Ingeniera Qumica
Ecuaciones 34
de
Estado
CONCLUSIONES
La eleccin de la ecuacin a utilizar depender de la precisin que se
requiere y de las condiciones de operacin en las que se trabaje.
La ecuacin de virial, basada en la mecnica estadstica, puede
representarse fielmente el comportamiento. Sin embargo, es poco utilizada en ingeniera debido a la complicacin del clculo de los coeficientes.
Con las ecuaciones mencionadas en el trabajo, uno puede medir o
expresar la diferencia entre el comportamiento real y el ideal.
RECOMENDACIONES
La idea de buscar una expresin funcional que represente el
comportamiento de fluidos reales es muy tentadora, pero todava no se ha encontrado una expresin mgica que describa perfectamente el comportamiento de los gases.
Para efectuar los clculos de una forma mas sencilla se debe hacer uso
de software previamente programado.
Ingeniera Qumica
Ecuaciones 35
de
Estado
Para algunos clculos una tcnica muy til, es la del factor de
compresibilidad generalizado.
BIBLIOGRAFIA LIBRO CONSULTADO:
Smith, J.M., Van Ness, H.C., & Abbott M.M. (2007). Introduccin a la
termodinmica McGrawHill.
en ingeniera
Qumica
MxicoD.F.
(7.ed.):
PAGINAS WEB CONSULATADAS:
http://es.scribd.com/doc/76353962/La-ecuacion-virial-de-estado http://es.scribd.com/doc/31575060/ECUACIONES-DE-ESTADO http://www.itescam.edu.mx/principal/sylabus/fpdb/recursos/r81701.PDF http://www.ing.unrc.edu.ar/materias/termodinamica/archivos/2_propieda
des_fisicas_de_sustancias.pdf
http://es.scribd.com/doc/34963989/Problemas-Resuelto-de-
Ecuaciones-de-Estado
Ingeniera Qumica
Ecuaciones 36
de
Estado
ANEXOS ANEXO N01: Constantes Crticas:
ANEXO N02: Tabla De Constantes De La Ecuacin De Redlich Kwong:
Ingeniera Qumica
Ecuaciones 37
de
Estado
ANEXO N03: Carta Generalizada De Compresibilidad
Ingeniera Qumica
Ecuaciones 38
de
Estado
Ingeniera Qumica
Вам также может понравиться
- Camacho Valdiviezo Villafuerte Macro3Документ16 страницCamacho Valdiviezo Villafuerte Macro3Antoni Cjr7Оценок пока нет
- Mi Parte de Tu PapáДокумент2 страницыMi Parte de Tu PapáKevin E Reyes DiazОценок пока нет
- Tema I Propiedades ResidualesДокумент38 страницTema I Propiedades ResidualesMaría Alejandra Ballesteros100% (3)
- PRACTICA No 2 QuimiometriaДокумент15 страницPRACTICA No 2 QuimiometriaDANIELA NERI FABIANI CONTRERAS100% (1)
- Ejemplos Balances C Reaccion Recirculado Purga09PДокумент5 страницEjemplos Balances C Reaccion Recirculado Purga09PArthursskОценок пока нет
- TEF Primer Examen Parcial Parte BДокумент6 страницTEF Primer Examen Parcial Parte BEstefanía Angel ClavijoОценок пока нет
- Equilibrio Sólido-Vapor Del Carbamato de AmónioДокумент9 страницEquilibrio Sólido-Vapor Del Carbamato de Amónioleomirazu0% (1)
- Problemas de Termodinámica QuímicaДокумент12 страницProblemas de Termodinámica QuímicaLeonardo Poublette VegasОценок пока нет
- Ejercicios 01 (Métodos Númericos) PDFДокумент9 страницEjercicios 01 (Métodos Númericos) PDFLaura Yuliana Archila GonzalezОценок пока нет
- Cinética Química: Factores que Gobiernan la Velocidad de ReacciónДокумент40 страницCinética Química: Factores que Gobiernan la Velocidad de Reacciónnicolas acostaОценок пока нет
- Null 9Документ19 страницNull 9ahsimОценок пока нет
- Práctica #1 (Medidas) - 1Документ12 страницPráctica #1 (Medidas) - 1Edwin Pachacuti ApazaОценок пока нет
- IBIO 2415 Tarea1P2 - Transición de Fases AGДокумент1 страницаIBIO 2415 Tarea1P2 - Transición de Fases AGCarlos Israel Esparza AndradeОценок пока нет
- Primera Ecuacion de BerthelotДокумент8 страницPrimera Ecuacion de BerthelotDanny Paredes Layza100% (1)
- Determinación Del Coeficiente de PoissonДокумент10 страницDeterminación Del Coeficiente de PoissonJimena Apaza GuachallaОценок пока нет
- Laboratorio de Volumen Molar ParcialДокумент7 страницLaboratorio de Volumen Molar ParcialNachoo DiazОценок пока нет
- Equilibrio químico y constantes de equilibrioДокумент31 страницаEquilibrio químico y constantes de equilibrioValentina BecerraОценок пока нет
- Práctica PHДокумент2 страницыPráctica PHDiego MoralesОценок пока нет
- Balance de Masa TransienteДокумент23 страницыBalance de Masa TransienteAriel Jesxs Torres Henriqxez100% (1)
- Sistema líquido de tres componentesДокумент16 страницSistema líquido de tres componentesJessica Flores MirandaОценок пока нет
- 5 Heredia Ticona Cristian Marcelo Inf-5Документ44 страницы5 Heredia Ticona Cristian Marcelo Inf-5JUAN CARLOS CHALLCO QUISPEОценок пока нет
- Reacciones Homogeneas Catalizadas y AutocatalizadasДокумент4 страницыReacciones Homogeneas Catalizadas y AutocatalizadasMarcos Condorí PacoОценок пока нет
- Jeyssón Margos T1Документ8 страницJeyssón Margos T1johanaОценок пока нет
- Momento1 Grupo 12Документ25 страницMomento1 Grupo 12TCOAndres15 xОценок пока нет
- Teoría Eltqmc Capítulo IIДокумент20 страницTeoría Eltqmc Capítulo IIgerman aguayoОценок пока нет
- Diagramas de fases binarios: representación gráfica de la composición vs temperaturaДокумент9 страницDiagramas de fases binarios: representación gráfica de la composición vs temperaturaIvánMolinaОценок пока нет
- Sistemas de 1 OrdenДокумент10 страницSistemas de 1 OrdenCristian JohnnyОценок пока нет
- Propiedades coligativas soluciones electrolitosДокумент9 страницPropiedades coligativas soluciones electrolitosRicardo CruzОценок пока нет
- Efectos Termicos en Procesos Que Intervienen Reacciones QuimicasДокумент21 страницаEfectos Termicos en Procesos Que Intervienen Reacciones QuimicasElizabeth Sandoval MartinezОценок пока нет
- Tema 3bДокумент18 страницTema 3bMarco RamírezОценок пока нет
- Guía #4 - Energía Libre - Clausius Clapeyron 2021Документ4 страницыGuía #4 - Energía Libre - Clausius Clapeyron 2021Andreina RicattoОценок пока нет
- Equipo 1 - Reporte Practica 1Документ8 страницEquipo 1 - Reporte Practica 1Anayuri TrejoОценок пока нет
- 5to Parcial FQ PDFДокумент26 страниц5to Parcial FQ PDFdiegoОценок пока нет
- Apuntes de Balances de Materia y Energía 1Документ117 страницApuntes de Balances de Materia y Energía 1Erick Garcia100% (1)
- Conductividad de Soluciones ElectróliticasДокумент12 страницConductividad de Soluciones ElectróliticasVictor Mauricio Ugarte MamaniОценок пока нет
- Inf. 8 de FisicoquimicaДокумент8 страницInf. 8 de FisicoquimicaLucía Molina RamírezОценок пока нет
- Guia de Ejercicios Sistemas de Un ComponДокумент5 страницGuia de Ejercicios Sistemas de Un ComponDianita Ruano ContrerasОценок пока нет
- Problemas Básicos-Cyrhom - R. Simples - MLHPДокумент3 страницыProblemas Básicos-Cyrhom - R. Simples - MLHPGilberto ObregónОценок пока нет
- Clase 1-Ing. Química y TextilДокумент28 страницClase 1-Ing. Química y TextilsergiosanuelmpОценок пока нет
- Método de Las Velocidades InicialesДокумент5 страницMétodo de Las Velocidades InicialesFitoFuckОценок пока нет
- CUESTIONARIOДокумент1 страницаCUESTIONARIOGustavo EspinozaОценок пока нет
- Cap02 (1) Primera Ley y Otros Conceptos de La TermodinámicaДокумент47 страницCap02 (1) Primera Ley y Otros Conceptos de La TermodinámicaTeofilo Donaires Flores100% (1)
- Reporte Post-Laboratorio. Práctica 6Документ5 страницReporte Post-Laboratorio. Práctica 6KarenОценок пока нет
- EXAMEN FINAL 1-2021 (Página 1 de 2)Документ3 страницыEXAMEN FINAL 1-2021 (Página 1 de 2)CarMarquzОценок пока нет
- 05 c1 BALANCES EN ESTADO TRANSITORIOДокумент32 страницы05 c1 BALANCES EN ESTADO TRANSITORIOMelisa ParedesОценок пока нет
- P1 3º Parcial PDFДокумент2 страницыP1 3º Parcial PDFXimena Linares LauraОценок пока нет
- Calor Molar de Una Reacción QuímicaДокумент6 страницCalor Molar de Una Reacción QuímicaSebastian PertuzОценок пока нет
- Unidad 2. Balances de Materia CON Reacción QuímicaДокумент40 страницUnidad 2. Balances de Materia CON Reacción QuímicaTania Ocampo AlzateОценок пока нет
- Taller Nº3 Curva de Saturación - Tablas de Vapor PDFДокумент1 страницаTaller Nº3 Curva de Saturación - Tablas de Vapor PDFLuisa SemperteguiОценок пока нет
- PolarimetriaДокумент11 страницPolarimetriaGiuseppe Jerónimo MezaОценок пока нет
- Equilibrio químico PCl5Документ13 страницEquilibrio químico PCl5Oscar GonzalezОценок пока нет
- Ejemplo InformeДокумент23 страницыEjemplo InformesantiagoОценок пока нет
- Solu Ejem 7Документ23 страницыSolu Ejem 7Christian Velez De VillaОценок пока нет
- Determinación de dureza total en aguasДокумент4 страницыDeterminación de dureza total en aguasRicardo Aragón100% (1)
- Práctica 3 - Síntesis de Fenolftaleína (19-20)Документ5 страницPráctica 3 - Síntesis de Fenolftaleína (19-20)Ronny GarzonОценок пока нет
- La Ecuacion Virial de EstadoДокумент8 страницLa Ecuacion Virial de EstadoAlejandro Vanegas100% (1)
- Ecuaciones de EstadosДокумент8 страницEcuaciones de Estadoseduardo fariasОценок пока нет
- Universidad Nacional de San Antonio Abad Del Cusco OptyДокумент10 страницUniversidad Nacional de San Antonio Abad Del Cusco OptyLeoncio Hilario UmiyauriОценок пока нет
- Ecuaciones de EstadoДокумент13 страницEcuaciones de EstadoDaniel AvendañoОценок пока нет
- Casos de estudio de termodinámica: Solución mediante el uso de ASPENHYSYSОт EverandCasos de estudio de termodinámica: Solución mediante el uso de ASPENHYSYSРейтинг: 4.5 из 5 звезд4.5/5 (7)
- Introduccion EsaДокумент69 страницIntroduccion EsaErick ChavezОценок пока нет
- CXS 096s PDFДокумент7 страницCXS 096s PDFeevelinmpОценок пока нет
- Resultados Posibles de CPДокумент2 страницыResultados Posibles de CPErick ChavezОценок пока нет
- Estimulacion Temprana: Conocimiento y Actitud Sobre Estimulacion Temprana de Madres de Menores de 1 Año Del Centro de Salud Huaura - 2013Документ85 страницEstimulacion Temprana: Conocimiento y Actitud Sobre Estimulacion Temprana de Madres de Menores de 1 Año Del Centro de Salud Huaura - 2013Erick ChavezОценок пока нет
- TERCERA CLASE DesarrolladaДокумент2 страницыTERCERA CLASE DesarrolladaErick ChavezОценок пока нет
- Longitudes EquivalentesДокумент1 страницаLongitudes EquivalentesErick ChavezОценок пока нет
- Pronombres ReflexivosДокумент2 страницыPronombres ReflexivosErick ChavezОценок пока нет
- Ejercicio de Aplicacion-TДокумент5 страницEjercicio de Aplicacion-TErick ChavezОценок пока нет
- Longitudes EquivalentesДокумент1 страницаLongitudes EquivalentesErick ChavezОценок пока нет
- Tiempo de EscurrimientoДокумент49 страницTiempo de EscurrimientoErick ChavezОценок пока нет
- El Método de TracyДокумент19 страницEl Método de TracyyerkoОценок пока нет
- Instalación y Puesta en Marcha Del Laboratorio de Gas en La Escuela de Ingeniería de Petróleos.Документ404 страницыInstalación y Puesta en Marcha Del Laboratorio de Gas en La Escuela de Ingeniería de Petróleos.Jaminton Andres CabreraОценок пока нет
- Ecuación de Estado Redlich-Kwong Sustancias PurasДокумент5 страницEcuación de Estado Redlich-Kwong Sustancias PurasJhefer Avila OlorteguiОценок пока нет
- Seminarios FisicoquimicaДокумент41 страницаSeminarios FisicoquimicaAgustin GonzálezОценок пока нет
- Libro de FicoДокумент1 374 страницыLibro de FicoSherlin Almanza ObregonОценок пока нет
- 4 Composicion Del Gas NaturalДокумент13 страниц4 Composicion Del Gas NaturalAlexander DazaОценок пока нет
- Tratamiento de GasДокумент5 страницTratamiento de GasGregory RobainaОценок пока нет
- 2.5 Comportamiento de Afluencia en Pozos de Gas PDFДокумент25 страниц2.5 Comportamiento de Afluencia en Pozos de Gas PDFCarlos GurierrezОценок пока нет
- Módulo 2-2C2015Документ3 страницыMódulo 2-2C2015Mati GonzalezОценок пока нет
- SEM 04 - Capitulo 4 Modelo de Gas IdealДокумент8 страницSEM 04 - Capitulo 4 Modelo de Gas IdealLUCIA MIRELLA SALDA�A CARRANZAОценок пока нет
- Guia de TermoДокумент2 страницыGuia de TermoSantosErnestoMamaniApazaОценок пока нет
- Practico No 1 QMC022 2022Документ4 страницыPractico No 1 QMC022 2022Rodrigo Delgadillo ArceОценок пока нет
- Solución Taller FugacidadesДокумент5 страницSolución Taller Fugacidadesjairo menesesОценок пока нет
- Riqueza Del Gas BrutoДокумент39 страницRiqueza Del Gas BrutoCapr PérezОценок пока нет
- Problemas de Flujos de FluidosДокумент366 страницProblemas de Flujos de FluidosMarcela Raby81% (32)
- Gases RealesДокумент32 страницыGases RealesJose Luis Saenz PayetОценок пока нет
- Tarea 1-2 - Unidad 1 - Pedro Joaquin Sanchez Tenorio.Документ45 страницTarea 1-2 - Unidad 1 - Pedro Joaquin Sanchez Tenorio.PEDRO JOAQUIN S�NCHEZ TENORIO100% (1)
- Formulario de TermodinamicaДокумент2 страницыFormulario de Termodinamicaimagen26Оценок пока нет
- Alejandro Sulbaran v22251703 Maracaibo Termo IIДокумент42 страницыAlejandro Sulbaran v22251703 Maracaibo Termo IIAlejandro SulbaranОценок пока нет
- 2020-1 Fenomenos de Transporte I.unidad I-TeoríaДокумент13 страниц2020-1 Fenomenos de Transporte I.unidad I-TeoríaAndreina UzcateguiОценок пока нет
- Proyecto de SimulacionДокумент21 страницаProyecto de Simulacionguido oscar huanca mamaniОценок пока нет
- Gases Chapi 2Документ7 страницGases Chapi 2reynaldoОценок пока нет
- Gases RealesДокумент3 страницыGases RealesAnai Gutierres FuentesОценок пока нет
- Trabajo de Fisicoquimica 2Документ15 страницTrabajo de Fisicoquimica 2Sayuri Elena Petro MaceaОценок пока нет
- Presentacion de Diseño de Separadores1.1Документ36 страницPresentacion de Diseño de Separadores1.1arian cardenasОценок пока нет
- Diseño de Loops GCCДокумент91 страницаDiseño de Loops GCCJ Weimar EspinozaОценок пока нет
- Ecuaciones de EstadoДокумент28 страницEcuaciones de EstadoAny Sanchez83% (12)
- Estados CorrespondientesДокумент16 страницEstados CorrespondientesROSARIOMARTINEZ25100% (2)
- Ecuaciones de estado gases reales: modelos Van der Waals, Dieterici, virialДокумент17 страницEcuaciones de estado gases reales: modelos Van der Waals, Dieterici, virialDavid Vp KydОценок пока нет
- Manejo de Campo Del Gas Natural PDFДокумент21 страницаManejo de Campo Del Gas Natural PDF-zip-Оценок пока нет