Академический Документы
Профессиональный Документы
Культура Документы
Cine Tica
Загружено:
Scott SimsАвторское право
Доступные форматы
Поделиться этим документом
Поделиться или встроить документ
Этот документ был вам полезен?
Это неприемлемый материал?
Пожаловаться на этот документАвторское право:
Доступные форматы
Cine Tica
Загружено:
Scott SimsАвторское право:
Доступные форматы
07/10/2013
CINETICA QUMICA
La Termodinmica nos indica si una reaccin qumica puede ocurrir o no: G<0
H2 (g)
reaccin espontnea
1 O2 (g) 2 H2O(l)
CO2 (g)
G
G
-237,1 kJ/ mol
-397 kJ/ mol
C(diam) O2 (g)
Pero estas reacciones no se producen en condiciones ambiente! Lo que ocurre es que son muy lentas La Termodinmica no nos da informacin acerca de la velocidad a la cual ocurren las reacciones qumicas
07/10/2013
Cintica qumica
Es la rama de la Qumica que estudia la velocidad de las reacciones
Ejemplos de reacciones qumicas que ocurren a velocidades muy diferentes
Factores que afectan la velocidad de las reacciones qumicas
Naturaleza de los reactivos rea superficial de reactivos
slidos o lquidos
Concentraciones (o presiones
parciales) de los reactivos
Temperatura Presencia de un catalizador
07/10/2013
La velocidad de reaccin se mide a travs de la velocidad de desaparicin de los reactivos o de la velocidad de formacin de los productos Para la reaccin: A B [B]
[A]
La velocidad de una reaccin qumica indica cmo vara la concentracin de reactivos o productos con el tiempo.
Velocidad media
v [A] t [B] t
B
A
A
v v
[B] t [A] t
(0,26 0) M (10 0) min
0,026 M / min 0,026 M / min
(0,74 1) M (10 0) min
v: unidades de concentracin x tiempo-1 (p. ej. M s-1) Para A B la velocidad a la que se consumen los reactivos es igual a la velocidad a la aparecen los productos Pero para la reaccin 2 A B no es as
07/10/2013
Velocidades media e instantnea
A B Velocidad media
v v [A] t
[A]
tangente al tiempo t
Velocidad instantnea d [A] v dt
Para una reaccin general: aA+bB
1 d[A] a dt
cC+dD
1 d[C] c dt 1 d[D] d dt
1 d[B] b dt
Ejemplos:
NO + O3 NO2 + O2
d[NO] dt 1 d[HI] 2 dt
d[O3 ] dt d[I2 ] dt
d[NO2 ] dt d[H2 ] dt
d[O2 ] dt
2 HI(g)
I2(g) + H2(g)
07/10/2013
Ley de velocidad
aA+bB cC+dD de las
La velocidad de una reaccin es funcin concentraciones de reactivos y productos.
Consideraremos los casos en los que v es slo funcin de las concentraciones de reactivos:
k [ A ]m [B]n
Ley de velocidad
v: velocidad k: constante de velocidad, o velocidad especfica m: orden de reaccin respecto de A n: orden de reaccin respecto de B n + m: orden global de reaccin n y m deben determinarse experimentalmente
En general el orden de reaccin no est relacionado con los coeficientes estequiomtricos de la ecuacin balanceada Ejemplos: I2(g) + H2(g) 2 HI(g)
v d[H2 ] dt k[H2 ] [I2 ]
Br2(g) + H2(g)
2 HBr(g)
d[H2 ] dt
k[H2 ] [Br2 ]1/ 2
Los rdenes de reaccin pueden ser nmeros enteros o fraccionarios
07/10/2013
Orden cero
Orden uno
Orden dos
Las unidades de la constante de velocidad (k) dependen del orden de reaccin n ley de veloc. unidades de k unidades de v
Molaridad (M) = moles L-1
07/10/2013
Leyes de velocidad integradas
Para conocer cmo varan las concentraciones de los reactivos y productos en funcin del tiempo podemos integrar las leyes de velocidad.
Tiempo medio de reaccin (t1/2): tiempo necesario para que la concentracin inicial de reactivo se reduzca a la mitad. Para t=t1/2,
A A0 2
Reacciones de orden cero
Para la reaccin A
d[A]
[A]
B:
k dt
t
v=
d[A] =
[A] 0 t =0
k dt
Veloc. de reaccin
d[A] =k dt
Tiempo
Conc. de reactivo
[ A ] [A] 0 = kt
[ A ] = [A] 0 kt
m= -k
Tiempo
07/10/2013
Reacciones de orden cero
Tiempo medio
[ A ] = [A] 0 kt Al tiempo medio : A A0 = [A] 0 kt1/2 2
[A]0/2
A0 2
t1/2
A0 2k
Reacciones de primer orden
Para la reaccin A
d[A] [A]
[A]
B:
v=
d[A] =k A dt
k dt
d[A] t = k dt [A] 0 [A] t =0
ln [A] = kt [A] 0
Tiempo (minutos)
ln[ A ] ln[A] 0 = kt
[A] [ A] 0 e -kt
Muchos procesos presentan una cintica de primer orden
07/10/2013
Reacciones de primer orden
Tiempo medio
ln ln
[ A ]t = kt [ A ]0 [ A ]0 = kt1 / 2 2[ A ]0
ln 2 = t1 / 2 k
(independiente de [A]0)
Relacin entre k y t1/2
k pequea Concentracin molar de A, [A] t1/2 largo
t1/2 corto k grande
Tiempo
07/10/2013
Reacciones de segundo orden
Para la reaccin A
d[A] [A] 2
[A]
B:
v=
d[A] =k A dt
k dt
d[A] t = k dt 2 [A] 0 [A] t =0
1 1 = kt [ A ] [A] 0 1 [A] 1 [A] 0 kt
Reacciones de segundo orden
Tiempo medio
1 1 = kt + [A] [A] 0
Si t = t1/2, [A]t = [A]0/2
t1/2 = 1 [A] 0 k
10
07/10/2013
Comparacin entre primer y segundo orden
Concentracin molar del reactivo,
Orden 2, k pequeo Orden 1, k pequeo
Orden 2, k grande Orden 1, k grande Tiempo
Orden
Ecuac. de veloc.
Ecuac. Integrada
Tiempo medio
Cero
v=k
[A] - [A]0
kt
t 1/ 2
[ A ]0 2k ln 2 k
Uno
v = k [A]
ln
[A] [A]0
kt
t 1/ 2
Dos
v = k [A]2
1 [A]
1 [ A ]0
kt
t 1/ 2
1 k[ A ]0
11
07/10/2013
Determinacin experimental de las leyes de velocidad
1) Mtodo de las velocidades iniciales Para la reaccin v = k [A]n [B]m A+2B C
Cules son los valores de n y m?
Se determina experimentalmente la velocidad inicial a diferentes concentraciones iniciales de reactivo:
vinicial /Ms-1 5.50 x 10-6 2.20 x 10-5 1.65 x 10-5 [A]0 0.10 0.20 0.10 [B]0 0.10 0.10 0.30
vinicial /Ms-1 v1 v2 v3 5.50 x 10-6 2.20 x 10-5 1.65 x 10-5
[A]0 0.10 0.20 0.10
[B]0 0.10 0.10 0.30
v1 v2
5.50 10 6 M/s 2.20 10 5 M/s 1 4 1 2
n
1 4
k(0.10 M)n (0.10 M)m k(0.20 M)m (0.10 M)m n 2
v1 v3
5.50 10 6 M/s 1.65 10 5 M/s 1 3 1 3
m
1 3
k(0.10 M)n (0.10 M)m k(0.10 M)n (0.30 M)m m 1
12
07/10/2013
Luego se debe hallar el valor de k:
5.50 10 6 Ms -1 (0.10 M)2 0.10 M
5.50 10 3 M-2s-1
Entonces la ley de velocidad es:
v = 5.50 x 10-3 M-2s-1 [A]2 [B]
Determinacin experimental de las leyes de velocidad
2) Mtodo de ensayo: se determina la concentracin de reactivo a distintos intervalos de tiempo. a) Se reemplaza en la ecuacin integrada de velocidad y se calcula k. Aquella ecuacin que proporcione el valor ms constante, es la que mejor corresponde al orden de reaccin. b) Se grafican los valores de acuerdo a las ecuaciones integradas de velocidad.
13
07/10/2013
Ejemplo: para la reaccin Br2(ac) + HCOOH(ac) 2 Br-(ac) + 2 H+(ac) + CO2(g)
se coloca un gran exceso de HCOOH y se mide la concentracin de Br2 en funcin del tiempo:
tiempo / s 0 50 100 150 200 250 300 350 400 [Br2] 0,0120 0,0101 0,00846 0,00710 0,00596 0,00500 0,00420 0,00353 0,00296
tiempo / s 0 50 100 150 200 250 300 350 400
[Br2] 0,0120 0,0101 0,00846 0,00710 0,00596 0,00500 0,00420 0,00353 0,00296
Orden cero:
0,0101 0,0120 = - k x 50 0,00596 0,0120 = - k x 200 0,00296 0,0120 = - k x 400 k = 1,98x10-4 M/s
k = 3,02x10-5 M/s
k = 2,26x10-5 M/s
0.014 0.012 0.010
[Br2]
0.008 0.006 0.004 0.002 0 100 200 300 400 500
t / seg
14
07/10/2013
tiempo / s 0 50 100 150 200 250 300 350 400
-4
[Br2] 0,0120 0,0101 0,00846 0,00710 0,00596 0,00500 0,00420 0,00353 0,00296
Primer orden:
ln 0.0101 0.0120 0.00596 0.0120 0.00296 0.0120 k 50 k 3.4 10 3 s 1
ln
k 200
3.5 10 3 s 1
ln
k 400
3.5 10 3 s 1
ln [Br2]
-5
-6 0 100 200 300 400 500
t/s
tiempo / s 0 50 100 150 200 250 300 350 400
400 350 300 250 200 150 100 50 0 0
[Br2] 0,0120 0,0101 0,00846 0,00710 0,00596 0,00500 0,00420 0,00353 0,00296
Segundo orden:
1 1 0.0101 0.0120 1 0.00596 1 0.00296 1 0.0120 1 0.0120 k 50 k 0.31
k 200
0.42
k 400
0.64
1 / [Br2]
100 200 300 400 500
t/s
15
07/10/2013
Determinacin experimental de las leyes de velocidad
3) Tiempo medio de reaccin
t 1/ 2
Ejemplo:
cte
1 1 Cn 0
En la descomposicin del acetaldehdo gaseoso a 528 C se encontr que el tiempo necesario para descomponer la mitad del material era 410 s cuando la concentracin inicial era 0,0363 M y 880 s para una concentracin inicial de 0,0169 M. Cul es el orden de la reaccin? Cunto vale la constante de velocidad?
Si es de segundo orden:
1 k C0 1 t 1/ 2 C 0
t 1/ 2
k k
1 410 s 0,0363 M 1 880 s 0,0169 M
6,72 10 2 M 1s 6,72 10 2 M 1s
(Era de segundo orden!)
16
07/10/2013
Mecanismos de reaccin
Experimento Ley de velocidad Ley de velocidad Mecanismo
El mecanismo de reaccin es el proceso molecular detallado mediante el cual procede una reaccin qumica. Proporciona los pasos a travs de los cuales los reactivos se transforman en productos Consiste en una serie de etapas elementales que se combinan para dar el mecanismo observado de reaccin.
Etapa elemental: es una ecuacin qumica o reaccin que describe un proceso tal cual ocurre a nivel molecular. Es un evento de reaccin sencillo que ocurre en una simple colisin atmica o molecular. Molecularidad: nmero de molculas que intervienen en una etapa elemental de reaccin. Los procesos pueden ser unimoleculares, bimoleculares o termoleculares.
17
07/10/2013
Mecanismo de reaccin
NO2 + CO NO + CO2
(reaccin global)
NO2 + NO2
k1
NO + NO3
NO3 + CO
k2
NO2 + CO2
Otro ejemplo: 2 N2O 2N2 + O2
Etapa 1
Etapa 2
18
07/10/2013
Molecularidad
Nmero de molculas de reactivo que intervienen en un proceso elemental. Proceso unimolecular:
Proceso bimolecular:
Proceso termolecular:
(son raros)
La molecularidad coincide con el orden de reaccin del proceso elemental. Las reacciones o etapas elementales unimoleculares presentan leyes de velocidad de primer orden: A productos v = k [A]
Las reacciones o etapas elementales bimoleculares presentan leyes de velocidad de segundo orden: A+A A+B productos productos v = k [A]2 v = k [A] [B]
19
07/10/2013
Cuando un mecanismo de reaccin est formado por una serie de etapas elementales la ley de velocidad global estar determinada por la etapa ms lenta, llamada paso determinante de la velocidad.
Para la reaccin: 3A+2B A+ B A+ E A+ F H+G+B 3A+2B C+D E+F H G C+D C+D
Si la primera etapa es la ms lenta:
1 d[ A ] 3 dt
k 1[ A ] [B]
20
07/10/2013
Un mecanismo de reaccin propuesto debe dar lugar a una ley de velocidad que concuerde con aqulla determinada experimentalmente Para la reaccin NO2 2 NO + O2
La ley de velocidad experimental es v = k[NO2]2 Se proponen dos mecanismos: NO2 NO + O O + NO2 O2 + NO 2 NO2 NO3 NO3 + NO NO + O2 (lento) (rpido) (lento) (rpido)
Cul sera el correcto?
Un mecanismo es posible si: da la correcta estequiometra global predice la ley de velocidad correcta parece qumicamente razonable Un mecanismo nunca puede ser probado en forma absoluta, pero se puede encontrar buena evidencia detectando alguno de los intermediarios postulados en l.
21
07/10/2013
Efecto de la temperatura sobre la velocidad de reaccin
En general la velocidad de una reaccin qumica aumenta al aumentar la temperatura. Esto se debe a que al cambiar T cambia el valor de k.
2 N 2 O5 temp / C 25 45 65
4 NO2 + O2 k 3.46 x 10-5 4.19 x 10-4 4.87 x 10-3
Ecuacin de Arrhenius
(Dependencia de la constante de velocidad con la temperatura)
S. Arrhenius
Ae
Ea
RT
A: factor pre-exponencial Ea: energa de activacin
T: temperatura absoluta (en K) R: contante universal de los gases R= 8,31 J/ K mol = 1,98 cal/ K mol
A y Ea son independientes de T, pero dependen de cada reaccin en particular
22
07/10/2013
Logaritmo de la constante de velocidad, ln k
Ae
Ea / RT
En forma linealizada:
ln k ln A Ea RT
Pendiente = -Ea/R
ln
k2 k1
Ea 1 R T2
1 T1
1/Temperatura, 1/T
Conociendo k a dos temperaturas diferentes es posible calcular Ea
Ej.: Calcular la energa de activacin de una reaccin para la cual las constantes de velocidad son 0,0162 y 0,0238 s-1 a 640 y 646 K, respectivamente. Cul ser el valor de la constante de velocidad a 650 K?
ln
T1= 640 K T2= 646 K T1= 640 K T3= 650 K
k2 k1
Ea 1 R T2
1 T1
k1= 0,0162 s-1 k2= 0,0238 s-1 k1= 0,0162 s-1 Ea hallado
despejamos Ea
despejamos k3
Rtas: Ea = 220,7 kJ/ mol ; k3 (650 K) = 0,0307 s-1
23
07/10/2013
Teora de las colisiones
Es una teora enunciada para reacciones en fase gaseosa. Al aumentar la temperatura las molculas tienen mayor energa (de acuerdo a la Teora Cintica de los Gases) y aumenta el nmero de colisiones. Los reactivos necesitan chocar para reaccionar, pero no se produce reaccin en todas las colisiones. Las molculas deben tener una cierta energa mnima para reaccionar.
Las molculas de los reactivos deben poseer la energa suficiente (llamada E de activacin) para que pueda ocurrir la ruptura de enlaces, un reordenamiento de los tomos y luego la formacin de los productos. Si no se dispone de la E suficiente las molculas rebotan sin formar los productos.
24
07/10/2013
Energa de activacin (Ea): es la mnima cantidad de energa necesaria para iniciar una reaccin qumica determinada.
Ea
La fraccin del nmero total de molculas que colisionan con una energa cintica mayor a Ea se muestran en las regiones sombreadas debajo de las curvas. Esta fraccin aumenta rpidamente al aumentar la temperatura.
Baja temperatura
Fraccin de molculas
Alta temperatura
Energa cintica
Adems, las molculas de los reactivos deben tener la orientacin adecuada durante el choque.
Reaccin
Sin reaccin
Cono de reaccin
25
07/10/2013
NO + N2O
NO2 + N2
Hay reaccin
Reactivos
Colisin
Productos
Colisin efectiva
NO + N2O
NO2 + N2
No No hay hay reaccin reaccin
Reactivos
Colisin
Reactivos
Colisin no efectiva
26
07/10/2013
NO + N2O
NO2 + N2
No hay reaccin
Reactivos
Colisin
Reactivos
Colisin no efectiva
Teora de colisiones
Ae
Ea / RT
A (factor pre-exponencial): depende de la frecuencia de colisiones entre molculas de reactivos y de la orientacin que adoptan las mismas. Ea (energa de activacin): energa mnima que deben tener las molculas de los reactivos para transformarse en productos. Si la colisin cumple con los dos requisitos (energa suficiente y orientacin adecuada) se dice que es efectiva y ocurre la reaccin.
27
07/10/2013
Teora del complejo activado
Puede considerarse una generalizacin de la Teora de Colisiones que sirve tambin para soluciones (incluye el efecto del solvente). Cuando los reactivos se aproximan se produce la formacin de un estado de transicin de alta energa, inestable y de corta duracin denominado complejo activado. La energa que necesitan los reactivos para alcanzar este complejo es la energa de activacin.
En el complejo activado los enlaces en los reactivos comienzan a debilitarse y los enlaces en los productos comienzan a formarse:
28
07/10/2013
A+B
C+D
Reaccin exotrmica
Reaccin endotrmica
HR< 0
HR > 0
N2O (g) + NO (g)
N2 (g) + NO2 (g)
29
07/10/2013
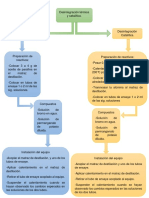
Catlisis
Un catalizador es una sustancia que afecta la velocidad de la reaccin pero cuya concentracin no se modifica y por tanto no participa en el balance de reaccin global. Si el catalizador acelera la reaccin se denomina acelerador o catalizador positivo. Si el catalizador frena la reaccin se denomina inhibidor o catalizador negativo. Catalizadores: Se recuperan al final de la reaccin Bastan pequeas cantidades Sufren cambios fsicos pero no qumicos
Catlisis
Los catalizadores proveen un camino de reaccin alternativo con menor energa de activacin.
30
07/10/2013
Catlisis homognea
El catalizador y los reactivos estn en la misma fase. Ejemplo:
Los iones Brcatalizan la reaccin
Catlisis heterognea
El catalizador y los reactivos estn en distinta fase.
C2H4 + H2
C2H6
Otro ejemplo: sntesis de NH3 en presencia de Fe metlico:
Fe
N2 + 3H2
2 NH3
31
07/10/2013
Conversores catalticos
Los conversores catalticos aceleran la oxidacin sustancias txicas o peligrosas para el medio ambiente. de
Contienen materiales cermicos y xidos (p. ej. CeO2). Los catalizadores son en general metales nobles (Pt, Pd, Rh) finamente divididos.
CO + hidrocarburos (combustin incompleta) + O2 2NO + 2NO2
conversor cataltico 2N2 + 3O2
conversor CO2 + H2O cataltico
Catlisis enzimtica
Es un tipo particular de catlisis homognea.
Las enzimas son catalizadores biolgicos muy selectivos y especficos.
E+S
E-S
E+P
32
Вам также может понравиться
- AmalgamaДокумент33 страницыAmalgamaCLAUDIA PATRICIA ROCHA FERNANDEZ100% (1)
- EJERCICIO 4 - EdwarДокумент4 страницыEJERCICIO 4 - EdwarMariluz RequenaОценок пока нет
- PDF Practica 6 DLДокумент11 страницPDF Practica 6 DLJuanОценок пока нет
- TESIS M. M. TREJO PEREZ R PDFДокумент62 страницыTESIS M. M. TREJO PEREZ R PDFLeticia M. ChoqueОценок пока нет
- Restaurante I Sanitarias 3Документ1 страницаRestaurante I Sanitarias 3MARLO MORENO TORRESОценок пока нет
- Informe de Queso UcayalinoДокумент23 страницыInforme de Queso UcayalinoCinthia GraceОценок пока нет
- Caracterizacion FitoquimicaДокумент11 страницCaracterizacion Fitoquimicaalanbecker_alОценок пока нет
- ResuemenДокумент3 страницыResuemenWendy PeralesОценок пока нет
- Identificación de Residuos PeligrososДокумент2 страницыIdentificación de Residuos PeligrososJacob LunaОценок пока нет
- Efecto Del PH en SedimentaciónДокумент2 страницыEfecto Del PH en SedimentaciónEmanuel Juan Flores ArbulúОценок пока нет
- Para ScribДокумент4 страницыPara ScribJose H. MezaОценок пока нет
- El Mercurio en BoliviaДокумент3 страницыEl Mercurio en BoliviaPaola Daniela Ossio EscobarОценок пока нет
- ACFrOgCzJv3bQxvfVWuIRtpchLHqYQqRn9pVPn jlhYgWachtTR7oBJQjqHtVg4TSd nHpRR8lkW7y0vUqu12MXVP2jMt06Zkap6Kdpo1DG758xnqewpZnD NeFNtGXrI1Hh4Mu77jZpm0gLD3oGДокумент9 страницACFrOgCzJv3bQxvfVWuIRtpchLHqYQqRn9pVPn jlhYgWachtTR7oBJQjqHtVg4TSd nHpRR8lkW7y0vUqu12MXVP2jMt06Zkap6Kdpo1DG758xnqewpZnD NeFNtGXrI1Hh4Mu77jZpm0gLD3oGZuñiga Garcia ErikОценок пока нет
- Estado de Oxidacion y Oxidos BasicosДокумент5 страницEstado de Oxidacion y Oxidos BasicosKennedy FloresОценок пока нет
- Cotización GENTICENTROДокумент10 страницCotización GENTICENTROjose diazОценок пока нет
- Icue T2 1 06 ATEXДокумент25 страницIcue T2 1 06 ATEXEugenio DíazОценок пока нет
- Diagrama de BloquesДокумент1 страницаDiagrama de BloquesNatyeli Gr100% (1)
- Trabajo 3. Crecimiento Microbiano - Contreras & LopezДокумент23 страницыTrabajo 3. Crecimiento Microbiano - Contreras & LopezMaria ContrerasОценок пока нет
- Analisis Quimico de Nutrientes en La Semilla de Hyptis Suaveolens ChanДокумент71 страницаAnalisis Quimico de Nutrientes en La Semilla de Hyptis Suaveolens ChanCarlos SalazarОценок пока нет
- P10. Inmunodifusión Radial - Carmen Paredes BermejoДокумент5 страницP10. Inmunodifusión Radial - Carmen Paredes BermejoMayca Paredes BermejoОценок пока нет
- Ingeniería Aplicada de Yacimientos Petrolíferos 1ra Edicion B. C. Craft, M. F. HawkinsДокумент282 страницыIngeniería Aplicada de Yacimientos Petrolíferos 1ra Edicion B. C. Craft, M. F. HawkinsIver Pachuri GuajareОценок пока нет
- S1 Práctica de AulaДокумент3 страницыS1 Práctica de AulaMaria Cabanillas DiazОценок пока нет
- Mss Prestigio C1 2022Документ93 страницыMss Prestigio C1 2022Dani Tanielita JaimesОценок пока нет
- Guía Transitoria Acorde A La Estrategia 1 Mediada Por Tecnología de Farmacotecnia 152001Документ19 страницGuía Transitoria Acorde A La Estrategia 1 Mediada Por Tecnología de Farmacotecnia 152001Sarat Valentina Angarita Rincon100% (1)
- Cuadernillo Biologia 4to Año-1Документ13 страницCuadernillo Biologia 4to Año-1Ezequiel QuirogaОценок пока нет
- Taller 1, Tercer CorteДокумент3 страницыTaller 1, Tercer Corteshirley leonОценок пока нет
- Infografía Sobre ConcretoДокумент5 страницInfografía Sobre ConcretoAndrea J. Luján RosalesОценок пока нет
- Examen Parcial de Elementos QuimicosДокумент2 страницыExamen Parcial de Elementos QuimicosTonatzin Sotelo GarciaОценок пока нет
- Coeficientes de Trasnferencia de Masa en Flujo LaminarДокумент19 страницCoeficientes de Trasnferencia de Masa en Flujo LaminarMelissa GómezОценок пока нет
- Obtencion Del Gas de Sisntesis A Partir de Carbono y Biomasa-PetroquimicaДокумент10 страницObtencion Del Gas de Sisntesis A Partir de Carbono y Biomasa-PetroquimicaDUANE MADELEINE MONTERO MENDEZОценок пока нет