Академический Документы
Профессиональный Документы
Культура Документы
942 1146 1 PB
Загружено:
Daniela Fernanda Hormazabal UbillaОригинальное название
Авторское право
Доступные форматы
Поделиться этим документом
Поделиться или встроить документ
Этот документ был вам полезен?
Это неприемлемый материал?
Пожаловаться на этот документАвторское право:
Доступные форматы
942 1146 1 PB
Загружено:
Daniela Fernanda Hormazabal UbillaАвторское право:
Доступные форматы
Reduca (Recursos Educativos)
Serie Qumica de Materiales. 4 (3): 211-284, 2012
ISSN: 1989-5003
211
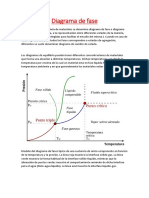
Diagramas y transformaciones de fase
6. Solidificacin
M Concepcin Merino Casals
Departamento de Ciencia de los Materiales e Ingeniera Metalrgica.
Facultad de Ciencias Qumicas. Ciudad Universitaria 28040 Madrid
cmerinoc@quim.ucm.es
Resumen: Se estudian las caractersticas de la nucleacin de slidos en lquidos, tanto
la nucleacin homognea como la nucleacin heterognea. Una vez producida la
nucleacin el proceso de solidificacin contina mediante el crecimiento de slidos en
lquidos. Las caractersticas del crecimiento de los metales estn controladas por que la
solidificacin se produzca bajo un determinado tipo de gradiente de temperaturas. Se
establece que formas de crecimiento adoptan tanto los metales puros como los no
metales. Para poder justificar las formas de crecimiento de las aleaciones hay que
establecer las condiciones de enfriamiento de una aleacin monofsica. Los lingotes
son unas piezas de elevada seccin que condicionan las formas de los cristales as
como los defectos que se producen en ellos. Continuamos con la solidificacin
eutctica, el crecimiento de eutcticos tanto facetados como no facetados y laminares
y el efecto de las impurezas en los eutcticos. Se explica tambin la zona de
crecimiento cooperativo de eutcticos, los eutcticos divorciados y las aleaciones de
composicin fuera del eutctico. La otra forma comn de solidificar una aleacin es
por reaccin peritctica, donde adems de las caractersticas de estas
transformaciones vemos las diferencias entre las estructuras eutcticas y peritcticas.
Palabras clave: Nucleacin de slidos en lquidos. Crecimiento de slidos en lquidos.
Enfriamiento de una aleacin monofsica. Solidificacin de lingotes. Solidificacin
eutctica. Solidificacin peritctica.
INTRODUCCIN
La solidificacin es una transformacin en la que un lquido que no tiene
estructura cristalina, pasa a un slido con estructura cristalina. Dentro de los procesos
que incluyen la solidificacin estn los procesos de colada ya sea en moldes, lingoteras
o por colada continua. Tambin en los procesos de soldadura est presenta la
solidificacin, as como en el crecimiento de monocristales (semiconductores) o en la
fabricacin de composites.
Podemos ver en la tabla 1 las diferencias fundamentales entre las propiedades
de la fase slida y la fase lquida. Como se observa en la tabla la primera diferencia
Reduca (Recursos Educativos)
Serie Qumica de Materiales. 4 (3): 211-284, 2012
ISSN: 1989-5003
212
fundamental es que sea o no una fase cristalina y que la ordenacin atmica sea de
largo o corto alcance. Este hecho est relacionado con que la estructura cristalina no
se altere o lo haga de forma ms o menos lenta, que est en contraposicin con el
cambio constante de la fase lquida. Las propiedades de los slidos estn
condicionadas por el tipo de enlace (metales, cermicos y polmeros) y en el caso de
los lquidos por los defectos. En cuanto a la conductividad es la misma independiente
de que sea fase lquida o slida.
Tabla 1. Propiedades de la fase slida y la fase lquida.
LA NUCLEACIN DE SLIDOS EN LQUIDOS
La solidificacin es una transformacin que se produce de forma discontinua. Es
necesaria la presencia simultnea de las fases slida y lquida y se produce por la
nucleacin y crecimiento de un slido en el seno de un lquido. Cuando la presin es
constante, normalmente la presin es la atmosfrica, la temperatura de equilibrio de
las dos fases slido y lquido es la temperatura de fusin
T
f
. Podemos seguir el proceso
de solidificacin mediante la figura 1. En ella se representa la variacin de energa libre
con la temperatura para la fase slida y lquida. Si la temperatura es mayor que T
f
la
fase lquida L es ms estable que la fase slida S. Por el contrario si la temperatura es
menor que T
f
fusin la fase slida S es ms estable que la fase lquida L. La temperatura
de fusin corresponde al punto donde las energas libres de la fase slida y la de la
liquida son iguales, G
S
= G
L
y por tanto el punto de interseccin de las dos curvas es la
temperatura de fusin.
Propiedad Fase lquida Fase slida
Tipo de fase No cristalina Cristalina
Ordenacin atmica Corto alcance Largo alcance
Movilidad atmica Alta Baja
Facilidad cambio estructura Cambio constante No se altera
Fluidez S No
Propiedades Similares f (defectos) Diferentes f (enlace)
Nmero de coordinacin Aproximadamente constante Diferente
Conductividad elctrica Similar Diferente
Conductividad trmica Similar Diferente
Reduca (Recursos Educativos)
Serie Qumica de Materiales. 4 (3): 211-284, 2012
ISSN: 1989-5003
213
Figura 1. Representacin esquemtica de G frente a la temperatura para las fases S y L. El punto de
interseccin corresponde al punto de equilibrio de fusin o de solidificacin T
f
.
Cuando durante el enfriamiento de la fase lquida se alcanza la temperatura de
solidificacin, no se produce la cristalizacin espontnea de la fase slida. Es necesario
que el lquido se subenfre una cantidad AT, llamado subenfriamiento o
sobreenfriamiento, como vemos en la figura 2. A esta temperatura, por debajo de la
de solidificacin, se produce la nucleacin del slido, se cede calor latente de cambio
de estado y sube la temperatura hasta la de solidificacin T
f
. Al terminar la
solidificacin no hay calor latente y la temperatura del slido desciende.
Figura 2. Representacin tpica de temperatura- tiempo para el anlisis trmico de un metal puro
mostrando un subenfriamiento AT antes de la nucleacin de la fase slida.
Reduca (Recursos Educativos)
Serie Qumica de Materiales. 4 (3): 211-284, 2012
ISSN: 1989-5003
214
En la tabla 2 podemos ver algunos datos de los valores mximos de
subenfriamiento que se pueden alcanzar en algunas sustancias puras.
Sustancia AT
max
C
Mercurio
Estao
Bismuto
Ploma
Aluminio
Plata
Oro
Cobre
Manganeso
Nquel
Cobalto
Hierro
Agua
Benceno
77
76
90
80
130
227
230
236
308
319
330
295
39
48
Tabla 2. Subenfriamiento mximo de algunas sustancias lquidas puras.
El subenfriamiento tambin se produce en aleaciones. As por ejemplo en las
aleaciones Cu-Ni, podemos alcanzar valores de subenfriamiento de hasta 300C en el
proceso de nucleacin homognea, como vemos en la figura 3.
Figura 3. Temperaturas de solidificacin de las aleaciones Cu-Ni en funcin de la composicin
Nucleacin homognea
Vamos a establecer cmo se produce la nucleacin homognea de un slido en
el seno de un lquido. Consideremos un volumen de lquido subenfriado AT por debajo
de la temperatura de equilibrio T
E
. La figura 4 A representa el volumen de lquido y que
le corresponde una energa libre G
1
Reduca (Recursos Educativos)
Serie Qumica de Materiales. 4 (3): 211-284, 2012
ISSN: 1989-5003
215
Figura 4. Nucleacin homognea de una partcula slida en el seno de un lquido. A) Fase lquida. B)
Formacin de una esfera de slido en el seno del lquido.
Cuando se forma una pequea esfera slida se produce un cambio de energa
libre como G
2
, figura 4 B. El valor de G
2
ser V
S
+ +
L
V L
S
V
G V G A
SL
SL
donde:
V
S
es el volumen de la esfera slida
V
L
es el volumen de la fase lquida
A
SL
es el rea de la interfase slido/lquido
S
V
G y
L
V
G son las energas libres por unidad de volumen de las fases slida y
lquida y
SL
es la energa libre interfacial slido/lquido
La energa libre del sistema antes de que se forme una partcula de fase slida es
G
1
= V
L
V
G = (V
S
+ V
L
)
L
V
G . Consideramos que el volumen de lquido es la suma del
liquido ms los tomos que van a formar el slido (V
S
+ V
L
). Al formarse el slido, se
pone en juego una energa libre AG cuya variacin ser la diferencia entre el estado 2,
G
2
y el estado 1, G
1
, y que podemos expresar como AG= V
S
S
V
G + V
L
L
V
G + A
SL
SL
- V
S
L
V
G -
V
L
L
V
G . Si agrupamos trminos, AG = V
S
(
S
V
G -
L
V
G ) + A
SL
SL
. Como AG
V
es la diferencia
entre la energa libre de la fase lquida
L
V
G y la de la fase slida
S
V
G , podemos escribir
AG = - V
S
AG
V
+ A
SL
SL
. Ecuacin que nos da la variacin de la energa libre del proceso
de solidificacin.
El exceso de energa libre asociado a la partcula slida puede reducirse si la
partcula adopta la forma de una esfera ya que la forma esfrica supone la forma
geomtrica que tiene el mayor volumen con la menor superficie. En este caso
consideramos que la tensin superficial,
SL
es isotrpica (que tiene el mismo valor en
todos sus puntos). Podemos entonces determinar cul es la variacin de energa libre
por la formacin de una esfera de radio r como AG
r
=
3
4
tr
3
AG
V
+ 4tr
2
SL
.
Reduca (Recursos Educativos)
Serie Qumica de Materiales. 4 (3): 211-284, 2012
ISSN: 1989-5003
216
La formacin de partculas pequeas har aumentar AG lo que supone que se
puede mantener una fase lquida metaestable casi por tiempo indefinido a
temperatura inferior a su temperatura de solidificacin T
f
. Podemos representar esta
ecuacin en la figura 5, donde representamos la variacin de la energa libre frente al
radio. En ella tenemos un trmino que depende del radio al cuadrado y otro trmino
del radio al cubo. La suma de los dos trminos nos da una curva, cuyo mximo
corresponde a un radio que llamamos r*, o radio critico y un valor mximo de AG
asociado a este radio critico que llamamos AG* o barrera energtica para la
nucleacin.
Podemos evaluar que ocurre si el radio de la partcula que se forma es inferior a
r*. En este caso y de acuerdo con la figura 5, el sistema disminuir se energa libre
redisolvindose. A estas partculas que no alcanzan el radio crtico se les denomina
embriones. Por el contrario, si la partcula alcanza un radio mayor que el crtico, el
sistema disminuye su energa libre a medida que aumenta el radio, es decir, cuando
crece el slido, en este caso hablamos de ncleos. Si el radio es igual al crtico se
alcanza el tamao del ncleo crtico. En estas condiciones la variacin de energa libre
es cero, dG = 0, lo que da lugar a un equilibrio inestable.
Figura 5. El cambio de energa libre asociado a la nucleacin de una esfera de radio r.
Para calcular cual es el valor del radio crtico y de la barrera energtica para la
nucleacin, podemos diferenciar con respecto a r e igualar a 0. Tenemos que r*=
V
SL
V
SL
G
2
G 4
8
A
=
A t
t
. Sustituyendo r*
en AG tenemos
( )
2
V
3
SL *
G 3
16
G
A
t
= A . Como AG
V
es
funcin del subenfriamiento, AT, podemos introducir este valor en la ecuacin anterior
si sabemos que
Reduca (Recursos Educativos)
Serie Qumica de Materiales. 4 (3): 211-284, 2012
ISSN: 1989-5003
217
AG
V
=
f
V
T
T L A
Donde L
V
es el calor de solidificacin. Nos quedarn las dos ecuaciones
siguientes, para el radio crtico y la barrera energtica para la nucleacin.
T
1
L
T 2
r
V
f SL *
A
|
|
.
|
\
|
=
( )
2 2
V
2
f
3
SL *
T
1
L 3
T 16
G
A
|
|
.
|
\
|
t
= A
Podemos representar en la figura 6 la variacin del radio con el subenfriamiento.
Tenemos por una parte que el radio crtico r*, disminuye cuando aumenta el
subenfriamiento, teniendo un trazado asinttico tanto para muy bajos
subenfriamientos como para subenfriamientos muy elevados. En el primer caso, hasta
que no se alcanza un valor mnimo de subenfriamiento, no comienza la solidificacin y
es necesario un r* mnimo y en el segundo, cuando el subenfriamiento es muy
elevado, la difusin est muy impedida por lo que el radio crtico ha de ser muy
grande. Por otra parte se representa la variacin del radio mximo. Este radio
representa el tamao de la mayor agrupacin de tomos que pueden convertirse en
ncleo y que se forma para un subenfriamiento dado. El punto de corte de las dos
curvas define el valor del subenfriamiento necesario para la nucleacin AT
N
. Cuando el
subenfriamiento es muy bajo el radio crtico es mucho mayor que el radio mximo, por
lo que no es posible formar un ncleo. Para subenfriamientos iguales o mayores que
AT
N
los embriones crecen y pueden formar ncleos cuyo r* es menor que el radio
mximo.
Figura 6. La variacin de r* y r
max
con el subenfriamiento AT.
En la figura 7 podemos ver la variacin tanto del radio crtico y la barrera
energtica para la nucleacin en funcin del subenfriamiento. Si el subenfriamiento AT
es pequeo, tanto el radio crtico r* como la barrera energtica para la nucleacin AG*
son muy grandes y al contrario. Este hecho supone que a bajos subenfriamientos los
Reduca (Recursos Educativos)
Serie Qumica de Materiales. 4 (3): 211-284, 2012
ISSN: 1989-5003
218
ncleos han de adquirir un tamao elevado y que la barrera energtica es muy
elevada, por lo que la nucleacin est impedida y al revs, con subenfriamientos
grandes los ncleos son pequeos y la barrera energtica AG*pequea, lo que
favorece la nucleacin.
Figura 7. Variacin de r* y AG* en funcin del subenfriamiento AT.
Podemos llamar n
0
al nmero de tomos por mm
3
de lquido, y podemos
establecer el nmero de embriones de radio r, n
r,
que por mm
3
se encuentran
presentes a una temperatura T que ser:
|
.
|
\
|
A
=
kT
G
exp n n
r
0 r
De acuerdo con esta ecuacin, el nmero de embriones que existirn a cada
temperatura ser tanto menor cuanto mayor sea el radio de este.
Nucleacin heterognea
Tenemos que el radio crtico r* depende del tamao del embrin y no del
nmero de tomos del embrin. A partir de la ecuacin de AG* vemos que para que la
nucleacin se produzca a subenfriamientos pequeos, el trmico de la energa
interfacial debe disminuir. Una forma sencilla de conseguirlo es que el ncleo se forme
en contacto con la pared del molde. Podemos considerar que se forma un embrin
slido en contacto con la pared del molde. Si se asume que la tensin superficial
SL
es
isotrpica, para un volumen dado de slido, la energa interfacial del sistema se
minimiza si el embrin tiene la forma de un casquete esfrico con un ngulo de
mojado u que debe cumplir
ML
=
MS
+
SL
cos u, figura 8, donde
ML
, es la tensin
superficial molde/lquido,
MS
, es la tensin superficial entre el molde y el slido y
SL
la
tensin superficial entre el slido y el lquido.
Reduca (Recursos Educativos)
Serie Qumica de Materiales. 4 (3): 211-284, 2012
ISSN: 1989-5003
219
Figura 8. Nucleacin heterognea de un casquete esfrico.
La formacin del embrin tiene asociada un exceso de energa libre
AG
het
= -V
S
V
G A + A
SL
SL
+ A
ML
ML
- A
MS
MS
donde V
S
es el volumen del casquete
esfrico, y A
ML
y A
MS
las reas de las interfases. La energa libre tiene tres
contribuciones de las tensiones superficiales. Las dos primeras son positivas y se deben
a la creacin de las interfases durante la solidificacin. La tercera es debida a la
eliminacin de la interfase Molde/Lquido y tiene por tanto una contribucin negativa.
Si el ngulo u es pequeo significa que el molde sera un buen nucleante. Por el
contrario si u es elevado significa que el molde es un mal nucleante. Se tiene que
producir un equilibrio de fuerzas, en el que se tiene que cumplir que
ML
=
SM
+
SL
cosu, lo que implica que las tensiones superficiales son istropas.
De la misma manera que establecimos para la nucleacin homognea la
variacin de energa libre, se puede demostrar que AG
het
=
( ) u
|
.
|
\
|
t + A t f r 4 G r
3
4
SL
2
V
3
. La barrera energtica para la nucleacin ser
2
V
3
SL *
G 3
4
G
A
t
= A (2 3cosu + cos
3
u). Cuando el ngulo u es cero la barrera energtica
AG* es tambin cero y el subenfriamiento es cero con lo que se produce la nucleacin
espontnea, no sera necesario vencer la barrera para la nucleacin. Si el ngulo u es
180 la barrera energtica AG
*
=
2
V
3
SL
G 3
16
A
t
la nucleacin es homognea. En la figura 9
vemos el valor de la barrera energtica para la nucleacin cuando esta es homognea
y heterognea. En ambos casos el radio crtico r* es el mismo, pero hay una diferencia
muy importante en el valor de la barrera energtica para la nucleacin.
Reduca (Recursos Educativos)
Serie Qumica de Materiales. 4 (3): 211-284, 2012
ISSN: 1989-5003
220
Figura 9. El exceso de energa libre de un embrin slido para la nucleacin homognea y
heterognea. r* es independiente del sitio de nucleacin.
El efecto del subenfriamiento en la barrera energtica para la nucleacin
heterognea
*
het
G A y la homognea
*
hom
G A , muestran un trazado similar y est
condicionada por la adicin de nucleantes ya que estos suponen puntos de nucleacin,
lo que favorecida la nucleacin y en consecuencia se obtiene un tamao de grano fino,
de forma que la efectividad de los nucleantes es funcin del ngulou.
Figura 10. A) Variacin de AG* con el subenfriamiento (AT) para la nucleacin homognea y
heterognea. B) Las correspondientes velocidades de nucleacin (se supone que tienen el mismo valor
de AG*).
Reduca (Recursos Educativos)
Serie Qumica de Materiales. 4 (3): 211-284, 2012
ISSN: 1989-5003
221
Velocidad de nucleacin
Como los ncleos se forman a partir de embriones de radio crtico (ganan un
tomo), parece razonable admitir que la velocidad de nucleacin expresada como
-
N se
defina como el nmero de ncleos que se forman en la unidad de tiempo por unidad
de volumen de lquido en la unidad de tiempo y que esta sea proporcional al nmero
de embriones presentes en la unidad de volumen as como al nmero de tomos que
rodean al embrin o superficie del embrin y que pueden unirse a l. Pero no todos los
tomos que se encuentran en contacto con esa superficie pueden unirse al embrin,
pues han de contener suficiente energa para vencer la barrera energtica ligada a la
superficie. Si esa energa es AG
a
para un tomo, la fraccin de tomos que poseen al
menos esta energa ser exp (-AG
a
/kT). Por ltimo la velocidad de nucleacin debe ser
proporcional a la frecuencia de vibracin de los tomos. Estos factores se expresan por
la ecuacin siguiente
|
.
|
\
|
A
|
.
|
\
|
A
v =
-
kT
* G
exp n
kT
G
exp N
0
a
El trmino v engloba la frecuencia de vibracin de los tomos y el factor
geomtrico de la superficie del embrin. Podemos entonces calcular la velocidad de
nucleacin en funcin de dos exponenciales una de ellas, como ya se ha comentado
corresponde a la fraccin de tomos que tienen la energa de activacin necesaria para
saltar la interfase y la otra corresponde a la barrera energtica para la nucleacin.
Por una parte AG
a
podemos suponer que es independiente de la temperatura,
por lo que al aumentar la temperatura el trmino decrece continuamente. Como
vimos AG* es inversamente proporcional al subenfriamiento al cuadrado AT
2
, por lo
que
kT
* G A
se puede escribir como
2
) T ( kT
A
A
donde A es una constante. A la temperatura
de fusin AT es cero, por lo que el exponente se hace infinito y
-
Nse hace cero, lo que
indica que a la temperatura de fusin la velocidad de nucleacin es nula, figura 10 B.
Cuando la temperatura es muy baja, el subenfriamiento es elevado, y el trmino
2
) T ( kT
A
A
se hace pequeo, pero el proceso estara condicionado por la velocidad a la
que los tomos saltan a travs de la interfase, AG
a
que a bajas temperaturas es muy
elevada y no se puede producir la nucleacin. La competencia entre estos dos factores
hace la mxima velocidad de nucleacin se alcance a temperaturas intermedias.
Reduca (Recursos Educativos)
Serie Qumica de Materiales. 4 (3): 211-284, 2012
ISSN: 1989-5003
222
EL CRECIMIENTO DE SLIDOS EN LQUIDOS
La forma en que los tomos se agregan sobre la interfase de un slido cristalino
creciendo en su fundido es el paso siguiente a la nucleacin y est influenciado por la
estructura atmica de la interfase slido/lquido. La estructura de la interfase depende
del carcter qumico del material en cuestin y tambin del medio trmico en el cual el
material crece. Un anlisis simple de la estructura de la interfase slido/lquido se basa
en que las fases slida y lquida estn en un equilibrio local en su plano de unin y por
tanto la estructura de la interfase ser tal que minimice la energa interfacial.
La variacin de energa en la interfase, AG
S
, que est formada por una cantidad
de tomos N
A
que se depositan al azar sobre N sitios atmicos posibles sobre la
interfase plana en la que slo consideramos una capa interfacial. El anlisis se reduce a
una expresin del tipo: AGs = f (AS
f
; g(N
A
,N); T); donde AS
f
es la entropa de fusin del
material, T es la temperatura absoluta y g(N
A
,N) es un factor de probabilidad que
representa la distribucin de una poblacin de N
A
tomos sobre N sitios interfaciales.
Esta ecuacin puede representarse como AGs/NkT
f
frente a N
A
/N para valores
determinados de AS
f
, como se ve en la figura 11. Tenemos que para valores de la
entropa de fusin inferiores a 2R los valores de AGs/NkT
f
son negativos y por encima
de este valor son positivos. En el caso de que la entropa de fusin tenga valor de 3R se
tienen valores positivos y negativos, como vemos en la figura 11.
La energa libre presenta un mnimo o dos dependiendo de que AS
f
sea menor o
mayor que 2R (siendo R la constante de los gases), o 16,8 J/mol/K. Para materiales en
los que la entropa de fusin AS
f
es menor de 16,8 J/mol/K la interfase de equilibrio es
aquella que tiene el 50% de las posiciones atmicas ocupadas (una interfase
atmicamente rugosa). Para valores de AS
f
mayores de 16,8 J/mol/K la interfase es
cristalogrficamente perfecta con muy pocos tomos aadidos o ausentes de ella (una
interfase atmicamente lisa).
Reduca (Recursos Educativos)
Serie Qumica de Materiales. 4 (3): 211-284, 2012
ISSN: 1989-5003
223
Figura 11. Energa libre relativa de la interfase slido-lquido como una funcin de la cantidad de
tomos que pueden incorporarse a la interfase y la entropa de fusin del material.
Otra descripcin aceptada de las interfases rugosas o lisas son no facetadas y
facetadas. Los metales tpicos tienen valores de AS
f
menores de 16,8 J/mol/K, y dan
lugar a interfases no cristalinas es decir interfases rugosas. Algunos compuestos
orgnicos tienen tambin bajas AS
f
y dan interfases rugosas. En el caso de los
metaloides (Bi, Ga, Sb y As), los semiconductores (Si y Ge) y la mayora de los
compuestos orgnicos tienen valores AS
f
mayores o iguales a 16,8 J/mol/K y presentan
grandes planos cristalogrficos con escalones en contacto con sus fundidos.
Un compuesto orgnico transparente como el canfeno cuya entropa de fusin
AS
f
es 9,7 J/mol/K muestra una pequea depresin en la interfase slido lquido, no
facetada, que corresponde a la posicin del lmite de grano, como vemos en la figura
12 A. La morfologa plana de la interfase corresponde a materiales puros con interfases
rugosas que tienen bajas entropas de fusin, cuando crecen bajo un gradiente de
temperatura positivo. Si el gradiente es negativo la interfase no es plana pero sigue
siendo no facetada.
Reduca (Recursos Educativos)
Serie Qumica de Materiales. 4 (3): 211-284, 2012
ISSN: 1989-5003
224
Figura 12. Modelos de las estructuras de las interfases slido-lquido que se observan durante el
crecimiento de materiales orgnicos transparentes. A) Interfase no facetada del canfeno. B) Interfase
facetada del salol.
Cuando la interfase slido/lquido es facetada como la del salol (AS
f
= 62 J/mol/K)
y la solidificacin se produce bajo un gradiente de temperaturas positivo delante de la
interfase, esta interfase no es plana ni isotrmica; las protuberancias facetadas son
formas de crecimiento estables y sus dimensiones dependen de la magnitud del
gradiente de temperaturas impuesto y de la velocidad de crecimiento.
En la figura 13 podemos ver un esquema de las interfases lisas y rugosas a nivel
microscpico y a nivel atmico. Una interfase facetada es dentada y con caras a escala
microscpica, como se ve en el dibujo de la parte superior de la figura 13 A, pero lisa a
escala atmica, dibujo inferior. Una interfase no facetada aparece microscpicamente
lisa, dibujo superior de la figura 13 B, pero est dentada a nivel atmico, dibujo
inferior.
Figura 13. A) Formas de interfases facetadas. Una interfase facetada es dentada y con caras a escala
microscpica, dibujo superior, pero lisa a escala atmica, dibujo inferior. B) Interfase no facetada. Una
interfase no facetada aparece microscpicamente lisa, dibujo superior, pero est dentada a nivel
atmico, dibujo inferior.
Reduca (Recursos Educativos)
Serie Qumica de Materiales. 4 (3): 211-284, 2012
ISSN: 1989-5003
225
Hemos de hacer notar que este anlisis terico simple del problema de la
interfase se basa en una estructura de equilibrio estacionario, mientras que las
observaciones dan como hecho el movimiento de las interfases. Esto hace que no
siempre sea correcto utilizar el criterio de la entropa de fusin para predecir la
estructura de la interfase por varias razones. Consideramos solo una capa interfacial.
En la interfase rugosa, un 50% de sitios atmicos estn ocupados, la capa interfacial
puede contener embriones lisos lo que equivaldra a pequeas facetas que
evolucionarn hacia rugosas. Una monocapa de interfase rugosa envolver a una
mltiple capa de interfase lisa.
Podemos entonces utilizar otros criterios para establecer las caractersticas de
las interfases. Uno de ellos sera mediante experimentos en los que las formas de
equilibrio dan una idea inmediata de la magnitud relativa de la energa interfacial que
es funcin de la orientacin y la presencia o ausencia de caras en la forma de
equilibrio. Esto nos mostrara las interfases de equilibrio que serian lisas o rugosas.
Puede ocurrir que sistemas que tienen formas de equilibrio no facetadas pueden
mostrar una interfase de equilibrio facetada y viceversa. Otro aspecto es, que solo
consideramos que puede haber una sola estructura de la interfase, modificndose
ligeramente, para un material dado. La estructura interfacial y el mecanismo de
crecimiento pueden alterarse con las condiciones de enfriamiento. Por ejemplo, el
fosforo blanco crece con una interfase facetada solido/lquido a bajas velocidades de
crecimiento, pero se hace no facetada al aumentar esta.
En la figura 14 se muestran dos ejemplos de interfases slido/lquido en sistemas
metlicos. En la primera de ellas 6.14 A, vemos la fase o primaria de una aleacin
hipoeutctica Cu-4,5%P en forma de dendritas no facetadas. En la figura 14 B tenemos
unos cristales facetados de la fase primaria de la aleacin Sn-10 %Sb.
Figura 14. Ejemplos de interfases slido-lquido en sistemas metlicos. A) Dendritas no facetadas de la
fase o en una matriz eutctica Cu-Cu
3
P. B) Cuboides facetados del compuesto |SnSb en una matriz
rica en Sn.
Reduca (Recursos Educativos)
Serie Qumica de Materiales. 4 (3): 211-284, 2012
ISSN: 1989-5003
226
Formas de crecimiento de los metales
La temperatura de la interfase de equilibrio estacionario es por definicin T
f
, es
decir la temperatura de fusin. A esta temperatura puede haber una migracin
constante de tomos dentro de la capa de la interfase y un cambio de tomos entre la
fase slida y lquida y no hay un crecimiento neto del cristal o disolucin. Para que el
crecimiento del cristal tenga lugar, la temperatura de la interfase debe ser menor que
T
f
. En esas condiciones un nmero mayor de tomos se agregarn a la interfase desde
el lquido a la vez que un nmero menor de tomos abandonaran la interfase desde el
slido. La fuerza motriz que provoca la solidificacin es el subenfriamiento AT.
Habamos visto que
i
f
T
T
L
G A = A , donde L es el calor latente de solidificacin y AT
i
subenfriamiento de la interfase. En estas condiciones la velocidad de solidificacin es
v
solidificacin
= k
1
AT
i
. Donde k
1
es una constante que depende de la movilidad de la
interfase.
La solidificacin de metales es un proceso controlado por la difusin. Difusin del
calor en metales puros y de soluto en aleaciones.
Figura 15. Representacin esquemtica de las condiciones trmicas de la interfase S/L bajo
condiciones de A) gradiente positivo de temperatura en el lquido. B) gradiente negativo de
temperatura en el lquido.
La velocidad de crecimiento es una funcin de la temperatura de la interfase y la
forma de crecimiento es funcin de las condiciones trmicas delante de la interfase.
Vamos a considerar los dos casos posibles: 1.- Gradiente de temperatura positivo y 2.-
Gradiente de temperatura negativo, figuras 6.15 A y B.
Gradiente de temperatura positivo
Para que se produzca un gradiente de temperaturas positivo, el calor latente de
solidificacin que se genera en la interfase deber eliminarse a travs del slido
Reduca (Recursos Educativos)
Serie Qumica de Materiales. 4 (3): 211-284, 2012
ISSN: 1989-5003
227
descendiendo el gradiente de temperaturas, figura 16 A. El movimiento de la interfase
va a ser funcin de la velocidad con que se elimina calor a travs del slido.
Figura 16. Gradiente de temperatura positivo. A) Distribucin de temperatura para la solidificacin. B)
Para una interfase plana S/L. C) Para una protuberancia. La parte derecha representa lo mismo para
un gradiente de temperatura negativo.
Si no se elimina el calor, la temperatura de la interfase aumentar y se detendra
el crecimiento. La interfase ser isoterma, a T
f
, y se mover con movimiento uniforme.
Si se crea una protuberancia entrar en un lquido ms caliente figura 16 B y su
velocidad de crecimiento se detendr, es decir la protuberancia se disolver, dando
Reduca (Recursos Educativos)
Serie Qumica de Materiales. 4 (3): 211-284, 2012
ISSN: 1989-5003
228
lugar a que la interfase se nivele y ser una interfase plana sin protuberancias, figura
16 C, siendo la interfase isotrmica y subenfriada AT. Por ltimo la interfase ser
atmicamente rugosa y no cristalogrfica.
Gradiente de temperatura negativo
En este caso el calor latente se conduce a travs de las dos fases slida y lquida,
figura 16 D. El movimiento de la interfase no est controlado por la eliminacin de
calor a travs del slido por lo que una protuberancia que entre en el lquido puede
avanzar ms al entrar en un lquido ms frio, figura 16 E. La interfase plana se hace
inestable y se forman brazos que avanzan hacia el lquido con una velocidad de
crecimiento tal que alcanza un estado estacionario cuando el calor generado en la
interfase es igual al calor cedido, figura 16 F.
Las protuberancias presentan formas parablicas rugosas a las cuales les salen
brazos de segundo o tercer orden formando el llamado crecimiento dendrtico. En la
figura 17 A y B podemos ver dos ejemplos de crecimiento dendrtico.
Figura 17. A) Esquema mostrando el crecimiento de las dendritas. B) Dendritas en plomo.
La direccin cristalogrfica del crecimiento dendrtico es funcin de la estructura
cristalina. Cada tipo de estructura favorece el crecimiento en unas determinadas
direcciones como se ve en la tabla 3.
Tabla 3. Direcciones de crecimiento dendrtico en varias estructuras cristalinas.
Estructura cristalina Direccin de crecimiento dendrtico
ccc
cc
hcp
tc
<100>
<100>
<10 1 0>
<110>
Reduca (Recursos Educativos)
Serie Qumica de Materiales. 4 (3): 211-284, 2012
ISSN: 1989-5003
229
Los metales lquidos subenfran solo unos pocos grados ya que el
subenfriamiento requerido en la interfase es solo de una fraccin de grado. Esto hace
que los metales normalmente solidifiquen como dendritas. La primera fraccin de
material solidifica a la temperatura del lquido subenfriado. El calor latente hace
aumentar la temperatura hasta justo por debajo de la temperatura de fusin y el flujo
de calor desde el slido al lquido provoca un gradiente negativo en la interfase S/L por
lo que la solidificacin tiene morfologa dendrtica.
Los cristales crecen bajo condiciones planares o dendrticas. Con vacantes,
dislocaciones y formacin de lmites de grano entre dos cristales de diferente
orientacin. Los defectos no participan en la solidificacin. Se pueden evitar
controlando las condiciones de solidificacin como en el caso de los monocristales.
Las fases primarias que se forman en los sistemas de aleacin pueden ser,
bsicamente, de dos tipos. O en se forma una solucin slida o un compuesto
intermetlico. El que se forme uno u otro es funcin de las caractersticas de los
tomos, como se vio en un captulo anterior. Desde el punto de vista de la forma que
adopta la fase slida primaria en la solidificacin de una aleacin, no se puede
predecir, como se ha comentado anteriormente.
Figura 18. Crecimiento de cristales en aleaciones. A) Dendritas primarias de fase o en la aleacin Cu-
4,5%P x 100. B) Dendritas primarias con caras de la fase Ag
3
Sn en una matriz eutctica en la aleacin
Ag-55%Sn x430. C) Cristales alargados en crecimiento primarios de la fase Ag
3
Sn en una matriz
eutctica en la aleacin Ag-90%Sn x 270. D) Cristales idiomrficos de la fase Ag
3
Sn en una matriz
eutctica en la aleacin Ag-90%Sn recocida x 400.
Reduca (Recursos Educativos)
Serie Qumica de Materiales. 4 (3): 211-284, 2012
ISSN: 1989-5003
230
En la figura 18 se muestran algunos ejemplos que ilustran este hecho. En la
micrografa 6.18 A vemos como la fase o primaria en las aleaciones hipoeutctica Cu-P,
forma dendritas. En el caso de las aleaciones Ag-Sn, cuando la composicin es
hipoeutctica con gran cantidad de fase primaria Ag
3
Sn, el sistema forma una
estructura casi dendrtica, donde las dendritas muestran caras cristalinas, figura 18
B. En la misma aleacin si la cantidad de fase primaria es pequea, esta crece en forma
de grandes cristales alargados donde est favorecida una de las direcciones de
crecimiento, figura 18 C. Estos cristales de la fase Ag
3
Sn, cuando se recuecen alcanzan
forma idiomrfica, como se observa en la figura 18 D.
Flujo de calor y estabilidad de la interfase
En los metales la solidificacin est controlada por la velocidad con que el calor
latente se extrae en la interfase S/L. Si la v es la velocidad de crecimiento de una
interfase plana en un lquido sobrecalentado, el flujo de calor desde la interfase hacia
el slido se igualar al calor del lquido ms el calor latente que se genera en la
interfase de acuerdo con la ecuacin K
S
T
S
= K
L
T
L
+ v L
v
, donde K es la conductividad
trmica, T gradiente de temperatura (dT/dx) y L
v
calor latente de fusin por unidad de
volumen.
Cuando el slido crece en un lquido sobrecalentado la interfase S/L plana es
estable, como se vio en la figura 16 A. Como consecuencia de un aumento local de la
velocidad de crecimiento se forma una protuberancia y si el radio de curvatura es
mayor que el efecto Gibbs-Thomson este puede ignorarse y la interfase permanece
isoterma y a la temperatura de fusin T
f.
Si el slido crece en un lquido subenfriado, como se indica en la figura 16 D la
punta de la protuberancia se encuentra en un gradiente ms negativo permitiendo un
crecimiento preferente. La interfase es inestable por lo que a partir de un ncleo
esfrico inicial, figura 19 A, se desarrollan brazos en muchas direcciones, figura 19 B. Al
alargarse los brazos, sus superficies, figura 19 C de nuevo se vuelven inestables y se
rompen en brazos secundarios y a menudo terciarios, figura 19 D. Esta forma de
crecimiento se denomina dendrtico.
Vamos a ver cmo se desarrolla el crecimiento. Si aceptamos que el slido es
isotermo (su gradiente T
S
es 0) la velocidad de crecimiento de la punta de la dendrita v
tendr una ecuacin similar a la anterior en la que el gradiente de temperatura del
lquido T
L
se mide en la direccin de la velocidad v.
La solucin para una punta semiesfrica de la ecuacin del flujo de calor muestra
que el gradiente de temperatura en el liquido (negativo) T
L
~ AT
c
/r donde AT
c
es la
diferencia entre temperatura de la interfase (T
i
) menos la temperatura del lquido
suficientemente alejado de la interfase T
Reduca (Recursos Educativos)
Serie Qumica de Materiales. 4 (3): 211-284, 2012
ISSN: 1989-5003
231
r
T
L
K
L
' T K
v
V
L
v
L L
A
~
=
Para un AT dado el crecimiento rpido se consigue para valores pequeos de r al
ser ms efectiva la conduccin de calor cuando r disminuye.
Figura 19. Representacin esquemtica del desarrollo de una forma dendrtica a partir de un ncleo
inicial.
Figura 20. Distribucin de temperatura en la punta de una dendrita trmica creciendo.
Reduca (Recursos Educativos)
Serie Qumica de Materiales. 4 (3): 211-284, 2012
ISSN: 1989-5003
232
El subenfriamiento AT no es independiente del radio de la punta de la dendrita r,
figura 20. Por el efecto Gibbs-Thomson en el equilibrio se produce la curvatura de la
interfase a un subenfriamiento AT por debajo de T
f
dado por
r L
T 2
T
v
f
r
= A . El radio
mnimo de curvatura posible de la punta ser aquel que cumpla que el
subenfriamiento debido al radio de curvatura AT
r
se iguale al subenfriamiento total
AT
o
. Este subenfriamiento total es la diferencia entre la temperatura de fusin T
f
y la
temperatura del lquido suficientemente alejado T
.
Este ser el radio del ncleo crtico r* dado por
|
|
.
|
\
|
A
0 v
f
T L
T 2
. El subenfriamiento
debido a la curvatura de la interfase, AT
r
estar dado por AT
o
r*/r y como AT
o
es la
suma de los dos subenfriamientos, el debido a la curvatura de la interfase AT
r
ms el
debido a la diferencia de temperaturas AT
c
, la ecuacin queda
|
.
|
\
|
=
r
* r
1
r
1
L
K
v
v
L
La velocidad de crecimiento de la punta tiende a cero cuando el radio tiende a r*,
por el efecto Gibbs-Thomson y tambin cuando el radio tiende a infinito debido a la
baja conduccin de calor. La mxima velocidad se obtiene cuando el radio r es dos
veces el r*.
Crecimiento a partir de soluciones metlicas diluidas
En algunos sistemas, cuando la concentracin de soluto es baja, la cantidad de la
fase primaria suele ser pequea se pueden producir distintas formas de crecimiento
que cuando la aleacin tiene mayor concentracin de soluto. Es el caso de la aleacin
Al-Sn, donde cambia la forma de las dendritas con elevadas concentraciones de soluto,
figura 21 A y B, a dendritas limitadas por planos cristalogrficos facetados, mostrando
dendritas facetadas en forma de flecha con planos {111} en el extremo de la dendrita,
figuras 21 C y D.
Reduca (Recursos Educativos)
Serie Qumica de Materiales. 4 (3): 211-284, 2012
ISSN: 1989-5003
233
Figura 21. Cambio en la morfologa de los cristales primarios de Al en una aleacin Al-Sn con
cantidades decrecientes de fase primaria. A) 85% at. Al. B) 65% at. Al. C) 33% at. Al. D) 10% at. Al.
(adaptado de Chadwick, G.A., 1972).
Formas de crecimiento de los no metales
Llamamos no metales a aquellas fases que solidifican con caras cristalinas o
interfases facetadas como el Ge, Sb, CuAl
2
, Cu
2
Sb.... Estas interfases S/L son
perfectamente cristalogrficas con muy pocos tomos en exceso o defecto, es decir
reproducen las caras del cristal.
En el proceso de solidificacin a la temperatura de fusin, T
f
los tomos de la
interfase apenas se mueven dando lugar a que la interfase sea estable y esttica. El
subenfriamiento AT proporciona la fuerza motriz para el crecimiento del cristal que
progresa por movimiento lateral de escalones atmicos a travs de la interfase, como
se observa en la figura 22
En los metales la interfase se propaga perpendicular a si misma por adicin de
tomos a cualquier punto de la superficie. En el caso de los no metales las diferencias
ms importantes son que el crecimiento se produce por migracin lateral de escalones
de crecimiento en puntos especficos del cristal. Para que el crecimiento sea efectivo
Reduca (Recursos Educativos)
Serie Qumica de Materiales. 4 (3): 211-284, 2012
ISSN: 1989-5003
234
deber haber bordes sobre la superficie del cristal que cuando se llenan se detiene el
crecimiento.
Las formas posibles de aumentar el nmero de escalones son en primer lugar por
nucleacin repetida de embriones de tomos sobre la superficie cristalina, figura 22 A
y en segundo por emergencia de dislocaciones helicoidales, figura 22 B. La dislocacin
forma un escaln permanente que se enrosca sobre si mismo alrededor de la
dislocacin creando una espiral en rampa, que hace que mantenga el escaln y por lo
tanto el crecimiento.
Figura 22. Representacin esquemtica de la nucleacin y crecimiento de nuevos embriones sobre
interfases S/L facetadas. A) Nucleacin de embriones sobre una interfase perfecta. B) Crecimiento en
espiral como un sitio de crecimiento continuo provocado por una dislocacin helicoidal emergente.
Otra posibilidad de crecimiento es la nucleacin de embriones sobre los lmites
de macla a ambos lados del cristal maclado como se representa en la figura 23 A. La
micrografa muestra un cristal en forma de H que ha crecido por el mecanismo de
nucleacin en las maclas, como se ve en la figura 23 B.
La forma de crecimiento tambin depende de las condiciones trmicas en el
fundido. As si el gradiente de temperatura en el lquido es positivo, la interfase no
puede avanzar sin que se produzca la disipacin del calor latente a travs del slido,
pero su forma la determina la orientacin cristalogrfica de la interfase. Si tiene planos
de ndices bajos ser lisa excepto el movimiento lateral de los escalones de
crecimiento.
En un gradiente de temperatura negativo, las interfases planas o serradas son
inestables ya que est favorecido el crecimiento dendrtico caracterstico de los
metales. Existen gran variedad de formas de crecimiento de los no metales. En la figura
24 se muestran algunas formas como la forma de embudo del bismuto, figura 24 A o
largos prismas hexagonales de teluro, figura 24 B. Estas estructuras de los no metales
pueden asociarse a las dendritas de los metales. El crecimiento de los no metales se
produce en superficies singulares pero su disolucin no tiene porque respetar los
planos cristalinos. As en aleaciones bifsicas, la fase primaria de una sustancia
facetada puede no presentar esta forma al haberse disuelto ligeramente despus del
crecimiento de otra fase o fases a partir de ella.
Reduca (Recursos Educativos)
Serie Qumica de Materiales. 4 (3): 211-284, 2012
ISSN: 1989-5003
235
Figura 23. A) La interseccin de un plano de macla con la interfase S/L produce un ngulo entrante en
el que puede darse el crecimiento. B) Morfologa tpica de H en seccin transversal de cristales
creciendo ayudado por el mecanismo de maclas.
Figura 24. Ejemplos de cristales facetados creciendo en lquidos subenfriados. A) Formas de embudo
de Bi. B) Largos prismas hexagonales de Te.
ENFRIAMIENTO DE METALES PUROS Y NO METALES
Un metal puro tiene una nica composicin y no se produce segregacin de
soluto y la solidificacin se produce en condiciones de equilibrio. Durante la
solidificacin se obtiene una morfologa dendrtica de grano ms o menos fino que es
funcin de la velocidad de enfriamiento. Una vez terminada la solidificacin el metal
presenta una estructura monofsica de granos cuya morfologa depende de las
Reduca (Recursos Educativos)
Serie Qumica de Materiales. 4 (3): 211-284, 2012
ISSN: 1989-5003
236
condiciones de enfriamiento, obtenindose estructura columnar o ms o menos
equiaxial, figura 25 A y B.
Figura 25. A) Granos columnares de cinc puro. B) Granos equiaxiales de un cobre impurificado .
Enfriamiento de una aleacin monofsica
Consideramos una aleacin monofsica como la de la figura 26 de composicin
X
0
en la que el coeficiente de reparto k es el cociente
L
S
X
X
. En este caso el coeficiente
de reparto de equilibrio es menor que la unidad. La figura 27 A y B muestran el trazado
de las curvas de solidus y liquidus donde el cociente entre la composicin de la fase
slida y liquida o coeficiente de reparto en equilibrio a cada temperatura es mayor o
menor que la unidad.
Suponemos que no hay barrera para la nucleacin de la fase slida, por lo que se
formar un ncleo heterogneo sin subenfriamiento en el fundido. La solidificacin de
equilibrio se produce a largos periodos de tiempo y supone que los gradientes de
concentracin se igualan en cada momento. Las condiciones reales de solidificacin
son ms rpidas que las de equilibrio y el tiempo es insuficiente para que se alcance el
equilibrio. La forma en que solidifican estas aleaciones es funcin de tres variables: el
gradiente de temperatura, las velocidades de enfriamiento y las velocidades de
crecimiento.
Reduca (Recursos Educativos)
Serie Qumica de Materiales. 4 (3): 211-284, 2012
ISSN: 1989-5003
237
Figura 26. Un diagrama de fases hipottico k = X
S
/X
L
es constante.
Figura 27. Esquema de diagramas que representa los coeficientes de reparto menor y mayor de la
unidad.
Reduca (Recursos Educativos)
Serie Qumica de Materiales. 4 (3): 211-284, 2012
ISSN: 1989-5003
238
Para simplificar vamos a considerar que el movimiento de la interfase es planar a
lo largo de una barra que nos permite considerar que la solidificacin es unidireccional
(como se produce en el proceso de fusin por zonas).
Veremos tres casos lmites:
1. Solidificacin de equilibrio
2. Solidificacin sin difusin en el slido pero mezcla perfecta en el lquido
3. Solidificacin sin difusin en el slido y solo mezcla por difusin en el lquido
Enfriamiento de equilibrio
Consideramos de nuevo la aleacin de composicin X
0
de la figura 26. A la
temperatura T
1
comienza a solidificar. Si k es el coeficiente de reparto y que es igual a
0
SOL
LIQ
SOL
X
X
X
X
= y por tanto la composicin del slido en equilibrio tendr una composicin
como X
SOL
= k X
0
Segn desciende la temperatura se va formando ms slido, cumplindose que
las fases S y L son en todo momento homogneas y sus composiciones siguen las lneas
de solidus y liquidus. Mediante la regla de la palanca podemos calcular en cada
momento las cantidades relativas de slido y lquido. Si representamos otro momento
de la solidificacin como es la temperatura T
2
en la figura 26, tendremos que la
composicin de slido ser X
s
y la del lquido
X
L
. En la figura 28 representamos la
solidificacin unidireccional de la aleacin X
0
.
Tenemos la barra en la que vemos que a una determinada distancia x, est la
interfase S/L planar y que el flujo de calor es axial, figura 28 A. En la figura 28 B se
muestra el perfil de composicin correspondiente a la temperatura T
2
asumiendo que
existe equilibrio. La conservacin de soluto requiere que las reas rayadas sean
iguales.
Cuando finaliza la solidificacin y se alcanza la temperatura T
3
la ltima gota de
lquido solidifica con la composicin del lquido
k
X
X
0
LIQ
= . Durante la solidificacin la
fase slida va aumentando su composicin en soluto al igual que lo hace la fase
lquida. La razn para que las dos fases aumenten su composicin es que las
cantidades relativas de una y otra se van modificando durante el proceso comenzando
en 100% de fase lquida y 0% de fase slida a las cantidades relativas de 0% de fase
lquida y 100% de fase slida al final de la solidificacin, de la misma composicin del
liquido inicial.
Reduca (Recursos Educativos)
Serie Qumica de Materiales. 4 (3): 211-284, 2012
ISSN: 1989-5003
239
Figura 28. Solidificacin unidireccional de la aleacin X
0
. A) Interfase S/L planar y flujo de calor axial.
B) Perfil de composicin correspondiente a T
2
asumiendo que existe equilibrio. La conservacin de
soluto requiere que las reas rayadas sean iguales.
No difusin en el slido y perfecta mezcla en el lquido
Muy frecuentemente la velocidad de enfriamiento es demasiado rpida para que
pueda producirse difusin apreciable en la fase slida. En esas condiciones el lquido
mantiene una composicin homognea mediante la agitacin.
Supongamos de nuevo la solidificacin unidireccional. La primera porcin de
slido que se forma a la temperatura T
1
tiene una composicin X
S
que es igual a X
0
k.
Al ser el primer slido ms puro que la composicin inicial de lquido X
0
, figura 29 A, en
la interfase slido/lquido se rechaza soluto hacia el lquido cuya composicin se hace
mayor que X
0
.
La temperatura de la interfase debe disminuir por debajo de T
1
para que
progrese la solidificacin. La siguiente capa de slido ser ms rica en soluto y as
continuar el proceso. Se establece un equilibrio local en la interfase cuyas
composiciones sern X
S
y X
L
que corresponden a las que define el diagrama de
equilibrio a cada temperatura, figura 29 B. Como no se produce la difusin en el slido
las capas separadas mantienen su composicin. Esto hace que la composicin media
S
X de la fase slida sea menor que la que le correspondera de acuerdo con el
diagrama de equilibrio como se muestra en la figura 29 A.
A medida que transcurre la solidificacin, la concentracin del slido formado
sigue una lnea como la mostrada en la figura 29 C, manteniendo en la interfase las
concentraciones X
S
y X
L
. La concentracin del lquido permanece constante e igual a X
L
.
Reduca (Recursos Educativos)
Serie Qumica de Materiales. 4 (3): 211-284, 2012
ISSN: 1989-5003
240
Figura 29 Frente de solidificacin planar de la aleacin X
0
. Sin difusin en el slido pero si en el lquido.
A) Sobre el diagrama de equilibrio se traza la composicin media de la aleacin X . B) Perfil de
composicin justo por debajo de T
1
. C) Perfil de composicin a T
3
. D) perfil de composicin a la T
E
y por
debajo
Las cantidades relativas de ambas fases se calculan por la regla de la palanca
considerando
S
X y X
L
. En este caso el lquido, a la ltima temperatura de solidificacin
de equilibrio, es ms rico que X
0
/k por lo que ese lquido, en pequeas cantidades,
puede alcanzar la composicin eutctica. Bajo estas condiciones, el ltimo lquido
Reduca (Recursos Educativos)
Serie Qumica de Materiales. 4 (3): 211-284, 2012
ISSN: 1989-5003
241
solidifica a la temperatura eutctica T
E
cuando la composicin media del slido
S
X
corresponde a la de la aleacin X
0
. Tendremos entonces, que cuando el coeficiente de
reparto es menor que la unidad, la ltima porcin de lquido que solidifica ser
siempre eutctico, figura 29 D.
En la figura 30 se muestra la microestructura de una aleacin Ag 40% en masa
de Hg. El enfriamiento fue lo suficientemente lento para evitar la formacin de otras
fases. Se aprecia la microsegregacin dendrtica en una estructura de granos
equiaxiales, donde adems se observa porosidad. Otra estructura tpica segregada
se ve en la figura 18 A, las dendritas de fase o muestran la microsegregacin o
coring donde la concentracin de soluto en el centro de la dendrita es inferior a la
del exterior.
Las variaciones de composicin del centro de los granos y sus lmites dependen
de la velocidad de solidificacin, de la amplitud de la separacin de las lneas de
liquidus y solidus y de la composicin inicial de la aleacin. (no hay segregacin en
metales puros ni aleaciones que funden congruentemente).
La separacin entre las lneas de solidus y liquidus se puede medir por el cociente
X
s
/X
L
o coeficiente de reparto. Si el coeficiente de reparto k es menor que la unidad el
soluto es rechazado por el slido y las regiones interdendrticas se enriquecen en
soluto. Si k es mayor que la unidad las regiones interdendrticas son ricas en
disolvente.
Figura 30. Segregacin dendrtica en aleaciones mostrando la segregacin interdendrtica, porosidad y
limites de grano.
Reduca (Recursos Educativos)
Serie Qumica de Materiales. 4 (3): 211-284, 2012
ISSN: 1989-5003
242
Solidificacin sin difusin en el slido y mezcla por difusin en el lquido (no
agitacin)
El soluto rechazado desde el slido se transporta slo por difusin en el lquido lo
que provoca que aumente la concentracin de soluto delante de la intercara
generndose una capa de difusin.
Si la solidificacin se realizara a velocidad constante, v, se puede demostrar que
se alcanza un estado estacionario cuando la interfase alcance la ltima temperatura de
solidificacin T
3
. El lquido adyacente al slido tendr una composicin X
0
/k y el slido
se estara formando con una composicin como X
0
, figura 31 A
En estado estacionario el perfil de composicin en el lquido deber ser tal que la
velocidad a que difunde el soluto descendiendo el gradiente de concentracin,
alejndose de la interfase, est equilibrada con la velocidad a que el soluto es
rechazado en el lquido que solidifica.
) X X ( v
dx
dX
D
S L
L
=
Donde D es la difusividad en el lquido, dX
L
/dx es el gradiente de concentracin
en la interfase y X
L
y X
S
las concentraciones de soluto en el lquido y en el slido en
equilibrio en la interfase. Ecuacin anloga a la conduccin de calor en la interfase
para la solidificacin de metales puros. En el caso de aleaciones la velocidad de
solidificacin est controlada por la dispersin del exceso de soluto (X
L
y X
S
) en lugar de
por el calor latente (L
v
).
En el caso de la aleacin habr que disipar por conduccin, el calor latente de
solidificacin pero es un problema menor comparado con la difusin de soluto, puesto
que la conduccin de calor es aproximadamente 10
4
veces ms rpida.
El perfil de la concentracin en el lquido para la solidificacin en un sistema en
estado estacionario viene dado por la ecuacin
)
`
=
) v / D (
x
exp
k
k 1
1 X X
0 L
que significa que X
L
decrece exponencialmente desde X
0
/k a x igual a 0
(interfase), hasta X
0
a gran distancia de la interfase. El perfil de concentracin tiene
una anchura dada por D/v, figura 31 B.
Cuando la interfase S/L est a una distancia aproximadamente igual a D/v del
extremo de la barra, la onda de soluto se reduce a un volumen muy pequeo y la
Reduca (Recursos Educativos)
Serie Qumica de Materiales. 4 (3): 211-284, 2012
ISSN: 1989-5003
243
concentracin aumenta rpidamente para llegar a un trnsito final con la formacin
del eutctico. figura 31 C.
En la prctica la solidificacin de aleaciones presentarn evidencia de los tres
casos citados. Siempre habr algo de agitacin (turbulencia al derramar o llenar,
corrientes de conveccin, efectos de gravedad), pero generalmente, no ser
suficientemente efectiva para evitar la formacin de una capa lmite y habr
fenmenos de difusin; la agitacin parcial reducir la amplitud de la capa lmite. Los
perfiles de concentracin que se encuentran en la prctica pueden presentar detalles
para situaciones comprendidas entre las representadas.
Debe tenerse en cuenta, la difusin en el slido, por ejemplo cuando se trate de
tomos intersticiales en red cbica centrada. En este caso el soluto puede difundir
desde la interfase que solidifica hacia el slido o hacia el lquido, resultando de ello que
despus de la solidificacin la aleacin es ms homognea. Incluso cuando no se trate
de una solidificacin monodireccional se pueden aplicar estas ideas para interpretar
estructuras microscpicas.
La solidificacin, monodireccional tiene importancia industrial en la produccin
de materiales resistentes al creep (estructuras con fases alineadas para turbinas de
gas), fabricacin de metales extra puros (afino por fusin por zonas).
Figura 31. Frente de solidificacin planar de la aleacin X
0
. Sin difusin en el slido y sin agitacin en el
lquido. A) Perfil de composicin cuando la interfase S/L est entre T
2
y T
3
. B) Solidificacin en estado
estacionario a T
3
. La composicin en la interfase es igual a la composicin del lquido delante del
slido X
0
C) Perfil de composicin a T
E
y por debajo.
Reduca (Recursos Educativos)
Serie Qumica de Materiales. 4 (3): 211-284, 2012
ISSN: 1989-5003
244
Solidificacin celular y dendrtica
Consideremos un frente de solidificacin plano. La difusin de soluto hacia el
interior del lquido durante la solidificacin de una aleacin es un fenmeno anlogo a
la conduccin de calor latente por el lquido durante la solidificacin de un metal puro.
Al variar la concentracin de soluto delante del frente de solidificacin se vara la
temperatura de solidificacin de equilibrio.
Figura 32. El origen del subenfriamiento constitucional delante de un frente plano de solidificacin A)
Perfil de composicin a travs de la interfase S/L durante la solidificacin en estado estacionario. La
lnea azul muestra el gradiente de concentracin dX
L
/dx en la interfase S/L. B) La temperatura del
lquido delante del frente de solidificacin sigue la lnea T
L
. La temperatura de equilibrio del lquido
adyacente a la interfase varia como T
e
. El subenfriamiento constitucional se alcanza cuando T
L
cae por
debajo del gradiente crtico.
Reduca (Recursos Educativos)
Serie Qumica de Materiales. 4 (3): 211-284, 2012
ISSN: 1989-5003
245
La temperatura real del lquido aumenta desde la intercara S/L hacia el interior
del lquido por la lnea de liquidus T
L,
figura 32 A Debido a la no existencia de agitacin
en el lquido, existen gradientes de concentracin en el lquido delante de la interfase.
Este hecho provoca que un frente de solidificacin plano sea muy difcil de formarse
para aleaciones con un gran intervalo de solidificacin y altas velocidades de
solidificacin.
Como consecuencia de la variacin de la concentracin de soluto en el frente de
solidificacin, habr una correspondiente variacin de la temperatura de solidificacin
de equilibrio, es decir de la temperatura representada por la lnea T
e
que se pude
obtener si trasladamos la concentracin del lquido en cada punto al diagrama de
equilibrio, y para esa composicin vemos cual es su temperatura de solidificacin. En la
intercara, la temperatura del lquido, T
L
es la temperatura de equilibrio, T
3,
figura 32 B.
Podemos definir el gradiente crtico como el que se produce bajo condiciones de
crecimiento en estado estacionario y que est dado por (T
1
T
3
)/(D/v) donde T
1
y T
3
son las temperaturas de liquidus y solidus.
La condicin para que se tenga una interfase planar es
) v / D (
) T T (
' T
3 1
L
> . Por tanto si
el gradiente de temperatura es menor que el valor del gradiente crtico, el lquido
estar subenfriado. Este subenfriamiento se debe a la diferente composicin del
liquido delante de la interfase, por lo que recibe el nombre de subenfriamiento
constitucional.
La condicin necesaria para que se formen protuberancias estables en una
intercara plana es que exista una regin de subenfriamiento, por lo que el
subenfriamiento constitucional en el lquido provoca la rotura de la interfase plana.
Si el gradiente de temperatura en el lquido frente a una interfase inicialmente
plana se reduce gradualmente hasta situarse por debajo del valor crtico el primer paso
en la rotura de la interfase es la formacin de una estructura celular, figura 33.
La formacin de la primera protuberancia determina un rechazo lateral de soluto
que se acumula en la base de la protuberancia figura 33 B, lo cual hace disminuir la
temperatura de solidificacin de equilibrio, produciendo un rechazo en el frente
slido, figura 33 C, que, a su vez, provoca la formacin de otras protuberancias figura
33 D, a partir de ellas, las protuberancias se desarrollan formando largos brazos o
celdas que crecen paralelas a la direccin del flujo calorfico (E).
Reduca (Recursos Educativos)
Serie Qumica de Materiales. 4 (3): 211-284, 2012
ISSN: 1989-5003
246
Figura 33. La rotura de un frente de solidificacin inicialmente plano. A) Frente plano. B) Formacin de
una protuberancia. C) El rechazo de soluto en los lados provoca la disolucin de los lados de la
protuberancia. D) El proceso continua. E) Formacin de celdas.
El soluto rechazado o segregado en el lquido se concentra en las paredes de las
celdas que solidificarn a las temperaturas ms bajas. Los extremos de las celdas
crecen penetrando en el lquido ms caliente y por tanto solidifican conteniendo
menos soluto, incluso cuando X
0
es mucho menor que la concentracin mxima X
mx
El
lquido intercelular puede alcanzar la composicin eutctica en cuyo caso las "paredes"
de las celdillas contendrn una segunda fase. En la figura 34 A podemos ver un
esquema de las clulas y en la figura 34 B la seccin transversal donde se aprecia que
las paredes de las celdas pueden tener una segunda fase. Todas las celdillas tienen
virtualmente la misma orientacin y juntas forman un solo grano.
Figura 34.Esquema de una microestructura celular. A) Seccin longitudinal de las celdas. B) Seccin
transversal de las celdas.
Reduca (Recursos Educativos)
Serie Qumica de Materiales. 4 (3): 211-284, 2012
ISSN: 1989-5003
247
Las estructuras celulares solo son estables para ciertos gradientes de
temperatura. Si los gradientes de temperatura son ms bajos se desarrollan brazos
secundarios y terciarios formando estructuras dendrticas. Adems, la tendencia a
formar dendritas aumenta con el intervalo de solidificacin. Una imagen de una
dendrita en una aleacin de hierro se muestra en la figura 35
Figura 35. Imagen de una microestructura dendrtica.
SOLIDIFICACIN DE LINGOTES
A un bloque de metal moldeado con una forma simple se llama lingote, en los
aceros los lingotes son de 6 a 8 toneladas. Los lingotes nunca se usan directamente en
aplicaciones comerciales, se convierten en otras formas por uno o ms procesos de
deformacin. La facilidad con que los lingotes pueden trabajarse para dar lugar a
piezas manufacturadas, depende a menudo de la estructura del lingote; forma,
tamao y distribucin de los granos individuales y de la localizacin y composicin de
alguna falta de homogeneidad que surja durante la solidificacin.
Durante la solidificacin de un lingote se producen tres zonas diferenciadas: 1.-
Zona de fra en la que se forman pequeos cristales equiaxiales; 2.- Zona columnar en
la que prevalece el crecimiento dendrtico direccional y 3.-Zona central donde de
nuevo se forman cristales equiaxiales, como se ven en la figura 36.
Reduca (Recursos Educativos)
Serie Qumica de Materiales. 4 (3): 211-284, 2012
ISSN: 1989-5003
248
Figura 36. Seccin a travs de un gran lingote y las tres zonas bsicas que se pueden formar.
Zona fra equiaxial en la pared del molde
Una vez colado el metal, la capa de lquido prxima a la pared del molde est
sometida a un elevado subenfriamiento, lo que conduce a que se produzca un
predominio de la nucleacin, nucleacin heterognea en las paredes del molde. Los
cristales en esa zona de enfriamiento rpido se desarrollan tanto por nucleacin como
por crecimiento. Estos cristales presentan una orientacin al azar y su crecimiento est
limitado por los cristales vecinos lo que da lugar a que se formen cristales pequeos de
carcter dendrtico y equiaxiales.
La extensin de la zona fra es una funcin del material del molde, (arena o
metlico), la temperatura del lquido a colar y la temperatura y conductividad trmica
del molde. El metal liquido se suele colar muy sobrecalentado y las paredes del molde
estn fras lo que da lugar a una zona fra estrecha pudiendo, el lquido muy caliente,
fundir la zona fra y no llegar a apreciarse en la estructura final del lingote. Si el lquido
se cuela a temperatura justo por encima de la temperatura de fusin se produce una
zona fra ancha.
Zona columnar
Una vez formada la zona equiaxial, predomina el crecimiento de cristales y se
observa poca nucleacin. La zona columnar se origina a partir de la zona fra de
cristales que tienen una orientacin favorable para el crecimiento rpido, hacia el
centro del lingote y en sentido contrario al flujo de calor como se observa en la figura
37. En la pared del molde se nuclean una serie de cristales que crecen hasta que se
chocan con sus vecinos. Solo aquellos cristales cuyo sentido de crecimiento es contario
al del flujo de calor avanzan hacia el lquido formando la zona columnar. La direccin
de crecimiento rpido ser aquella en la que las dendritas estn orientadas
perpendiculares a la zona fra, dando lugar a la zona columnar de cristales con
Reduca (Recursos Educativos)
Serie Qumica de Materiales. 4 (3): 211-284, 2012
ISSN: 1989-5003
249
orientacin preferente en el lingote. Para aleaciones con un amplio margen de
solidificacin, los cristales columnares sern dendrticos debido al subenfriamiento
constitucional de la interfase S/L.
Figura 37. Crecimiento competitivo despus del colado. Las dendritas con brazos primarios
perpendiculares a la pared del molde, paralelos al gradiente mximo, crecen ms favorablemente que
sus vecinos.
En metales puros, los cristales columnares crecen dendrticamente en un frente
plano S/L, dependiendo de que el gradiente de temperatura sea positivo o negativo. El
crecimiento de los cristales columnares avanza hasta el centro del lingote. Cada grano
columnar originado por nucleacin heterognea puede contener muchas dendritas
primarias como vemos en la figura 38 que muestra un mayor avance del crecimiento
dendrtico que la figura 37.
Figura 38. Las dendritas orientadas favorablemente se desarrollan en granos columnares. Cada grano
columnar originado por nucleacin heterognea puede contener muchas dendritas primarias.
Reduca (Recursos Educativos)
Serie Qumica de Materiales. 4 (3): 211-284, 2012
ISSN: 1989-5003
250
Zona central equiaxial
El lquido del centro del lingote puede llegar a subenfriarse tanto por efecto
trmico como constitucional dando lugar a una zona central de cristales dendrticos
equiaxiales. Los metales puros no suelen presentar zona central. Existen varios
mecanismos que intentan explicar la formacin de esta zona equiaxial central en
aleaciones. El primero supone que algunos cristales formados en la superficie fra del
molde se funden parcialmente, se separan y por conveccin llegan a la zona central del
lingote, y el segundo que los brazos secundarios de las dendritas pueden llegar a fundir
debido a que al difundirse el calor latente de la solidificacin, se puede acumular en el
lateral de la dendrita que avanza, provocando la fusin parcial de la base del brazo
dendrtico y la posibilidad de que se separen.
Podemos entonces justificar los dos tipos de subenfriamiento que se producen
en la solidificacin de las aleaciones subenfriamiento trmico y constitucional. Las dos
primeras zonas se forman de manera anloga a la de los metales puros. El liquido se
subenfria debido a que el molde retira calor rpidamente, por lo que se produce el
subenfriamiento trmico. La figura 39 muestra como se produce el subenfriamiento
constitucional. Inicialmente una vez formada la zona fra, figura 39 A, se producen a
ambos lados del molde, dos zonas de subenfriamiento constitucional delante de la
interfase S/L. A medida que avanza la zona columnar en el centro del lingote se juntan
las dos zonas de subenfriamiento provocando que la temperatura real del lquido, sea
bastante inferior a la de solidificacin, lo que provoca un gran subenfriamiento y se
favorece de nuevo la nucleacin formando una zona central equiaxial.
Figura 39. Desarrollo de la regin subenfriada constitucionalmente en el centro de un lingote de
aleacin que produce una zona equiaxial central.
Reduca (Recursos Educativos)
Serie Qumica de Materiales. 4 (3): 211-284, 2012
ISSN: 1989-5003
251
En consecuencia, por subenfriamiento constitucional se forma una zona equiaxial
central. El subenfriamiento es tan elevado en el centro del lingote por solapamiento de
las dos zonas de subenfriamiento constitucional que da lugar a la nucleacin y
crecimiento de nuevos cristales equiaxiales.
En la figura 40 podemos ver tres ejemplos de estructuras de solidificacin de
lingotes. En la primera la zona equiaxial es estrecha, figura 40 A la zona columnar
tambin estrecha y la zona equiaxial central grande. Por el contrario en la figura 40 B,
la zona columnar es grande y la zona equiaxial central es estrecha. En la ltima imagen
figura 40 C apenas hay zona fra, la zona columnar es muy estrecha y la zona equiaxial
central es muy grande.
Figura 40. Estructuras de solidificacin de lingotes. A) Zona equiaxial estrecha, zona columnar estrecha
y la zona equiaxial central grande. B) Zona columnar grande y zona equiaxial central estrecha. C) Zona
columnar muy estrecha y zona equiaxial central muy grande.
Efecto de la contraccin
La mayora de los metales contraen al solidificar. En las aleaciones con estrecho
margen de solidificacin la zona pastosa es estrecha lo que da lugar a una cavidad
central en el lingote, ya que sta es la ltima zona en solidificar. Cuando la aleacin
tiene un amplio margen de solidificacin, la zona pastosa puede ocupar todo el lingote
y no se forma una cavidad central. En este caso, el lquido remanente que rodea a las
dendritas no puede fluir hacia el centro, y la contraccin se produce en los espacios
interdendrticos producindose pequeos huecos o poros, que posteriormente pueden
eliminarse por conformacin plstica, figura 41 A.
Segregacin en lingotes y fundiciones
En un lquido metlico existen una serie de elementos que vamos a enumerar
para analizar la influencia que pueden tener en la microestructura final del lingote. El
primero de ellos es el soluto aadido, adems existen elementos impureza, solutos
procedentes de los minerales a partir de los cuales se obtiene el metal, restos de
revestimientos del tabique refractario del horno, gases y por ltimo inoculantes
Reduca (Recursos Educativos)
Serie Qumica de Materiales. 4 (3): 211-284, 2012
ISSN: 1989-5003
252
aadidos para favorecer una determinada microestructura en el lingote que actan,
todos ellos, como centros de nucleacin heterognea proporcionando un tamao de
grano fino.
En los lingotes se pueden dar tres tipos de segregacin: macrosegregacin,
microsegregacin y segregacin inversa.
Macrosegregacin
Se refiere a los cambios de composicin a lo largo de toda la pieza. Como hemos
comentado, los lingotes tienen un tamao apreciable, la macrosegregacin puede
conducir a modificaciones importantes de la composicin a lo largo del lingote, lo que
hara que las piezas que se pueden obtener de ellos, tuvieran propiedades diferentes.
Hay cuatro factores importantes que pueden conducir a la macrosegregacin en
los lingotes: la contraccin trmica debido a la solidificacin y a la diferencia de
temperaturas, las diferencias de densidad en el lquido interdendrtica, las diferencias
de densidad entre el slido y el lquido y por ltimo las corrientes de conveccin
impulsadas por la temperatura e inducidas por las diferencias de densidad del lquido.
El slido es ms denso que lquido y desciende hacia el fondo del lingote,
llevando menos soluto que el lquido dando lugar a una regin de segregacin negativa
en el fondo del lingote. En general la macrosegregacin no es deseable ya que
deteriora las propiedades mecnicas del material. Podemos analizar un ejemplo: en el
sistema PbSb presenta un eutctico con una composicin 11%Sb a 252C. Si tenemos
una aleacin del 20%Sb, y como la densidad del antimonio puro es menor que la del
lquido, los cristales de antimonio suben a la superficie y el eutctico se queda en la
parte inferior del lingote como se ve en la figura 41 B.
Figura 41. A) Porosidad interdendrtica en el lingote. B) Esquema de la segregacin del Sb en la parte
superior del lingote de una aleacin Sn20% Sb.
Reduca (Recursos Educativos)
Serie Qumica de Materiales. 4 (3): 211-284, 2012
ISSN: 1989-5003
253
La macrosegregacin solo puede combatirse o eliminarse con un buen control
del proceso de solidificacin.
Microsegregacin
Este efecto se refiere a la segregacin que se produce en la distancia de
separacin de los brazos secundarios de las dendritas. Est asociada a la estructura
celular debida a subenfriamiento constitucional. La segregacin dendrtica de las
aleaciones da lugar a brazos dendrticos con composicin en soluto inferior a la del
lquido, estos brazos estn rodeados de un lquido que tiene una concentracin de
soluto elevada lo que conduce a la segregacin en la que los brazos dendrticos tienen
una composicin variable.
Las impurezas con coeficientes de reparto menores que la unidad, son ms
solubles en el lquido y se segregan al final de la solidificacin. La microsegregacin
puede mitigarse por homogeneizacin posterior del lingote, pero la difusin en el
slido es lenta.
Segregacin inversa
La segregacin dendrtica puede producir el fenmeno de segregacin inversa.
Entre las dendritas columnares hay lquido con elevada concentracin de soluto, que
debe fluir entre ellas para compensar la contraccin y aumentar la concentracin de
soluto en otros puntos del lingote, que no es en el centro. El flujo de lquido
interdendrtico se desplaza por gravedad. Como ejemplo podemos ver que en
aleaciones Al/Cu, el cobre segregado en el lquido aumenta su densidad y hace se
hunda. Este efecto se ve aumentado por las diferencias de temperatura que aumentan
las corrientes de conveccin.
La succin que atrae el lquido hacia la superficie es debida a la presencia de los
canales interdendrticos, a la contraccin hacia el centro de la pieza y a que las paredes
se separan del molde.
Porosidad
En la solidificacin se produce porosidad en el lingote que es debida a dos
causas bsicas. La primera de ellas es por la evolucin gaseosa durante la
solidificacin y por la contraccin de volumen que acompaa a la solidificacin. No
consideramos la posibilidad de agrietamiento por la contraccin que se produce por
la diferente velocidad de solidificacin de las piezas moldeadas.
La solubilidad de los gases es una funcin de la presin de acuerdo con la
ecuacin C
g
= k P . Donde C
g
es la solubilidad del gas, k es una constante y P la
presin del gas, siendo los gases que se disuelven normalmente diatmicos O
2
, N
2
,
H
2
y cuya solubilidad es baja. As por ejemplo en el caso de la solubilidad del H
2
en
Reduca (Recursos Educativos)
Serie Qumica de Materiales. 4 (3): 211-284, 2012
ISSN: 1989-5003
254
Mg cuyo punto de fusin es 650C tenemos la grafica de la figura 42. En ella vemos
que la representacin es una lnea recta a las tres temperaturas representadas, por
encima y por debajo de punto de fusin lo que indica que la ecuacin anterior es
vlida tanto en magnesio lquido como slido.
Figura 42. Solubilidad del H
2
en Mg tanto lquido como slido en funcin de la presin parcial de
hidrgeno.
Tambin la solubilidad de los gases es funcin de la temperatura y en la
mayora de los casos es una funcin exponencial C
g
= Be
-Q/RT
, siendo Q el trabajo
para introducir un mol de tomos de gas en el metal y B una constante.
En la figura 43 est representada la solubilidad del H
2
en Cu a la presin
constante de 1 atmosfera, donde vemos que la solubilidad aumenta hasta 1083,
temperatura de fusin del cobre y como sta de nuevo aumenta en la fase liquida.
Durante la solidificacin estos cambios se producen igual, es decir, desciende la
solubilidad con la temperatura. De forma que cuando un metal solidifica disminuye
mucho su capacidad para retener gases. Si el proceso de solidificacin es rpido no hay
tiempo para que escapen, estos solutos se segregan en el lquido de la misma forma
que otros solutos. Las elevadas concentraciones de gas en zonas determinadas
provocan la nucleacin y crecimiento de burbujas en la interfase S/L. Estas burbujas
gaseosas crecen de la misma forma que un slido en el seno del lquido por lo que
adoptan formas esfricas, llamadas sopladuras. A veces se pueden producir cavidades
tubulares que se forman cuando la burbuja crece en longitud a la misma velocidad que
se desplaza la interfase S/L.
Reduca (Recursos Educativos)
Serie Qumica de Materiales. 4 (3): 211-284, 2012
ISSN: 1989-5003
255
Figura 43. Solubilidad del H
2
en Cu a una atm de presin.
Figura 44. Dos formas de porosidad gaseosa. A) sopladuras. B) Cavidades tubulares, ambas de tamao
macroscpico en contraste con la porosidad dendrtica que es microscpica.
Si la parte superior del lingote no ha solidificado las burbujas se escapan a la
atmsfera. Cuando la velocidad de crecimiento de las burbujas es baja, quedan
atrapadas por el crecimiento del slido, como se observa en la figura 44 A y se forman
sopladuras. Las sopladuras pueden no ser perjudiciales si al lingote se le somete a un
proceso posterior de conformacin plstica. Si no se han oxidado, las cavidades se
sueldan y el defecto desaparece, siendo el gas absorbido por el slido. Si por el
contario se oxidan, quedan en forma de grietas en el material. Los efectos de la
formacin de burbujas durante la solidificacin, en la estructura metlica dependen de
Reduca (Recursos Educativos)
Serie Qumica de Materiales. 4 (3): 211-284, 2012
ISSN: 1989-5003
256
varios factores como el hecho de que las burbujas quedan atrapadas y de la forma de
las cavidades que las alojan. Las burbujas con velocidades de crecimiento elevadas se
liberan de la intercara.
Si la velocidad de crecimiento de las burbujas es intermedia se originan
cavidades tubulares en las que las burbujas crecen a la misma velocidad que se
desplaza la intercara S/L y en la direccin del flujo de calor, figura 44 B. Cuando se
combinan los efectos de la contraccin y de la evolucin del gas se produce una
porosidad fina e irregular.
En resumen, las formas que adopta la porosidad pueden ser de tres tipos: la
porosidad interdendrtica en la que los poros son paralelos a los brazos dendrticos con
formas angulosas, poros de contraccin que son finos y muy numerosos y poros ms o
menos esfricos que son debidos a la evolucin del gas y producen cavidades grandes
y menos numerosas.
SOLIDIFICACIN EUTCTICA
En la solidificacin de aleaciones o mezclas de composiciones eutcticas binarias
se forman dos fases slidas cooperativamente desde la fase lquida, es decir, la fase
lquida se transforma en las fases o + |, L o + |, a la temperatura de equilibrio T
E
.
Figura 45. A) diagrama eutctico con los campos de las fases marcados. B) Representacin
esquemtica de las diferentes morfologas de aleaciones.
Reduca (Recursos Educativos)
Serie Qumica de Materiales. 4 (3): 211-284, 2012
ISSN: 1989-5003
257
Las caractersticas de un diagrama eutctico son dos: la primera de ellas es que
exista completa miscibilidad en la fase lquida y parcial solubilidad en la fase slida y
que las lneas de solidus y liquidus tengan un coeficiente de reparto k, menor que la
unidad, como se ve en la figura 45 A. La caracterstica fundamental es la mezcla ntima
de dos fases, figura 45 B, en la que se muestra tanto las fases primarias como la
estructura de las dos fases del eutctico en forma laminar. Son posibles distintas
formas de solidificacin eutctica que dependen de las caractersticas individuales de
cada fase (facetadas o no facetadas).
Podemos agrupar a los eutcticos en tres categoras, eutcticos no facetados-no
facetados, eutcticos no facetadosfacetados y eutcticos facetadosfacetados. La
inclusin de las fases slidas o y | en estas categoras dependen de la interfase. El
crecimiento de cada interfase depender de su entropa de fusin. As en el caso de las
aleaciones Cu-Ag se forman interfases no facetadas de baja entropa de fusin. En este
caso ser el eutctico no facetado-no facetado.
En las aleaciones Al-Si las interfases sern no facetadas y facetadas ya que tienen
respectivamente baja y alta entropa de fusin. Sera un ejemplo de los eutcticos no
facetado-facetado. Para muchos compuestos intermetlicos no es fcil conocer a
priori, las entropas de fusin y hay que recurrir a la observacin directa pero se
pueden englobar dentro de uno de los tres grupos anteriores.
Se puede tambin hacer otra clasificacin en la que los eutcticos se denominan
normales y anmalos. Las estructuras normales se producen cuando ambas fases
tienen bajas entropas de fusin dando lugar a eutcticos no facetado-no facetado. Las
estructuras anmalas se producen cuando una o las dos fases forman caras cristalinas,
que tienen elevadas entropa de fusin. Estos eutcticos son no facetadofacetado o
facetadofacetado.
En la figura 46 se muestran una serie de micrografas de microestructuras de
eutcticos con distintas morfologas.
Reduca (Recursos Educativos)
Serie Qumica de Materiales. 4 (3): 211-284, 2012
ISSN: 1989-5003
258
Figura 46. Microfotografas de microestructuras de eutcticos (adaptado de Chadwick G.A., 1972).
Reduca (Recursos Educativos)
Serie Qumica de Materiales. 4 (3): 211-284, 2012
ISSN: 1989-5003
259
Crecimiento de eutcticos no facetados-no facetados.
En los eutcticos normales, las dos fases que crecen presentan una estructura
alternada en forma de lminas, cintas, varillas o fibras de la fase minoritaria embebida
en la otra fase matriz, como se observa en la figura 47. Durante la solidificacin ambas
fases crecen simultneamente manteniendo una interfase S/L esencialmente plana. La
interfase S/L es no facetada o rugosa y el crecimiento no est controlado por la adicin
de tomos en planos especficos. Las dos fases estn subenfriadas y las caractersticas
de crecimiento son funcin de la direccin y flujo de calor, de la interdifusin de los
componentes y de las relaciones de orientacin de ambas fases.
Figura 47 Microestructura tpica metal-metal en seccin transversal. A) Laminas Prof T W Clyne.
Department of Materials Science and Metallurgy, University of Cambridge, cortesia DoITPoms). B)
Cintas o listones (Tomado de Martin j.W.1976). C) Fibras o varillas (cortesa de F. Dynys)
Ejemplos con estas caractersticas los presentan las aleaciones Cu-Al y Ag-Cu, en
las que el eutctico es laminar, en las aleaciones Ag-Al el eutctico tiene formas
fibrosas y con formas de cinta lo presentan las aleaciones Al-Ni. Un caso especial es el
de las aleaciones Zn-MgZn
2
. Cuando esta aleacin es suficientemente pura y el
enfriamiento bastante rpido se forma un eutctico metaestable entre el Zn y el
ZnMg
2
antes que el estable entre el Zn y Mg
2
Zn
11
. La figura 48 muestra la morfologa
caracterstica en espiral del eutctico metaestable Zn-ZnMg
2
visto en seccin
transversal en condiciones de estado estacionario as como un esquema de cmo se
forman las espirales.
Reduca (Recursos Educativos)
Serie Qumica de Materiales. 4 (3): 211-284, 2012
ISSN: 1989-5003
260
Figura 48. Microestructura del eutctico metaestable Zn-ZnMg
2
y esquema del crecimiento en espiral
(tomado de Chalmers B. 1964).
Nucleacin de eutcticos laminares
La nucleacin y crecimiento de eutcticos se produce a una velocidad uniforme
en todas las direcciones con un frente de crecimiento esfrico sin anisotropa en su
crecimiento. El ndulo del eutctico laminar consiste en lminas de las dos fases
colocadas radialmente a partir del centro. En la figura 49 se muestra como a partir de
un ncleo inicial, se produce el desarrollo radial de las dos fases del eutctico. En una
aleacin Al-Cu eutctica, primero nuclea el Al y sobre l se forma un fino halo de CuAl
2
a partir del cual radialmente crece el eutctico. Las dos fases no nuclean
independientes si no que provienen de un crecimiento sencillo que se ramifica, sin
necesidad de posterior nucleacin.
Figura 49. Seccin de un dimetro en una aleacin eutctica Al-CuAl
2
mostrando como de un ndulo
de una de las fases salen las dos fases del eutctico de forma radial.
Podemos representar de forma esquemtica, como a partir de un pequeo
ncleo ms o menos esfrico de una de las fases, la o, se produce sobre l la
nucleacin heterognea de la fase | y la posterior multiplicacin de las lminas, figura
50 A y B formando un ndulo eutctico. Una vez formadas las primeras lminas el
Reduca (Recursos Educativos)
Serie Qumica de Materiales. 4 (3): 211-284, 2012
ISSN: 1989-5003
261
crecimiento de la fase | se produce por el mecanismo de puenteo y ramificado de
ambas fases, figura 50 C, dando lugar al crecimiento con un frente esfrico sin
necesidad de que produzcan nuevas nucleaciones. El la figura 50 D se muestra la
definicin del espaciado interlminar como la distancia entre dos lminas contiguas
o bien entre la mitad de dos lminas de la misma fase. Por ltimo se muestra la forma
del crecimiento unidireccional de un grano de eutctico, figura 50 E, en la que se
aprecia las lminas de ambas fases. He de hacer notar que las fases de un eutctico, no
tienen porque ocupar el mismo volumen ya que su relacin est indicada por la regla
de la palanca.
Figura 50. Representacin esquemtica de la nucleacin y multiplicacin de las lminas en un ndulo
eutctico. A) Ncleo primario de fase o y nucleacin heterognea de la fase |. B) Crecimiento de la
fase | por puenteo y ramificado de ambas fases. C) Crecimiento con un frente esfrico que da lugar a
la multiplicacin de las lminas. D) Definicin de . E) Crecimiento unidireccional de un grano de
eutctico.
En la figura 51 se muestra la microestructura de una aleacin eutctica en la que
se observan los granos orientados en la direccin de la solidificacin y como dentro de
ellos estn la colonias eutcticas con orientaciones distintas.
Figura 51 Microestructura eutctica de una aleacin Cu-Ag.
Reduca (Recursos Educativos)
Serie Qumica de Materiales. 4 (3): 211-284, 2012
ISSN: 1989-5003
262
Crecimiento de eutcticos laminares
Vamos a explicar el crecimiento de un eutctico laminar utilizando el esquema
de la figura 52 en el que las fases son o y | y los componentes A y B. Al solidificar la
fase o rica en A, se produce un exceso de B delante de la interfase o/L, que difunde
lateralmente por el lquido a una distancia corta hasta delante de la interfase |/L,
donde se incorpora a la fase | rica en B. De la misma forma los tomos de A
rechazados o segregados frente a la fase | difunden a los extremos de las lminas
adyacentes de o, haciendo que crezcan las dos fases simultneamente. La velocidad a
que crece el eutctico depender de la rapidez con que se produzcan esas difusiones,
lo cual, a su vez depender del espaciado interlminar .
Figura 52. Interdifusin en el lquido en el frente de solidificacin.
Si el espaciado interlminar, es pequeo el crecimiento ser rpido. Sin
embargo hay un lmite inferior para determinado por la necesidad de proporcionar la
energa interfacial a la interfase o/|,
o|
. Para un espaciado hay un total de 2/ m
2
de interfase o/| por m
3
de eutctico. Si sabemos la energa asociada a la interfase,
podremos calcular la energa libre de Gibbs.
La variacin de energa libre AG asociada a la solidificacin de un mol de lquido,
con un espaciado interlminar , ser:
+ A = A
o|
m
) ( ) (
V 2
G G
Donde V
m
es el volumen molar del eutctico y AG
()
es la disminucin de energa
libre para valores muy grandes de . Puesto que la solidificacin no tendr lugar si la
AG
()
es mayor que cero, AG
()
deber ser suficientemente grande para compensar el
valor del trmino de energa interfacial, es decir la interfase eutctico/lquido debe
subenfriarse por debajo de la temperatura de equilibrio del eutctico T
E
.
Reduca (Recursos Educativos)
Serie Qumica de Materiales. 4 (3): 211-284, 2012
ISSN: 1989-5003
263
Si el subenfriamiento total es AT se puede demostrar que AG
()
viene dado
aproximadamente por
E
0
) (
T
T H
G
A A
= A
, por lo que el espaciado mnimo posible (*)
se obtiene utilizando la relacin AG
(*)
e igualndola a cero. Tendremos
*
V 2
G
m
) (
= A
o|
y
0
2
T H
V T
*
m E
A A
=
o|
Cuando el eutctico tiene este espaciado, la energa libre del lquido G
L
es igual a
la del eutctico slido, G
eutctico(slido)
es decir, las tres fases estn en equilibrio. Esto es
as porque la interfase o/| eleva las energas libres de o y | desde G
o
() y G
|
() hasta
G
o
(*) y G
|
(*), como se muestra en la figura 53.
La causa de esta elevacin de la energa libre est en la curvatura de las
interfases o/lquido y |/lquido y que tienen su origen en la necesidad de equilibrar las
tensiones interfaciales en el punto triple o/|/L. As si el espaciado es infinito
tendramos la menor contribucin de la tensin superficial a la energa libre, por lo que
las curvas de las fases o y | se sitan a menores valores de energa libre. Al aumentar
el espaciado interlminar , hay una mayor contribucin de la tensin superficial por lo
que los valores de la energa libre son mayores. En cualquier caso al existir una
interfase, S/L habr una contribucin de la tensin superficial a la energa libre que se
pone en juego, siendo esta diferencia AG
()
.
Figura 53. Diagrama de energa libre molar a la temperatura AT
0
por debajo de la temperatura
eutctica, para el caso de = *.
Reduca (Recursos Educativos)
Serie Qumica de Materiales. 4 (3): 211-284, 2012
ISSN: 1989-5003
264
Figura 54. A) Diagrama de energa libre molar a (T
E
- AT
0
) para el caso que * < < , mostrando la
diferencia de composicin que permite la difusin a travs del lquido (AX). B) Modelo utilizado para
calcular la velocidad de crecimiento.
El aumento de la energa libre de cada fase ser diferente para cada una de ellas,
pero en los casos ms sencillos se demuestra que, para ambas, es 2
o|
V
m
/. Para que
se pueda producir el avance del proceso de solidificacin eutctica, deber haber un
flujo de tomos entre los extremos de las lminas de las fases o y | y ello requiere una
diferencia finita en su composicin AX. La diferencia de composicin se establece
porque la concentracin del componente B en el punto marcado en la figura delante
de la fase o es mayor que frente a la fase |, dado por los diferentes puntos de
tangencia de las fases o y | con la fase lquida, como se ve en la figura 54 A.
Reduca (Recursos Educativos)
Serie Qumica de Materiales. 4 (3): 211-284, 2012
ISSN: 1989-5003
265
Los tomos de B rechazados (segregados) al formarse la fase o tienen que
difundir hacia los extremos de las lminas donde se est formando |. Si el espaciado
interlminar es el * (figura 53) en el que las tres fases estn en equilibrio, el
crecimiento sera infinitamente lento porque el lquido en contacto con ambas fases
tendra la misma composicin, la del eutctico X
E
. Si por el contrario es mayor que *
habra menos energa retenida en las interfases y G
o
y G
|
seran menores. En este caso
se establece un equilibrio local del liquido con la fase o cuya composicin sera
o / L
B
X
que es ms rico en B que el lquido en equilibrio local con la fase |
| / L
B
X , figura 54 B.
Si las interfases o/L y |/L fuesen muy mviles el crecimiento estara controlado
por la difusin en cuyo caso la velocidad (v) de crecimiento eutctico, sera
proporcional al flujo de soluto a travs del lquido. Se puede demostrar que la
velocidad de avance del eutctico es
A
=
X
D K v
1
y que la sobresaturacin es
| o
= A
/ L
B
/ L
B
X X X . K
1
es una constante de proporcionalidad y la sobresaturacin AX
depender del espaciado interlminar ya que cuando es igual a *, no hay
sobresaturacin y AX es 0, y al crecer , AX tender a un valor mximo AX
o
que puede
obtenerse extrapolando las lneas liquidus en el diagrama de equilibrio ( = ), figura
55. Por tanto la diferencia de composicin en el lquido la podemos expresar como
|
.
|
\
|
A = A
*
1 X X
o
Figura 55. Diagrama de fase de un eutctico mostrando la relacin entre AX y AX
o
(Se muestra de
forma exagerada para mayor claridad).
Reduca (Recursos Educativos)
Serie Qumica de Materiales. 4 (3): 211-284, 2012
ISSN: 1989-5003
266
Cuando el subenfriamiento que se produce en la solidificacin es pequeo, la
diferencia de concentracin AX
o
es proporcional al subenfriamiento AT
o
, como se ve
en la figura 55. La lneas de trazos son las lneas liquidus cuando el espaciado es
mayor que * pero menor que
. Si combinamos las ecuaciones anteriores
tendremos que la velocidad de crecimiento del eutctico
|
.
|
\
|
A =
*
1
1
T D K v
0 2
,
donde K
2
es otra constante. Si analizamos esta ecuacin podemos establecer que
variando el subenfriamiento en la interfase (AT
0
) es posible variar tanto la velocidad V
como el espaciado interlminar independientemente, siendo posible predecir el
que se observar a una velocidad dada.
Cuando el espaciado es dos veces *, la velocidad de crecimiento del eutctico
es mxima para un subenfriamiento AT dado o al revs el subenfriamiento requerido
es un mnimo para una velocidad dada. Si asumimos que el crecimiento se produce en
condiciones ptimas cuando el espaciado
o
es 2* la velocidad de crecimiento es v
0
=
K
2
D AT
0
/2*. Como el subenfriamiento AT
o
es proporcional a 1/* podemos sustituir y
tendremos que v
o
2
o
= K
3
y
4
0
0
K
) T (
v
=
A
. No hay una base fsica para suponer que el
espaciado es dos veces * y se pueden hacer otras suposiciones.
El subenfriamiento total (AT
o
) tiene dos contribuciones, AT
o
= AT
r
+ AT
D
, donde
AT
r
es el subenfriamiento requerido para compensar los efectos interfaciales debidos a
la curvatura de la interfase y AT
D
el subenfriamiento requerido para dar lugar a la
diferencia de composicin que permita la difusin. Podemos suponer que habra un
trmino ms llamado AT
i
debido a la barrera que supone cruzar la interfase pero es
despreciable debido a la movilidad de la interfase, por lo que no se tiene en cuenta.
La figura 56 A muestra la seccin transversal de unas lminas de las dos fases. La
composicin del lquido en contacto con la interfase y, por tanto, AT
D
vara
peridicamente con un periodo igual a , figura 56 B. La temperatura de solidificacin
de cada punto ser menor que la de equilibrio eutctica T
E
y su variacin es la
representada en la figura 56 D. Para conseguir que la interfase sea isoterma las
superficies de las lminas en contacto con el lquido debern tener una curvatura
variable para compensar las diferencias de AT
D
. Las lminas estarn ms curvadas en
las posiciones prximas al lmite de la intercara, figura 56 C.
Reduca (Recursos Educativos)
Serie Qumica de Materiales. 4 (3): 211-284, 2012
ISSN: 1989-5003
267
Figura 56. A) Seccin transversal delante de la interfase S/L. B) Se produce la fluctuacin peridica de
la composicin de longitud de onda que llega da lugar a diferencias en la temperatura de
solidificacin de equilibrio en el lquido. C) La interfase adopta una mayor curvatura en el lmite de la
intercara entre las lminas que en el centro para compensar esto y mantener la interfase isoterma. D)
Variacin de la temperatura de la interfase en funcin de la curvatura como suma de AT
D
y AT
r
.
No siempre la solidificacin eutctica se produce en un frente plano. Si la
aleacin binaria contuviese alguna impureza la interfase tiende a "romperse" y formar
una estructura de morfologa celular.
Efecto de las impurezas en los eutcticos metal-metal
Si las impurezas presentes tienen un coeficiente de reparto menor que 1 en
ambas fases slidas, estas segregarn la impureza al lquido y la concentracin de
impurezas en la interfase puede ser muy alta. Se puede producir subenfriamiento
constitucional aunque el gradiente de temperaturas impuesto sea pequeo
provocando que no sea estable una interfase plana y formando una estructura en
colonia. En la figura 57 A se muestra una simulacin del crecimiento eutctico en
colonia. En el crecimiento laminar de las interfases slido/lquido las lminas son
aproximadamente paralelas pero si la interfase es convexa como se produce en la
estructura celular, hay divergencia de las lminas durante el crecimiento.
Reduca (Recursos Educativos)
Serie Qumica de Materiales. 4 (3): 211-284, 2012
ISSN: 1989-5003
268
Figura 57. A) Simulacin del crecimiento celular de una aleacin eutctica con una impureza. B)
Imagen de una colonia eutctica de muestra un grano con varias colonias. (cortesa M. Plapp, A.
Karma).
Un hecho a destacar es que las colonias no separan granos eutcticos. Se
producen cambios en la direccin de las colonias eutcticas pero en todas las colonias
que se originan en un grano eutctico la orientacin cristalogrfica de las fases dentro
de cada colonia es aproximadamente constante, figura 57 B. Existen relaciones de
orientacin en las dos fases del eutctico, pero no se ha podido comprobar si esta
relacin se establece en la nucleacin o en el crecimiento.
La figura 58 muestra una simulacin de cmo va avanzando el crecimiento de las
lminas de las dos fases. La modificacin del espaciado interlminar es funcin de la
velocidad de crecimiento del eutctico.
Figura 58. Simulacin del crecimiento eutctico.
Reduca (Recursos Educativos)
Serie Qumica de Materiales. 4 (3): 211-284, 2012
ISSN: 1989-5003
269
Zona de crecimiento cooperativo de eutcticos
Por debajo de la temperatura de equilibrio eutctico T
E
es posible solidificar los
lquidos de un amplio rango de composiciones formando slidos con morfologa
eutctica y que crecen con una intercara plana estable. Se puede trazar una regin de
crecimiento estable a temperatura inferior a T
E
denominada zona conjunta, como la
representada en la figura 59 A. Tenemos varias posibilidades. En la primera de ellas i)
se traza una zona conjunta simtrica respecto a ambas fases, que ms o menos
representa la prolongacin de las lneas de lquidus. En el caso ii) la zona conjunta est
ligeramente desplazada hacia una de las fases y en el tercero iii) la zona conjunta est
muy desplazada hacia la fase de mayor punto de fusin. Con estos esquemas podemos
apreciar que existe una gran variedad de posibilidades de desplazamiento de las zonas
conjuntas de precipitacin eutctica. Los dos casos ms caractersticos de las zonas
conjuntas estn representados en la figura 59 B. Muestran que justo por debajo de la
temperatura eutctica las zonas estn ensanchadas justificando el hecho de que
cuando el enfriamiento es muy lento pueden formarse las dos fases simultneamente
en sistemas en los que la zona conjunta est desplazada. Vemos adems que la zona
de crecimiento conjunto aumenta conforme aumenta el subenfriamiento AT.
Figura 59. A) Ejemplos de los muchos posibles de la zona conjunta en aleaciones eutcticas, i)
Simtrica. ii) Ligeramente desplazada. iii) Muy desplazada. B) Dos casos tpicos de zonas conjuntas con
el ensanchamiento debajo de T
E
. i) Simtrica. ii) Desplazada hacia la fase de mayor punto de fusin.
Reduca (Recursos Educativos)
Serie Qumica de Materiales. 4 (3): 211-284, 2012
ISSN: 1989-5003
270
La forma de la zona conjunta no influye sobre la morfologa del eutctico,
solamente establece las caractersticas de la cintica de solidificacin de las fases que
lo componen. La zona crecimiento conjunto a temperaturas menores de la de
equilibrio T
E
es explicable en trminos de la velocidad de crecimiento de las
microestructuras bifsicas en relacin con las velocidades de crecimiento de las fases
que forman el eutctico aisladas.
Dentro de la zona, las dos fases son capaces de crecer cooperativamente por
mecanismos normales de difusin de corto alcance a una velocidad superior que la de
las dos fases componentes separadamente. Si las fases primarias nucleasen en la zona
conjunta, el crecimiento dendrtico libre se anula rpidamente porque el eutctico
engulle a las dendritas. Fuera de la zona conjunta crece primero una fase primaria
hasta que el lquido se enriquece suficientemente en el otro componente para permitir
el crecimiento eutctico.
En sistemas donde los puntos de fusin de las fases componentes son muy
diferentes, y por tanto la composicin eutctica est desplazada respecto al centro del
diagrama de fases, la zona conjunta se desplaza tambin de la posicin de simetra
entorno a la composicin eutctica, figura 59 A iii y B ii.
Cuando la temperatura es menor que la de equilibrio eutctico, T
E
el
subenfriamiento AT del lquido es relativamente mayor para la fase de temperatura de
fusin ms alta que para la fase de temperatura de fusin ms baja y por eso la
temperatura tiene mucha mayor influencia en la velocidad de crecimiento de la
primera que la de la segunda. Esta diferencia en la velocidad decrecimiento produce el
desplazamiento de la zona conjunta. Podemos ver un ejemplo de una aleacin
hipereutctica en el caso de la aleacin con zona no simtrica, figura 59 B ii. Si esta
aleacin se sita por debajo de la temperatura de solidificacin eutctica, se encuentra
en una zona en la que no est favorecido el crecimiento conjunto de las dos fases. Se
formara fase primaria |, y de esta forma la composicin del lquido se desplaza hacia la
izquierda, enriquecindose en A, hasta que se alcanza la zona de precipitacin
conjunta, y entonces se pueden formar las dos fases cooperativamente. En este caso la
microestructura de la aleacin tendra mayor cantidad de fase primaria que la que le
correspondera y se compensara con menor cantidad de esa fase en el eutctico.
En aquellos sistemas eutcticos que la zona conjunta sea muy asimtrica figura
59 A iii, suele desplazarse hacia la fase de mayor temperatura de solidificacin. Desde
el punto de vista de la microestructura de la aleacin, la zona conjunta permite
explicar los halos de segunda fase alrededor de la fase primaria en aleaciones hipo e
hipereutcticas. Este hecho es frecuente en aleaciones eutcticas metal-no metal.
Reduca (Recursos Educativos)
Serie Qumica de Materiales. 4 (3): 211-284, 2012
ISSN: 1989-5003
271
Eutcticos facetados-no facetados
Los principios cinticos y termodinmicos de eutcticos facetados-no facetados
son iguales a los de los eutcticos metal-metal. Las nicas diferencias apreciables son
su morfologa y se deben a los mecanismos de crecimiento atmico diferente entre los
metales y no metales. La morfologa dplex que se desarrolla depende de la
anisotropa especfica de crecimiento del constituyente no metlico, siendo este el
factor que normalmente controla la microestructura. Las caractersticas de crecimiento
de los no metales condicionan la morfologa del crecimiento de estas, en aleaciones
eutcticas.
Dos casos caractersticos son el silicio y el germanio que se forman como cristales
finos en forma de cinta o cristales idiomrficos facetados. Si la aleacin es eutctica
Me-no Me, el Si y el Ge tienden a crecer como cristales en forma de cinta o en forma
de tela de araa como vemos en la figura 60 A para el caso del eutctico Al-Si y el Sn-Bi
en la figura 60 B. El bismuto tiende a crecer como cristales tridimensionales cuando
crece a partir de sus fundidos, pero en aleaciones Pb-Bi y Sn-Bi la microestructura
muestra complejas unidades de crecimiento tridimensional del eutctico. La fase Bi
anistropa, controla el tipo de crecimiento.
Figura 60. Microestructura de eutcticos que muestran la formacin de telas de araa. A) Eutctico Al-
Si (cortesa Guthy H, 2002). B) Eutctico Sn-43Bi (cortesa Dr. Morris).
La formacin del halo alrededor de las fases primarias es muy frecuente y
representa la acumulacin del soluto del segundo componente en la interfase
solido/lquido debido a la incapacidad de la fase primaria para nuclear a la segunda
fase del eutctico (por la asimetra de la zona de precipitacin cooperativa). La
acumulacin del soluto puede desplazar la concentracin del lquido hacia la zona de
crecimiento cooperativo con lo que se debe formar primero el halo de segunda fase
para llevar la composicin hasta la zona conjunta. En aquellos sistemas en los que se
observa la presencia de halo en composiciones a un lado del eutctico y la ausencia en
el otro indica que la zona conjunta es asimtrica.
Reduca (Recursos Educativos)
Serie Qumica de Materiales. 4 (3): 211-284, 2012
ISSN: 1989-5003
272
En la figura 61 A y B se muestra un ejemplo de una aleacin Nb-Si En el caso de
que la aleacin sea hipoeutctica se forman dendritas de Nb de color claro junto con el
eutctico, donde la fase oscura es Nb
3
Si. Si la aleacin es hipereutctica alrededor de
los cristales primarios del compuesto Nb
3
Si se forma un halo blanco de la fase Nb antes
de producirse la precipitacin cooperativa del eutctico.
Figura 61. A) Microestructura de una aleacin Nb-Si hipoeutctica en la que alrededor de las dendritas
de Nb no se forma halo. X 500. B) Microestructura de una aleacin Nb-Si hipereutctica. Halo blanco
de Nb alrededor de los cristales primarios del compuesto Nb
3
Si. X 1000 (cortesa J.L. Raviart ONERA,
the French Aerospace Lab).
El proceso de nucleacin en los eutcticos metal-no metal es muy similar a la
nucleacin de los eutcticos metal-metal. La aleacin eutctica se subenfra un poco
por debajo de la temperatura de equilibrio eutctico, T
E
y un cristal primario de una de
las fases crece independientemente en el lquido. La magnitud del crecimiento del
cristal primario depende de la facilidad con que la segunda fase se nuclee a partir de la
primera.
La segunda fase nuclear normalmente como un halo rodeando completamente
los cristales primarios. Una vez que estn las dos fases se produce el crecimiento
conjunto de ambas. Normalmente el metal produce una interfase no facetada
mientras que el no metal da lugar a interfases facetadas. Aunque el crecimiento del
eutctico se produce de una forma cooperativa, se requiere difusin cruzada a travs
de la interfase de las dos especies atmicas para mantener el crecimiento de las dos
fases contiguas. A pesar de las consideraciones expuestas, ninguna teora permite el
anlisis cualitativo de las caractersticas que van a dar lugar a las morfologas
irregulares de estos eutcticos.
Los eutcticos de las aleaciones Fe-C y Al-Si son dos ejemplos tpicos de gran
importancia industrial por lo que vamos a ver con algn detalle las caractersticas de
estas aleaciones eutcticas.
Reduca (Recursos Educativos)
Serie Qumica de Materiales. 4 (3): 211-284, 2012
ISSN: 1989-5003
273
Crecimiento de aleaciones Al-Si y Fe-C
En la figura 62 se muestra el diagrama de equilibrio de las aleaciones aluminio
silicio, situndose la composicin del eutctico en el 12,6 % en masa de Si. En las
aleaciones eutcticas las dos fases crecen simultnea y contiguamente por procesos de
crecimiento cooperativo. La interfase no ha de ser plana. La fase facetada puede
adelantar a la posicin media de la interfase como vimos en la figura 58. La fase Si
adquiere distintas formas en funcin velocidad de crecimiento.
Figura 62. Diagrama de equilibrio del sistema Al-Si.
En la aleacin eutctica, moldeada en arena, se obtiene una estructura de agujas
de la fase Si embebidas en una matriz de la fase o, figura 63 A, como consecuencia de
una velocidad de crecimiento muy lento (0.28m/s y AT 3/min). Sin embargo, si el
enfriamiento es mucho ms rpido como el enfriamiento en coquilla, el Si forma fibras
ramificadas y filamentosas y la microestructura cambia completamente y a pesar de
ser una aleacin eutctica se obtienen dendritas primarias de fase o como se muestra
en la figura 63 B.
Reduca (Recursos Educativos)
Serie Qumica de Materiales. 4 (3): 211-284, 2012
ISSN: 1989-5003
274
Figura 63. A) Microestructura de la aleacin eutctica Al-Si enfriada en arena. B) Microestructura de la
misma aleacin enfriada en coquilla.
La figura 64 A muestra la parte del diagrama de equilibrio del sistema Fe-C del
eutctico. Se observa que el eutctico se sita en 4,3 % en masa de C. La aleacin
eutctica est formada por dos fases austenita y Fe
3
C, llamada ledeburita, figura 64 B.
Figura 64. A) Diagrama de equilibrio sistema Fe-C mostrando el eutctico. B) Eutctico Austenita- Fe
3
C
(ledeburita).
Las fundiciones pueden ser hipo o hipereutcticas en las que la fase primaria es
la austenita que solidifica en forma de dendritas (que posteriormente se transforma en
perlita) o el carburo de hierro en forma de grandes agujas, que como fase primaria
presenta un pronunciado carcter facetado en una matriz eutctica. En ambos casos
las fundiciones se denominan fundiciones blancas ya que la forma del carbono es el
Fe
3
C. En la figura 65 A se muestra la estructura de una fundicin blanca hipoeutctica y
la figura 65 B la estructura de las grandes agujas primarias de Fe
3
C en una matriz
eutctica, de una fundicin hipereutctica. En el detalle a mayores aumentos vemos
como las dendritas de austenita se transforman en una estructura laminar de perlita,
figura 65 C y D.
Reduca (Recursos Educativos)
Serie Qumica de Materiales. 4 (3): 211-284, 2012
ISSN: 1989-5003
275
Figura 65 A) Microestructura de una fundicin blanca hipoeutctica. Dendritas de austenita que
posteriormente durante el enfriamiento se transforma en perlita. B) Microestructura de una fundicin
blanca hipereutctica. C) X 200 y D) X 1000. Detalle MEB a mayores aumentos de las dendritas de
austenita en la fundicin blanca (cortesa Criado A. 2009)
Efecto de las impurezas en los eutcticos metal-no metal
De nuevo vamos a mostrar la influencia de las impurezas en las aleaciones Fe-C y
Al-Si. En ambos casos la forma facetada de la fase primaria del no metal, conduce a
malas propiedades mecnicas. Por ello si se consigue modificar la microestructura se
alcanzan mejoras importantes en las propiedades.
En las aleaciones Al-Si para afinar la microestructura (que se consegua con
enfriamientos muy rpidos) y mejorar la ductilidad de la aleacin se aade sodio. Este
elemento aadido al caldo antes de colar, reduce la temperatura del eutctico y se
alcanza un elevado subenfriamiento. Como consecuencia de ello, se favorece la
nucleacin de las fases del eutctico, proceso que se conoce como modificacin. En la
figura 66 A se muestra una aleacin eutctica Al-Si a la que en la colada se ha aadido
sodio. Se forman dendritas primarias de aluminio y el eutctico formado por la matriz
de aluminio con pequesimas acculas de Si. Cuando se aade sodio en exceso a la
colada se produce la sobremodificacin en la que aumenta el tamao de los cristales
Reduca (Recursos Educativos)
Serie Qumica de Materiales. 4 (3): 211-284, 2012
ISSN: 1989-5003
276
de Si probablemente debido a la presencia de fosforo y la interaccin de este con el
sodio, figura 66 B.
Figura 66. A) Microestructura de una aleacin eutctica Al-Si modificada con sodio. B) La misma
aleacin sobremodificada con sodio.
En las fundiciones de hierro se puede conseguir que en vez de las agujas
primarias del carburo de hierro Fe
3
C, se forme grafito. Para ello es necesario que la
aleacin lleve al menos un 2% de Si consiguindose las llamadas fundiciones grises en
las que el carbono de la aleacin est en forma de grafito y cuya fractura es gris. Para
que se obtengan fundiciones grises, adems de Si en su composicin, se puede jugar
con la velocidad de enfriamiento obtenindose distintas formas del carbono.
En la figura 67 se muestra una representacin esquemtica de las distintas
formas que puede adoptar el carbono en las fundiciones. En la figura 67 A se tiene una
fundicin gris con la forma ms comn del grafito, en forma de lminas, hojuelas,
copos o escamas. En el dibujo de la figura 67 B corresponde a una fundicin blanca con
dendritas de austenita que en el enfriamiento se transforma en perlita (color oscuro) y
el eutctico de austenita y carburo de hierro (blanco), fundicin blanca. Hay otras
formas del carbono como grafito, una de ellas es como ndulos ms o menos
esferoidales, que da lugar a dos tipos de fundiciones grises. La fundicin gris maleable
figura 67 C, que se obtiene mediante tratamiento trmico de la fundicin blanca y la
adicin de inoculantes y el segundo la fundicin gris dctil o esferoidal figura 67 D, que
se obtiene mediante la adicin de magnesio o cerio en la colada. El otro tipo de grafito
es una forma intermedia entre ndulos y hojuelas, llamado fundicin gris de grafito
compacto o vermicular, figura 67 E. En todos los casos se consiguen las formas del
grafito que mejoran la ductilidad.
Reduca (Recursos Educativos)
Serie Qumica de Materiales. 4 (3): 211-284, 2012
ISSN: 1989-5003
277
Figura 67. Esquemas de las diferentes microestructuras de fundiciones de hierro. A) Fundicin gris. B)
Fundicin blanca. C) Fundicin gris maleable. D) Fundicin gris de grafito esferoidal. E) Fundicin gris
de grafito compacto.
En las aleaciones eutcticas del sistema Fe-C, la adicin de Ce o Mg a las estas
aleaciones provoca una alteracin en la forma de crecimiento del grafito. En vez de
lminas unidas por planos basales de la estructura hexagonal del grafito, se desarrolla
una morfologa nodular o esferoidal. Aumentando las velocidades de enfriamiento
tambin se modifica la morfologa del grafito. En las micrografas la figura 68 se
muestran un detalle de SEM de los distintos tipos de grafito. Grafito en forma de
hojuelas o lminas, figura 68 A. En la figura 68 B se observa el aspecto del grafito
vermicular o en forma de estructura coralina. Por ltimo en la figura 68 C se muestra el
grafito esferoidal.
Figura 68. A) detalle de las hojuelas de grafito. B) Grafito vermicular. C) Grafito esferoidal.
Reduca (Recursos Educativos)
Serie Qumica de Materiales. 4 (3): 211-284, 2012
ISSN: 1989-5003
278
En las fundiciones de hierro, como se muestra en la figura 69, el enfriamiento
posterior de las aleaciones da lugar a unas reacciones que se vern posteriormente,
donde aparece ferrita y perlita. En muchos casos, alrededor del grafito, 100% C, se
favorece la formacin de la ferrita (solucin slida o pobre en C) mostrndose como
zonas blancas, figura 69 A alrededor de las hojuelas de grafito o bien un halo blanco
que rodea a las esferas de grafito, figura 69 B, denominados bulls eye. El diagrama
de equilibrio muestra una reaccin eutectoide que da lugar a perlita que forma la
matriz de la aleacin.
Figura 69. A) Microestructura de una fundicin gris con hojuelas de grafito, ferrita y una matriz de
perlita B) Microestructura de una fundicin gris esferoidal mostrando bull's-eye de grafito en una
matriz perltica.
Eutcticos divorciados
Los eutcticos divorciados no son una clase especial de eutcticos ya que es un
tipo de microestructura que se desarrolla en aleaciones hipo o hipereutcticas cuando
la fase primaria est en gran cantidad y el eutctico no presenta una microestructura
dplex. En el caso de una aleacin Cu-O la fase de cobre primaria se forma como
dendritas. En la figura 70 se muestra el diagrama Cu-O y un detalle la zona de las
aleaciones donde se sita el eutctico. La solubilidad del oxgeno en el cobre es muy
baja, 0.008% O y el eutctico se sita en un 0.43% O. Al llegar a la temperatura
eutctica, se deben formar las dos fases, pero debido a las dificultades de nucleacin
del compuesto Cu
2
O en el cobre, las dendritas primarias siguen solidificando y se
forma una distribucin de las partculas de Cu
2
O en espacios interdendrticos. Por
solidificacin direccional tambin es posible obtener los eutcticos divorciados.
Reduca (Recursos Educativos)
Serie Qumica de Materiales. 4 (3): 211-284, 2012
ISSN: 1989-5003
279
Figura 70. Diagrama de equilibrio del sistema Cu-O.
En la figura 71 se muestra la microestructura de una aleacin que presenta este
tipo de eutctico como es el cobre-oxigeno. Durante el proceso de fabricacin del
cobre se disuelve el oxigeno en pequeas cantidades dando lugar a un eutctico
divorciado, en el que las partculas del oxidulo estn agrupadas en algunas zonas figura
71 A en una matriz de cristales de cobre. La figura 71 B muestra un detalle de las
partculas de oxidulo de cobre. Sin embargo la forma que adquiere la estructura
eutctica provoca problemas tanto de soldabilidad del cobre como deterioro de las
propiedades mecnicas y por ello y por la elevada porosidad que tienen estas
aleaciones despus de la solidificacin se somete a un proceso de hechurado en
caliente que da lugar a cristales de pequeo tamao de la matriz de cobre y una
distribucin de las partculas del oxidulo de cobre en la direccin de hechurado, figura
71 C.
Reduca (Recursos Educativos)
Serie Qumica de Materiales. 4 (3): 211-284, 2012
ISSN: 1989-5003
280
Figura 71. A) Microestructura de aleacin Cu-O solidificada mostrando un eutctico divorciado 100X.
B) Detalle de las partculas de oxidulo de cobre. 1000X. C) Microestructura despus del hechurado.
100X.
Aleaciones de composicin fuera del eutctico
Cuando la composicin global de la aleacin X
o
no corresponde a la composicin
eutctica, X
E
, como se observa en la figura 72 A, la solidificacin empieza por la
formacin de la fase primaria en forma de dendritas de la fase o. Al engrosar las
dendritas, el soluto se segrega en el lquido remanente hasta que su composicin llega
a la composicin eutctica solidificando el eutctico a T
E
. En condiciones de
solidificacin unidireccional y rgimen estacionario, bajo un gradiente suave de
temperatura, la temperatura de la punta de las dendritas estarn por debajo de la
primera temperatura de solidificacin de la aleacin un valor como AT
d
y la
temperatura del frente eutctico, a T
E
, como se aprecia en la figura 72 B y C. Se
produce la solidificacin dendrtica con coring o microsegregacin en la estructura
como vemos en la figura 72 D. Controlando las condiciones de solidificacin es posible
que una aleacin de composicin no eutctica tenga una estructura sin las dendritas
primarias.
Reduca (Recursos Educativos)
Serie Qumica de Materiales. 4 (3): 211-284, 2012
ISSN: 1989-5003
281
Figura 72. Solidificacin de una aleacin fuera del eutctico en un gradiente de temperatura. A)
Diagrama de equilibrio. B) esquema del frente de solidificacin. C) Variacin de temperatura a travs
del frente de solidificacin. D) Seccin transversal de la dendrita.
Reaccin peritctica
La figura 73 A muestra el diagrama de fases de equilibrio de un peritctico
idealizado en el que se muestra las caractersticas de esta reaccin invariante. Por una
parte tiene completa miscibilidad en estado lquido junto con la parcial solubilidad en
estado slido y por otra tiene dos lneas de reparto con un coeficiente k menor que la
unidad y otras dos con un k mayor que la unidad.
La solidificacin de una aleacin de composicin X
0
a una velocidad finita y bajo
un gradiente de temperatura suave da lugar a la secuencia de solidificacin que
describimos. A partir del lquido y al descender la temperatura aparecer la primera
fase slida, o
1
a la temperatura T
1
, figura 73 B, posteriormente se formar ms fase o
hasta que se alcance la temperatura del peritctico T
p
, temperatura en la que la fase o
formada reacciona con el lquido para dar fase |. Las dendritas de o deben disolverse a
Reduca (Recursos Educativos)
Serie Qumica de Materiales. 4 (3): 211-284, 2012
ISSN: 1989-5003
282
la vez que se forma |. Posteriormente cuando haya desaparecido la fase o precipitar
ms fase | hasta que toda la aleacin sea | homognea y de composicin X
0
.
Sin embargo, las condiciones de enfriamiento de equilibrio no se cumplen en un
enfriamiento normal, por lo que la solidificacin peritctica sigue otro camino. En
primer lugar la fase o primaria crecer normalmente de forma dendrtica por capas
sucesivas que solidifican con composiciones determinadas por la temperatura local en
cada punto. Si la difusin en las dendritas es lenta, el lquido alcanzar la composicin
del lquido peritctico L
P
y por posterior enfriamiento (extraccin de calor, sin cambiar
la temperatura) reaccionar con la fase o
P
para producir una capa de fase |
P
, marcada
en rojo en la figura 73 C.
Figura 73. A) Representacin idealizada del diagrama de equilibrio peritctico. B) Representacin
esquemtica de transformacin peritctica idealizada. C) Representacin esquemtica de lo que
ocurre en una reaccin peritctica.
Reduca (Recursos Educativos)
Serie Qumica de Materiales. 4 (3): 211-284, 2012
ISSN: 1989-5003
283
A la temperatura del peritctico la reaccin de disolucin se realiza en la
superficie de las dendritas de o y es tambin donde se forma la fase |. Las dendritas
de la fase primaria son aisladas o protegidas de posteriores reacciones y se conservan
hasta temperatura ms bajas. Mientras tanto la fase | contina formndose a partir
del lquido. En estas condiciones la microestructura final consistir en dendritas de fase
o segregada, rodeadas por una capa peritctica de fase |.
El sistema Fe-C contiene una reaccin peritctica, a elevada temperatura, pero
por la gran difusividad del C a las temperaturas en que se sita se trata de una reaccin
muy rpida y todas las dendritas de fase o se convierten en austenita ms estable por
lo que esta reaccin no se tiene en cuenta en el estudio de estas aleaciones.
La figura 74 A muestra el diagrama de equilibrio de las aleaciones Ag-Sn. La lnea
azul marca la composicin de una aleacin Ag-16% en masa de Sn, situada a la derecha
de la composicin del peritctico. Esta composicin supone que en la reaccin
peritctica se consume la fase slida o. A temperaturas inferiores la fase lquida
solidifica como |, para, a menores temperaturas, transformarse en fase |. La fase
primaria que se forma desde la fase lquida, es la fase o que puede observarse en la
figura 74 B, como dendritas primarias, rodeadas por la fase | formada tanto por
reaccin peritctica como por solidificacin directa, quedando fase slida o sin
reaccionar. Se observa cmo sobre la superficie de las dendritas de la fase primaria se
ha producido la disolucin parcial de las dendritas, aunque no se pudo terminar la
reaccin peritctica. En este caso, el lquido remanente, durante el enfriamiento,
continua formando ms fase | en los espacios interdendrticos de la fase o. Las
reacciones peritcticas raramente se completan ya que la formacin de la fase | en la
interfase L/o separa est del lquido e impide su posterior crecimiento.
Figura 74. A) Diagrama de equilibrio Ag-Sn. B) Microestructura de la aleacin con 16% en masa de Sn
mostrando dendritas primarias de fase o rodeada de | en espacios interdendrticos.
Diferencias entre las estructuras eutcticas y peritcticas
Reduca (Recursos Educativos)
Serie Qumica de Materiales. 4 (3): 211-284, 2012
ISSN: 1989-5003
284
En la mayora de los casos ambas reacciones dan estructuras bifsicas o + |
aunque debido a su proceso de formacin las microestructuras son completamente
diferentes. En el caso del eutctico las dos fases se forman simultneamente a partir
del lquido, dando una microestructura de las dos fases finamente dispersas en sus
proporciones de equilibrio. En el caso de un peritctico en el que inicialmente se ha de
formar una fase primaria, que normalmente se forman dendritas y a partir de ella por
reaccin con el lquido, se forma la segunda fase. Las fases por tanto se forman
sucesivamente a partir del lquido, y casi nunca estn en sus proporciones de
equilibrio. Como hemos comentado, no se completan las reacciones peritcticas.
BIBLIOGRAFA DE CONSULTA
Calvo F.A. 1972. Metalografa prctica. Ed. Alhambra. Madrid
Chadwick G.A. 1972. Metallography of phase transformation. Butterwoths. London
Chalmers B. 1964. Principles of solidification. John Wiley & Sons.
Criado A. 2009. Aceros y fundiciones. Ed. On line
Dynys F. 2005. Structures Self-Assembled Through Directional Solidification. Glenn
Research Center. NASA
Guthy H. V. 2002 Evolution of the Eutectic Microstructure in Chemically Modified and
Unmodified Aluminum Silicon Alloys. Master Thesis. WORCESTER POLYTECHNIC
INSTITUTE.
Plapp M,. Karma A., 2002.Eutectic colony formation: A phase field study, Phys. Rev. E
66, 061608.
Martin J.W., Doherty R.D. 1976. Stability of microstructure in metallic systems.
Cambridge Solid State Series. Cambridge
Porter, D.A. and Easterling, K.E. 1992. Phase transformations in metals and alloys. 2nd
edition. Chapman & Hall, London.
Rostoquer W, Dvorak J.R. 1977. Interpretation of metallographic structures. Academic
Press. USA.
Recibido: 5 mayo 2011.
Aceptado: 25 febrero 2012.
Вам также может понравиться
- Monografia SolidificacionДокумент48 страницMonografia SolidificacionVeronica ValdezОценок пока нет
- Base Teorica Metafisica SOLIDIFICACIONДокумент6 страницBase Teorica Metafisica SOLIDIFICACIONZibor Alejandro Obreque LobosОценок пока нет
- Diagrama de FaseДокумент11 страницDiagrama de FaseAnonymous o5FX4oqBОценок пока нет
- Nucleacion, Crecimiento y SolidificaciónДокумент9 страницNucleacion, Crecimiento y SolidificaciónNatalia Estrada RamírezОценок пока нет
- Transformaciones de Fase o Cambios de EstadoДокумент7 страницTransformaciones de Fase o Cambios de EstadooswaldoОценок пока нет
- Solidificación Ui Nucleación MalnДокумент108 страницSolidificación Ui Nucleación MalnMiguel Angel López Navarrete100% (1)
- Diagrama de FaseДокумент25 страницDiagrama de FasegilbertoОценок пока нет
- II Trabajo de Cs de Los MaterialesДокумент8 страницII Trabajo de Cs de Los Materialesnoelyis camposОценок пока нет
- Diagramas de fases, reacciones y pruebas de durezaДокумент8 страницDiagramas de fases, reacciones y pruebas de durezaJuan Diego Riano MurciaОценок пока нет
- Libro Del Tratamiento TermicoДокумент166 страницLibro Del Tratamiento Termicopetete83% (12)
- Metalotecnia - Solidificación de AleacionesДокумент25 страницMetalotecnia - Solidificación de AleacionesRony FelicianoОценок пока нет
- DiagramadeFase-Fundamentos de MaterialesДокумент13 страницDiagramadeFase-Fundamentos de Materialeschristian fernandezОценок пока нет
- Diagrama de FasesДокумент31 страницаDiagrama de FasesIsabel Delta Calero LazoОценок пока нет
- Grupo 95Документ27 страницGrupo 95William CastilloОценок пока нет
- Tecnologia de Losmateriales 2.corte 10%Документ20 страницTecnologia de Losmateriales 2.corte 10%Miguel MontañoОценок пока нет
- HandbookДокумент277 страницHandbookAlecita GabyОценок пока нет
- Tema 13. Diagrama de Equilibrio Entre Fases.Документ18 страницTema 13. Diagrama de Equilibrio Entre Fases.demouroОценок пока нет
- Proiedades Sustacia PuraДокумент22 страницыProiedades Sustacia PuraFelipe Andres EspinozaОценок пока нет
- Diagrama de FaseДокумент5 страницDiagrama de FaseKevin Perez YalleОценок пока нет
- Informe Equilibrio Liquido VaporДокумент25 страницInforme Equilibrio Liquido VaporPaolo Guerra SteinОценок пока нет
- Sustancias PurasДокумент54 страницыSustancias PurasMayra Leal92% (13)
- Diagramas de fase y transiciones termodinámicasДокумент5 страницDiagramas de fase y transiciones termodinámicasJosue DávilaОценок пока нет
- Clasificacion Diagrama de FaseДокумент16 страницClasificacion Diagrama de FaseMaría Jose Aranza Morales PalafoxОценок пока нет
- Diagrama de Fase y FisicoquimicaДокумент4 страницыDiagrama de Fase y FisicoquimicaRonal Vásquez BautistaОценок пока нет
- Clase 06 - Metalurgia Fisica I - Modulo IДокумент19 страницClase 06 - Metalurgia Fisica I - Modulo IJordyn Gavidia RodriguezОценок пока нет
- Solidificación de Un Metal Puro (2009)Документ19 страницSolidificación de Un Metal Puro (2009)anggelo_0203Оценок пока нет
- Diagrama de FaseДокумент24 страницыDiagrama de Fasejulio gomezОценок пока нет
- Teoria de SolidificacionДокумент12 страницTeoria de SolidificacionJonathan Duchi OleasОценок пока нет
- Apunte 7 Diagramas de FaseДокумент18 страницApunte 7 Diagramas de FaseAdolfo Rojas ArellanoОценок пока нет
- Apunte 7 Diagramas de Fase PDFДокумент18 страницApunte 7 Diagramas de Fase PDFJaime MendozaОценок пока нет
- Laboratorio 4 - MaterialesДокумент17 страницLaboratorio 4 - MaterialesRoxana SánchezОценок пока нет
- SEMANA 04 - Equilibrio de Fases. Ecuación de Clapeyron. Regla de Trouton. Regla de La Palanca.Документ23 страницыSEMANA 04 - Equilibrio de Fases. Ecuación de Clapeyron. Regla de Trouton. Regla de La Palanca.Alcajer Miguel Alarcon EspinozaОценок пока нет
- Propiedades sustancias purasДокумент31 страницаPropiedades sustancias purasJavier Enrique Bermudez Daza100% (1)
- S8 L1.en - EsДокумент35 страницS8 L1.en - Esyeferson tamayoОценок пока нет
- SILIDIF U 3,4 2020mzoenvДокумент27 страницSILIDIF U 3,4 2020mzoenvFabio Alejandro Rodriguez RaudaОценок пока нет
- Apuntes Completos Temas 5-11Документ99 страницApuntes Completos Temas 5-11Lucía RodríguezОценок пока нет
- Laboratorio 2 Fisicoquimica IIДокумент17 страницLaboratorio 2 Fisicoquimica IIJose Manuel Benites Palomares100% (2)
- Sustancias puras y primera ley termodinámicaДокумент3 страницыSustancias puras y primera ley termodinámicaLuis Alberto Torres OchoaОценок пока нет
- 0005 - Solidificación de Los Metales - MZ NAV 2020Документ7 страниц0005 - Solidificación de Los Metales - MZ NAV 2020facundo batistaОценок пока нет
- Solidificación metalesДокумент32 страницыSolidificación metalesPablo Romero0% (1)
- Diagramas de FaseДокумент15 страницDiagramas de FaseDiego NogalesОценок пока нет
- Resumen de SolidificaciónДокумент36 страницResumen de SolidificaciónMiguel Angel López Navarrete100% (1)
- Capitulo V Transformaciones de Fase (Solidificación)Документ30 страницCapitulo V Transformaciones de Fase (Solidificación)danteОценок пока нет
- Suarez-Equilibrio de FasesДокумент14 страницSuarez-Equilibrio de FasesSusan Jeny Suarez AbadОценок пока нет
- Sistema binario paradiclorobenceno-naftalenoДокумент71 страницаSistema binario paradiclorobenceno-naftalenoMalu AisneОценок пока нет
- Traducción 1ciencias 2Документ10 страницTraducción 1ciencias 2Kevin ReascosОценок пока нет
- Energía en Los Cambios QuímicosДокумент12 страницEnergía en Los Cambios QuímicossofiaОценок пока нет
- SolidificacionДокумент65 страницSolidificacionGerman Van der OlguinОценок пока нет
- Gibbs Aliaciones Isoformas PDFДокумент7 страницGibbs Aliaciones Isoformas PDFAnderson Flores RiveraОценок пока нет
- Informe N°3 Sistema Binario-FISICOQUIMICAДокумент10 страницInforme N°3 Sistema Binario-FISICOQUIMICACarlos Bryan AvilaОценок пока нет
- Hierro CarburoДокумент17 страницHierro CarburoPeña Largo OzielОценок пока нет
- Unidad 2 TermodinamicaДокумент10 страницUnidad 2 TermodinamicaFilix QMОценок пока нет
- Actividad 10 Diagrama de FasesДокумент8 страницActividad 10 Diagrama de FasesCitlaly Montalvo100% (1)
- Separata #10 Principios y Fenomenos de SolidificaciónДокумент11 страницSeparata #10 Principios y Fenomenos de SolidificaciónrodrigoОценок пока нет
- Superficie P V TДокумент12 страницSuperficie P V TWilman Freddy Arista TafurОценок пока нет
- Construcción de diagramas de fasesДокумент6 страницConstrucción de diagramas de fasesJashmin Manhualaya YaurivilcaОценок пока нет
- Teoría Del Gas Real: La Relación Exacta Para Gases RealesОт EverandTeoría Del Gas Real: La Relación Exacta Para Gases RealesОценок пока нет
- U03 Ficha Resumen SeguridadДокумент1 страницаU03 Ficha Resumen SeguridadSebastianОценок пока нет
- Cai CaaДокумент6 страницCai CaasoinethОценок пока нет
- U03 Ficha Resumen SeguridadДокумент1 страницаU03 Ficha Resumen SeguridadSebastianОценок пока нет
- U03 Ficha Resumen SeguridadДокумент1 страницаU03 Ficha Resumen SeguridadSebastianОценок пока нет
- Un Solo ProblemaДокумент1 страницаUn Solo ProblemasoinethОценок пока нет
- Informe de Gestión Convenio UNEXPO SIDOR 2016Документ7 страницInforme de Gestión Convenio UNEXPO SIDOR 2016soinethОценок пока нет
- Carburizacin Atmsfera GaseosaДокумент47 страницCarburizacin Atmsfera GaseosasoinethОценок пока нет
- Mu Dislr PN PJ 2017Документ48 страницMu Dislr PN PJ 2017Mary Andreina Cote de TarabehОценок пока нет
- Lean Manufacturing PDFДокумент77 страницLean Manufacturing PDFHugo VentimigliaОценок пока нет
- Aceros InoxidablesДокумент40 страницAceros InoxidablesAtanacio Molina100% (2)
- Anteproyecto TematicasДокумент1 страницаAnteproyecto TematicassoinethОценок пока нет
- Manual de Practicas Profesionales de Pregrado 12dic2012Документ28 страницManual de Practicas Profesionales de Pregrado 12dic2012Hipolito GarciaОценок пока нет
- Tabla Conversion CompletaДокумент12 страницTabla Conversion CompletaPeter Harold El Tigre86% (64)
- 01 AspECTOSДокумент16 страниц01 AspECTOSsoinethОценок пока нет
- Pmi PprojectssДокумент10 страницPmi PprojectsssoinethОценок пока нет
- MemòriaДокумент71 страницаMemòriasoinethОценок пока нет
- 1.0.5 CódigoДокумент11 страниц1.0.5 CódigosoinethОценок пока нет
- Proceso de Reduccion DirectaДокумент9 страницProceso de Reduccion Directayehime1Оценок пока нет
- Guia para La Seleccion de Valvulas en La Conduccion de FluidosДокумент51 страницаGuia para La Seleccion de Valvulas en La Conduccion de FluidossoinethОценок пока нет
- Agrociencia Vol16 Num1 2012Документ211 страницAgrociencia Vol16 Num1 2012Andres PalaciosОценок пока нет
- OsmometriaДокумент21 страницаOsmometriaeduardoОценок пока нет
- Práctica Uso de La Reomolacha Como Indicador de PHДокумент10 страницPráctica Uso de La Reomolacha Como Indicador de PHSandra Liliana50% (10)
- Manual de elaboración de productos a partir del jitomateДокумент22 страницыManual de elaboración de productos a partir del jitomateJoséRomeroОценок пока нет
- PROBLEMAS DE CONTAMINACIÓN DEL AGUA para ImprimirДокумент12 страницPROBLEMAS DE CONTAMINACIÓN DEL AGUA para ImprimirFrank Mucha LopezОценок пока нет
- Unac Quimica ProblemasДокумент9 страницUnac Quimica ProblemasEduardo CastañedaОценок пока нет
- Validacion Sulfatos y CLДокумент87 страницValidacion Sulfatos y CLIngrid CarabaliОценок пока нет
- Microondas, Calentamiento Electrico, Inyeccion Alcalina yДокумент38 страницMicroondas, Calentamiento Electrico, Inyeccion Alcalina ySebastian Morales SuarezОценок пока нет
- Sustancias Puras y MezclasДокумент25 страницSustancias Puras y MezclasSilvana BastidaОценок пока нет
- 00-Calculos en Quimica Analitica - Skoog-9edДокумент20 страниц00-Calculos en Quimica Analitica - Skoog-9edMarcial Chicchi LlanosОценок пока нет
- Presión osmótica solución NaClДокумент17 страницPresión osmótica solución NaClmarcos abalОценок пока нет
- Soluciones ElectroliticasДокумент43 страницыSoluciones Electroliticaspikapika1996Оценок пока нет
- Quimica en Ejercicios2013 U6 - 2 PDFДокумент11 страницQuimica en Ejercicios2013 U6 - 2 PDFCelestte RodriguezОценок пока нет
- Cuadernillo Problemas Curso 2009-10Документ21 страницаCuadernillo Problemas Curso 2009-10Rafael Baena Sánchez0% (1)
- Producción de Mermeladas: Flujo y EscalasДокумент17 страницProducción de Mermeladas: Flujo y EscalasSimar Leaño PrietoОценок пока нет
- Licencias, Permisos, Autorizaciones y Concesiones AmbientalesДокумент29 страницLicencias, Permisos, Autorizaciones y Concesiones AmbientalesKevin DelacruzОценок пока нет
- Balance de Masa y Energia en Un Evaporador de Simple EfectoДокумент27 страницBalance de Masa y Energia en Un Evaporador de Simple EfectoVictor Camez91% (22)
- CUALITATIVA+1 Inicio de La Quimica AnaliticaДокумент29 страницCUALITATIVA+1 Inicio de La Quimica AnaliticaCbasRamirezPérezОценок пока нет
- Jorge González - Cálculo 1 PDFДокумент148 страницJorge González - Cálculo 1 PDFFidelHuamanAlarcon100% (1)
- Difusión gases líquidos sólidosДокумент29 страницDifusión gases líquidos sólidossabukdОценок пока нет
- Guia Laboratorio Extracción Por SolventesДокумент10 страницGuia Laboratorio Extracción Por SolventesMatias Esteban Cuevas Arce67% (3)
- Problemas 5Документ73 страницыProblemas 5Anderson ArandaОценок пока нет
- Proyecto Elaboracion de Una Bebida Tipo Nectar A Partir Del Guaraco (Reparado) 1Документ36 страницProyecto Elaboracion de Una Bebida Tipo Nectar A Partir Del Guaraco (Reparado) 1Cristian Aroni QuispeОценок пока нет
- Mermelada de Mango y MaracuyaДокумент13 страницMermelada de Mango y MaracuyaRegina Tacuche Ventura100% (1)
- (379258610) Quimica TVДокумент37 страниц(379258610) Quimica TVparvomoquilloОценок пока нет
- Teñido de Fibra AcrilicaДокумент28 страницTeñido de Fibra AcrilicaAlexis VelaОценок пока нет
- El Principio de Le Chatelier Establece Que Si Una Reacción en Equilibrio Es Perturbada Desde El ExteriorДокумент24 страницыEl Principio de Le Chatelier Establece Que Si Una Reacción en Equilibrio Es Perturbada Desde El ExteriorManuel Flores ÆОценок пока нет
- Agua y Sales Minerales (EJERCICIOS)Документ2 страницыAgua y Sales Minerales (EJERCICIOS)Jaime Herrera50% (2)
- Al Aire Libre de Interior A La Corrosión de Los Metales en Ambientes Costeros TropicalesДокумент30 страницAl Aire Libre de Interior A La Corrosión de Los Metales en Ambientes Costeros TropicalesJavier AyalaОценок пока нет
- Métodos Experimentales para Determinar Velocidades de ReacciónДокумент5 страницMétodos Experimentales para Determinar Velocidades de ReacciónAlina RamosОценок пока нет