Академический Документы
Профессиональный Документы
Культура Документы
Enzimas Cinetica Enzimatica
Загружено:
raul18010 оценок0% нашли этот документ полезным (0 голосов)
11 просмотров31 страницаОригинальное название
Enzimas_Cinetica_Enzimatica
Авторское право
© Attribution Non-Commercial (BY-NC)
Доступные форматы
PDF, TXT или читайте онлайн в Scribd
Поделиться этим документом
Поделиться или встроить документ
Этот документ был вам полезен?
Это неприемлемый материал?
Пожаловаться на этот документАвторское право:
Attribution Non-Commercial (BY-NC)
Доступные форматы
Скачайте в формате PDF, TXT или читайте онлайн в Scribd
0 оценок0% нашли этот документ полезным (0 голосов)
11 просмотров31 страницаEnzimas Cinetica Enzimatica
Загружено:
raul1801Авторское право:
Attribution Non-Commercial (BY-NC)
Доступные форматы
Скачайте в формате PDF, TXT или читайте онлайн в Scribd
Вы находитесь на странице: 1из 31
Enzimas
Las Enzimas Son Catalizadores
Poderosos
Enzimas son protenas que pueden acelerar
reacciones bioqumicas en factores de 10
5
to
10
17
! Esto es mucho mayor que catalizadores
qumicos.
Enzimas pueden ser extremadamente
especficas en trminos de sustratos y
productos en las reacciones.
Enzimas catalizan reacciones bajo condiciones
moderadas (e.g. pH 7.4, 37C).
La actividad cataltica de muchas enzimas
pueden ser regulada por efectore alostricos.
Caractersticas
Casi todas enzimas son protenas.
Son termosensibles
Son hidrosolubles
Pueden ser precipitadas por reactivos que precipitan las
protenas
Contienen el 16% de su peso como nitrgeno.
Clasificacin
Nombres caprichosos.
Pepsina, tripsina, quimotripsina.
Luego se agrego el sufijo asa.
En funcin de la reaccin que catalizan o el sustrato
sobre el cual actan.
Lactasa acta sobre su sustrato lactosa.
Clasificacin
La Unin Internacional de Bioqumica y Biologa
Molecular (IUBMB).
Sistema de nomenclatura para las enzimas.
El nombre comienza con EC,
Primer digito representa la clase
Segundo digito significa la subclase
Tercer digito es la subsubclase o subgrupo
Cuarto digito da el numero de la enzima particular en la
lista
Clasificacin
1. Oxidorreductasas: Transferencia de hidrgeno o
adicin de oxigeno. (Lactato deshidrogenasa)
2. Transferasas: Transferencia de grupos diferentes del
hidrgeno. (aminotranferasas)
3. Hidrolasas: Ruptura de enlace con adicin de agua.
(Tripsina)
4. Liasas: Ruptura sin adicin de agua. (Aldolasa)
5. Isomerasas: Transferencia intramolecular. (triosa
fosfato isomerasa)
6. Ligasas: Condensacin de dos molculas ATP
dependiente. (acetil CoA carboxilasa)
Ejemplo
Alcohol deshidrogenasa
Alcohol-NAD-oxidorreductasa (IUBMB)
EC.1.1.1.1
Diagramas de Energa Libre
K
eq
= e
G/RT
For A A
[A]
/[A]
o
= e
G/RT
[A]
= [A]
o
e
G/RT
K
eq
= constante de equilibrio
[A]
= concentracion de las moleculas con la energia de activacion
[A]
o
= concentration total
G
= cambio en la energia libre estandar de la energia de activacion
Efecto de un Catalizador en la Energa de
Activacin
Catalizador no afecta G
A
(inicial) o G
B
(final) por lo que no afectan el cambio de
enregia libre (G = G
B
- G
A
) o la constante de equilibrio K
eq
.
Concentracion en el equilibrio de A y B es determinada por el cambio en energia
libre.
Catalizadores solamente afectan G
, disminuyendo la energia de activacion.
Aceleran ambos sentidos de las reacciones en sentido hacia la derecha y la
reaccion inversa (incrementando la constante cinetica k
1
and k
-1
).
Intermediarios en una Reaccion de
Multiples Pasos
Cintica Enzimtica
Efecto de la Concentracion del Sustrato
en la Velocidad de Reaccion
Cintica de Michaelis-Menten (1)
v = k
2
[ES]
(Nota: k
2
tambien se le llama k
cat
)
[Enzima]
total
= [E]
t
= [E] + [ES]
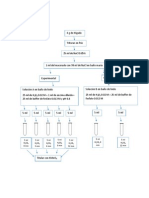
Como encontrar [ES]?
1. Asumir el equilibrio, si k
-1
>> k
2
:
K
S
= k
-1
/k
1
= [E][S]/[ES]
or
2. Asumir estado estacionario:
d[ES]/dt = 0
(Michaelis y
Menten, 1913)
(Briggs y
Haldane, 1925)
E = enzima, S = sustrato,
ES = complejo enzima-sustrato,
P = producto
Cintica del Estado Estacionario en
Enzimas
Nota: Esto significa que v en
v = k
2
[ES] debe ser la
velocidad inicial, v
o
, la
velocidad de la reaccion
despues del estado pre-
estacionario y al inicio del
estado estacionario, i.e.,
antes de que ~10% del
sustrato sea convertido a
producto.
Cintica de Michaelis-Menten Continua (2)
Porque se asume el estado estacionario:
d[ES]/dt = k
-1
[ES] + k
2
[ES] - k
1
[E][S] = 0
Por lo que: k
1
[E][S] = k
-1
[ES] + k
2
[ES]
Rearreglo: [ES] = (k
1
/(k
-1
+ k
2
))[E][S]
Sustituyendo (constante de Michaelis = K
M
= (k
-1
+ k
2
)/k
1
) = K
S
+ k
2
/k
1
:
[ES] = ([E][S])/K
M
Entonces:
K
M
[ES] = [E][S]
Cintica de Michaelis-Menten Continua (3)
Sustituyendo ([E] = [E]
t
- [ES]):
K
M
[ES] = [E]
t
[S] - [ES][S]
Rearreglo: [ES](K
M
+ [S]) = [E]
t
[S]
Entonces: [ES] = [E]
t
[S]/(K
M
+ [S])
Ahora podemos sustituir por [ES] en la ecuacion de
velociad v
o
= k
2
[ES], entonces
Ecuacion de Michaelis-Menten
v
o
= k
2
[E]
t
[S]/(K
M
+ [S])
or
v
o
= V
max
[S]/(K
M
+ [S])
(Ya que V
max
= k
2
[E]
t
cuando [S] >> K
M
)
Lineweaver-Burk (Doble Reciproco)
Eadie-Hofstee
Reaccion de Multiples Pasos
E + S ES EP E + P
v
o
= k
cat
[E]
t
[S]/(K
M
+ [S])
k
2
k
3
k
1
k
-1
(k
cat
= constante de velocidad
general que incorpora k
2
y
k
3
)
Eficiencia Catalitica (k
cat
/K
M
)
=> Enzima Perfecta
Limite de reaccion
controlada por Difusion:
10
8
-10
9
M
-1
s
-1
Preferencia de
sustrato de la
quimotripsina
Dependencia del pH para la Actividad de
la Enzima
Reacciones de Bisustratos Catalizadas
por Enzimas: Dos Ejemplos
Reacciones de Bisustratos
S1 + S2 P1 + P2
A-X + B A + B-X (en reacciones de
transferasas)
Union secuencial de S1 y S2 antes de la catalisis:
Union aleatoria del sustrato Ya sea S1 o S2
pueden enlazarse primero, y luego el otro se une.
Union ordenada del sustrato - S1 debe unirse
primero que S2.
Reaccion de Ping Pong primero S1 P1, P1 es
liberado antes de que S2 se una, entonces S2 P2.
E
E
Reaccion de Ping Pong
Union secuencial
Complejo Ternario
Indicativo de la formacion de un complejo ternario y un
mecanismo secuencial
Indicativo de un mecanismo de Ping Pong
Вам также может понравиться
- Ecoli Bacterias Termo PDFДокумент1 страницаEcoli Bacterias Termo PDFraul1801Оценок пока нет
- PeroxidoДокумент1 страницаPeroxidoraul1801Оценок пока нет
- Gluconeogénesis, Síntesis y Degradacion de Glucógeno y Vía de Las Pentosas de Fosfato - 2Документ15 страницGluconeogénesis, Síntesis y Degradacion de Glucógeno y Vía de Las Pentosas de Fosfato - 2raul1801Оценок пока нет
- RMN & Rayos-XДокумент10 страницRMN & Rayos-Xraul1801Оценок пока нет
- Métodos Extracción ADNДокумент5 страницMétodos Extracción ADNraul1801Оценок пока нет
- 4 AphycomplexasДокумент0 страниц4 Aphycomplexasraul1801Оценок пока нет
- Membranas 2Документ8 страницMembranas 2raul1801Оценок пока нет
- Membranas Transporte 2Документ21 страницаMembranas Transporte 2raul1801Оценок пока нет
- Tema 6. Las RodófitasДокумент24 страницыTema 6. Las Rodófitasraul1801Оценок пока нет
- ManualДокумент218 страницManualraul1801Оценок пока нет
- Tema 13b. Monilophyta - Marattiopsida - PolypodiopsidaДокумент45 страницTema 13b. Monilophyta - Marattiopsida - Polypodiopsidaraul18010% (1)
- CelenteradosДокумент2 страницыCelenteradosraul1801Оценок пока нет
- Degradación de Polifenoles Por Procesos de Oxidación AvanzadaДокумент15 страницDegradación de Polifenoles Por Procesos de Oxidación AvanzadaRicardo GamarraОценок пока нет
- Ejercicios de OrganicaДокумент2 страницыEjercicios de OrganicaMayra MartinezОценок пока нет
- Evaluación Continua 1 Arnold AlejandroДокумент2 страницыEvaluación Continua 1 Arnold AlejandroMrChemy3Оценок пока нет
- Accion de Una Enzima de Tejidos Vegetales y AnimalesДокумент10 страницAccion de Una Enzima de Tejidos Vegetales y AnimalesJodie Rey Romero100% (1)
- MetanolДокумент14 страницMetanolTony PalacioОценок пока нет
- Guía #2 Cinética Enzimática 2020Документ6 страницGuía #2 Cinética Enzimática 2020tomas contrerasОценок пока нет
- Polimerización de Etileno y Esencia de Trementina Con Un Sistema Catalítico Tipo Ziegler PDFДокумент71 страницаPolimerización de Etileno y Esencia de Trementina Con Un Sistema Catalítico Tipo Ziegler PDFNicandroGonzalesОценок пока нет
- Estudio de Los Alquinos-Reacciones QuímicasДокумент18 страницEstudio de Los Alquinos-Reacciones QuímicasCAMILA KARELIS HURTADO ILIGUANОценок пока нет
- Biocatálisis Clase 1 PDFДокумент19 страницBiocatálisis Clase 1 PDFAlejandraОценок пока нет
- Métodos de limpieza y reutilización de catalizadores automotricesДокумент5 страницMétodos de limpieza y reutilización de catalizadores automotricesLuis Javier Montes SalazarОценок пока нет
- Trabajo 2Документ2 страницыTrabajo 2Lizeth Martinez RamirezОценок пока нет
- HIDROGENOДокумент88 страницHIDROGENOJayRo HdezОценок пока нет
- Manual VictorДокумент84 страницыManual VictorJose Eusebio Caro Pacheco80% (5)
- Unidad IV - Parte 2Документ17 страницUnidad IV - Parte 2altagraciaОценок пока нет
- Tecnicas de Analisis y Caracterizacion de MaterialДокумент16 страницTecnicas de Analisis y Caracterizacion de MaterialSergio AlexanderОценок пока нет
- Proyecto de MetanolДокумент55 страницProyecto de MetanolJean Wilmer G HОценок пока нет
- Resumen Analitico en Educacion RaeДокумент8 страницResumen Analitico en Educacion RaeJorge Alberto Carrillo BernalОценок пока нет
- Transferencia de masa en problemas de difusión y reacciónДокумент13 страницTransferencia de masa en problemas de difusión y reacciónKatherine CuevaОценок пока нет
- Hidrólisis y fermentación de biomasaДокумент2 страницыHidrólisis y fermentación de biomasaRicardo HernandezОценок пока нет
- Tarea 2.0 PDFДокумент8 страницTarea 2.0 PDFJean MarcoОценок пока нет
- Estil BencenoДокумент9 страницEstil BencenoMoises Valdivia BaldomeroОценок пока нет
- Syllabus EIQ447 2s 2019Документ7 страницSyllabus EIQ447 2s 2019Elías SepúlvedaОценок пока нет
- Informacion de YesoДокумент14 страницInformacion de YesoShaolin FrankОценок пока нет
- 5to Informe de Laboratorio de Quimica OrganicaДокумент14 страниц5to Informe de Laboratorio de Quimica OrganicaKatty AtocheОценок пока нет
- Determinación de azufre en hidrocarburosДокумент8 страницDeterminación de azufre en hidrocarburosBrenda Rubí Hdz BetancourtОценок пока нет
- Saúl Uriel Corona Bautista Problemas de Cinética EnzimáticaДокумент10 страницSaúl Uriel Corona Bautista Problemas de Cinética EnzimáticaSaúl Uriel Corona Bautista100% (1)
- ¿En Toda Reacción Enzimática Hay Liberación de Energía - Prácticas o Problemas - Andresfrn09Документ4 страницы¿En Toda Reacción Enzimática Hay Liberación de Energía - Prácticas o Problemas - Andresfrn09Kelly BenitezОценок пока нет
- Problemario Capítulo 3 Ingeniería de Procesos MicrobiológicosДокумент10 страницProblemario Capítulo 3 Ingeniería de Procesos MicrobiológicosKenia CarrilloОценок пока нет
- Tratamiento de EnzimasДокумент6 страницTratamiento de EnzimasRaithismer MarinОценок пока нет
- Reacciones de aldehídos y cetonas con aminasДокумент10 страницReacciones de aldehídos y cetonas con aminasdugamianОценок пока нет