Академический Документы
Профессиональный Документы
Культура Документы
Determinacion de Iones Sulfato
Загружено:
Manuela MendozaИсходное описание:
Авторское право
Доступные форматы
Поделиться этим документом
Поделиться или встроить документ
Этот документ был вам полезен?
Это неприемлемый материал?
Пожаловаться на этот документАвторское право:
Доступные форматы
Determinacion de Iones Sulfato
Загружено:
Manuela MendozaАвторское право:
Доступные форматы
UNIVERSIDAD NACIONAL DE TRUJILLO
FACULTAD DE INGENIERIA QUIMICA
DETERMINACIN DE IONES SULFATO POR ESPECTROFOTOMETRA MOLECULAR
1. Objetivo a) Determinar por espectrofotometra molecular la cantidad de iones sulfato que contiene una muestra de agua. 2. Fundamento terico
Al igual que los cloruros, el contenido en sulfatos de las aguas naturales es muy variable y puede ir desde muy pocos miligramos por litro hasta cientos de miligramos por litros. Los sulfatos pueden tener su origen en que las aguas atraviesen terrenos ricos en yesos o a la contaminacin con aguas residuales industriales. El contenido de sulfatos no suele presentar problema de potabilidad a las aguas de consumo pero, en ocasiones, contenidos superiores a 300 mg/l pueden ocasionar trastornos gastrointestinales en los nios. Se sabe que los sulfatos de sodio y magnesio pueden tener accin laxante, por lo que no es deseable un exceso de los mismos en las aguas de bebida. La determinacin del contenido de sulfatos puede hacerse por diferentes mtodos. Uno de ello es el Test rpido de sulfatos. El Mtodo gravimtrico, mediante precipitacin con cloruro de bario, es un mtodo muy preciso y aplicable a concentraciones superiores a 10 mg/l. Los resultados previamente precipitados con cloruro de bario, en medio cido, son secados a 110C y calcinados a 600C. El Mtodo nefelomtrico, mediante turbidmetro nefelomtrico, es menos preciso que el gravimtrico para concentraciones inferiores a 10 mg/l. Se recomienda, preferentemente, para la determinacin de sulfatos en aguas con contenidos superiores a 60 mg/l y siempre que se disponga de turbidmetro. Este mtodo no es recomendable para aguas con color, materias en suspensin o con elevado contenido en materias orgnicas. El ion sulfato SO42- precipita, en un medio de cido actico, con ion Ba 2+de modo que forma cristales de sulfato de bario BaSO4 de tamao uniforme, los que deben mantenerse en suspensin homognea durante un periodo de tiempo que resulte suficiente para medir la absorbancia que la misma produzca. El contenido de SO42- de cada muestra se obtiene a partir de la curva de calibrado previamente obtenida.
LABORATORIO
ANALISIS QUIMICO INSTRUMENTAL
UNIVERSIDAD NACIONAL DE TRUJILLO
FACULTAD DE INGENIERIA QUIMICA
En esta tcnica interfieren fundamentalmente el color y la turbidez. Esta puede eliminarse por filtracin o centrifugacin. La interferencia del color puede soslayarse utilizando la muestra coloreada como testigo, a la que o se le agrega reactivo de la disolucin precipitante de bario, o empleando como instrumento de medida un nefelmetro de doble posicin de cubeta, con lo que elimina la influencia del color. Otra interferencia es la materia suspendida en gran cantidad. Parte de la materia en suspensin puede ser eliminada por filtracin. Interferir tambin un exceso de slice superior a 500 mg/l, y en las aguas con gran cantidad de materia orgnica puede no ser posible precipitar el BaSO4 satisfactoriamente.
3. Reactivos, Materiales y Equipos a. Na2SO4(s) QP; HCl cc; glicerina; alcohol etlico; NaCl(s) QP; BaCl22H2Cl2(s) QP b. Vasos de precipitacin de 250 mL; fiolas de 250 mL y 50 mL; embudo; papel de filtro. c. Espectrofotmetro UV/Vis de HP 8452
4. Procedimiento Preparacin de soluciones a. Solucin estndar de 1000,0 mg SO42- /L: pesar 0,4438 g de Na2SO4 en una balanza analtica, depositarla en un vaso de 250,0 mL, diluirla con agua y transferirla a una fiola de 250,0 mL donde se afora con agua. b. Solucin estndar diluida de 100,0 mg SO42-/L: en una fiola de 100,0 mL depositarla exactamente 10,0 mL de la solucin estndar de (a.) y aforar con agua. c. Solucin A: en un vaso de precipitacin se disuelven 60,0 g de NaCl en 200 mL de agua, se aaden 5,0 mL de HCl cc y se afora con agua en una fiola de 250,0 mL. d. Solucin B: diluir 50 mL de glicerina con 100 mL de alcohol etlico absoluto.
LABORATORIO
ANALISIS QUIMICO INSTRUMENTAL
UNIVERSIDAD NACIONAL DE TRUJILLO
FACULTAD DE INGENIERIA QUIMICA
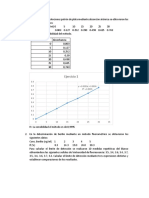
5. Clculos Datos obtenidos experimentalmente:
MUESTRA 1 2 3 4 5 PROMEDIO
ABSORBANCIA 0.173 0.160 0.162 0.180 0.169 0.169
a. La concentracin de iones sulfato en las muestras: empleando la ecuacin de la curva de calibracin o la grfica de la curva de calibracin encontramos la concentracin de la muestra diluida Cm. Luego las concentraciones de la muestra son: mg de SO42- /L = ___________ x (50,0 mL / 25,0 mL) = _______
LABORATORIO
ANALISIS QUIMICO INSTRUMENTAL
UNIVERSIDAD NACIONAL DE TRUJILLO
FACULTAD DE INGENIERIA QUIMICA
ESQUEMA EXPERIMENTAL:
Pesamos 0,1470 g de Na2SO4 en una balanza analtica, depositamos en un vaso de 250 mL. En una fiola de 100,0 mL depositamos 10 mL de la solucin estndar de (a.) y aforamos con agua.
Diluimos con agua y transferimos a una fiola de 250 mL donde aforamos con agua.
Diluimos 50 mL de glicerina con 100 mL de alcohol etlico absoluto.
En un vaso de precipitacin se disuelven 60,0 g de NaCl en 200 mL de agua.
Aadimos 5 mL de HCl 0,0858 M y aforamos con agua en una fiola de 250 mL.
LABORATORIO
ANALISIS QUIMICO INSTRUMENTAL
Вам также может понравиться
- Determinación de Sulfatos en Aguas Por Método Espectrofotometrico.Документ5 страницDeterminación de Sulfatos en Aguas Por Método Espectrofotometrico.anon_653229726100% (2)
- Practican 7 MuestreoypreservacionДокумент7 страницPractican 7 MuestreoypreservacionMARIA DEL PILAR VILCHEZ MOLINAОценок пока нет
- Informe 12 - Dureza Cálcica y Total - González, Elizabeth - Paralelo 101Документ8 страницInforme 12 - Dureza Cálcica y Total - González, Elizabeth - Paralelo 101Elizabeth González DíazОценок пока нет
- Potenciometría y ConductimetríaДокумент30 страницPotenciometría y ConductimetríaAxel TuyubОценок пока нет
- 12.1 Biorecuperación en Vía SólidaДокумент24 страницы12.1 Biorecuperación en Vía SólidaCHRISTHIAN ALEJANDRO RAMOS ROSASОценок пока нет
- Determinación de Cloruros en Una Muestra de Agua de Mar A Través Del Método de MohrДокумент7 страницDeterminación de Cloruros en Una Muestra de Agua de Mar A Través Del Método de MohrMaximiliano GuanipaОценок пока нет
- Experimento Del CalorimetroДокумент2 страницыExperimento Del CalorimetromarymoareОценок пока нет
- Informe Determinacion de Materia OrganicaДокумент8 страницInforme Determinacion de Materia OrganicaSandra Gutiérrez AcostaОценок пока нет
- Informe N°9 Determinación de ClorurosДокумент16 страницInforme N°9 Determinación de ClorurosRonyОценок пока нет
- Informe de Laboratorio - Grupo 2 Métodos InstrumentalesДокумент31 страницаInforme de Laboratorio - Grupo 2 Métodos InstrumentalesMaryori C. Kimarath Reyes RodriguezОценок пока нет
- Síntesis de Alumbre A Partir de Latas de AluminioДокумент7 страницSíntesis de Alumbre A Partir de Latas de Aluminiofernanda oviedoОценок пока нет
- Informe Laboratorio Kps (Constante de Equilibrio)Документ3 страницыInforme Laboratorio Kps (Constante de Equilibrio)Sara CatañoОценок пока нет
- Informe 1 de BiotecnologiaДокумент9 страницInforme 1 de BiotecnologiaROSMERYОценок пока нет
- Para EjerciciosДокумент3 страницыPara EjerciciosGonzalo GarciaОценок пока нет
- Laboratorio KMnO4Документ10 страницLaboratorio KMnO4AndresОценок пока нет
- Informe 9Документ9 страницInforme 9Marcela QuijanoОценок пока нет
- Informes de Quimica BazanДокумент42 страницыInformes de Quimica BazanKevin Pablo Meruvia PintoОценок пока нет
- Ejercicio 1y 2 de CurvasДокумент2 страницыEjercicio 1y 2 de CurvasNatasha VargasОценок пока нет
- Analítica Práctica 5. Determinación de Cloruros en Aguas NaturalesДокумент12 страницAnalítica Práctica 5. Determinación de Cloruros en Aguas NaturalesGianela Vega PinedoОценок пока нет
- Guia 5 - Od - Dqo - DboДокумент27 страницGuia 5 - Od - Dqo - Dboanon_362115992Оценок пока нет
- Espectrofotometrà A - UV - Análisis de Nitratos en AguaДокумент16 страницEspectrofotometrà A - UV - Análisis de Nitratos en AguaLuis Diego Cardenas PadillaОценок пока нет
- Práctica 8 - Volumetría RedoxДокумент3 страницыPráctica 8 - Volumetría RedoxLady GiraldoОценок пока нет
- Práctica Columna WinogradskyДокумент12 страницPráctica Columna WinogradskyIvan Ruiz100% (1)
- Examen BME U II 2020 IДокумент2 страницыExamen BME U II 2020 IGian Carlos Joel CAIRO GONZALEZОценок пока нет
- Interferómetro de MichelsonДокумент2 страницыInterferómetro de MichelsonFrank HurtadoОценок пока нет
- Extracción Líquido-Líquido Seminario de QuimicaДокумент14 страницExtracción Líquido-Líquido Seminario de QuimicadipamgmaОценок пока нет
- Determinación Del Contenido de Ácido Tartárico en Una Muestra de VinoДокумент1 страницаDeterminación Del Contenido de Ácido Tartárico en Una Muestra de VinoOriana Salas100% (1)
- Laboratorio Fotometria de LlamaДокумент13 страницLaboratorio Fotometria de LlamaNehemias Ruiz mamaniОценок пока нет
- Practica de Laboratorio No 4 Determinación de Cloruro en AguaДокумент3 страницыPractica de Laboratorio No 4 Determinación de Cloruro en AguaIsabel Tacunan CastilloОценок пока нет
- Determinación de La Conductividad Eléctrica en Líquidos AlimenticiosДокумент8 страницDeterminación de La Conductividad Eléctrica en Líquidos AlimenticiosAlba Ximena Quispe MartinezОценок пока нет
- INFORME de AQ 1 Solidos Totales DisueltosДокумент14 страницINFORME de AQ 1 Solidos Totales DisueltosFlavio CacataОценок пока нет
- PrecipitacionДокумент23 страницыPrecipitacionRonal Michel CallejasОценок пока нет
- Análisis Prueba de Fehling y Tollen's - WPS OfficeДокумент3 страницыAnálisis Prueba de Fehling y Tollen's - WPS OfficeJohan CárdenasОценок пока нет
- Deber Quimica AnaliticaДокумент8 страницDeber Quimica AnaliticaFabian Cabrera GuerraОценок пока нет
- Infografía - Demanda Bioquímica de Oxigeno DBO (Ingeniería Ambiental)Документ1 страницаInfografía - Demanda Bioquímica de Oxigeno DBO (Ingeniería Ambiental)José Joaquín Urbina MontesОценок пока нет
- Volumetría de NeutralizaciónДокумент5 страницVolumetría de Neutralizaciónsern03Оценок пока нет
- DecoloraciónДокумент7 страницDecoloraciónluceroОценок пока нет
- Determinacion Del Porcentaje de Hidratacion de Un CompuestoДокумент7 страницDeterminacion Del Porcentaje de Hidratacion de Un CompuestoDaniel DazaОценок пока нет
- Informe N°8 de Análisis - Sólidos - Grupo N°7 (21Документ23 страницыInforme N°8 de Análisis - Sólidos - Grupo N°7 (21DIANA ESTHEFANY MORI SOLANOОценок пока нет
- Informe - Preparacion y Valoracion NaOH 0,10000 NДокумент10 страницInforme - Preparacion y Valoracion NaOH 0,10000 NPEREDA UTRILLA MANUEL ALEXANDER0% (2)
- 1.informe de Destilación FraccionadaДокумент9 страниц1.informe de Destilación FraccionadaSacha OrdazОценок пока нет
- LAB 1 - PH, Color, Turbidez y ConductividadДокумент10 страницLAB 1 - PH, Color, Turbidez y ConductividadRIKMATT100% (1)
- Aplicaciones de Las Titulaciones PotenciométricasДокумент8 страницAplicaciones de Las Titulaciones Potenciométricas708170Оценок пока нет
- Seminario 6 GRUPO 6Документ14 страницSeminario 6 GRUPO 6Pamela MamaniОценок пока нет
- Cinetica DBOДокумент11 страницCinetica DBOJRОценок пока нет
- Informe 4 Actividad Enzimatica en Procesos de TransformacionДокумент23 страницыInforme 4 Actividad Enzimatica en Procesos de TransformacionMoni AntolinezОценок пока нет
- Determinacion de Calcio y Magnesio (ANALITICA) InformeДокумент12 страницDeterminacion de Calcio y Magnesio (ANALITICA) InformeDixon LealОценок пока нет
- Un 8 Problema 4 YmДокумент7 страницUn 8 Problema 4 Ymalein100% (1)
- Laboratorio Nº13-Fotometría de LlamaДокумент3 страницыLaboratorio Nº13-Fotometría de LlamaRodrigo Morales100% (2)
- Informe AlcalinidadДокумент16 страницInforme AlcalinidadPiky96100% (1)
- Informe de Laboratorio-Filtro Percolador-Mesa 3Документ14 страницInforme de Laboratorio-Filtro Percolador-Mesa 3Sebastian CarvajalОценок пока нет
- Informe Practica DqoДокумент8 страницInforme Practica DqowilmerОценок пока нет
- Informe YodometriaДокумент8 страницInforme YodometriaEmiliano Picconi0% (1)
- Ejercicios 4. Complejometría PDFДокумент2 страницыEjercicios 4. Complejometría PDFJuliana PNОценок пока нет
- Determinación de Carbonatos y Bicarbonatos 2Документ3 страницыDeterminación de Carbonatos y Bicarbonatos 2GermanBrassiniОценок пока нет
- Metodo MohrДокумент2 страницыMetodo MohrEdgar Pineda50% (2)
- CURVA TITULACION NH3 HCLДокумент2 страницыCURVA TITULACION NH3 HCLArmando MoraОценок пока нет
- Problema. Ecuaciones de Estado Muñoz Ortiz Erick RaphaelДокумент3 страницыProblema. Ecuaciones de Estado Muñoz Ortiz Erick RaphaelRaul JesusОценок пока нет
- Practica de Laboratorio #7 SulfatosДокумент16 страницPractica de Laboratorio #7 SulfatosMaileeBathshebaDelgadoCamiloОценок пока нет
- Determinación de SulfatosДокумент7 страницDeterminación de SulfatosEdson DeschanelОценок пока нет
- Lima - Perú, Setiembre 2018Документ28 страницLima - Perú, Setiembre 2018Manuela MendozaОценок пока нет
- 7 Libros para Tu Fortaleza MentalДокумент9 страниц7 Libros para Tu Fortaleza MentalManuela MendozaОценок пока нет
- CatálogoДокумент14 страницCatálogoManuela MendozaОценок пока нет
- Programa GMM 2022Документ20 страницPrograma GMM 2022Manuela MendozaОценок пока нет
- Procedimiento para La Conexión Del Tanque Criogenico Al IcpДокумент2 страницыProcedimiento para La Conexión Del Tanque Criogenico Al IcpManuela MendozaОценок пока нет
- La Reactividad Materia PrimaДокумент1 страницаLa Reactividad Materia PrimaManuela MendozaОценок пока нет
- Preparación LechadaДокумент1 страницаPreparación LechadaManuela MendozaОценок пока нет
- Ing - Quimica Manuela MendozaДокумент1 страницаIng - Quimica Manuela MendozaManuela MendozaОценок пока нет
- Mineria ODSДокумент48 страницMineria ODSManuela MendozaОценок пока нет
- CaratulaДокумент8 страницCaratulaManuela MendozaОценок пока нет
- Sistema TetragonalДокумент11 страницSistema TetragonalManuela MendozaОценок пока нет
- Resumen ReactividadДокумент3 страницыResumen ReactividadManuela MendozaОценок пока нет
- Ing - Quimica - Manuela Mendoza PDFДокумент2 страницыIng - Quimica - Manuela Mendoza PDFManuela MendozaОценок пока нет
- ANEXOS Educación AmbientalДокумент11 страницANEXOS Educación AmbientalManuela Mendoza100% (1)
- Guía Rápida Básica de AutoCAD PDFДокумент57 страницGuía Rápida Básica de AutoCAD PDFWilder Rimac MendezОценок пока нет
- Problemas Economia de ProcesosДокумент6 страницProblemas Economia de ProcesosManuela MendozaОценок пока нет
- Movimiento Rectilineo UniformeДокумент5 страницMovimiento Rectilineo UniformeManuela MendozaОценок пока нет
- Proyección SocialДокумент3 страницыProyección SocialManuela MendozaОценок пока нет
- Relleno Sanitario Semi MecanicoДокумент28 страницRelleno Sanitario Semi MecanicoManuela MendozaОценок пока нет
- Industria Del PotasioДокумент12 страницIndustria Del PotasioManuela MendozaОценок пока нет
- Gardnerella VaginalisДокумент11 страницGardnerella VaginalisVictor Pier Chuquipoma RojasОценок пока нет
- Examen Farmacología 1Документ10 страницExamen Farmacología 1Ricardo HernándezОценок пока нет
- Viscosidad de Masa de Pan - En.esДокумент7 страницViscosidad de Masa de Pan - En.esIvan Quispe TiconaОценок пока нет
- Los Componentes de La Inyección de Combustible y de OperaciónДокумент29 страницLos Componentes de La Inyección de Combustible y de Operaciónmanuel panchoОценок пока нет
- Qué Es La PorfiriaДокумент6 страницQué Es La PorfiriaYessica GuerreroОценок пока нет
- Agri 1991 708 636 638Документ3 страницыAgri 1991 708 636 638ooteropraviaОценок пока нет
- LubricantsДокумент21 страницаLubricantsFrancisco RománОценок пока нет
- MSDS Cherteston 274Документ8 страницMSDS Cherteston 274Italo JaureguiОценок пока нет
- Brochure Sika La Solución Efectiva para Su ObraДокумент8 страницBrochure Sika La Solución Efectiva para Su ObraJOHNNY CASTILLO LAGOSОценок пока нет
- Grupo Contra Incendios KRIPFIREДокумент20 страницGrupo Contra Incendios KRIPFIREpano356Оценок пока нет
- C11 - Fisiología Del Ejercicio 3 - Sistemas de Producción de EnergíaДокумент25 страницC11 - Fisiología Del Ejercicio 3 - Sistemas de Producción de EnergíaCarlos Alberto AcevedoОценок пока нет
- DolorДокумент3 страницыDolorJuan Martín Loli VillarrealОценок пока нет
- Procedimiento Determinación Cafeina en Bebidas EnergeticasДокумент2 страницыProcedimiento Determinación Cafeina en Bebidas EnergeticasSantiago CorreaОценок пока нет
- Fundición GrisДокумент3 страницыFundición GrislollihopОценок пока нет
- Top Diez Perfumes de Mujer Más Vendidos en Dos Mil QuinceДокумент2 страницыTop Diez Perfumes de Mujer Más Vendidos en Dos Mil Quinceclassysemester449Оценок пока нет
- Informe Final Del Internado - Chero Juarez Cinthia 2018.Документ49 страницInforme Final Del Internado - Chero Juarez Cinthia 2018.CalleNuñezCarlosJuanОценок пока нет
- Entregable 2Документ5 страницEntregable 2Sandra GutiérrezОценок пока нет
- GOLFIELDДокумент27 страницGOLFIELDJessi Gálvez ChávezОценок пока нет
- Acidos CarboxilicosДокумент7 страницAcidos CarboxilicosRosi MeraОценок пока нет
- Biosintesis de Acidos GrasosДокумент16 страницBiosintesis de Acidos GrasosCarolinamcr95Оценок пока нет
- Isosorbide DinitratoДокумент3 страницыIsosorbide DinitratoRoberto LlanesОценок пока нет
- Calculo EstructuralДокумент1 страницаCalculo EstructuralFelipe TunОценок пока нет
- Ciencia y Tecologia Actividad Semana 11Документ6 страницCiencia y Tecologia Actividad Semana 11Jharen Jhosselin Calua Flores,Оценок пока нет
- Mal SaborДокумент31 страницаMal SaborCarlosEstrada100% (3)
- Informe de Eucalipto LizДокумент16 страницInforme de Eucalipto LizLiz Betsi CUADROS DE LA CRUZОценок пока нет
- Inicial Lista 4 Años 2022 - 2Документ1 страницаInicial Lista 4 Años 2022 - 2illari jenny50% (2)
- King Clor Lista NuevaДокумент17 страницKing Clor Lista NuevaDamian HermidaОценок пока нет
- Capitulo V: CBR (California Bearing Ratio Relacion Soporte de California) ASTM D 1883Документ6 страницCapitulo V: CBR (California Bearing Ratio Relacion Soporte de California) ASTM D 1883César Alonso Posaico SaldarriagaОценок пока нет
- 38 - Miel de AbejaДокумент1 страница38 - Miel de AbejaRaul Antonio Pacheco Arias100% (1)