Академический Документы
Профессиональный Документы
Культура Документы
Trabajo Sena
Загружено:
Ktalina BeltranАвторское право
Доступные форматы
Поделиться этим документом
Поделиться или встроить документ
Этот документ был вам полезен?
Это неприемлемый материал?
Пожаловаться на этот документАвторское право:
Доступные форматы
Trabajo Sena
Загружено:
Ktalina BeltranАвторское право:
Доступные форматы
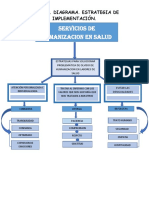
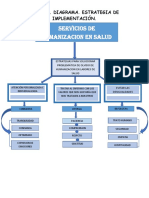
COMO PUEDE MANTENER LA EMPRESA UN CONTROL DE REGISTROS
EFICIENTES?
La organizacin debe establecer un procedimiento documentado para definir los
controles necesarios, para la identificacin, el almacenamiento, la proteccin, la
recuperacin, la retencin y la disposicin de los registros.
QUIEN DEBE ASUMIR LA RESPONSABILIDAD DE LA ACTUALIZACION
DE REGISTROS EN LA EMPRESA?
La responsabilidad la debe tener
IMPORTANCIA DEL CONTROL DE LOS REGISTRO EN UN SGC
La importancia del sistema documental radica principalmente en que se pasa de una
cultura oral a una cultura escrita. En que se especifican con claridad los procedimientos
del trabajo, las responsabilidades de cada area, los compromisos de calidad, las
especificaciones tcnicas que deben cumplir los productos o servicios.
GENERALIDADES SOBRE REGISTROS
Se constituyen en la principal evidencia del funcionamiento del sistema de gestin de
calidad de la Organizacin. La orma requiere de algunos registros pero las
organizaciones son libres de desarrollar otros registros que puedan necesitarse para
demostrar conformidad de sus procesos, productos y sistemas.
FUNCIONALIDAD DE LOS REGISTROS
a.- Garantiza la confianza de los clientes
b.- Demuestra la conformidad del producto
c.- Auditorias internas
d.- Establece Acciones Preventivas y Correctivas
e.- Detecta oportunidades de mejoramiento
f.- Realiza la Revision General
g.- Demuestra conformidad con los reuisitos
!.- Demuestra la operaci"n eficaz del #GC
i.- Detecta necesidades de entrenamiento
j- $razabilidad
$%P&# DE REG%#$R&#
'os registros pueden ser tanto magneticos( como f)sicos.
REG%#$R&# RE*+ER%D&# P&R 'A ,&R-A %#& .//0
1.2.0 Revisin por la direccin
2.3.3 e4 Educacin, formacin, habilidades y experiencia
5.0 d4 Evidencia de que los procesos de realizacin y el producto
resultante cumplen los requisitos
5.3.3 Resultados de la revisin de los requisitos relacionados con el
producto y de las acciones originadas por la misma
5.6.3 Elementos de entrada para el diseo y desarrollo
5.6.7 Resultados de las revisiones del diseo y desarrollo y de
cualquier accin necesaria
5.6.1 Resultados de la verificacin del diseo y desarrollo y de
cualquier accin que sea necesaria
5.6.2 Resultados de la validacin del diseo y desarrollo y de
cualquier accin que sea necesaria
5.6.5 Resultados de la revisin de los cambios del diseo y desarrollo
y de cualquier accin necesaria
5.7.0 Resultados de las evaluaciones del proveedor y de cualquieraccin necesaria
que se derive de las mismas
5.1.3 d4 Segn se requiera por las organizaciones, demostrar la
validacin de los procesos donde los productos resultantes no
puedan verificarse mediante actividades de seguimiento o
medicin posteriores
5.1.6 dentificacin nica del producto, cuando la trazabilidad sea un
Requisito
5.1.7 !ualquier bien que sea propiedad del cliente que se pierda,
deteriore o que, de algn otro modo, se considere inadecuado
para su uso
5.2 a4 "a base utilizada para la calibracin o la verificacin del equipo
de medicin cuando no existen patrones de medicin
nacionales o internacionales
5.2 #alidez de los resultados de las mediciones anteriores cuando
se detecte que el equipo de medicin no est$ conforme con los
Requisitos
5.2 Resultados de la calibracin y la verificacin del equipo de
%edicin
8.3.3 Resultados de la auditoria interna y de las actividades de
seguimiento
8.3.7 dentificacin de la&s' persona&s' responsable&s' de la liberacin
del producto
8.6 (aturaleza de las no conformidades del producto y de cualquier
accin tomada posteriormente, incluyendo las concesiones que
se hayan obtenido
8.1.3 Resultados de la accin correctiva
8.1.6 Resultados de la accin preventiva
Вам также может понравиться
- Examen AtsДокумент2 страницыExamen AtsPedro Fernando Blacido CollasОценок пока нет
- Pares de Apriete Estandar de VolvoДокумент5 страницPares de Apriete Estandar de Volvojrincon26Оценок пока нет
- Punto de EquilibrioДокумент24 страницыPunto de EquilibrioKtalina BeltranОценок пока нет
- Estrategias Asociadas A Promoción de La Donación de Sangre - Diciembre 2018Документ13 страницEstrategias Asociadas A Promoción de La Donación de Sangre - Diciembre 2018Sara QuinteroОценок пока нет
- Medidas de Tendencia CentralДокумент27 страницMedidas de Tendencia CentralyeihardОценок пока нет
- Costos de SaludДокумент11 страницCostos de SaludKtalina BeltranОценок пока нет
- Costos de SaludДокумент11 страницCostos de SaludKtalina BeltranОценок пока нет
- Solución - Ejercicio Hada MadrinaДокумент2 страницыSolución - Ejercicio Hada MadrinaKtalina BeltranОценок пока нет
- Manual de Atencion Al UsuarioДокумент26 страницManual de Atencion Al UsuarioKtalina Beltran100% (1)
- Cs M TB 01 Caracteriz Banco de Sangre v2Документ10 страницCs M TB 01 Caracteriz Banco de Sangre v2Ktalina BeltranОценок пока нет
- EnsayoДокумент2 страницыEnsayodialaОценок пока нет
- AA3 EV01 Diagrama Estrategia de ImplementacionДокумент1 страницаAA3 EV01 Diagrama Estrategia de ImplementacionKtalina Beltran100% (1)
- Banco de SangreДокумент88 страницBanco de SangredominguoОценок пока нет
- AA3 EV01 Diagrama Estrategia de ImplementacionДокумент1 страницаAA3 EV01 Diagrama Estrategia de ImplementacionKtalina Beltran100% (1)
- AA3 EV01 Diagrama Estrategia de ImplementacionДокумент1 страницаAA3 EV01 Diagrama Estrategia de ImplementacionKtalina BeltranОценок пока нет
- Abece Sistema Obligatorio Garantia Calidad (Habilitacion)Документ16 страницAbece Sistema Obligatorio Garantia Calidad (Habilitacion)MARIAОценок пока нет
- Anexo Crucigrama AA3-EV01Документ1 страницаAnexo Crucigrama AA3-EV01Luisita Erazo Eraso Salas0% (1)
- Procedimiento de Transporte de Hemocomponentes en ColombiaДокумент13 страницProcedimiento de Transporte de Hemocomponentes en ColombiaKtalina BeltranОценок пока нет
- APTr 1.3 APDs Procedimiento Trazabilidad UMT V2 2016Документ10 страницAPTr 1.3 APDs Procedimiento Trazabilidad UMT V2 2016Ktalina BeltranОценок пока нет
- Buenas Practicas de SangreДокумент40 страницBuenas Practicas de SangreOmariniYepezОценок пока нет
- Iso 15189 17025 PDFДокумент23 страницыIso 15189 17025 PDFAna Carolina NegreteОценок пока нет
- Guia Requisitos Ev CalidadДокумент72 страницыGuia Requisitos Ev CalidadArgenis rojasОценок пока нет
- Estandares de Trabajo en Banco de Sangre - Republica de El SalvadorДокумент107 страницEstandares de Trabajo en Banco de Sangre - Republica de El SalvadorMichiru LainzОценок пока нет
- Manual de Verificadores ColombiaДокумент109 страницManual de Verificadores ColombiaDiosas Cárites100% (1)
- Estandares de Trabajo en Banco de Sangre - Republica de El SalvadorДокумент107 страницEstandares de Trabajo en Banco de Sangre - Republica de El SalvadorMichiru LainzОценок пока нет
- Infografia 01Документ1 страницаInfografia 01Ktalina BeltranОценок пока нет
- Componentes-Esenciales Del Ser Humano2Документ3 страницыComponentes-Esenciales Del Ser Humano2Ktalina BeltranОценок пока нет
- Balance GeneralДокумент1 страницаBalance GeneralKtalina BeltranОценок пока нет
- Anexo Ejemplo Plantilla Mapa ConceptualДокумент1 страницаAnexo Ejemplo Plantilla Mapa ConceptualKtalina BeltranОценок пока нет
- Er EjemploДокумент1 страницаEr EjemploKtalina BeltranОценок пока нет
- Componentes-Esenciales Del Ser HumanoДокумент3 страницыComponentes-Esenciales Del Ser HumanoKtalina BeltranОценок пока нет
- Lenguaje Ensamblador y Cuadro ComparativoДокумент3 страницыLenguaje Ensamblador y Cuadro ComparativoSaulOjedaОценок пока нет
- Z4 Estructuras - Cisterna y Tanque Elevado 1Документ20 страницZ4 Estructuras - Cisterna y Tanque Elevado 1Cesar Augusto Tardeo De La CruzОценок пока нет
- Ivan Paul Martinez SeparadoresДокумент12 страницIvan Paul Martinez SeparadoresLuis LeonОценок пока нет
- Defectos en La Produccion de Bolas de Acero para MolinosДокумент13 страницDefectos en La Produccion de Bolas de Acero para MolinosCristian CariОценок пока нет
- Practica MicrometroДокумент10 страницPractica MicrometroalexОценок пока нет
- Ejemplo de MonografiaДокумент7 страницEjemplo de MonografiaRick JaimesОценок пока нет
- Impedancia CaracterísticaДокумент54 страницыImpedancia CaracterísticaAlexVega100% (1)
- Cinematica DirectaДокумент8 страницCinematica DirectamikelkatenaОценок пока нет
- Ensayo Apple vs. Microsoft, Historia de TitanesДокумент4 страницыEnsayo Apple vs. Microsoft, Historia de TitanesFrida BurgosОценок пока нет
- FilmArray Torch Ficha TecnicaДокумент2 страницыFilmArray Torch Ficha TecnicaJosé Sánchez NiñoОценок пока нет
- 2019a Silabo Energias Renovables CompletoДокумент13 страниц2019a Silabo Energias Renovables CompletoEnzo VizcardoОценок пока нет
- Sustentacion Trabajo Colaborativo - Escenario 7 - PRIMER BLOQUE-CIENCIAS BASICAS - CALCULO II - (GRUPO B02)Документ4 страницыSustentacion Trabajo Colaborativo - Escenario 7 - PRIMER BLOQUE-CIENCIAS BASICAS - CALCULO II - (GRUPO B02)Jorge GarzonОценок пока нет
- Sistemas Cad (Exposicion)Документ26 страницSistemas Cad (Exposicion)JemОценок пока нет
- Gancho de PerforacionДокумент8 страницGancho de PerforacionDavid Santiago ManillaОценок пока нет
- 1 PRACTICAOPERATIVADOScorregidoДокумент9 страниц1 PRACTICAOPERATIVADOScorregidoVladimir Calle MayserОценок пока нет
- INFORME Situacional de Obra VivancoДокумент10 страницINFORME Situacional de Obra VivancoRitta Monica Verastegui Quispe100% (1)
- 2485 - Nexans Freetox LSHF CT - 2019Документ2 страницы2485 - Nexans Freetox LSHF CT - 2019ChristianRiosHincapieОценок пока нет
- MetradoДокумент82 страницыMetradoJosé Sáenz NeriaОценок пока нет
- Clase05 BДокумент18 страницClase05 BCristian Rey SanchezОценок пока нет
- Introduccion A Los NDT e IzajeДокумент16 страницIntroduccion A Los NDT e IzajeOverhaul Mining EirlОценок пока нет
- Te MarioДокумент2 страницыTe Mariorodrigo reyesОценок пока нет
- C y T Potencia MecanicaДокумент3 страницыC y T Potencia Mecanicamayu BvОценок пока нет
- 1 Parcial 2021 Recu MFДокумент6 страниц1 Parcial 2021 Recu MFGuada Alvarez SandezОценок пока нет
- NMS5LX CLaro EcuadorДокумент46 страницNMS5LX CLaro EcuadorFusilInsurgente100% (1)
- Centri Fug AДокумент3 страницыCentri Fug ADaniel Escalante Guzman100% (2)
- Tutorial 6 - JTable - Movimiento Mouse, Teclas DireccionalesДокумент10 страницTutorial 6 - JTable - Movimiento Mouse, Teclas DireccionalesNorman ArauzОценок пока нет
- Descripción. de Vivienda Normas 1Документ15 страницDescripción. de Vivienda Normas 1Wilfredo Crespo ChavezОценок пока нет
- 2601 14 07028 PDFДокумент105 страниц2601 14 07028 PDFFrancisco Mendez0% (1)