Академический Документы
Профессиональный Документы
Культура Документы
Informe N
Загружено:
Mayi C LopezИсходное описание:
Оригинальное название
Авторское право
Доступные форматы
Поделиться этим документом
Поделиться или встроить документ
Этот документ был вам полезен?
Это неприемлемый материал?
Пожаловаться на этот документАвторское право:
Доступные форматы
Informe N
Загружено:
Mayi C LopezАвторское право:
Доступные форматы
INFORME N 7: ISOTERMAS DE ADSORCIN
MARIA ANGELICA COGOLLO LOPEZ
KATIUSKA ANGULO TORDECILLA
YUMIRIS MURILLO PATERNINA
Presentado a:
DAIRO PEREZ SOTELO
ING. QUIMICO
UNIVERSIDAD DE CORDOBA
FACULTAD DE CIENCIAS BASICAS
QUIMICA
SEMESTRE VII
MONTERIA
2013
INFORME N7: ISOTERMAS DE ADSORCIN
RESUMEN EJECUTIVO
La adsorcin es un proceso por el cual los tomos en la superficie de un slido,
atraen y retienen molculas de otros compuestos. Estas fuerzas de atraccin son
conocidas como Fuerzas de Van Der Waals.
Los experimentos sobre adsorcin, que con ms frecuencia se realizan, consisten
en la medida de la relacin entre la cantidad de gas o lquido adsorbido, sobre una
determinada cantidad de adsorbente. Estas medidas se realizaran a una
temperatura constante y los resultados se representan grficamente en las
llamadas Isotermas de Adsorcin. Lo que se mide experimentalmente es el
volumen del lquido o gas adsorbido por una cantidad de adsorbente, o la
variacin del peso que experimenta el adsorbente cuando ha estado en contacto
con el adsorvato.
La prctica denominada Isotermas de Adsorcin tiene como objetivos Estudiar la
adsorcin sobre el carbn vegetal (activado), de un soluto en disolucin acuosa;
determinar la relacin existente de cido actico adsorbido por carbn activado as
como la concentracin de equilibrio del cido actico en la fase acuosa y
determinar el rea superficial del carbn vegetal (activado) aplicando las isotermas
Langmuir.
Para cumplir con los objetivos previamente expuestos se realizara la parte
experimental Determinacin de la Isoterma de Adsorcin, de la cual se obtendrn
los datos y valores correspondientes para la realizacin de las graficas
respectivas.
OBJETIVOS
OBJETIVO GENERAL: Estudiar la adsorcin de cido actico en carbn y
determinar el rea superficial del carbn activado mediante la isoterma de
adsorcin.
OBJETIVO ESPECFICO:
Estudiar la adsorcin sobre carbn (activado) de un soluto en disolucin
acuosa.
Determinar el rea superficial del carbn (activado) aplicando las Isotermas
de Langmuir.
Determinar la relacin existente de cido actico adsorbido por carbn
activado y la concentracin de equilibrio del cido en la fase acuosa.
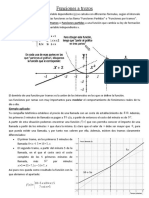
FUNDAMENTOS TEORICOS
Una isoterma es una curva que describe, para una temperatura dada, la relacin
de equilibrio entre la cantidad de agua del alimento y la presin de vapor
humedad relativa.
El trmino de sorcin, se usa para relacionar el comportamiento de un producto,
dependiendo de su contenido inicial de humedad, el cual perder o ganar
(adsorber) agua durante el proceso de equilibrio con la atmosfera que rodea al
producto.
La isoterma de sorcin de agua relaciona, a una temperatura constante, el
contenido de hmedad con la actividad termodinmica del agua en el producto, en
un intervalo dado de humedad o actividad. Es interesante recordar que en el
equilibrio de la actividad de agua es igual a la humedad relativa del aire que rodea
al producto a una temperatura determinada.
Se puede graficar el contenido de agua (humedad) vs. Aw HR y dicha grfica
toma el nombre de isotermas de absorcin y desorcin.
La isoterma de sorcin del agua, es una forma adecuada de analizar el grado de
interaccin del agua con el sustrato. Normalmente se puede dividir en tres
intervalos en funcin de la Aw:
Zona A. Agua fuertemente ligada correspondiente a una Aw de 0.2-0.3
inferior: el agua se encuentra en forma monomolecular, que se desarrolla
cuando una fraccin de agua presente interacciona con la superficie del
alimento.
Zona B: Agua moderadamente ligada ( Aw= 0.3-0.7) : es la ms interesante,
corresponde a multicapas de agua y presenta caractersticas muy
particulares. Es una zona en la que un pequeo cambio en el contenido
acuoso se traduce en grandes variaciones de los valores de su actividad.
Zona C: Agua poco ligada: correspondiente a una Aw de 0.7-0.8 y superior:
el alimento presenta actividades bastantes prximas a la del agua pura. Se
elimina con facilidad llegando slo a un valor de 0.8 y es la responsable de
cualquier tipo de reaccin y crecimiento microbiano.
Figura 12: Isoterma de sorcin de agua y sus zonas A,B yC. Fuente: Bello, Jos:
Ciencia Bromatolgica. Principios generales de los alimentos. 2008, editorial Daz
de Santos, Brasil.
Existen diversos modelos matemticos, tericos, semiempricos y empricos para
la prediccin y el ajuste de datos experimentales de sorcin de humedad en
funcin de la actividad de agua. La bondad de los ajustes depende de la
naturaleza de los alimentos, el rango de actividad de agua y otros parmetros
experimentales.
Una de las primeras isotermas de sorcin desarrolladas fue la del BET (Brunauer-
Emett- Teller), la cual es vlida para los valores bajos de actividad de agua.
El conocimiento de las isotermas de sorcin de un alimento es esencial para poder
determinar su Aw, conociendo su contenido de humedad.
8.2 Isoterma de adsorcin:
Hace referencia al comportamiento de alimentos deshidratados almacenados a
una HR atmosfrica alta, tienden a ganar agua para equilibrar las presiones de
vapor de agua tanto del alimento como de la atmsfera.
Isoterma de desorcin: Hace referencia al comportamiento de los alimentos
hidratados con Aw bajas y %HR bajas. Es la grfica para alimentos que sufren
prdida de agua para equilibrarse con el las presiones de vapor de la atmsfera.
Badui, Slavador, presenta este tipo de grficas llamadas Isotermas de sorcin nos
muestra la actividad acuosa de un alimento en funcin del contenido de agua del
mismo, a determinada temperatura. Las isotermas indican la cantidad de agua
retenida por un alimento en funcin de la HR de la atmsfera que lo rodea bajo
condiciones de equilibrio a una temperatura constante[2]. Ver figura 13.
Figura 13. Isotermas de adsorcin y desorcin
En cada punto, la ordenada (eje x) indica la actividad del agua del alimento en
equilibrio con las presiones de vapor de agua del alimento y la atmsfera a
temperatura constante. En el eje de las abscisas (eje y) el contenido de agua del
alimento, gramos de agua / 100 gramos de materia seca.
El fenmeno de histresis en las isotermas desorcin: Las curvas de adsorcin y
desorcin no son superponibles, significa que los fenmenos de ganar o perder
humedad no son reversibles en el alimento, la no "coincidencia" en ganar y perder
agua sobre la isoterma se denomina histresis.
Los valores de humedad obtenidos de la curva de desorcin son en teora
ligeramente superiores a los obtenidos en la curva de adsorcin. Este fenmeno
se denomina Histresis. La histresis puede ser explicada por la desnaturalizacin
que puede ocurrir durante la desnaturalizacin que puede ocurrir durante la
desorcin de las protenas, o la concentracin de solutos en el alimento. Las
protenas desnaturalizadas reducen su capacidad de retencin de agua una vez
han sufrido fenmenos de desorcin.
Figura 14: Prediccin del comportamiento de un alimento en funcin de sus
procesos de hidratacin y desecacin. Fuente: Bello, Jos (2008). Ciencia
Bromatolgica. Principios generales de los alimentos. Brasil: editorial Daz de
Santos, Brasil
Para Bello, Jos en la figura 14, se aprecia muy raras veces las isotermas de un
proceso de hidratacin (fenmenos de adsorcin) coinciden en su representacin
grfica con las isotermas de los procesos de desecacin (fenmenos de
desorcin). Esto significa que uno y otro proceso siguen caminos diferentes en los
alimentos. Es decir, en esta zona de la isoterma, ambos procesos no son
reversibles. Estas curvas de histresis, pueden variar ampliamente para los
diversos alimentos y, a menudo, alimentos idnticos pueden presentar patrones de
isotermas diferentes cuando cambia la temperatura. Esta diversidad puede ser
interpretada como una consecuencia de la variabilidad que acompaa a la
concentracin de los componentes qumicos de los alimentos, as como a la
incidencia de algunos cambios producidos en los factores de porosidad capilar,
que caracteriza a cada alimento.
Como consecuencia de estos fenmenos de histresis puede ocurrir que para un
mismo contenido acuoso del alimento, su actividad de agua sea muy diferente,
segn ser est considerando la hidratacin del producto o la desecacin del
mismo, pues en la zona intermedia de actividades, la isoterma sigue caminos
diferentes. De aqu su importancia en la repercusin de la tecnologa de alimentos,
donde este fenmeno alcanza un gran inters de tipo prctico. As, una vez
conocidas las isotermas que caracterizan los procesos de hidratacin y
desecacin para la elaboracin de un alimento concreto, es posible hacer
predicciones acerca de su comportamiento, tanto en el tratamiento tecnolgico
como en su conservacin.
Explicando la grafica 14, cuando un alimento se ha deshidratado hasta un
contenido acuoso de Ho, su situacin en la isoterma corresponde al punto A, con
una actividad acuosa Aw1. Si por diferentes causas pierde agua, como puede
ocurrir en un mal almacenamiento o un control incorrecto en su proceso de
desecacin, al hidratarlo de nuevo para que alcance el contenido acuoso
adecuado para su comercializacin (Ho), en este caso, su situacin sobre la
isoterma corresponde al punto A2, que tiene una actividad de agua Aw2, que
resulta mayor que la del punto A1. Por consiguiente, debido al fenmeno de
histresis, un alimento que ha tenido que ser rehidratado despus de una
desecacin, contiene para un mismo nivel acuso una disponibilidad de agua
bastante mayor (Aw2), que implica graves inconvenientes porque significa una
mayor facilidad para que se pueda alterar.
HIPOTESIS
Para determinar la adsorcin del cido actico, en soluciones acuosas a distintas
concentraciones, por el carbn activado se utiliza un mtodo muy Sencillo. A partir
de las cantidades de soluto adsorbido, la cantidad de adsorbente y la variacin de
concentracin de las soluciones se logran determinar el tipo de adsorcin que se
presenta en el experimento y se construyen las isotermas de adsorcin de
Langmuir., a fin de determinar el tipo de isoterma que caracteriza este fenmeno.
MODELOS MAEMATICOS
La isoterma de adsorcin de Freundlich:
Modelo de Langmuir tiene el siguiente esquema dinmico para representar la
adsorcin:
A(g) + S(s) AS
DISEO DE LA PRCTICA
VARIABLES Y PARMETROS
Para el desarrollo de esta prctica se tuvieron en cuenta las siguientes variables:
Temperatura
Volumen
Masa
Entre los parmetros tenemos la presin atmosfrica estndar.
ELECCIN DEL SISTEMA
Se trabajara un sistema donde se determinara la adsorcin sobre el carbn
vegetal de un soluto en disolucin acuosa, donde el cido actico adsorbido por el
carbn activado y la concentracin del equilibrio del acido actico, definir el rea
superficial del carbn activado mediante una isoterma de adsorcin de Langmuir.
HOJA DE DATOS
Tabla 1: datos principales tomados para cada erlenmeyer.
MASA DE
CARBN
ACTIVADO
(g)
VOLUMEN
DE
CH3COOH
(mL)
VOLUMEN
DE H2O (mL)
VOLUMEN
DE NaOH
GASTADO
(mL)
1,0020 50 -- 22.7
23.1
1,0092 25 25 19.5
20.0
1,0098 15 35 10.4
10.5
1,0075 7,5 42,5 3.8
3.8
1,0048 4 46 4.6
4.5
1,0064 2 48 2.6
2.7
Tabla 2: concentracin CH3COOH para cada erlenmeyers
MASA DE
CARBN
ACTIVADO (g)
CH3COOH [M] n
CH3COOH
(mol)
1,0020 0.400 0.0200
1,0092 0.200 0.0100
1,0098 0.120 0.0060
1,0075 0,060 0.0030
1,0048 0.032 0.0016
1,0064 0.016 0.0008
EQUIPO Y MATERIALES
Bureta 50ml
6 embudos
12 erlenmeyer 125ml
Pipeta 10ml
Soporte universal
Gradilla
Tapones
Esptula
Pera
Papel filtro
Reactivo
Carbn activado
cido actico 0.4M
NaOH 0.1M
Fenolftalena
NaOH
Frmula: NaOH
Masa molar: 39,997 g/mol
Densidad: 2,13 g/cm
Punto de fusin: 318 C
Punto de ebullicin: 1.388 C
CH
3
COOH
Estado de agregacin: lquido
Apariencia: incoloro o cristales (no inodoro)
Densidad: 1049 kg/m3; 1,049 g/cm3
Masa molar: 60.05 g/mol
Punto de fusin: 290 K (17 C)
Punto de ebullicin: 391,2 K (118 C)
DESARROLLO DE LA PRCTICA
Se pes 1g de carbn activado para 6 erlenmeyers, Se agreg diferentes
volmenes de cido actico y se completan hasta 50ml con agua destilada. Luego
se agitaron por aproximadamente una hora los 6 erlenmeyers juntos. Finalmente
filtramos las seis soluciones y tomamos 10ml de la 1 y 2, 20ml de 3 y 4, y 40ml de
5 y 6, para titular con NaOH 0,1M.
REALIZACION DE LA PRCTICA
OBSERVACIONES
A medida que transcurra el procedimiento se tuvieron las siguientes
observaciones:
Las soluciones siempre presentaban el carbn activado insoluble en ellas,
sobre nadante a pesar de la agitacin pero al titular nos dabamos cuenta
que se gastaba ms volumen de NaOH del que se esperaba.
A medida que bajaba la concentracin el volumen de titulante era menor y
la concentracin despus de la adsorcin por ende tambin.
RESULTADOS
Tabla n3: concentracin y moles en el equilibrio y moles adsorbidas.
VOLUMEN DE
NaOH
GASTADO
(mL)
CH3COOH [M]
equi.
n
CH3COOH
eq.
(mol)
n
CH3COOH adso.
(mol)
22.7
23.1
0.2497
0.2541
0.002497
0.002541
0.0175
0.0174
19.5
20.0
0.2145
0.2200
0.002145
0.002200
0.0078
0.0078
10.4
10.5
0.1144
0.1155
0.001144
0.001155
0.0048
0.0048
3.8
3.8
0.0418
0.0418
0.000418
0.000418
0.0026
0.0026
4.6 0.0253 0.000506 0.0011
4.5 0.0248 0.000495 0.0011
2.6
2.7
0.0143
0.0149
0.000286
0.000297
0.0005
0.0005
Tabla n4: concentracin de acido actico y factor C/X
Moles Ad. / gcar.
Ad (C/N)
CH3COOH [M] C/X
0.017 0.25 34.4
0.007 0.21 28.0
0.004 0.11 23.9
0.002 0,04 16.3
0.001 0.02 22.9
0.0005 0.01 8.8
GRAFICA C/N Vs C
DISCUSION Y CONCLUSIONES
Aunque en general el mtodo descrito introduce cierta incertidumbre en la
determinacin de X, debido a que la diferencia C
inicial
C
final
es muy pequea, los
resultados a los que da lugar permiten analizar las dependencias del grado de
absorcin de un material con su concentracin y los alcances del modelo de
Langmuir para representar su comportamiento.
y = 75,793x + 14,299
0
5
10
15
20
25
30
35
40
0 0.05 0.1 0.15 0.2 0.25 0.3
C
/
X
(
L
/
g
)
[CH3COOH] (mol/L)
A medida que aumenta la concentracin del cido actico aumenta la relacin
entre la cantidad adsorbida por gramo de carbn. El carbn activado proporciona
datos de manera eficiente y en tiempo corto en comparacin con otros materiales,
debido a su velocidad de llegar al equilibrio.
Debido a la isoterma de absorcin aqu observada, es claro determinar que el tipo
de adsorcin que se presenta en el cido actico- carbn activado es qumica.
SUGERENCIAS
Se debe tener cuidado a la hora de pesar el carbn activado, puesto que esto
puede influir en el grado de adsorcin. Tambin, hay que tener en cuenta la
medida de los volmenes adicionados al momento de preparar las soluciones de
cido actico. No se puede olvidar, la agitacin de las soluciones, la cual debe ser
homognea y constante por un tiempo determinado.
REFERENCIAS BIBLIOGRAFIA
SKOOG, D.; WEST, D. y HOLLER, F. (1995). "Qumica Analtica", McGraw
Hill. Sexta Edicin. Pgs. 308-316.
SMITH, J.; VAN NESS, H. (1997) "Introduccin a la Termodinmica en
Ingeniera qumica" Quinta Edicin. McGraw Hill. Mxico
TREYBAL. "Transferencia de masa".
Вам также может понравиться
- Isoterma de Sorción de AguaДокумент5 страницIsoterma de Sorción de AguaNoemi Esther Panca VasquezОценок пока нет
- Informe-Isotermas-De-Sorción-Y-Aw 2017Документ6 страницInforme-Isotermas-De-Sorción-Y-Aw 2017Canicani KimОценок пока нет
- Quimica de Alimentos 1Документ12 страницQuimica de Alimentos 1Dennis Castelo HuarancaОценок пока нет
- Isotermas de AdsorcionДокумент15 страницIsotermas de AdsorcionginoОценок пока нет
- GUIA Isotermas de SorciónДокумент4 страницыGUIA Isotermas de SorciónNeidyMoraJimenezОценок пока нет
- Ope 2 InformeДокумент14 страницOpe 2 InformeJose Tello CandiaОценок пока нет
- Isotermas de Adorsión.Документ8 страницIsotermas de Adorsión.96884643*50% (2)
- Dterminacion de Isoterma QuimicaДокумент11 страницDterminacion de Isoterma Quimicagregorio joelОценок пока нет
- Isotermas de Adsorción 1Документ10 страницIsotermas de Adsorción 1Manuel Albujar ZeladaОценок пока нет
- Quimica de Alimentos. Informe 1 1Документ12 страницQuimica de Alimentos. Informe 1 1Mayk Espinoza VegaОценок пока нет
- Modelos de Isotermas de Sorción para AlimentosДокумент13 страницModelos de Isotermas de Sorción para AlimentosJOSE MARIA MOLINA PALACIOSОценок пока нет
- Fisicoquímica MonocapaДокумент3 страницыFisicoquímica MonocapaPedro CUICAPUSA QUISPE100% (1)
- Actividad Del Agua 1Документ69 страницActividad Del Agua 1Raiza Zurita CamachoОценок пока нет
- Determinación de Las Isotermas de Adsorción y Del Valor de La Cobertura MonomolecularДокумент15 страницDeterminación de Las Isotermas de Adsorción y Del Valor de La Cobertura MonomolecularCristian VelásquezОценок пока нет
- Actividad de AguaДокумент10 страницActividad de Aguaerika jimenaОценок пока нет
- Clase Agua en AlimentosДокумент49 страницClase Agua en AlimentosIngenieriaAlimentosОценок пока нет
- Isotermas de AdsorciónДокумент19 страницIsotermas de AdsorciónDIEGO RODOLFO FASABI MONCADAОценок пока нет
- Qué Es Una Isoterma de AdsorciónДокумент3 страницыQué Es Una Isoterma de AdsorciónKevin VasquezОценок пока нет
- PRÁCTICA #02 Isotermas de AdsorcionДокумент15 страницPRÁCTICA #02 Isotermas de AdsorcionJavier MoisésОценок пока нет
- Contenido de Humedad y Actividad de Agua en Los AlimentosДокумент5 страницContenido de Humedad y Actividad de Agua en Los AlimentosJessica candoОценок пока нет
- Isotermas de SorciónДокумент10 страницIsotermas de SorciónEdivar CarrascoОценок пока нет
- Informe 1Документ16 страницInforme 1Mary Liz Astoquillca SantoyoОценок пока нет
- Isotermas de Sorción PDFДокумент6 страницIsotermas de Sorción PDFirene zetinaОценок пока нет
- 1 INFOR QUIMI ALIM 1 RecuperadoДокумент25 страниц1 INFOR QUIMI ALIM 1 RecuperadoOmarHusseinZegarraОценок пока нет
- Informe de Laboratorio - Isotermas de AdsorciónДокумент18 страницInforme de Laboratorio - Isotermas de AdsorciónEver Cerna Vargas100% (1)
- Absorción de Agua en AlimentosДокумент7 страницAbsorción de Agua en AlimentosCA SegismundoОценок пока нет
- Determinación de Isoterma de Sorcionara Imrimira ColoresssДокумент8 страницDeterminación de Isoterma de Sorcionara Imrimira ColoresssGrisela AlbertoОценок пока нет
- Aw de Los Alimentos y Ajuste de Isotermas de SorcionДокумент20 страницAw de Los Alimentos y Ajuste de Isotermas de SorcionChrystian ParedesОценок пока нет
- Resumen Actividad de AguaДокумент5 страницResumen Actividad de AguaAdriana CastellanosОценок пока нет
- Laboratorio #02 Determinacion de IsotermasДокумент11 страницLaboratorio #02 Determinacion de IsotermasAlex Romero SurcoОценок пока нет
- Isotermas de AdsorciònДокумент4 страницыIsotermas de AdsorciònMiguelRCОценок пока нет
- Actividad Del AguaДокумент51 страницаActividad Del AguaIngenieriaAlimentosОценок пока нет
- Informe 1 - Q.AДокумент24 страницыInforme 1 - Q.ALuОценок пока нет
- Solucionario Bioquimica 1Документ13 страницSolucionario Bioquimica 1Peleg Moreno CastilloОценок пока нет
- Lab 1 QaДокумент11 страницLab 1 QaAngela IquiseОценок пока нет
- Practica de IsotermasДокумент14 страницPractica de IsotermasLisbeth Huancas OrdoñesОценок пока нет
- Guias de Practica de Laboratorio de Bioquimica Agroindustrial PDFДокумент44 страницыGuias de Practica de Laboratorio de Bioquimica Agroindustrial PDFBraShan Rober A O̲̲̅f̲̲̅̅ı̲̲̅̅c̲̲̅̅ı̲̲̅a̲̲̅̅l̲̲̅̅'̲̲̅̅F̲̲̅̅bОценок пока нет
- 1er Informe Aw+mejoradoДокумент28 страниц1er Informe Aw+mejoradoKarina OrtizОценок пока нет
- Determinacion de Las IsotermasДокумент24 страницыDeterminacion de Las IsotermasLuis TasaycoОценок пока нет
- ISOTERMAS DE ADSORCION Y DESORCION DEL AJI SECO (Informe)Документ3 страницыISOTERMAS DE ADSORCION Y DESORCION DEL AJI SECO (Informe)Lesli Medaline Tafur SaucedoОценок пока нет
- Práctica N 04 Lab. FisicoquímicaДокумент10 страницPráctica N 04 Lab. FisicoquímicaVíctor Gustavo Díaz PaucarОценок пока нет
- Preparacion Muestra - Determinacion Agua en AlimentosДокумент67 страницPreparacion Muestra - Determinacion Agua en AlimentosPame Quispe RodriguezОценок пока нет
- El Agua en Los Alimentos.20092Документ17 страницEl Agua en Los Alimentos.20092arrodriguezz100% (6)
- Práctica No.1 Aw e Isotermas de SorciónДокумент9 страницPráctica No.1 Aw e Isotermas de SorciónOscar AguirreОценок пока нет
- Termodinamica de Agua en AlimentosДокумент11 страницTermodinamica de Agua en AlimentosJulio Santana100% (1)
- Actividad de Agua y Curvas de AdsorcionДокумент16 страницActividad de Agua y Curvas de AdsorcionMadelleyTamarizCaceresОценок пока нет
- Actividad Del Agua Qua1Документ4 страницыActividad Del Agua Qua1DENIS EVERALDO TORRES ALFAROОценок пока нет
- Terminar AwДокумент5 страницTerminar AwNoemi Esther Panca VasquezОценок пока нет
- 1-Humedad y Materia SecaДокумент52 страницы1-Humedad y Materia SecaAdriana Marianela QAОценок пока нет
- Info 2Документ21 страницаInfo 2Jhonatan CáceresОценок пока нет
- Copia de IsotermasДокумент18 страницCopia de IsotermasDaniel Aliaga GaragattiОценок пока нет
- Absorcion de AguaДокумент11 страницAbsorcion de AguaAlexanderJerRamirezОценок пока нет
- Andrade P. Ricardo D. Models of Sorption Isotherms For Food, Uses and LimitationsДокумент10 страницAndrade P. Ricardo D. Models of Sorption Isotherms For Food, Uses and LimitationsPedro GarcíaОценок пока нет
- Actividad de Agua en Los AlimentosДокумент11 страницActividad de Agua en Los AlimentosDaniela AcostaОценок пока нет
- Absorcion de Agua Marco TeoricoДокумент4 страницыAbsorcion de Agua Marco TeoricoJavier CLОценок пока нет
- 1 150525051453 Lva1 App6892Документ33 страницы1 150525051453 Lva1 App6892Javier MoisésОценок пока нет
- Actividad de Agua para PresentarДокумент8 страницActividad de Agua para PresentarKristel SolisОценок пока нет
- Química de macrocomponentes de alimentosОт EverandQuímica de macrocomponentes de alimentosОценок пока нет
- Técnicas analíticas básicas: En el control de la calidad del agua según normatividadОт EverandTécnicas analíticas básicas: En el control de la calidad del agua según normatividadОценок пока нет
- Estatus ácido-base: Conceptos, desequilibrios e interpretaciónОт EverandEstatus ácido-base: Conceptos, desequilibrios e interpretaciónОценок пока нет
- Velocidad de ReacciónДокумент8 страницVelocidad de ReacciónMayi C LopezОценок пока нет
- Juego de ProteinasДокумент8 страницJuego de ProteinasMayi C LopezОценок пока нет
- Energía de ReacciónДокумент2 страницыEnergía de ReacciónMayi C LopezОценок пока нет
- Examen de PHДокумент2 страницыExamen de PHMayi C Lopez100% (1)
- Análisis Literario Del Cuento Espuma y Nada Más de Hernando TéllezДокумент4 страницыAnálisis Literario Del Cuento Espuma y Nada Más de Hernando TéllezMayi C Lopez33% (6)
- Funciòn Relaciòn PlantaДокумент2 страницыFunciòn Relaciòn PlantaMayi C LopezОценок пока нет
- Evaluacion DiagnosticaДокумент6 страницEvaluacion DiagnosticaMayi C LopezОценок пока нет
- 1 PropanolДокумент3 страницы1 PropanolMayi C Lopez100% (1)
- Instructivo para La Elaboracion de Proyectos Iutai-Ver 1.0Документ50 страницInstructivo para La Elaboracion de Proyectos Iutai-Ver 1.0Joaura Jakeline Romero AlvarezОценок пока нет
- Medicina YorubaДокумент4 страницыMedicina YorubavitryОценок пока нет
- OfimaticaДокумент80 страницOfimaticameducacion1aОценок пока нет
- Planeacion de Recurso HumanoДокумент40 страницPlaneacion de Recurso Humanomado921028Оценок пока нет
- PE22 - TP6. Modularidad - FuncionesДокумент5 страницPE22 - TP6. Modularidad - FuncionesPalacios MarcoОценок пока нет
- Licenciado en Biotecnología Genómica - Plan de Estudio PDFДокумент1 страницаLicenciado en Biotecnología Genómica - Plan de Estudio PDFAndreaMartinezОценок пока нет
- Catalogo POSДокумент7 страницCatalogo POSFrancisco CatalánОценок пока нет
- Georges CormДокумент1 страницаGeorges CormRex IbéricusОценок пока нет
- Manual Manufactura IntДокумент169 страницManual Manufactura IntKarime BenitezОценок пока нет
- Indicadores de Gestion de Mantenimiento y Confiabilidad. Mejores Practicas para Metas en La Industria Petrolera UpstreamДокумент1 страницаIndicadores de Gestion de Mantenimiento y Confiabilidad. Mejores Practicas para Metas en La Industria Petrolera UpstreamDanny AlejandroОценок пока нет
- Evaluacion Final - Escenario 8 - Segundo Bloque-Teorico - Legislacion en Seguridad y Salud para El Trabajo - (Grupo b02)Документ12 страницEvaluacion Final - Escenario 8 - Segundo Bloque-Teorico - Legislacion en Seguridad y Salud para El Trabajo - (Grupo b02)Laura Natalia Valderrama paezОценок пока нет
- 7 Desperdicios de La Manufactura EsbeltaДокумент2 страницы7 Desperdicios de La Manufactura EsbeltaEliana Pilco100% (1)
- Apunte Funciones Por TramosДокумент4 страницыApunte Funciones Por TramosBERYLL ZICARELLIОценок пока нет
- Espacios RecubridoresДокумент10 страницEspacios RecubridoresJefferson PradaОценок пока нет
- Tarea 4. Documento de ApoyoДокумент7 страницTarea 4. Documento de ApoyoIvan BriseñoОценок пока нет
- Herpes Simple Y Herpes Zoster: Seminario de Dermatologia IgrДокумент68 страницHerpes Simple Y Herpes Zoster: Seminario de Dermatologia IgrIliana GarciaОценок пока нет
- Don Quijote de La Mancha - EnsayoДокумент22 страницыDon Quijote de La Mancha - Ensayosinsforsale90% (10)
- Caso Constructora ExitosaДокумент2 страницыCaso Constructora ExitosaJosé EspinozaОценок пока нет
- Estudio Hidrológico de La Micro Cuenca Huertas - Cuenca JequetepequeДокумент75 страницEstudio Hidrológico de La Micro Cuenca Huertas - Cuenca JequetepequeAnthony Jeanpier Fow EstevesОценок пока нет
- Guión HHBBB 2022 1º CuatrimestreДокумент14 страницGuión HHBBB 2022 1º CuatrimestrePedroОценок пока нет
- Imagen de La Ciudad de Quilpué, Sebastian TejadaДокумент7 страницImagen de La Ciudad de Quilpué, Sebastian TejadaSebastian Tejada EstevezОценок пока нет
- Franz Bardon Practica de La Evocacion MagicaДокумент520 страницFranz Bardon Practica de La Evocacion MagicaSandino Grullon100% (2)
- Indicadores para PreescolarДокумент31 страницаIndicadores para PreescolarMaykelis Yeinimar Chirinos Brito100% (2)
- Protocolo de Preparacion para Imagenes DX OkДокумент18 страницProtocolo de Preparacion para Imagenes DX OkCheryl RamirezОценок пока нет
- Laboratorio IiiДокумент27 страницLaboratorio IiiYhon Polanco AimitumaОценок пока нет
- Informe GeoestadisticaДокумент7 страницInforme GeoestadisticaFabri Leiva ZavalaОценок пока нет
- eHUMANISTA Persiles PDFДокумент565 страницeHUMANISTA Persiles PDFNoelia VitaliОценок пока нет
- S1 Sesion 9 Resolvemos Problemas A Través de EcuacionesДокумент7 страницS1 Sesion 9 Resolvemos Problemas A Través de EcuacionesDOCENTE MARÍAОценок пока нет
- Cormac McCarthyДокумент15 страницCormac McCarthyKevin Berger100% (4)
- MAICILLOSДокумент5 страницMAICILLOSCarlos Rocha FernandezОценок пока нет