Академический Документы
Профессиональный Документы
Культура Документы
09 - Taller 9 - Estequiometria y Balance de Masa
Загружено:
Hector Tineo0 оценок0% нашли этот документ полезным (0 голосов)
381 просмотров5 страницEste documento presenta 10 problemas de estequiometría y balance de masa. Los problemas involucran reacciones químicas con gases, soluciones y sustancias sólidas, y requieren calcular masas, volúmenes y concentraciones de reactivos y productos. También incluye 3 problemas sobre diagramas de flujo que representan procesos industriales como la producción de cobre, plata y aluminio.
Исходное описание:
Оригинальное название
09_Taller 9- Estequiometria y Balance de Masa
Авторское право
© © All Rights Reserved
Доступные форматы
PDF, TXT или читайте онлайн в Scribd
Поделиться этим документом
Поделиться или встроить документ
Этот документ был вам полезен?
Это неприемлемый материал?
Пожаловаться на этот документEste documento presenta 10 problemas de estequiometría y balance de masa. Los problemas involucran reacciones químicas con gases, soluciones y sustancias sólidas, y requieren calcular masas, volúmenes y concentraciones de reactivos y productos. También incluye 3 problemas sobre diagramas de flujo que representan procesos industriales como la producción de cobre, plata y aluminio.
Авторское право:
© All Rights Reserved
Доступные форматы
Скачайте в формате PDF, TXT или читайте онлайн в Scribd
0 оценок0% нашли этот документ полезным (0 голосов)
381 просмотров5 страниц09 - Taller 9 - Estequiometria y Balance de Masa
Загружено:
Hector TineoEste documento presenta 10 problemas de estequiometría y balance de masa. Los problemas involucran reacciones químicas con gases, soluciones y sustancias sólidas, y requieren calcular masas, volúmenes y concentraciones de reactivos y productos. También incluye 3 problemas sobre diagramas de flujo que representan procesos industriales como la producción de cobre, plata y aluminio.
Авторское право:
© All Rights Reserved
Доступные форматы
Скачайте в формате PDF, TXT или читайте онлайн в Scribd
Вы находитесь на странице: 1из 5
MA41-Qumica UPC 2014-1
Taller N 9: Estequiometra y balance de masa Los profesores
TALLER N 9 DE QUMICA
ESTEQUIOMETRIA CON GASES, SOLUCIONES Y BALANCE DE MASA
Estequiometria con gases y soluciones
1. Monxido de nitrgeno, (NO), reacciona inmediatamente con el oxgeno gaseoso para
formar dixido de nitrgeno (NO
2
), un gas caf oscuro: 2NO
(g)
+ O
2(g)
2NO
2(g)
En un experimento se mezclaron 0.886 moles de NO con 0.503 moles de O
2
, calcule:
a) Cul de los dos reactivos es el limitante.
b) El volumen producido de gas
NO
2
a C.N
Rpta: a) NO es el reactivo limitante. b) 19.83L
2. La plata pierde su brillo con el uso debido a la presencia de pequeas cantidades de H
2
S
en el aire (un gas con olor a huevos podridos). La ecuacin qumica de la reaccin es
como sigue:
4Ag
(s)
+ 2H
2
S
(g)
+ O
2(g)
2Ag
2
S
(s)
+ 2H
2
O
(l)
Si una muestra de 95 g de plata reacciona con 135 g de H
2
S y exceso de oxgeno.
Determine:
a) El reactivo que se consume completamente.
b) Los gramos de sulfuro de plata formados en la reaccin.
c) Qu volumen de O
2
gaseoso se requiere a 700mmHg y 30C?
Rpta: a) R.L es Ag, b) 109.07 g Ag
2
S, c) 5.94L O
2
3. Cuando reaccionan 30,0 g de benceno lquido, C
6
H
6
, con 30,0 g de bromo lquido, Br
2
,
se obtiene bromobenceno lquido, C
6
H
5
Br, y bromuro de hidrgeno gaseoso, HBr:
a) Escribir la ecuacin qumica completa del proceso qumico
C
6
H
6(l)
+ Br
2(l)
C
6
H
5
Br
(l)
+ HBr
(g)
b) Determinar el reactivo limitante y al reactivo en exceso.
c) Determinar la masa (en gramos) del bromobenceno obtenido al final de la reaccin.
d) Qu volumen de HBr gaseoso se produce a C.N.?
Rpta: b) R.L. Br
2
, R. en exceso: C
6
H
6
, c) 29,44 g C
6
H
5
Br, d) 4,20 L HBr
4. Los anticidos comunes y los complementos alimenticios de calcio que se emplean para
prevenir la osteoporosis (un trastorno en el que ocurre un debilitamiento de los huesos
por descalcificacin) contienen carbonato de calcio (CaCO
3
). Cuando se consume una
tableta, esta se disuelve en el jugo gstrico, que contiene cido clorhdrico, HCl, siendo
la ecuacin la siguiente:
CaCO
3(s)
+ 2HCl
(ac)
CaCl
2(ac)
+ CO
2(g)
+ H
2
O
(l)
a) Qu masa de CaCl
2
se producir si reaccionan dos tabletas de anticido con 2,0 g
de HCl, si cada tableta pesa 0,5 g?
b) Cul es la presin (en atm) del gas CO
2
obtenido a condiciones de 37 C y un
volumen de 5 L?
Rpta: a) 2,74 g CaCO
3
, b) 0,05 atm CO
2
MA41-Qumica UPC 2014-1
Taller N 9: Estequiometra y balance de masa Los profesores
5. El etanol (C
2
H
5
OH) se quema con el oxgeno del aire segn la ecuacin qumica:
C
2
H
5
OH + 3O
2 (g)
2CO
2 (g)
+ 3H
2
O
(l)
a) Determine el volumen de oxgeno, O
2
, en litros a 35 C y 790 mmHg que se
requieren para quemar 227 g de etanol.
b) Determine la presin del CO
2
, en atm, si este gas se recoge en un recipiente de 50 L
a 35 C.
Rpta: a) 360,06 L O
2
, b) 5 atm CO
2
6. Uno de los mtodos para obtener cobre metlico es mediante la siguiente ecuacin de la
reaccin ocurrida en hornos metalrgicos:
Cu
2
S
(s)
+ O
2 (g)
2Cu
(s)
+ SO
2 (g)
a) Qu cantidad en kilogramos de cobre se pueden obtener si se queman, con
suficiente oxgeno, 5000 kg de un mineral que contiene 80 % de sulfuro de cobre?
b) Cuntos kilogramos de oxgeno sern necesarias para consumir todo el sulfuro de
cobre presente en el mineral?
c) Determine la presin (en atm) del gas SO
2
generado, si este gas es recogido en
recipientes de 5,0 m
3
de capacidad a 200 C.
Rpta: a) 3194,97 Kg Cu, b) 805 Kg O
2
, c) 195,15 atm SO
2
7. Un mtodo utilizado por la EPA (Agencia de Proteccin Ambiental) de Estados Unidos
para determinar la concentracin de ozono, O
3
, en el aire consiste en hacer pasar la
muestra de aire por un burbujeador que contiene yoduro de sodio, NaI, el cual captura el
ozono segn la siguiente ecuacin qumica de la reaccin:
O
3(g)
+ 2NaI
(ac)
+ H
2
O
(l)
O
2(g)
+ I
2(s)
+ 2NaOH
(ac)
a) Qu volumen, en litros, de ozono a condiciones normales se puede determinar con
60 g de yoduro de sodio?
b) Cuntos gramos de yoduro de sodio se requieren para capturar ozono, si se
generan 2,5 L de oxgeno a condiciones de 1,0 atm de presin y 25 C?
Rpta: a) 4,48 L O
2
, b) 30 g NaI
8. Calcule la concentracin (en molaridad) de una disolucin de NaOH si se necesitan
25.0mL de la disolucin para neutralizar 17.4mL de una disolucin de HCl 0.312 M.
HCl
(aq)
+ NaOH
(aq)
H
2
O
(l)
+ NaCl
(aq)
Rpta: 0.216M
9. Para la obtencin de 20 g de Cl
2(g)
, determine los gramos de KMnO
4(s)
y la molaridad de
500 mL solucin de cido clorhdrico utilizados.
2KMnO
4(s)
+ 16HCl
(ac)
5Cl
2(g)
+ 2KCl
(ac)
+ MnCl
2(ac)
+ 8H
2
O
(l)
Rpta: 1,8 M
10. El cido sulfhdrico se elimina del agua potable mediante la siguiente ecuacin:
H
2
S
(ac)
+ Cl
2(g)
2HCl
(ac)
+ S
(s)
MA41-Qumica UPC 2014-1
Taller N 9: Estequiometra y balance de masa Los profesores
Si se hace reaccionar 2 litros de solucin H
2
S 0,02 M, cuntas moles de Cl
2
se
necesitar para eliminar todo el H
2
S del agua? y cuntos gramos de azufre slido se
formarn?
Rpta: 0,04 moles Cl
2
, 1,28 g S
Balance de masa
11. La produccin de cobre (Cu) se lleva a cabo mediante el proceso cuyo diagrama de flujo
es el mostrado, entonces:
i. El reactivo limitante es O
2
ii. El reactivo limitante es CuS (Rpta)
iii. El reactivo limitante es el N
2
iv. El reactivo limitante es el SO
2
12. La produccin de plata se lleva a cabo mediante el proceso cuyo diagrama de bloques
es el que se muestra, entonces el reactivo en exceso es:
i. N
2
.
ii. Ag
2
S.
iii. O
2
. (Rpta)
iv. SO
2
.
13. La reaccin global para la produccin electroltica de aluminio es mediante la ecuacin
qumica:
Al
2
O
3(s)
+ 3C
(s)
2Al
(s)
+ 3CO
(g)
Si el mineral que contiene al xido de aluminio tiene una pureza del 65 %, determine:
a) La cantidad de mineral (en kilogramos) que se tendr que procesar para obtener
1000 kg de aluminio.
b) Realice el diagrama de flujo indicando las entradas y salidas de materia y compruebe
el balance de masa.
Rpta: a) 2905,98 Kg mineral, b)
Impurezas Mineral C Al CO
m m m m m
2905.98 666.67 1000 1555.56 1017.09 Kg Kg Kg Kg Kg
3572.65 3572.65 Kg Kg
14. El qumico ms usado como conservante de alimentos es el benzoato de sodio,
C
7
H
5
O
2
Na, este se puede obtener por reaccin del cido benzoico, C
7
H
6
O
2
, con
hidrxido de sodio, NaOH, segn la siguiente ecuacin qumica:
C
7
H
6
O
2(ac)
+ NaOH
(ac)
C
7
H
5
O
2
Na
(ac)
+ H
2
O
(l)
N2
O2
SO2
Cu
O
2
C
Mineral (Al2O3)
CuS
Al
Horno
Horno
CO
Impurezas
O
2
O
2
Aire (N
2
+ O
2
)
Ag
2
S
SO
2
Horno
Ag
N
2
MA41-Qumica UPC 2014-1
Taller N 9: Estequiometra y balance de masa Los profesores
Si se mezclan 120 kg de un reactivo que contiene 80 % de cido benzoico y 200 kg de
hidrxido de sodio, determinar:
a) El reactivo limitante y el reactivo en exceso.
b) La cantidad en kg del reactivo en exceso
c) La cantidad en kg de los productos obtenidos
d) Realice el diagrama de bloques de entradas y salidas y compruebe el balance de
masa.
Rpta: a) R.L. C
7
H
6
O
2
y R. en exceso NaOH, b) 168,52 Kg NaOH, c) 113,32 Kg C
7
H
5
O
2
Na y 14,16
Kg H
2
O, d)
2
Re Impurezas activo NaOH Benzoato NaOH H O
m m m m m m
120 200 113.32 168.52 14.16 24 Kg Kg Kg Kg Kg Kg
320 320 Kg Kg
15. Una planta industrial envasadora de gases, produce gas acetileno (C
2
H
2
) a partir de
carburo de calcio, como se muestra en la siguiente ecuacin qumica:
CaC
2 (s)
+
2H
2
O
(l)
Ca(OH)
2
(ac)
+
C
2
H
2
(g)
Diariamente se procesan 850 kg de mineral que contiene 90 % de CaC
2
con 500 kg de
agua lquida. Con esta informacin determine:
a) Los kg de gas acetileno (C
2
H
2
)
obtenidos diariamente.
b) Los kg de reactivo en exceso que quedan sin reaccionar al final de la reaccin.
c) Realice el diagrama de entrada y salida de materiales y compruebe el balance de
masa.
Rpta: a) 310,78 Kg C
2
H
2
, b) 69,69 Kg H
2
O, c)
2 2 2 2 2
( ) Impurezas Mineral H O Ca OH C H H O
m m m m m m
850 500 884.53 310.78 69.69 85 Kg Kg Kg Kg Kg Kg
1350 1350 Kg Kg
MA41-Qumica UPC 2014-1
Taller N 9: Estequiometra y balance de masa Los profesores
16. Para producir hierro a partir de minerales se emplea la siguiente ecuacin qumica de la
reaccin:
Fe
2
O
3(s)
+ 3CO
(g)
2Fe
(s)
+ 3CO
2(g)
Si en el alto horno se colocan 200 toneladas de xido frrico (Fe
2
O
3
), y 90 toneladas de
CO, determine:
a) Las toneladas de las entradas y salidas en el diagrama de flujo y compruebe el
balance de masa.
b) El rendimiento del proceso, si se obtiene en la prctica 110 toneladas de Fe.
Rpta: a) , b) 91,67%
2 3 2 3 2
Fe O CO Fe O CO Fe
m m m m m
200 90 28.57 141.43 120 Ton Ton Ton Ton Ton
290 290 Ton Ton
Вам также может понравиться
- Problemas Coleccion Estequiometria ResueltosДокумент6 страницProblemas Coleccion Estequiometria ResueltosAlejandro RapalliniОценок пока нет
- Ejercicios y Problemas de Estequiometría y Ecuaciones QuímicasДокумент5 страницEjercicios y Problemas de Estequiometría y Ecuaciones QuímicasBruno IzquierdoОценок пока нет
- Taller 10 - Estequiometr A II y Balance de MasasДокумент6 страницTaller 10 - Estequiometr A II y Balance de MasasNeyson Osorio JananpaОценок пока нет
- Clase Práctica 10Документ2 страницыClase Práctica 10correofake09Оценок пока нет
- TALLER 08 Solucionado PDFДокумент15 страницTALLER 08 Solucionado PDFjeyra mendoza huamaniОценок пока нет
- Guía de Ejercicios de Estequiometría I - v2Документ4 страницыGuía de Ejercicios de Estequiometría I - v2JaredMárquezMaldonadoОценок пока нет
- 07 Taller 7 Balance de Masa y GasesДокумент3 страницы07 Taller 7 Balance de Masa y GasesCarlos QuintoОценок пока нет
- ESTEQUIOMETRÍAДокумент8 страницESTEQUIOMETRÍAPablo LemaОценок пока нет
- MA465 S10 S26 CS10 Caso 7 Produccion de Zinc 2021 AlumnosДокумент4 страницыMA465 S10 S26 CS10 Caso 7 Produccion de Zinc 2021 AlumnosNicole AparcanaОценок пока нет
- S04 S10 1 Lenguaje Químico 2021Документ27 страницS04 S10 1 Lenguaje Químico 2021Walter Perez JuscamaitaОценок пока нет
- QB Estequiometría IIДокумент2 страницыQB Estequiometría IINick Negrillo CalderónОценок пока нет
- Ejercicios Resueltos. Unidad 8 - QuímicaДокумент7 страницEjercicios Resueltos. Unidad 8 - QuímicaMax ChazzОценок пока нет
- Ejercicios Tema 1 - La Estructura de La MateriaДокумент3 страницыEjercicios Tema 1 - La Estructura de La MateriaAngelillo CañaillaОценок пока нет
- 10 Clase HalogenosДокумент60 страниц10 Clase HalogenosClaudiaОценок пока нет
- Informe de Laboratorio - Cinética QuímicaДокумент28 страницInforme de Laboratorio - Cinética QuímicaSTEPHANIE MILAGROS AVILA ALANYAОценок пока нет
- Estequiometría QuímicaДокумент6 страницEstequiometría QuímicaJess¡Liz GarzónОценок пока нет
- Unidades Quimicas SabДокумент4 страницыUnidades Quimicas SabLUISA ESPERANZA JORDAN CHOQQUEОценок пока нет
- Ejercicios de Caida Libre PDFДокумент1 страницаEjercicios de Caida Libre PDFEDISON PALMAОценок пока нет
- Solucion Prob. 2 y 3 Esteq.Документ8 страницSolucion Prob. 2 y 3 Esteq.Claudia AscencioОценок пока нет
- Ejercicios Quimica InorganicaДокумент6 страницEjercicios Quimica InorganicaGustavo AlboОценок пока нет
- Unidad 14 Reacciones Químicas. Ejercicios PropuestosДокумент3 страницыUnidad 14 Reacciones Químicas. Ejercicios Propuestosanon_335376133Оценок пока нет
- U3.1 - Reacciones - Quimicas (5) TODO LO DE BALANCEOДокумент25 страницU3.1 - Reacciones - Quimicas (5) TODO LO DE BALANCEOLEIDY CATHERINE MEDINA NAVARROОценок пока нет
- S11 Solucionario EstequiometríaДокумент8 страницS11 Solucionario EstequiometríaAngel EitanОценок пока нет
- Electroquimica 2013Документ19 страницElectroquimica 2013Julio OriaОценок пока нет
- COQ1 2020 C PDFДокумент1 175 страницCOQ1 2020 C PDFStiven AlvarezОценок пока нет
- Ejemplos de Quimica InorganicaДокумент3 страницыEjemplos de Quimica InorganicaRAUL VARGAS CHОценок пока нет
- Estequiometria IIДокумент36 страницEstequiometria IIEdgar PinedaОценок пока нет
- Cuestionario de Nomenclatura de Compuestos de Coordinación QUI 160Документ7 страницCuestionario de Nomenclatura de Compuestos de Coordinación QUI 160Adriana Toro RosalesОценок пока нет
- Taller de Quimica IonesДокумент2 страницыTaller de Quimica Ionesvictor herrera100% (1)
- Presentación 9Документ12 страницPresentación 9Juan Carlos Ibarra CaceresОценок пока нет
- Reacciones QuimicasДокумент4 страницыReacciones QuimicasEuder Goicochea ZamoraОценок пока нет
- Guia de Ejercicios 530024 2TДокумент8 страницGuia de Ejercicios 530024 2TJerico JosuéОценок пока нет
- Ejercicios Equilibrio QuímicoДокумент5 страницEjercicios Equilibrio Químicofaltriquera0% (1)
- Ejercicios de Quimica Molaridad PH y RedoxДокумент12 страницEjercicios de Quimica Molaridad PH y RedoxJhonny CehОценок пока нет
- Lab3 c3 Bim2. Conservación Mat.Документ2 страницыLab3 c3 Bim2. Conservación Mat.eduwigisruiz0% (1)
- Porcentaje en VollumenДокумент3 страницыPorcentaje en VollumenKarla SalazarОценок пока нет
- Ejercicios AnaliticaДокумент2 страницыEjercicios AnaliticaAle SalazarОценок пока нет
- Tema 2 - Estequiometria y Reacc QcasДокумент31 страницаTema 2 - Estequiometria y Reacc QcasJulietaRocioAmeriОценок пока нет
- Taller de HidroxidosДокумент5 страницTaller de Hidroxidosjoaquin albertoОценок пока нет
- 00 Cuaderno de Trabajo 2021 02Документ220 страниц00 Cuaderno de Trabajo 2021 02MILKAR NEIRA RUIZОценок пока нет
- Problemas de La Mol PDFДокумент3 страницыProblemas de La Mol PDFItzelОценок пока нет
- Problemas Resueltos Estequiometria y GasesДокумент15 страницProblemas Resueltos Estequiometria y GasesDiego AndrésОценок пока нет
- CG-Sem2-Ejercicios - Números CuánticosДокумент3 страницыCG-Sem2-Ejercicios - Números Cuánticosyordan reyna100% (1)
- Problemas EstequiométricosДокумент3 страницыProblemas EstequiométricosjramosburgosОценок пока нет
- Practica Dirigida 05 (Enlace Químico) ClaseДокумент9 страницPractica Dirigida 05 (Enlace Químico) ClaseNormiss Castro VincesОценок пока нет
- Repaso 5Документ5 страницRepaso 5lizethОценок пока нет
- Taller de Enlace QuímicoДокумент4 страницыTaller de Enlace QuímicoYulanis Avila100% (1)
- EjerciciosdexidosДокумент3 страницыEjerciciosdexidosCarlos Ricardo Prado ElíasОценок пока нет
- EnlaceQuim EjercДокумент24 страницыEnlaceQuim Ejercmaria100% (2)
- Estequiometria de La ComposiciónДокумент5 страницEstequiometria de La ComposiciónAlberto Córdoba100% (1)
- 7 Estequiometria PDFДокумент8 страниц7 Estequiometria PDFFernanda Patiño BardalesОценок пока нет
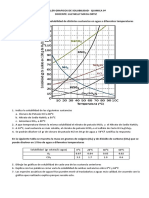
- Taller Graficos de SolubilidadДокумент1 страницаTaller Graficos de SolubilidadLuz Nelly Maya OrtizОценок пока нет
- Quimica N3Документ5 страницQuimica N3Josué ChimarroОценок пока нет
- Estequiometria Problemas 02Документ1 страницаEstequiometria Problemas 02andres_old_condeОценок пока нет
- Cinética y Equilibrio Químico.-Test 02Документ3 страницыCinética y Equilibrio Químico.-Test 02Diego ParedesОценок пока нет
- Nivel1 Serie1Документ12 страницNivel1 Serie1Cesar OviedoОценок пока нет
- Ejercicios Tema 3. EstequiometriaДокумент4 страницыEjercicios Tema 3. EstequiometriaKarla GОценок пока нет
- TP-reacciones QuimicasДокумент4 страницыTP-reacciones QuimicasdelfinaОценок пока нет
- Guia de Discusion 2 Reaccion QuimicaДокумент8 страницGuia de Discusion 2 Reaccion QuimicaDanny RiveraОценок пока нет
- Problemas de Quimica I - 8 JulioДокумент5 страницProblemas de Quimica I - 8 JulioAndre BarrantesОценок пока нет
- Interpretación de Datos de Química Del AguaДокумент65 страницInterpretación de Datos de Química Del AguaHector TineoОценок пока нет
- Leacom Sílabo Por Competencias - Coaching y Resolución de Conflictos 2017-2 VFinalДокумент7 страницLeacom Sílabo Por Competencias - Coaching y Resolución de Conflictos 2017-2 VFinalHector TineoОценок пока нет
- SyllabusДокумент6 страницSyllabusHector TineoОценок пока нет
- Seminario de Investigacion Academica IIДокумент7 страницSeminario de Investigacion Academica IIHector TineoОценок пока нет
- Tabla Frec VCCДокумент19 страницTabla Frec VCCHector TineoОценок пока нет
- Guía General Del CursoДокумент9 страницGuía General Del CursoHector Tineo100% (1)
- Caso DanfossДокумент3 страницыCaso DanfossHector Tineo0% (1)
- Cálculo I 2014 01-2Документ7 страницCálculo I 2014 01-2Hector TineoОценок пока нет
- Tipos y Grados de Conocimiento en SpinozaДокумент4 страницыTipos y Grados de Conocimiento en SpinozaHelmut AmadeusОценок пока нет
- El Imperialismo JaponésДокумент1 страницаEl Imperialismo JaponéstobepuОценок пока нет
- Educacion y Desarrollo Social PDFДокумент9 страницEducacion y Desarrollo Social PDFRosita Ocas QuilicheОценок пока нет
- AporofobiaДокумент5 страницAporofobiaalfmotattoОценок пока нет
- Ley 27444 Ley Del Procedimiento Administrativo GeneralДокумент2 страницыLey 27444 Ley Del Procedimiento Administrativo GenerallusolОценок пока нет
- Tipos de ReproducciónДокумент6 страницTipos de Reproducciónsat wesx zuunОценок пока нет
- Amor y Sexo Consciente Una Guía Práctica para Crear Relaciones ExtraordinariasДокумент222 страницыAmor y Sexo Consciente Una Guía Práctica para Crear Relaciones ExtraordinariasGiuliana BozoОценок пока нет
- Arcadia Quest Modo SolitarioДокумент6 страницArcadia Quest Modo SolitarioDaniel ValdiviesoОценок пока нет
- EcfrasisДокумент5 страницEcfrasisNirabeth Ovalles RondónОценок пока нет
- Desarrollo Motor, Habilidades y Destrezas Del IndividuoДокумент12 страницDesarrollo Motor, Habilidades y Destrezas Del IndividuoMaria RiveoОценок пока нет
- JustificacionДокумент1 страницаJustificacionSheyla GarcésОценок пока нет
- Endocarditis Bacteriana: Refiere A Una Infección Bacteriana de Superficie Endocárdica y Válvulas CardiacasДокумент20 страницEndocarditis Bacteriana: Refiere A Una Infección Bacteriana de Superficie Endocárdica y Válvulas CardiacasluisОценок пока нет
- Periodico MuralДокумент5 страницPeriodico MuralJuanmatias ZalasarОценок пока нет
- Presentación CefaleasДокумент65 страницPresentación CefaleasTaquito My LoveОценок пока нет
- Mapa Conceptual Cultura y ValoresДокумент1 страницаMapa Conceptual Cultura y Valoresgalo Galo472100% (2)
- Bimferénciate Especialista3DДокумент15 страницBimferénciate Especialista3DMiguel SambranoОценок пока нет
- Monografia Disidentes en La IASDДокумент28 страницMonografia Disidentes en La IASDEdgardo Iuorno90% (10)
- Auditoria IntegralДокумент118 страницAuditoria IntegralLuciano Pier Bedón RavichaguaОценок пока нет
- Flexiòn BiaxialДокумент20 страницFlexiòn BiaxialIsaac QuevedoОценок пока нет
- Universidad Nacional Del Callao: Dirección Estratégica en La Indústria PesqueraДокумент62 страницыUniversidad Nacional Del Callao: Dirección Estratégica en La Indústria PesqueraMax Rios PonceОценок пока нет
- Los Fundamentos Teóricos de La Historia de Los ConceptosДокумент18 страницLos Fundamentos Teóricos de La Historia de Los ConceptosClaudio RamosОценок пока нет
- Historia de La CalidadДокумент6 страницHistoria de La CalidadRubén Perez AlonsoОценок пока нет
- Mayquel Bernal Diagnostico y Desarrollo Organizacional Tarea 3Документ11 страницMayquel Bernal Diagnostico y Desarrollo Organizacional Tarea 3Mayquel Bernal0% (1)
- Matriz Planificacion de Objetivos Del Plan de MercadosДокумент2 страницыMatriz Planificacion de Objetivos Del Plan de MercadosJuan MaldiñigОценок пока нет
- TEMA 11 DueloДокумент15 страницTEMA 11 DueloMaría Pilar GonzálezОценок пока нет
- Ya Te Perdi La FeДокумент2 страницыYa Te Perdi La FeOscar TorresОценок пока нет
- Informe Fractura ExpuestaДокумент4 страницыInforme Fractura ExpuestaDayana ChuquimiaОценок пока нет
- Häring, B., El Sacramento de La ReconciliaciónДокумент180 страницHäring, B., El Sacramento de La Reconciliaciónlamontoya100% (1)
- Guias de Laboratorio Resistencia de MaterialesДокумент21 страницаGuias de Laboratorio Resistencia de MaterialesHarold Valle ReyesОценок пока нет
- Informe de Laboratiorio de Densidad en El TerrenoДокумент19 страницInforme de Laboratiorio de Densidad en El TerrenostivenОценок пока нет