Академический Документы
Профессиональный Документы
Культура Документы
Lab Oratorio
Загружено:
Manuela MendozaАвторское право
Доступные форматы
Поделиться этим документом
Поделиться или встроить документ
Этот документ был вам полезен?
Это неприемлемый материал?
Пожаловаться на этот документАвторское право:
Доступные форматы
Lab Oratorio
Загружено:
Manuela MendozaАвторское право:
Доступные форматы
LABORATORIO N1
VOLUMEN MOLAR PARCIAL
Objetivo.-
Determinar los volmenes molares parciales de los constituyentes de una mezcla y
estudiar la variacin de los mismos con la concentracin. Se considera para el estudio
una solucin binaria de solvente y soluto.
Fundamento Terico.-
El volumen total V de una solucin binaria en trminos de los volmenes molares
parciales
, y nmeros de moles
, respectivamente para solvente y soluto,
se expresa:
(1.1)
Un mtodo para medir el volumen parcial es determinando el volumen molar aparente
, el cual se define:
(1.2)
En donde,
(1.3)
Y,
(1.4)
Siendo
las masas molares de solvente y soluto.
El volumen molar del
solvente puro. La densidad de la solucin y
la densidad del solvente puro.
Combinando (1.2), (1.3) y (1.4) obtenemos:
+ (1.5)
Si la masa del solvente
(la molalidad).
+ (1.6)
Una vez conocido
se puede determinar: (
graficando
En el caso
de electrolitos se encuentra que
aumenta linealmente con .
Es decir:
Podemos usar las dos siguientes ecuaciones para hallar los volmenes molares
parciales
] (1.7)
(1.8)
Material y Equipo.-
Acetona, agua destilada y cloruro de sodio; esptula, matraces volumtricos de 100ml.
Papel filtro, picnmetro; pinzas para bureta, pipeta volumtricas de 50ml; termmetro,
etc.
Procedimiento.-
Se separan 100ml de una solucin acuosa 3-2m de NaCl. Con esta solucin madre se
preparan otras soluciones de 1.2, 0.8, 0,6; 0,4; 0,2 molar. Las densidades de las
soluciones se determinan con un picnmetro, pudiendo usarse el de Ostwald
Sprengel o el de Weld.
Determinar el volumen del picnmetro utilizando la densidad del agua destilada y la
diferencia de masa entre el picnmetro con agua y vaco.
Utilizacin de Datos, Clculos y resultados.-
Tabulamos los datos detalladamente. Calcular la molalidad (m) de las soluciones a
partir de la molaridad (M) y la densidad (d) de las mismas.
) (
)
En donde
es la masa molar del soluto.
Calcular el volumen molar aparente de soluto usando la ecuacin (1.6). Graficar
y determinar (
Calcular
usando las ecuaciones (1.7) y (1.8).
Para la mezcla de M = 0,4 de agua y NaCl (
), encontraremos su molalidad
(m), encontraremos
y tambin
paso por paso y luego especificaremos solo
los datos de cada una de las dems mezclas para abreviar pasos.
PICNMETRO 1
1) Peso Picnmetro Vaco: 16.6315 g
2) Peso Picnmetro con Agua: 41.3623 g
Calculando V
p
(Volumen del picnmetro) con la ecuacin (1.8)
Luego, hallamos la densidad de cada solucin
Para el picnmetro con solucin 0.9 M
Para el picnmetro con solucin 0.8 M
PICNMETRO 2
1) Peso Picnmetro Vaco: 15.5449 g
2) Peso Picnmetro con Agua: 40.5239 g
Calculando V
p
(Volumen del picnmetro) con la ecuacin (1.8)
Luego, hallamos la densidad de cada solucin
Para el picnmetro con solucin 0.4 M
PICNMETRO 3
1) Peso Picnmetro Vaco: 16.5038 g
2) Peso Picnmetro con Agua: 41.5807 g
Calculando V
p
(Volumen del picnmetro) con la ecuacin (1.8)
Luego, hallamos la densidad de cada solucin
Para el picnmetro con solucin 0.2 M
Para el picnmetro con solucin 0.6 M
Para el picnmetro con solucin 1.0 M
Ahora podemos hallar la molalidad:
Para la solucin 0.2 M
) (
) (
)
Necesitamos para graficar la funcin:
Hallamos
[
( )()
Tabla de datos obtenidos anteriormente
Muestra M m
1 0.2 0.2014 15.00 0.4488
2 0.4 0.4047 19.74 0.6362
3 0.6 0.6083 16.34 0.7799
4 0.8 0.8145 17.63 0.9025
5 0.9 0.9199 19.85 0.9591
6 1.0 1.0305 25.94 1.0151
Representaremos la grfica de los valores respectivos:
Grfica
Segn la grfica, (
Aplicando mtodo de los mnimos cuadrados
N x y x^2 x*y
1 0.4488 15 0.201421 6.732
2 0.6362 19.74 0.404750 12.558588
3 0.7799 16.34 0.608244 12.743566
4 0.9025 17.63 0.814506 15.911075
5 0.9591 19.85 0.919873 19.038135
6 1.0151 25.94 1.030428 26.331694
SUMATORIA 4.7416 114.5 3.979223 93.315058
( )
()
() ()
() ()
( )
()
() ()
() ()
Calculando
2
y
1
con las ecuaciones (1.12) y (1.15) respectivamente.
Determinando
para la solucin 0.2 M, con
(
y = 12.191x + 9.449
R = 0.464
0
5
10
15
20
25
30
0 0.2 0.4 0.6 0.8 1 1.2
Q
2
m^1/2
( )()
o Determinando
[ () ()
()]
Tabla que representa los datos obtenidos en el laboratorio y clculos.
Conclusiones.-
Concluimos en que obtuvimos los valores correctos en la prctica siguiendo los pasos
que se dieron en el laboratorio y en los clculos.
Mezcla M d (agua) d(solucin) m
2
m^(1/2) V V
1 0.2 0.9962 1.0049 0.2014 15.00 0.4488 17.7356 18.0588
2 0.4 0.9962 1.0117 0.4047 19.74 0.6362 23.6378 18.0405
3 0.6 0.9962 1.0215 0.6083 16.34 0.7799 21.0942 18.0166
4 0.8 0.9962 1.0289 0.8145 17.63 0.9025 23.1313 17.9881
5 0.9 0.9962 1.0310 0.9199 19.85 0.9591 25.6964 17.9719
6 1 0.9962 1.0288 1.0305 25.94 1.0151 32.1279 17.9539
LABORATORIO N2
TEMPERATURA CRTICA DE SOLUCIN
Objetivo.-
Estudiar el equilibrio heterogneo de dos lquidos. Determinar su curva de solubilidad y
aplicando la regla de las fases de Gibbs. Se considera para el estudio el sistema Fenol
Agua.
Fundamento Terico.-
Existen sistemas lquidos parcialmente miscibles cuya solubilidad es alterada con la
variacin de la temperatura. Si se grafica la temperatura de solubilidad vs la
composicin se obtiene una curva llamada curva de solubilidad o de equilibrio.
Algunos sistemas exhiben una temperatura mxima de solucin (temperatura crtica
de solucin), por ejemplo agua anilina. Otros exhiben temperatura mnima de
solucin, agua trietilamina; otros mxima y mnima, agua nictica; y aun otros ni
mxima ni mnima.
El sistema Fenol Agua presenta solubilidad mutua con una temperatura mxima de
solucin.
Si un par lquido con temperatura crtica de solucin alto se encuentra a una
temperatura inferior a esta y si existen 2 fases independientes de las cantidades de las
2 fases existentes.
Una mayor interpretacin del comportamiento de estos sistemas bajo ciertas
condiciones se consigue graficando la temperatura vs la composicin.
Material y Equipo.-
Agua y fenol (80%), tubos de ensayo pequeos con sus respectivos tapones de
corcho; rejilla con asbesto, trpode, mechero, u otro equipo de calentamiento para
bao mara; termmetro de 0C a 110C, bureta y vasos de 250ml.
Procedimiento.-
Se prepara una solucin acuosa de fenol al 80%, aadiendo 125ml de agua a 500g de
fenol tipo reactivo; se agita hasta la obtencin de una solucin homognea.
De la solucin madre se vierte a travs de una bureta a 10 tubos de ensayo,
volmenes de 10, 9, 8, 7, 6, 5, 4, 3, 2 y 1,25ml; anteriores 0, 1, 2, 3, 4, 5, 6, 7, 8, y
8,75ml de agua destilada. Obtenindose as un intervalo de concentracin de fenol de
10 a 80%.
Cada tubo de ensayo con tapn, insertamos un termmetro de 110C dentro de l, y
luego lo ponemos a bao mara. Se calienta lentamente el agua, agitando
constantemente tubo siempre dentro del bao mara. Cuando el lquido turbio se
aclara se anota la temperatura. Se omite el calentamiento manteniendo el tubo dentro
del bao, cuando reaparezca la turbidez se anota nuevamente la temperatura que
marca el termmetro. Como temperatura de miscibilidad se considera el promedio de
las 2 temperaturas, para cada tubo en particular. No calentar las mezclas a
temperaturas mayores a 75C ya que pueden descomponerse.
Utilizacin de Datos, Clculos y Resultados.-
mezcla Volumen (ml) Temperatura Solubilidad, C
Fenol (80%) agua T
1
T
2
T
PROM
1 10 0 28.5 13.5 13.5
2 9 1 44 45 44.5
3 8 2 59 58 58.5
4 7 3 64 62 63
5 6 4 26 50 38
6 5 5 71 70 70.5
7 4 6 76 74 75
8 3 7 61 65 63
9 2 8 52 45 50.5
10 1.25 8.75 30 30 30
()
En el sistema Fenol Agua calculamos %fenol y %molar
Para la mezcla 1
Tabla de resultados obtenidos anteriormente
Mezcla %peso
(fenol)
%molar
(fenol)
T
SOLUBILIDAD
1 80 43.37 13.5
2 72.29 33.32 44.5
3 64.52 25.83 58.5
4 56.69 20.04 63
5 48.79 15.43 38
6 40.83 11.67 70.5
7 32.80 8.55 75
8 24.70 5.91 63
9 16.54 3.65 50.5
10 10.37 2.17 30
Conclusin.-
Se determin la temperatura crtica de solucin. Tambin se grafic correctamente la
temperatura vs fraccin molar y temperatura vs porcentaje en peso agua fenol.
-20
0
20
40
60
80
-20 0 20 40 60 80 100 T
e
m
p
e
r
a
t
u
r
a
d
e
s
u
l
u
b
i
l
i
d
a
d
%peso
Temperatura de sulubilidad y
%peso
-10
0
10
20
30
40
50
60
70
80
-10 0 10 20 30 40 50
T
e
m
p
e
r
a
t
u
r
a
d
e
s
u
l
u
b
i
l
i
d
a
d
%molar
Temperatura de sulubilidad y %molar
LABORATORIO N 3
DESTILACIN FRACCIONADA
Objetivo.-
Estudiar la separacin de una mezcla lquida binaria por destilacin fraccionada a
reflujo total, usando mediciones del ndice de refraccin para determinar la
composicin del destilado y residuo.
Fundamento Terico.-
La destilacin fraccionada ha permitido enormes adelantos en las operaciones de
separacin de materiales por destilacin tales como en la refinacin de petrleo y en la
concentracin de istopos, y por consiguiente, un progreso notable en el diseo de
equipo para estos fines.
La separacin de dos lquidos por simple vaporizacin y condensacin no es efectiva,
excepto cuando sus respectivos puntos de ebullicin difieren ampliamente. Una mejor
separacin se consigue a base de una serie de destilaciones simples, lo cual sin
embargo, es laborioso. Se obtiene el mismo resultado usando una columna de
fraccionamiento, dentro de la cual asciende vapor ponindose en contacto con parte
del condensado que desciende dentro de la misma. Los componentes menos voltiles
se condensan de los vapores ascendentes y los ms voltiles de vaporizan de la fase
lquida descendente, por lo que la destilacin a travs de la columna es equivalente a
varias destilaciones simples sucesivas. La separacin es mejor, si la mejor parte de
vapor condensado en la parte superior de la columna regresa como reflujo. La razn
de reflujo se define como la razn de lquido que regresa a la columna a la cantidad de
lquido separado como destilado. La temperatura ser ms baja en la parte superior,
donde se concentra el componente ms voltil, que en la parte inferior, donde se
encuentra en mayor proporcin el componente menos voltil.
Si se usan columnas empaquetadas, se consiguen mejor contacto de las fases lquido
vapor, pero el empaquetamiento no debe retener una fraccin grande del lote que se
destila ya que disminuye el grado de separacin.
La efectividad de una columna de destilacin se expresa en trminos de platos
tericos. El plato terico se define como una seccin hipottica de columna que
produce separacin tal de componentes que el vapor que sale por la parte superior de
la seccin tiene la composicin de vapor que est en equilibrio con el lquido que cae
por el fondo de la seccin. Una columna formada por un simple tubo de 1cm de
dimetro y un metro de alto podra ser equivalente slo a un plato terico, mientras
que el mismo tubo relleno de empaquetamiento adecuado puede equivaler a 20 o ms
platos tericos. El nmero de platos tericos aumenta al disminuir la relacin de
reflujo.
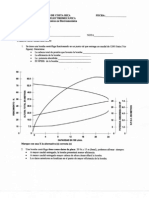
Para determinar el nmero de platos tericos debe disponerse de datos de equilibrio
lquido (L) vapor (V) de las substancias consideradas para trazar grficas como la
grfica siguiente:
Para el sistema
; o contar con datos de temperatura
Vs composicin,
para trazado de una grfica y en base a la cual se obtiene los datos de composicin de
equilibrio lquido vapor
Material y Equipo.-
Sistemas lquidos:
, etc.; columna vigreux, columnas
empaquetadas (empaquetamiento: conos dobles, sillas de acero inoxidables, hlices
de vidrio o bolitas de vidrio), cabeza de destilacin con refrigerante de dedo y
termmetro, manta de calentamiento con tela de vidrio y autotransformador variable,
probeta graduada de 100ml, tubos de ensayo pequeos y corchos; refractmetro,
soportes, pinzas, mangueras, etc.
Procedimiento Experimental.-
Se mezcla 10ml de
con 10 ml de
en el matraz de destilacin, el cual, se
calienta con manta de calentamiento controlada con autotransformador variable. El
lquido debe hervir vigorosamente hasta que se produzca condensacin en la parte
superior de la columna. En caso de que sta sea inundada, se debe disminuir el
calentamiento. El refrigerante se instala en una posicin tal que todo el condensado
regrese a la columna.
Despus de establecerse el equilibrio, tomar las lecturas de temperatura en el
termmetro cuando stas sean constantes. Separar muestras de destilado y residuo.
Para la coleccin del destilado, el refrigerante debe estar instalado en una posicin tal
que permita que el destilado gotee a una probeta graduada. Desechar las 3 primeras
gotas, y recolectar una muestra de un mml para anlisis respectivo con un
Refractmetro. Por el brazo lateral del matraz de destilacin separar con una pipeta 1
ml de lquido y guardarlo para su anlisis en el refractmetro (dependiendo de las
circunstancias previamente puede quitarse el calentamiento). La eficiencia de la
columna determinada en base a estas dos muestras corresponde a la eficiencia de la
columna a reflujo total.
Se puede repetir el procedimiento con la columna empaquetada para fraccionamiento,
la cual requiere mayor tiempo para alcanzar el equilibrio pero se obtiene mayor
eficiencia de separacin. Puede usarse tambin una columna de platos de burbujeo. Si
se usa la columna empaquetada, la columna y matraz de destilacin se evacan y
secan, y se introducen 30ml de cloroformo y 30 ml de benceno. El condensado de
reflujo se ajusta para razn de reflujo 5:1 a 10:1, segn se ha calculado de las
velocidades de goteo del refrigerante a reflujo y del tubo de destilacin. El destilado se
colecta en una probeta. Despus de cada 3ml de destilado se toma una muestra de
1ml en una botellita provista de tapn, y posteriormente a esas muestras se les mide el
ndice de refraccin. Se debe llevar un registro del volumen total de lquido destilado y
de la lectura del termmetro al tiempo de tomar cada muestra. Tambin se anota el
volumen total final del destilado.
Utilizacin de Datos, Clculos y Resultados.-
Tabular los datos detalladamente. Los ndices de refraccin del benceno, tetracloruro
de metilo y de mezclas de los 2 vs %molar de tetracloruro de metilo, se grafica en
papel coordenado. Con la curva obtenida determinar la composicin de una mezcla
lquida desconocida por interpolacin del ndice de refraccin. En esta forma se
determinan las composiciones del destilado y residuo. Con datos de composicin L V
o en base a datos de temperatura (de ebullicin) composicin, trazar la curva de
equilibrio. Fijar los puntos representativos del destilado y residuo, y proceder a la
determinacin del nmero de paltos tericos tal como se ha explicado en la seccin
terica.
En nuestro caso tomamos como A: agua (18g/mol) y B: metanol (32g/mol) con
densidades de 0,9852 y 0,7880g/ml respectivamente.
Tabla de los datos obtenido en el laboratorio, detalladamente.
Mezcla d(g/ml) W(g) Moles (mol) Fraccin Molar (Xi) I.R.M.
N V(ml)
A B A B A B A B A B
1 5 0 0.9852 0 4.9260 0 0.2737 0 1 0 1.3332
2 4 1 0.9852 0.7880 3.9408 0.788 0.2189 0.0246 0.8989 0.1011 1.3320
3 3 2 0.9852 0.7880 2.9556 1.576 0.1642 0.0493 0.7693 0.2307 1.3310
4 2 3 0.9852 0.7880 1.9704 2.364 0.1095 0.0739 0.5971 0.4029 1.3295
5 1 4 0.9852 0.7880 0.9852 3.152 0.0547 0.0985 0.3572 0.6428 1.3280
6 0 5 0 0.7880 0 3.940 0 0.1231 0 1 1.3260
7 3.5 1.5 0.9852 0.7880 3.4482 1.182 0.1916 0.0369 0.8384 0.1616 1.3315
6 2.5 2.5 0.9852 0.7880 2.463 1.970 0.1368 0.0616 0.6897 0.3103 1.3300
9 1.5 3.5 0.9852 0.7880 1.477 2.758 0.0821 0.0862 0.4879 0.5121 1.329
10 0.5 4.5 0.9852 0.7880 0.4926 3.546 0.0274 0.1108 0.1981 0.8019 1.327
El compuesto ms voltil es el metanol, entonces, hacemos una grfica Fraccin molar
de metanol Vs ndice de Refraccin de la mezcla para hallar las fracciones molares
que ms adelante usaremos para hallar el nmero de platos tericos.
Calculando presin del metanol en vapor puro
1.324
1.326
1.328
1.33
1.332
1.334
0 0.2 0.4 0.6 0.8 1
I
R
FRACCION MOLAR metanol
IR vs FRACCION MOLAR
SUSTANCI
A
A B C D E
METANOL 45.6171 -3.2447x10
3
-1.3988x10
1
6.6365x10
-3
-1.0507x10
-13
AGUA 29.8605 -3.1522x10
3
-7.3037 2.4247x10
-9
1.809x10
-6
A una temperatura de: 65, 70, 75, 80, 85, 90, 95, 100 C
Temperatura
(C)
Presin de vapor para el
agua
Presin de vapor
para el metanol
65 186.50 769.21
70 232.39 933.17
75 287.47 1124.97
80 353.18 1348.12
85 431.05 1606.36
90 522.80 1903.74
95 630.29 2244.57
100 755.54 2633.44
Calculando fraccin molar en el lquido del metanol
)
(
)
Calculando fraccin molar de vapor del metanol
Fraccin molar en el
lquido del metanol
Fraccin molar de
vapor del metanol
0.9842 0.9961
0.7529 0.9245
0.5642 0.8351
0.4089
0.6053
0.2799
0.5916
0.1718
0.4303
0.0803
0.2372
0.0024
0.0083
Conclusin.-
Se grafic correctamente el diagrama temperatura composicin para un sistema
binario completamente soluble en la fase lquida.
Se grafic correctamente la grfica lquido vapor para el sistema metanol agua
para luego determinar el nmero de platos tericos.
Se encontr el nmero de platos tericos correctamente.
0
20
40
60
80
100
120
0 0.2 0.4 0.6 0.8 1 1.2
T
e
m
p
e
r
a
t
u
r
a
(
C
)
fraccin molar del metanol
Diagrama temperatura-composicion
metanol
Series1
Series2
Poly. (Series1)
Poly. (Series2)
LABORATORIO N 4
DIAGRAMA DE EQUILIBRIO DE FASES DE UN SISTEMA LQUIDO
TRICOMPONENTE
Objetivo.-
Trazar un diagrama de equilibrio de fases para un sistema lquido ternario con 2
componentes originalmente inmiscibles, en base a mediciones experimentales de
solubilidad y equilibrio, analizando el diagrama resultante con aplicacin de la regla de
las fases de Gibbs. Estos diagramas se usan principalmente en los clculos de los
procesos de extraccin con solvente.
Para este estudio se considera el sistema Benceno cido Actico Agua, con los
componentes inmiscibles benceno y agua, a presin y temperatura ambiente.
Fundamento Terico.-
A presin y temperatura constante, las composiciones de mezclas lquidas ternarias
pueden representarse en un diagrama coordenado triangular trazado en 2
dimensiones, usndose para tal fin un triangulo equiltero. Cada lado del triangulo
representa la composicin de 2 componentes, cada vrtice un componente puro y un
punto dentro del triangulo una mezcla ternaria. Si adems de la composicin se
involucra otra variable, por ejemplo la temperatura; para determinacin del diagrama
de equilibrio la fase se requerir de una tercera dimensin, resultando una figura en el
espacio.
Si a mezclas binarias de lquidos inmiscibles o parcialmente miscibles, se adiciona un
tercer lquido soluble en cada uno de estos, se obtiene un tercer lquido soluble en
cada uno de estos, se obtienen mezclas ternarias formando una sola fase o
separables en 2 fases (o capas), dependiendo de las concentraciones. Los puntos
representativos de las composiciones de las mezclas ternarias comenzando a formar
una sola fase, dentro del triangulo equiltero, determinan una curva llamada curva de
solubilidad o de equilibrio.
Diagrama de equilibrio de fases para un sistema liquido ternario
con 2 componentes parcialmente miscibles A y B.
Esta curva puede pasar por dos vrtices del triangulo cuando dos de los componentes
son inmiscibles inicialmente, caso del benceno agua en el sistema benceno agua
acido actico, o puede interceptar a un lado del triangulo cuando dos de los
componentes son parcialmente miscibles como agua y tricloruro de metilo en el
sistema tricloruro de metilo acido actico agua.
Todo punto de afuera de la curva representa un sistema ternario completamente
miscible (una sola fase), y un punto por debajo de la curva un sistema separable de 2
fases. La lnea que une 2 puntos de la curva tal como a y b en la primera figura se
denomina lnea de unin o de reparto, que no es necesariamente paralela a la base o
paralela a otra y otras lneas de unin. Se pueden preparar varias mezclas lquidas
ternarias separables en 2 capas y obtener varias lneas de reparto, como cd, ef y gh
en la segunda figura antes mostradas; las composiciones de las capas
respectivamente dependen de las composiciones de las mezclas ternarias originales.
A medidas que se aade el componente miscible (al sistema binario inmiscible o
parcialmente miscible) las composiciones de las 2 capas conjugadas se tornan ms
semejantes una de otra, hasta que se obtiene una sola fase o capa. El punto
representativo de la composicin de esta fase nica se denomina punto crtico.
Material y Equipo.-
cido actico glacial, benceno puro, agua destilada, soluciones diluidas de hidrxido
de sodio 0,5N, 0,01N y 0,001N; y fenolftalena. Frascos de vidrio de aproximadamente
125ml con tapn de vidrio esmerilado, bureta de 50ml, embudos de decantacin,
pipetas de 5ml y bombilla. Equipo de agitacin magntica, soportes y pinzas. Papel
coordenado triangular.
Procedimiento Experimental.-
Diagrama de equilibrio de fases para un sistema lquido ternario con dos
componentes inmiscibles A y B
A. Determinacin de la curva de solubilidad:
N V(ml) ml de
C
%A %B %C %TOTAL
A B total
1 0.3 9.7 10 5.0 2.9 62.8 34.3 100
2 0.4 9.6 10 6.6 3.5 55.8 40.7 100
3 0.5 9.5 10 7.9 4.0 51.0 45.0 100
4 1 9 10 10.5 6.9 41.6 51.5 100
5 2 8 10 11.0 13.2 35.3 51.5 100
6 3 7 10 11.3 19.1 29.8 51.0 100
7 4 6 10 11.8 24.4 24.5 51.1 100
8 5 5 10 12.1 29.6 19.8 50.7 100
9 6 4 10 10.8 36.7 16.4 46.9 100
10 7 3 10 10.5 42.6 12.2 45.2 100
11 8 2 10 7.8 53.8 9.0 37.2 100
12 9 1 10 7.1 61.2 4.5 34.2 100
13 9.3 0.7 10 5.3 68.8 3.5 27.8 100
14 9.5 0.5 10 5.0 71.0 2.5 26.5 100
15 9.6 0.4 10 4.4 73.9 2.1 24.0 100
B. Determinacin de las lneas de reparto:
Preparar mezclas ternarias (en cantidades adecuadas) de formol, cido actico y
agua, con las siguientes composiciones de volumen:
N V(ml) %A %B %C %TOTAL
A B C TOTAL
L-1 4.5 4.5 1 10 54.8 36.6 8.6 100
L-2 4.5 3.5 2 10 54.5 28.3 17.2 100
L-3 4.5 2.5 3 10 54.2 20.1 25.6 100
L-4 4.5 1.5 4 10 54.0 12.0 34.0 100
Siendo A: cloroformo, B: agua y C: cido actico
Adicionar cada mezcla a un embudo de decantacin, agitar vigorosamente y dejarlo
reposar para permitir la formacin de 2 capas. Separar una cantidad adecuada de
cada capa (dependiendo de la cantidad de mezcla original), pesarla y titularla con
solucin diluida de NaOH, usando solucin de NaOH de mayor dilucin para la capa
bencnica; utilizar como indicador fenolftalena. Determinar el contenido de HAc en
cada capa en porcentaje en peso o en fraccin molar, para su representacin en la
porcin correspondiente de la curva de solubilidad.
Hallamos las lneas de reparto:
V(ml) W (g) Gasto NaOH
(0.5N)
WHAc(g) %W (HAc)
L-1
CA 3 2.8911 17.3 0.5194 17.9
CC 3 4.0262 2.10 0.0631 1.6
L-2
CA 3 2.9253 33.7 1.0118 34.6
CC 3 4.0236 8.80 0.2642 6.6
L-3
CA 3 3.0399 51.1 1.5343 50.5
CC 3 3.7813 21.4 0.6425 16.9
L-4
CA 2.9 3.0921 59.3 1.7805 57.6
CC 3 3.7167 32.4 0.9728 26.2
Para hallar el porcentaje en peso de Hac de la capa acuosa en la lnea de reparto, se
tomo el siguiente paso:
()
Para hallar el porcentaje en peso de Hac de la capa clorofrmica en la lnea de
reparto, se tomo el siguiente paso:
()
Conclusin.-
Se pudo determinar satisfactoriamente la curva de solubilidad en el sistema lquido
tricomponente. Tambin se pudo determinar sus respectivas lneas de reparto (L-1, L-
2, L-3, L-4). Hallamos tambin el punto crtico para este sistema ternario graficando los
datos:
LABORATORIO N 5
MASA MOLAR DE UN SOLUTO NO VOLATIL
Objetivo.-
Determinar la masa molar de un soluto no voltil en base a mediciones
experimentales de la elevacin del punto de ebullicin del solvente en solucin de este
soluto, usando el termmetro diferencial Beckman.
Fundamento Terico.-
En soluciones de solutos no voltiles, la presencia de soluto aumenta el punto de
ebullicin del solvente; este incremento o ascenso ebulloscpico
se determina por
la ecuacin:
] ()
Donde R es la constate de los gases, To la temperatura normal de ebullicin del
solvente puro.
el calor molar de vaporizacin y nmero de moles de
solvente respectivamente, y m la molalidad de la solucin. El trmino entre corchetes
es funcin de la naturaleza del solvente y se le denomina constante ebulloscpica del
solvente, Ke; y as la ecuacin (6.19 se puede escribir en la forma:
()
La molalidad se da por:
()
En la que
son la masa y la masa molar del soluto respectivamente, y
la
masa del solvente (lquido).
De la combinacin de (6.2) y (6.3):
()
La ecuacin (6.4) es la expresin matemtica para la determinacin de la masa molar
del soluto
, midiendo experimentalmente la elevacin del punto de ebullicin del
solvente
, causada por la disolucin de
gramos soluto en
gramos de
solvente.
Material y Equipo.-
Solventes lquidos como benceno, acetona, etc.; soluto que en ese caso fue urea.
Aparato para ascenso ebulloscpico de Cottrell Chopin con cmara de ebullicin y
otros accesorios; refrigerante, termmetro diferencial Beckman, lupa, micromechero,
rejilla y gas propano; podra usarse como equipo y medio de calentamiento lmpara de
rayos infrarrojos y manta de calentamiento que funciona con electricidad. Prensa para
comprimidos, soportes, pinzas, etc.
Procedimiento Experimental.-
Para el solvente:
()
Para el soluto:
()
( )
( )
( )
Por tablas sabemos que:
Entonces la masa molar terica de la urea es
La masa molar experimental ser:
()()
()()
Por lo que observamos, existe un error:
Conclusin.-
Obtuvimos la masa molar de un soluto no voltil (urea) con un margen de error del
valor terico de 3.33%, esto quiere decir que, es muy aceptable el valor y se obtuvo
una buena toma de datos.
Вам также может понравиться
- 5.30, 5.42Документ3 страницы5.30, 5.42Orlando Samudio100% (9)
- 7 Libros para Tu Fortaleza MentalДокумент9 страниц7 Libros para Tu Fortaleza MentalManuela MendozaОценок пока нет
- Lima - Perú, Setiembre 2018Документ28 страницLima - Perú, Setiembre 2018Manuela MendozaОценок пока нет
- Programa GMM 2022Документ20 страницPrograma GMM 2022Manuela MendozaОценок пока нет
- BFFC 36 Af 1Документ1 страницаBFFC 36 Af 1Manuela MendozaОценок пока нет
- Procedimiento para La Conexión Del Tanque Criogenico Al IcpДокумент2 страницыProcedimiento para La Conexión Del Tanque Criogenico Al IcpManuela MendozaОценок пока нет
- La Reactividad Materia PrimaДокумент1 страницаLa Reactividad Materia PrimaManuela MendozaОценок пока нет
- CatálogoДокумент14 страницCatálogoManuela MendozaОценок пока нет
- CaratulaДокумент8 страницCaratulaManuela MendozaОценок пока нет
- Peru 2030 La Visión Del Perú Que Queremos y Los 17 ODSДокумент93 страницыPeru 2030 La Visión Del Perú Que Queremos y Los 17 ODSneyser alayoОценок пока нет
- Cal CaracterísticasДокумент1 страницаCal CaracterísticasManuela MendozaОценок пока нет
- Preparación LechadaДокумент1 страницаPreparación LechadaManuela MendozaОценок пока нет
- Cal Procesos MinerosДокумент1 страницаCal Procesos MinerosManuela MendozaОценок пока нет
- La Reactividad Materia PrimaДокумент1 страницаLa Reactividad Materia PrimaManuela MendozaОценок пока нет
- Diseño Mascarilla de CobreДокумент5 страницDiseño Mascarilla de CobreManuela MendozaОценок пока нет
- Resumen ReactividadДокумент3 страницыResumen ReactividadManuela MendozaОценок пока нет
- Red de JóvenesДокумент3 страницыRed de JóvenesManuela MendozaОценок пока нет
- INTRODUCCIÓNДокумент16 страницINTRODUCCIÓNManuela MendozaОценок пока нет
- Normas Basicas de Un EnsayoДокумент4 страницыNormas Basicas de Un EnsayoRoberto RodriguezОценок пока нет
- Memoria 2016 PDFДокумент47 страницMemoria 2016 PDFEfrain Alave ChoqueОценок пока нет
- Aportaciones AlqimistasДокумент8 страницAportaciones Alqimistas5614784Оценок пока нет
- Mineria ODSДокумент48 страницMineria ODSManuela MendozaОценок пока нет
- Memoria 2016 PDFДокумент47 страницMemoria 2016 PDFEfrain Alave ChoqueОценок пока нет
- Ebook Universia MXДокумент31 страницаEbook Universia MXBroncoОценок пока нет
- OdsДокумент40 страницOdsAlejandra SnchezОценок пока нет
- Aplik Vol 3Документ31 страницаAplik Vol 3Manuela MendozaОценок пока нет
- PDFДокумент43 страницыPDFCarlos Trejo GuerraОценок пока нет
- Colores y Colorantes de AméricaДокумент0 страницColores y Colorantes de AméricaDaniel VargasОценок пока нет
- ConvocatoriaДокумент12 страницConvocatoriaManuela MendozaОценок пока нет
- Normas Basicas de Un EnsayoДокумент4 страницыNormas Basicas de Un EnsayoRoberto RodriguezОценок пока нет
- Ing - Quimica Manuela MendozaДокумент1 страницаIng - Quimica Manuela MendozaManuela MendozaОценок пока нет
- Ejercicios Curvas Bombas001Документ4 страницыEjercicios Curvas Bombas001Gabriel MoralesОценок пока нет
- Monitoreo de Emisiones Enero 2023Документ30 страницMonitoreo de Emisiones Enero 2023Yaker Soto GoitiaОценок пока нет
- Ejerciccios 11-12-13de DinamicaДокумент5 страницEjerciccios 11-12-13de DinamicaKarina Landa MartinezОценок пока нет
- Hidrodesalquilación Del Tolueno (Hda)Документ14 страницHidrodesalquilación Del Tolueno (Hda)Alicia PastranaОценок пока нет
- Método de Doble IntegraciónДокумент3 страницыMétodo de Doble IntegraciónAguilar Huaman JhoanОценок пока нет
- CMR XДокумент8 страницCMR XsodecasurОценок пока нет
- Primer Parcial PDFДокумент28 страницPrimer Parcial PDFJorgeguarayoОценок пока нет
- Ejercicios Rocha y Ruiz Resueltos PDFДокумент17 страницEjercicios Rocha y Ruiz Resueltos PDFLino Anderson Velazque CarrascoОценок пока нет
- Prob Neumatica Ramon Lopez ResueltosДокумент31 страницаProb Neumatica Ramon Lopez ResueltosCristina Camba FontevedraОценок пока нет
- Marcos Hiperestaticos y Vigas ContinuasДокумент3 страницыMarcos Hiperestaticos y Vigas ContinuasFRANCISCO JAVIER TAM�Z RENTER�AОценок пока нет
- Química Décimo GradoДокумент12 страницQuímica Décimo GradoJuan Pablo CastañedaОценок пока нет
- TupiДокумент35 страницTupiFrancisco Gabriel Cruz MexОценок пока нет
- Control de Lectura N01Документ8 страницControl de Lectura N01Julián GuerreroОценок пока нет
- Guía de Ejercicios Química General I 2012 PDFДокумент91 страницаGuía de Ejercicios Química General I 2012 PDFDiego Gaston Enrich0% (1)
- Laboratorio3 1LX 231Документ21 страницаLaboratorio3 1LX 231jorgeОценок пока нет
- Sistema de BombeoДокумент9 страницSistema de BombeoDaniel TapiaОценок пока нет
- Sensores de Humedad para Aplicaciones IndustrialesДокумент10 страницSensores de Humedad para Aplicaciones IndustrialesJose PaguayОценок пока нет
- Practica Nº3 Humedad RelativaДокумент6 страницPractica Nº3 Humedad RelativaDiego CondoriОценок пока нет
- Practica Punto de Ebullición y FusiónДокумент11 страницPractica Punto de Ebullición y FusiónJomaОценок пока нет
- Instrumentos Optométricos APUNTESДокумент52 страницыInstrumentos Optométricos APUNTESTyler marcial NtutumuОценок пока нет
- Masa Resorte Fisica 2Документ5 страницMasa Resorte Fisica 2Laura AndreaОценок пока нет
- Metalurgia de PolvosДокумент10 страницMetalurgia de PolvosPaola MaradiagaОценок пока нет
- Trabajo 14 7063133Документ16 страницTrabajo 14 7063133Campos OscarОценок пока нет
- Escritos EletronicaДокумент6 страницEscritos Eletronicajhon arbelaezОценок пока нет
- TECNOMECANICA2Документ13 страницTECNOMECANICA2Victor CruzОценок пока нет
- Trabajo 1Документ119 страницTrabajo 1Sthayler RamirezОценок пока нет
- MC 324-SilДокумент4 страницыMC 324-Sillides fernandez saldivarОценок пока нет
- Experimentos Leyes de La TermodinamicaДокумент5 страницExperimentos Leyes de La TermodinamicalihumaОценок пока нет