Академический Документы
Профессиональный Документы
Культура Документы
Enlace Quimico - FCF
Загружено:
GR Omar0 оценок0% нашли этот документ полезным (0 голосов)
25 просмотров22 страницыОригинальное название
ENLACE QUIMICO - FCF
Авторское право
© © All Rights Reserved
Доступные форматы
DOCX, PDF, TXT или читайте онлайн в Scribd
Поделиться этим документом
Поделиться или встроить документ
Этот документ был вам полезен?
Это неприемлемый материал?
Пожаловаться на этот документАвторское право:
© All Rights Reserved
Доступные форматы
Скачайте в формате DOCX, PDF, TXT или читайте онлайн в Scribd
0 оценок0% нашли этот документ полезным (0 голосов)
25 просмотров22 страницыEnlace Quimico - FCF
Загружено:
GR OmarАвторское право:
© All Rights Reserved
Доступные форматы
Скачайте в формате DOCX, PDF, TXT или читайте онлайн в Scribd
Вы находитесь на странице: 1из 22
UNIVERSIDAD NACIONAL
MAYOR DE SAN MARCOS
Facultad: Ciencias Fsicas
E.A.P: Fsica
Curso: Laboratorio de Qumica General
Prctica: # 02
Profesor: Ing. Hugo Galarreta Diaz
Horario: 13:00 17:00 Horas
Fecha de entrega: 25/09/2014
Integrantes:
Garrido Rospigliosi, Alexander Omar 14130076
Rojas Apcho Cristian Paul 07130130
Ccasani Guillm Jess Cristian 10131175
UNIVERSIDAD NACIONAL MAYOR DE SAN MARCOS
Facultad de Ciencias Fsicas E.A.P FSICA
Laboratorio de Qumica General 2
INDICE
1. Objetivos
2. Introduccin
3. Resumen
4. Principios Tericos
5. Materiales Y Reactivos
6. Procedimientos Experimentales e Imgenes
7. Cuestionario
8. Bibliografa
UNIVERSIDAD NACIONAL MAYOR DE SAN MARCOS
Facultad de Ciencias Fsicas E.A.P FSICA
Laboratorio de Qumica General 3
1. OBJETIVOS
Determinar el tipo de enlace de algunas sustancias por medio de la conductividad
elctrica en su estado slido o lquido o en sus respectivas soluciones.
Encontrar una relacion entre la solubilidad y la polaridad de una sustancia con respecto a
un solvente determinado.
Establecer la diferencia entre una solucin inica, parcialmente inica y covalente de
acuerdo a su conductividad elctrica.
2. INTRODUCCIN
El mundo de las ciencias qumicas cada da nos sorprende ms y mas puesto que en
cada proceso de la naturaleza o utilizacin de la tecnologa est presente en nuestra
realidad que hace que da a da se mejore en diferentes disciplinas y que haya ms
esperanza de vida en la poblacin mundial.
El hecho fundamental de la qumica es que los elementos como el oxigeno, el hidrogeno,
el carbono, el hierro pueden combinarse para formar compuestos como el agua, el
metano, u el oxido de hierro, cuyas propiedades son completamente diferentes a las de
sus elementos constituyentes. La interpretacin de este hecho, segn la teora atmica,
es que los tomos de los elementos pueden unirse para formar molculas. El resultado de
la unin de los tomos en las molculas se conoce como enlace qumico.
Entonces dicho de otra manera: enlace qumico es la fuerza de atraccin de los tomos,
con la finalidad de formar molculas o cuerpos compuestos.
En el presente trabajo trataremos sobre el tema del enlace qumico de una manera ms
didctica y as poder comprender e identificar estas fuerzas en los diferentes compuestos
qumicos.
UNIVERSIDAD NACIONAL MAYOR DE SAN MARCOS
Facultad de Ciencias Fsicas E.A.P FSICA
Laboratorio de Qumica General 4
3. RESUMEN
Llenar con agua potable hasta la mitad del volumen del vaso de 100ml introducimos los
electrodos del equipo hasta la mitad del lquido ensayar la conductividad.
Repetir la experiencia anterior pero ahora usando agua destilada.
Repetimos el mismo procedimiento para las sustancias dadas.
Para el caso del cobre y carbono tomamos la muestra con una pinza aislante y conectar
directamente a los electrodos cerrando el circuito.
SUSTANCIAS
H
2
0 POTABLE
H
2
0 DESTILADA
NaCl
CuSO
4
NaOH
NH
4
Cl
NH
3
CH
3
COOH
H
2
SO
4
Sacarosa
Aceite
UNIVERSIDAD NACIONAL MAYOR DE SAN MARCOS
Facultad de Ciencias Fsicas E.A.P FSICA
Laboratorio de Qumica General 5
4. PRINCIPIOS TEORICOS
Enlace Qumico: es el conjunto de fuerzas que mantienen unidos a los tomos, iones y
molculas cuando estos forman distintas agrupaciones estables. Los tomos de distintos
elementos pueden unirse mediante enlaces para formar compuestos con propiedades
muy distintas de las que tienen cuando se presentan en forma de elemento aislado.
Tipos de enlace:
Es importante indicar que el enlace qumico es una situacin de equilibrio, donde las
fuerzas de atraccin entre los tomos son contrarrestadas por fuerzas equivalentes y de
sentido contrario (fuerzas de repulsin). El punto de equilibrio suele ser caracterizado por
el radio de enlace y la energa. La explicacin de las fuerzas involucradas en un enlace
qumico son descritas por las leyes de la electrodinmica cuntica. Sin embargo al ser un
problema de muchos cuerpos se recurre con frecuencia a teoras simplificadas.
a) Enlace inico: es la fuerza de atraccin electrosttica que mantiene unidos a los
iones, un tomo no metlico y otro metlico que tengan una elevada diferencia de
electronegatividades, con cargas opuestas para formar un agregado. Los
compuestos inicos son elctricamente neutros, a pesar de estar constituidos por
iones, ya que contienen igual carga positiva que negativa
El enlace inico se presenta generalmente entre los tomos de los grupos:
I A - VI
II A - VI A
III A - V
UNIVERSIDAD NACIONAL MAYOR DE SAN MARCOS
Facultad de Ciencias Fsicas E.A.P FSICA
Laboratorio de Qumica General 6
b) Enlace covalente: consiste en la comparticin de uno o ms pares de electrones
entre dos tomos, generalmente entre dos no metales.
Si se presenta en la unin de tomos del mismo elemento entonces el enlace se
llama covalente apolar. Pero, si se da en entre tomos diferentes entonces el
enlace se llama covalente polar.
c) Enlace metlico: es el que se establece entre un gran nmero de cationes (iones
positivos) que se mantienen unidos por una nube de electrones.
UNIVERSIDAD NACIONAL MAYOR DE SAN MARCOS
Facultad de Ciencias Fsicas E.A.P FSICA
Laboratorio de Qumica General 7
ENLACE
INICO:
Este enlace se origina cuando se
transfiere uno o varios electrones de
un tomo a otro. Debido al
intercambio electrnico, los tomos
se cargan positiva y negativamente,
establecindose as una fuerza de
atraccin electrosttica que los
enlaza. Se forma entre dos tomos
con una apreciable diferencia de
electronegatividades, los elementos
de los grupos I y II A forman enlaces
inicos con los elementos de los
grupos VI y VII A.
EJEMPLO:
ENLACE
COVALENTE
Se presenta cuando se comparten
uno o ms pares de electrones entre
dos tomos cuya diferencia de
electronegatividad es pequea.
EJEMPLO:
Enlace
covalente
apolar:
Se establece entre
tomos con igual
electronegatividad.
tomos del mismo
elemento presentan
este tipo de enlace.
EJEMPLO:
Enlace
covalente
polar:
Se establece entre
tomos con
electronegatividades
prximas pero no
iguales
EJEMPLO:
Enlace
covalente
coordinado:
Se establece por
comparticin de
electrones entre dos
tomos pero un
tomo aporta el par
de electrones
compartidos.
EJEMPLO:
ENLACE
METLICO
Los electrones que participan en l se mueven libremente, a causa de la poca
fuerza de atraccin del ncleo sobre los electrones de su periferia.
UNIVERSIDAD NACIONAL MAYOR DE SAN MARCOS
Facultad de Ciencias Fsicas E.A.P FSICA
Laboratorio de Qumica General 8
Propiedades de los enlaces:
Propiedades de los
compuestos inicos
Propiedades de los
compuestos covalentes
Propiedades de los
compuestos metlicos
* Se da entre cationes y
aniones.
* Uno cede electrones y el
otro recibe.
* Presenta interacciones
multidireccionales.
* La energa de enlace es
de 100 a 1000 Kj/mol.
* Son solubles en agua.
* Son slidos a
temperatura ambiente.
* Conducen la electricidad
en disolucin o fundidos.
* En general sus puntos de
fusin son altos.
*la fuerza que se da entre
cationes y aniones es
electrosttica.
* Se da entre tomos y
tomos.
* Ambos comparten el par
electrnico.
* Este tipo de enlace se
subdivide en :
- Sencillo.
- Doble.
- Triple.
* Las interacciones que
presenta son
unidireccionales.
* La energa de enlace es
de 250 a 400 Kj/mol.
* Son gases y lquidos a
temperatura ambiente.
* No son solubles en
agua, pero s lo son en
benceno y otros
compuestos orgnicos.
* No conducen la corriente
elctrica ni en estado
slido ni estado liquido
por lo general
* En general tienen puntos
de fusin bajos.
* Donde una nube de
electrones baa a los
ncleos positivos.
* Los electrones que
forman parte de la nube
tambin son llamados
electrones des-
localizados.
* Las interacciones que
presentan son
multidireccional.
* Son insolubles en agua.
* Conducen la corriente
elctrica.
* La mayora se
encuentran en estado
slido salvo el mercurio
(Hg).
UNIVERSIDAD NACIONAL MAYOR DE SAN MARCOS
Facultad de Ciencias Fsicas E.A.P FSICA
Laboratorio de Qumica General 9
Conductibilidad Elctrica: es la capacidad de un cuerpo o medio para conducir la
corriente elctrica, es decir, para permitir el paso a travs de l de partculas cargadas,
bien sean los electrones, los transportadores de carga en conductores metlicos o
semimetlicos, o iones, los que transportan la carga en disoluciones de electrolitos.
UNIVERSIDAD NACIONAL MAYOR DE SAN MARCOS
Facultad de Ciencias Fsicas E.A.P FSICA
Laboratorio de Qumica General 10
Solubilidad: es una medida de la capacidad de una determinada sustancia para
disolverse en otra. Puede expresarse en moles por litro, en gramos por litro, o en
porcentaje de soluto; en algunas condiciones la solubilidad se puede sobrepasar,
denominndose a estas soluciones sobresaturadas.
5. Materiales y Reactivos:
Materiales:
Vaso de 100 mL
Equipo de conductibilidad elctrica
Pinzas aislantes
Reactivos:
Aceite: es un compuesto orgnico obtenido a partir de semillas u otras partes de las
plantas en cuyos tejidos se acumula como fuente de energa.
UNIVERSIDAD NACIONAL MAYOR DE SAN MARCOS
Facultad de Ciencias Fsicas E.A.P FSICA
Laboratorio de Qumica General 11
cido actico (CH
3
COOH): ste es un cido que se encuentra en el vinagre, siendo el
principal responsable de su sabor y olor agrios.
Cloruro de sodio (NaCl): tambin llamado sal de mesa, es una de las sales responsable
de la salinidad del ocano y del fluido extracelular de muchos organismos.
Cloruro de amonio (NH
4
Cl): En estado slido la coloracin vara entre incoloro y blanco.
Es inodoro e higroscpico en diversas formas.
cido sulfrico (H
2
SO
4
): es un compuesto qumico muy corrosivo y que por una gran
parte se emplea en la obtencin de fertilizantes. Tambin se usa para la sntesis de otros
cidos y sulfatos y en la industria petroqumica.
UNIVERSIDAD NACIONAL MAYOR DE SAN MARCOS
Facultad de Ciencias Fsicas E.A.P FSICA
Laboratorio de Qumica General 12
Hidrxido de sodio (NaOH): es un hidrxido custico usado en la industria en la
fabricacin de papel, tejidos, y detergentes.
Grafito (C): es una de las formas alotrpicas en las que se puede presentar el carbono
junto al diamante.
Lmina de cobre (Cu): se caracteriza por ser uno de los mejores conductores de
electricidad. Gracias a su alta conductividad elctrica, ductilidad y maleabilidad, se ha
convertido en el material ms utilizado para fabricar cables elctricos y otros componentes
elctricos y electrnicos.
UNIVERSIDAD NACIONAL MAYOR DE SAN MARCOS
Facultad de Ciencias Fsicas E.A.P FSICA
Laboratorio de Qumica General 13
Agua potable: es el agua para el consumo humano, que adems contiene diferentes
iones y minerales.
Agua destilada: es aquella cuya composicin se basa en la unidad de molculas de
H2O. Es aquella a la que se le han eliminado las impurezas e iones mediante destilacin.
UNIVERSIDAD NACIONAL MAYOR DE SAN MARCOS
Facultad de Ciencias Fsicas E.A.P FSICA
Laboratorio de Qumica General 14
6. DETALLES EXPERIMENTALES
CRITERIOS
ENLACE INICO ENLACE COVALENTE
POLAR
ENLACE COVALENTE
APOLAR
SOLUBILIDAD EN H2O
S S NO
CONDUCTIVIDAD
ELCTRICA
S NO NO
SUSTANCIAS SOLUBILIDAD
EN H20
CONDUCTIVIDAD
ELCTRICA
ENLACE
QUMICO
H
2
0 POTABLE
S
COVALENTE
POLAR
H
2
0 DESTILADA
NO
COVALENTE
POLAR
NaCl
SOLUBLE
S
INICO
CuSO
4
SOLUBLE
S
INICO
NaOH
SOLUBLE
S
INICO
NH
4
Cl
SOLUBLE
S
INICO
NH
3
SOLUBLE
S
INICO
CH
3
COOH
SOLUBLE
S
INICO
H
2
SO
4
SOLUBLE
S
INICO
Sacarosa
SOLUBLE
NO
COVALENTE
POLAR
Aceite
NO SOLUBLE
NO
COVALENTE
APOLAR
Cobre Cu
NO SOLUBLE
S
METLICO
Grafito C
NO SOLUBLE
S
COVALENTE
APOLAR
UNIVERSIDAD NACIONAL MAYOR DE SAN MARCOS
Facultad de Ciencias Fsicas E.A.P FSICA
Laboratorio de Qumica General 15
Imgenes y observaciones
1. Limpiando los utensilios con agua destilada ya que el agua potable tiene sales minerales,
metales disueltos, que pueden afectar el resultado de la prctica.
2. H
2
O Potable S conduce electrones
3. H
2
O Destilada No conduce electrones.
UNIVERSIDAD NACIONAL MAYOR DE SAN MARCOS
Facultad de Ciencias Fsicas E.A.P FSICA
Laboratorio de Qumica General 16
4. CuSO
4
(Aq.) S conduce electrones.
5. Recordar que en cada prueba se tienen que lavar los utensilios con agua destilada.
6. NaOH (Aq.) S conduce electrones.
7. NH
4
Cl S conduce electrones.
UNIVERSIDAD NACIONAL MAYOR DE SAN MARCOS
Facultad de Ciencias Fsicas E.A.P FSICA
Laboratorio de Qumica General 17
8. NH
3
S conduce electrones.
9. CH
3
COOH S conduce electrones.
10. H
2
SO
4
S conduce electrones
11. Sacarosa No conduce electrones
UNIVERSIDAD NACIONAL MAYOR DE SAN MARCOS
Facultad de Ciencias Fsicas E.A.P FSICA
Laboratorio de Qumica General 18
12. Aceite No conduce electrones
13. Usar agua destilada en todas las pruebas.
UNIVERSIDAD NACIONAL MAYOR DE SAN MARCOS
Facultad de Ciencias Fsicas E.A.P FSICA
Laboratorio de Qumica General 19
14. Cobre Cu S conduce electrones.
15. Grafito C S conduce electrones.
7. CUESTIONARIO
1. Cmo puede determinar experimentalmente si una sustancia forma o no una
solucin electroltica?
Para probar experimentalmente que una sustancia forma una solucin electroltica se
necesita un vaso de 100ml, un equipo aislante de conductividad elctrica, un foco de
75W y en algunos casos como el del cobre y el carbn se utiliza las pinzas aislantes.
Antes de comenzar el experimento se debe limpiar con agua destilada los electrodos del
equipo aislante de conductividad elctrica para evitar errores en la conclusin del
experimento.
Si la sustancia es slida, primero debe disolverse en agua destilada con la finalidad de
facilitar el experimento a excepcin del cobre y el grafito que se conectan directamente
con los electrodos del equipo, luego se sumergen los electrodos en la solucin y se
conecta a una fuente de corriente elctrica. Si el foco se enciende, se estara
demostrando que la solucin es electroltica ya que una caractersticas de este tipo de
solucin es la de conducir la corriente elctrica, en caso contrario la solucin no es
electroltica.
UNIVERSIDAD NACIONAL MAYOR DE SAN MARCOS
Facultad de Ciencias Fsicas E.A.P FSICA
Laboratorio de Qumica General 20
2. Cules de las sustancias con las que ha trabajado en esta prctica, son slidos
inicos?
Cloruro de Sodio..........................................................................................NaCl
(aq)
Sulfato de Cobre.......................................................................................CuSO
4
(aq)
Hidrxido de Sodio....................................................................................NaOH
(aq)
Cloruro de Amonio.......................................................................................H
4
Cl
(aq)
Amonaco......................................................................................................NH
3
(aq)
cido Actico......................................................................................CH
3
COOH
(aq)
cido Sulfrico..........................................................................................H
2
SO
4
(aq)
3. Distinga entre electrlitos y no electrlitos
Un electrlito es una sustancia que contiene iones libres, los que se comportan como un
medio conductor elctrico. Debido a que generalmente consisten de iones en solucin, los
electrlitos tambin son conocidos como soluciones inicas, pero tambin son posibles
electrlitos fundidos y electrlitos slidos. Comnmente, los electrlitos existen como
soluciones de cidos, bases o sales.
Los no electrlitos son sustancias que no conducen la corriente elctrica al estar en
disolucin acuosa, no se disocian y no forman iones. Un ejemplo sera el azcar de mesa,
los no electrlitos se disuelven como molculas neutras que no pueden moverse en
presencia de un campo elctrico, adems son poco solubles a excepcin de los que
pueden forman puentes de hidrgeno.
UNIVERSIDAD NACIONAL MAYOR DE SAN MARCOS
Facultad de Ciencias Fsicas E.A.P FSICA
Laboratorio de Qumica General 21
4. Cules de las sustancias usadas en la experiencia de enlace qumico son
electrolticos y cules son no electrolticos?
Las sustancias electrolticas son:
Agua potable..............................................................................................H
2
O potable
Cloruro de Sodio...............................................................................................NaCl
(aq)
Sulfato de Cobre............................................................................................CuSO
4
(aq)
Hidrxido de Sodio..........................................................................................NaOH
(aq)
Cloruro de Amonio..........................................................................................NH
4
Cl
(aq)
Amonaco...........................................................................................................NH
3
(aq)
cido Actico...........................................................................................CH
3
COOH
(aq)
cido Sulfrico................................................................................................H
2
SO
4
(aq)
Cobre.....................................................................................................................Cu
(s)
Grafito......................................................................................................................C
(s)
Las sustancias no electrolticas son:
Agua destilada.........................................................................................H
2
O destilada
Sacarosa........................................................................................................C
12
H
22
O
11
Aceite
UNIVERSIDAD NACIONAL MAYOR DE SAN MARCOS
Facultad de Ciencias Fsicas E.A.P FSICA
Laboratorio de Qumica General 22
5. Por qu algunas de las sustancias trabajadas en esta prctica no conducen
bien la electricidad? Cules son estas sustancias?
Porque son sustancias no electrolticas y se disuelven como molculas neutras que no
pueden moverse en presencia de un campo elctrico y por el tipo de enlace qumico que
presentan a excepcin de algunas sustancias, por tal motivo no pueden conducir bien la
corriente elctrica.
Estas sustancias son:
Agua destilada..................................................................................................H
2
O destilada
Sacarosa.................................................................................................................C
12
H
22
O
11
Aceite
8. BIBLIOGRAFIA
Academia Cesar Vallejo. Qumica. Editorial Lumbreras. Lima- Per.
Whitten Kenneth. Qumica General. Edit MC Graw Hill. Tercera edicin.1992.
http://www.profesorenlinea.cl/quimica/enlace_quimico.htm
http://www.quimicafisicanet.com.ar/quimica/electrolitos/ap05_conduccion.php
Chang, Raymond. Qumica. Sptima edicin. Editorial Mc Graw Hill. Mxico
Вам также может понравиться
- Actividad4 Química VMBSДокумент10 страницActividad4 Química VMBSVirgilio Blanco100% (6)
- Enlaces Químicos en MedicinaДокумент30 страницEnlaces Químicos en MedicinaChristian Raul Rojas Tarrillo25% (4)
- Infografia PDFДокумент1 страницаInfografia PDFGR OmarОценок пока нет
- Compresor de Tornillo Helicoidal 1Документ11 страницCompresor de Tornillo Helicoidal 1Héctor Hugo MoyaОценок пока нет
- (Tutorial) Grabador BIOS SPI Por Puerto Paralelo in Herramientas para Taller - Bios - Windows XPДокумент7 страниц(Tutorial) Grabador BIOS SPI Por Puerto Paralelo in Herramientas para Taller - Bios - Windows XPÁlvaro Basulto RuízОценок пока нет
- POO ProblemasДокумент16 страницPOO ProblemasLuis GarridoОценок пока нет
- Informe de Enlace Quimico 1 Enlace QuimicoДокумент20 страницInforme de Enlace Quimico 1 Enlace QuimicoXiomyArriolaAtoОценок пока нет
- Informe de EnlaceДокумент7 страницInforme de EnlaceWilliams ChoqueОценок пока нет
- Practica N 2 Enlace QuimicoДокумент19 страницPractica N 2 Enlace QuimicoSteve HyugaОценок пока нет
- Informe Laboratorio 03 - Quimica GeneralДокумент14 страницInforme Laboratorio 03 - Quimica GeneralJohan EnriqueОценок пока нет
- Practica2 - Enlaces QuimicosДокумент6 страницPractica2 - Enlaces QuimicosALEJANDRA MONTANTESОценок пока нет
- Conductividad ElecДокумент14 страницConductividad ElecMilagros Acuña FarfanОценок пока нет
- Química - Enlaces QuímicosДокумент11 страницQuímica - Enlaces QuímicosMariangelis José Lozada AcuñaОценок пока нет
- Practica 5 CompletaДокумент19 страницPractica 5 CompletaHADID ESTEBAN MORALESОценок пока нет
- Informe 2Документ24 страницыInforme 2Mary Kely Chambi ChoqueОценок пока нет
- Informe 03 Quimica - Grupo 6Документ14 страницInforme 03 Quimica - Grupo 6Rodrigo Franco Huaringa AlvarezОценок пока нет
- Tema 3. Enlace Químico. 2º BachДокумент18 страницTema 3. Enlace Químico. 2º Bachxenia.lunaОценок пока нет
- Guía N°5 de Aprendizaje Química Grado 10°Документ12 страницGuía N°5 de Aprendizaje Química Grado 10°Andres BallestaОценок пока нет
- INTRODUCCIÓNДокумент6 страницINTRODUCCIÓNArturo MontalvanОценок пока нет
- Informe de Práctica 6Документ4 страницыInforme de Práctica 6Cisneros Gomez Angel OctavioОценок пока нет
- Cuestionario de Enlaces QuímicosДокумент4 страницыCuestionario de Enlaces QuímicosCastillo Fajardo Jesus GuadalupeОценок пока нет
- Laboratorio Nº4. Enlace Químico.Документ18 страницLaboratorio Nº4. Enlace Químico.Cristian CustodioОценок пока нет
- Unidad 5 Enlaces QuímicosДокумент39 страницUnidad 5 Enlaces QuímicosJorge Ocaña DiazОценок пока нет
- Tarea 6 QuimicaДокумент4 страницыTarea 6 QuimicaESMARLIS BELLO JOSEОценок пока нет
- Practica 6Документ7 страницPractica 6gil vasquez laskmi danaeОценок пока нет
- Unidad2 Actividad 1 ResumenДокумент10 страницUnidad2 Actividad 1 ResumenDroite RonaldoОценок пока нет
- Guia de PracticaДокумент15 страницGuia de PracticaElmer Cadillo LimasОценок пока нет
- CIENCIA E ING DE MAT T1 J.TrannyДокумент7 страницCIENCIA E ING DE MAT T1 J.TrannyJorge TrannyОценок пока нет
- Enlaces QuimicosДокумент9 страницEnlaces QuimicosRaysa AguilarОценок пока нет
- 5) B - Reporte Prác. Lab. 5 - (Sem. 6) - Enlace Qco - GHHJHKHJHДокумент16 страниц5) B - Reporte Prác. Lab. 5 - (Sem. 6) - Enlace Qco - GHHJHKHJHGINA FLOR HUAMANI NAJARROОценок пока нет
- Conductividad de Los ElementosДокумент10 страницConductividad de Los ElementosAlejandro De La Cruz HuertaОценок пока нет
- Inf. Laboratorio N°3Документ22 страницыInf. Laboratorio N°3Eduardo SalinasОценок пока нет
- IP Práctica 7 - Equipo 1Документ21 страницаIP Práctica 7 - Equipo 1José Luis Urbiola RodríguezОценок пока нет
- Guia 4 de QuimicaДокумент9 страницGuia 4 de QuimicaCarlos GutierrezОценок пока нет
- Informe 5 de Quimica - Enlace QuimicoДокумент13 страницInforme 5 de Quimica - Enlace Quimicojudith churaОценок пока нет
- Enlace QuímicoДокумент22 страницыEnlace QuímicoLizbeth Montalico PachapumaОценок пока нет
- PDF Practica Laboratorio Enlaces - CompressДокумент15 страницPDF Practica Laboratorio Enlaces - CompressRuben DiazОценок пока нет
- Uniones QuímicasДокумент15 страницUniones QuímicasFelipe Alejandro JaraОценок пока нет
- 5) B - Reporte Prác. Lab. 5 - (Sem. 6) - Enlace Qco.Документ16 страниц5) B - Reporte Prác. Lab. 5 - (Sem. 6) - Enlace Qco.GINA FLOR HUAMANI NAJARROОценок пока нет
- Informe Quimica 55555Документ13 страницInforme Quimica 55555MahilerMircoVasquezGonzalesОценок пока нет
- Práctica 5 QuímicaДокумент9 страницPráctica 5 QuímicaBraulio HernándezОценок пока нет
- Enlace Quimico UtpДокумент8 страницEnlace Quimico UtpGabo SichaОценок пока нет
- Laboratorio 4Документ19 страницLaboratorio 4GustavoLopezОценок пока нет
- Ot21 Sep Quim5 2Документ6 страницOt21 Sep Quim5 2JonathanArandaAОценок пока нет
- Reporte Enlaces KarlaДокумент11 страницReporte Enlaces KarlaLuis AlbertoОценок пока нет
- Cuestionario Previo No.6Документ4 страницыCuestionario Previo No.6Bryan MОценок пока нет
- Laboratorio 3 Quimica (Enlaces Quimicos)Документ15 страницLaboratorio 3 Quimica (Enlaces Quimicos)Antony Quispe AlvaresОценок пока нет
- Q I - Lab 3-Enlace Quimico-23Документ5 страницQ I - Lab 3-Enlace Quimico-23Quimica IndustrialОценок пока нет
- Enlaces Químicos en MedicinaДокумент30 страницEnlaces Químicos en MedicinaoazaruОценок пока нет
- Practica 2Документ14 страницPractica 2Luis AlcantaraОценок пока нет
- Resumen de Enlace QuimicosДокумент7 страницResumen de Enlace QuimicosSergio CruzОценок пока нет
- Grupo 6 - Química General - Capitulo - 8Документ13 страницGrupo 6 - Química General - Capitulo - 8GabrielaОценок пока нет
- Practica N°6 Enlace QuímicoДокумент28 страницPractica N°6 Enlace QuímicoJhoel Daniel Gamboa Mejia0% (1)
- Inform 03 Enlace QuimicoДокумент11 страницInform 03 Enlace QuimicoErnesto GálvezОценок пока нет
- Enlace QuímicoДокумент26 страницEnlace QuímicoBruno FernándezОценок пока нет
- Enlaces Quimicos 190502210922 PDFДокумент19 страницEnlaces Quimicos 190502210922 PDFCarlos Araneda MelladoОценок пока нет
- Tipos de EnlacesДокумент11 страницTipos de EnlacesDavid LucasОценок пока нет
- Material de Apoyo Enlace QuimicoДокумент4 страницыMaterial de Apoyo Enlace QuimicoMartin CabreraОценок пока нет
- 1mer Informe de QuimicaДокумент15 страниц1mer Informe de QuimicaNancy Vargas MoralesОценок пока нет
- Cuestionario No.1 EnlacesДокумент5 страницCuestionario No.1 EnlacesLuis LopezОценок пока нет
- Practica Modulo III-1Документ15 страницPractica Modulo III-1Erick Henry Trujillo EustaquioОценок пока нет
- Guía 1 de Aprendizaje Virtual 2021 Química Grado OctavoДокумент4 страницыGuía 1 de Aprendizaje Virtual 2021 Química Grado Octavojose valderramaОценок пока нет
- Practica Nº3 Enlace QuimicoДокумент5 страницPractica Nº3 Enlace QuimicoPaolo Morante RiosОценок пока нет
- Teoría electromagnética para estudiantes de ingeniería: Notas de claseОт EverandTeoría electromagnética para estudiantes de ingeniería: Notas de claseРейтинг: 4.5 из 5 звезд4.5/5 (7)
- Pro 0005 Funciones 2 LimitesДокумент19 страницPro 0005 Funciones 2 LimitesHopper JavierОценок пока нет
- Diagramas de FaseДокумент4 страницыDiagramas de FaseGR OmarОценок пока нет
- Ciclo de Refrigeracion 1 PDFДокумент1 страницаCiclo de Refrigeracion 1 PDFGR OmarОценок пока нет
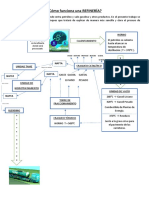
- Cómo Funciona Una REFINERÍAДокумент2 страницыCómo Funciona Una REFINERÍAGR OmarОценок пока нет
- Informe EeДокумент8 страницInforme EeGR OmarОценок пока нет
- Problemas Resueltos de LimitesДокумент52 страницыProblemas Resueltos de LimitesJorge Cardenas100% (5)
- Informe TermodinamicaДокумент6 страницInforme TermodinamicaGR OmarОценок пока нет
- Informe TermodinamicaДокумент6 страницInforme TermodinamicaGR OmarОценок пока нет
- INFOGRAFIAДокумент1 страницаINFOGRAFIAGR OmarОценок пока нет
- Ex Final 2018-1Документ4 страницыEx Final 2018-1GR OmarОценок пока нет
- Física 5to Secundaria 1Документ26 страницFísica 5to Secundaria 1Paul AlarconОценок пока нет
- Documento-Final proyPDT06 PDFДокумент90 страницDocumento-Final proyPDT06 PDFGR OmarОценок пока нет
- Solucionario Demidovich Analisis Matematico 1 ByPriale PDFДокумент530 страницSolucionario Demidovich Analisis Matematico 1 ByPriale PDFjordan94% (16)
- 2 2 Introduccion Experimental Al Sistema PeriodicoДокумент29 страниц2 2 Introduccion Experimental Al Sistema PeriodicoGR OmarОценок пока нет
- Inf 1Документ2 страницыInf 1GR OmarОценок пока нет
- Termodinámica de Los MetalesДокумент29 страницTermodinámica de Los MetalesGR OmarОценок пока нет
- Guia de Lab. Fis. IVДокумент88 страницGuia de Lab. Fis. IVFrank FacundoОценок пока нет
- Medina Fisica2 PresentacionДокумент12 страницMedina Fisica2 PresentacionPercy PazОценок пока нет
- Cuaderno de Nuclear 1 PDFДокумент54 страницыCuaderno de Nuclear 1 PDFJonathan Cristhian Muñoz LeónОценок пока нет
- Reactivo Limitante FCFДокумент15 страницReactivo Limitante FCFGR Omar100% (1)
- Difusion de Gases - FCFДокумент15 страницDifusion de Gases - FCFGR OmarОценок пока нет
- Ley de Proporciones Definidas - FCFДокумент12 страницLey de Proporciones Definidas - FCFGR OmarОценок пока нет
- Densidad - FCFДокумент18 страницDensidad - FCFGR OmarОценок пока нет
- Medina Fisica2 Cap3Документ46 страницMedina Fisica2 Cap3Ángeles Campaña Olmos100% (1)
- Medina Fisica2 Cap2Документ40 страницMedina Fisica2 Cap2manuellamoОценок пока нет
- Medina Fisica2 Cap4Документ48 страницMedina Fisica2 Cap4Hector Manuel Mejia CurielОценок пока нет
- Ejercicios Termometria DilatacionДокумент70 страницEjercicios Termometria Dilatacionprofe.alex50% (4)
- Elasticidad - Física 2Документ33 страницыElasticidad - Física 2José Manuel Toledo Vásquez67% (3)
- EcualizadoresДокумент10 страницEcualizadoresDavid PeñalveОценок пока нет
- Profit RaceДокумент7 страницProfit RaceRodrigoBurgosОценок пока нет
- Como Trabaja Un Transpondedor LinealДокумент7 страницComo Trabaja Un Transpondedor LinealfaridvbОценок пока нет
- Definición de ExcelДокумент3 страницыDefinición de ExcelIvánMolinaОценок пока нет
- Examen Ecuaciones Diferencial 2018Документ9 страницExamen Ecuaciones Diferencial 2018xy70Оценок пока нет
- Utilizar El TemporizadorДокумент3 страницыUtilizar El TemporizadorLázaro de Jesús Cruz HernándezОценок пока нет
- GFPI-F-019 - Guia de Aprendizaje Introducción A Las Redes HFC. (V N-FDS)Документ10 страницGFPI-F-019 - Guia de Aprendizaje Introducción A Las Redes HFC. (V N-FDS)DAVID ESTEBAN GUTIERREZ FONSECAОценок пока нет
- Capitulor1 Deteccion FallasДокумент17 страницCapitulor1 Deteccion FallasManuel Alberto Aguirre RojasОценок пока нет
- ManualДокумент49 страницManualDynamo100% (2)
- Cia. Minera Agregados Calcareos S.A.: RUC #20100037689 Guía de Remisión Electrónica Remitente T028-00000023Документ1 страницаCia. Minera Agregados Calcareos S.A.: RUC #20100037689 Guía de Remisión Electrónica Remitente T028-00000023Jean Deyvid Arias GarciaОценок пока нет
- Procesamiento SegmentadoДокумент50 страницProcesamiento SegmentadoFabricio Rodriguez AvalosОценок пока нет
- Formulas ElectronicaДокумент1 страницаFormulas ElectronicaJose Antonio Sanchez SegoviaОценок пока нет
- QZ4284 PDFДокумент4 страницыQZ4284 PDFAndres Domingo TierrablancaОценок пока нет
- ConectorizaciónДокумент11 страницConectorizaciónDanielОценок пока нет
- Lic EnfermeriaДокумент18 страницLic EnfermeriaSolange ZavalaОценок пока нет
- Sistema DelphiДокумент8 страницSistema DelphiDavidMoretaОценок пока нет
- PDH EquiposДокумент25 страницPDH EquiposHugo G. RuedaОценок пока нет
- Atajos para PhotoshoppsДокумент4 страницыAtajos para PhotoshoppsChristhian DarkОценок пока нет
- Criterios de Elección de TransformadoresДокумент29 страницCriterios de Elección de TransformadoresLarry FlowersОценок пока нет
- Análisis de Imagen TEM SEMДокумент3 страницыAnálisis de Imagen TEM SEMAdriana Paola TCОценок пока нет
- Ccna1 Examen Modulo 1Документ9 страницCcna1 Examen Modulo 1rukismenОценок пока нет
- Informe 4Документ34 страницыInforme 4Wenceslao Avalos ArgoteОценок пока нет
- LuminiscenciaДокумент30 страницLuminiscenciaSantiago PerdigonОценок пока нет
- Robotica CamДокумент11 страницRobotica CamGaby SaavedraОценок пока нет
- Informe Final FotoelectricosДокумент7 страницInforme Final FotoelectricosDANNY VASQUEZ MARCAQUISPEОценок пока нет