Академический Документы
Профессиональный Документы
Культура Документы
P07 - Tranferencia de Calor
Загружено:
enriquegomezcruzАвторское право
Доступные форматы
Поделиться этим документом
Поделиться или встроить документ
Этот документ был вам полезен?
Это неприемлемый материал?
Пожаловаться на этот документАвторское право:
Доступные форматы
P07 - Tranferencia de Calor
Загружено:
enriquegomezcruzАвторское право:
Доступные форматы
Prctica 6: Transferencia de calor
Aguila Castro Fernando Jefte, Herrera Ruz Diego Arturo
y Rodrguez Ramrez Alejandro
Facultad de Ciencias, UNAM
Av. Universidad 3000, Circuito Exterior S/N
Delegacin Coyoacn, CP: 04510
Ciudad Universitaria, DF, Mxico
lunes 14 de octubre de 2013
1 RESUMEN
En esta prctica medimos la variacin de la temperatura de una mezcla criognica de alcohol y
nitrgeno lquido respecto al tiempo. Con los datos obtenidos se encontr una ecuacin que modela
el fenmeno estudiado con un margen de error aceptable.
2 INTRODUCCIN
2.1 CALOR
El calor es transferencia de energa de un cuerpo a otro a causa de una diferencia de temperatura. La
cantidad de calor Q necesaria para elevar la temperatura de una cantidad de material en una cantidad
pequea T es proporcional a T. Si se agrega calor a un cuerpo, el calor Q correspondiente es
positivo; si se le quita, Q es negativo. El principio bsico de la calorimetra es la conservacin de la
energa. En un sistema aislado, cuyas partes interactan intercambiando calor, la suma algebraica de
los Q para todas las partes del sistema debe de ser cero.
2.2 TRANSFERENCIA DE CALOR CONDUCCIN, CONVECCIN Y RADIACIN
La conduccin es transferencia de energa debido al movimiento molecular dentro de un material, sin
movimiento del material. La corriente de calor H o conduccin depende del rea A por la que fluye
el calor, la longitud L del trayecto de flujo del calor, la diferencia (
) y la conductividad
trmica k del material. La conveccin es un proceso complejo de transferencia de calor, que implica
movimiento de masa de una regin a otra, depende del rea superficial, la orientacin y la diferencia
de temperatura entre un cuerpo y su entorno. La radiacin es transferencia de energa por radiacin
electromagntica, la corriente de calor H causada por la radiacin depende del rea superficial A, la
emisividad de de la superficie (un nmero puro adimensional entre 0 y 1) y la temperatura T en
Kelvin.
3 DESARROLLO EXPERIMENTAL
3.1 MATERIAL
Tabla 3.1 - Material
No Instrumento u objeto Incertidumbre Cantidad
1 Termopar 0.05 [C] 1
2 Cronmetro 0.5 [s] 1
3 Nitrgeno Lquido / 1
4 Alcohol / 1
5 Recipiente metlico / 2
3.2 EXPERIMENTO
Utilizamos 250 ml de alcohol que se vaciaron en el
recipiente metlico, despus se fue vaciando el
nitrgeno lquido, la cantidad de nitrgeno lquido no se
midi debido a que constantemente estuvimos
aadiendo ms para que el alcohol alcanzara la
temperatura deseada y mantenerla as hasta que
empezramos a tomar datos. La temperatura ms baja
que logramos conseguir fue de aproximadamente -80
C, pero para nuestro propsito consideramos un
intervalo de -60C a -5C, despus medimos como fue
variando la temperatura conforme avanzaba el tiempo,
el fenmeno al principio segua un patrn, pero hubo
un momento en el que la temperatura vari de una
manera drstica, no sabemos por qu ocurri ese salto,
suponemos que el aparato con el que mediamos la
temperatura fall por un momento, aun as despus la
lectura sigui con el mismo patrn que al inicio,
entonces a pesar de un salto, todos los dems datos
tienen la misma tendencia, por lo cual podemos hacer
un anlisis.
fig. 1.1 Mezcla a 11.8 C
4 RESULTADOS Y ANLISIS
A continuacin presentamos la serie de datos obtenida en la siguiente tabla, como notaremos es
difcil ver a simple vista un comportamiento, por lo que es necesario graficar los datos. La tabla
contiene 156 mediciones.
Tabla 4.1 Serie de datos de la mezcla criognica
Tiempo
t 0.5 [s]
Temperatura
0.05 [C]
1 2 3 4 5
t t t t t
0 -60 320 -53.3 900 -34.8 1540 -19.5 2180 -9.8
10 -59.7 330 -53.6 920 -34.3 1560 -19 2200 -9.7
20 -59.5 340 -53.2 940 -34.1 1580 -18.7 2220 -9.5
30 -59.3 350 -52.7 960 -33.1 1600 -18.4 2240 -9.3
40 -59 360 -52.3 980 -31 1620 -18.2 2260 -8.9
50 -58.8 370 -52.2 1000 -30.7 1640 -17.7 2280 -8.8
60 -58.5 380 -51.6 1020 -30.6 1660 -17.2 2300 -8.7
70 -58.2 400 -51.2 1040 -30.9 1680 -16.7 2320 -8.5
80 -57.9 420 -50.9 1060 -31.9 1700 -16.6 2340 -8
90 -57.6 440 -50.3 1080 -33 1720 -16.2 2360 -7.7
100 -57.3 460 -49.8 1100 -32 1740 -16 2380 -7.4
110 -57.2 480 -49.4 1120 -31.4 1760 -15.5 2400 -7.2
120 -56.9 500 -48.8 1140 -30.7 1780 -15.1 2420 -7.1
130 -56.8 520 -48.4 1160 -30.7 1800 -15 2440 -7
140 -56.7 540 -48 1180 -30.3 1820 -15 2460 -6.9
150 -56.5 560 -47.6 1200 -26.3 1840 -14.6 2480 -6.6
160 -56.3 580 -47.2 1220 -25.3 1860 -14.5 2500 -6.5
170 -55.9 600 -46.6 1240 -24.8 1880 -14.3 2520 -6.4
180 -55.7 620 -46.3 1260 -24.5 1900 -13.9 2540 -6.5
190 -55.7 640 -45.8 1280 -23.8 1920 -13.2 2560 -6.2
200 -55.5 660 -45.6 1300 -23.5 1940 -13.1 2580 -6.3
210 -55.2 680 -45 1320 -23.3 1960 -12.6 2600 -5.9
220 -55 700 -44.7 1340 -23 1980 -12.3 2620 -5.7
230 -54.8 720 -44.2 1360 -22.5 2000 -12.1 2640 -5.6
240 -54.6 740 -43.7 1380 -22.2 2020 -11.9 2660 -5.5
250 -54.5 760 -43.3 1400 -21.9 2040 -11.7 2680 -5.5
260 -54.3 780 -42.8 1420 -21.6 2060 -11.2 2700 -5.4
270 -54.2 800 -41.8 1440 -21.2 2080 -11.1 2720 -5
280 -54.1 820 -40.2 1460 -20.9 2100 -10.9 / /
290 -54 840 -35.1 1480 -20.6 2120 -10.6 / /
300 -53.7 860 -35.4 1500 -20.1 2140 -10.4 / /
310 -53.5 880 -34.9 1520 -20 2160 -10.1 / /
Al graficar los datos y hacer un ajuste cuadrtico y otro exponencial, obtenemos:
fig. 4.1 Grfica de datos dispersos y ajuste cuadrtico
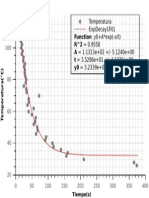
fig. 4.2 Grfica de datos dispersos y ajuste exponencial
0 500 1000 1500 2000 2500 3000
-60
-55
-50
-45
-40
-35
-30
-25
-20
-15
-10
-5
0
5
-60
-55
-50
-45
-40
-35
-30
-25
-20
-15
-10
-5
0
5
T
e
m
p
e
r
a
t
u
r
a
(
C
)
Tiempo (s)
Temperatura (C)
Parabola Fit of Temperatura
Temperatura vs Tiempo
0 500 1000 1500 2000 2500 3000
-60
-55
-50
-45
-40
-35
-30
-25
-20
-15
-10
-5
0
5
-60
-55
-50
-45
-40
-35
-30
-25
-20
-15
-10
-5
0
5
T
e
m
p
e
r
a
t
u
r
a
(
C
)
Tiempo (s)
Temperatura (C)
ExpDec1 Fit of Temperatura
Temperatura vs Tiempo
Al realizar el ajuste cuadrtico y el ajuste exponencial obtenemos las siguientes ecuaciones:
() = (4.8510
6
2.3510
7
) [
2
]
[
2
] +(0.03 6.2810
4
)[] +(62.81 0.33)[]()
() = (90.13 3.14)[]
(
[]
(2470.89150.08)[]
)
+(27.22 3.37)[] ()
Ahora bien, deberamos de preguntarnos qu significado fsico tienen las ecuaciones, en otras
palabras para que valores de t son vlidas las ecuaciones.
Ajuste cuadrtico: Observamos que cuando = 0 [], la temperatura es de 62.81 , este valor es
cercano al valor real del cual empezamos a tomar las mediciones, vemos que con = 2720 [] el
cul es nuestro ltimo dato obtenemos una temperatura de -17.01 [C], lo cual no corresponde con
los valores reales, si derivamos la ecuacin e igualamos a cero para obtener un punto crtico y
evaluando ese valor en la ecuacin, obtenemos: (3092.78 []) = 16.32 [], este nmero es el
valor mximo que puede tener nuestra ecuacin, lo que significa que cuando > 3092.78 [s], la
temperatura comenzara a disminuir segn el ajuste cuadrtico, lo cual es completamente errado, por
lo tanto descartamos este modelo ya que nuestro sistema jams alcanzara la temperatura ambiente
segn este ajuste cuadrtico.
Ajuste exponencial: Observamos que cuando = 0 [], la temperatura es de 62.91 , este valor al
igual que el ajuste anterior es un valor cercano al valor real inicial, ahora evaluamos el ltimo valor
obteniendo (2720 []) = 2.76 [], el cual es distinto del valor real pero slo difieren en 2.24 C,
como el ajuste exponencial es una funcin continua, entonces no hay lmites para valores de t, aun
as slo tomaremos en cuenta los valores que tienen sentido fsico, esto es tomaremos a t en el
intervalo: 60 [] () 24 [] que corresponden a la temperatura inicial hasta la temperatura
ambiente.
R de correlacin correspondiente a cada caso:
1
= 9921
2
= 9903
Notamos que la R de correlacin en ambos casos es muy buena, pero eso es porque cumple con la
serie de datos obtenidos sin tomar en cuenta que clase de fenmeno natural es.
5 CONCLUSIONES
Para fenmenos de este tipo es necesario realizar ajustes de tal manera que nos quede una funcin
continua, de otra manera el modelo ser incorrecto, podemos notar que el ajuste exponencial fue el
adecuado, o de cierta manera el que mejor modela este comportamiento, a pesar de que nuestros datos
en un intervalo de tiempo dieron saltos debido al instrumento de medicin, al final el modelo obtenido
funciona de una manera aceptable, si nuestra serie de datos hubiese tenido un mejor comportamiento,
el ajuste sera an ms preciso.
6 REFERENCIAS
Hugh D. Young y Roger A. Freedman, Fsica Universitaria vol.1, decimosegunda edicin,
editorial Pearson, 2009, pgs. 591-597.
Berta Oda Noda, Introduccin al anlisis grfico de datos experimentales, tercera edicin, las
prensas de ciencias, Facultad de Ciencias, UNAM.
Вам также может понравиться
- Principios Activos de Un CosméticoДокумент14 страницPrincipios Activos de Un CosméticoGlorivy E. Mora Gonzalez100% (1)
- EXCRECION EN PLANTAS GRADO 7.docx2Документ4 страницыEXCRECION EN PLANTAS GRADO 7.docx2Fabian Franco Valbuena100% (1)
- Nenn U2 A2 Salr.Документ6 страницNenn U2 A2 Salr.Ney RodriguezОценок пока нет
- Pegado de Uniones de Tubos de FRPДокумент22 страницыPegado de Uniones de Tubos de FRPWilfredoCaveroCarrascoОценок пока нет
- Practica 3Документ6 страницPractica 3enriquegomezcruzОценок пока нет
- P08 - Practica FinalДокумент5 страницP08 - Practica FinalenriquegomezcruzОценок пока нет
- Ley de Enfriamiento de NewtonДокумент9 страницLey de Enfriamiento de NewtonenriquegomezcruzОценок пока нет
- Tarea 4Документ2 страницыTarea 4enriquegomezcruzОценок пока нет
- Cilindro AluminioДокумент1 страницаCilindro AluminioenriquegomezcruzОценок пока нет
- Ley de Enfriamiento de NewtonДокумент9 страницLey de Enfriamiento de NewtonenriquegomezcruzОценок пока нет
- Comentarios y OpinionesДокумент1 страницаComentarios y OpinionesenriquegomezcruzОценок пока нет
- M.F.rosales LógicaДокумент25 страницM.F.rosales LógicaenriquegomezcruzОценок пока нет
- Tarea 4Документ3 страницыTarea 4enriquegomezcruzОценок пока нет
- Tarea 4Документ3 страницыTarea 4enriquegomezcruzОценок пока нет
- Papel Indicador de PHДокумент3 страницыPapel Indicador de PHArévaloОценок пока нет
- Porcentaje de Solidos Totales de La Leche y El Metodo de GerberДокумент15 страницPorcentaje de Solidos Totales de La Leche y El Metodo de GerberKEVIN SAAVEDRA FARFANОценок пока нет
- JuntasДокумент9 страницJuntasJuan Carlos VacaflorОценок пока нет
- Escalas de Temperatura TallerДокумент3 страницыEscalas de Temperatura TallerLaura Camila Medina PatiñoОценок пока нет
- Incendios y Explosiones.Документ4 страницыIncendios y Explosiones.leidyОценок пока нет
- Electivo Química Disoluciones GUIA. Unidades de Concentración FisicasДокумент4 страницыElectivo Química Disoluciones GUIA. Unidades de Concentración FisicasJohana TipanОценок пока нет
- Guia QuimicaДокумент17 страницGuia QuimicaLuisRdz1230% (1)
- Pre Presentacion 13 7v Nomenclatura 1 2023 1Документ27 страницPre Presentacion 13 7v Nomenclatura 1 2023 1Nicolle Campos chamorroОценок пока нет
- Practica 8Документ2 страницыPractica 8Roberto AlfanoОценок пока нет
- Manual de SoldadurasДокумент0 страницManual de SoldadurasLlacho Colque W. DavidОценок пока нет
- Microestructura 5Документ30 страницMicroestructura 5Juancho MendozaОценок пока нет
- Problemas Repaso 1º Ev. 1º BatДокумент2 страницыProblemas Repaso 1º Ev. 1º BatEstela ClooneyОценок пока нет
- Actividad 6 Propiedades Fisicas. Unidad 4Документ4 страницыActividad 6 Propiedades Fisicas. Unidad 4JuanCarlosGonzalezОценок пока нет
- EQUILIBRIO QUIMICO KpsДокумент27 страницEQUILIBRIO QUIMICO KpsxmarioxxОценок пока нет
- Fruta en Almíbar-1Документ2 страницыFruta en Almíbar-1Eliza MoralesОценок пока нет
- Examen de Recuperación QuímicaДокумент5 страницExamen de Recuperación QuímicaJuan Alberto HernandezОценок пока нет
- Introducción Al Balance de EnergíaДокумент18 страницIntroducción Al Balance de Energíagioeli321Оценок пока нет
- Anexo V Memoria de Calculo de Compresor AireДокумент9 страницAnexo V Memoria de Calculo de Compresor AireCarlos Seg SantОценок пока нет
- Cuadro Sinoptico SIGДокумент1 страницаCuadro Sinoptico SIGRamon AgundezОценок пока нет
- Clase 3 - Diseño Del MoldeДокумент6 страницClase 3 - Diseño Del Moldeok100% (1)
- 4 Cavitacion PDFДокумент23 страницы4 Cavitacion PDFVan SanchezОценок пока нет
- C5 M1 Quimica Anexo 03Документ5 страницC5 M1 Quimica Anexo 03Sofia NavaОценок пока нет
- Ana0001230 PDFДокумент209 страницAna0001230 PDFArmando Alejandro Ynquilla RuizОценок пока нет
- PRACTICA 9 Disribucion de Tiempos de ResidenciaДокумент16 страницPRACTICA 9 Disribucion de Tiempos de ResidenciaAriel Flores OrtuñoОценок пока нет
- Tratamiento de Aguas Residuales Domesticas e IndustrialesДокумент96 страницTratamiento de Aguas Residuales Domesticas e Industrialesanon_727083560Оценок пока нет