Академический Документы
Профессиональный Документы
Культура Документы
Ejemplos
Загружено:
Jose ReynosoОригинальное название
Авторское право
Доступные форматы
Поделиться этим документом
Поделиться или встроить документ
Этот документ был вам полезен?
Это неприемлемый материал?
Пожаловаться на этот документАвторское право:
Доступные форматы
Ejemplos
Загружено:
Jose ReynosoАвторское право:
Доступные форматы
https://procesosbio.wikispaces.
com/Kla
KLa coeficiente de transferencia de masa
En reactores que son de tipo tanque agitado, el coeficiente volumtrico de transferencia de
materia, k
La
, aumenta conforme se incrementa el caudal de aire suministrado, esto puede ser
tanto en agua como en lquidos orgnicos.
La prediccin del coeficiente de transferencia de materia en columnas de burbujeo con
recirculacin se realiza mediante un modelo terico propuesto en el equipo de investigacin y
desarrollado a partir de un modelo fluido dinmico de Garca Calvo, 1989, basado en un
balance de energa y en las teoras de la Penetracin de Higbie y la Turbulencia Isotrpica de
Kolmogoroff, para sistemas bifsicos y trifsicos G-L-S y diferentes configuraciones de reactor
(columnas de burbujeo con y sin recirculacin).
Debe distinguirse entre la transferencia de masa y el movimiento de masas de fluido (o flujo de
fluidos) que se presenta en un nivel macroscpico conforme un fluido se transporta de un lugar
a otro. La transferencia de masa requiere la presencia de dos regiones con composiciones
qumicas diferentes y se refiere al movimiento de especies qumicas desde una regin de alta
concentracin hacia una de concentracin menor. La fuerza impulsora primaria para el flujo de
fluidos es la diferencia de presin, en tanto que, para la transferencia de masa, es la diferencia
de concentracin.
FACTORES QUE AFECTA A KLa
El kLa va a ser afectado por varias condiciones como la configuracin del reactor, las
condiciones de operacin, la velocidad de agitacin, el caudal de aire suministrado y la fraccin
de fase orgnica, en el caso de emplear medios bifsicos en lugar de lquidos puros.
En el caso de ser afectado por sustancias orgnicas que segn su estructura qumica irn
aumentando o disminuyendo el k
La
. La exagerada o moderada velocidad de agitacin y la
alta viscosidad tambin afectan enormemente la k
La
, otros factores que afectan la K
La
son el
exceso deaireacin y la temperatura, esta ltima afecta el coeficiente de difusin y solubilidad.
La teora de Penetracin de Higbie establece que el coeficiente de transferencia de materia en
fase liquida es funcin del tiempo de contacto, , entre un elemento del lquido y la superficie
del gas, pudindose expresar como:
El tiempo de contacto (), puede ser deducido considerando la teora de la Turbulencia
Isotrpica, en la que la disipacin de la energa se produce principalmente por los remolinos o
turbulencia a escala microscpica. Estos remolinos de pequeo tamao son los que
interaccionan con la superficie de las burbujas como un elemento de contacto liquido.
1. Efecto de la Temperatura
Est definido por la relacin de Arhenius
Kt= K20
o
*^(T-20
o
)
Kt coficiente global de transferencia de oxgeno (K
La
) a la temperatura T, (C)
coeficiente sin dimensin cuyos valores varan entre 1,016 y 1,037
Para la aireacin mecnica el valor de puede tomarse como 1,024 1,028
En el siguiente documento existe una lista de coeficientes de difusion con la temperatura a la
cual fueron medidos COEFICIENTES DE DIFUSION
2. Saturacion de oxigeno
La saturacion de oxigeno en agua esta relacionada con la temperatura. Ademas esta
relacionada con la presion parcial del oxigeno en fase gaseosa (Ley de Henry). Es comveniente
usar una saturacion promedio en la profundidad del tanque que puede ser estimada como:
3. Nivel de oxigeno disuelto
Para sistemas de tratamiento biologico que remueven carbonos organicos, el nivel de oxigeno
disuelto CL, cuando esta operando puede variar entre 0,5 y 1.5 mg/l. Cuando la nitrificacion
esta por alcanzarse el oxigeno disueto puede estar en un exceso de 2,0 mg/l.
MEDICIN DE kLa
La medicin del K
La
es muy importante en un cultivo microbiano aerobio dentro de un
biorreactor, donde se analiza la transferencia de O
2
de las burbujas de aire provenientes de un
aireador a las clulas bacterianas, adems se estudia el balance de Oxgeno en el cultivo para
mantener las condiciones aptas para las clulas. La velocidad de transferencia de O
2
(rO
2
)
desde el seno de la fase gaseosa (burbujas) hasta la fase lquida (medio lquido) est
determinada por la siguiente ecuacin :
rO
2
= K
La
(C*- C)
Donde:
K
La
--> Coeficiente volumtrico de transferencia de oxgeno C--> Concentracin de O
2
disuelto
en el seno del lquido C --> Concentracin de O
2
disuelto en equilibrio con la presin parcial de
oxgeno de la fase gaseosa.
El K
La
y por lo tanto el grado de transferencia de oxgeno desde el seno del lquido hasta las
clulas o microorganismos en cultivo, dependen de lo mencionado anteriormente; del diseo
del biorreactor y de las condiciones de operacin del sistema de cultivo: caudal de aire,
volumen del lquido, rgimen de agitacin, rea de transferencia y viscosidad del cultivo. En
general, disminuyen el K
La
: la viscosidad y el volumen del lquido y aumentan el K
La
: el rea de
transferencia, la agitacin y la presencia de dispositivos que aumenten una o ambas.
Dentro del cultivo, la tasa especfica de consumo de oxgeno de las bacterias est determinada
por la velocidad de transferencia de oxgeno (rO
2
) y el K
La
. Se debe conocer la rO
2
para poder
determinar el K
La
; el valor de rO
2
se consigue en la literatura; la concentracin de oxgeno
disuelto en el lquido (C) es equivalente al valor de OD, e instrumentalmente, se llama: razn
de toma de oxigeno (OUR) por sus siglas en ingls; el equivalente a C* (concentracin de
oxgeno disuelto en el lquido en equilibrio con el gas) es la demanda bioqumica de oxgeno
(DBO) que, instrumentalmente se llama: razn especfica de toma de oxigeno: SOUR (specific
oxygen uptake rate).
Ambas razones se pueden medir al regularlas con un controlador OUR/SOUR de uso
comercial.
Debido a la dificultad existente para predecir K
La
existen 2 mtodos (Balance de oxgeno y
dinmico); en cualquier mtodo que se utilice para medir K
La
las condiciones de medida deben
ser lo ms similares posibles a las existentes en el fermentador durante la operacin Vant Riet
ha recopilado las tcnicas existentes para medir K
La
.
MTODO DE BALANCE DE OXIGENO
Este mtodo de medida de Kla se basa en un balance de materia en estado estacionario para
el 02, en el cual se mide el contenido de 02 de las corrientes gaseosas hacia o desde el
fermentador.
Esta tcnica se basa en la ecuacin 1 mencionada anteriormente que defina la transferencia
de materia gas-lquido . En este mtodo se mide desde el fermentador. De un balance de
materia en estado estacionario, la diferencia entre el flujo de oxgeno a la entrada y a la salida
debe ser igual a la velocidad de transferencia de oxgeno desde el gas hacia el lquido: (Dorn
P.,1998)
Donde:VL: Volumen del lquido en el fermentador Fg: Caudal volumtrico de gas.CAG:
Concentracin de oxgeno en fase de gas y los subndices i y ose refieren a las corrientes de
entrada y salida, respectivamente en el primer trmino de la parte derecha de la ecuacin
representa la velocidad a la que el oxgeno entra en el fermentador mientras que el segundo
representa la velocidad de salida. La diferencia entre ellas es la velocidad a la que se transfiere
oxgeno del gas al lquido, NA. Dado que la concentracin de gas se mide generalmente como
presin parcial, puede incorporarse la ley de los gases ideales con lo cual se obtiene la
siguiente expresin: (Dorn P.,1998)
Donde:
R--> constante universal de los gases.
P
AG
--> Presin parcial de oxgeno en el gas
T --> Temperatura absoluta.
Las presiones parciales de oxgeno en las corrientes de entrada y de salida no suelen ser muy
diferentes durante la operacin por lo que es necesario medirlas con una gran precisin, por
ejemplo, utilizando un espectrmetro de masas. La temperatura y el caudal de gases tambin
dese ser medido con cuidado para asegurar un valor preciso de NA. Una vez que se
conoce NA se han encontrado los valores de CAL Y C*AL mediante los mtodos descritos
anteriormente, el parmetro K
La
puede calcularse a partir de la ecuacin 1.
Ventajas del mtodo:
-El mtodo de balance de oxgeno en estado estacionario es el procedimiento ms fiable para
medir kLa
-Permite su determinacin con tan solo una medida
-El mtodo puede aplicarse a los fermentadores durante la operacin.
-Desventajas del mtodo:
-depende de la precisin en la medida de la composicin de gas, caudal, presin y
temperatura.
-Pueden cometerse errores de ms o menos el 100% si las tcnicas de medicin no son
adecuadas.
Dibujo.bmp
Details
Download
305 KB
MTODO DINMICO
Este mtodo de medida de K
La
se basa en un balance de materia en estado no estacionario
para el oxgeno.
Existen varias versiones diferentes del mtodo dinmico. Inicialmente, el fermentador contiene
clulas en un cultivo discontinuo. Como se muestra en la figura , en un determinado instante to
el caldo es desoxigenado bien por introduccin de nitrgeno en el recipiente o parando el flujo
de aire si el cultivo consume oxgeno. La concentracin de oxgeno disuelto CAL disminuye
drsticamente durante este perodo. Posteriormente se bombea aire en el cultivo con un caudal
tiempo. Es importante que la concentracin de oxgeno permanezca siempre por encima de
Ccrit para que la velocidad de consumo de oxgeno existente. Suponiendo que la reoxigenacin
del caldo es suficientemente rpida para permitir el crecimiento de la clulas, el nivel de
oxgeno disuelto alcanzar pronto un valor en estado estacionario CAL promedio que refleja un
balance entre el suministro de oxgeno y el consumo existentes en el sistema. CAL
1
y CAL
2
son
dos concentraciones de oxgeno medidas durante la reoxigenacin a tiempos t
1
y t
2
,
respectivamente. De esta manera puede desarrollarse una ecuacin para K
La
en funcin de
estos datos experimentales.
Durante la etapa de reoxigenacin, el sistema se encuentra en estado no estacionario. La
velocidad con que vara la concentracin de oxgeno disuelto durante este perodo es igual a la
velocidad de transferencia de oxgeno desde el gas hasta el lquido menos la velocidad de
consumo de oxgeno por las clulas: (Dorn P.,1998)
Donde:qox --> Velocidad de consumo de oxgeno.
De esta manera puede determinarse una expresin para qox considerando el estado final de
concentracin de oxgeno disuelto, C*AL. CuandoCAL=C*AL, dCAL/dt= 0 por que no existe
variacin en CAL con el tiempo. Por lo tanto, de la ecuacin anterior
Sustituyendo este resultado en la ecuacin y cancelando los trminos K
La
C*AL se obtiene:
Suponiendo que k
La
constante en el tiempo la ecuacin puede integrarse entre t
1
y t
2
utilizando
las reglas de integracin. La ecuacin resultante para k
La
es:
Ventajas del mtodo:
-Menor coste del equipo utilizado.
Desventajas del mtodo:
-no tiempos de respuesta rpido de las sonda de 02
-tiempo de respuesta de electrodo similar a tiempo necesario para transferencia de materia.
- valores de CAL medidos no reflejan conc. Instantnea de oxgeno.
-tiempo medio de residencia del gas en el sistema cuando a la desoxigenacin le sigue la
aireacin (gases residuales).
- media de CA no refleja la cintica de la transferencia de 02 hasta que se establece de nuevo
el contenido total de ste.
- medicin de kLa se encuentra restringido a recipientes con alturas menores a 1m.
-inapropiados para caldos viscosos por grandes tiempos de residencia de las burbujas.
EJEMPLO 1
Un fermentador agitado de 20L que contiene un cultivo de Bacillus Thuringiensis a 30 C se
utiliza para la produccin de un insecticida microbiano. El valor de KLa se determina mediante
el metodo dinmico. Se corta aire durante unos pocos minutos disminuyentdo el nivel de
oxgeno disuelto y posteriormente se viuelve a restablecer. Cuando se alcanza el estado
estacionario, la tensin del oxgeno disuelto es el 78% de aire. Se obtuvieron los siguientes
datos :
||Tiempo
5 15
Tensin de oxgeno 50 66
a) Calcular K
La
b) Se comete un error en la determinacin del nivel de oxgeno disuelto en estado estacionario,
de manera que en vez del 78% se ha tomado un valor del 70%. Cul es el porcentaje de error
en K
La
como resultado de eeste 10% de error en la medicin de CAL.
Solucin:
a) CAL = 78% de saturacin de aire. Si se define t1= 5s, CAL1 = 66%.
K
La
= Ln (78-50 / 78-66) / (15-5)s
K
La
= 0.085 s-1
b) Si CAL se considera ser el 70% de saturacin de aire
K
La
= Ln (70-50 / 70-66) / (15-5)s
K
La
= 0.16 s-1
El error en K
La
es casi del 100%. Esto muestra la importancia de tener datos
EJEMPLO 2
Se utiliza el metodo dinamico para medir Kla en un fermentador que opera a 30C. Los datos de
concentracion de oxigeno disuelto en funcion del tiempo durante la etapa de reoxigenacion son
los siguientes:
Tiempo (s) CAL (% de saturacin de aire)
10 43,5
15 53,5
20 60,0
30 67,5
40 70,5
50 72,0
70 73,0
100 73,5
130 73,5
La concentracin de equilibrio del oxigeno en el caldo es 7,9x10^-3 kg/m3. Calcular Kla.
Solucion
El Kla se calcula mediante la ecuacin siguiente:
Tomando como t1= 10 segundos y CAL=43% de saturacin de aire. El estado estacionario de
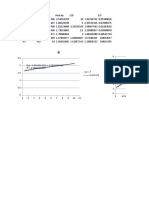
oxigeno disuelto es 73,5%. Los valores de In y t se muestran en la siguiente tabla:
(s)
0,00 0
0,41 5
0,80 10
1,60 20
2,30 30
3,00 40
4,10 6
Con los datos obtenidos en la tabla anterior procedemos a realizar la grafica:
El valor de la pendiente es igual al kla en este caso es de 0,069 s-1.
DIFUSIN
N DE MASA
La ley de Fick de la difusin, propuesta en 1855, afirma que la razn de difusin de una
especie qumica en el espacio de una mezcla gaseosa (o de una solucin lquida o slida) es
proporcional al gradiente de concentracin de esa especie en ese lugar. Aunque una
concentracin ms elevada para una especie significa ms molculas de ella por unidad de
volumen, la concentracin de una especie puede expresarse de varias maneras. A
continuacin, se describen dos formas comunes.
Base msica
En una base msica, la concentracin se expresa en trminos de densidad (o concentracin de
masa), la cual es la masa por unidad de volumen. Si se considera un volumen pequeo V en
un lugar dentro de la mezcla, las densidades de una especie (subndice i) y de la mezcla (sin
subndic
e) en ese lugar quedan dadas por:
Por lo tanto, la densidad de una mezcla en un lugar es igual a la suma de las densidades de
sus constituyentes en ese lugar. La concentracin de masa tambin puede expresarse en
forma adimensional en trminos de la fraccin de masa, w, como
Ntese que la fraccin de masa de una especie vara entre 0 y 1, y la conservacin de la masa
requiere que la suma de las fracciones de masa de los constituyentes de una mezcla sea igual
a 1. Es decir, wi 1. Asimismo, obsrvese que, en general, la densidad y la fraccin de masa
de un constituyente en una mezcla varan con el lugar, a menos que los gradientes de
concentracin sean cero.
Base molar
En una base molar, la concentracin se expresa en trminos de concentracin molar (o
densidad molar), la cual es la cantidad de materia, en kmol, por unidad de volumen. Una vez
ms, si se considera un volumen pequeo V en un lugar dentro de la mezcla, las
concentraciones molares de una especie (subndice i) y de la mezcla (sin subndice) en ese
lugar quedan dadas por
Por lo tanto, la concentracin molar de una mezcla en un lugar es igual a la suma de las
concentraciones molares de sus constituyentes en ese lugar. La concentracin molar tambin
puede expresarse en forma adimensional en trminos de la fraccin molar y como
Una vez ms, la fraccin molar de una especie vara entre 0 y 1, y la suma de las fracciones
molares de los constituyentes de una mezcla es la unidad, yi 1. La masa m y el nmero de
moles, N, de una sustancia estn relacionados entre s por m NM (o, para una unidad de
volumen, r CM), en donde M es la masa molar (tambin llamada peso molecular) de la
sustancia. Esto es de esperarse, puesto que la masa de 1 kmol de la sustancia es M kg, por lo
que la masa de N kmol es NM kg. Por lo tanto, las concentraciones de masa y molar estn
relacionadas entre s por
donde M es la masa molar de la mezcla, la cual puede determinarse a partir de
Las fracciones de masa y molar de la especie i de una mezcla estn relacionadas entre s por
En los prrafos anteriores, se presentan dos enfoques diferentes para la descripcin de la
concentracin en un lugar y puede ser que el lector se est preguntando cul de ellos es mejor
para ser aplicado. Bien, la respuesta dependee la situacin en la que se encuentre. Los dos
enfoques son equivalentes y el mejor de ellos para un problema dado es el que proporcione
con ms facilidad la solucin deseada.
ANALOGA ENTRE LA TRANSFERENCIA DE MASA Y LA DE CALOR
Se ha consumido una cantidad considerable de tiempo en el estudio de la transferencia de
calor y se podra consumir el mismo en el estudio de la transferencia de masa. Empero, los
mecanismos de ambas son anlogos entre s y, como consecuencia, puede desarrollarse una
comprensin de la transferencia de masa en corto tiempo y con poco esfuerzo, sencillamente al
trazar paralelos entre ellas. El establecimiento de esos puentes entre las dos reas, no
relacionadas en apariencia, har posible usar el conocimiento de la transferencia de calor para
resolver problemas de transferencia de masa. De manera alterna, adquirir un conocimiento
aplicable de transferencia de masa ayudar a comprender mejor los procesos de transferencia
de calor, al concebir a ste como una sustancia sin masa, como lo hicieron en el siglo XIX. La
teora de corta duracin del calrico, referente al calor, es el origen de la mayor parte de la
terminologa de la transferencia de calor usada en la actualidad y sirvi bien para sus fines
hasta que se reemplaz por la teora cintica. En esencia, la masa es energa, ya que masa y
energa pueden convertirse una en la otra segn la frmula de Einstein E mc2, en donde c es la
velocidad de la luz.
Por lo tanto, la masa y el calor pueden mirarse como dos formas diferentes de energa y
explotar ventajosamente esto, sin irse por la borda.
Temperatura
La fuerza impulsora para la transferencia de calor es la diferencia de temperatura. Como
contraste, la fuerza impulsora para la transferencia de masa es la diferencia de concentracin.
Puede verse la temperatura como una medida de la concentracin de calor y, de este modo,
una regin a alta temperatura es aquella que tiene una alta concentracin de calor. Por lo tanto,
tanto el calor como la masa se transfieren de las regiones ms concentradas hacia las menos
concentradas. Si no hay diferencia de temperatura entre dos regiones, entonces no existe
transferencia de calor. De modo semejante, si no existe diferencia entre las concentraciones de
una especie en regiones diferentes de un medio, no habr transferencia de masa.
Conduccin
El lector recordar que el calor se transfiere por conduccin, conveccin y ra-diacin. Sin
embargo, la masa se transfiere slo por conduccin (llamada di-fusin) y conveccin, y no
existe algo llamado radiacin de masa (a menos que haya algo que Scotty sepa y nosotros
no, cuando transporta a las personas a travs de un rayo hacia cualquier parte en el espacio,
a la velocidad de la luz). La razn de conduccin del calor en una direccin x es pro-porcional
al gradiente de temperatura dT/dx en esa direccin y se expresa por la ley de Fourier de la
conduccin del calor como
donde k es la conductividad trmica del medio y A es el rea normal a la di-reccin de
transferencia del calor. De modo semejante, la razn de difusin de masa, mdif, de una
especie qumica A en un medio en reposo, en la direccin x, es proporcional al gradiente de
concentracin dC/dx en esa direccin y se expresa mediante la ley de Fick de la difusin
donde DAB es el coeficiente de difusin (o difusividad de la masa) de la especie en la mezcla y
CA es la concentracin de esa especie en la mezcla en ese lugar.
Puede demostrarse que las ecuaciones diferenciales, tanto para la conduccin de calor como
para la difusin de masa, tienen la misma forma. Por lo tanto, con slo cambiar los coeficientes
y variables correspondientes, pueden obtenerse las soluciones de las ecuaciones de la difusin
de masa a partir de las soluciones de las ecuaciones correspondientes de la conduccin del
calor, para el mismo tipo de condiciones de frontera.
Generacin de calor
La generacin de calor se refiere a la conversin de alguna forma de energa, como la
elctrica, la qumica o la nuclear, en energa trmica sensible en el medio. La generacin de
calor se desarrolla en toda la extensin del medio yse exhibe como una elevacin de la
temperatura. De manera anloga, en algunos problemas de transferencia de masa intervienen
reacciones qumicas que ocurren dentro del medio y dan como resultado la generacin de una
especie en toda su extensin. Por lo tanto, la generacin de especies es un fenmeno
volumtrico y la razn de generacin puede variar de punto a punto en el medio. Esas
reacciones que ocurren dentro del medio se llaman reacciones homogneas y son anlogas a
la generacin interna de calor. En contraste, algunas reacciones qumicas dan como producto
la generacin de una especie en la superficie, como resultado de que ocurren en la superficie
debido al contacto entre el medio y los alrededores. ste es un fenmeno superficial y, como
tal, necesita tratarse como una condicin de frontera. En los estudios de transferencia de masa,
esas reacciones se conocen como reacciones heterogneas y son anlogas al flujo
especificado de calor en la superficie.
Conveccin
El lector recordar que la conveccin de calor es el mecanismo de transferencia de calor en el
que intervienen tanto la conduccin de calor (difusin molecular) como el movimiento de la
masa de fluido. El movimiento del fluido mejora en forma considerable la transferencia de calor,
al quitar el fluido calentado cercano a la superficie y reemplazarlo por el ms fro que se
encuentra ms alejado. En el caso lmite de que no hay ningn movimiento de la masa de
fluido, la conveccin se reduce a conduccin. De modo semejante, la conveccin de masa (o
transferencia de masa por conveccin) es el mecanismo de transferencia de masa entre una
superficie y un fluido en movimiento en el que intervienen tanto la difusin de masa como el
movimiento de la masa de fluido. El movimiento del fluido mejora tambin en forma
considerable la transferencia de masa, al quitar el fluido con alta concentracin cercano a la
superficie y reemplazarlo por el de concentracin ms baja que se encuentra ms alejado. En
la conveccin de masa, se define una capa lmite de concentracin de manera anloga a la
capa lmite trmica y se determinan nuevos parmetros adimensionales, que son las
contrapartes de los nmeros de Prandtl y de Nusselt.
La razn de la conveccin de calor para el flujo externo se expres en forma conveniente por la
ley de Newton del enfriamiento como
donde hconv es el coeficiente de transferencia de calor, As es el rea superficial y Ts T es la
diferencia de temperatura de uno a otro lado de la capa lmite trmica. De modo semejante, la
razn de la conveccin de masa puede expresarse como
donde hmasa es el coeficiente de transferencia de masa, As es el rea superficial y Cs C es
una diferencia apropiada de concentracin de uno a otro lado de la capa lmite de
concentracin.
La analoga es vlida para los casos de baja razn de transferencia de masa, en los cuales el
gasto de las especies que experimentan el flujo de masa es bajo (menor a 10%) en relacin
con el gasto total de la mezcla lquida o gaseosa.
TRANSFERENCIA DE OXIGENO EN GRANDES
RECIPIENTES
La medicin de transferencia de oxgeno en grandes recipeintes presenta dificultades
especiales. Esto requiere que la fase gas y liquido esten perfectamente mezcladas y con
turbulencias uniformes.
En los reactores de taano comercial (>10 m3), la mezcla perfecta es difcil de alcanzar por lo
que el valor de K
La calculado puede depender del tanque donde se realicen las medidas de concentracin.Incluso cuando exista una
buena mezcla la variacin en la composicion es inevitable debido a los cambios en la presin esttica y a la continua disolucin del oxgeno.
En el siguiente documento se encuentra informacin ms detallada acerca del coeficiente de transferencia de Oxgeno:
Coeficiente volumtrico de transferencia de O2.pdf
Details
Download
1 MB
Вам также может понравиться
- Mip Assal 2 - 2018Документ12 страницMip Assal 2 - 2018Jose ReynosoОценок пока нет
- Modulo3 - PRINCIPIO 2Документ5 страницModulo3 - PRINCIPIO 2Jose ReynosoОценок пока нет
- Modulo7 HaccpДокумент8 страницModulo7 HaccpJose ReynosoОценок пока нет
- Modulo8 HaccpДокумент6 страницModulo8 HaccpJose ReynosoОценок пока нет
- Glosario HaccpДокумент3 страницыGlosario HaccpJose ReynosoОценок пока нет
- Modulo2 - PRINCIPIO 1Документ8 страницModulo2 - PRINCIPIO 1Jose ReynosoОценок пока нет
- Modulo5 HaccpДокумент4 страницыModulo5 HaccpJose ReynosoОценок пока нет
- Modulo6 HaccpДокумент8 страницModulo6 HaccpJose ReynosoОценок пока нет
- Unidad 1Документ19 страницUnidad 1Jose ReynosoОценок пока нет
- 5s InicioДокумент14 страниц5s InicioharopatricioОценок пока нет
- 5s InicioДокумент14 страниц5s InicioharopatricioОценок пока нет
- Modulo4 - PRINCIPIO 3Документ3 страницыModulo4 - PRINCIPIO 3Jose ReynosoОценок пока нет
- Reacciones ParaleloДокумент12 страницReacciones Paralelokarito2005Оценок пока нет
- Estimulo RespuestaДокумент9 страницEstimulo RespuestaJose ReynosoОценок пока нет
- Unidad 4 El Aparato LocomotorДокумент21 страницаUnidad 4 El Aparato LocomotorJose ReynosoОценок пока нет
- Etas Alimentos Que EnfermanДокумент29 страницEtas Alimentos Que EnfermanJose ReynosoОценок пока нет
- 8 Reactores para Reacciones Sólido-Fluido CatalíticasДокумент11 страниц8 Reactores para Reacciones Sólido-Fluido CatalíticasJose ReynosoОценок пока нет
- RexperimentalesДокумент5 страницRexperimentalesAnaBelenMedranoBarrientosОценок пока нет
- Apuntes de Cinética QuímicaДокумент321 страницаApuntes de Cinética QuímicaBarryBurton83Оценок пока нет
- CatalisisДокумент21 страницаCatalisisKev LhuillierОценок пока нет
- RtasДокумент1 страницаRtasJose ReynosoОценок пока нет
- Certificado Famiq - Testificacion Inspeccion InoxpaДокумент1 страницаCertificado Famiq - Testificacion Inspeccion InoxpaJose ReynosoОценок пока нет
- Nota de Calidad: Famiq S.R.LДокумент1 страницаNota de Calidad: Famiq S.R.LJose ReynosoОценок пока нет
- RtasДокумент1 страницаRtasJose ReynosoОценок пока нет
- Perfil Cargo SoldadorДокумент3 страницыPerfil Cargo SoldadorJosé Aqueda Muñoz100% (1)
- RtasДокумент1 страницаRtasJose ReynosoОценок пока нет
- Actualizacion ISO 9001-2015Документ69 страницActualizacion ISO 9001-2015Mharlos CeОценок пока нет
- ORD 6402 Codigo Edificacion PDFДокумент107 страницORD 6402 Codigo Edificacion PDFJose ReynosoОценок пока нет
- Cinetica de Las FermentacionesДокумент28 страницCinetica de Las FermentacionesJose ReynosoОценок пока нет
- Ejercicio de 9Документ2 страницыEjercicio de 9Jose ReynosoОценок пока нет
- Copia de Matriz Legal de Medio Ambiente 09 04 13Документ423 страницыCopia de Matriz Legal de Medio Ambiente 09 04 13JulissaОценок пока нет
- Gustavo Bueno - Análisis Del Protágoras de Platón - 1980Документ64 страницыGustavo Bueno - Análisis Del Protágoras de Platón - 1980Luis PurisОценок пока нет
- Ccs de La TierraДокумент8 страницCcs de La TierraVictoria MartinezОценок пока нет
- Ambiente y EcosistemaДокумент11 страницAmbiente y EcosistemaKatherineОценок пока нет
- Sanchez Daniel R3 U1Документ7 страницSanchez Daniel R3 U1aaronОценок пока нет
- Natural Gas DehydrationДокумент17 страницNatural Gas DehydrationRené EstradaОценок пока нет
- Norma de Gases Venezolana 5011-2020-1Документ537 страницNorma de Gases Venezolana 5011-2020-1David DuqueОценок пока нет
- Campo LénticosДокумент9 страницCampo LénticosEstefany Arias BernalОценок пока нет
- Informe Introducción Ing 2Документ30 страницInforme Introducción Ing 2YHEISON AGUILAR PONTEОценок пока нет
- Memoria Descriptiva de CocharcasДокумент15 страницMemoria Descriptiva de CocharcasKevin PiñinОценок пока нет
- 30 Plan Mitigacion y Monitoreo AmbientalДокумент6 страниц30 Plan Mitigacion y Monitoreo AmbientalElizabeth WrightОценок пока нет
- Captacion de Agua UesДокумент256 страницCaptacion de Agua UesdanyОценок пока нет
- Clima en ChinchaДокумент15 страницClima en ChinchaIvan Carbajal GonzalesОценок пока нет
- Presentación de Programa de EcologíaДокумент26 страницPresentación de Programa de EcologíaVeronica BuenrostroОценок пока нет
- Tarea3 PS3Документ4 страницыTarea3 PS3karla guevaraОценок пока нет
- Mapa ConceptualДокумент2 страницыMapa ConceptualNicol MayoОценок пока нет
- (Informe 6) Ley de HookeДокумент9 страниц(Informe 6) Ley de HookeAnverly Zamora100% (1)
- Matriz de LeopoldДокумент25 страницMatriz de LeopoldMaYra RamiRezОценок пока нет
- Cuadro SinopticoДокумент2 страницыCuadro SinopticoMiguel Bonilla JahОценок пока нет
- Alex Leonel Cañar RivasДокумент92 страницыAlex Leonel Cañar RivasJorge JaramilloОценок пока нет
- Mineria SubterraneaДокумент34 страницыMineria SubterraneaPablo Andres Sandoval50% (4)
- Brayan Alexis Moto Calvo - Primer ParcialДокумент5 страницBrayan Alexis Moto Calvo - Primer ParcialMfcj Catemaco Uno VerОценок пока нет
- Práctica 4 FISICA BASICA USACДокумент6 страницPráctica 4 FISICA BASICA USACEddie MaczОценок пока нет
- Rocas MetamorficasДокумент52 страницыRocas Metamorficaslouweey100% (1)
- Suelos Principio de ArquimidesДокумент16 страницSuelos Principio de ArquimidesWaldir Pariatanta Irene100% (1)
- Cuestionario Practica N°1 de Laboratorio de Quimica 100LДокумент2 страницыCuestionario Practica N°1 de Laboratorio de Quimica 100LJhoel ChoqueОценок пока нет
- Litosfera - Wikipedia, La Enciclopedia LibreДокумент2 страницыLitosfera - Wikipedia, La Enciclopedia LibreDeyОценок пока нет
- Informe Lab Quimica CalorimetriaДокумент11 страницInforme Lab Quimica CalorimetriaRocio Andrea Casilla100% (1)
- Revista SPIAДокумент32 страницыRevista SPIAChristian J. McLeanОценок пока нет
- LAS VINAZAS Nota Tecnica Manejo de Vinaz PDFДокумент38 страницLAS VINAZAS Nota Tecnica Manejo de Vinaz PDFFlor Lisbet Bustamante SalazarОценок пока нет