Академический Документы
Профессиональный Документы
Культура Документы
Efect Odel A Temperatura
Загружено:
Jorge Luis OlivarОригинальное название
Авторское право
Доступные форматы
Поделиться этим документом
Поделиться или встроить документ
Этот документ был вам полезен?
Это неприемлемый материал?
Пожаловаться на этот документАвторское право:
Доступные форматы
Efect Odel A Temperatura
Загружено:
Jorge Luis OlivarАвторское право:
Доступные форматы
INSTITUTO
POLITCNICO
NACIONAL
ESCUELA NACIONAL
DE CIENCIAS BIOLGICAS
QUMICO BACTERILO
PARASITLOGO
4QM2 SECCIN: 1
FRANCO HERNANDEZ ERIKA JAYET
OLIVAR VILLEGAS JORGE LUIS
PRCTICA 5.4 EFECTO DE LA
TEMPERATURA
Introduccin.
Al aumentar la temperatura,
aumenta la energa cintica de las
molculas reaccionantes, y por
consiguiente es mayor la
probabilidad de que ocurran
colisiones efectivas para que la
reaccin se lleve a cabo. Como las
reacciones enzimticas no son una
excepcin a esta regla, su velocidad
aumenta con la temperatura. Pero
cuando la temperatura llega a cierto
valor, variable segn la enzima de
que se trate, sta empieza a
desnaturalizarse y la velocidad de la
reaccin comienza a disminuir. Se
habla as de una temperatura
ptima, que es aquella en la que la
velocidad de la reaccin es mayor.
La energa de activacin, Ea, para
las reacciones catalizadas por
enzimas es inferior a la de las
reacciones no catalizadas, ya que
las enzimas actan disminuyendo la
barrera energtica que hay que
sobrepasar para que la reaccin
pueda tener lugar. Determinando la
actividad enzimtica a diferentes
temperaturas es posible calcular el
coeficiente Q10, que indica cuntas
veces se incrementa la velocidad
por cada aumento de la
temperatura en 10C. Para las
reacciones qumicas se acepta que
Q10 debe valer 2, en las reacciones
enzimticas suele ser menor de 2,
ya que son menos sensibles a los
cambios de temperatura.
Resultados.
1
0.05
6
1.3
Abs.
2
0.08
1
1.5
3
0.76
7
9.8
4
0.65
5
8.5
5
0.41
9
5.6
6
0.00
6
0.3
A.R.
(mole
s)
Vo(UI)
0.13
0.15
0.98
0.85
0.56
0.03
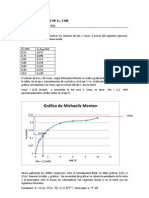
Fig.1 Tabla de resultados de las abosorbancias de
los tubos problema, su concentracin de azcares
reductores y velocidad de reaccin.
T
(C)
0
25
37
55
74
92
Vo
0.13
0.15
0.98
0.85
0.56
0.03
ln(Vo
)
1.897
1
1.771
9
0.020
0.083
1.203
9
-2.30
T(K)
1/T(K)
293.1
5
3.41 x10-
298.1
5
3.35 x10-
310.1
5
308.1
5
303.1
5
3.22 x10-
273.1
5
3.66x10-3
3.24 x103
3.29 x103
Fig.2 Tabla de velocidades de reaccin a
diferentes temperaturas.
Discusin.
En una reaccin qumica , la
velocidad de reaccin catalizada
por una enzima aumenta al
incrementarse la temperatura ,
al ubicar los resultados
obtenidos de velocidad y
temperatura en una grfica ,al
realizar una seria de tubos donde
el sustrato , la concentracin de
enzimas y el pH se mantenan
constantes variando solo as la
temperatura en cada tubo se
observa que la temperatura
influye directamente sobre la
velocidad de reaccin,
aumentndola hasta llegar a una
temperatura mxima donde la
actividad de la enzima es
mayor , efectiva y optima al
encontrarse en las condiciones
favorables , sin embargo ,
despus de esta temperatura la
velocidad de reaccin empieza a
disminuir y a temperaturas
mayores la actividad de la
enzima es casi nula , debido a la
inactivacin generalmente por
desnaturalizacin de la enzima .
( ver grafica 1 )
Al graficar los valores del
logaritmo natural de la velocidad
con los del inverso de la
temperatura, obtuvimos la
pendiente de la recta teniendo
un valor de -1.150, misma que
nos ayud a calcular la energa
de activacin, que result ser de
2.2850
L atm
mol K
grfica)
Conclusiones.
(Clculos en la
La temperatura es un factor
fsico que influye sobre la
velocidad de una reaccin
enzimtica, dependiendo de la
enzima, se tendr una velocidad
mxima, que es en la que las
colisiones efectivas sern
mayores. Pasando esta
temperatura, al ser una enzima
proteica, se comienza a
desnaturalizar, disminuyendo la
velocidad de la reaccin. En una
reaccin en la que interviene una
enzima, la energa de activacin
disminuye, pues su efecto de
catalizador minimiza la energa
que necesita la reaccin para
llevarse a cabo.
Bibliografa.
Pea. Et al. Bioqumica. Limusa,
2da ed. Mxico 2004. Pp 201.
Gutias, Mara Elena. Influencia
de la temperatura y de la
humedad en la dinmica de la
materia orgnica de los suelos
de Galcia y su relacin con el
cambio climtico. Universidad de
Santiago de Compostella. Pp 56,
57.
Pregunta extra:
Qu es energa de
activacin?
La Energa de activacin en
qumica y biologa es la energa
que necesita un sistema antes
de poder iniciar un determinado
proceso. La energa de activacin
suele utilizarse para denominar
la energa mnima necesaria para
que se produzca una reaccin
qumica dada. Para que ocurra
una reaccin entre dos
molculas, stas deben
colisionar en la orientacin
correcta y poseer una cantidad
de energa mnima. A medida
que las molculas se aproximan,
sus nubes de electrones se
repelen. Esto requiere energa
(energa de activacin) y
proviene del calor del sistema,
es decir de la energa
traslacional, vibracional, etctera
de cada molcula.
Вам также может понравиться
- Mod3 Estrategias de Seguridad ClinicaДокумент48 страницMod3 Estrategias de Seguridad ClinicaJorge Luis OlivarОценок пока нет
- Mod4 Asistencia Inicial Al Paciente CriticoДокумент23 страницыMod4 Asistencia Inicial Al Paciente CriticoJorge Luis OlivarОценок пока нет
- Inocuidad y BPM BiotekaxДокумент37 страницInocuidad y BPM BiotekaxJorge Luis OlivarОценок пока нет
- Tema 1 PDFДокумент49 страницTema 1 PDFJorge Luis OlivarОценок пока нет
- Electroforesis de Proteínas Ya AnДокумент25 страницElectroforesis de Proteínas Ya AnJorge Luis OlivarОценок пока нет
- Mod1 La Simulacion Clinica Metodologia Docente InnovadoraДокумент33 страницыMod1 La Simulacion Clinica Metodologia Docente InnovadoraJorge Luis OlivarОценок пока нет
- 2-RCP Basica y Avanzada PDFДокумент76 страниц2-RCP Basica y Avanzada PDFAngel Benavides LopezОценок пока нет
- Practica 3 Succinato DeshidrogenasaДокумент9 страницPractica 3 Succinato DeshidrogenasaReiina GarciiaОценок пока нет
- Telefonia Movil y Telefonia Fija (Codigos Secretos)Документ92 страницыTelefonia Movil y Telefonia Fija (Codigos Secretos)Remigio Rabel Huamani40% (5)
- P13 Biodegradacion de SurfactantesДокумент5 страницP13 Biodegradacion de SurfactantesJorge Luis OlivarОценок пока нет
- PROBLEMAS ENZIMÁTICOSДокумент5 страницPROBLEMAS ENZIMÁTICOSJulio Cesar Castañeda Mancipe80% (5)
- Sistemas-Mecanismos Biológicos de Control HomeostáticosДокумент8 страницSistemas-Mecanismos Biológicos de Control HomeostáticosJorge Luis OlivarОценок пока нет
- Tutorial Calculos de KM y VmaxДокумент3 страницыTutorial Calculos de KM y VmaxFrancisca Fuentes100% (1)
- Tema 2 PDFДокумент58 страницTema 2 PDFJorge Luis OlivarОценок пока нет
- Preguntas Resuletas InmunologiaДокумент26 страницPreguntas Resuletas InmunologiaJorge Luis Olivar100% (1)
- Electroforesis de Proteínas Ya AnДокумент25 страницElectroforesis de Proteínas Ya AnJorge Luis OlivarОценок пока нет
- DiscusiónДокумент2 страницыDiscusiónJorge Luis OlivarОценок пока нет
- MicorrizacionДокумент12 страницMicorrizacionJorge Luis OlivarОценок пока нет
- Bases Moleculares de La Señalización NeuronalДокумент20 страницBases Moleculares de La Señalización NeuronalKatia Diaz BenitesОценок пока нет
- Examen Corregidos de MicrobiologiaДокумент72 страницыExamen Corregidos de MicrobiologiaJailer Vega58% (12)
- La Biodiversidad de Los Hongos Ectomicorrízicos y SuimportanciaДокумент17 страницLa Biodiversidad de Los Hongos Ectomicorrízicos y SuimportanciaJorge Luis OlivarОценок пока нет
- Preguntas Resuletas InmunologiaДокумент26 страницPreguntas Resuletas InmunologiaJorge Luis Olivar100% (1)
- Examencito P16 SuelosДокумент1 страницаExamencito P16 SuelosJorge Luis OlivarОценок пока нет
- Fermentacion DiscusionДокумент5 страницFermentacion DiscusionJorge Luis Olivar100% (2)
- Ensayos inmunológicos (39Документ18 страницEnsayos inmunológicos (39Jorge Luis Olivar100% (1)
- Hill DiscusionДокумент2 страницыHill DiscusionJorge Luis OlivarОценок пока нет
- Vol 29-Num 1-291073Документ9 страницVol 29-Num 1-291073Jorge Luis OlivarОценок пока нет
- Ecologia Molecular de Hongos Ectomicorr PDFДокумент12 страницEcologia Molecular de Hongos Ectomicorr PDFJorge Luis OlivarОценок пока нет
- Menisco 2Документ2 страницыMenisco 2Jorge Luis OlivarОценок пока нет
- Dis CushionДокумент2 страницыDis CushionJorge Luis OlivarОценок пока нет
- Corrección Del Factor de Potencia - Lab Circuitos2Документ17 страницCorrección Del Factor de Potencia - Lab Circuitos2Alexisluigi Collahua PadillaОценок пока нет
- Aprovechamiento de Energia de Un Motor Magnético BediniДокумент15 страницAprovechamiento de Energia de Un Motor Magnético Bedinioscar canchariОценок пока нет
- Expo Motores 2 T 4 TДокумент19 страницExpo Motores 2 T 4 Temolbe132Оценок пока нет
- Rectificador de Onda CompletaДокумент4 страницыRectificador de Onda CompletaJosé Luis SonccoОценок пока нет
- Sistema de Ventilacion de Un Buque TanqueДокумент128 страницSistema de Ventilacion de Un Buque TanqueMihuler Yordy Romero Rojas0% (1)
- Guía 6 - Trabajo y EnergiaДокумент2 страницыGuía 6 - Trabajo y EnergiaBastian Vargas ZúñigaОценок пока нет
- Proteccion 1 5Документ5 страницProteccion 1 5MARIA LUISA CALLE GUARDAPUCLLAОценок пока нет
- Guía de Ejercicios CondensadoresДокумент2 страницыGuía de Ejercicios Condensadorescanchicaalbert5Оценок пока нет
- La energía: definición, fuentes y tiposДокумент25 страницLa energía: definición, fuentes y tiposcarolina del Pilar Valdiviezo CoveñasОценок пока нет
- Silabus Fisica IДокумент6 страницSilabus Fisica IYhomn AcerОценок пока нет
- Mecanica I PDFДокумент12 страницMecanica I PDFnoelcohenОценок пока нет
- Proyecto de Inves.Документ28 страницProyecto de Inves.dayiro lara gallardoОценок пока нет
- Resumen de Visita Se SachicaДокумент5 страницResumen de Visita Se SachicaAndrés Enrique Canchano ReyesОценок пока нет
- Formulario Maquinas Eléctricas 1Документ2 страницыFormulario Maquinas Eléctricas 1Daniel Lastra Encabo100% (1)
- Guia Producto MT 2021 Mas UtilizadoДокумент14 страницGuia Producto MT 2021 Mas UtilizadoFerran MunyósОценок пока нет
- Informe Final Chilca UnoДокумент184 страницыInforme Final Chilca UnoRolando Henry Flores CamavilcaОценок пока нет
- Optimización energética cadenas logísticas transporte carga pesada EcuadorДокумент7 страницOptimización energética cadenas logísticas transporte carga pesada EcuadorJhordan ErraezОценок пока нет
- PreciosДокумент11 страницPreciosCesar SierraОценок пока нет
- Control y alimentación de breakers CB1 y CB2 del IDMДокумент7 страницControl y alimentación de breakers CB1 y CB2 del IDMJohn SuarezОценок пока нет
- Guia de Estudio Del Parcial de Quimica I Cuarto SemestreДокумент3 страницыGuia de Estudio Del Parcial de Quimica I Cuarto SemestreAdrian BcОценок пока нет
- Trane Manual Stylus NuevoДокумент36 страницTrane Manual Stylus NuevoRafael MoralesОценок пока нет
- El Manuscrito de Magdalena Magia SexualДокумент51 страницаEl Manuscrito de Magdalena Magia SexualLaura Nardi100% (8)
- AUDITORIA Energetica PDFДокумент4 страницыAUDITORIA Energetica PDFJames García PuellesОценок пока нет
- Pregunta 1 Del A Al DДокумент6 страницPregunta 1 Del A Al Dorlando salas orihuelaОценок пока нет
- Carga y DescargaДокумент11 страницCarga y DescargaLuisa Fernanda Giraldo LopezОценок пока нет
- CyT 2° - SESIÓN 17 DE OCTUBREДокумент6 страницCyT 2° - SESIÓN 17 DE OCTUBREJohn Wilson Condori CpndoriОценок пока нет
- New Me Card 8.0Документ22 страницыNew Me Card 8.0NinnaОценок пока нет
- Señales y Sistemas.Документ15 страницSeñales y Sistemas.Ariel GálvezОценок пока нет
- Qué Es La Energía LimpiaДокумент4 страницыQué Es La Energía LimpiaEsther CarrilloОценок пока нет
- Historia Arquitectura AmbientalДокумент2 страницыHistoria Arquitectura AmbientalDiego Alejandro Espinoza GarciaОценок пока нет