Академический Документы
Профессиональный Документы
Культура Документы
Quimicahojadetrabajo13 PDF
Загружено:
Neftaly Gabriel Escobar Romero0%(1)0% нашли этот документ полезным (1 голос)
39 просмотров2 страницыes un buen material de apoyo
Оригинальное название
Quimicahojadetrabajo13.pdf
Авторское право
© © All Rights Reserved
Доступные форматы
PDF, TXT или читайте онлайн в Scribd
Поделиться этим документом
Поделиться или встроить документ
Этот документ был вам полезен?
Это неприемлемый материал?
Пожаловаться на этот документes un buen material de apoyo
Авторское право:
© All Rights Reserved
Доступные форматы
Скачайте в формате PDF, TXT или читайте онлайн в Scribd
0%(1)0% нашли этот документ полезным (1 голос)
39 просмотров2 страницыQuimicahojadetrabajo13 PDF
Загружено:
Neftaly Gabriel Escobar Romeroes un buen material de apoyo
Авторское право:
© All Rights Reserved
Доступные форматы
Скачайте в формате PDF, TXT или читайте онлайн в Scribd
Вы находитесь на странице: 1из 2
UNIVERSIDAD DE SAN CARLOS DE GUATEMALA
CENTRO UNIVERSITARIO DE OCCIDENTE
DIVISIN DE CIENCIAS DE LA SALUD
PRIMER AO
AREA DE QUIMICA
QUIMICA 1
INGA. EDITH REYES
ING. PABLO DAVID ESTRADA
ING. SERGIO DURINI
Hoja de Trabajo
Semana 13
Entrega esta hoja resuelta en la prxima
sesin de clases
PROPIEDADES COLIGATIVAS DE SOLUCIONES
En qumica se llaman propiedades coligativas a aquellas propiedades de una disolucin
que dependen nicamente de la concentracin. Generalmente expresada como
concentracin equivalente, es decir, de la cantidad de partculas de soluto por partculas
totales, y no de la composicin qumica del soluto.
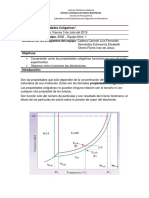
Estn estrechamente relacionadas con la presin de vapor, que es la presin que ejerce la
fase de vapor sobre la fase lquida, cuando el lquido se encuentra en un recipiente
cerrado. La presin de vapor depende del solvente y de la temperatura a la cual sea
medida (a mayor temperatura, mayor presin de vapor). Se mide cuando el sistema llega
al equilibrio dinmico, es decir, cuando la cantidad de molculas de vapor que vuelven a la
fase lquida es igual a las molculas que se transforman en vapor.
Propiedades Coligativas ms comunes de la qumica
Descenso de la presin de vapor Artculo principal: Aumento ebulloscpico.
Cuando se prepara una solucin con un solvente voltil y un soluto no voltil (que no se
transformar en vapor) y se mide su presin de vapor, al compararla con la presin de
vapor de su solvente puro (medidas a la misma temperatura y presin atmosfrica), se
observa que la solucin es menor que la del solvente. Esto es consecuencia de la
presencia del soluto no voltil.El fenmeno observable es un aumento del punto de
ebullicin de la disolucin.
Presin osmtica:
La presin osmtica puede definirse como la presin que se debe aplicar a una solucin
para detener el flujo neto de disolvente a travs de una membrana semipermeable.[1] La
presin osmtica es una de las cuatro propiedades coligativas de las soluciones
(dependen del nmero de partculas en disolucin, sin importar su naturaleza). Se trata de
una de las caractersticas principales a tener en cuenta en las relaciones de los lquidos
que constituyen el medio interno de los seres vivos, ya que la membrana plasmtica regula
la entrada y salida de soluto al medio extracelular que la rodea, ejerciendo de barrera de
control.
Cuando dos soluciones se ponen en contacto a travs de una membrana semipermeable
(membrana que deja pasar las molculas de disolvente pero no las de los solutos), las
molculas de disolvente se difunden, pasando habitualmente desde la solucin con menor
concentracin de solutos a la de mayor concentracin. Este fenmeno recibe el nombre de
smosis, palabra que deriva del griego osmos, que significa "impulso".[2] Al suceder la
smosis, se crea una diferencia de presin en ambos lados de la membrana
semipermeable: la presin osmtica.
Coloide:
El nombre de coloide proviene de la raz griega colaire que significa que puede pegarse.
Este nombre que hace referencia a una de las principales propiedades de los coloides: su
tendencia espontnea a agregar o formar cogulos.
Los coloides tambin afectan el punto de ebullicin del agua y son contaminantes.
Los coloides se diferencian de las suspensiones qumicas, principalmente en el tamao de
las partculas de la parte dispersa.
En algunos casos las partculas son molculas muy grandes como protenas. En la fase
acuosa, una molcula se pliega de tal manera que su parte hidroflica se encuentra en el
exterior, es decir la parte que puede formar interacciones con molculas de agua a travs
de fuerzas in-dipolo o fuerzas puente de hidrgeno se mueven a la parte externa de la
molcula.
Dilisis:
La dilisis (del griego dialusis, significando disolucin, da, significa a travs, y lysis,
separacin) es un proceso mediante el cual se extraen las toxinas y el exceso de agua de
la sangre, normalmente como terapia renal sustitutiva tras la prdida de la funcin renal en
personas con fallo renal. La dilisis puede usarse para aquellos con un trastorno agudo de
la funcin renal (insuficiencia renal aguda) o progresiva pero empeorando crnicamente la
funcin renal - un estado conocido como enfermedad renal crnica en etapa 5 (antes
conocida como insuficiencia renal crnica).
PARTE TEORICA:
Instrucciones: Describe las siguientes definiciones
Membrana semipermeable Osmosis
Dispersiones coloidales
Efecto Tyndall
Emulsin
Dilisis
Osmosis
Solucin isotnica
Dispersiones coloidales
SEGUNDA SERIE:
1. Un compuesto qumico ha sintetizado un compuesto amarillo verdoso de cloro y
oxgeno y encuentra que su densidad es de 7.71 g/ litro a 36 grados centgrados y
2.88 atmosferas. Calcule la masa molar del compuesto. R. 67.9 g/mol
2. Calcular la densidad del dixido de carbono en gramos por litro a 0.99 atmosferas y
55 C. R. 1.6 g/L
3. Una disolucin acuosa diluida de un compuesto orgnico soluble en agua se forma
disolviendo 2.35g del compuesto en agua para formar 0.250L de disolucin. La
disolucin as preparada tiene una presin osmtica de 0.605atm a 25 C.
Asumiendo que el compuesto orgnico es no electrolito, Cul es su masa molar?
R. 1.75*104 g/mol
4. Una disolucin de 6.85 g de un carbohidrato en 100 g. de agua tiene una densidad
de 1.024 g/mL y una presin Osmtica de 4.61 atm a 20 C. Calcule la masa molar
del carbohidrato. R. 343 g/mol (Resolver el mismo problema con 300 torr)
5. Qu sera ms eficaz como anticongelante al agregarse a un radiador, 5
kilogramos de etanol C2H5OH o 5 kilogramos de metanol, CH3OH?
6. Cul es la presin osmtica formada por la disolucin de 44.2mg de aspirina
(C9H8O4) en 0.358L de agua a 25C?
Вам также может понравиться
- Desintoxicacion Con Sal - Basado En Las Enseñanzas De Frank Suarez: Limpiando Tu OrganismoОт EverandDesintoxicacion Con Sal - Basado En Las Enseñanzas De Frank Suarez: Limpiando Tu OrganismoОценок пока нет
- Propiedades ColigativasДокумент4 страницыPropiedades ColigativasNicole RomanОценок пока нет
- Propiedades ColigativasДокумент4 страницыPropiedades ColigativasReymundo SeguraОценок пока нет
- Actividad Propiedades ColigativasДокумент11 страницActividad Propiedades ColigativasMemo GranadosОценок пока нет
- Propiedades ColigativasДокумент9 страницPropiedades ColigativasAlex LozadaОценок пока нет
- Propiedades ColigativasДокумент9 страницPropiedades Coligativasluis albertoОценок пока нет
- PROPIEDADES COLIGATIVAS DE LAS SOLUCIONES Y DE LOS COLOIDES NirleyДокумент9 страницPROPIEDADES COLIGATIVAS DE LAS SOLUCIONES Y DE LOS COLOIDES NirleyKathy JaimesОценок пока нет
- Cuestionario de BiofisicaДокумент17 страницCuestionario de BiofisicaMarina ValenzuelaОценок пока нет
- Propiedades Coligativas, Osmosis, Dialisis y ColoidesДокумент9 страницPropiedades Coligativas, Osmosis, Dialisis y ColoideskimberlyОценок пока нет
- Soluciones ColigativasДокумент19 страницSoluciones ColigativasmadefernanОценок пока нет
- 6 - Propiedades Coligativas de Las SolucionesДокумент7 страниц6 - Propiedades Coligativas de Las SolucionesLautaro CastilloОценок пока нет
- Informe 7 - Propiedades ColigativasДокумент12 страницInforme 7 - Propiedades ColigativasAlex Ostos AlvaОценок пока нет
- Leonardo. ElectrolitosДокумент11 страницLeonardo. ElectrolitosJHON JAIRO REYESОценок пока нет
- Propiedades Coligativas de Soluciones No ElectoliticasДокумент26 страницPropiedades Coligativas de Soluciones No ElectoliticasYris EchezuriaОценок пока нет
- Clase 8 Soluciones - Propiedades - Unidades de ConcentracionДокумент10 страницClase 8 Soluciones - Propiedades - Unidades de ConcentracionFabricio Joel Camacho GarabitoОценок пока нет
- POSTLAB 1 (Difusion, Osmosis y Dialisis)Документ7 страницPOSTLAB 1 (Difusion, Osmosis y Dialisis)Rodro Marro100% (1)
- Masa Molar Aplicando Propiedades FINALДокумент23 страницыMasa Molar Aplicando Propiedades FINALGerardo RecioОценок пока нет
- Osmosis y Disoluciones Isotónicas Química II FinalДокумент3 страницыOsmosis y Disoluciones Isotónicas Química II FinalAndrea UribeОценок пока нет
- Propiedad ColigativaДокумент5 страницPropiedad ColigativamaxОценок пока нет
- 2 Informe SolubilidadДокумент23 страницы2 Informe Solubilidadgianmb182150% (4)
- Osmosis y HemodialisisДокумент50 страницOsmosis y HemodialisisWal RamosОценок пока нет
- Importancia de Las Propiedades ColigativasДокумент4 страницыImportancia de Las Propiedades ColigativasJavier Giménez100% (1)
- Propiedades Coligativas Del AguaДокумент6 страницPropiedades Coligativas Del AguaIzhmyy Dje100% (1)
- Pregunta 2 FQДокумент5 страницPregunta 2 FQMilade CantilloОценок пока нет
- Importancia de Las SolucionesДокумент50 страницImportancia de Las SolucionesJorge Manuel Atarama Vera67% (6)
- 8-AS-QUIM-Udproco-REC. - DE - QUIMICA - 8-RECUPERACION DEL TERCER PERIODO-2098722144-1649739377 (1) DILAN BECERRAДокумент9 страниц8-AS-QUIM-Udproco-REC. - DE - QUIMICA - 8-RECUPERACION DEL TERCER PERIODO-2098722144-1649739377 (1) DILAN BECERRAAntonio UstarizОценок пока нет
- Soluciones en El Cuerpo HumanoДокумент27 страницSoluciones en El Cuerpo HumanoGiancarlo David Viviano Reyes0% (3)
- Practica 8 Propiedades ColigativasДокумент5 страницPractica 8 Propiedades ColigativasBlackPork54Оценок пока нет
- Conceptos de Físico QuimicaДокумент52 страницыConceptos de Físico QuimicaPerafan Garcia HildaОценок пока нет
- 2 Informe SolubilidadДокумент23 страницы2 Informe SolubilidadIliana DelMoral100% (1)
- Propiedades ColigativasДокумент14 страницPropiedades ColigativasSergio Luis Fernández SalinasОценок пока нет
- Propiedades ColigativasДокумент12 страницPropiedades ColigativaslosmisteriosdemovilleОценок пока нет
- Propiedades Coligativas Sol. RODOLFOДокумент10 страницPropiedades Coligativas Sol. RODOLFOrodolfoОценок пока нет
- Investigacion 3 Operaciones Unitarias de CristalizacionДокумент4 страницыInvestigacion 3 Operaciones Unitarias de CristalizacionLuisa DoraОценок пока нет
- Citofisica 2019Документ14 страницCitofisica 2019Gary LopezОценок пока нет
- INFORMES DEL LABORATORIO QUIMICA GENERAL RubenДокумент5 страницINFORMES DEL LABORATORIO QUIMICA GENERAL RubenLynBCОценок пока нет
- Propiedades ColigativasДокумент5 страницPropiedades ColigativasYoseleyn SuarezОценок пока нет
- Soluiones y DisolucionesДокумент31 страницаSoluiones y DisolucionesWiliam AcharteОценок пока нет
- Laboratorio de Química General Nro 6Документ14 страницLaboratorio de Química General Nro 6Jhon Humerez PairumaniОценок пока нет
- Liquidos y Soluciones Ideales y RealesДокумент17 страницLiquidos y Soluciones Ideales y RealesMONSALVE RODRIGUEZ JHON ANTHONYОценок пока нет
- Teoria Biofisica y FisiologicaДокумент144 страницыTeoria Biofisica y FisiologicaShirley AntezanaОценок пока нет
- Propiedades Coligativas AguaДокумент3 страницыPropiedades Coligativas Aguacarlosventosa86% (7)
- Mezclas, Sustancias, ElementosДокумент24 страницыMezclas, Sustancias, ElementosCleivismar QueroОценок пока нет
- Cap 6Документ4 страницыCap 6Miguel LópezОценок пока нет
- 10 Osmosis y DialisisДокумент52 страницы10 Osmosis y DialisisAbigailОценок пока нет
- Generalidades Del AguaДокумент21 страницаGeneralidades Del Aguarock2312Оценок пока нет
- Disolución AcuosaДокумент4 страницыDisolución AcuosaJose Rosero0% (1)
- Clases de Quimica Conclusiones IntroДокумент9 страницClases de Quimica Conclusiones IntroRosendo PatoniОценок пока нет
- Disoluciones en Química Parte 2Документ7 страницDisoluciones en Química Parte 2Sofía Luna DelgadilloОценок пока нет
- Intro Ducci OnДокумент10 страницIntro Ducci Onreal_bertОценок пока нет
- Propiedades ColigativasДокумент6 страницPropiedades ColigativasFabio Ortega WeberОценок пока нет
- Práctica 4 Solubilidad y MezclasДокумент8 страницPráctica 4 Solubilidad y Mezclasesluse93Оценок пока нет
- Resumen Segundo ParcialДокумент16 страницResumen Segundo ParcialAilén RestanoОценок пока нет
- Informe de Lectura Capítulo 12Документ4 страницыInforme de Lectura Capítulo 12Raylin Ismael MordanОценок пока нет
- Nº1 Dispersiones y Propiedades ColigativasДокумент5 страницNº1 Dispersiones y Propiedades ColigativasMartin CitoОценок пока нет
- 13.-Propiedades ColigativasДокумент3 страницы13.-Propiedades ColigativasgigigelpОценок пока нет
- Importancia de Las SolucionesДокумент15 страницImportancia de Las SolucionesIzueJanОценок пока нет
- Presión OsmóticaДокумент5 страницPresión OsmóticaMichelle MarianaОценок пока нет
- Bupropion Informe CompletoДокумент24 страницыBupropion Informe CompletoNeftaly Gabriel Escobar RomeroОценок пока нет
- PE Zentel 400 MGДокумент10 страницPE Zentel 400 MGNeftaly Gabriel Escobar RomeroОценок пока нет
- Características Histológicas de Una Mucosa en GeneralДокумент5 страницCaracterísticas Histológicas de Una Mucosa en GeneralNeftaly Gabriel Escobar RomeroОценок пока нет
- Clasificacion de Soplos Cardiacos.Документ3 страницыClasificacion de Soplos Cardiacos.Neftaly Gabriel Escobar RomeroОценок пока нет
- Modelo Presentación Trabajo de InvestigaciónДокумент6 страницModelo Presentación Trabajo de InvestigaciónNeftaly Gabriel Escobar RomeroОценок пока нет
- Definición de Climaterio y MenopausiaДокумент2 страницыDefinición de Climaterio y MenopausiaNeftaly Gabriel Escobar RomeroОценок пока нет
- 23 Remedios Caseros para Eliminar El AcneДокумент3 страницы23 Remedios Caseros para Eliminar El AcneBrayeОценок пока нет
- AforismosДокумент10 страницAforismosNeftaly Gabriel Escobar RomeroОценок пока нет
- György LukácsДокумент15 страницGyörgy LukácsValeria MontañoОценок пока нет
- Diagnóstico y Tratamiento de La Diabetes en El EmbarazoДокумент18 страницDiagnóstico y Tratamiento de La Diabetes en El EmbarazoJaime Uziel Mendez GomezОценок пока нет
- Articulo de Rectificacion de ValvulasДокумент7 страницArticulo de Rectificacion de ValvulasJose LuisОценок пока нет
- 1 Cos Pat 3Документ9 страниц1 Cos Pat 3Libros De Ciencia y TecnologiaОценок пока нет
- 59 Casos Practicos Educacion Primaria (257 Paginas)Документ257 страниц59 Casos Practicos Educacion Primaria (257 Paginas)Lucia Bermejo100% (1)
- Actividad # 6 (Ética y Empresa)Документ8 страницActividad # 6 (Ética y Empresa)Mauren AlejandraОценок пока нет
- Informe de Gestión Cualitativo y Cuantitativoformato12102020Документ6 страницInforme de Gestión Cualitativo y Cuantitativoformato12102020yeximarОценок пока нет
- CPMS-CPT HomologaciònДокумент280 страницCPMS-CPT HomologaciònClaudioOrdoñezОценок пока нет
- Sujetos Procesales Sistema Acusatorio AdversarialДокумент12 страницSujetos Procesales Sistema Acusatorio AdversarialJosé Luis Candela100% (1)
- Tesis Mercadeo, Frank Gomez - Lulibet Dostal-1Документ100 страницTesis Mercadeo, Frank Gomez - Lulibet Dostal-1Gereliz Arias100% (1)
- Rocol Agrolube Ultra 2 - PPДокумент9 страницRocol Agrolube Ultra 2 - PPRoberto Alfaro EspinozaОценок пока нет
- Amplificadores Operacionales PDFДокумент5 страницAmplificadores Operacionales PDFDaniel SolisОценок пока нет
- Conceptos PiagetianosДокумент10 страницConceptos PiagetianosYannina Chumioque PisfilОценок пока нет
- Circuito de Control de Potencia Con SCR o TriacДокумент3 страницыCircuito de Control de Potencia Con SCR o TriacAnonymous ZMwWk2vОценок пока нет
- 2220 26603565 20200211180751Документ1 страница2220 26603565 20200211180751RennyОценок пока нет
- 1964 Vida - Con - El - LamaДокумент215 страниц1964 Vida - Con - El - LamaKathia D KostlichОценок пока нет
- 15-Salud-Preescolar-Padres de FamiliaДокумент5 страниц15-Salud-Preescolar-Padres de FamiliaJany ArteagaОценок пока нет
- Caso Practico de La Unidad 1Документ2 страницыCaso Practico de La Unidad 1Jaki GiraldoОценок пока нет
- Monografia SociolllДокумент19 страницMonografia SociolllMarko CCОценок пока нет
- CefalosporinasДокумент92 страницыCefalosporinasRosa Pilar Mamani HilasacaОценок пока нет
- Ejercicio en Limpio Liquidación de Gananciales CecyДокумент10 страницEjercicio en Limpio Liquidación de Gananciales CecyCecy De Las Mercedes Millán FernándezОценок пока нет
- Formato EvaluacionДокумент2 страницыFormato EvaluacionPepeito PerezОценок пока нет
- Plan de VidaДокумент3 страницыPlan de VidaCristian José Villalobos100% (1)
- Copia de GEOLOGIA LINCE - ESTEFANIA - OTROSДокумент36 страницCopia de GEOLOGIA LINCE - ESTEFANIA - OTROSmauricio velizОценок пока нет
- Redaccion de Documentos (Electiva)Документ4 страницыRedaccion de Documentos (Electiva)Ayaris MosquedaОценок пока нет
- Programa Doulas DefinitivoДокумент26 страницPrograma Doulas DefinitivoTuty García MorodoОценок пока нет
- Ángel Palerm Historia de La Etnologia-Tylor y Los Profesionales Britanicos Lectura 1Документ33 страницыÁngel Palerm Historia de La Etnologia-Tylor y Los Profesionales Britanicos Lectura 1marherreyОценок пока нет
- Nahuas TexcocoДокумент58 страницNahuas TexcocoBeto EscalanteОценок пока нет
- 2023CV JavieraAlaideElizabethHerreraPedrozaДокумент5 страниц2023CV JavieraAlaideElizabethHerreraPedrozaCatherine Cordón AlfaroОценок пока нет
- Salud y Seguridad en ObraДокумент16 страницSalud y Seguridad en ObraMV SCОценок пока нет