Академический Документы
Профессиональный Документы
Культура Документы
Insuficiencia Cardiaca 1
Загружено:
Cindy Berrocal ValenzuelaОригинальное название
Авторское право
Доступные форматы
Поделиться этим документом
Поделиться или встроить документ
Этот документ был вам полезен?
Это неприемлемый материал?
Пожаловаться на этот документАвторское право:
Доступные форматы
Insuficiencia Cardiaca 1
Загружено:
Cindy Berrocal ValenzuelaАвторское право:
Доступные форматы
01 Actualizacin 2279-90 14/6/05 17:15 Pgina 2279
Documento descargado de http://www.doyma.es el 14/08/2007. Copia para uso personal, se prohbe la transmisin de este documento por cualquier medio o formato.
ACTUALIZACIN
Insuficiencia
cardaca: concepto,
epidemiologa,
clasificacin,
etiologa y
fisiopatologa
G. Aldama Lpez, M. Pieiro Portela,
R. Campo Prez y P. Pin Esteban
Servicio de Cardiologa. rea del Corazn.
Complejo Hospitalario Universitario Juan Canalejo.
La Corua. Espaa.
Concepto de insuficiencia cardaca
A lo largo del siglo XX se ha producido un enorme avance en
la comprensin y el conocimiento de la fisiopatologa y los
mecanismos compensadores que se ponen en marcha cuando un paciente desarrolla insuficiencia cardaca (IC). Fruto
de esa evolucin, la definicin de este cuadro tambin ha sufrido modificaciones, cambiando los modelos que lo explicaban conforme se iban incorporando los nuevos conceptos.
En los aos 50, la IC era un cuadro congestivo, con retencin hdrica secundaria al fallo cardaco y el modelo que lo
explicaba era el cardiorrenal. En los 70, la monitorizacin de
estos pacientes llev a explicar el cuadro como un problema
de presiones, volmenes y resistencias. Surgi entonces el
modelo hemodinmico, que supuso tambin cambios en los
fundamentos y aplicaciones teraputicas. A principios de
los aos noventa, el descubrimiento de la participacin del
sistema nervioso autnomo y la activacin secundaria de varios sistemas endocrinos como fenmenos compensatorios
en la IC llev a idear un modelo neurohormonal. Este modelo se ha mantenido en los ltimos 10 aos. Sin embargo, las
nuevas tecnologas han permitido adentrarse en el interior
de las clulas, conocemos ms mecanismos celulares que participan en la disfuncin ventricular y hemos desarrollado
herramientas teraputicas para modificarlos. Estamos evolucionando hacia un modelo biomolecular tremendamente pro11
PUNTOS CLAVE
Concepto. La insuficiencia cardaca (IC) es un tipo
de insuficiencia circulatoria. El diagnstico de IC
es sindrmico y se debe buscar siempre
el diagnstico etiolgico.
Epidemiologa. Tanto la prevalencia como
la incidencia de IC aumentan conforme lo hace la
edad. Ambas se sitan en torno al 1% para
personas mayores de 40 y 65 aos
respectivamente Las mujeres con IC son,
respecto a los hombres, ms ancianas, ms
sintomticas, ms diabticas y ms hipertensas
La prevalencia e incidencia de IC en mujeres
y hombres es igual, pero ellas sobreviven ms
La IC es la primera causa de ingreso
hospitalario en pacientes mayores de 65 aos
La mortalidad ha decrecido en los ltimos
50 aos, es mayor para los hombres y globalmente
hablando se cifra en el 50% a los 5 aos
La IC representa entre el 2% y el 5% del
presupuesto sanitario de los pases
industrializados.
Clasificacin. La IC puede ser diastlica
o sistlica, izquierda o derecha, de alto o bajo
gasto y aguda o crnica El estadio funcional se
realiza con la clasificacin de la NYHA.
La Sociedad Americana del Corazn ha
distinguido los distintos estadios evolutivos de IC:
A, con factor de riesgo para IC pero sin dao
estructural; B, dao estructural pero asintomtico;
C, sntomas de IC en alguna ocasin,
y D, IC terminal.
Etiologa. Las causas etiolgicas ms
importantes de IC en nuestro medio son, por este
orden: la cardiopata isqumica, la hipertensin
arterial y la diabetes mellitus .
Fisiopatologa. Para el desarrollo de IC es
necesaria la muerte de una masa crtica
de miocitos Una vez desarrollado el sndrome,
ste tiende a propagarse, afectando a otros
rganos Conceptualmente existen tres
mecanismos de compensacin: los modificadores
de la mecnica contrctil (ley de Frank-Starling,
principalmente), los neurohormonales y el
remodelado ventricular La IC como sndrome se
retroalimenta y genera ms IC. Los mismos
mecanismos compensadores son los que la
perpetan.
Medicine 2005; 9(35): 2279-2290
2279
01 Actualizacin 2279-90 14/6/05 17:15 Pgina 2280
Documento descargado de http://www.doyma.es el 14/08/2007. Copia para uso personal, se prohbe la transmisin de este documento por cualquier medio o formato.
ENFERMEDADES CARDIOVASCULARES (I)
metedor. Cada uno de estos modelos asume al anterior y lo
perfecciona, sin perder las ventajas adquiridas previamente.
Desde un punto de vista ms acadmico, si tuviramos
que elegir entre las muchas definiciones que intentan conceptuar lo que se entiende por IC, podramos elegir la aportada en 1980 por uno de los padres de la Cardiologa. Segn
Eugene Braunwald la insuficiencia cardaca es un estado fisiopatolgico en el que el corazn es incapaz de bombear el
suficiente volumen sanguneo para adaptarse a los requerimientos del metabolismo, o lo hace, a costa de elevar las presiones de llenado ventricular1.
Desde un punto de vista conceptual deberamos distinguir entre insuficiencia circulatoria, IC e insuficiencia miocrdica. La insuficiencia circulatoria es un estado en el que el sistema cardiovascular es incapaz de aportar la cantidad
suficiente de nutrientes para satisfacer la demanda tisular.
Cuando la insuficiencia circulatoria se debe a un fracaso cardaco se denomina IC, y si el fracaso es estrictamente del
msculo cardaco, estando preservadas el resto de las estructuras, la insuficiencia se denomina miocrdica. As pues la IC
es un caso particular de la insuficiencia circulatoria.
Finalmente desde un punto de vista clnico, la IC es un
sndrome conformado por la constelacin de sntomas y signos derivados tanto del fracaso del corazn como bomba,
como de los mecanismos compensadores que se ponen en
marcha para hacer frente a dicho fracaso.
Por ltimo es muy importante aclarar que, cuando diagnosticamos a un paciente de IC, estamos haciendo un diagnstico sindrmico que, aunque til, es insuficiente. Idealmente debera ir siempre acompaado de un esfuerzo para
alcanzar un diagnstico etiolgico si es que ste no ha sido
aclarado todava.
Epidemiologa
La IC ha sido definida como la epidemia del siglo XXI2,
su prevalencia y sus costes sanitarios se han visto incrementados de forma casi exponencial en las ltimas dcadas.
Cualquier intento a la hora de describir la epidemiologa,
etiologa o pronstico de este sndrome pasa por establecer
una definicin clara. Los estudios iniciales tomaron como
criterios de IC los descritos por el grupo de Framingham3.
Recientemente, las guas europeas para el diagnstico y tratamiento de la IC han propuesto nuevos criterios diagnsticos, tanto para la IC sistlica4, como para la diastlica5. La
mayora de los datos epidemiolgicos provienen de los
EE.UU., donde millones de personas la padecen y es la primera causa de ingreso en pacientes mayores de 65 aos6. En
Europa con una poblacin total de 900 millones de personas, unos 10 millones de personas padecen IC4. Se sabe que
las verdaderas cifras acerca de la IC son desconocidas. Es difcil establecer la verdadera prevalencia, incidencia o morbilidad, adems de por la prctica ausencia de registros (especialmente en Espaa), porque muchos de los pacientes se
encuentran totalmente asintomticos. Se ha calculado que la
prevalencia de disfuncin ventricular asintomtica oscilara
entre el 3%-12%, dependiendo del diseo del estudio7. Su
importancia radica en que la mayor parte de estos pacientes
2280
Medicine 2005; 9(35): 2279-2290
asintomticos no sern tratados y acabarn desarrollando IC
clnica de forma ms precoz y grave. En un reciente estudio
se observ que hasta la mitad de los pacientes de entre 25 y
75 aos, con fraccin de eyeccin (FE) < 30%, se encontraban libres de sntomas8. A esto hay que aadir el hecho de
que muchos de los registros se han basado en pacientes con
evidencia de disfuncin ventricular. Hoy sabemos que entre
un 40% a un 60% de los pacientes que ingresan por IC tienen una FE preservada, son el grupo principalmente compuesto por mujeres de los pacientes con IC diastlica. Como
observaremos a continuacin, buena parte de los datos conocidos sobre la prevalencia, incidencia, morbilidad, mortalidad y costes de esta pandemia provienen del estudio de
Framingham. Se trata de un seguimiento de 5.209 sujetos
pertenecientes a esta poblacin norteamericana que fueron
seguidos de forma bianual desde 1948. En 1971 se aadieron a esta cohorte los descendientes de los sujetos originarios. Veamos las escalofriantes cifras de la IC.
Prevalencia
Los estudios de prevalencia arrojan diferentes nmeros segn el mtodo en el que se basan para detectar casos de pacientes con IC. En general existen dos tipos de aproximaciones: a) contabilizar a los sujetos que demandan atencin
sanitaria por IC, y b) identificar, dentro de una poblacin
dada, a los pacientes que cumplen criterios de IC, bien identificando a los sujetos con criterios clnicos, como el estudio
de Framingham3, bien con criterios ecocardiogrficos de
funcin ventricular, como lo hace el estudio escocs de Glasgow8 bien combinando ambos criterios como lo hace el Echocardiographic Heart of England Screening Study9. Este ltimo
tipo de estudios son los que ms se acercan a las cotas
reales sobre prevalencia.
Globalmente hablando, en los pases industrializados, el
1% de la poblacin mayor de 40 aos padece IC. En los
EE.UU. se espera que para el ao 2007 la sufran unos 10
millones de habitantes. En Espaa, si bien slo existe hasta
la fecha un estudio sobre prevalencia, los porcentajes son similares10. Se sabe adems que la prevalencia de IC aumenta
con la edad y se duplica por cada dcada de vida. En el estudio de Framingham, entre los 50 y 59 aos la prevalencia
se situaba en el 0,8%, en el 2,3% entre los habitantes de entre 60 y 69 aos, en el 5% entre los de 70 y 79 y alcanzaba
casi el 10% en los mayores de 79 aos (fig. 1A)3. Hay que
recordar que este estudio se realiz basndose en criterios
clnicos y muchos autores sostienen que estas cifras estn infraestimadas.
Como se ha comentado anteriormente, la prevalencia de
IC ha ido en aumento constante. Existen al menos dos razones que explican esta tendencia: la primera es la aparicin de
nuevos tratamientos que han permitido por un lado un mejor control de la hipertensin arterial (HTA), la cardiopata
isqumica y la diabetes mellitus (DM), principales sustratos
que alimentan las cifras de pacientes con IC y, por otro, que
una vez que el paciente desarrolla IC sobrevive ms tiempo
gracias a estas terapias.
12
01 Actualizacin 2279-90 14/6/05 17:15 Pgina 2281
Documento descargado de http://www.doyma.es el 14/08/2007. Copia para uso personal, se prohbe la transmisin de este documento por cualquier medio o formato.
INSUFICIENCIA CARDACA: CONCEPTO, EPIDEMIOLOGA, CLASIFICACIN, ETIOLOGA Y FISIOPATOLOGA
Incidencia
Prevalencia de IC
9,8 9,7
10
Hombre
Mujer
6,8 6,6
6,2
6
4
3,4
1,8
2
0,1 0,1
20-24
25-34
35-44
45-54
55-64
65-74
75 +
98
20
01
0,1 0,1
1,3
0,7 0,5
94
96
Grupos de edad
B
Altas en miles dce personas
600
500
Hombres
Mujeres
400
300
200
100
90
92
84
86
88
82
80
72
74
76
78
70
0
19
Se sabe mucho menos acerca de la incidencia de la IC que
lo que se conoce acerca de su prevalencia. Los datos ms
exhaustivos provienen, una vez ms, del estudio de Framingham, en el que tras un seguimiento de 34 aos, la incidencia de IC era de 2 casos/1.000 habitantes/ao entre las
personas de entre 45 y 54 aos y se incrementaba hasta los
40 casos/ 1.000 habitantes/ao en los hombres mayores de
85 aos3. Para los mayores de 65 aos la incidencia estimada se sita en torno al 1% anual11. Estas cifras, sorprendentemente, se han mantenido estables en las ltimas dcadas,
y la razn reside en el equilibrio ocurrido entre dos fuerzas
opuestas: de un lado aquellas que han disminuido la cantidad de pacientes que desarrollan IC gracias a los avances
aplicados en el tratamiento de la HTA o de los eventos coronarios agudos (sobre todo a partir de la dcada de los
ochenta, con la introduccin de la fibrinlisis)12, y de otro
lado, la incidencia ha crecido fruto de otras dos grandes
epidemias que a principios de este siglo XXI estn surgiendo en los pases desarrollados, a saber, la DM tipo 2 y la
obesidad.
Ao
Diferencias por sexos
Distribucin del gasto por IC en EE.UU.
Por sexos, las mujeres presentan la misma prevalencia de
IC que los hombres. Esto se debe a que aunque la incidencia de IC es menor en ellas11, la longevidad de las mujeres es mayor (el 60% de la poblacin norteamericana mayor de 65 aos es mujer) y la mortalidad por IC incluso
cuando se ajusta por edad es menor entre las mujeres13. Los
factores de riesgo para el desarrollo de IC asociados a las
mujeres son la DM y la HTA, mientras que la cardiopata
isqumica es el principal factor de riesgo para los hombres14. Adems, es sabido que para el mismo factor de riesgo las mujeres presentan mayor probabilidad de desarrollar
IC. Las mujeres hipertensas tienen un 59% ms de riesgo
que sus homnimas normotensas de desarrollar IC. En los
varones esta cifra se sita en el 39%3. En el ensayo clnico
SOLVD las mujeres diabticas presentaban mayor riesgo
de padecer IC que los hombres (49,3% frente al 37,2%;
p < 0,02)15. Finalmente, aunque la incidencia de infarto de
miocardio es mucho menor en mujeres, stas desarrollan
con ms frecuencia IC16. En la mayor parte de los ensayos clnicos las mujeres se encuentran infrarrepresentadas
y se ha postulado que ellas responden peor al tratamiento
mdico que tan buen resultado ha dado en los hombres17.
El estudio DIG, que incluy a pacientes con IC sintomtica y disfuncin ventricular grave, haba demostrado en
1997 que aunque la digoxina no aumentaba la supervivencia, s que disminua los sntomas y reduca los ingresos
por IC. Pues bien un reciente anlisis post hoc, parece demostrar que entre las mujeres incluidas en este estudio,
tratadas con digoxina, la mortalidad era significativamente mayor respecto a aqullas a las que se administr placebo17.
13
Ingresos
60,7%
$ 23,1 billones
Trasplante
0,7%
$ 270 millones
Ambulatorio
38,6%
Coste total: $ 38,1 billones
(5,4% del gasto sanitario en EE.UU.)
$14,7 billones
3,4 consultas/paciente/ao
Tasa de mortalidad ajustada por edad/1.000 habitantes
D
140
120
100
80
60
40
20
0
IC
No IC
Mortalidad
total
Muerte sbita
Hombre
Mujer
Hombre
Mujer
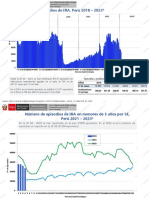
Fig. 1. Prevalencia de insuficiencia cardaca (IC) en EE.UU. por grupos de
edad y sexo. NHANES-III: 1988-1994. Fuente: CDC (Center for Disease Control). (A). Nmero de altas por IC en EE.UU. Se incluyen tambin los pacientes fallecidos. Fuente: CDC (Center for Disease Control). (B). Distribucin de
los costes por IC. Modificada de OConnell JB, et al. J Heart Lung Transplant.
1994;13:S107-12. (C). Datos del estudio Framingham, con un seguimiento de 38
aos Se observan las diferencias de mortalidad entres los pacientes que desarrollaron IC y los que no. Igualmente se evidencia la diferencia de mortalidad por sexos. En pacientes con IC las mujeres presentan menores tasas de
muerte total y sbita que sus homlogos varones. Modificada de Kannel WB,
et al. Am Heart J. 1998;136:205). (D).
Medicine 2005; 9(35): 2279-2290
2281
01 Actualizacin 2279-90 14/6/05 17:15 Pgina 2282
Documento descargado de http://www.doyma.es el 14/08/2007. Copia para uso personal, se prohbe la transmisin de este documento por cualquier medio o formato.
ENFERMEDADES CARDIOVASCULARES (I)
Morbilidad
Costes
Tanto en EE.UU. como en nuestro pas, la IC es la principal causa de ingreso en pacientes mayores de 65 aos. Ocasiona unos 15 millones de visitas mdicas anuales y 6,5 millones de das de ingreso por ao18. En la ltima dcada el
nmero de admisiones hospitalarias se ha incrementado en
un 160% y se sabe que un tercio de los pacientes volver a
reingresar al menos una vez en el siguiente semestre. La figura 1B muestra el incremento de altas hospitalarias por IC
en los EE.UU. En Espaa ingresan anualmente unos 80.000
pacientes por IC, lo que supone el 5% de todos los ingresos hospitalarios. Existe un cierto patrn estacional con mayor nmero de admisiones durante los meses de verano e invierno.
Por patologas, la IC supone una de las mayores cargas econmicas para un pas, superando incluso los gastos devenidos
por el cncer o el infarto de miocardio (fig. 1C). Durante
1991, en los EE.UU., la cuenta de gastos derivados del tratamiento de la IC sum un monto de 38.000 millones de
dlares, lo que supuso el 5,4% del total del presupuesto dedicado a sanidad en ese pas. El gasto farmacutico, en ese
mismo ao, ascendi a 500.000 millones de dlares21. Se ha
estimado que cada ingreso por IC cuesta entre 7.174 y
10.000 dlares22, lo que supone que esta patologa se lleva
entre el 1% y el 2% del presupuesto sanitario de los pases
industrializados. La mayor parte de este gasto se deriva de
los ingresos hospitalarios23. La figura 1C muestra el reparto
del gasto en IC. Es de esperar que las cifras crezcan, fruto de
unos tratamientos ms eficaces pero tambin ms caros y
tambin del aumento de la supervivencia de los pacientes con
fallo cardaco.
Mortalidad
En las ltimas dcadas se ha producido un notable descenso en el nmero de pacientes que fallece por IC. Tras 50
aos de seguimiento de los pacientes de la cohorte de Framingham, se produjo una considerable reduccin de la
mortalidad, pasando del 70% de fallecimientos a 5 aos entre los hombres de 1950 al 59% de muertes en el ao 2000.
En las mujeres la reduccin fue del 57% al 45%, en el mismo perodo. Globalmente se observ una disminucin de
los eventos mortales del 12% por dcada19. En nuestro pas
la IC se ha constituido como la tercera causa de muerte por
enfermedad cardiovascular y sus cotas superan a las del cncer, con una supervivencia media a 5 aos que ronda el
50%. En el ao 2000 la IC supuso el 4% de todas las muertes acaecidas en hombres y el 10% del total de muertes cardiovasculares. En mujeres estos porcentajes alcanzaron el
8% y 18%, respectivamente. Adems de stas diferencias
en el sexo, tambin se observan diferencias geogrficas, con
una tendencia a incrementarse la tasa de mortalidad conforme nos desplazamos de Norte a Sur11. Por ltimo tambin se han observado diferencias de mortalidad segn las
estaciones. En invierno y verano se alcanzan las mayores tasas de mortalidad, independientemente del sexo del paciente, siendo primavera y otoo las pocas de menor mortalidad por IC20.
Las arritmias son la principal causa de muerte en los pacientes con IC de poco tiempo de evolucin. Se estima que
entre un 30% a un 50% de los pacientes mueren de esta forma13. Posteriormente, conforme evoluciona el cuadro, los
pacientes supervivientes suelen fallecer por la progresin de
la enfermedad o por otro cuadro intercurrente en el que la
IC desempea un papel decisivo.
Se puede decir que hemos logrado disminuir la mortalidad por IC entre los ms jvenes, pero sta se mantiene entre los de mayor edad. Estamos cambiando el tipo de muerte cardiovascular. Quien originariamente falleca hace unos
aos de un infarto agudo de miocardio, ahora sobrevive a
l y muere, quiz algunas dcadas ms tarde, bien de IC bien
por otro proceso en el que la IC interviene como factor
fatal.
2282
Medicine 2005; 9(35): 2279-2290
Clasificacin de la insuficiencia cardaca1
Ms que una clasificacin propiamente, vamos a detallar diversos trminos que definen a este sndrome. Algunos de
ellos son fisiopatolgicos y otros clnicos, que en su conjunto ayudan a distinguir cul es el problema y definen la forma
de IC a la que nos enfrentamos.
Insuficiencia cardaca sistlica frente
a diastlica
La IC diastlica ha adquirido protagonismo al observarse
que es la responsable del fallo cardaco en la mitad de los pacientes que ingresan con un diagnstico de IC. Adems se ha
sabido que la morbilidad y mortalidad son muy parecidas en
uno y otro caso. Recientemente, la Sociedad Europea de
Cardiologa ha establecido unos criterios para el diagnstico
de IC diastlica. El desarrollo de fallo diastlico supone que,
o bien las fibras musculares cardacas no se relajan lo suficiente ni con la suficiente rapidez o que existe un impedimento al llenado ventricular (por ejemplo, una constriccin
pericrdica), en cualquier caso, el dbito de sangre oxigenada que proviene desde los pulmones no es admitido por el
ventrculo, que encuentra su llenado restringido. La consecuencia es que los volmenes, y por tanto las presiones retrgradas se elevan ocasionando dos tipos de sntomas: los
congestivos o retrgrados (edema de miembros y ascitis en
lado derecho y edema agudo de pulmn en el izquierdo) y los
de bajo gasto o antergrados (fatigabilidad, intolerancia al
ejercicio, debilidad, etc.). En la IC sistlica, la admisin de
sangre al ventrculo no est impedida y la relajacin es normal, sin embargo, el corazn es incapaz de bombear con eficacia la sangre. Las consecuencias son las mismas sea el fallo
cardaco sistlico o diastlico.
La causa ms importante de fallo sistlico izquierdo es la
cardiopata isqumica y la del fallo derecho es el fallo iz14
01 Actualizacin 2279-90 14/6/05 17:15 Pgina 2283
Documento descargado de http://www.doyma.es el 14/08/2007. Copia para uso personal, se prohbe la transmisin de este documento por cualquier medio o formato.
INSUFICIENCIA CARDACA: CONCEPTO, EPIDEMIOLOGA, CLASIFICACIN, ETIOLOGA Y FISIOPATOLOGA
quierdo sostenido en el tiempo y, en segundo lugar, la hipertensin pulmonar. En cuanto a la causa ms importante
de fallo diastlico izquierdo en nuestro medio es la HTA
y de fallo diastlico derecho, la pericarditis constrictiva.
Insuficiencia cardaca de alto frente
a bajo gasto
El ndice cardaco normal (gasto cardaco/m2) oscila entre 2,2
y 3,5 litros/minuto/m2. Cuando el paciente sufre sntomas y
signos de IC diremos que padece una IC de bajo gasto si su ndice cardaco es menor de 2,2 y de alto gasto si es mayor de 3,5
litros/minuto/m2. Entre las causas ms importantes de IC de
bajo gasto se encuentran: la cardiopata isquemia, las valvulopatas y las miocardiopatas. Entre las de alto gasto: el embarazo, la tirotoxicosis, la enfermedad de Paget, los pacientes
que presentan fstulas arteriovenosas y el dficit de vitamina
B1, que causa un proceso llamado beri-beri hmedo. El beriberi hmedo ocasiona generalmente una IC de alto gasto,
aunque tambin puede producir bajo gasto cardaco, denominndose entonces enfermedad de Shoshin.
Insuficiencia cardaca aguda frente a crnica
Cuando un paciente padece una IC aguda, los mecanismos
de adaptacin que habitualmente se ponen en marcha no tienen tiempo de hacerlo y se producen, generalmente, cuadros
catastrficos. Ejemplos de esta situacin son: rotura de una
valva cardaca o la pared libre del ventrculo en el seno de un
infarto agudo de miocardio (IAM), perforacin cardaca por
arma blanca o infartos masivos.
En la IC crnica los mecanismos compensadores se han
puesto en marcha y el paciente puede estar sintomtico pero
estable. Decimos que la IC crnica esta compensada cuando
los mecanismos de compensacin permiten que a pesar de la
IC el individuo siga vivo. Se denomina IC crnica descompensada cuando fruto de alguna agresin externa (trasgresin
diettica, infeccin intercurrente, etc.), estos mecanismos se
ven desbordados y son insuficientes para mantener la vida
del individuo.
Insuficiencia izquierda frente a derecha
Aunque las fibras miocrdicas son compartidas por ambos
ventrculos, existen causas que daan selectivamente ms a
uno de ellos. El IAM produce un dao preferente sobre el
ventrculo izquierdo (VI), y fruto de ello se desarrollan sntomas congestivos retrgrados (disnea, ortopnea y edema
agudo de pulmn) y antergrados (debilidad e intolerancia al
ejercicio). Cuando la noxa daa predominantemente el ventrculo derecho (VD), por ejemplo una hipertensin pulmonar primaria, los sntomas antergrados son idnticos a los
del lado izquierdo (datos de bajo gasto), pero los retrgrados
cambian y se produce la famosa trada de edema perifrico,
ingurgitacin yugular y hepatomegalia. Finalmente, repetir
una vez ms que la causa ms frecuente de fallo derecho es el
15
fallo izquierdo. Decimos que un paciente sufre una IC congestiva cuando presenta signos y sntomas de disfuncin en
ambos ventrculos.
Estadios de la insuficiencia cardaca
Adems del ventrculo afectado, de la parte del ciclo cardaco en el que se produce la disfuncin, del volumen circulatorio manejado y de la cronopatologa del proceso, para
caracterizar a un paciente con IC se han descrito dos clasificaciones ms. La de la NYHA (New York Heart Association),
describe la capacidad funcional que es capaz de desarrollar
un paciente con IC. Se dice que un paciente est en clase
funcional: NYHA I, si es capaz de desarrollar su actividad
diaria sin sntomas de IC; NYHA II, si los sntomas aparecen
con la actividad ordinaria; NYHA III, cuando los sntomas
aparecen con actividades inferiores a las ordinarias, y NYHA
IV, si el paciente padece sntomas incluso en reposo.
La clasificacin de la NYHA es universalmente aplicada.
Ha sido utilizada en medicina laboral y legal para estratificar
la limitacin de estos pacientes y es muy til para monitorizar la respuesta al tratamiento. Sin embargo, posee algunas
limitaciones que conviene conocer. La primera es su grado
de subjetividad tanto por parte del paciente como por parte
del mdico, distintos pacientes con idntico grado de enfermedad pueden referir distintos grados funcionales. En segundo lugar, la clase funcional puede oscilar entre los distintos estadios en cuestin de horas, sobre todo en situaciones
de descompensacin cardaca. Por ltimo, la NYHA guarda
una pobre correlacin tanto con la fraccin de eyeccin del
ventrculo izquierdo (FEVI), como con el pronstico. No
nos facilita informacin sobre la verdadera situacin del paciente. Un paciente con disfuncin moderada del VI puede
ingresar en clase IV y poseer un mejor pronstico que otro
paciente con disfuncin grave que se mantiene en clase II.
Debido a estas limitaciones, recientemente, en las nuevas
guas que la AHA/ACC realiz sobre IC21, se definieron 4
estadios de evolucin que definen la progresin de la enfermedad. Cada uno de ellos es irreversible, de modo que cuando un paciente se encuentra en uno de ellos, a pesar del tratamiento no regresa a un estadio anterior salvo que sea
trasplantado. Vamos a describirlos:
1. Estadio A: identifica a los pacientes que presentan algn factor de riesgo para desarrollar IC, pero que no presentan alteraciones estructurales en su corazn. Ejemplos de
pacientes en este estadio son los pacientes diabticos o hipertensos asintomticos y con ecocardiograma normal.
2. Estadio B: identifica a pacientes asintomticos que ya
presentan alguna alteracin estructural en su corazn que les
predispone al desarrollo de IC sintomtica. El paradigma de
este grupo son los pacientes que han sufrido un IAM, tras el
que la FEVI ha quedado disminuida, pero que se encuentran
libres de sntomas. Padecen lo que se denomina una disfuncin ventricular asintomtica.
3. Estadio C: son pacientes con alguna alteracin cardaca
estructural que tienen o han tenido en algn momento de su
evolucin sntomas de IC, aunque en el momento actual podran estar asintomticos.
Medicine 2005; 9(35): 2279-2290
2283
01 Actualizacin 2279-90 14/6/05 17:15 Pgina 2284
Documento descargado de http://www.doyma.es el 14/08/2007. Copia para uso personal, se prohbe la transmisin de este documento por cualquier medio o formato.
ENFERMEDADES CARDIOVASCULARES (I)
4. Estadio D: se trata de pacientes que se encuentran en estado final de su evolucin y que requieren tratamientos adicionales especiales como soporte inotropo o asistencia ventricular. Son los potenciales candidatos a trasplante cardaco.
Como se puede observar, esta nueva clasificacin reconoce que hasta ahora en los ensayos farmacolgicos sobre
IC, slo se haban tenido en cuenta a los pacientes de los estadios C y D y, por otro lado, que existen factores de riesgo
que predisponen al desarrollo de IC y que, por tanto, su tratamiento precoz podra suponer una reduccin en la prevalencia, incidencia y morbimortalidad de esta entidad.
Etiologa
La lista de enfermedades que pueden conducir al desarrollo
de IC es muy extensa. Como ya hemos apuntado anteriormente, dado que el conocimiento de la causa subyacente tiene repercusiones teraputicas y pronsticas, junto con el
diagnstico del sndrome de IC debera ir siempre la causa
subyacente que lo ha originado.
Tradicionalmente, los libros de texto distinguen tres tipos de causas, a saber: las predisponentes, las determinantes
y las precipitantes. Un mismo factor puede ser a la vez predisponente, determinante y desencadenante. Por ejemplo la
cardiopata isqumica predispone al desarrollo de IC, es un
determinante claro en caso de infartos masivos, y sucesivos
episodios de angina pueden descompensar a un paciente y
precipitar nuevos episodios de IC1.
Causas predisponentes
Son tambin llamadas factores de riesgo. Se dividen en:
Causas predisponentes etiolgicas
La principal es la cardiopata isqumica. En los EE.UU., el
50% de los casos de IC se deben a ella. El riesgo de desarrollar IC tras un IAM se multiplica por 10 el primer ao y por
20 en los sucesivos24.
Causas probablemente etiolgicas
Son condicionantes necesarios pero no suficientes. Slo si no
son tratadas o si se asocian a otros factores el paciente acabar desarrollando IC. La ms importante es la HTA. El
riesgo de desarrollar IC en los pacientes con HTA por encima de 160/90 mmHg se cuadriplica respecto a la poblacin
no hipertensa. Si adems existe hipertrofia del VI, el riesgo
se multiplica por 17. Respecto a la DM, el otro protagonista
de este grupo, las mujeres diabticas presentan 5 veces ms
riesgo de desarrollar IC que las sanas19.
Causas no etiolgicas
Incluye a los marcadores de riesgo (no modificables), como
la edad, la raza y el sexo y otros que s son modificables,
como la obesidad y el sedentarismo. En los anlisis multivariantes de grandes estudios poblacionales se han identificado
como factores asociados a mayor probabilidad para el desarrollo de IC, pero no existe una clara relacin causa-efecto.
2284
Medicine 2005; 9(35): 2279-2290
Causas determinantes
Su aparicin supone, de forma indefectible, la aparicin de
IC. Se subdividen en:
Miocardiopatas
Primarias. Como la miocardiopata dilatada, en la que en un
20% de los pacientes existe una carga gentica demostrada.
La miocardiopata hipertrfica, que se transmite de forma
autonmica dominante y ocasiona buena parte de las muertes sbitas entre los jvenes deportistas y la miocardiopata
restrictiva, tan rara en nuestro medio como letal.
Secundarias. Fundamentalmente la cardiopata isqumica.
Menos frecuentes son las miocarditis infecciosas, en su mayora vricas (tambin las asociadas al Chagas, Toxoplasma o
Rickettsia), que si producen destruccin celular miocrdica,
pueden condicionar un cuadro extremadamente grave. Las
miocardiopatas txicas tambin pertenecen a este grupo. A
destacar las secundarias a quimioterpicos (agentes alquilantes) y a alcohol. Las miocardiopatas asociadas a enfermedades neuromusculares como la de Becker, Steinert o Friedrich
son raras aunque a menudo mortales para los pacientes. Las
miocardiopatas asociadas a dficits carenciales (vitamina B1,
carnitina), las asociadas a enfermedades endocrinas (Cushing, hipo e hipertiroidismo) y las de origen inflamatorio
(sarcoidosis, lupus, artritis reumatoide) son otros ejemplos
de este grupo.
Sobrecargas de volumen o presin mantenidas
Tambin terminan por deteriorar el miocardio y condicionan la aparicin de IC.
Arritmias
Por ltimo una taquicardia mantenida en el tiempo puede
ocasionar una taquimiocardiopata. Se trata de una miocardiopata reversible si se logra controlar la frecuencia cardaca del paciente.
Causas precipitantes
Son factores que ocasionan IC en pacientes con un dao cardaco estructural conocido o no. Las causas ms frecuentes
de descompensacin son las arritmias y las infecciones, seguidas de cerca por el incumplimiento diettico o farmacolgico y la isquemia miocrdica, aunque hasta en un 40% de
las ocasiones no se consigue identificar el factor que ha precipitado la descompensacin25.
En las ltimas dcadas se ha producido un cambio en los
factores etiolgicos de la IC. El diagnstico precoz y ms
preciso de los factores predisponentes, junto a tratamientos
tanto mdicos como quirrgicos, cada vez ms eficaces, han
hecho que la HTA y las valvulopatas ya no ostenten los primeros puestos de la lista. Por el contrario la cardiopata isqumica sigue como el principal factor determinante de IC,
y la DM ha surgido en las sociedades occidentales como una
nueva epidemia, que ha trascendido el mbito de la endocri16
01 Actualizacin 2279-90 14/6/05 17:15 Pgina 2285
Documento descargado de http://www.doyma.es el 14/08/2007. Copia para uso personal, se prohbe la transmisin de este documento por cualquier medio o formato.
INSUFICIENCIA CARDACA: CONCEPTO, EPIDEMIOLOGA, CLASIFICACIN, ETIOLOGA Y FISIOPATOLOGA
0
20
40
60
C. isq
DM
HTA
Valv.
Fig. 2. Cambio en los factores causales de insuficiencia cardaca (IC) en el
estudio de Framingham durante el perodo de 1950 a 1987. Modificada de
Kannel WB, et al. Am Heart J. 1998;136:205). C.isq: cardiopata isqumica;
DM: diabetes mellitus; HTA: hipertensin arterial; Valv.: valvulopata.
nologa y se esta empezando a considerar como una enfermedad tambin cardiovascular. La figura 2 ilustra cmo se
han modificado en las ltimas dcadas los principales factores desencadenantes de la IC.
Fisiopatologa
Podramos agrupar en dos los patrones por los que se inicia
el proceso de fallo cardaco. El primero se podra denominar el patrn de dao agudo, cuyo paradigma es el IAM.
En l se produce un evento ndice que supone una rpida
prdida de masa celular cardaca (miocitos). Los mecanismos compensadores que se ponen en marcha inicialmente
intentan suplir dicha prdida. Estos mecanismos desarrollados a lo largo de millones de aos mantienen el equilibrio inicial a costa de exprimir a los miocitos supervivientes. La sobredemanda de esfuerzo hace que incluso estos
miocitos vayan pereciendo paulatinamente. Finalmente la
masa celular es insuficiente, las fuerzas de equilibrio se
rompen y ni siquiera los mecanismos de compensacin
son suficientes para mantener la supervivencia del individuo.
El otro patrn es el de dao crnico, en esta ocasin
la causa subyacente produce una erosin continua en el sistema cardiovascular, inicialmente la reserva funcional cardaca es suficiente para afrontar ese dao, pero conforme
pasa el tiempo, el nmero de miocitos perdidos es mayor.
Cuando se alcanza una cifra crtica, el dao estructural es
tal que el corazn no es capaz de adaptarse a las exigencias
de los rganos de la economa sin ayuda de los mecanismos
compensadores. stos se ponen en marcha, y como ocurra
en caso del patrn de dao agudo, aunque reestablecen
temporalmente el equilibrio, a largo plazo sus efectos son
deletreos. El paradigma del patrn de dao crnico es la
HTA.
Cuando un paciente entra en la espiral de deterioro que
supone la IC, se mantiene en ella merced a dos mecanismos:
uno el originario, el que inici todo el proceso, el otro, el de
los mecanismos compensadores, que a cambio de mantener
un gasto cardaco aceptable van minando la reserva funcional
del rgano. Debemos recordar que existen algunos casos en
17
Modificaciones autnomas en la mecnica
contrctil
Existen dos mecanismos que responden a cambios en la hemodinmica cardaca. Ambos modifican la mecnica contrctil de forma autnoma e independiente de otros mecanismos
compensadores.
El primero de ellos es el denominado heteromtrico,
ms conocido como ley de Frank-Starling. Merced a l, un
incremento en la longitud de las fibras cardacas conlleva
una mejora en la fuerza de contraccin. La figura 3 ilustra
este fenmeno y la figura 4 explica su mecanismo intrnseco.
Funcin
ventricular
normal
Perfusin normal
Hombre
Mujer
20
Gasto cardaco
Porcentaje (%)
40
los que la IC es reversible, pero incluso en ellos existe un
punto crtico de no retorno, a partir del cual, incluso la correccin de la causa subyacente no detendr en absoluto la
progresin de la IC.
Con un fin didctico hemos dividido la respuesta al dao
miocrdico en tres tipos de mecanismos compensadores, a
saber: modificaciones autnomas en la mecnica contrctil,
activacin de los sistemas neurohormonales y remodelado
ventricular.
Los dos primeros se ponen en marcha precozmente, en
cuestin de minutos u horas, mientras el tercero es una adaptacin ms tarda. Aunque los expliquemos por separado, estn ntimamente imbricados y los cambios acaecidos en uno
de ellos suponen modificaciones en los dems.
A
Disfuncin
ventricular
Hipoperfusin
IC terminal
Sntomas congestivos
+
hipoperfusin
Presin telediastlica de ventrculo izquierdo
Fig. 3. Este grfico muestra el mecanismo por el que la ley de Frank-Starling
compensa la disfuncin ventricular en los pacientes con insuficiencia cardaca (IC). La curva en AZUL representa el rendimiento contrctil de un corazn sano en funcin de sus presiones de llenado. Cuando se produce un dao
miocrdico el gasto cardaco decrece de A hasta B. Con las presiones de llenado anteriores el gasto es insuficiente y los tejidos se encuentran hipoperfundidos, se deben incrementar las presiones telediastlicas para que el
gasto se eleve. Sin embargo con disfuncin ventricular la pendiente de la
curva (en marrn) es menor que la de un corazn indemne y por tanto el rendimiento de la compensacin por el mecanismo de Frank-Starling tambin lo
es. Finalmente si el dao es masivo o supera un determinado nivel, la compensacin es insuficiente y el corazn no es capaz de elevar suficientemente su gasto cardaco como para suplir los requerimientos del organismo (curva roja). Aparecen entonces los sntomas congestivos y de hipoperfusin.
Medicine 2005; 9(35): 2279-2290
2285
01 Actualizacin 2279-90 14/6/05 17:15 Pgina 2286
Documento descargado de http://www.doyma.es el 14/08/2007. Copia para uso personal, se prohbe la transmisin de este documento por cualquier medio o formato.
ENFERMEDADES CARDIOVASCULARES (I)
Activacin de los sistemas
neurohormonales
B 900
48
LS 1,65 m
100
Una compleja serie de mecanismos
neurohormonales se ponen en
80
marcha debido fundamentalmente
F
a dos alteraciones: la hipoperfusin
0
0
60
secundaria a la cada del gasto car48
daco y el aumento de las presiones
900
LS 2,15 m
40
retrgradas auriculares. Los princiCa2+
pales mecanismos neurohormoF
Ca2+
20
nales compensadores son tres: a)
F
activacin del sistema nervioso au0
tnomo adrenrgico (SNAA); b)
60
70
80
90
100
0
0
activacin del eje renina-angioten360 ms
Longitud (% del mximo)
sina-aldosterona (SRAA), y c) secrecin de pptidos reguladores.
En la fase aguda estos cambios
Fig. 4. Mecanismo de Frank-Starling. A. La grfica representa la tensin mxima (fuerza contrctil) que es
capaz de realizar una fibra muscular en funcin del porcentaje de la longitud mxima alcanzada. Tanto en el
neurohormonales son cruciales
msculo esqueltico como en el cardaco, un incremento en la longitud supone un aumento en la eficacia de
para la supervivencia del individuo,
la fuerza contrctil. En el msculo esqueltico se necesita mayor elongacin para alcanzar la mxima teny permiten la redistribucin del
sin. Los sarcmeros de los miocitos, sin embargo, ya se encuentran estirados al 80% de su longitud mxima, de forma que pequeos estiramientos adicionales incrementan mucho la fuerza contrctil. Las fibras
gasto cardaco hacia los territorios
de los miocitos responden antes y con mayor contundencia al estiramiento. En el grfico tambin se puede
vitales, pero a la larga se comporobservar que, en parte, la reserva contrctil se consigue porque para un determinado nivel de estiramiento
tan como armas de doble filo, ya
los filamentos de actina y miosina estn menos solapados y por tanto es ms eficaz el movimiento de deslizamiento de los filamentos. Sin embargo si la elongacin supera un lmite, stos se desacoplan y la fibra
que en la fase crnica de la enferpierde toda su funcin. (Modificada de Backx PH, ter Keurs HEDJ. Am J Physiol. 1993;264:H1098-110.) B. La
medad tienden a producir sobreley de Frank-Starling no se puede explicar slo por la aposicin ms eficaz de los filamentos de actina y
carga de volumen por retencin
miosina al elongarse el sarcmero. El aumento de la fuerza de la fibra es mayor de lo que este mecanismo
de forma aislada podra predecir. Se sabe que al aumentar la longitud de la fibra, sta se hace ms sensible
excesiva de agua y sal, aumento de
al calcio, y para una misma corriente de entrada de calcio intracelular la respuesta contrctil es mucho malas resistencias perifricas, toxiciyor en fibras elongadas hasta su mximo (grfico inferior) que cuando la fibra se encuentra ms acortada
dad directa de los miocitos, altera2+
(grfico superior). Modificada de Fuchs F, et al. Mechanical modulation of the Ca regulatory protein comciones electrolticas y arritmias.
plex in cardiac muscle. NIPS. 1995;10:6-12.
Por el contrario, junto a estos mecanismos, tambin se activan otros
que tienden a compensar estos
efectos adversos. As, se secretan pptidos natriurticos que
En la IC, el volumen latido se halla disminuido y la canadems de ser vasodilatadores producen diuresis, natriuresis
tidad de sangre que queda remanente en el ventrculo tras la
y una inhibicin del SNAA. Del equilibrio de estas fuerzas
contraccin es mayor que en un corazn sano. Ese incremendepende el que el individuo permanezca en una situacin de
to del volumen telediastlico final en los corazones insufiIC compensada o no.
cientes es el que produce una elongacin de los sarcmeros.
Estas fibras ms alargadas ofrecen un mayor rendimiento
Activacin del sistema nervioso autnomo adrenrgico
contrctil (adaptacin heteromtrica) y por tanto consiguen
Cuando el gasto cardaco disminuye y los tejidos son hipouna mejora en el gasto cardaco. As se soluciona o al menos
perfundidos, los baro y quimiorreceptores repartidos a lo
se pala de forma temporal la prdida de masa celular que orilargo de toda la economa activan el SNAA. ste consta fungin inicialmente la disfuncin cardaca26.
damentalmente de un pptido que funciona principalmente
El otro mecanismo es menos conocido y menos potente
como neurotransmisor, la noradrenalina (NAd), y otro que
a la hora de compensar a un corazn insuficiente. Se trata del
lo hace como una neurohormona, la adrenalina (Ad). Se sabe
efecto Anrep o mecanismo homeomtrico. En l, un aumenque las concentraciones en sangre de NAd, Ad y dopamina
to de la tensin en las fibras miocrdicas (por ejemplo debide sujetos con IC duplican o triplican a las de los sujetos
do a una estenosis artica o a una crisis hipertensiva) produsanos. Estos niveles se encuentran elevados incluso en pace, tambin de forma autnoma e inmediata, un incremento
cientes con disfuncin ventricular asintomtica y se correlaen la fuerza contrctil de los sarcmeros, sin que sea necesacionan estrechamente con las presiones de llenado del venrio que stos modifiquen su longitud.
trculo izquierdo, la magnitud de la disfuncin cardaca y el
Como se puede observar el corazn presenta dos mecapronstico27. La activacin del SNAA produce a nivel carnismos propios y completamente autnomos para incrementar casi instantneamente el gasto cardaco. Uno, la ley de
daco un aumento de la fuerza contrctil (inotropismo) y de
Frank-Starling, est especialmente diseado para hacer frenla frecuencia cardaca (cronotropismo), merced a la estite a un exceso de precarga, mientras que el otro, el efecto Anmulacin de los receptores 1 que son mayoritarios en el
rep, compensa los aumentos de postcarga.
msculo cardaco. Sin embargo, la estimulacin a largo pla2286
M
car sculo
da
co
Ca2+
M
esq scu
uel lo
tic
o
Tensin (% del mximo)
Ca2+
Medicine 2005; 9(35): 2279-2290
18
01 Actualizacin 2279-90 14/6/05 17:15 Pgina 2287
Documento descargado de http://www.doyma.es el 14/08/2007. Copia para uso personal, se prohbe la transmisin de este documento por cualquier medio o formato.
INSUFICIENCIA CARDACA: CONCEPTO, EPIDEMIOLOGA, CLASIFICACIN, ETIOLOGA Y FISIOPATOLOGA
zo de los pocos receptores 1 presentes en el miocardio inducir la sntesis de factores de crecimiento celular, que hipertrofiarn el msculo, as como la expresin de un programa gentico fetal que supondr la sntesis de miofibrillas
inmaduras con menor eficiencia contrctil.
A nivel renal, los receptores mayoritarios son los 1, sin
embargo existen receptores 1 en el aparato yuxtaglomerular de la mcula densa y su estimulacin produce la liberacin de renina. Por su parte, la estimulacin de los receptores 1 ocasiona la vasoconstriccin de la arteriola eferente,
que conllevar la retencin de sodio y agua. Por ltimo a nivel vascular, donde los receptores adrenrgicos son de predominio 1 en la periferia y 2 en la regin esplcnica, producen una redistribucin del gasto cardaco con aumento de
resistencias y mantenimiento de la perfusin a nivel central.
Todos estos cambios inicialmente logran compensar una
cada en el gasto cardaco, sin embargo aunque el SNAA est
diseado para producir rendimientos tremendamente eficaces no puede ser mantenido durante mucho tiempo. Cuando
la situacin de IC se hace crnica, se produce una deplecin
de las reservas de NAd por un mecanismo de extenuacin.
Adems, los receptores adrenrgicos sufren modificaciones
cuando son estimulados continuamente. Se sabe que los 1
aumentan en densidad, favoreciendo la vasoconstriccin, la
toxicidad directa miocitaria y la expresin de protenas con
fenotipo embrionario. Los receptores 1 disminuyen y los
2 se desacoplan de sus segundos mensajeros26.
Pasado un tiempo el SNAA no ser capaz de mantener el
gasto cardaco, sus acciones compensadoras irn desapareciendo y comenzarn a prevalecer las acciones deletreas que
empeorarn an ms el cuadro de IC.
Activacin del eje renina-angiotensina-aldosterona
Existen dos mecanismos que activan el sistema SRAA. El
primero de ellos ya fue descrito en el apartado anterior. La
activacin del SNAA produce estimulacin de los receptores 1 de la mcula densa, induciendo la liberacin de renina. El otro mecanismo, independiente del anterior, es la
disminucin de la perfusin renal. Una cada en la misma
es detectada por los barorreceptores renales que de forma
local liberan renina. La renina es una proteasa que transforma el angiotensingeno (tetradecapptido sintetizado en
el hgado), en angiotensina I (A-I). La A-I a su vez se transformar en angiotensina II (A-II), merced a la enzima conversora de angiotensina (ECA), de predominio pulmonar.
La A-II posee varias acciones: estimula directamente el
SNAA, aumentando la liberacin de NAd en las terminaciones nerviosas y promueve la liberacin de aldosterona
por parte de la capa glomerulosa de la corteza suprarrenal.
La aldosterona induce la reabsorcin de sodio y agua, promoviendo la secrecin de potasio. Adems, cuando la secrecin es mantenida crnicamente, ocasiona fibrosis miocrdica. Por otro lado, la A-II es un potente vasoconstrictor
y, una vez ms, aunque de forma aguda ste sea un mecanismo que ayude a sobrevivir al individuo, a largo plazo supone un aumento de la postcarga y, por ende, del trabajo
miocrdico, ayudando as a perpetuar el crculo vicioso de
la IC. Otros efectos a largo plazo de la A-II son: hipertrofia de miocitos, inicio de un programa fetal cardaco, por el
19
que se expresan protenas contrctiles inmaduras y por ltimo fibrosis miocrdica.
Se han caracterizado 4 receptores de la A-II, pero de momento slo dos son universalmente aceptados en la nomenclatura internacional: el AT1 y el AT2. En los tejidos la proporcin de ellos es 1:2 a favor del receptor AT2. La
estimulacin del receptor AT1 sera la responsable de todos
los efectos deletreos asociados a la A-II (vasoconstriccin,
fibrosis, remodelado vascular, etc.), mientras que la accin de
los receptores AT2 sera ms beneficiosa (vasodilatacin, inhibicin de las seales presoras y cronotropas, etc.).
Como ocurra con la activacin del SNAA, la activacin
del sistema SRAA es un mecanismo compensador, con efectos nocivos a largo plazo. La interrelacin entre ambos sistemas es estrecha y posee un efecto sinrgico26.
Secrecin de pptidos reguladores28
Adems de los pptidos que participan de los sistemas adrenrgico y SRAA, existen otras sustancias que participan de la
neuromodulacin de la IC. Entre ellas cabe destacar las siguientes:
Pptidos natriurticos. Son fundamentalmente tres: el
ANP o pptido natriurtico atrial, sintetizado en las aurculas como consecuencia del estiramiento de las fibras musculares atriales; el BNP (brain natriuretic peptide) inicialmente
descubierto en el cerebro, de ah su nombre, pero que posteriormente se observ en miocardio ventricular, y finalmente,
el CNP, cuya principal fuente es el endotelio vascular y, en
menor medida, el sistema nervioso central. Los tres pptidos
son secretados como consecuencia de la estimulacin de mecanorreceptores de estiramiento. Una vez liberados al torrente sanguneo, producen diuresis, natriuresis y vasodilatacin. Se oponen por tanto a las acciones de la NAd, A-II,
aldosterona, vasopresina y endotelina.
Vasopresina. Neurohormona secretada por la neurohipfisis, como consecuencia de un descenso en la presin arterial. Produce vasoconstriccin y antidiuresis, ocasionando
hiponatremia dilucional. Sus valores en plasma son especialmente altos en pacientes que reciben tratamiento diurtico.
Endotelinas. Secretadas por el endotelio vascular, poseen
acciones auto y paracrinas. Producen una profunda vasoconstriccin a nivel perifrico y esplcnico, induciendo la
retencin de sodio y agua a nivel renal. Las concentraciones plasmticas de endotelinas poseen valor pronstico
y se correlacionan bien con el grado de disfuncin ventricular.
Otros. En la IC mantenida, existen otros sistemas compensadores que intentar mantener el equilibrio entre una
vasodilatacin suficiente como para aportar nutrientes a los
tejidos y una vasoconstriccin adecuada para mantener presiones de perfusin. Entre ellos destaca el sistema de la
kinina-kalicrena, cuyo producto es la bradicinina, potente natriurtico y vasodilatador. ste a su vez activa el sistema de las prostaglandinas (sobre todo PGE2 y PGI2), con
Medicine 2005; 9(35): 2279-2290
2287
01 Actualizacin 2279-90 14/6/05 17:15 Pgina 2288
Documento descargado de http://www.doyma.es el 14/08/2007. Copia para uso personal, se prohbe la transmisin de este documento por cualquier medio o formato.
ENFERMEDADES CARDIOVASCULARES (I)
Dao miocrdico
Gasto cardaco
Hipertrofia
Remodelado
Apoptosis
Toxicidad directa
Perfusin
ANP
BNP
Presiones de llenado
Sntomas congestivos
+
Activacin de
SNAA
SRAA
Retencin de Na y H2O
pales responsables del consumo de
oxgeno cardaco, junto con la contractilidad y la frecuencia cardaca.
La tensin parietal (T), segn la
Ley de Laplace, depende directamente de la presin (Pr) y del radio
(r) intracavitarios y es inversamente proporcional al grosor parietal
(g).
Ley de Laplace:
T = Pr r
2g
En condiciones patolgicas,
tambin se desarrolla hipertrofia
ventricular como mecanismo
Fig. 5. Fisiopatologa de la insuficiencia cardaca, mecanismos compensadores y perpetuacin del crculo
vicioso (ver explicacin en el texto). SNAA: activacin del sistema nervioso autnomo adrenrgico; SRAA:
compensador, pero sus efectos
sistema renina-angiotensina-aldosterona; ANP: pptido natriurtico atrial; BNP: brain natriuretic peptide.
son, una vez ms, deletreos a largo plazo.
Existen dos patrones de hipertrofia ventricular: el patrn de hipertrofia excntrica que es
acciones vasodilatadoras y protectoras de la perfusin
un fenmeno de adaptacin frente a las sobrecargas de volurenal.
men, mientras que el patrn de hipertrofia concntrica comLa figura 5 intenta esquematizar las intrincadas relaciopensa las sobrecargas de presin.
nes existentes entre estos mecanismos compensadores y el
Las sobrecargas crnicas de volumen debidas a condiciocrculo vicioso al que se ve abocado el paciente una vez que
nes patolgicas, como por ejemplo una insuficiencia artica
son mantenidos crnicamente.
o un IAM extenso, inducen una dilatacin de la cmara cardaca (radio), que tiende a ser compensada por un ligero aumento del grosor. El grosor parietal se consigue hipertroRemodelado ventricular29,30
fiando las fibras miocrdicas y creando nuevas miofibrillas
que se disponen en serie. Se desarrolla as una hipertrofia exSe denomina remodelado a los cambios en la arquitectura
cntrica, con dilatacin del ventrculo afecto.
miocrdica que se producen para compensar el aumento de
Cuando lo que existe es una sobrecarga de presin crla demanda contrctil. A diferencia de los dos anteriores,
nica, como por ejemplo la que sufren los pacientes hiperrequiere cierto tiempo para ponerse en funcionamiento,
tensos o aqullos con una estenosis artica, el corazn se
aunque es igual de eficaz en compensar corazones insufienfrenta a un aumento de la presin intracavitaria y por
cientes.
ende, del radio. Para intentar mantener la tensin parietal,
El remodelado puede ser fisiolgico y adecuado o, por el
el msculo incrementa notablemente su grosor por medio
contrario, en situaciones patolgicas, maladaptativo.
de una hipertrofia ms marcada de las fibrillas existentes y
El proceso de remodelado, en los pacientes con IC, prede la creacin de nuevas miofibrillas, que en esta ocasin se
senta dos fases. En la primera, los estmulos mecnicos de
disponen en paralelo. Se desarrolla as una hipertrofia condistensin parietal y la estimulacin de los receptores neucntrica.
rohormonales presentes en los miocitos inducen una hiperLa aparicin de hipertrofia ventricular viene determinatrofia adecuada a la situacin. Si la situacin se mantiene
da por varios estmulos: unos locales, de estiramiento a nivel
crnicamente, la reserva funcional cardaca se va agotando,
celular, en los miocitos, y otros neurohormonales. Ya se ha
los miocitos exhaustos comienzan a morir y la hipertrofia
comentado anteriormente que tanto la A-II como la NAd
inicial no es suficiente para compensar el aumento de las deeran capaces de inducir hipertrofia ventricular. Existen ademandas. Se llega as a la segunda fase, la de dilatacin venms factores para y autocrinos como las endotelinas, el factricular. Sea cual sea el remodelado inicial, en la fase final de
tor de necrosis tumoral alfa (TNF-) o caquectina, el factor
remodelado se produce una dilatacin ventricular por prde crecimiento tisular beta (TGF-), que son tambin capadida de unidades contrctiles. Con la expansin de la cmaces de inducir la hipertrofia de las miofibrillas cardacas. El
ra cardaca el radio se incrementa y el grosor disminuye y
resultado es un crecimiento de la masa ventricular que inpor tanto la tensin parietal aumenta dramticamente. Con
tenta adaptarse a los nuevos requerimientos en la tensin pael aumento de la tensin, tambin se dispara el consumo de
rietal.
oxgeno. En esta fase la contractilidad se deprime an ms
La hipertrofia ventricular no es el nico mecanismo de
rpidamente por la prdida de miocitos y por el aumento de
remodelado. El miocardio est integrado por tres compolas demandas.
nentes: los miocitos, la matriz extracelular y la microvasculaTanto en corazones insuficientes como en situaciones fitura. Cambios en la composicin de la matriz extracelular y
siolgicas, la hipertrofia miocrdica se desarrolla para manla sustitucin de miocitos por otras clulas no contrctiles
tener constante la tensin parietal. sta es una de las princi2288
Medicine 2005; 9(35): 2279-2290
20
01 Actualizacin 2279-90 14/6/05 17:15 Pgina 2289
Documento descargado de http://www.doyma.es el 14/08/2007. Copia para uso personal, se prohbe la transmisin de este documento por cualquier medio o formato.
INSUFICIENCIA CARDACA: CONCEPTO, EPIDEMIOLOGA, CLASIFICACIN, ETIOLOGA Y FISIOPATOLOGA
son tambin modificaciones que se observan en los casos de
remodelado maladaptativo tpico de la IC. El ejemplo mejor estudiado es el remodelado que se produce tras un IAM.
La prdida inicial de fibras activa las seales de reparacin
tisular. Ya en las primeras horas, se puede observar una infiltracin de neutrfilos y macrfagos que producen una
respuesta inflamatoria. Los miocitos muertos son retirados
y la matriz extracelular degradada. Durante esta fase inicial,
se produce lo que se ha llamado la fase de expansin del infarto, en la que se observa muerte celular adicional debida
a dos mecanismos: a) la necrosis de los miocitos que se encuentran en el rea del infarto y que son atacados por las
proteasas del infiltrado inflamatorio, y b) otros miocitos
mueren al iniciar procesos de apoptosis (muerte celular
programada, que consume energa), bien porque han sufrido daos que hacen inviable su supervivencia o bien porque
se encuentran en reas de penumbra isqumica en las que
el aporte de nutrientes es insuficiente para mantener activos los sistemas vitales de la clula. El resultado final es que
el rea inicialmente afectada por el infarto puede duplicarse y lo que antes era tejido contrctil es sustituido ahora por
fibroblastos y tejido colgeno que constituyen una cicatriz
inerte. La cmara cardaca se dilata, aumentando el estrs
parietal y por tanto induciendo hipertrofia de los miocitos
sanos. Asimismo, la prdida de masa celular provoca una
cada inicial en el gasto cardaco, lo que activar el SNAA y
el SRAA, que inducen a corto plazo hipertrofia, pero que a
largo plazo producirn toxicidad directa y apoptosis de los
miocitos sanos. No debemos olvidar adems, que la hipertrofia inducida por estos sistemas es maladaptativa y en ella
se observan miocitos inmaduros que expresan protenas
embrionarias, apareciendo lo que se ha dado en llamar el
retorno a un patrn gnico fetal. Finalmente el incremento de los requerimientos sobre las clulas supervivientes las
somete a un estrs superior al que estn programadas para
soportar. Sus sistemas enzimticos y sus fibras contrctiles,
crnicamente sobrecargadas, sufren un desgaste acelerado
y terminan por claudicar. El resultado es una espiral en la
que cada vez son menos las clulas sanas que compensan la
masa celular perdida.
Se conocen los cambios sufridos por las clulas en las
distintas fases de la compensacin cardaca. Inicialmente,
tras el evento ndice, la clula sufre un proceso de hipertrofia acelerado por el que se sintetizan nuevas miofibrillas,
no siempre maduras. Existe un incremento en la relacin
de mitocondrias respecto a la cantidad de fibrillas creadas.
En una fase posterior, la cantidad de miofibrillas supera
al de mitocondrias y la gnesis de energa empieza a comprometerse. En el estadio final, existe una desproporcin insostenible entre miofibrillas y mitocondrias. La
produccin de energa no slo compromete la contractilidad sino tambin la vida de la clula, que termina por
morir26.
El remodelado ventricular, por tanto, es un mecanismo
de compensacin ms tardo, igualmente eficaz y que produce profundos cambios en la cmara cardaca. Como todos los
fenmenos de compensacin vistos anteriormente, inicialmente ayuda al sobrevivir al individuo, pero a largo plazo lo
condenar a pagar un elevadsimo precio.
21
Bibliografa
Importante Muy importante
Metaanlisis
Ensayo clnico controlado
Epidemiologa
1. Branwald E, Colucci WS, Grossman W. Clinical aspects of heart failure.
Chap.15. En: Branwald E, editor. Heart disease. A text book of Cardiovascular Medicine. 5th edition.Vol 1. Philadelphia: W.B. Saunders; 1997.
p. 445.
Pulpon LA. La epidemia de insuficiencia cardaca: son todos los que
estn y estn todos los que son? Rev Esp Cardiol. 2002;55:211-4.
Ho KK, Pinsky JL, Kannel WB, Levy D. The epidemiology of
heart failure: the Framingham Study. J Am Coll Cardiol. 1993;22:
6A-13.
Remme J, Swedberg K. Guidelines of the European Society of Cardiology for the diagnosis and treatment of chronic heart failure. Eur Heart
J. 2001;22:1527-60.
European Study Group on Diastolic Heart Failure: how to diagnose diastolic heart failure. Eur Heart J. 1998;19:1003.
Boix MR, Almazan IJ, Medrano Albero MJ. Heart failure mortality in
Spain, 1977-1998. Rev Esp Cardiol. 2002;55:219-26.
The SOLVD investigators. Effect of enalapril on mortality and the development of heart failure in asympotmatic patients with reduced left ventricular ejection fraction. N Engl J Med. 1992;685-91.
McDonagh TA, Morrison CE, Lawrence A, Ford I, Tunstall-Pedoe H,
mcMurray JJ, et al. Symptomatic and asymptomatic left ventricular systolic dysfunction in an urban population. Lancet. 1997;350:829-33.
Davies M, Hobbs F, Davis R, Kenkre J, Roalfe AK, Hare R, et al. Prevalence of left-ventricular systolic dysfunction and heart failure in the
Echocardiographic Heart of England Screening study: a population based study. Lancet. 2001;358:439-44.
Cortina A, Reguero J, Segovia E, Rodrguez Lambert JL, Cortina R,
Arias JC, et al. Prevalence of heart failure in Asturias (a region in the
north of Spain). Am J Cardiol. 2001;87:1417-9.
Rodrguez-Artalejo F, Banegas B Jr, Guallar-Castillon P. Epidemiology
of heart failure. Rev Esp Cardiol. 2004;57:163-70.
Hellermann JP, Goraya TY, Jacobsen SJ, Weston SA, Reeder GS, Gersh
BJ, et al. Incidence of heart failure after myocardial infarction: is it changing over time? Am J Epidemiol. 2003;157:1101-7.
Mosterd A, Cost B, Hoes AW, de Bruijne MC, Deckers JW, Hofman A,
et al. The prognosis of heart failure in the general population: The Rotterdam Study. Eur Heart J. 2001;22:1318-27.
Hoppe BL, Hermann DD. Sex differences in the causes and natural history of heart failure. Curr Cardiol Rep. 2003;5:193-9.
Johnstone D, Limacher M, Rousseau MF. Clinical characteristics of patients in studies of left ventricular dysfunction. Am J Cardiol. 1992;894900.
Kannel WB. Epidemiology aspects of heart failure. Cardiol Clin.
1989;1-9.
Rathore SS, Wang Y, Krumholz HM. Sex-based differences in the effect
of digoxin for the treatment of heart failure. N Engl J Med. 2002;347:
1403-11.
Haldeman GA, Croft JB, Giles WH, Rashidee A. Hospitalization of patients with heart failure: National Hospital Discharge Survey 1985-1995.
Am Heart J. 1999;137:352-60.
Levy D, Kenchaiah S, Larson MG, Benjamin EJ, Kupka MJ, Ho KK, et
al. Long-term trends in the incidence of and survival with heart failure.
N Engl J Med. 2002;347:1397-402.
Boulay F, Berthier F, Sisteron O. Seasonal variation in chronic heart failure hospitalizations and mortality in France. Circulation. 1999;280.
Hunt SA, Backer DW, Chin MH, Cinquegrani MP, Feldman AM,
Francis GS, et al. ACC/AHA Guidelines for the Evaluation and Management of Chronic Heart Failure in the Adult: a report of the American College of Cardiology/American Heart Association Task Force on
practice Guidelines (Committee to revise the 1995 Guidelines for the
Evaluation and Management of Heart Failure). Circulation. 2001;104:
2996-3007.
Galbreath AD, Krasuski RA, Smith B, Satjduhar KC, Kwan MD, Ellis R,
et al. Long-term healthcareand cost outcomes of disease management in
a large, randomized, community-based population with heart failure.
Circulation. 2004;110:3518-26.
McMurray JJ, Stwart S. Epidemiology, eatiology, and prognosis of heart
failure. Heart. 2000;596-602.
Gheorghiade M, Bonow RO. Chronic heart failure in the United States:
a manifestation of coronary artery disease. Circulation. 1998;282-9.
Opasich C, Rapezzi C, Lucci D, Gorini M, Pozzar F, Zanelli E, et al.
Precipitating factors and decision-making processes of short-term worsening heart failure despite optimal treatment (from the IN-CHF Registry). Am J Cardiol. 2001;88:382-7.
2.
3.
4.
5.
6.
7.
8.
9.
10.
11.
12.
13.
14.
15.
16.
17.
18.
19.
20.
21.
22.
23.
24.
25.
Medicine 2005; 9(35): 2279-2290
2289
01 Actualizacin 2279-90 14/6/05 17:15 Pgina 2290
Documento descargado de http://www.doyma.es el 14/08/2007. Copia para uso personal, se prohbe la transmisin de este documento por cualquier medio o formato.
ENFERMEDADES CARDIOVASCULARES (I)
26. Colucci WS, Braunwald E. Pathophysiology of heart failure.
En: Braunwald E, editor. Heart disease: a textbook of Cardiovascular Medicine. Philadelphia: Saunders W.B.; 1997. p. 394-415.
27. Vidal B, Roig E, Perez-Villa F, Orus J, Prez J, Jimnez V, et al. Prog
nostic value of cytokines and neurohormones in severe heart failure. Rev
Esp Cardiol. 2002;55:481-6.
28. Jackson G, Gibbs CR, Davies MK, Lip GY. ABC of heart failure. Pat
hophysiology. BMJ. 2000;320:167-70.
29. Sutton M, Sharpe N. Left ventricular remodeling after myocardial in
farction. Pathophysiology and therapy. Circulation. 2000;2981-8.
30.
Udelson JE, Patten RD, Konstam MA. New concepts in post-infarction
ventricular
remodeling. Rev Cardiovasc Med. 2003;S3-12.
2290
Medicine 2005; 9(35): 2279-2290
Вам также может понравиться
- ANTIPALIDICOT1C3Документ5 страницANTIPALIDICOT1C3LINA MARIA AVILA PEÑAОценок пока нет
- AnestesiologiaДокумент34 страницыAnestesiologiaarlink84Оценок пока нет
- Protocolo Terapia OcupacionalДокумент11 страницProtocolo Terapia OcupacionalRocio Jaramillo AlvarezОценок пока нет
- Cannabis Medicinal InternetДокумент73 страницыCannabis Medicinal Internetarecrosario100% (4)
- Rciu SelectivoДокумент17 страницRciu SelectivoAlfredito Peñarredonda FdzОценок пока нет
- Manuel de SindromesДокумент102 страницыManuel de SindromesAmneryss AndreaОценок пока нет
- Perfil HepaticoДокумент22 страницыPerfil HepaticoRichard David Aguirre Barrientos100% (2)
- SDR TIPO I Y II: ENFERMEDAD DE MEMBRANA HIALINA Y SÍNDROME DE ASPIRACIÓN MECONIALДокумент47 страницSDR TIPO I Y II: ENFERMEDAD DE MEMBRANA HIALINA Y SÍNDROME DE ASPIRACIÓN MECONIALJose SantanaОценок пока нет
- Norma de Diagnostico y Tratamiento de OftalmologiaДокумент169 страницNorma de Diagnostico y Tratamiento de OftalmologiafelipeОценок пока нет
- Sd. Munchausen Por PoderesДокумент6 страницSd. Munchausen Por Poderespsychforall100% (1)
- GPC 548 Asma Infantil Osteba Compl CaducДокумент162 страницыGPC 548 Asma Infantil Osteba Compl CaducTatty GrzОценок пока нет
- EL ABORTO en LAS ADOLESENTES Presentacion Entornos VirtualesДокумент10 страницEL ABORTO en LAS ADOLESENTES Presentacion Entornos VirtualesWilliam VilleОценок пока нет
- MolaДокумент7 страницMolaBeatriz Carolina VásquezОценок пока нет
- Informe Psicologico ClinicoДокумент6 страницInforme Psicologico Clinicoyuly mar toro arceОценок пока нет
- Parásitos y amebiasisДокумент2 страницыParásitos y amebiasisliliana delgadoОценок пока нет
- Cuadro Sinóptico - Primer Respondiente y Evaluación de La EscenaДокумент1 страницаCuadro Sinóptico - Primer Respondiente y Evaluación de La EscenaBrito Chan Dania Irazet100% (1)
- Lista de Enfermedades de Notificacin ObligatoriaДокумент5 страницLista de Enfermedades de Notificacin ObligatoriaMaría Del Carmen CastroОценок пока нет
- Aplicacion Del Codigo de Bioetica para El Personal de Salud en MexicoДокумент18 страницAplicacion Del Codigo de Bioetica para El Personal de Salud en MexicoJames Smith75% (4)
- Manual Historia Clinica MSP 31 103Документ73 страницыManual Historia Clinica MSP 31 103cristina pazosОценок пока нет
- NeumoniaДокумент19 страницNeumoniaBrandon RyanОценок пока нет
- Cotización Ambulancia TSPP evento 04 abril 2024Документ1 страницаCotización Ambulancia TSPP evento 04 abril 2024Arely de Jesús Villalobos MontoyaОценок пока нет
- 7 Quirofano-1Документ3 страницы7 Quirofano-1Vianca TorrezОценок пока нет
- Caso Clínico.Документ4 страницыCaso Clínico.TonyОценок пока нет
- RAU1153Документ3 страницыRAU1153MANUELОценок пока нет
- Documentos necesarios para tu farmaciaДокумент66 страницDocumentos necesarios para tu farmaciaRocio Méndez FrancoОценок пока нет
- INSULINOMAДокумент6 страницINSULINOMAPedro Alejandro Aparcana MendozaОценок пока нет
- Síndrome CerebelosoДокумент4 страницыSíndrome CerebelosoDenis VernazaОценок пока нет
- IrasДокумент2 страницыIrasNaomi MartinezОценок пока нет
- Procedimiento de Derivacion de PacientesДокумент4 страницыProcedimiento de Derivacion de PacientesmruizmontesОценок пока нет
- Discapacidad: InstructivoДокумент30 страницDiscapacidad: InstructivoGisele LuengasОценок пока нет