Академический Документы
Профессиональный Документы
Культура Документы
Metales Representativos
Загружено:
Felipe Zantoz0%(1)0% нашли этот документ полезным (1 голос)
5K просмотров3 страницыGY
Оригинальное название
Metales representativos
Авторское право
© © All Rights Reserved
Доступные форматы
DOCX, PDF, TXT или читайте онлайн в Scribd
Поделиться этим документом
Поделиться или встроить документ
Этот документ был вам полезен?
Это неприемлемый материал?
Пожаловаться на этот документGY
Авторское право:
© All Rights Reserved
Доступные форматы
Скачайте в формате DOCX, PDF, TXT или читайте онлайн в Scribd
0%(1)0% нашли этот документ полезным (1 голос)
5K просмотров3 страницыMetales Representativos
Загружено:
Felipe ZantozGY
Авторское право:
© All Rights Reserved
Доступные форматы
Скачайте в формате DOCX, PDF, TXT или читайте онлайн в Scribd
Вы находитесь на странице: 1из 3
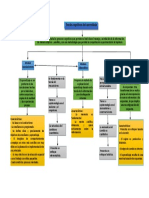
Metales representativos
En qumica y fsica atmicas, los elementos representativos o elementos de los
grupos principales1 son elementos qumicos de los grupos largos de la tabla
peridica, encabezados por los elementos hidrgeno, berilio, boro, carbono,
nitrgeno, oxgeno, flor y helio, tal como aparecen en la tabla peridica de los
elementos. Se caracterizan por presentar configuraciones electrnicas "externas"1
en su estado fundamental que van desde ns1 hasta ns2np6, a diferencia de los
elementos de transicin y de los elementos de transicin interna.
Los elementos representativos son los elementos de los grupos 1 y 2 (bloque s), y
de los grupos de 13 a 18 (bloque p).2 Hasta hace unos aos, estos grupos se
identificaban con nmeros romanos del I al VII con la letra A.3 Los elementos del
grupo 12 son generalmente considerados como metales de transicin, sin
embargo, el zinc (Zn), el cadmio (Cd), y el mercurio (Hg) comparten algunas
propiedades de ambos grupos, y algunos cientficos creen que deben ser incluidos
como elementos representativos o elementos de los grupos principales.4
Metal de transicin
Los elementos de transicin son aquellos elementos qumicos que estn situados
en la parte central del sistema peridico, en el bloque d, cuya principal
caracterstica es la inclusin en su configuracin electrnica del orbital d,
parcialmente lleno de electrones. Esta definicin se puede ampliar considerando
como elementos de transicin a aquellos que poseen electrones alojados en el
orbital d, esto incluira a zinc, cadmio, y mercurio. La IUPAC define un metal de
transicin como "un elemento cuyo tomo tiene una subcapa d incompleta o que
puede dar lugar a cationes".1
Son metales de transicin, ya que tienen una configuracin d10. Solo se forman
unas pocas especies transitorias de estos elementos que dan lugar a iones con
una subcapa d parcialmente completa. Por ejemplo mercurio (I) solo se encuentra
como Hg22+, el cual no forma un ion aislado con una subcapa parcialmente llena,
por lo que los tres elementos son inconsistentes con la definicin anterior.2 Estos
forman iones con estado de oxidacin 2+, pero conservan la configuracin 4d10.
El elemento 112 podra tambin ser excluido aunque sus propiedades de
oxidacin no son observadas debido a su naturaleza radioactiva. Esta definicin
corresponde a los grupos 3 a 11 de la tabla peridica.
No metal
Se denomina no metales, a los elementos qumicos opuestos a los metales pues
sus caractersticas son totalmente diferentes. Los no metales, excepto el
hidrgeno, estn situados en la tabla peridica de los elementos en el bloque p.
Los elementos de este bloque son no-metales, excepto los metaloides (B, Si, Ge,
As, Sb, Te), todos los gases nobles (He, Ne, Ar, Kr, Xe, Rn), y algunos metales (Al,
Ga, In, Tl, Sn, Pb).
Tienden a formar aniones u oxianiones en solucin acuosa, y forma xidos cidos
con los metales, ganando electrones, o enlaces covalentes , con otros no metales,
compartiendo electrones.
En su mayora existen en condiciones ordinarias como molculas diatmicas. En
esta lista estn incluidos cinco gases (H2, N2, O2, F2 y Cl2), un lquido (Br2) y un
slido voltil (I2).
Gases nobles
Los gases nobles son un grupo de elementos qumicos con propiedades muy
similares: por ejemplo, bajo condiciones normales, son gases monoatmicos
inodoros, incoloros y presentan una reactividad qumica muy baja. Se sitan en el
grupo 18 (VIIIA) 1 de la tabla peridica (anteriormente llamado grupo 0). Los siete
gases son helio (He), nen (Ne), argn (Ar), kriptn (Kr), xenn (Xe), el radiactivo
radn (Rn) y ununoctio (Uuo).
Las propiedades de los gases nobles pueden ser explicadas por las teoras
modernas de la estructura atmica: a su capa electrnica de electrones valentes
se la considera completa, dndoles poca tendencia a participar en reacciones
qumicas, por lo que solo unos pocos compuestos de gases nobles han sido
preparados hasta 2008. El xenn reacciona de manera espontnea con el flor
(debido a la alta electronegatividad de ste), y a partir de los compuestos
resultantes se han alcanzado otros. Tambin se han aislado algunos compuestos
con kriptn. Los puntos de fusin y de ebullicin de cada gas noble estn muy
prximos, difiriendo en menos de 10 C; consecuentemente, solo son lquidos en
un rango muy pequeo de temperaturas.
Lantnidos
Los lantnidos (o lantanoides como la IUPAC recomienda) son un grupo de
elementos que forman parte del periodo 6 de la tabla peridica. Estos elementos
son llamados tierras raras debido a que se encuentran en forma de xidos, y
tambin, junto con los actnidos, forman los elementos de transicin interna.
El nombre procede del elemento qumico lantano, que suele incluirse dentro de
este grupo, dando un total de 15 elementos, desde el de nmero atmico 57 (el
lantano) al 71 (el lutecio). Aunque se suela incluir en este grupo, el lantano no
tiene electrones ocupando ningn orbital f, mientras que los catorce siguientes
elementos tienen este orbital 4f parcial o totalmente lleno (vase configuracin
electrnica).
Estos elementos son qumicamente bastante parecidos entre s puesto que los
electrones situados en orbitales f son poco importantes en los enlaces que se
forman, en comparacin con los p y d. Tambin son bastante parecidos a los
lantnidos los elementos itrio y escandio, debido a que tienen un radio similar y, al
igual que los lantnidos, su estado de oxidacin ms importante es el +3. ste es
el estado de oxidacin ms importante de los lantnidos, pero tambin presentan
el estado de oxidacin +2 y +4.
Actinido
Los actnidos (o actinoides como la IUPAC recomienda) son un grupo de
elementos que forman parte del periodo 7 de la tabla peridica perteneciendo a las
tierras raras. Estos elementos, junto con los lantnidos, son llamados elementos
de transicin interna. El nombre procede del elemento qumico actinio, que suele
incluirse dentro de este grupo, que da un total de 15 elementos, desde el de
nmero atmico 89 (el actinio) al 103 (lawrencio).
Estos elementos presentan caractersticas parecidas entre s. Los de mayor
nmero atmico, no se encuentran en la naturaleza y tienen tiempos de vida
media cortos; todos sus istopos son radiactivos.
En la tabla peridica, estos elementos se suelen situar debajo del resto, junto con
los lantnidos, dando una tabla ms compacta que si se colocaran entre los
elementos del bloque s y los del bloque d, aunque en algunas tablas peridicas s
que se pueden ver situados entre estos bloques, dando una tabla mucho ms
ancha.
Вам также может понравиться
- Formato Cuadro Comparativo Actividad N°5Документ8 страницFormato Cuadro Comparativo Actividad N°5KlderonLemus100% (1)
- SemiconductoresДокумент52 страницыSemiconductoresSohiky SohikyyОценок пока нет
- Propiedades de Las Aleaciones y Metales Ferrosos y No FerrososДокумент4 страницыPropiedades de Las Aleaciones y Metales Ferrosos y No FerrososAswlord AlexОценок пока нет
- Clasificación de Las Reacciones QuimicasДокумент2 страницыClasificación de Las Reacciones QuimicasEmma Margarita Torres MendezОценок пока нет
- Propiedades Físicas y Químicas de Los MaterialesДокумент20 страницPropiedades Físicas y Químicas de Los MaterialesValentina TB100% (1)
- Procesos de manufactura de materialesДокумент36 страницProcesos de manufactura de materialesErick Adame100% (1)
- Enlaces Químicos y Estructuras CristalinasДокумент26 страницEnlaces Químicos y Estructuras CristalinasAlejandro TeveraОценок пока нет
- 1.propiedad de Los MaterialesДокумент277 страниц1.propiedad de Los MaterialesFernanda Barrera100% (1)
- Materiales Ferrosos Trabajo ManufacturaДокумент21 страницаMateriales Ferrosos Trabajo Manufacturaadrian50% (2)
- Clasificación y Selección de Aceros Según SaeДокумент3 страницыClasificación y Selección de Aceros Según SaeAnonymous msqTwtjplОценок пока нет
- Estructura AmorfaДокумент7 страницEstructura AmorfaAlejandra ManceraОценок пока нет
- 2a - Componentes RectangularesДокумент14 страниц2a - Componentes RectangularesMarzo ZlarciОценок пока нет
- Ensayo de Materiales: Defectos e ImperfeccionesДокумент21 страницаEnsayo de Materiales: Defectos e ImperfeccionesAlexis100% (1)
- Estudio General de Los Elementos. No Metales IiДокумент29 страницEstudio General de Los Elementos. No Metales Iifroz90% (1)
- AlotropiaДокумент4 страницыAlotropiaAxl PalominoОценок пока нет
- Resumen Teoría Cuántica y Estructura AtómicaДокумент6 страницResumen Teoría Cuántica y Estructura AtómicaCarlos YaelОценок пока нет
- Clasificar Sustancias Según Corresponda en Elementos, Compuestos y MezclasДокумент3 страницыClasificar Sustancias Según Corresponda en Elementos, Compuestos y MezclasmanuelОценок пока нет
- Punto de Fusion y EbullicionДокумент14 страницPunto de Fusion y Ebullicionjeampol100% (1)
- Estructuras de LewisДокумент4 страницыEstructuras de LewisUrdaneta Rogelio100% (1)
- RadiactividadДокумент6 страницRadiactividadFabian AdamexОценок пока нет
- Enlaces iónico y covalenteДокумент13 страницEnlaces iónico y covalenteDavid Conza TorresОценок пока нет
- Clase 4 GranoДокумент34 страницыClase 4 GranoANDERSON0% (1)
- Factores Que Afectan La ResistividadДокумент8 страницFactores Que Afectan La ResistividadjonathanОценок пока нет
- 2.19. Metalurgia. Principales Metales y Aleaciones Utilizados en La Industria - Enlaces Químicos y El Estado Sólido (Cristalino)Документ4 страницы2.19. Metalurgia. Principales Metales y Aleaciones Utilizados en La Industria - Enlaces Químicos y El Estado Sólido (Cristalino)Fernando Tomás Martínez MartínezОценок пока нет
- Estructura Cristalina PaperДокумент14 страницEstructura Cristalina PaperALEXANDER CADENILLAS DIAZОценок пока нет
- Calculo IntegralДокумент6 страницCalculo IntegralRuben Ruben100% (1)
- Estados de Agregación de La MateriaДокумент2 страницыEstados de Agregación de La MateriaRicardo BautistaОценок пока нет
- AleacionesДокумент4 страницыAleacionesChristian Dioses LeónОценок пока нет
- Practica No 4Документ7 страницPractica No 4Jesus Enrique Martinez GarciaОценок пока нет
- 11-Tipos de Aleaciones MetálicasДокумент44 страницы11-Tipos de Aleaciones MetálicasAngél VargasОценок пока нет
- El Hierro y Sus AleacionesДокумент12 страницEl Hierro y Sus Aleacionesdalila8697Оценок пока нет
- Procesos de Manufactura Del MetalДокумент69 страницProcesos de Manufactura Del MetalPaul Huerta100% (1)
- Técnicas básicas de laboratorioДокумент13 страницTécnicas básicas de laboratorioIsraelОценок пока нет
- Soluciones SòlidasДокумент36 страницSoluciones SòlidasLuis Miguel LluenОценок пока нет
- Propiedades mecánicas y físicas materialesДокумент19 страницPropiedades mecánicas y físicas materialesSteven RamosОценок пока нет
- 1.1 Definición de Un Vector en El Plano y en El EspacioДокумент27 страниц1.1 Definición de Un Vector en El Plano y en El EspacioZain Simons100% (1)
- Propiedades Del HierroДокумент3 страницыPropiedades Del HierroTorres EimerОценок пока нет
- Mecanismos de Endurecimiento Solucion Solida N.Castillo PDFДокумент22 страницыMecanismos de Endurecimiento Solucion Solida N.Castillo PDFNicole Margarita Castillo Aguilar [ Geologia ]100% (1)
- Cargas Electricas y Ley de CoulombДокумент4 страницыCargas Electricas y Ley de CoulombJose CotaОценок пока нет
- Sistema TetragonalДокумент23 страницыSistema TetragonalChristian Isla ZegarraОценок пока нет
- Ley de Lenz, Faraday y WattДокумент7 страницLey de Lenz, Faraday y WattFRANCISCO MANUEL RODRIGUEZ RUBIOОценок пока нет
- Marco TeóricoДокумент4 страницыMarco TeóricoKevin Chavez ChavezОценок пока нет
- Resumen Materiales PurosДокумент7 страницResumen Materiales PurosHector Hernandez RicarteОценок пока нет
- Presentación Teoria de Las AleacionesДокумент68 страницPresentación Teoria de Las AleacionesStiven SanabriaОценок пока нет
- Puntos, Direcciones y Planos en La Celda UnitariaДокумент7 страницPuntos, Direcciones y Planos en La Celda UnitariaVeronica GuerreroОценок пока нет
- ConfiguracionesEstructuralesДокумент12 страницConfiguracionesEstructuralesManuel OjedaОценок пока нет
- Mecanismos de DeformaciónДокумент9 страницMecanismos de DeformaciónAlejoОценок пока нет
- Clasificacion y Seleccion de AcerosДокумент19 страницClasificacion y Seleccion de AcerosManuel Ojeda100% (1)
- Practica Estructuras CristalinasДокумент10 страницPractica Estructuras CristalinasDaniel MateoОценок пока нет
- Unidad 8. - Estructuras.Документ5 страницUnidad 8. - Estructuras.Alex Garcia UlloaОценок пока нет
- Propiedades térmicas de los materiales: capacidad calorífica, dilatación térmica y conductividadДокумент6 страницPropiedades térmicas de los materiales: capacidad calorífica, dilatación térmica y conductividadcarlys lopezОценок пока нет
- Conceptos Básicos de Los Enlaces QuímicosДокумент39 страницConceptos Básicos de Los Enlaces QuímicosAlexander Rojas67% (3)
- Practica de Laboratorio #2Документ3 страницыPractica de Laboratorio #2Mubara Kid100% (1)
- Clasificación de Los Procesos de FabricaciónДокумент12 страницClasificación de Los Procesos de Fabricaciónairam29_degil0% (1)
- Ensayo SemiconductoresДокумент16 страницEnsayo SemiconductoresenriqueОценок пока нет
- Materiales amorfos: características y formaciónДокумент2 страницыMateriales amorfos: características y formaciónFelipe Silva LuceroОценок пока нет
- Teoría atómica: Descubrimiento del átomo y sus partículasДокумент6 страницTeoría atómica: Descubrimiento del átomo y sus partículasAnonymous RCNlzLY9zTОценок пока нет
- Ensayo de La Clasificacion de Los Elementos de La Tablaperiodica ModernaДокумент18 страницEnsayo de La Clasificacion de Los Elementos de La Tablaperiodica ModernaJoel AzaelОценок пока нет
- Metales y Metaloides RepresentativosДокумент12 страницMetales y Metaloides Representativos5latanОценок пока нет
- Magni TudДокумент4 страницыMagni TudFelipe ZantozОценок пока нет
- Señor EsquipulasДокумент4 страницыSeñor EsquipulasFelipe ZantozОценок пока нет
- Estados Del AguaДокумент2 страницыEstados Del AguaFelipe ZantozОценок пока нет
- IsotoposДокумент3 страницыIsotoposFelipe ZantozОценок пока нет
- Gabinete de Gobierno de Guatemala 2014Документ9 страницGabinete de Gobierno de Guatemala 2014Felipe ZantozОценок пока нет
- Día Mundial de La PoblaciónДокумент2 страницыDía Mundial de La PoblaciónFelipe ZantozОценок пока нет
- Trabajo InfantilДокумент2 страницыTrabajo InfantilFelipe ZantozОценок пока нет
- BarrocoДокумент4 страницыBarrocoFelipe ZantozОценок пока нет
- XincaДокумент1 страницаXincaFelipe ZantozОценок пока нет
- Valor Expresivo de La Line2Документ4 страницыValor Expresivo de La Line2Felipe ZantozОценок пока нет
- EMETRAДокумент1 страницаEMETRAFelipe ZantozОценок пока нет
- Adición de PolinomiosДокумент8 страницAdición de PolinomiosFelipe Zantoz100% (2)
- EuropaДокумент14 страницEuropaFelipe ZantozОценок пока нет
- José MojicaДокумент3 страницыJosé MojicaFelipe ZantozОценок пока нет
- Salsa 1Документ3 страницыSalsa 1Felipe ZantozОценок пока нет
- Palabras relacionadas con el sector primarioДокумент3 страницыPalabras relacionadas con el sector primarioFelipe ZantozОценок пока нет
- IndependenciaLatinoaméricaДокумент7 страницIndependenciaLatinoaméricaFelipe ZantozОценок пока нет
- Nomenclatura QuímicaДокумент2 страницыNomenclatura QuímicaFelipe ZantozОценок пока нет
- Ventajas de La Leche MaternaДокумент1 страницаVentajas de La Leche MaternaFelipe ZantozОценок пока нет
- ArmoníaДокумент1 страницаArmoníaFelipe ZantozОценок пока нет
- La Reforma EducativaДокумент6 страницLa Reforma EducativaFelipe ZantozОценок пока нет
- SalsaДокумент6 страницSalsaFelipe ZantozОценок пока нет
- REGGAETO1Документ2 страницыREGGAETO1Felipe ZantozОценок пока нет
- EstadoДокумент10 страницEstadoFelipe ZantozОценок пока нет
- BachataДокумент3 страницыBachataFelipe ZantozОценок пока нет
- HistologíaДокумент8 страницHistologíaFelipe ZantozОценок пока нет
- SustantivosДокумент2 страницыSustantivosFelipe ZantozОценок пока нет
- Himno Nacional ArgentinoДокумент7 страницHimno Nacional ArgentinoFelipe ZantozОценок пока нет
- FutbolДокумент5 страницFutbolFelipe ZantozОценок пока нет
- DIS96 LookДокумент49 страницDIS96 LookAnderson ThiagoОценок пока нет
- Lección Evaluativa Unidad 1Документ8 страницLección Evaluativa Unidad 1monica mendozaОценок пока нет
- Teorías CognitivasДокумент1 страницаTeorías CognitivasJonha GuevaraОценок пока нет
- Diagrama Unifilar de Una Instalacion Solar FotovoltaicaДокумент1 страницаDiagrama Unifilar de Una Instalacion Solar FotovoltaicaJohn Jairo LatacumbaОценок пока нет
- Proyecto 18Документ6 страницProyecto 18amariscme11Оценок пока нет
- Mejoramiento y Ampliacion Integral Del Sistema de Agua Potable y Alcantarillado de JkaДокумент96 страницMejoramiento y Ampliacion Integral Del Sistema de Agua Potable y Alcantarillado de Jkaclaudifc2614Оценок пока нет
- Unidad - N°1 - DSM - Parte 1Документ99 страницUnidad - N°1 - DSM - Parte 1Alexis SaraviaОценок пока нет
- Solución Tarea 5 UNAM Posgrado Ciencias FísicasДокумент2 страницыSolución Tarea 5 UNAM Posgrado Ciencias FísicasLUZ ELENA TISCAREÑO MONTOYAОценок пока нет
- PTS-001 Trabajo en Altura o Distinto NivelДокумент14 страницPTS-001 Trabajo en Altura o Distinto NivelAndreaОценок пока нет
- Angulo cohesion El TamboДокумент2 страницыAngulo cohesion El TambodannyОценок пока нет
- Ponte en sus zapatos: la importancia de la empatía y la compasiónДокумент7 страницPonte en sus zapatos: la importancia de la empatía y la compasiónFernando RodriguezОценок пока нет
- Análisis de Riesgos Clase 1 IntroducciónДокумент23 страницыAnálisis de Riesgos Clase 1 IntroducciónJulioIgnacioCereyОценок пока нет
- Chinos Coreanos JaponesesДокумент23 страницыChinos Coreanos Japonesesjulia_gpОценок пока нет
- Ensayo Confort AmbientalДокумент22 страницыEnsayo Confort AmbientalPaula Huiqui NavarreteОценок пока нет
- Matemática aplicada a los negocios: optimización y diferencialДокумент14 страницMatemática aplicada a los negocios: optimización y diferencialJuan ChrОценок пока нет
- Tarea ACS - 04.11.2022Документ4 страницыTarea ACS - 04.11.2022ARTURO CASTAÑEDA VARGASОценок пока нет
- Six Sigma Polleria La EspadaДокумент15 страницSix Sigma Polleria La EspadaYemis Alva Palacios50% (2)
- Componentes de Una Planta Termoelectrica-2Документ69 страницComponentes de Una Planta Termoelectrica-2SAMUEL JOSE MEJIA PINTOОценок пока нет
- Calculo Del PV2 Estado 2 Zona 4Документ17 страницCalculo Del PV2 Estado 2 Zona 4Jose MedinaОценок пока нет
- Guia Análisis UrbanoДокумент3 страницыGuia Análisis Urbanocinthia rodriguezОценок пока нет
- Grupo 8 - Fase 3Документ26 страницGrupo 8 - Fase 3EIGNY GARZAОценок пока нет
- PuerperioДокумент28 страницPuerperioAbril Morales100% (1)
- Producción y CostosДокумент6 страницProducción y CostosALEОценок пока нет
- Consentimiento Informado TatuajeДокумент2 страницыConsentimiento Informado Tatuajepedro ogazОценок пока нет
- 30 Años de Cine Experimental - Hans Richter PDFДокумент3 страницы30 Años de Cine Experimental - Hans Richter PDFTomy OnetoОценок пока нет
- Anexo 37 Clasificacion ArancelariaДокумент10 страницAnexo 37 Clasificacion ArancelariaJosé Fabio LouОценок пока нет
- CánticosAlabanzaДокумент3 страницыCánticosAlabanzaCoro Sendero RealОценок пока нет
- Nutritivo Agar: Medio de cultivo no selectivoДокумент5 страницNutritivo Agar: Medio de cultivo no selectivopaulaОценок пока нет
- N 211Документ39 страницN 211Hideo KojimaОценок пока нет
- Cardiopatia IsquemicaДокумент85 страницCardiopatia IsquemicaFily AranoОценок пока нет