Академический Документы
Профессиональный Документы
Культура Документы
Capítulo 5 Propiedades y Teoria de Los Gases
Загружено:
Mayba MillaresАвторское право
Доступные форматы
Поделиться этим документом
Поделиться или встроить документ
Этот документ был вам полезен?
Это неприемлемый материал?
Пожаловаться на этот документАвторское право:
Доступные форматы
Capítulo 5 Propiedades y Teoria de Los Gases
Загружено:
Mayba MillaresАвторское право:
Доступные форматы
CAPITULO 5 PROPIEDADES Y TEORIA DE LOS GASES
5.1
INRODUCCION
Para entender y predecir el comportamiento volumtrico de los reservorios de gas y
petrleos como funcin de la presin, debemos tener conocimiento de las propiedades
fsicas de los fluidos del reservorio. Estas propiedades de fluidos son normalmente
determinadas por experimentos en laboratorio efectuados en muestras de los fluidos reales
del reservorio. En ausencia de propiedades medidas experimentalmente, es necesario, en
ingeniera petrolera, determinar las propiedades de correlaciones derivadas empricamente.
El objetivo de este captulo es conocer varias de las correlaciones para propiedades fsicas
bien establecidas para los gases naturales.
5.2
GENERALIDADES
El gas se define como un fluido homogneo de baja viscosidad y densidad que no tiene
un volumen definido sino que se expande para llenar completamente el recipiente que lo
contiene. Generalmente el gas natural es una mezcla de gases de hidrocarburos y no
hidrocarburos. Los hidrocarburos gaseosos que normalmente se encuentran en el gas
natural son metano, etano, propano, butano, pentano y pequeas porciones de hexano y
superiores. Los gases no hidrocarburos (o impurezas) incluyen el dixido de carbono, sulfuro
de hidrgeno y nitrgeno.
El conocimiento de las relaciones presin-volumen-temperatura (PVT) y las dems
propiedades fsicas y qumicas de los gases es esencial para resolver problemas en
ingeniera de reservorios del gas natural. Estas propiedades incluyen:
Peso molecular aparente, Ma
Gravedad especfica, g
Factor de compresibilidad, z
Densidad, g
Volumen especfico, V
Coeficiente de compresibilidad isotrmica del gas, cg
Factor volumtrico de formacin del gas, Bg
Factor de expansin del gas, Eg
Viscosidad, g
Estas propiedades del gas pueden obtenerse de medidas directas en laboratorio o por
prediccin de expresiones matemticas generalizadas. Revisaremos las leyes que describen
el comportamiento volumtrico de los gases en trminos de presin y temperatura y
correlaciones matemticas que son ampliamente usadas en la determinacin de las
propiedades fsicas de los gases naturales.
5.3
COMPORTAMIENTO DE LOS GASES IDEALES
La teora cintica de los gases postula que los gases son compuestos de un gran
nmero de partculas llamadas molculas. Para un gas ideal, se asume que el volumen de
estas molculas es insignificante comparado con el volumen total ocupado por el gas.
Tambin se asume que estas molculas no tienen fuerzas atractivas o repulsivas entre ellas,
y que todas las colisiones de las molculas son perfectamente elsticas.
Basado en la teora cintica de los gases anterior, la ecuacin matemtica denominada
ecuacin de estado puede derivarse para expresar la relacin existente entre la presin p, el
volumen V y la temperatura T para una determinada cantidad de moles de gas n. Esta
Ing. Hermas Herrera Callejas
Pgina: 5 - 1
PET204 Ingeniera de Reservorios I
Captulo 5 Propiedades y Teora de los Gases
relacin para gases perfectos se llama la ley de los gases ideales y se expresa
matemticamente por la siguiente ecuacin:
pV = nRT
5.1
donde p = presin absoluta, psia
V = volumen, ft3
T = temperatura absoluta, R
n = numero de moles de gas, lb-mole
R = la constante universal de los gases que, par alas unidades anteriores, tiene el
valor de 10.73 psia ft3/lb-mole R
5.4
EL NMERO DE LIBRAS MOL
El nmero de libras mol, n, es igual a la masa del gas m dividida por su peso molecular M.
m
n
5.2
M
Reenlazando en la ecuacin de los gases da:
m
pV
RT
5.3
M
donde m = masa del gas, lb
M = peso molecular, lb/lb-mol
5.5
DENSIDAD
Debido a que la densidad se define como la masa por unidad de volumen de la
sustancia, la ecuacin 5.3 puede reordenarse para estimar la densidad del gas a cualquier
presin y temperatura:
m pM
g
5.4
V
RT
donde g = densidad del gas, lb/ft3
Deber resaltarse que lb se refiere a lbs masa en cualquiera de las posteriores
discusiones de densidad.
Ejercicio 5.1
Tres libras de n-butano se colocan en un vaso a 120 F y 60 psia. Calcular el volumen
del gas asumiendo un comportamiento de gas ideal.
Solucin
Paso 1. Se determina el peso molecular del n-butano de la Tabla 1-2 para dar:
M = 58.123
Paso 2. Resolviendo la ecuacin 5.3 para el volumen del gas:
m RT
V
M p
3 (10.73)(120 460)
V
5.35 ft 3
58
.
123
60
Ejercicio 5.2
Usando los datos dados en el ejercicio anterior, calcular la densidad del n-butano.
Solucin
Ing. Hermas Herrera Callejas
Pgina: 5 - 2
PET204 Ingeniera de Reservorios I
Captulo 5 Propiedades y Teora de los Gases
Se resuelve para la densidad aplicando la ecuacin 5.4:
(60)(58.123)
g
0.56lb / ft 3
(10.73)(580)
Al Ingeniero Petrolero normalmente le interesa el comportamiento de mezclas y
raramente debe trabajar con componentes puros de gases. Debido a que el gas natural es
una mezcla de componentes de hidrocarburos, las propiedades fsicas y qumicas de la
mezcla pueden determinarse de las propiedades fsicas de los componentes individuales en
la mezcla mediante el uso de reglas apropiadas de mezclas.
Las propiedades bsicas de estos gases comnmente se expresan en trminos del
peso molecular aparente, volumen estndar, densidad, volumen especfico y gravedad
especfica. Estas propiedades las definimos a continuacin:
5.6
PESO MOLECULAR APARENTE
Una de las principales propiedades del gas que es frecuentemente de inters para los
ingenieros es el peso molecular aparente. Si yi representa la fraccin molar del componente
i de la mezcla de gas, el peso molecular aparente se define a partir del peso molecular
individual de los componentes de la mezcla matemticamente por la siguiente ecuacin:
n
M a yi M i
5.5
i 1
donde Ma = peso molecular aparente de una mezcla de gas
Mi = peso molecular del componente i de la mezcla
yi = fraccin molar del componente i de la mezcla
5.7
VOLUMEN ESTNDAR
En muchos clculos de ingeniera del gas natural, es conveniente medir el volumen
ocupado por 1 lb-mol de gas a una presin y temperatura de referencia. Estas condiciones
de referencia son generalmente de 14.7 psia y 60F, y normalmente se refieren como las
condiciones estndar. Entonces el volumen estndar se define como el volumen de gas
ocupado por 1 lb-mol de gas a condiciones estndar. Aplicando las condiciones anteriores a
la ecuacin 5.1 y resolviendo para el volumen, esto es, el volumen estndar, da:
Vsc
(1) RTsc
(1)(10.73)(520)
Psc
14.7
5.6
o sea
Vsc = 379.56 scf/lb-mol
Donde Vsc = volumen estndar, scf/lb-mol
scf = pies cbicos estndar
Tsc = temperatura estndar, R
psc = presin estndar, psia
5.8
5.7
DENSIDAD DE LA MEZCLA
La densidad de una mezcla de gases ideales se calcula simplemente reemplazando
el peso molecular del componente puro de la ecuacin 5.4 con el peso molecular aparente
de de la mezcla de gases para dar:
m pM a
V
RT
5.8
donde g = densidad del gas, lb/ft3
Ing. Hermas Herrera Callejas
Pgina: 5 - 3
PET204 Ingeniera de Reservorios I
Captulo 5 Propiedades y Teora de los Gases
Ma = Peso molecular aparente
5.9
VOLUMEN ESPECFICO
El volumen especfico se define como el volumen ocupado por una unidad de masa del
gas. Para un gas ideal, esta propiedad puede calcularse por aplicacin de la ecuacin 5.3
V
RT
1
v
5.9
m pM a g
donde v = volumen especfico, ft3/lb
g = densidad del gas, lb/ft3
5.10
GRAVEDAD ESPECFICA DEL GAS
La gravedad especfica se define como la relacin de la densidad del gas a la
densidad del aire. Ambas densidades se miden o expresan a la misma presin y
temperatura. Normalmente la presin estndar Psc y la temperatura estndar Tsc se usan al
definir la gravedad especfica del gas:
aire
5.10
Asumiendo que el comportamiento tanto de la mezcla de gas como del aire se describe
por la ecuacin de gas ideal, la gravedad especfica puede entonces expresarse como:
p sc M a
RTsc
g
p sc M aire
RTsc
o
Ma
Ma
M aire 28.96
donde g = gravedad especfica del gas
aire = densidad del aire
Maire = peso molecular aparente del aire = 28.96
Ma = peso molecular aparente del gas
Psc = presin estndar, psia
Tsc = temperatura estndar, R
5.11
Ejercicio 5.3
Un pozo de gas est produciendo gas con una gravedad especfica de 0.65 a un caudal
de 1.1 MMscf/dia. La presin y temperatura promedias del reservorio son 1,500 psi y 150F
respectivamente. Calcular:
a. El peso molecular aparente del gas
b. La densidad del gas a condiciones de reservorio
c. El caudal de flujo en lb/dia
Solucin
a. De la ecuacin 5.11 se resuelve el peso molecular aparente:
Ma = 28.96g
Ma = (28.96) (0.65) = 18.82
Ing. Hermas Herrera Callejas
Pgina: 5 - 4
PET204 Ingeniera de Reservorios I
Captulo 5 Propiedades y Teora de los Gases
b. Aplicar la ecuacin 5.8 para determinar la densidad del gas:
(1500)(18.82)
g
4.31 _ lb / ft 3
(10.73)(610)
c. Paso 1. Como 1 lb-mol de cualquier gas ocupa 379.4 scf a condiciones estndar, entonces
el nmero de moles diario que el pozo de gas est produciendo puede calcularse de:
(1.1)(10) 6
n
2898 _ lb mol
379.56
Paso 2. Determinar la masa diaria m del gas producido de la ecuacin 5.2:
m = (n)(Ma)
m = (2898)(18.82) = 54540 lb/day
Ejercicio 5.4
Un pozo de gas est produciendo gas natural con la siguiente composicin:
Componente
i
.
CO2
0.05
C1
0.90
C2
0.03
C3
0.02
Asumiendo un comportamiento de gas ideal, calcular:
a. El peso molecular aparente
b. La gravedad especfica
c. La densidad del gas a 2000 psia y 150F
d. El volumen especfico a 2000 psia y 150F
Solucin
Componente
CO2
C1
C2
C3
i
0.05
0.90
0.03
0.02
Mi
44.01
16.04
30.07
44.10
Ma =
i * Mi .
2.200
14.436
0.902
0.882
18.42
a. Aplicar la ecuacin 5.5 para calcular el peso molecular aparente:
Ma = 18.42
b. Calcular la gravedad especfica usando la ecuacin 5.11:
g = 18.42 / 28.96 = 0.636
c. Resolver la densidad aplicando la ecuacin 5.8:
(2000)(18.42)
g
5.628 _ lb / ft 3
(10.73)(610)
d. Determinar el volumen especfico de la ecuacin 5.9:
1
v
0.178 _ ft 3 / lb
5.628
Ing. Hermas Herrera Callejas
Pgina: 5 - 5
PET204 Ingeniera de Reservorios I
5.11
Captulo 5 Propiedades y Teora de los Gases
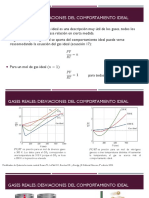
COMPORTAMIENTO DE LOS GASES REALES
Al tratar los gases a muy baja presin, la relacin de gases ideales es una herramienta
conveniente y generalmente satisfactoria. A presiones ms elevadas, el uso de la ecuacin
de estado de los gases ideales puede conducirnos a errores tan grandes como del orden de
500%, comparados a errores de 2 a 3% a presin atmosfrica.
Bsicamente la desviacin de los gases reales de las condiciones de la ley de gas ideal
se incrementa a medida que crece la presin y temperatura y vara ampliamente con la
composicin del gas. Los gases reales se comportan de modo diferente a los gases ideales.
La razn para esto es que la ley de los gases perfectos fue derivada bajo la suposicin de
que el volumen de las molculas es insignificante y que no hay atraccin o repulsin
molecular entre ellas. Este no es el caso para los gases reales.
Se han desarrollado numerosas ecuaciones de estado con el intento de correlacionar
las variables de presin-volumen-temperatura para gases reales con datos experimentales.
Con el fin de expresar una relacin ms exacta entre las variables p, V y T, un factor de
correccin llamado factor de compresibilidad de los gases, factor de desviacin de los gases,
o simplemente factor Z debe introducirse en la ecuacin 5.1 para tomar en cuenta el
alejamiento de los gases de la idealidad. La ecuacin tiene la siguiente forma:
pV= znRT
5.12
Donde el factor de compresibilidad del gas z es una cantidad adimensional y se define
como la relacin del volumen actual de n-moles de gas a T y p al volumen ideal del mismo
nmero de moles a la misma T y p:
V
V
z actual
Videal
(nRT ) / p
5.11.1 El Factor z
Estudios de los factores de compresibilidad del gas natural de varias composiciones
han mostrado que los factores de compresibilidad pueden generalizarse con suficiente
exactitud para la mayora de los propsitos de ingeniera cuando son expresados en
trminos de las dos siguientes propiedades adimensionales:
Presin seudo reducida
Temperatura seudo reducida
Estos trminos adimensionales se definen por las siguientes expresiones:
p
p pr
5.13
p pc
T
T pr
5.14
T pc
donde p = presin del sistema, psia
ppr = presin seudo-reducida, adimensional
T = Temperatura del sistema, R
Tpr = Temperatura seudo-reducida, adimensional
ppc, Tpc = Presin y Temperatura seudo-crticas, respectivamente, y definidas por las
siguientes relaciones:
p pc y i p ci
5.15
i 1
T pc y i Tci
i 1
Ing. Hermas Herrera Callejas
5.16
Pgina: 5 - 6
PET204 Ingeniera de Reservorios I
Captulo 5 Propiedades y Teora de los Gases
Debe destacarse que estas propiedades seudo crticas, como, ppc y Tpc, no representan
las propiedades crticas actuales de la mezcla de gas. Estas seudo propiedades se usan
como parmetros de correlacin en la generacin de propiedades del gas.
Basado en el concepto de propiedades seudo reducidas, Standing y Katz (1942)
presentaron un grfico generalizado del factor de compresibilidad del gas como se muestra
en la Figura 5.1. El grfico representa factores de compresibilidad de gas natural dulce como
funcin de ppr y Tpr. Este grfico es generalmente confiable para gas natural con menor
cantidad de no hidrocarburos. Es una de las correlaciones ms ampliamente aceptadas en la
industria de petrleo y gas.
Ejercicio 5.5
Un reservorio de gas tiene la siguiente composicin de gas: la presin y temperatura
inicial del reservorio son 3000 psia y 180 oF, respectivamente.
Componente
CO2
N2
C1
C2
C3
i C4
n C4
yi .
0.02
0.01
0.85
0.04
0.03
0.03
0.02
Calcular el factor de compresibilidad del gas bajo condiciones iniciales del reservorio.
Solucin
Componente
CO2
N2
C1
C2
C3
i C4
n C4
yi
0.02
0.01
0.85
0.04
0.03
0.03
0.02
Tci (oR)
547.91
227.49
343.33
549.92
666.06
734.46
765.62
yiTci
pci
yipci
10.96
1071
21.42
2.27
493.1
4.93
291.83
666.4
566.44
22.00
706.5
28.26
19.98
616.0
18.48
22.03
527.9
15.84
15.31
550.6
11.01
Tpr = 384.38
ppc = 666.38
Paso 1. Determinamos la presin seudo crtica de la ecuacin 5.15:
ppc = 666.38
Paso 2. Clculo de la temperatura seudo crtica de la ecuacin 5.16
Tpc = 384.38
Paso 3. Clculo de la presin y temperatura seudo reducidas aplicando la ecuacin 5.13 y
5.14, respectivamente.
3000
p pr
4.5
666.38
640
T pr
1.67
384.38
Paso 4. Determinamos el factor z de la Figura 5.1, para dar:
z = 0.85
La ecuacin 5.12 puede escribirse en trminos del peso molecular aparente M a y el
peso del gas m:
Ing. Hermas Herrera Callejas
Pgina: 5 - 7
PET204 Ingeniera de Reservorios I
Captulo 5 Propiedades y Teora de los Gases
m
RT
pV z
Ma
Resolviendo la relacin anterior para el volumen especfico del gas y la densidad, da:
V
zRT
v
5.17
m pM a
1 pM a
v zRT
5.18
donde v =volumen especfico, ft3/lb
g =densidad, lb/ft3
Ejercicio 5.6
Usando los datos del ejercicio 5.5 y asumiendo comportamiento de gas real, calcular
la densidad de la fase gas bajo condiciones iniciales de reservorio. Comparar los resultados
con los del comportamiento de gas ideal.
Solucin
Componente
CO2
N2
C1
C2
C3
i C4
n C4
yi
0.02
0.01
0.85
0.04
0.03
0.03
0.02
Mi
44.01
28.01
16.04
30.07
44.10
58.12
58.12
yi*Mi
0.88
0.28
13.63
1.20
1.32
1.74
1.16
Ma = 20.21
Tci/oR
547.91
227.49
343.33
549.92
666.06
734.46
765.62
yiTci
10.96
2.27
291.83
22.00
19.98
22.03
15.31
Tpc = 384.38
pci
yipci
1071
21.42
493.1
4.93
666.4 566.44
706.5
28.26
616.4
18.48
527.9
15.84
550.6
11.01
Ppc = 666.38
Paso 1. Clculo del peso molecular aparente de la ecuacin 5.5:
Ma =20.21
Paso 2. Determinamos la presin seudo crtica de la ecuacin 5.15:
ppc =666.38
Paso 3. Clculo de la temperatura seudo crtica de la Ecuacin 5.16:
Tpc =384.38
Paso 4. Clculo de la presin y temperatura seudo reducida aplicando las Ecuaciones 5.13 y
5.14, respectivamente:
3000
p pr
4.5
666.38
640
T pr
1.66
384.38
Paso 5. Determinamos el factor z de la Figura 5.1:
z = 0.85
Paso 6. Clculo de la densidad mediante la Ecuacin 5.18:
(3000)(20.21)
g
10.39 _ lb 3
ft
(0.85)(10.73)(640)
Ing. Hermas Herrera Callejas
Pgina: 5 - 8
PET204 Ingeniera de Reservorios I
Captulo 5 Propiedades y Teora de los Gases
Figura 5.1 Grfico de factores de compresibilidad de Standing y Katz. (Cortesa de GPSA y GPA Engineering
Data Book, EO Edicin, 1987.)
Paso 7. Clculo de la densidad del gas asumiendo un comportamiento de gas ideal haciendo
uso de la ecuacin 5.8:
(3000)(20.21)
g
8.83 _ lb 3
ft
(10.73)(640)
Ing. Hermas Herrera Callejas
Pgina: 5 - 9
PET204 Ingeniera de Reservorios I
Captulo 5 Propiedades y Teora de los Gases
Los resultados del ejercicio anterior muestran que la ecuacin del gas ideal estim la
densidad del gas con un error absoluto de 15% cuando se compara con el valor de densidad
encontrada con la ecuacin de gas real.
En casos donde la composicin de un gas natural no est disponible, las propiedades
seudo crticas, ppc y Tpc, pueden predecirse solamente de la gravedad especfica del gas.
Brown y socios (1948) presentaron un mtodo grfico para una aproximacin
conveniente de la presin seudo crtica y temperatura seudo crtica de los gases cuando solo
la gravedad especfica del gas est disponible. La correlacin se presenta en la Figura 5.2.
Standing (1977) expres esta correlacin grfica en la siguiente forma matemtica:
Caso 1: Sistemas de Gas Natural
T pc 168 325 g 12.5 g2
p pc 677 15.0 g 37.5
5.19
2
g
5.20
Caso 2: Sistemas de Gas-Condensado
T pc 187 330 g 71.5 g2
p pc 706 51.7 g 11.1
2
g
5.21
5.22
Donde Tpc = Temperatura Seudo Crtica, R
Ppc = Presin Seudo Crtica, psia
g = Gravedad especfica de la mezcla de gas
Ejercicio 5.7
Volver a trabajar con el ejercicio 5.5 calculando las propiedades seudo crticas de las
ecuaciones 5.19 y 5.20.
Solucin
Paso 1. Clculo de la gravedad especfica del gas:
Ma
20.21
0.698
28.96 28.96
Paso 2. Solucin de las propiedades seudo crticas aplicando las ecuaciones 5.19 y 5.20:
Tpc =168 + 325(0.698) - 12.5 (0.698)2 = 388.8 R
ppc = 677 + 15 (0.698) - 37.5 (0.698)2 = 669.2 psia
Paso 3. Clculo de ppr y Tpr.
3000
p pr
4.48
669.2
640
T pr
1.65
388.8
Paso 4. Determinamos el factor de compresibilidad del gas de la Figura 5.1:
z = 0.845
Paso 5. Clculo de la densidad de la ecuacin 5.18:
(3000)(20.21)
g
10.45 _ lb 3
ft
(0.845)(10.73)(640)
Ing. Hermas Herrera Callejas
Pgina: 5 - 10
PET204 Ingeniera de Reservorios I
Captulo 5 Propiedades y Teora de los Gases
Gravedad Especfica del Gas
Figura 5.2 Propiedades seudo crticas de gases naturales (Cortesa del grupo GPSA y GPA de Ingeniera 10ma
edicin, 1987)
5.11.2 Efecto de Componentes No Hidrocarburos en el Factor Z
Los gases naturales frecuentemente contienen materiales distintos de componentes
hidrocarburos, tales como nitrgeno, dixido de carbono y sulfuro de hidrgeno. Los
hidrocarburos gaseosos se clasifican como dulces o agrios dependiendo del contenido de
sulfuro de hidrgeno. Tanto los gases dulces como los agrios pueden contener nitrgeno,
dixido de carbono o ambos. Un hidrocarburo gaseoso es catalogado como gas agrio si
contiene un grano de H2S por 100 pies cbicos.
La ocurrencia comn de pequeos porcentajes de nitrgeno y dixido de carbono es,
en parte, considerada en las correlaciones citadas anteriormente. Concentraciones de hasta
5 % de estos componentes no hidrocarburos no afectarn seriamente la exactitud. Errores
en los clculos del factor de compresibilidad del orden de 10% pueden ocurrir en
concentraciones mayores de componentes no hidrocarburos en mezclas de gas.
Hay dos mtodos desarrollados para ajustar las propiedades seudo crticas de los
gases para determinar la presencia de los componentes no hidrocarburos. Estos son:
Mtodo de correccin Wichert-Aziz
Mtodo de correccin Carr-Kobayashi-Burrows
5.11.2.1 Mtodo de Correccin Wichert-Aziz
Los gases naturales que contienen H2S y/o CO2 frecuentemente exhiben diferente
comportamiento de factores de compresibilidad a los dulces. Wichert y Aziz (1972)
Ing. Hermas Herrera Callejas
Pgina: 5 - 11
PET204 Ingeniera de Reservorios I
Captulo 5 Propiedades y Teora de los Gases
desarrollaron un procedimiento de clculo simple, fcil de usar, para contabilizar estas
diferencias. Este mtodo permite el uso de la grfica de Standing-Katz, Figura 5.1, por uso
de un factor de ajuste de la temperatura seudo crtica, que es una funcin de la
concentracin de CO2 y H2S en el gas agrio. Este factor de correccin es entonces usado
para ajustar la temperatura y presin seudo crticas de acuerdo a las siguientes expresiones:
T pc' T pc
5.23
p
'
pc
p pc T pc'
5.24
T pc B (1 B )
donde Tpc = temperatura seudo-crtica, R
ppc = presin seudo-crtica, psia
Tpc = temperatura seudo-crtica corregida, R
Ppc = presin seudo-crtica corregida, psia
B = fraccin molar de H2S en la mezcla de gas
= factor de ajuste de temperatura seudo-crtica y es definida matemticamente por
la siguiente expresin
= 120[A0.9 - A1.6] + 15(B0.5 - B4.0)
5.25
donde el coeficiente A es la suma de las fracciones molares de H 2S y CO2 en la mezcla de
gas, o:
A = yH2S + yCO2
Los pasos computacionales para incorporar el factor de ajuste en los clculos del
factor z se resumen a continuacin:
Paso 1. Calcular las propiedades seudo-crticas de la mezcla completa de gas aplicando las
ecuaciones 5.19 y 5.20 o ecuaciones 5.21 y 5.22.
Paso 2. Calcular el factor de ajuste de la ecuacin 5.25.
Paso 3. Ajustar las ppc y Tpc seudo crticas (calculadas en el paso 1) aplicando las
ecuaciones 5.23 y 5.24.
Paso 4. Calcular las propiedades seudo reducidas, ppr y Tpr, de las ecuaciones 5.13 y 5.14
Paso 5. Leer el factor de compresibilidad de la figura 5.1.
Ejercicio 5.8
Un gas natural agrio tiene una gravedad especfica de 0.7. El anlisis composicional
del gas muestra que contiene 5% de CO 2 y 10% de H2S. Calcular la densidad del gas a 3500
psia y 160F.
Solucin
Paso 1. Clculo de las propiedades seudo crticas no corregidas del gas con las ecuaciones
5.19 y 5.20:
Tpc = 168 + 325 (0.7) - 12.5 (0.7)2 = 389.38 R
ppc = 677 + 15 (0.7) - 37.5 (0.7)2 = 669.1 psia
Paso 2. Clculo del factor de ajuste de temperatura seudo crtica de la ecuacin 5.25:
= 120 (0.150.9 - 0.151.6) + 15 (0.10.5 - 0.14) = 20.735
Paso 3. Clculo de la temperatura seudo crtica corregida aplicando la ecuacin 5.23:
Ing. Hermas Herrera Callejas
Pgina: 5 - 12
PET204 Ingeniera de Reservorios I
Captulo 5 Propiedades y Teora de los Gases
Tpc = 389.38 - 20.735 = 368.64
Paso 4. Ajuste de la presin seudo crtica ppc aplicando la ecuacin 5.24:
(669.1)(368.64)
p 'pc
630.44
389.38 0.1(1 0.1)(20.735)
Paso 5. Clculo de ppr y Tpr:
3500
p pr
5.55
630.44
160 460
T pr
1.68
368.64
Paso 6. Determinamos el factor z de la Figura 5.1:
z = 0.89
Paso 7. Clculo del peso molecular aparente del gas mediante la ecuacin 5.11:
Ma = (28.96) (0.7) = 20.27
Paso 8. Solucin de la densidad del gas:
(3500)(20.27)
g
11.98 _ lb 3
ft
(0.89)(10.73)(620)
5.11.2.2 Mtodo de correccin Carr-Kobayashi-Burrows
Carr, Kobayashi, y Burrows (1954) propusieron un procedimiento simplificado para
ajustar las propiedades seudo crticas de los gases naturales cuando estn presentes
componentes no hidrocarburos. El mtodo puede usarse cuando no est disponible la
composicin del gas natural. El procedimiento propuesto se resume en los siguientes pasos:
Paso 1. Conociendo la gravedad especfica del gas natural, calcular la presin y temperatura
seudo crticas, aplicando las ecuaciones 5.19 y 5.20.
Paso 2. Ajustar las propiedades seudo crticas estimadas usando las dos siguientes
expresiones:
Tpc = Tpc - 80yCO2 + 130yH2S - 250yN2
5.26
Ppc = ppc + 440yCO2 + 600yH2S - 170yN2
5.27
Donde Tpc = temperatura seudo crtica ajustada, R
Tpc = temperatura seudo-crtica no ajustada, R
yCO2 = fraccin molar de CO2
yH2S = fraccin molar de H2S en la mezcla de gas
yN2 = fraccin molar del Nitrgeno
ppc = presin seudo crtica ajustada, psia
ppc = presin seudo crtica no ajustada, psia
Paso 3. Usar la temperatura y presin seudo crticas ajustadas para calcular las propiedades
seudo reducidas.
Paso 4. Calcular el factor z de la Figura 5.1.
Ejercicio 5.9
Ing. Hermas Herrera Callejas
Pgina: 5 - 13
PET204 Ingeniera de Reservorios I
Captulo 5 Propiedades y Teora de los Gases
Usando los datos del Ejercicio 5.8, calcular la densidad empleando el procedimiento de
correccin anterior.
Solucin
Paso 1. Clculo de las propiedades seudo crticas corregidas de las Ecuaciones 5.26 y 5.27:
Tpc = 389.38 - 80(0.05) + 130(0.10) - 250(0) = 398.38 R
ppc = 669.1 + 440(0.05) + 600(0.10) - 170(0) = 751.1 psia
Paso 2. Clculo de ppr y Tpr:
3500
p pr
4.66
751.1
620
T pr
1.56
398.38
Paso 3. Determinamos el factor de compresibilidad del gas de la Figura 5.1:
z = 0.820
Paso 4. Clculo de la densidad del gas:
(3500)(20.27)
g
13.0 _ lb ft 3
(0.82)(10.73)(620)
5.11.3 Correccin para Gases de Peso Molecular Elevado
Debe notarse que el Grfico (Figura 5.1) del factor de compresibilidad de Standing y
Katz se prepar de los datos de mezclas binarias de metano con el propano, etano y butano,
y en los gases naturales, cubriendo una gama amplia en composicin de mezclas de
hidrocarburos que contienen metano. Ninguna mezcla que tiene pesos moleculares ms de
40 se incluyeron al preparar este grfico.
Sutton (1985) evalu la exactitud del grfico de factor de compresibilidad de Standing y
Katz usando composiciones de gas medidas en laboratorio y factores z, y encontr que el
grfico proporciona la exactitud satisfactoria para clculos de ingeniera. Sin embargo, las
reglas de mezcla de Kay, Ecuaciones 5.14 y 5.15 (o relaciones de gravedad comparables
para calcular presin y temperatura seudo-crtica), result en factor z poco satisfactorio para
gases de reservorio de peso molecular altos. El autor observ que desviaciones grandes
ocurren en gases con altas concentraciones de heptano plus. l seal que las reglas de
mezcla de Kay no deben usarse para determinar la presin y temperatura seudo crtica para
reservorios de gas con gravedades especficas mayores de aproximadamente 0.75.
Sutton propuso que esta desviacin puede minimizarse utilizando las reglas de
mezclando desarrolladas por Stewart y socios (1959), junto con el factor de ajuste emprico
recientemente introducido (FJ, EJ, y EK) que se relacionan a la presencia de la fraccin de
heptano plus en la mezcla de gas. El enfoque propuesto se perfila en lo siguiente pasos:
Paso 1. Calcular los parmetros j y k de las siguientes relaciones:
j
1
3
2
y i (Tci / p ci )
3
i 1
K ( y i Tci /
i 1
yi (Tci / pci ) 0.5
i 1
p ci )
5.28
5.29
Donde J = Parmetro de correlacin de Stewart-Burkhardt-Voo, R/psia
K = Parmetro de correlacin de Stewart-Burkhardt-Voo, R/psia
Ing. Hermas Herrera Callejas
Pgina: 5 - 14
PET204 Ingeniera de Reservorios I
Captulo 5 Propiedades y Teora de los Gases
yi = fraccin molar del componente i en la mezcla de gas.
Paso 2. Calcular los parmetros de ajuste FJ, EJ, y EK de las siguientes expresiones:
2
1
2
F j y (Tc / p c ) c 7 y (Tc / p c ) 0.5 c 7
5.30
3
3
E j 0.6081F j 1.1325 F j2 14.004 F j yc7 64.434 F j y 2 c7
5.31
E k (Tc / Mpc ) c7 (0.3129 yc7 4.8156( yc7 ) 2 27.3751( yc7 ) 3 )
5.32
donde yC7+ = fraccin molar del componente heptano-plus
(Tc)C7+ = temperatura crtica del C7+
(pc)C7+ = presin crtica del C7+
Paso 3. Ajuste de los parmetros J y K aplicando los factores de ajuste EJ y EK, segn las
relaciones:
J = J - EJ
5.33
K = K - EK
5.34
donde J, K = calculados de las ecuaciones 2-27 y 2-28
EJ, EK = calculados de las ecuaciones 2-30 y 2-31
Paso 4. Calcular la temperatura y presin seudo-crtica ajustadas de las expresiones:
(K ' ) 2
5.35
T pc'
J'
T pc'
5.36
p 'pc
J'
Paso 5. Habiendo calculado las Tpc y ppc ajustadas se sigue el procedimiento regular para
calcular el factor de compresibilidad del grfico de Standing y Katz.
Sutton propuso reglas de mezcla para calcular las propiedades seudo-crticas de gases
de reservorio de alto peso molecular, g > 0.75, lo que mejora significativamente la exactitud
del factor z calculado.
Ejercicio 5.10
Un sistema de hidrocarburo gaseoso tiene la siguiente composicin:
Componente
.
C1
0.83
C2
0.06
C3
0.03
n - C4
0.02
n - C5
0.02
C6
0.01
C7+
0.03
La fraccin de heptano plus se caracteriza por un peso molecular y una gravedad
especfica de 161 y 0.81, respectivamente.
a. Usando la metodologa de Sutton, calcular la densidad del gas a 2000 psi y 150F.
b. Recalcular la densidad del gas sin ajustar las propiedades seudo crticas.
Solucin
Parte A.
Ing. Hermas Herrera Callejas
Pgina: 5 - 15
PET204 Ingeniera de Reservorios I
Captulo 5 Propiedades y Teora de los Gases
Paso 1. Clculo de las propiedades crticas de la fraccin de heptano plus por la correlacin
de Riazi-Daubert
a ( M ) b c e d ( M ) e f ( M )
donde = Cualquier propiedad fsica
a-f = constantes para cada propiedad como se da en la Tabla 2.4
= gravedad especfica de la fraccin
M = peso molecular
Tc = temperatura crtica, R
Pc = presin crtica, psia (Tabla 2.4)
Tb = temperatura del punto de ebullicin, R
Vc = volumen crtico, ft3/lb
(Tc ) Ct 544.2(161) 0.2998 0.811.0555 e 1.3478(10
1189 o R
)(161) 0.3084 ( 0.81)
318.4
)(161) 0.61641( 0.81)
( p c ) C7 4.5203(10 4 )1610.8063 0.811.6015 e 1.8078(10
Paso 2. Construimos la siguiente tabla:
Componente
C1
C2
C3
N C4
N C5
C6
C7+
yi
0,83
0,06
0,03
0,02
0,02
0,01
0,03
Mi
Tci
16,0 343,33
30,1 549,92
44,1 666,06
58,1 765,62
72,2 845,60
84,0 923,00
161,0 1189,00
pci
666,4
706,5
616,4
550,6
488,6
483,0
318,4
Total
yiMi
13,31
1,81
1,32
1,16
1,45
0,84
4,83
24,72
yi(Tci/pci yiz(Tc/pc)i yi(Tc/zpc)i
0,43
0,596
11,039
0,05
0,053
1,241
0,03
0,031
0,805
0,03
0,024
0,653
0,04
0,026
0,765
0,02
0,014
0,420
0,11
0,058
1,999
0,70
0,802
16,922
Paso 3. Clculo de los parmetros J y K de las ecuaciones 2-27 y 2-28:
J = (1/3)[0.700] + (2/3)[0.802]2 = 0.662
K = 16.922
Paso 4. Determinamos el factor de ajuste: FJ, EJ y EK por aplicacin de las ecuaciones 5.30 a
5.32:
1
2
2
F j 0.112 0.058 0.0396
3
3
E j 0.6081(0.04) 1.1325(0.04) 2 14.004(0.04)(0.03) 64.434(0.04)0.3 2 0.012
E k 66.634 0.3129(0.03) 4.8156(0.03) 2 27.3751(0.03) 3 0.386
Paso 5. Clculo de los parmetros J y K de las ecuaciones 2-32 y 2-33:
J = 0.662 - 0.012 = 0.650
K = 16.922 - 0.386 = 16.536
Paso 6. Clculo de las propiedades seudo crticas ajustadas de las Ecuaciones 5.34 y 5.37:
16.536 2
T pc'
420.7
0.65
420.7
p 'pc
647.2
0.65
Ing. Hermas Herrera Callejas
Pgina: 5 - 16
PET204 Ingeniera de Reservorios I
Captulo 5 Propiedades y Teora de los Gases
Paso 7. Clculo de las propiedades seudo reducidas del gas aplicando las Ecuaciones 5.12 y
5.13, para dar:
2000
p pr
3.09
647.2
610
T pr
1.45
420.7
Paso 8. Clculo del factor z de la Figura 5.1, para dar:
z = 0.745
Paso 9., Clculo de la densidad del gas mediante la ecuacin 5.17:
( 2000)(24.72)
g
10.14 lb ft 3
(10.73)(610)(0.745)
Parte B.
Paso 1. Clculo de la gravedad especfica del gas:
Ma
24.73
0.854
28.96 28.96
Paso 2. Clculo de las propiedades seudo crticas aplicando las Ecuaciones 5.19 y 5.20:
Tpc = 168 + 325(0.854) - 12.5(0.854)2 = 436.4R
ppc = 677 + 15(0.854) - 37.5(0.854)2 = 662.5 psia
Paso 3. Clculo de ppr y Tpr:
2000
p pr
3.02
662.5
610
T pr
1.40
436.4
Paso 4. Clculo del factor z de la Figura 5.1, para dar:
z = 0.710
Paso 5. De la Ecuacin 5.17, calculamos la densidad del gas:
(2000)(24.73)
g
10.64 lb ft 3
(10.73)(610)(0.710)
5.11.4 Calculo Directo de los Factores de Compresibilidad
Despus de 4 dcadas de existencia, el grfico del factor z de Standing-Katz es an
ampliamente usado como una fuente prctica de los factores de compresibilidad del gas
natural. Como resultado, hubo una necesidad aparente para una descripcin matemtica
simple de la grfica. Varias correlaciones empricas para el clculo del factor z se han
desarrollado a travs de los aos. Las siguientes tres correlaciones empricas se describen a
continuacin:
Hall-Yarborough
Dranchuk-Abu-Kassem
Dranchuk-Purvis-Robinson
Ing. Hermas Herrera Callejas
Pgina: 5 - 17
PET204 Ingeniera de Reservorios I
Captulo 5 Propiedades y Teora de los Gases
5.11.4.1 El Mtodo de Hall-Yarborough
Hall y Yarborough (1973) presentaron una ecuacin de estado que representa
exactamente la grfica del factor z de Standing y Katz. La expresin propuesta se basa en
las ecuaciones de estado de Starling-Carnahan. Los coeficientes de la correlacin fueron
determinados ajustndolos a los datos tomados de la grfica del factor z de Standing y Katz.
Hall y Yarborough propusieron la siguiente formula matemtica:
0.06125 p pr t 1.2 (1t ) 2
z
5.37
e
donde ppr = presin seudo reducida
t = reciproca de la temperatura seudo reducida, Tpc/T
Y = densidad reducida que puede obtenerse como solucin de la siguiente ecuacin:
2 3 4
F ( ) X 1
( x 2) 2 ( X 3) X 4 0
5.38
(1 ) 3
La ecuacin 5.38 es una ecuacin no lineal y puede ser convenientemente resuelta
para la densidad reducida Y usando la tcnica de iteracin de Newton-Raphson.
El procedimiento computacional de resolver la ecuacin 2.37 a cualquier presin seudo
reducida especificada ppr y temperatura Tpr se resume en los siguientes pasos:
Paso 1. Hacer una estimacin inicial del parmetro desconocido, Yk, donde k es un contador
de iteracin. Un intento inicial apropiado de Y se da por la siguiente relacin:
2
k 0.0125 p pr te 1.2 (1t )
Paso 2. Sustituir este valor inicial en la ecuacin 5.38 y evaluar la funcin no lineal. A no ser
que el valor correcto de Y se haya seleccionado inicialmente, la ecuacin 5.38 tendr un
valor un valor diferente de cero para F(Y):
Paso 3. Una nueva estimacin mejorada de Y, como Yk+1, se calcula de la siguiente
expresin:
f ( k )
k 1 k
5.39
f ' ( k )
donde f(Yk) se obtiene evaluando la derivada de la ecuacin 5.38 a Yk, o:
f ' ( )
1 4 4 2 4 3 4
2( X 2) ( X 3)( X 4) ( X 4 1)
4
(1 )
5.40
Paso 4. Los pasos 23 se repiten n veces, hasta que el error, abs(Y k Yk+1), llegue a ser ms
pequeo que una tolerancia establecida, como 10-12:
Paso 5. El valor correcto de Y entonces se usa para evaluar la ecuacin 5.37 para el factor
de compresibilidad.
Hall y Yarborough resaltaron que el mtodo no se recomienda para su aplicacin si la
temperatura seudo reducida es menor a 1.
5.11.4.2 El mtodo de Dranchuk-Abu-Kassem
Dranchuk y Abu-Kassem (1975) derivaron una expresin analtica para calcular la
densidad reducida del gas que puede usarse para estimar el factor de compresibilidad del
Ing. Hermas Herrera Callejas
Pgina: 5 - 18
PET204 Ingeniera de Reservorios I
Captulo 5 Propiedades y Teora de los Gases
gas. La densidad reducida del gas, r se define como la relacin de la densidad del gas a
una presin y temperatura especificadas a la del gas a su presin y temperatura crticas, o
pM a
p
r
zRT zT
pc
c pc M a
z c RTc
z cTc
El factor de compresibilidad crtico del gas z c es aproximadamente 0.27 que conduce a
la siguiente expresin simplificada para la densidad reducida del gas:
0.27 p pr
r
5.41
zT pr
Los autores propusieron la siguiente ecuacin de estado de once constantes para
calcular la densidad reducida del gas:
2
R
f ( r ) ( R1 ) r 2 ( R3 ) r2 ( R4 ) r5 ( R5 )(1 A11 r2 )e A11 r 1 0
5.42
Con los coeficientes R1 a R5 definidos por las siguientes relaciones:
A
A
A
A
R1 A1 2 33 4r 5t
T pr T pr T pr T pr
0.27 p pr
R2
T pr
A
A
R3 A6 7 28
T pr T pr
A
A
R4 A9 7 28
T pr T pr
A
R5 103
5.43
T pr
Las constantes A1 a la A11 fueron determinadas ajustando la ecuacin, usando
modelos de regresin no lineal, a 1,500 puntos de datos de la grfica del factor z de Standing
y Katz. Los coeficientes tienen los siguientes valores:
A1 = 0.3265
A2 = 1.0700
A3 = 0.5339
A4 = 0.01569
A5 = 0.05165
A6 = 0.5475
A7 = 0.7361
A8 = 0.1844
A9 = 0.1056
A10 = 0.6134
A11 = 0.7210
La Ecuacin 5.42 puede resolverse para la densidad reducida del gas r aplicando la tcnica
de iteracin de Newton-Raphson como se resume en los siguientes pasos:
Paso 1. Hacer una estimacin inicial del parmetro desconocido, r k, donde k es un contador
de iteraciones. Una estimacin inicial apropiada de r k se da por la siguiente relacin:
0.27 p pr
r
T pr
Paso 2. Sustituir este valor inicial en la Ecuacin 5.42 y evaluar la funcin no lineal. A menos
que el valor correcto de r k haya sido seleccionado inicialmente, la Ecuacin 5.42 tendr
un valor distinto de cero para la funcin f(r k).
Ing. Hermas Herrera Callejas
Pgina: 5 - 19
PET204 Ingeniera de Reservorios I
Captulo 5 Propiedades y Teora de los Gases
Paso 3. Se calcula un nuevo valor estimado mejorado de r, o sea, r
expresin:
rk 1 rk
, de la siguiente
k+1
f ( rk
f ' ( rk
donde
f ' ( r ) ( R1 )
2
3
2
2
R2
2( R3 ) r 5( R4 ) r4 2( R5 ) r e A11 r (1 2 A11 r ) A11 r (1 A11 r )
2
r
Paso 4. Los pasos 2 y 3 se repiten n veces, hasta que el error, o sea, abs( r k - r k+1), llegue a
ser ms pequeo que una tolerancia pre-establecida, por ejemplo de 10-12.
Paso 5. El valor correcto de r es entonces usado para evaluar la Ecuacin 5.41 para el
factor de compresibilidad, esto es:
0.27 p pr
z
r T pr
La correlacin propuesta se report que duplic los factores de compresibilidad de la
grfica de Standing y Katz con un error promedio absoluto de 0.585 % y es aplicable a los
rangos:
0.2 ppr < 30
1.0 < Tpr 3.0
5.11.4.3 El Mtodo de Dranchuk-Purvis-Robinson
Dranchuk, Purvis, y Robinson (1974) desarrollaron una correlacin basada en la
ecuacin de estado del tipo de Benedict-Webb-Rubin. Ajustando la ecuacin a los 1,500
puntos de datos de la grfica del factor z de Standing y Katz optimizaron los ocho
coeficientes de las ecuaciones propuestas. La ecuacin tiene la siguiente forma:
2
T
1 T1 r T2 r2 T3 r5 T4 r2 (1 A8 r2 )e ( A8 r ) 5 0
5.44
r
con
A
A
T1 A1 2 33
T pr T pr
A
T2 A4 5
T pr
A A
T3 5 6
T pr
A
T4 37
T pr
0.27 p pr
T5
T pr
donde r se define por la Ecuacin 5.42 y los coeficientes A1 al A8 tienen los siguientes
valores:
A1 = 0.31506237
A3 = 0.57832720
A5 = 0.61232032
A7 = 0.68157001
Ing. Hermas Herrera Callejas
Pgina: 5 - 20
PET204 Ingeniera de Reservorios I
Captulo 5 Propiedades y Teora de los Gases
A2 = 1.0467099
A4 = 0.53530771
A6 = 0.10488813
A8 = 0.68446549
El procedimiento de solucin de la Ecuacin 5.44 es similar a la de Dranchuk y Abu-Kassem.
El mtodo es vlido dentro de los siguientes rangos de temperatura y presin seudo
reducida:
1.05 Tpr < 3.0
0.2 ppr 3.0
5.12
COMPRESIBILIDAD ISOTERMICA DE LOS GASES NATURALES
El conocimiento de la variabilidad de la compresibilidad de los fluidos con la presin y
la temperatura es esencial al efectuar varios clculos de ingeniera de reservorios. Para una
fase lquida, la compresibilidad es pequea y usualmente se asume que es constante. Para
una fase gaseosa, la compresibilidad no es pequea ni constante.
Por definicin, la compresibilidad isotrmica del gas es el cambio en volumen por
unidad de volumen para un cambio unitario en la presin o, en forma de ecuacin:
cg
1
V
5.45
T
donde cg = compresibilidad isotrmica del gas, 1/psi.
De la ecuacin de estado de los gases reales:
V
nRTz
p
Diferenciando la anterior ecuacin con respecto a la presin a una temperatura
constante T nos da:
1 z
V
z
nRT
2
p
p T
p P
Substituyendo en la Ecuacin 5.45 produce la siguiente relacin generalizada:
cg
1 1 z
p z p
5.46
T
Para un gas ideal, z = 1 y (z/p)T = 0, por lo tanto:
cg
1
p
5.47
Debe destacarse que la Ecuacin 5.47 es til para determinar el orden esperado de
magnitud de la compresibilidad isotrmica del gas.
La Ecuacin 5.46 puede expresarse convenientemente en trminos de la presin y
temperaturas seudo reducidas simplemente reemplazando p con (ppc ppr), o:
cg
1
1
z
p pr p pc
z ( p pr p pc )
T pr
Multiplicando la anterior ecuacin por ppc resulta:
c g p pc c pr
1
1 z
p pr
z p pr
5.48
Tr
El trmino cpr se conoce como la compresibilidad isotrmica seudo-reducida y se define
por la relacin:
cpr = cgppc
5.49
donde cpr =compresibilidad isotrmica seudo-reducida
cg = compresibilidad isotrmica del gas, psi1
ppc = presin seudo-reducida, psi
Ing. Hermas Herrera Callejas
Pgina: 5 - 21
PET204 Ingeniera de Reservorios I
Captulo 5 Propiedades y Teora de los Gases
Los valores de (z/ppr)Tpr pueden calcularse de la pendiente de Tpr isotrmica en la
grfica del factor z de Standing y Katz.
Ejercicio 5.11
Una mezcla de hidrocarburos gaseosos tiene una gravedad especfica de 0.72.
Calcular el coeficiente de compresibilidad isotrmica del gas a 2000 psia y 140 F
asumiendo:
a. Un comportamiento de gas ideal
b. Un comportamiento de gas real
Solucin
a. Asumiendo comportamiento de gas ideal, determinamos cg aplicando la Ecuacin 5.46:
1
cg
500 x10 6 psi 1
2000
b. Asumiendo un comportamiento de gas real
Paso 1. Calculamos Tpc y ppc aplicando las Ecuaciones 5.18 y 5.19
Tpc = 168 + 325(0.72) - 12.5(0.72)2 = 395.5 R
PPc = 677 + 15(0.72) - 37.5(0.72)2 =668.4 psia
Paso 2. Calculamos ppr y Tpr de las Ecuaciones 5.12 y 5.13.
2000
p pr
2.99
668.4
600
T pr
1.52
395.5
Paso 3. Determinamos el factor z de la Figura 5.1:
z = 0.78
Paso 4. Se calcula la pendiente [z/ppr]Tpr = 1.52
p pr
0.022
T pr
Paso 5. Se resuelve para cpr aplicando la Ecuacin 5.48:
1
1
c pr
0.022 0.3627
2.99 0.78
Paso 6. Clculo de cg de la Ecuacin 5.49:
0.327
cg
543 x10 6 psi 1
668.4
Trube (1957) present grficos de los cuales se pueden obtener la compresibilidad
isotrmica de los gases naturales. Los grficos, como se muestran en las Figuras 5.3 y 5.4
dan la compresibilidad isotrmica seudo reducida como funcin de la presin y temperatura
seudo reducidas.
Ejercicio 5.12
Usando las grficas generalizadas de Trube, rehacer el Ejercicio 5.11.
Solucin
Paso 1. De la Figure 5.3, se encuentra cpr:
cpr = 0.36
Ing. Hermas Herrera Callejas
Pgina: 5 - 22
PET204 Ingeniera de Reservorios I
Captulo 5 Propiedades y Teora de los Gases
Paso 2. Se resuelve para cg aplicando la Ecuacin 5.50:
0.36
cg
539 x10 6 psi 1
668.4
Matter, Brar, y Aziz (1975) presentaron una tcnica analtica para calcular la
compresibilidad isotrmica del gas. Los autores expresaron cpr como funcin de p/r en
vez de p/ppr.
La Ecuacin 5.42 es diferenciada con respecto a ppr para dar:
z
r T pr
0.27
5.50
zT pr
r z
p pr
z r T
pr
La Ecuacin 5.50 puede ser substituida en la Ecuacin 5.48 para expresar la
compresibilidad seudo-reducida como:
r T pr
1
0.27
c pr
2
5.51
p pr z T pr
r z
z r T
pr
donde r = densidad seudo-reducida del gas.
Figura 5.3 Compresibilidad seudo-reducida de Trube para gases naturales. (Permiso para publicar por la
Society of Petroleum Engineers of AIME. Copyright SPE-AIME.)
Ing. Hermas Herrera Callejas
Pgina: 5 - 23
PET204 Ingeniera de Reservorios I
Captulo 5 Propiedades y Teora de los Gases
La derivada parcial que aparece en la Ecuacin 5.51 sale de la Ecuacin 5.44 para dar:
z
T1 2T2 r 5T3 r4 2T4 r (1 A8 r2 A82 r4 )e ( A8 r )
5.52
T pr
donde los coeficientes T1 a T4 y A1 al A8 se definen previamente por la Ecuacin 5.44.
5.13
Factor Volumtrico de Formacin del Gas Bg,
El Factor Volumtrico de Formacin del Gas se usa para relacionar el volumen del gas,
medido a condiciones de reservorio, al volumen del gas medido a condiciones estndar, o
sea 60 oF y 14.7 psia. Esta propiedad del gas es entonces definida como el volumen real
ocupado por una cierta cantidad de gas a una presin y temperatura especficas, dividido por
el volumen ocupado por la misma cantidad del gas a condiciones estndar. En forma de
ecuacin, la relacin se expresa como:
V p ,T
Bg
5.53
Vsc
donde Bg = Factor volumtrico de formacin del gas, ft3/scf
Vp,T = Volumen del gas a la presin p y temperatura T, ft3
Vsc = Volumen del gas a condiciones estndar, scf
Aplicando la ecuacin de estado de los gases reales, Ecuacin 5.12 y sustituyendo por
el volumen V, nos da:
znRT
p zT
p
Bg
sc
z sc nRTsc
Tsc p
p sc
donde zsc = Factor z a condiciones estndar = 1.0
psc, Tsc = Presin y temperatura estndar
Ing. Hermas Herrera Callejas
Pgina: 5 - 24
PET204 Ingeniera de Reservorios I
Captulo 5 Propiedades y Teora de los Gases
Figura 5.4 Compresibilidad seudo-reducida de Trube para gases naturales. (Permiso para publicar de la
Society of Petroleum Engineers of AIME. Copyright SPE-AIME.)
Asumiendo que las condiciones estndar se representan por psc = 14.7 psia y Tsc = 520 oR, la
expresin anterior se puede reducir a la siguiente relacin:
B g 0.02827
zT
p
5.54
donde Bg = Factor volumtrico de formacin del gas, ft3/scf
z = Factor de compresibilidad del gas
T = Temperatura, R
En otras unidades de campo, el factor volumtrico de formacin del gas puede expresarse
en bbl/scf, para dar:
B g 0.005035
5.14
zT
p
5.55
LA EXPANSIN DEL GAS
La propiedad recproca del factor volumtrico de formacin del gas se llama factor de
expansin del gas y se designa por el smbolo Eg, o sea:
p
E g 35.37
scf/ft3
5.56
zT
En otras unidades:
Ing. Hermas Herrera Callejas
Pgina: 5 - 25
PET204 Ingeniera de Reservorios I
E g 198.6
Captulo 5 Propiedades y Teora de los Gases
p
scf/bbl
zT
5.57
Ejercicio 5.13
Un pozo gasfero est produciendo a un caudal de 15,000 ft3/dia de un reservorio de
gas a una presin promedio de 2,000 psia y una temperatura de 120 F. La gravedad
especfica es 0.72. Calcular el caudal de flujo del gas en scf/dia.
Solucin
Paso 1. Clculo de las propiedades seudo crticas de las ecuaciones 5.19 y 5.20, para dar:
Tpc = 395.5 R
ppc = 668.4 psia
Paso 2. Clculo de ppr y Tpr:
2000
p pr
2.99
668.4
600
T pr
1.52
395.5
Paso 3. Determinacin del factor z de la Figura 2-1:
z = 0.78
Paso 4. Clculo del factor de expansion del gas de la Ecuacin 5.56:
2000
E g 35.37
151.15 scf/ft3
(0.78)(600)
Paso 5. Clculo del caudal de flujo del gas en scf/da multiplicando el caudal de flujo del gas
(en ft3/da) por el factor de expansin del gas Eg expresado en scf/ft3:
Caudal de flujo del gas = (151.15)(15,000) = 2.267 MMscf/da
5.15
VISCOSIDAD DEL GAS
La viscosidad del gas es la medida de la friccin interna del fluido o resistencia al flujo
que afecta a la cada de presin por influjo del reservorio al agujero del pozo y a lo largo de
las instalaciones. Si la friccin entre capas del fluido es pequea, o sea, baja viscosidad, una
fuerza distribuida aplicada resultar en un gradiente de velocidad grande. Mientras la
viscosidad aumenta, cada capa del fluido ejerce una mayor friccin de arrastre en las capas
adyacentes y el gradiente de velocidad decrece.
La viscosidad de un fluido generalmente se define como la relacin de la fuerza
distribuida por unidad de rea al gradiente de viscosidad local. Las viscosidades se expresan
en trminos de poises, centipoises o micro-poises. Un poise es igual a la viscosidad de 1
dina-seg/cm2 y puede ser convertido a otras unidades de campo por las siguientes
relaciones:
1 poise = 100 centipoises
= 1 x106 micropoises
= 6.72 x102 lb mass/ft-sec
= 2.09 x103 lb-sec/ft2
Ing. Hermas Herrera Callejas
Pgina: 5 - 26
PET204 Ingeniera de Reservorios I
Captulo 5 Propiedades y Teora de los Gases
La viscosidad del gas comnmente no se mide en laboratorio porque puede estimarse
con precisin de correlaciones empricas. Como todas las propiedades intensivas, la
viscosidad del gas natural es descrito completamente por la siguiente funcin:
g = f(p,T,yi)
donde g = viscosidad de la fase gas.
La relacin anterior simplemente establece que la viscosidad es una funcin de la
presin, temperatura, y composicin. Varias de las correlaciones para la viscosidad del gas
ampliamente usadas pueden ser vistas como modificaciones de la expresin anterior.
5.16
MTODOS DE CLCULO DE LA VISCOSIDAD DE GASES NATURALES
Dos mtodos populares que son comnmente usados en la industria petrolera son:
Mtodo de Carr-Kobayashi-Burrows
Mtodo de Lee-Gonzalez-Eakin
5.16.1 Mtodo de Carr-Kobayashi-Burrows
Carr, Kobayashi, y Burrows (1954) desarrollaron correlaciones grficas para estimar la
viscosidad del gas natural como funcin de la temperatura, presin y gravedad del gas. El
procedimiento computacional para aplicar las correlaciones propuestas se resume en los
siguientes pasos:
Paso 1. Calcular la presin seudo-crtica, temperatura seudo-crtica y el peso molecular
aparente de la gravedad especfica o la composicin del gas natural. Correcciones a estas
propiedades seudo crticas por la presencia de gases no hidrocarburos (CO2, N2 y H2S) se
haran si estos estn presentes en concentraciones mayores a 5 % molar.
Paso 2. Obtener la viscosidad del gas natural a una atmsfera y la temperatura de inters de
la Figura 5.5. Esta viscosidad, denotada por 1, debe corregirse por la presencia de los
componentes no hidrocarburos usando los insertos de la Figura 5.5. Las fracciones no
hidrocarburos tienden a incrementar la viscosidad de la fase gas. El efecto de componentes
no hidrocarburos en la viscosidad del gas natural puede expresarse matemticamente por
las siguientes relaciones:
1 ( 1 ) no corregido ( ) N 2 ( ) CO2 ( ) H 2 S
5.58
donde 1=viscosidad del gas corregida a presin atmosfrica y temperatura de reservorio, cp
()N2 = correcciones a la viscosidad debido a la presencia de N2
()CO2 = correcciones a la viscosidad debido a la presencia de CO2
()H2S = correcciones a la viscosidad debido a la presencia de H2S
(1)no-corregido = viscosidad del gas no-corregida, cp
Paso 3. Calcular la presin y temperatura seudo-reducida.
Paso 4. De la presin y temperatura seudo-reducidas, obtener la relacin de viscosidad
(g/1) de la Figura 5.7. El trmino g representa la viscosidad del gas a las condiciones
requeridas.
Paso 5. La viscosidad del gas, g, a la presin y temperatura de inters se calcula
multiplicando la viscosidad a una atmsfera y temperatura del sistema, 1, por la relacin de
viscosidad.
Ejercicio 5.14
Ing. Hermas Herrera Callejas
Pgina: 5 - 27
PET204 Ingeniera de Reservorios I
Captulo 5 Propiedades y Teora de los Gases
Un pozo de gas est produciendo a un caudal de 15000 ft3/dia de un reservorio con una
presin promedia de 2000 psia y una temperatura de 120 oF. La gravedad especfica del gas
es de 0.72. Calcular la viscosidad del gas.
Solucin
Paso 1. Clculo del peso molecular aparente del gas:
Ma = (0.72)(28.96) = 20.85
Paso 2. Determinacin de la viscosidad del gas a 1 atm y 140F de la Figura 5.5:
1 = 0.0113
Figura 5.5 Correlacin de viscosidad atmosfrica del gas de Carr. (Permiso para publicar por la Society of
Petroleum Engineers of AIME. Copyright SPE-AIME.)
Paso 3. Clculo de ppr y Tpr:
ppr = 2.99
Tpr = 1.52
Paso 4. Determinacin de la relacin de viscosidad de la Figura 5.6:
g
1
1. 5
Paso 5. Solucin de la viscosidad del gas natural:
g
1
( 1 ) (1.5)(0.0113) 0.01695 cp
Ing. Hermas Herrera Callejas
Pgina: 5 - 28
PET204 Ingeniera de Reservorios I
Captulo 5 Propiedades y Teora de los Gases
Temperatura seudo-reducida
Figura 5.6 Correlacin de Carr de la relacin de viscosidad. (Permiso para publicar por la Society of Petroleum
Engineers of AIME. Copyright SPEAIME.)
Standing (1977) propuso una expresin matemtica conveniente para calcular la
viscosidad del gas natural a presin atmosfrica y temperatura del reservorio, 1. Standing
tambin present ecuaciones para describir los efectos del N 2, CO2, y H2S en 1. Las
relaciones propuestas son:
1 ( 1 ) no corregido ( ) CO2 ( ) H 2 S ( ) N 2
5.59
donde
( 1 ) no corregido 1.709(10 5 2.062(10 6 ) g (T 460) 8.118(10 3 ) 6.15(10 3 ) log( g )
5.60
( ) CO2 y CO2 9.08(10 3 ) log g 6.24(10 3 )
( ) N 2 y N 2 8.48(10 ) log g 9.59(10 )
3
( ) H 2 S y H 2 S 8.49(10 3 ) log g 3.73(10 3 )
5.61
5.62
5.63
donde 1 = viscosidad del gas a presin atmosfrica y temperatura de reservorio, cp
T = temperatura del reservorio, R
g = gravedad del gas
yN2, yCO2, yH2S = fraccin molar del N2, CO2, y H2S, respectivamente
Dempsey (1965) expres la relacin de viscosidad g/1 por la siguiente relacin:
Ing. Hermas Herrera Callejas
Pgina: 5 - 29
PET204 Ingeniera de Reservorios I
Captulo 5 Propiedades y Teora de los Gases
2
3
2
3
ln T pr
a 0 a1 p pr a 2 p pr a3 p pr T pr ( a 4 a5 p pr a 6 p pr a 7 p pr )
1
T pr2 ( a8 a9 p pr a10 p 2pr a11 p 3pr ) T pr3 ( a12 a13 p pr a14 p 2pr a15 p 3pr )
5.64
donde Tpr = temperatura seudo-reducida de la mezcla de gas, R
ppr = presin seudo-reducida de la mezcla de gas, psia
a0 . . . a15 = coeficientes de las ecuaciones que se dan a continuacin:
a0 =
a1 =
a2 =
a3 =
a4 =
a5 =
a6 =
a7 =
- 2.46211820
2.970547414
- 2.86264054 (10-1)
8.05420522 (10-3)
2.80860949
- 3.49803305
3.60373020 (10-1)
- 1.044324 (10-2)
a8 =
a9 =
a10 =
a11 =
a12 =
a13 =
a14 =
a15 =
- 7.93385648 (10-1)
1.39643306
- 1.49144925 (10-1)
4.41015512 (10-3)
8.39387178 (10-2)
- 1.86408848 (10-1)
2.03367881 (10-2)
- 6.09579263 (10-4)
5.16.2 Mtodo de Lee-Gonzalez-Eakin
Lee, Gonzalez y Eakin (1966) presentaron una relacin semi-emprica para calcular la
viscosidad de los gases naturales. Los autores expresaron la viscosidad del gas en trminos
de la temperatura del reservorio, densidad del gas y el peso molecular del gas. Su ecuacin
propuesta est dada por:
g
X
62.4
g 10 4 Ke
donde
(9.4 0.02 M a )T 1.5
K
209 19 M a T
986
X 3.5
0.01M a
T
Y 2.4 0.2 X
g = densidad del gas a presin y temperatura del reservorio, lb/ft3
T = temperatura del reservorio, R
Ma = peso molecular aparente de la mezcla del gas
5.65
5.66
5.67
5.68
La correlacin propuesta puede predecir valores de viscosidad con una desviacin
estndar de 2.7% y una desviacin mxima de 8.99%. La correlacin es menos exacta para
gases con gravedades especficas muy altas. Los autores resaltaron que el mtodo no
puede usarse para gases agrios (sour).
Ejercicio 5.15
Rehacer el Ejercicio 5.14 y calcular la viscosidad del gas usando el mtodo de LeeGonzalez-Eakin.
Paso 1. Clculo de la densidad del gas de la Ecuacin 5.17:
( 2000)(20.85)
g
8.3 lb/f3
(10.73)(600)(0.78)
Ing. Hermas Herrera Callejas
Pgina: 5 - 30
PET204 Ingeniera de Reservorios I
Captulo 5 Propiedades y Teora de los Gases
Paso 2. Solucin de los parmetros K, X e Y usando las Ecuaciones 5.66,
5.67, y 5.68, respectivamente:
9.4 0.02(20.85)(600)1.5 119 .72
K
209 19(20.85) 600
986
X 3.5
0.01( 20.85) 5.35
600
Y 2.4 0.2(5.35) 1.33
Paso 3. Clculo de la viscosidad de la Ecuacin 5.65:
g 10 (119 .72)e
4
5.17
8.3
62.4
5.35
1.33
0.0173
cp
VALOR CALORFICO
Representa el contenido energtico; las ventas de gas son generalmente hechas en
trminos de valor o poder calorfico que es la energa entregada cuando el gas es quemado.
Se lo calcula a partir de los contenidos calorficos de los componentes individuales de la
mezcla:
H = yiHi
5.69
5.18
ECUACIONES DE ESTADO DE LOS GASES REALES
Habamos mencionado que a presiones elevadas, el uso de la ecuacin de estado de
los gases ideales puede conducirnos a errores tan grandes como del orden de 500%,
comparados a errores de 2 a 3% a presin atmosfrica.
Bsicamente la desviacin de los gases reales de las condiciones de la ley de gas ideal
se incrementa a medida que crece la presin y temperatura y vara ampliamente con la
composicin del gas. Los gases reales se comportan de modo diferente a los gases ideales.
La razn para esto es que la ley de los gases ideales fue derivada bajo las siguientes
suposiciones:
a) El volumen de las molculas de gas es insignificante comparado con el volumen del
recipiente que lo contiene y la distancia entre molculas
b) No existen fuerzas de atraccin o repulsin entre molculas, ni las paredes del recipiente
Pero este no es el caso para los gases reales y con la finalidad de superar estas
restricciones se han desarrollado numerosas ecuaciones de estado con el intento de
correlacionar las variables de presin-volumen-temperatura para gases reales con datos
experimentales. Con el fin de expresar una relacin ms exacta entre las variables p, V y T.
La ecuacin de estado ms simple y al mismo tiempo la ms conocida es la Ecuacin
5.1 que expresa: PV = nZRT mencionada en la seccin 5.3, que relaciona la variacin
volumtrica de los gases reales en funcin de la presin y la temperatura. Esta ecuacin es
conveniente de usar cuando la presin es cercana a la atmosfrica, por ser stas las
condiciones en las que fue determinada en forma experimental.
Donde:
P = Presin (Psi)
V = Volumen (Pie3/ Mol)
n = nmero de moles del gas (Lb Mol)
Z = Factor de compresibilidad para los gases reales
R = Constante de los gases (10.73 Psi Pie3 / Lb Mol oR)
Ing. Hermas Herrera Callejas
Pgina: 5 - 31
PET204 Ingeniera de Reservorios I
Captulo 5 Propiedades y Teora de los Gases
T = Temperatura absoluta (oR)
A continuacin se plantean las Ecuaciones de Estado de los Gases Reales ms
conocidas:
5.18.1
Ecuacin de Van Der Waals
Van der Waals intent eliminar las suposiciones mencionadas y estableci una
ecuacin experimental para gases reales, de la siguiente forma:
RT
a
2
V b V
5.70
donde p = presin del sistema, psia
T = temperatura del sistema, R
R = constante de los gases: 10,73 psi-pie3/lb-mol
V = volumen, pies3/mol.
Esta ecuacin puede ser expresada en forma ms general del siguiente modo:
p = p (repulsiva) p (atractiva)
que corresponden a cada trmino de la ecuacin 5.70, o sea: .p (repulsiva) =
y p (atractiva) =
5.18.2
5.71
RT
V -b
a
V
Ecuacin de Redlich-Kwong.
Redlich y Kwong, demostraron que con un simple ajuste, el trmino de la presin de
atraccin a/V2 de la ecuacin de Van der Waals, se poda mejorar notablemente la prediccin
de las propiedades fsicas y volumtricas de la fase vapor. Los autores reemplazaron el
trmino de la presin de atraccin con un trmino
generalizado dependiente de la temperatura. La
ecuacin adquiere la siguiente forma:
RT
a
p
5.72
V b V (V b)T 0.5
donde T es la temperatura del sistema en R.
Redlich y Kwong en el desarrollo de la ecuacin,
notaron que cuando la presin del sistema se haca
muy grande p , el volumen molar V de la
sustancia se encoge aproximadamente en 26% del
volumen crtico sin considerar la temperatura. De
acuerdo a sto, ellos construyeron la ecuacin
anterior para satisfacer la condicin:
Fig. 5.7 Isoterma ideal de un componente
b = 0.26Vc
5.73
Para una sustancia pura, en el punto crtico, hay un volumen crtico que es el mximo y
adems se produce una inflexin, tal como se muestra en la Fig. 5.7. Por lo tanto se
establece que:
p
0
5.74
V
Tc
2 p
2
V
5.75
Tc
Ing. Hermas Herrera Callejas
Pgina: 5 - 32
PET204 Ingeniera de Reservorios I
Captulo 5 Propiedades y Teora de los Gases
Imponiendo la ecuacin de estado a las condiciones del punto crtico, y resolviendo el
sistema de ecuaciones resultante, se tiene que:
RTc
b b
5.76
pc
R 2Tc2.5
pc
a a
5.77
donde: a = 0.42747
b = 0.08664
igualando las ecuaciones 5.58 y 5.77 para b, se tiene:
pcVc = 0.333RTc
5.78
La ecuacin de Redlich-Kwong muestra que para todas las sustancias existe un Z
crtico de 0.333.
La ecuacin 5.72 se puede escribir como una ecuacin cbica para V, efectuando
operaciones algebraicas, tal que:
ab
RT 2
a
bRT
0
V
V 3
b 2 V
5.79
0 .5
0.5
p
p
pT
pT
Reemplazando el volumen molar V = ZRT/p en la ecuacin de R-K, se tiene, en
trminos de Z:
Z3-Z2+(A-B-B2)Z-AB = 0
5.80
donde:
ap
A 2 2.5
5.81
R Tc
bp
B
5.82
RT
Esta ecuacin da una raz real en la
regin monofsica (regin de fase gas o lquida)
y tres races reales en la regin de dos fases.
En este ltimo caso, la raz ms grande
corresponde al factor de compresibilidad de la
fase gas ZV, en tanto que la raz ms pequea
corresponde al lquido ZL (ver Fig. 5.8)
Redlich y Kwong extendieron la aplicacin
de sus ecuaciones a las mezclas lquida y
gaseosa de hidrocarburos, por medio de aplicar
las siguientes reglas:
Fig 5.8 Diagrama de fase PV de un componente puro
x a
am
i 1
0.5
i
5.83
bm xi bi
5.84
i 1
donde: n = nmero de componentes de la mezcla
ai = parmetro a de RK para el componente i de la mezcla,
bi = parmetro b de RK para el componente i de la mezcla,
am = parmetro a de la mezcla
bm = parmetro b de la mezcla,
xi = fraccin molar del componente i en la fase lquida.
Ing. Hermas Herrera Callejas
Pgina: 5 - 33
PET204 Ingeniera de Reservorios I
5.18.3
Captulo 5 Propiedades y Teora de los Gases
Ecuacin de Soave-Redlich-Kwong
Uno de los aportes mas significativos en el desarrollo de las ecuaciones cbicas de
estado, fu la publicacin de Soave, en 1972, que introdujo una modificacin en la ecuacin
de Redlich-Kwong en el parmetro "a" presin de atraccin. Soave reemplaz el trmino
a/T0.5 por un trmino dependiente de la temperatura ms general a, de la siguiente forma:
RT
a
p
5.85
V b V (V b)
donde es un factor adimensional que toma el valor de la unidad cuando T=Tc. Para
otras temperaturas diferentes a la crtica, este parmetro est definido por la expresin:
= [1+m(1-Tr0.5)]2
5.86
el parmetro m se correlaciona con el factor acentrico, de la siguiente forma:
m = 0.480+1.574 - 0.1762
5.87
donde: Tr = temperatura reducida T/Tc
= factor acntrico de la sustancia.
Para cualquier componente puro, las constantes a y b de la ecuacin de SRK, son
halladas imponiendo las restricciones para el punto crtico, tal como se procedi para el caso
de la ecuacin de RK. Entonces:
2
a = a R T c
pc
5.88
b = b RT c
pc
5.89
donde 1 y 2 son los parmetros adimensionales de Soave-Redlich-Kwong para
componentes puros, con sus valores:
1= 0.42747
2= 0.08664
La ecuacin de SRK puede ponerse en su forma cbica y dar:
RT
a bRT
a b
3
)V 2 + (
- b 2 )V - (
)= 0
V -(
5.90
p
La ecuacin de SRK, igual que en el caso anterior, da un valor constante del factor Z a
la Tc igual a 0.333, de modo que, procediendo anlogamente, se tiene:
b = 0.26Vc
5.91
Expresando la ecuacin cbica en trminos de Z por medio de introducir la relacin
ZRT/p, se obtiene:
Z3-Z2+(A-B-B2)Z-AB = 0
5.92
Donde:
( a ) p
A
5.93
( RT ) 2
bp
B
5.94
RT
Estas ecuaciones han sido desarrolladas para componentes puros. Para aplicarlas a
mezclas de hidrocarburos, los parmetros son los siguientes:
n
(a ) m ( xi ai xi i ) 0.5 ( k i 1)
5.95
i 1
Ing. Hermas Herrera Callejas
Pgina: 5 - 34
PET204 Ingeniera de Reservorios I
Captulo 5 Propiedades y Teora de los Gases
bm xi bi
5.96
i 1
con:
(a )m p
(RT )2
p
B = bm
RT
A=
5.97
5.98
El parmetro ki es en realidad un factor de correccin llamado coeficiente de interaccin
binaria y es determinado empricamente.
5.18.4
Ecuacin de Peng-Robinson
Peng y Robinson, en 1975, mostraron la necesidad de mejorar la habilidad de la
ecuacin de estado para predecir densidades de lquidos y otras propiedades de fluidos
particularmente en la vecindad de la regin crtica. Como una base para la creacin de un
modelo mejorado, Peng y Robinson propusieron la siguiente expresin:
RT
a
p=
5.99
V - b (V + b )2 - cb2
donde a, b y tienen el mismo significado que para el caso del modelo de SRK y c es
un nmero completo optimizado, analizando Zc y b/Zc. Generalmente se acepta que Zc est
prximo a 0.28 y que b/V c se aproxime a 0.26. Un valor ptimo de c es 2, lo que d Z c=0.307
y por lo tanto b/Vc=0.253. Basndose en este valor de c, Peng y Robinson propusieron la
siguiente ecuacin de estado:
RT
a
p=
5.100
V - b V(V + b) + b(V - b)
Imponiendo las acostumbradas restricciones al punto crtico y resolviendo el sistema de
ecuaciones, se determinan los valores de a y b, dando:
2
a = a R T c
pc
b = b RT c
pc
5.101
5.102
donde:
a = 0.45724
b = 0.07780
Esta ecuacin predice un factor crtico universal de compresibilidad del gas de 0.307,
cercano al de SRK de 0.333.
La ecuacin de PR tambin adopta la aproximacin de SRK para :
= [1+m(1-Tr0.5)]2
5.103
donde:
m = 0.3746+1.5423 0.26992
5.104
PR ampliaron sus investigaciones ms adelante, y en 1978 dieron la siguiente nueva
relacin:
m = 0.379642 + 1.48503- 0.16442 + 0.0166673
5.105
Poniendo la ecuacin de estado de Peng Robinson en su forma cbica en funcin de Z,
se tiene:
Z3 + (B-1)Z2 + (A-3B2-2B)Z - (AB-B2-B3) = 0
5.106
Ing. Hermas Herrera Callejas
Pgina: 5 - 35
PET204 Ingeniera de Reservorios I
Ing. Hermas Herrera Callejas
Captulo 5 Propiedades y Teora de los Gases
Pgina: 5 - 36
Вам также может понравиться
- Programa Ing. Ambiental UMSA 6-04-19Документ1 страницаPrograma Ing. Ambiental UMSA 6-04-19Mayba MillaresОценок пока нет
- Cap 1 PDFДокумент39 страницCap 1 PDFMayba MillaresОценок пока нет
- Capítulo 5 Propiedades y Teoria de Los GasesДокумент36 страницCapítulo 5 Propiedades y Teoria de Los GasesMayba MillaresОценок пока нет
- CAP 1 - Introduccion Ingenieria PetroleraДокумент26 страницCAP 1 - Introduccion Ingenieria PetroleraMayba Millares100% (1)
- Tipos de Yacimientos Petrolíferos y sus Zonas en BoliviaДокумент8 страницTipos de Yacimientos Petrolíferos y sus Zonas en BoliviaMayba MillaresОценок пока нет
- Ley General de Higiene y Seguridad Ocupacional y BienestarДокумент114 страницLey General de Higiene y Seguridad Ocupacional y BienestarGrover Condorcet RamosОценок пока нет
- CAP 4-Mecanismos de ProduccionДокумент3 страницыCAP 4-Mecanismos de ProduccionMayba MillaresОценок пока нет
- Nociones Básicas para La Interpretación de Perfiles de PozoДокумент100 страницNociones Básicas para La Interpretación de Perfiles de PozoJhadra Yamile Houssein LaraОценок пока нет
- Seguridad IndustrialДокумент21 страницаSeguridad IndustrialferminhernandezОценок пока нет
- Proyecto SociointegradorДокумент33 страницыProyecto SociointegradorkarladanielanunezteОценок пока нет
- Seguridad IndustrialДокумент21 страницаSeguridad IndustrialferminhernandezОценок пока нет
- Seguridad IndustrialДокумент21 страницаSeguridad IndustrialferminhernandezОценок пока нет
- Segundo Trabajo de TermodinamicaДокумент18 страницSegundo Trabajo de TermodinamicaAlfonzo Antonio Natera OrtegaОценок пока нет
- Tema 2a - Propiedades de Los Fluidos Petróleo y Gas - UdabolДокумент84 страницыTema 2a - Propiedades de Los Fluidos Petróleo y Gas - UdabolJose luis lazcano aguilarОценок пока нет
- Ejercicio de Diseño Separador Trifasico HorizontalДокумент13 страницEjercicio de Diseño Separador Trifasico HorizontalDavid Jose Calderin Brango0% (1)
- Presentación Guía - Balances de MateriaДокумент98 страницPresentación Guía - Balances de MateriaDaniel100% (1)
- Metodo DeshidratacionДокумент32 страницыMetodo DeshidratacionAnonymous Gssg1ePaSОценок пока нет
- CAP 1 GASES REALES. Parte 4 Desviación Del Comportamiento Ideal PuntualДокумент21 страницаCAP 1 GASES REALES. Parte 4 Desviación Del Comportamiento Ideal PuntualDaniel FeymanОценок пока нет
- Sistema de Recolección Campo SirariДокумент219 страницSistema de Recolección Campo SirariAlexsandro CossioОценок пока нет
- Factor de Compresibilidad PDFДокумент36 страницFactor de Compresibilidad PDFerickОценок пока нет
- Propiedades Del Gas Natural y El Factor de Compresibilidad Del GasДокумент18 страницPropiedades Del Gas Natural y El Factor de Compresibilidad Del GasMarcos Daniel Vargas InocheaОценок пока нет
- Validaci N de Pruebas PVT de Gas CondensadoДокумент14 страницValidaci N de Pruebas PVT de Gas Condensadoalexis salazarОценок пока нет
- QuishpeNicolas - Cap 3 ManriqueДокумент23 страницыQuishpeNicolas - Cap 3 ManriqueJOB NICOLAS QUISHPE URRUTIAОценок пока нет
- Prueba de Agotamiento A Composición Constante y DiferencialДокумент9 страницPrueba de Agotamiento A Composición Constante y DiferencialAlejandra Alarcon SuarezОценок пока нет
- Factor Compresibilidad Standing Katz Programacion PDFДокумент23 страницыFactor Compresibilidad Standing Katz Programacion PDFHansel QuintanillaОценок пока нет
- Gases RealesДокумент25 страницGases RealesCARLOS SOSAОценок пока нет
- Gas IdealДокумент51 страницаGas IdealAnother Boy On InternetОценок пока нет
- Segundo Examen ParcialДокумент2 страницыSegundo Examen ParcialJorge PazОценок пока нет
- Clase 5 - TermodinámicaДокумент54 страницыClase 5 - Termodinámicayuri DávilaОценок пока нет
- Determinacion de Las Propiedades Del Gas Natural yДокумент18 страницDeterminacion de Las Propiedades Del Gas Natural yCarlitos VelasquezОценок пока нет
- Clase 3 Fisicoquímica - V2122020Документ25 страницClase 3 Fisicoquímica - V2122020yhon manuelОценок пока нет
- TERMODINAMICA Carta de Comprensibilidad PDFДокумент4 страницыTERMODINAMICA Carta de Comprensibilidad PDFalexis basultoОценок пока нет
- ML602AMT Apuntes.1 2021 I.Документ10 страницML602AMT Apuntes.1 2021 I.alfredobenitoОценок пока нет
- Parámetros Del Gas NaturalДокумент146 страницParámetros Del Gas Naturalaminta26Оценок пока нет
- Gases Ideales Segunda ClaseДокумент32 страницыGases Ideales Segunda ClaseCarla Calixtro100% (1)
- FseyndrxuДокумент4 страницыFseyndrxuMiguel SaavedraОценок пока нет
- Conportamirnto de Pozos FluyentesДокумент404 страницыConportamirnto de Pozos FluyentesDpMartínez100% (1)
- Dimensionamiento de Separadores BifásicosДокумент47 страницDimensionamiento de Separadores BifásicosMily hernandez hernandezОценок пока нет
- Propiedades Fisicas, Quimicas y Termodinamicas Del Gas NaturalДокумент79 страницPropiedades Fisicas, Quimicas y Termodinamicas Del Gas NaturalDIEGO ARMANDO FLROES GUTIERREZОценок пока нет
- Explotacion Del GasДокумент372 страницыExplotacion Del GasAnghyBMОценок пока нет
- Gases 2019Документ73 страницыGases 2019Angélica PorbeОценок пока нет
- Practica FQДокумент8 страницPractica FQFabritzio- KunОценок пока нет