Академический Документы
Профессиональный Документы
Культура Документы
Practica #Bioquimica
Загружено:
RickyFrancoCoaguilaОригинальное название
Авторское право
Доступные форматы
Поделиться этим документом
Поделиться или встроить документ
Этот документ был вам полезен?
Это неприемлемый материал?
Пожаловаться на этот документАвторское право:
Доступные форматы
Practica #Bioquimica
Загружено:
RickyFrancoCoaguilaАвторское право:
Доступные форматы
Manual de laboratorio Bioqumica General
PRACTICA N 01
TEORA Y EMPLEO DEL ESPECTROFOTOMETRO
Manual de laboratorio Bioqumica General
I.
INTRODUCCION
La espectrofotometra es el mtodo de anlisis ptico ms usado en
las investigaciones biolgicas. El espectrofotmetro es un
instrumento que permite comparar la radiacin absorbida o
transmitida por una solucin que contiene una cantidad desconocida
de soluto, y una que contiene una cantidad conocida de la misma
sustancia.
Todas las sustancias pueden absorber energa radiante, aun el vidrio
que parece ser completamente transparente absorbe longitud de
ondas que pertenecen al espectro visible; el agua absorbe
fuertemente en la regin del infrarrojo.
La absorcin de las radiaciones ultravioleta, visibles e infrarrojas
depende de la estructura de las molculas, y es caracterstica para
cada sustancia qumica.
Cuando la luz atraviesa una sustancia, parte de la energa es
absorbida; la energa radiante no puede producir ningn efecto sin
ser absorbida.
El color de las sustancias se debe a que stas absorben ciertas
longitudes de onda de la luz blanca que incide sobre ellas y solo
dejan pasar a nuestros ojos aquellas longitudes de onda no
absorbida.
II.
MARCO TERICO
INSTRUMENTAL BSICO PARA COLORIMETRIA
La comparacin de la intensidad de color producida por una
muestra con la producida por un patrn conocido de referencia se
ha utilizado durante mucho tiempo en el laboratorio de qumica
clnica. Originalmente se usaba un comparador visual en el cual se
situaban los dos tubos de las soluciones uno al lado del otro para
comparacin. El aparato estaba diseado de tal forma que la
fuente de la luz pasaba a travs de los tubos y as a travs de la
columna de solucin contenida en los tubos. Se evitaba que la luz
extraa entrara por las partes laterales del tubo utilizando el
simple proceso de construirlos de cristal negro opaco.
Manual de laboratorio Bioqumica General
La longitud del paso de luz se meda introduciendo un embolo
opaco dentro de las soluciones. De nuevo, se evitaba que la luz
entrara por los lados del embolo y su nico paso era a travs de la
longitud del embolo. Los mbolos se introducen en el interior de
las soluciones hasta que el ojo del operador juzgaba que el color
en el tubo de muestra problema, era igual al del tubo patrn. Los
principios de calorimetra se basan en las leyes de Beer y Lambert.
LEY DE BEER.
Dice: que la cantidad de la luz absorbida por una solucin, es
directamente proporcional a la concentracin del slido en aquella
solucin.
LEY DE LAMBERT.
Dice: que la cantidad de la luz absorbida por una solucin, es
proporcional al espesor o intensidad de color de la solucin.
El mayor inconveniente del comparador visual de color, era que
dos personas no llegaban a obtener el mismo resultado debido a
variaciones individuales al juzgar el color. Adems, algunas
personas son ciegos para un color o para las matices y como tales
son incapaces de usar un instrumento de comparacin de este
tipo.
FOTOMETROS FOTOELECTRICOS
Es un instrumento para medir la intensidad de la luz. La luz que
incide sobre una fotoclula o fototubo, produce una corriente
elctrica dentro de la clula o tubo. Esta corriente es transferida a
un galvanmetro donde puede medirse su intensidad.
Las desviaciones de la aguja del galvanmetro son directamente
proporcionales a la cantidad de corriente que pasa por l, a su vez,
es directamente proporcional a la cantidad de luz que ndice sobre
la fotoclula.
Combinada con el fotmetro hay una fuente de luz
monocromtica. El rayo monocromtico se produce de varias
formas. El mtodo ms simple es usar una luz blanca pasarla a
travs de un filtro selectivo que tenga una gama espectral
relativamente estrecha.
TIPOS DE COLORIMETROS FOTOELECTRICOS.
Manual de laboratorio Bioqumica General
Los fotmetros de filtros o colormetros existen o bien como
instrumentos de fotoclula simple. Fotoclula doble. Los
instrumentos de fotoclula simple estn sujetos a las fluctuaciones
del voltaje, y necesitan ser suministrados con algn tipo de
regulador de voltaje. Los instrumentos de doble clula, no estn
sujetos a las fluctuaciones a las fluctuaciones del voltaje, ya que
ellos emplean fotoclulas equilibradas y una de clulas es siempre
una clula de referencia. Cualquier clase de cambios de intensidad
de la luz debido a cambio de voltaje. Afecta a ambas clulas por
igual no afecta a las lecturas correspondientes a muestra
sucesivas.
A los fotmetros de prisma y de red de distraccin se les conoce
como espectrofotmetros, y son generalmente instrumentos de
clula simple. Ambos necesitan una fuente de voltaje constante
para un funcionamiento ptimo.
Generalmente, los espectrofotmetros proporcionan una lectura
ms sensible que los instrumentos de filtro.
LONGITUD DE ONDA.
La luz se transmite por ondas y la distancia entre las dos cimas de
una onda, se mide en milimicras. A tales distancias se les conoce
como longitudes de onda.
ESPECTRO VISIBLE: Longitudes de onda entre 400 a 700 nm.
ESPECTRO ULTRAVIOLETA: Longitudes de onda por debajo de
400 nm.
ESPECTRO INFRAROJO: Longitudes de onda por encima de
700nm.
El sistema ms delicado emplea un prisma que descompone la luz
blanca en sus bandas componentes. La luz monocromtica se
selecciona luego mediante una rendija. El montaje de los prismas
es muy delicado y relativamente fcil alterar. Un sistema ms
tosco emplea la red de difraccin, que descompone la luz blanca
de una forma muy parecida a como lo hace el prisma. Como las
redes de difraccin, permiten la seleccin de bandas espectrales
relativamente estrechas.
Los calormetros visuales utilizan al espectro visible completo,
mientras que los fotmetros y los espectrofotmetros, son ms
Manual de laboratorio Bioqumica General
selectivos y utilizan bandas mucho ms estrechas. En la mayora
de los ensayos en qumica clnica, se utiliza el espectro visible.
Algunos constituyentes pueden ser medidos nicamente en
bandas ultravioletas (UV) o infrarrojas (IR) y los fotmetros que se
usan en las tcnicas (UV) o (IR), son fabricados especialmente. La
seleccin de las longitudes de onda adecuadas para cualquier
anlisis fotomtrico, lleva consigo, la construccin de una curva de
transmisin espectral (ts) usando soluciones conteniendo el color
final producido en la reaccin, para determinar el constituyente de
la sangre que se est considerando. La longitud de onda
seleccionada es aquella en la que las sustancias especficas
coloreadas absorben la mayor cantidad de luz, o transmiten la
menor cantidad de luz.
La curva (TS) (transmisin espectral) se prepara representando en
un simple papel cuadriculado las lecturas de porcentaje de
transmisin mnima. Es obvio que este procedimiento, no se puede
usar con instrumentos de filtros, ya que raramente hay disponibles
filtros suficientes, para permitir una seleccin tan precisa.
Consecuentemente, el filtro correcto para cualquier tcnica
colorimtrica se indica generalmente en las instrucciones de la
tcnica. Normalmente el filtro a usar es aquel cuya transmisin
espectral es opuesta a la de la materia que se est valorando.
En otras palabras, el filtro a usar deber ser uno que transmita la
mayor cantidad de luz. No obstante, hay excepciones a esto, y que
en ciertos casos habr tal punto de sensibilidad que har
imposible lecturas exactas.
En estas condiciones se debern usar un filtro arbitrario. Algunos
fabricantes de colormetros suministran listas de filtros coloreados
junto con soluciones coloreadas para las que siguieren usar estos
filtros. Un laboratorio har uso de tales tablas, cuando ponga en
marcha nuevas tcnicas y cuando no este especificado el filtro.
TUBOS DE COLORIMETRO Y CUBETAS
Tan importante como la correcta seleccin de una longitud de onda
o de los filtros que han de utilizarse, es la seleccin de tubos o
cubetas del tamao adecuado y caractersticas optimas
aceptables. Debe recordarse que la cubeta es una parte del
sistema ptimo del instrumento. Se introducen errores
importantes, cuando se usan cubetas que estn rayadas,
grabadas, sucias o con marcas de dedos, o se utilizan otros
materiales extraos. Durante una serie de anlisis es de vital
importancia, que totas las cubetas se siten en el aparato siempre
Manual de laboratorio Bioqumica General
con la misma orientacin. Todos los fabricantes de instrumentos
marcan sus cubetas de alguna forma e indican el alineamiento
correcto de estas marcas.
Probablemente la forma ms eficaz de eliminar los errores de las
cubetas, es usar una sola cubeta para todas las lecturas. Sin
embargo, esta puede ser no practico, dado que se pierde tiempo y
exige que el tubo sea en juagado muy bien entre lecturas de las
muestra. Las cubetas cuadradas estn disponibles y son
probablemente las ms exactas de todas. Los dos lados opuestos
de una cubeta cuadrada son rectificados y pulidos para asegurar
las condiciones ptimas mximas. Como una proteccin ms, los
otros lados tienen su acabado satinado o de vidrio deslustrado, de
forma que incluso el operario ms descuidado, tendr que
detenerse en situar la cubeta en el espectrofotmetro, en la forma
correcta. Las cubetas redondas debern igualarse cuidadosamente
para una transmisin de +- 0.68. El tamao es importante en ello,
ya que su dimetro rige la longitud del paso de luz a travs de la
solucin coloreada que se est midiendo. Al seleccionar cubetas
para un ensayo dado, deber recordarse, que las lecturas ms
exactas se obtienen de cubetas en las lecturas de porcentaje de
transmisin importantes resultan entre 10 y 80 T.
Los extremos de la escala del fotmetro no proporcionan medidas
exactas.
LECTURAS DEL FOTOMETRO
La lectura de los instrumentos depende o bien de la cantidad de a
luz absorbida por una solucin, o de la cantidad de luz no
absorbida que pasa a travs de la solucin. La cantidad de luz
absorbida por una solucin se la conoce como densidad ptica, es
una escala logartmica. Para representar las lecturas de una escala
de densidad ptica hay que utilizar papel milimetrado. La luz no
absorbida que pasa a travs de una solucin, se la conoce como
porcentaje de transmisin. Las divisiones de calibrado sobre la
escala de las lecturas del instrumento graduado en %T, son
divisiones iguales y para representar las curvas con estas lecturas
hay que utilizar papel semi-logartmico. Algunos instrumentos
utilizan las dos escalas graduadas con lecturas de densidad ptica
y de porcentaje de transmisin y en estos casos como la escala de
porcentaje de transmisin es ms fcil de leer, los valores se
toman de la escala en trminos de porcentaje de transmisin %T,
y la continuacin se transforman en DO, para efectuar los clculos.
Manual de laboratorio Bioqumica General
Las soluciones blancas, son importantes especialmente en
ensayos donde los reactivos tienen color. La concentracin de
color de ensayo est formada con el color producido por la
substancia que se est investigando, ms el color de los reactivos
iniciales. Para conseguir resultados exactos, la lectura del blanco
efectuada en le fotmetro, deber restarse de las dems lecturas.
Este ajuste se puede efectuar en una de estas dos formas.
1. Leer el blanco fijando el cero de DO, con agua destilada, y
rescatar esta lectura de todas las otras lecturas de patrones
y muestras.
2. Ajustar el fotmetro a 100%T, o cero de DO, con el blanco en
lugar de agua destilada. Esto resta la lectura de blanco
mecnicamente, en lugar de matemticamente.
A. CURVAS PATRON
Las curvas patrn son tiles:
1. Para comprobar un ensayo y determinar su conformidad con la ley
de Beer.
2. En determinaciones donde el patrn es difcil de obtener.
3. En determinaciones donde los patrones son extremadamente
inestables.
Por reflexiones sobre -2 y -3, es esencial que estas curvas sean
comprobadas detenidamente a intervalos regulares y efectuar un
control con cada coleccin de muestras problema.
Para preparar una curva patrn, se preparan varias concentraciones
de un patrn y se leen a una longitud de onda especfica contra un
blanco adecuado. El porcentaje de transmisin, o las lecturas de
densidad ptica para estos patrones, se representan contra sus
concentraciones correspondientes. Se trata una lnea desde el origen,
y uniendo todos los puntos las veces que una de las condiciones del
ensayo cambie. Esto incluir la preparacin de reactivos nuevos
III.
OBJETIVOS
Conocer e interpretar un espectro de absorcin
Aprender a construir una curva de calibracin
Manual de laboratorio Bioqumica General
IV.
V.
MATERIALES
Papel milimetrado
Lpiz
DETERMIMACION DE LOS ESPECTROS DE ABSORCION
A partir de la solucin stock de azul de bromo fenol y anaranjado de
metilo se prepara una solucin diluida de 1:25.
Se fija el instrumento a una transmisin de 100q% con agua destilada.
La solucin diluida de colorante 1:25 debe dar una lectura de
aproximadamente en 30-40%
Seleccionar una longitud de onda para cada colorante: 580Mu para el
azul de bromo fenol; 460Mu para el anaranjado de metilo.
Para determinar el espectro de absorcin del azul de bromo fenol se
debe leer las absorbancias usando la muestra diluida (1:25)
Se emplea el agua para fijar el instrumento a una transmisin de
100%.
El agua se utiliza cada vez que se lee las absorbancias a las distintas
longitudes de onda
Leer la muestra diluida de azul de bromo fenol diluido (1:25) a las
siguientes longitudes de onda
Representar grficamente las longitudes de onda (abscisas) en
funcin de las absorbancias (ordenada) trazando una curva suave que
una todos los puntos. Indicar el punto de mxima de absorcin.
VI.
RESULTADOS
LONGITUD DE
LECTURA DE
ONDA
400 mu
ABSORVANCIAS
0,03
430
mu
0,05
520
mu
0,26
570
mu
0,38
620
mu
0,14
700
mu
0,01
PRACTICA N 02
Manual de laboratorio Bioqumica General
EXAMEN BIOQUIMICO DE ORINA PATOLGICA
ANLISIS: cualitativo
DESCRIPCION: visual-olfativo
I. INTRODUCCION
La orina es un liquido muy complejo formado por
95% de agua y 5% de slidos, constituye el
producto final realizado por millones de clulas del
sistema renal y urinario del metabolismo y tiene un gasto promedio
de 1 a 1.5 litros de orina por da, que depende de la ingestin de
lquidos. A travs de la orinase excretan una gran variedad de
productos metablicos de desecho. La orina contiene miles de
sustancias disueltas, aunque las 3 principales son agua, urea y
cloruro desodio. Se excretan ms slidos a travs de la orina que por
cualquier otra va, la composicin de la orina depende en gran parte
de la calidad y cantidad de material excretado. Algunos componentes
de la sangre, como al glucosa, tiene un umbral renal, esto es, que
deben alcanzar un nivel en la sangre antes de que cada sustancia
sea excretada en la orina
CARACTERSTICAS FSICAS DE LA ORINA
II.
COLOR
En un individuo sano, la intensidad del color depender de la
cantidad de la orina emitida. El color va desde el amarillo claro hasta
el amarillo oscuro en funcin de su concentracin. Cuando la orina
est muy concentrada el color se oscurece, mientras que ser ms
claro cuando est menos concentrada como consecuencia del exceso
de agua. Es clara cuando se encuentra recin emitida y puede
hacerse turbia por la formacin de depsitos de fosfatos, oxalatos o
uratos. El color de la orina puede ser clave para identificar una
enfermedad ms rpidamente, pero adems hay una serie de signos
que nos pueden revelar muchos datos como son alguno de los
siguientes: Espuma: sugiere la presencia de proteinuria. Pus: se
denomina piuria. Orina lechosa: donde hay presencia de gran
cantidad de grasa. Puede ser debido a una concentracin elevada
de colesterol y triglicridos por un sndrome nefrtico o fractura
sea, denominndose lipiduria, es decir, concentracin de lpidos en
orina. Presencia de moco. Linfa: la presencia de linfa en la orina es
muy extraa de encontrarla y se denomina quiluria
MARCO TEORICO
Manual de laboratorio Bioqumica General
El anlisis de la orina comienza con su inspeccin visual, para
comprobar si a simple vista se observan clculos, hematuria,
coloracin oscura o coluria por eliminacin excesiva de
Urobilingeno, aspecto claro o turbio de la orina, lo que facilita, el
diagnstico de infeccin urinaria.
Mediante el anlisis elemental de la orina puede saberse si existe o
no glucosa en ella, su densidad y pH, el exceso de cuerpos cetnicos,
iones en orina, la existencia de clulas, pus o bacterias, bilirrubina y
urobilingeno excesivos, la presencia o ausencia de protenas, as
como la deteccin de sustancias diversas (cannabis, herona,
cocana, benzodiacepinas y otros frmacos).
En condiciones normales no debe haber glucosa en la orina. Aunque
una pequea parte de la poblacin elimina glucosa con la orina sin
padecer ningn trastorno,si aparece suele indicar que es muy
elevado el nivel de glucosa en la sangre, por lo que interesa
especialmente en el diagnstico de la diabetes, intolerancia
hidrocarbonada y algunas alteraciones renales.
La densidad de la orina debe estar entre 1003 y 1030. Su pH debe
ser de entre 4,6 y 8 segn la dieta: si aumenta, la orina se hace ms
bsica y facilita la infeccin por algunos microorganismos y la
formacin de clculos. Si hay un exceso de cuerpos cetnicos,
posiblemente se deba a una cetoacidosis, diabtica en la mayora de
los casos. Cuantificar los iones sodio y potasio sirve para conocer si
la persona toma diurticos.
Si aparecen glbulos rojos en la orina, visibles al microscopio o a
simple vista, ms que tratar los sntomas a nivel local debe buscarse
las causas, Podemos encontrarnos ante una hematuria en estos
casos: Nefropata, clculos, procesos infecciosos, quistes renales,
hidronefrosis, traumatismos, etc.La existencia de pus en orina, es
patolgica, se conoce como piuria, y obliga a pensar en infeccin del
tracto urinario.
Existe leucocituria si la cifra de leucocitos en orina es mayor de 2000
clulas. Puede ser debida a un proceso inflamatorio, causado a su vez por
un proceso infeccioso o por una enfermedad inflamatoria, ante una cifra
alta de leucocitos, solicita un cultivo de orina, para comprobar si hay o no
infeccin, y si stos son positivos, pondremos el tratamiento oportuno. Sin
embargo si los cultivos son negativos, hay que investigar la posibilidad de
una enfermedad inflamatoria o de una infeccin no bacteriana
III.
OBJETIVOS
muestra
patolgica
de
sencillos.
Mediante
ensayos
muestra
deorina
orina
Mediante
patolgica
sencillos.
ensayos
Manual de laboratorio Bioqumica General
Analizar una muestra de orina patolgica Mediante ensayos
sencillos.
Determinar la acides en una muestra de orina
VII.
VIII.
MATERIALES Y METODO
MATERIALES
Tubos de ensayos
Tiras reactivas
Mechero
Gradilla
Pinza
Matraz erlenmeyer
Pipetas
REACTIVOS
Reactivo de Fehling
Azufre
PROCEDIMIENTO
Primero se hace un anlisis visual y olfativo de la muestra de
orina:
*Color: amarillo mbar
*Turbidez: la muestra de orina se presentaba muy turbia.
*Olor: amoniacal (olor intenso)
Para anlisis de sustancias eliminadas por la orina
1. Para hacer el anlisis de las sustancias eliminadas por la orina
se utilizar la tira reactiva.
2. En un tubo de ensayo, se agrega la orina y luego colocamos la
tira reactiva dejamos unos segundos y luego la retiramos para
observar y comparar la tira con la leyenda.
Manual de laboratorio Bioqumica General
3. Se
colocar lo
siguiente dependiendo el resultado
o (+)
. De baja cantidad
o (+)(+). En cantidades regulares
o (+)(+)(+) en grandes cantidades
Leucocitos..(+)
Nitratos --Urobilingeno:...(+)
Protenas... (+)
Ph. --Sangre.. --Gravedad especifica (+)(+)
Cetona. --Bilirrubina... (+)
Glucosa..... (+)
IDENTIFICACIN DE GLUCOSA ( PRUEBA FEHLING)
Otros mtodos para la determinacin de glucosa en orina:
Manual de laboratorio Bioqumica General
o Mtodo de benedict:
o nylander
o tiras reactivas.
FUNDAMENTO
El ensayo con el licor de Fehling se fundamenta en el poder reductor
del grupo carbonilo de un aldehdo.
ste se oxida
un cido
carboxlico y reduce la sal de cobre (II) en medio alcalino a xido de
cobre(I),
que
forma
un precipitado de
color
rojo.
Un
aspecto
importante de esta reaccin es que la forma aldehdo puede
detectarse fcilmente aunque exista en muy pequea cantidad. Si
un azcar reduce el licor de Fehling a xido de cobre (I) rojo, se dice
que es un azcar reductor.
Esta reaccin se produce en medio alcalino fuerte, por lo que algunos
compuestos no reductores pueden enolizarse dando lugar a un falso
positivo
MUESTRA 1:
Para identificar si hay presencia de glucosa se procede a hacer la
prueba.
1. En un tubo de ensayo colocamos 5ml de reactivo fehling junto con
la orina que se va a analizar, se pone a calentar la muestra hasta
que esta ebulla
2. Observamos que el azul mantiene su misma coloracin
Manual de laboratorio Bioqumica General
MUESTRA 2:
Para identificar si hay presencia de glucosa se procede
a hacer la prueba.
1. En un tubo de ensayo colocamos 5ml de reactivo
fehling junto con la orina que se va a analizar, se pone
a calentar la muestra hasta que esta ebulla.
Manual de laboratorio Bioqumica General
2.
Observamos que el azul se torno rojo (+)(+)(+)
Nota: la
reaccin que se
produce entre la
glucosa y el
reactivo fehling
es una reaccin
IDENTIFICACION
DE SALES
redox
BILIARES
MUESTRA 1:
1. En
un tubo de ensayo se agrega 1gr, de
azufre, junto a la orina la cantidad de
del
tubo.
2.
Observamos que el azufre se mantiene
en
la superficie, lo que indica que no hay
presencia de patgenos.
Manual de laboratorio Bioqumica General
IX.
RESULTADOS
IDENTIFICACION DE GLUCOSA
La prueba de fehling ser positiva si aparece un precipitado,
en funcin del cual nos indicar si existe ms o menos cantidad
de glucosa.
o Si aparece un precipitado amarillo se considera +,
o si el color que aparece es amarillo-anaranjado, se considerar
++
o y, por ltimo, habr +++ cuando el precipitado sea rojo.
1. MUESTRA 1:
Al realizar la prueba apareci un precipitado de color rojo por lo
que resulta tener alto contenido de glucosa (+)(+)(+).
Manual de laboratorio Bioqumica General
2.
MUESTRA 2:
Al realizar el segundo anlisis no
se vio un precipitado (la
coloracin no cambia se mantiene en azul).
IDENTIFICACIN DE SALES BILIARES:
X.
DISCUCIONES
XI.
CONCLUSIONES
La orina patolgica:
Aspecto:
o La orina que analizamos tubo una turbidez intensa ( patlogica)
o La turbidez se presenta como resultado de infecciones urinarias
o La orina tambin se enturbia por la presencia de eritrocitos,
leucocitos y bacterias.
Manual de laboratorio Bioqumica General
PRACTICA N 03
AISLAMIENTO DE CASEINA
I.
INTRODUCCION:
II.
MARCO TERORICO:
La casena es un conjunto heterogneo de protenas por lo que es difcil
fijar una definicin, sin embargo todas las protenas englobadas en lo
que se denomina casena tienen una caracterstica comn que
precipitan cuando se acidifica la leche a pH 4.6 por ello a la casena
tambin se le suele denominar protena insoluble de la leche.
A este pH (4,6), la casena precipita, debido a la reduccin de
repulsiones intermoleculares. A diferencia de muchas otras protenas, la
casena no precipita al calor. Precipita bajo la accin de la renina (enzima
proteoltica presente en el estmago de terneros) para formar la
paracasena. Al precipitar por accin de cidos se le llama casena cida.
Este precipitado blanco forma la base para la elaboracin de todo tipo de
quesos. La secuencia peptdica de la casena contiene un nmero
inusual de residuos de prolina (Ca. 15%). Como resultado, es
relativamente hidrofbica (poco soluble en agua) y carece de estructura
secundaria o terciaria definidas. En la leche se encuentra como
suspensin de partculas que asemeja a las micelas de surfactantes
(pequeas esferas hidroflicas en el exterior e hidrofbicas en el interior).
Estas micelas de casena se estabilizan por iones de calcio e
interacciones hidrofbicas.
Manual de laboratorio Bioqumica General
La casena es una protena de la leche del tipo fosfoprotena que se
separa de la leche por acidificacin y forma una masa blanca. Las
fosfoprotenas son un grupo de protenas que estn qumicamente
unidas a una sustancia que contiene cido fosfrico, por lo tanto su
molcula contiene un elemento fsforo. La casena representa cerca del
77 al 82 por ciento de las protenas presentes en la leche y el 2.7 por
ciento en la composicin de la leche lquida.
Cuando coagula con renina, es llamada paracasena, y cuando coagula a
travs de la reduccin del pH es llamada casena cida. Cuando no est
coagulada se le llama caseingeno.
La casena es un slido blanco-amarillento, sin sabor ni olor, insoluble en
agua. Se dispersa bien en un medio alcalino, como una solucin acuosa
de hidrxido de sodio: NaOH, formando caseinatos de sodio.
La reaccin de Biuret es un procedimiento utilizado para identificar la
presencia de protenas en una mezcla. La reaccin debe su nombre al
biuret, una molcula formada a partir de dos de urea (H2N-CO-NH-CONH2), que es la ms sencilla que da positiva esta reaccin. El reactivo de
Biuret contiene CuSO4 en solucin acuosa alcalina de NaOH o KOH. La
reaccin se basa en la formacin de un compuesto de color violeta (cuya
intensidad de color depende de la concentracin de protenas), debido a
la formacin de un complejo de coordinacin entre los iones Cu2+ y los
pares de electrones no compartidos del nitrgeno que forma parte de los
enlaces peptdicos.
PUNTO ISOELCTRICO.
Todas las protenas tienen una carga neta dependiendo del pH del medio
en el que se encuentren y de los aminocidos que la componen, as
como de las cargas de cualquier ligando que se encuentre unido a la
protena de forma covalente (irreversible).
Debido a la composicin en aminocidos de la protena, los radicales
libres pueden existir en tres formas dependiendo del pH del medio:
catinicos, neutros y aninicos.
Las protenas tienen un pH caracterstico, en donde su carga neta es
cero. A este pH se le denomina punto isoelctrico (pI). En el punto
isoelctrico (pI), se encuentran en equilibrio las cargas positivas y
negativas por lo que las protenas presenta su mxima posibilidad para
ser precipitadas al disminuir su solubilidad y facilitar su agregacin.
III.
OBJETIVOS:
Manual de laboratorio Bioqumica General
Aislar la protena casena de la leche de vaca, aprovechando el
punto isoelctrico de dicha protena.
Determinar la concentracin de protenas en la leche
Determinar el pH.
Determinar la densidad de la leche.
IV.
MATERIALES Y METODOS:
MATERIALES:
vasos de precipitacin
pipetas
buretas
soporte universal
tiras reactivas para determinar pH(0-7)
lactodensmetro
REACTIVOS:
Fenolftalena
Formol neutro
NaOH 0,1N
Leche fresca
Cultivo
Pastilla para cuajar
V.
PROCEDIMEINTOS
1. AISLAMIENTO DE CASEINA
Utilizamos formol neutro para el aislamiento de casena.
Se preparan 2 muestras en un matraz 20ml cada una.
2. CALCULO DE PH
FUNDAMENTO:
La leche de vaca recin ordeada y sana, es ligeramente cida,
con un pH comprendido entre 6,5 y 6,8 como consecuencia de la
presencia de casenas, aniones fosfrico y ctrico, principalmente.
Estos valores se aplican solamente a temperaturas cercanas a
25C
PROCEDIMIENTO:
Colocamos la leche en un vaso de precipitacin.
Manual de laboratorio Bioqumica General
Colocar la tira reactiva para clculo de pH dentro del vaso de
precipitacin.
Observamos la coloracin en la tira y la comparamos con el
de la leyenda para as determinar el pH de la leche.
3. CALCULO DE ACIDEZ
FUNDAMENTO
Los valores normales de acidez titulable en leche estn
comprendidos entre 16D y 19D (grados Dornic) que expresado
en porcentaje del cido mayoritario seran 0.16-0.19% de cido
lctico. Las alteraciones en la leche durante la sntesis o
almacenamiento pueden originar cambios en la acidez. Adems,
determinadas adulteraciones hacen variar estos valores: el
aguado la rebaja, el desnatado y adicin de suero no la modifican
y la neutralizacin la rebaja considerablemente. Aunque existen
diferentes modos de expresar la acidez la forma ms habitual de
expresin son los grados Dornic (D) y el procentaje de cido
lctico.
PROCEDIEMIENTO:
Se toma los 20 ml de leche (de la muestra que aislamos la
casena anteriormente) y se agrega 3 gotas de fenolftalena.
Luego procedemos a titular con NaOH 0.1 N., observar el
viraje y anotar el volumen gastado de NaOH.
Calculamos el porcentaje de acidez, y para ello utilizamos la
siguiente formula.
Acidez = Vgastado x NaOH x K x100
Manual de laboratorio Bioqumica General
Vtotal
MUESTRA 1:
Volumen gastado: 4.4ml
Realizamos los clculos
Acidez = 4.4 x 0.1N x 0.09 x 100
20ml
Acidez = 0.198%
4.
MUESTRA 2:
Volumen gastado: 3.1ml
Realizamos los clculos
Acidez = 3.1ml x 0.1N x 0.09 x 100
20ml
Acidez = 0.14%
CALCULO DE PROTEINAS ( METODO DE SORENSEN WALKER)
FUNDAMENTO
Est tcnica determina el contenido en protenas de la leche mediante
una valoracin cido-base, ya que tras la adicin de formol a la muestra,
el formaldehido se une a los grupos amino de los aminocidos de las
protenas dejando los grupos carboxilos libres. Este hecho produce
cambios en la acidez titulable de la leche siendo valorada con hidrxido
sdico. La cantidad de hidrxido sdico utilizado en la neutralizacin es
utilizado para calcular la cantidad de protenas presente en la muestra.
PROCEDIMIENTO:
Tomar 20 mL de leche en un matraz erlenmeyer.
Adicionar unas gotas de fenolftalena.
Neutralizar la acidez titulable natural de la leche con la solucin de
hidrxido sdico hasta la aparicin de un color rosa.
Aadir posteriormente a la leche neutralizada 4 mL de formol para
dejar libres los grupos carboxilos de los aminocidos. Tras la adicin del
formol la muestra se vuelve a acidificar y se muestra nuevamente de
color blanco.
Manual de laboratorio Bioqumica General
Aadir unas gotas de fenolftalena y valorar la acidez con hidrxido
sdico, hasta la aparicin nuevamente del color rosa.
Protenas = Vgastado x K
Protenas = Vgastado x K
Manual de laboratorio Bioqumica General
5. CALCULO DE DENSIDAD: (TECNICA DEL
LACTODENSIMETRO)
FUNDAMENTO
La densidad es una propiedad fsica utilizada para comparar las masas
de diferentes sustancias o de una misma bajo diferentes condiciones. En
la densidad de la leche influyen todos los constituyentes normales, as
como todas aquellas sustancias extraas que se adicionan de forma
fraudulenta, tanto slidos como lquidos. Existen muchas causas que
actan variando la densidad de la leche, como son la composicin
qumica,
la
temperatura
de
medicin,
la
temperatura
de
almacenamiento, el tiempo transcurrido desde el ordeo, el ordeo
fraccionado, la centrifugacin y otras operaciones tecnolgicas. As, la
Manual de laboratorio Bioqumica General
densidad depende no slo, de la temperatura del momento de la
determinacin, sino tambin de las temperaturas anteriores, y adems
este parmetro adquiere su valor ms bajo poco despus del ordeo,
aumentando despus lentamente. Por ello la temperatura a que ha
estado sometida la muestra de leche influye muy ligeramente en el
resultado final.
Para la determinacin de la densidad de la leche vamos a utilizar la
tcnica de lactodensimetra. Los lactodensmetros son aermetros,
cuerpos flotadores de vidrio lastrados en su parte inferior con varilla
graduada, y que en ocasiones pueden llevar incorporado un termmetro,
permitiendo la lectura paralela de la densidad. Y la temperatura. Cuando
el aermetro se introduce en la leche sufre un impulso hacia arriba igual
al peso del lquido desaloja, quedando el valor de densidad reflejado en
la varilla graduada.
PROCEDIMIENTO:
Llenamos la probeta con la leche
Medimos la temperatura de la leche (se encontr a 25C)
Introducimos con cuidado el lactodensmetro en la leche manteniendo
el aparato en el eje de la probeta y provocar un ligero movimiento de
rotacin.
Esperamos a que se estabilice y realizamos la lectura de la densidad.
El valor que obtuvimos fue de 0.027, pero se le suma uno al este valor
por lo tanto el valor de la densidad seria 1.027.
Manual de laboratorio Bioqumica General
VI.
RESULTADOS:
CALCULO DE ACIDEZ
La leche fresca tiene normalmente de 1619Dornic lo que en porcentaje seria 0.16
o
0.19
o Una acidez inferior a 16D son sospechosas de aguado,
neutralizacin, o de proceder de vacas con mamitis.
o Valores de acidez superior a 19D son imputables a leches de ms
de 10 horas (ordeo de la noche)
o y valores superiores a 23D corresponden a leches muy cidas
que han perdido la estabilidad trmica por lo que no podran
pasterizarse y/o esterilizarse, ya que se producira una
coagulacin.
MUESTRA 1:
El resultado que se obtuvo al realizar la prueba de acidez
fue 0.198% lo que nos indica que leche utilizada para esta
prueba si esta dentro del rango aceptable como se explica en el
fundamento presentado anteriormente.
MUESTRA 2:
Al realizar el anlisis para la segunda muestra de leche se
obtuvo el siguiente resultado; 0.14%, lo que vendra a ser un
nivel muy bajo de acidez, por lo que se concluimos que la leche
fue adulterada.
CALCULO DE pH:
MUESTRA 1:
Manual de laboratorio Bioqumica General
Para la muestra 1 el valor del pH fue de 5
MUESTRA 2:
Para la muestra 2 el valor de pH fue de 6
CALCULO DE PROTEINAS:
Las protenas normales en la leche estn en un rango de 2,8 3.4
MUESTRA1:
El resultado que obtuvimos para la primera muestra fue 2.2, un
rango muy bajo en el contenido de protenas en la leche, y esto
se debe a distintos factores (adulteracin de la leche, etc)
MUESTRA 2:
El resultado que se obtuvo en esta muestra fue 2,0; por lo tanto
el contenido de protenas de la muestra 2 es relativamente bajo,
y esto tambin se debe a que la leche pudo ser adulterada.
CALCULO DE DENSIDAD:
La densidad vara segn el tipo de leche.
o Para la leche de vaca oscila entre 1.028 y 1.042, siendo el valor
medio de 1.031.
o Las adulteraciones influyen sobre el valor de la densidad. As el
aguado la rebaja, el desnatado y la adicin de leche desnatada
la aumentan. Sin embargo la densidad de la leche permanece
invariable si la leche es aguada con soluciones preparadas que
tengan la misma densidad o es aguada y desnatada al mismo
tiempo.
MUESTRA1:
Al realizar la prueba para esta muestra obtuvimos un valor de
1.027.
VII.
DISCUSIONES:
Manual de laboratorio Bioqumica General
VIII. CONCLUSIONES
Podemos concluir que las diferentes pruebas qumicas empleadas
en la leche, nos ayudan a conocer la composicin qumica,
determinar la calidad de la leche, si ha sufrido alteraciones y si
pueden ser utilizadas para el consumo humano.
Cada prueba es importante ya que determina varios factores que
pueden alterar la calidad de la leche como son, la acidez, pH,
protenas entre otras.
Todas las pruebas empleadas son diferentes, ya que todo depende
del mtodo utilizado para la determinacin de las pruebas ya
mencionadas.
Manual de laboratorio Bioqumica General
PRACTICA N 05:
DETERMINACIN DEL SISTEMA REDOX DETERMINACIN DE LA VITAMINA C
I.
INTRODUCCIN:
Las vitaminas son compuestos orgnicos sencillos que nos sirven
como combustible metablico. Son indispensables para el
mantenimiento de la vida, actuando en biocatalizadores en gran
cantidad de reacciones bioqumicas ya que las vitaminas suelen ser
coenzimas o componentes de coenzimas.
Son producidas por vegetales y microorganismos. Los animales y, en
especial el hombre, no suelen sintetizarlas o, si lo hacen, es en
cantidades insuficientes.
Los seres vivos necesitan ciertas cantidades diarias de cada vitamina
y cualquier alteracin de4 estos lmites origina trastornos de los
procesos metablicos, que pueden derivar de tres tipos de
alteraciones: si la carencia es total (avitaminosis), si la insuficiencia o
carencia es parcial (hipovitaminosis); si existe un exceso de
vitaminas (hipervitaminosis).
Las vitaminas son sustancias que se alteran con facilidad, resisten
mal a los cambios de temperatura y los almacenamientos
prolongados. Comprenden un gran nmero de molculas, que se han
desglosado en dos grupos: vitaminas liposolubles, de naturaleza
lipdica (vitaminas A, D, E y K) y vitaminas hidrosolubles(C, H-biotinay las vitaminas del complejo).
II.
MARCO TEORICO
El enantimero L del acido ascrbico, tambin conocido como
vitamina C, es un acido orgnico y un antioxidante perteneciente al
grupo de vitaminas hidrosolubles. No se sintetiza en el organismo,
por lo cual tiene que ser aportada en la dieta. Se encuentra,
principalmente en verduras y frutas frescas y en zumos de ctricos.
La mayora de las especies de animales y vegetales sintetizan su
propia vitamina C; por lo cual no constituye una vitamina para ellos.
La sntesis se realiza en etapas catalizadas por cuatro enzimas que
convierten la glucosa en acido ascrbico.
Se considera que las necesidades diarias de acido ascrbico para un
adulto no exceden de los 60mg y que las cantidades superiores a las
3 g diarios causan acidificacin de la orina e incrementa el
consiguiente riesgo de clculos urinarios.
cido ascrbico (C6H8O6)
Manual de laboratorio Bioqumica General
El acido ascrbico y sus sales de sodio, potasio y calcio (ascorbatos
minerales) son solubles en agua por lo que no protegen a las grasas
de la oxidacin. Los ascorbatos minerales se preparan a partir de
reaccin del acido con los respectivos carbonatos y bicarbonatos de
calcio, magnesio, potasio y sodio,
Los ascorbatos minerales pueden ser mejor tolerados que la vitamina
en su forma acida. El ascorbato acta como antioxidante debido a
que su oxidacin es menos energtica que a de las otras especies.
Las especies oxidantes, tales como el radical hidroxilo formado a
partir de perxido de hidrgeno, contienen un electrn no apareado
que las hace extremadamente reactivas y dainas a nivel molecular,
tanto para el ser humano como para las plantas.
Esto se debe a su interaccin con cidos nucleicos, las protenas y los
lpidos. Las especies oxidantes con oxgenos reactivos pueden
abstraer un tomo de hidrogeno del ascorbato, que se convierte en
monodeshiroascorbato que inmediatamente pierde otro electrn
para convertirse en deshidroascorbato.
III.
OBJETIVOS:
Objetivo general
Determinar el contenido de acido ascrbico (vitamina C) en zumos de frutas ctricas y
comparar el contenido de dicha vitamina en bebidas comerciales que dicen ser
enriquecidas con la misma.
IV.
V.
MATERIALES Y METODOS:
MATERIALES:
probeta
matraz erlenmeyer
tubos de ensayo
gradilla
zumos de fruta
PROCEDIEMIENTO:
PASO 1:
1. En un tubo de ensayo se vierten 1 ml. de zumo de fruta.
2. Posteriormente se titula aadiendo gotas de diclorofenol-indofenol
que se encuentra en la bureta y observamos el cambio de
coloracin que pasa del azul-oscuro a rosa plido acabando
prcticamente incoloro.
3. Seguir aadiendo gotas hasta que el color rosado se mantenga
Manual de laboratorio Bioqumica General
4. Anotamos el volumen gastado. (el volumen gastado nos dar idea
de la cantidad de vitamina C que contiene cada una de las frutas
que se est analizando)
5. Repetir el mismo proceso con cada una de las muestras
EXPLICACION:
La causa de
sta prdida de
color se debe a
que los tomos de
hidrgeno de los
carbonos unidos por
un doble enlace
se eliminan, oxidada
de la vitamina,
actuando el
diclorofenol
-indofenol como dador
de electrones (hidrgenos) y dando la forma reducida de colorante
transformndose-n cido de-hidro-ascrbico que es la forma.
VI.
RESULTADOS:
Gasto en la titulacin:
Zumo de naranja: 1.1ml
Cifrut de naranja: 0.4ml
Cifrut de granadilla: 0.3ml
Zumo de lima: -- Zumo de limn: 0.7ml
Manual de laboratorio Bioqumica General
Jugo de
fruta
Solucin
Lima
2ml zumo/ 9 ml
de agua
destilada
1ml zumo/ 9 ml
de agua
destilada
1ml zumo/ 9 ml
de agua
destilada
Limn
Cifrut de
granadill
a
Naranja
Cifrut de
naranja
1ml zumo/ 9 ml
de agua
destilada
1ml zumo/ 9ml
de agua
destilada
Cambio de
color
(azul a
rosa palido)
Nro de
gotas
ml
NO
______
______
SI
13 gotas
0.7 ml
SI
5 gotas
0.3 ml
SI
17 gotas
1.1 ml
SI
7 gotas
0.4ml
Ahora se proceder a hacer los respectivos clculos para ver
cul de todos los ctricos tiene ms vitamina C. para ello se
utilizar la siguiente formula
Vgastado x K x 100 =
%vitamina C
Donde:
1ml
Vgastado: es el volumen gastado en
la titulacin
K: constante de ctricos
1ml: esto es en relacin al valor de jugo del ctrico utilizado en el
tubo de ensayo
Zumo de naranja:
1.1x 0.088 x 100 = %vitamina C
1ml
9.68 = %vitamina C
Bebida comercial (cifrut naranja)
0.4 x 0.088 x 100 = %vitamina C
1ml
3.52 = %vitamina C
Manual de laboratorio Bioqumica General
Bebida comercial (cifrut de granadilla)
0.7 x 0.088 x 100 = %vitamina C
1ml
VI.16 = %vitamina C
Zumo de lima:
No se pudo determinar ya que el zumo
de lima no reacciono con 2-6
diclorofenol.
Zumo de limn:
0.7 x 0.088 x 100 = %vitamina C
1ml
6.16 = %vitamina
VII.
DISCUSION:
Manual de laboratorio Bioqumica General
VIII.
CONCLUSIONES:
Con la experiencia llegamos a la conclusin de que notablemente el
zumo de frutas con mayor cantidad de vitamina C de los zumos de
diferentes frutas utilizadas es la naranja con un porcentaje de 9.68
%, lo que nos hace llegar a la conclusin de que no influye la acides
de la fruta para la determinacin de contenido de Vitamina C.
El contenido de cido ascrbico (vitamina C) en los jugos de frutas
puede variar por prdidas durante el procesado y almacenamiento.
La determinacin del cido ascrbico nos permite inferir sobre el
valor nutritivo del alimento.
A diferencia de otras vitaminas el humano no sintetiza vitamina C
y tenemos que tomarlas de frutas principalmente, ya que es
necesario para el ser humano, se necesita 60mg diarios en adultos.
El mtodo por titulacin visual con 2,6 diclorofenol indofenol
es un mtodo rpido y seguro para determinar el porcentaje de cido
ascrbico (vitamina C) en los zumos de frutas.
Вам также может понравиться
- Instalaciones Sanitarias Domiciliarias Industriales e Ingeniería de Medio AmbienteДокумент340 страницInstalaciones Sanitarias Domiciliarias Industriales e Ingeniería de Medio AmbienteBrandon Baquerizo-Salas100% (4)
- Bicarbonato de Sodio Sircus 4Документ5 страницBicarbonato de Sodio Sircus 4Ulisez NocturnalОценок пока нет
- Ensayos de Cables - NormativaДокумент11 страницEnsayos de Cables - Normativastarki__066100% (1)
- Protocolos de Catacion de SCAAДокумент6 страницProtocolos de Catacion de SCAARickyFrancoCoaguila100% (2)
- Control de Calidad de Los AlimentosДокумент124 страницыControl de Calidad de Los Alimentosdiciembre25100% (1)
- Cables de 0'6 - 1kvДокумент22 страницыCables de 0'6 - 1kvvladekiОценок пока нет
- Anexo 06 - Determinacion Del Punto de CongelacionДокумент3 страницыAnexo 06 - Determinacion Del Punto de CongelacionRickyFrancoCoaguilaОценок пока нет
- Medición de pH en leche con analizador ultrasónicoДокумент9 страницMedición de pH en leche con analizador ultrasónicoRickyFrancoCoaguilaОценок пока нет
- Anexo 05 - Calibracion Facil Del Equipo Con Parametros BasicosДокумент3 страницыAnexo 05 - Calibracion Facil Del Equipo Con Parametros BasicosRickyFrancoCoaguilaОценок пока нет
- Anexo 08 - Medición de ConductividadДокумент5 страницAnexo 08 - Medición de ConductividadRickyFrancoCoaguilaОценок пока нет
- Fiscalizacion Laboral UigvДокумент45 страницFiscalizacion Laboral UigvAnonymous PvjOfZHsОценок пока нет
- Aprueban Norma Sanitaria para Restaurantes y Servicios Afin Resolucion Ministerial No 822 2018minsa 1689230 3Документ2 страницыAprueban Norma Sanitaria para Restaurantes y Servicios Afin Resolucion Ministerial No 822 2018minsa 1689230 3hbazanОценок пока нет
- ElevacionesДокумент1 страницаElevacionesRickyFrancoCoaguilaОценок пока нет
- Baño Escala 1 10 A4Документ1 страницаBaño Escala 1 10 A4RickyFrancoCoaguilaОценок пока нет
- Goma GellanДокумент5 страницGoma GellanRickyFrancoCoaguilaОценок пока нет
- Análisis leche LactoscanДокумент6 страницAnálisis leche LactoscanRickyFrancoCoaguilaОценок пока нет
- Diagrama de Operaciones y ProcesosДокумент2 страницыDiagrama de Operaciones y ProcesosRickyFrancoCoaguilaОценок пока нет
- Reglamento Residuos SolidosДокумент23 страницыReglamento Residuos SolidosAbner Segundo Lescano PachamoraОценок пока нет
- Control Ambiental de VinoДокумент4 страницыControl Ambiental de VinoRickyFrancoCoaguilaОценок пока нет
- CocimientoДокумент7 страницCocimientoRickyFrancoCoaguilaОценок пока нет
- Insumos de La Elaboración de VinoДокумент3 страницыInsumos de La Elaboración de VinoRickyFrancoCoaguilaОценок пока нет
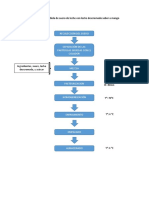
- Elaboración de Bebida de Suero de Leche Con Leche Descremada Sabor A MangoДокумент1 страницаElaboración de Bebida de Suero de Leche Con Leche Descremada Sabor A MangoRickyFrancoCoaguilaОценок пока нет
- Envases de HojalataДокумент1 страницаEnvases de HojalataRickyFrancoCoaguilaОценок пока нет
- Yogurt Frutado Etiqueta FinalДокумент1 страницаYogurt Frutado Etiqueta FinalRickyFrancoCoaguilaОценок пока нет
- Examen FinalДокумент1 страницаExamen FinalRickyFrancoCoaguilaОценок пока нет
- LABmatlab PDFДокумент8 страницLABmatlab PDFRickyFrancoCoaguilaОценок пока нет
- Planificacion y Control de La ProduccionДокумент80 страницPlanificacion y Control de La ProduccionRickyFrancoCoaguilaОценок пока нет
- Determanación de Contenido de HumedadДокумент2 страницыDetermanación de Contenido de HumedadRickyFrancoCoaguilaОценок пока нет
- Yogurt Frutado Etiqueta FinalДокумент1 страницаYogurt Frutado Etiqueta FinalRickyFrancoCoaguilaОценок пока нет
- Comunicacion Inalambrica 1Документ13 страницComunicacion Inalambrica 1Wilmer SalvadorОценок пока нет
- Erp en El Peru1Документ9 страницErp en El Peru1RickyFrancoCoaguilaОценок пока нет
- Importancia de AceitesДокумент3 страницыImportancia de AceitesRickyFrancoCoaguilaОценок пока нет
- Aceites de OlivaДокумент2 страницыAceites de OlivaRickyFrancoCoaguilaОценок пока нет
- Vida UtilДокумент3 страницыVida UtilRickyFrancoCoaguilaОценок пока нет
- Cortes de ResДокумент8 страницCortes de ResRickyFrancoCoaguilaОценок пока нет
- Proceso de elaboración de yogurtДокумент45 страницProceso de elaboración de yogurtIvan Dario Pineda PatiñoОценок пока нет
- Manual PracticasДокумент46 страницManual PracticasZerrath Zamudio100% (2)
- Determinaciones Analiticas en Leche FrescaДокумент10 страницDeterminaciones Analiticas en Leche FrescaCristian R. RoldánОценок пока нет
- p10 Glicólisis PH y Acidez de CarnesДокумент8 страницp10 Glicólisis PH y Acidez de CarnesAlvaro ChacónОценок пока нет
- Parametro Fisico-Quimicos de La LecheДокумент13 страницParametro Fisico-Quimicos de La LecheDaKa GongoraОценок пока нет
- Parámetros Inorganicos y Calidad Del AguaДокумент9 страницParámetros Inorganicos y Calidad Del AguaRaví García AreuОценок пока нет
- Ejercicios Sobre Equilibrio Ionico (Acido-Base) PDFДокумент3 страницыEjercicios Sobre Equilibrio Ionico (Acido-Base) PDFCamila MosqueraОценок пока нет
- ANÁLISIS DE HARINASДокумент9 страницANÁLISIS DE HARINASFiorella SotoОценок пока нет
- Durazno Blanquillo Cayran Tesis 1Документ2 страницыDurazno Blanquillo Cayran Tesis 1Jhonatan Torres QuirozОценок пока нет
- Trabajo Del Ing Raul, Navarrete - LISTOДокумент13 страницTrabajo Del Ing Raul, Navarrete - LISTOGerson G. Pachas LoyolaОценок пока нет
- Determinación de parámetros físicos y químicos de frutas y verdurasДокумент15 страницDeterminación de parámetros físicos y químicos de frutas y verdurasGabriel ZambranoОценок пока нет
- GOWIN-TABLAS 2. (Reparado) PDFДокумент1 страницаGOWIN-TABLAS 2. (Reparado) PDFlchemistry10Оценок пока нет
- PRACTICA N1 Leche Final 2Документ23 страницыPRACTICA N1 Leche Final 2Jhonathan Camacho CaceresОценок пока нет
- Drenaje Ácido en RocaДокумент13 страницDrenaje Ácido en RocaJhoe LozaОценок пока нет
- Tecnica para La Determinacion de AcidezДокумент8 страницTecnica para La Determinacion de AcidezAndrea Rojas VargasОценок пока нет
- Laboratorio 9 - Cinetica QuimicaДокумент4 страницыLaboratorio 9 - Cinetica QuimicaAlex Ostos AlvaОценок пока нет
- Capituo Xi Acidez Total Titulable PDFДокумент26 страницCapituo Xi Acidez Total Titulable PDFMaria Guadalupe Yaranga AvendañoОценок пока нет
- VinoДокумент11 страницVinoAnnekary Olivares HernandezОценок пока нет
- Reaccion Del SueloДокумент20 страницReaccion Del SueloEnmanuel Valero100% (1)
- Informe 6 PectinaДокумент4 страницыInforme 6 PectinaNico Ariel JaramilloОценок пока нет
- Guia 7 Acidez IntercambiableДокумент5 страницGuia 7 Acidez IntercambiableHernan DmgzОценок пока нет
- Control de Calidad de Grasas y Aceites ComestiblesДокумент3 страницыControl de Calidad de Grasas y Aceites ComestiblesMauricio Tuiran RuizОценок пока нет
- Informe de Potenciometria - PHДокумент18 страницInforme de Potenciometria - PHNicole Melly HuertaОценок пока нет
- Edafologia - Informe 06 (Determinacion Del PH)Документ15 страницEdafologia - Informe 06 (Determinacion Del PH)Edy Leon ChavezОценок пока нет