Академический Документы
Профессиональный Документы
Культура Документы
Mineralización Ósea
Загружено:
Emmanuel CieloОригинальное название
Авторское право
Доступные форматы
Поделиться этим документом
Поделиться или встроить документ
Этот документ был вам полезен?
Это неприемлемый материал?
Пожаловаться на этот документАвторское право:
Доступные форматы
Mineralización Ósea
Загружено:
Emmanuel CieloАвторское право:
Доступные форматы
medigraphic
Artemisa
en lnea
Jul.-Sep. 2008
Volumen 4, Nmero 3
El proceso de remodelacin sea
Jaime Gutirrez Gmez*
INTRODUCCIN
Objetivos:
El proceso de remodelacin sea
a) Analizar la historia del proceso de remodeimplica una serie de pasos que se
lacin sea y del neoformato durante el alargamiento de un hueso.
inician a partir de un estmulo del
b) Revisar la fisiologa sea durante un procetejido seo, que puede ser induciso de alargamiento.
do o provocado por una lesin.
En el proceso para alargar un
hueso reviste gran importancia saber que el mecanismo clave es la regeneracin sea (osteognesis), el proceso natural que repara las fracturas. Aqu, con
la ayuda de la ciruga y de un dispositivo ortopdico, se logra confundir al
hueso y hacerlo crecer un milmetro diario en promedio.
Para comprender mejor este proceso, es necesario revisar algunos aspectos
histolgicos y fisiolgicos del hueso. La homeostasis esqueltica, tambin llamada
homeostasis mineral del organismo, est regulada por interacciones entre rganos,
clulas, factores de seal, hormonas y factores de crecimiento que actan a nivel
intra y extracelular para regular el metabolismo del calcio, el cual es fisiolgicamente necesario para la formacin y remodelado seo a lo largo de la vida.1
El tejido seo se considera un tejido conectivo especializado que se caracteriza por su rigidez y gran resistencia, tanto a la traccin como a la compresin,
existiendo dos tipos de hueso: Compacto (Figura 1) y esponjoso (Figura 2).
Adems, el tejido seo est constituido por cuatro componentes microestructurales: clulas, matriz orgnica, matriz inorgnica y factores solubles de seal
integrados dentro de ste.1,2
CLULAS SEAS
Los osteoblastos, los osteocitos y los osteoclastos son las clulas identificables en el tejido seo. Las primeras derivan de clulas mesenquimatosas pluripotenciales, tambin llamadas clulas madre. Son clulas polarizadas diferen-
Catedrtico Departamento de Morfofisiologa. Escuela de Medicina IESCH Tuxtla Gutirrez,
Chiapas, y Profesor adjunto del Curso de Postgrado en Ortopedia, Hospital General Regional
Tuxtla Gutirrez, Chiapas. Vicepresidente de la AMOT.
www.medigraphic.com
Direccin para correspondencia:
Dr. Jaime Gutirrez Gmez.
Mdica Norte, 4 Norte-Poniente 836-3 Col. Centro. Tuxtla Gutirrez, Chiapas, Mxico.
Correo Electrnico: jaimegtz_doc@yahoo.com.mx
170
Gutirrez Gmez J. El proceso de remodelacin sea
Lminas
intersticiales
Lminas
concntricas
Conductos de Havers
Lminas
circunferenciales
Periostio
Vasos dentro de
los conductos de
Havers
Ostefitos en
sus nichos
Vasos comunicantes
en los canales de
Volkman
Figura 1. Hueso compacto con todas sus estructuras.
ciadas que sintetizan
el colgeno y la sustancia fundamental
sea. Participan en el
Espacios que contienen
proceso de mineralimdula sea y vasos
zacin de la matriz or- Trabculas
seas
gnica produciendo
vesculas de matriz
que acumulan iones
Calcio y Fosfato y son
ricas en fosfatasa alcalina y pirofosfatasa,
enzimas que inducen
Figura 2. Hueso esponjoso.
la creacin de centros
de nucleacin para el
depsito de las sales minerales. Su vida activa se encuentra entre una y diez
semanas; al final de este periodo toman dos destinos posibles: ser rodeadas por
la matriz sea que producen y convertirse en osteocitos (15%), o permanecer
en la superficie del tejido seo recin formado, aplanndose y constituyendo las
clulas de revestimiento seo (Figura 3a).2
El osteocito es la clula sea madura, relativamente inactiva. Su nutricin
depende de canalculos que penetran la matriz sea y se conectan a los osteocitos por sus extensiones. La nutricin sea se realiza a travs de canales vasculares que penetran al hueso o se ubican en las membranas conjuntivas que
revisten el periostio y el endostio (Figura 3b).2
El osteoclasto es la clula encargada del mantenimiento de la homeostasis
sea. Son capaces de sintetizar y reabsorber, en forma limitada, componentes
www.medigraphic.com
171
Ortho-tips Vol. 4 No. 3 2008
de la matriz sea (ostelisis osteoctica) regulando la calcemia. Su vida media
es de varios aos, incluso dcadas; es incapaz de renovarse; su reemplazo se
hace a travs de la diferenciacin de las clulas precursoras de los osteoblastos. Se localizan en depresiones superficiales de la matriz sea llamadas lagunas de Howship, adosadas a la superficie de tejido seo que debe ser removido. Tienen receptores para la calcitonina y producen fosfatasa cida tartrato
resistente (Figura 3c).1,2
PROTENAS NO COLGENAS
Osteonectina. Es una protena de peso molecular de 32,000 Kd, que se une al
colgeno y a su vez a los cristales de hidroxiapatita para favorecer la mineralizacin.
Osteocalcina. Tiene un peso molecular de 6,000 Kd, se identifica por la presencia de residuos y carboxiglutamato que tienen afinidad por el calcio y una
fuerte avidez por la hidroxiapatita sin cristalizar.
Protenas morfogenticas seas. Constituyen una superfamilia de protenas
secretadas por los osteoblastos. Incluyen la BMP-2, BMP-4, BMP-7 y TGF-p.
Estas protenas aumentan la rapidez de formacin y reparacin sea.
Proteoglicanos. Es un grupo de macromolculas asociadas a la superficie
celular, compuestas por una protena central a la que se adhieren cadenas de
glucosaminoglicanos. Su funcin es servir como receptor de membrana (Syndecan), y unirse al colgeno de la matriz extracelular.1-3
Retculo
endoplsmico
Vescula secretora
Mitocondria
Lisosomas
Aparato de
Golgi
www.medigraphic.com
c
Figura 3. a. Osteoblasto.
b. Osteocito.
c. Osteoclasto.
Vacuolas
172
Gutirrez Gmez J. El proceso de remodelacin sea
FISIOLOGA SEA
Fisiolgicamente, la interaccin entre osteoblastos y osteoclastos dinamiza el
proceso de reabsorcin en el que se produce un descenso del pH por la accin de
la anhidrasa carbnica que liberan los osteoclastos para disolver la matriz inorgnica exponiendo la matriz orgnica a la accin de las enzimas proteolticas. La
hormona paratiroidea y la 1,25-dihidroxivitamina D3 influyen sobre los osteoblastos para producir la activacin de los osteoclastos.
Todo este proceso ocurre en la matriz sea, compuesta por colgeno fibrilar (tipos I, II, III, V y XI), no fibrilar (tipo IV) y colgenos de triple hlice interrumpida,
adems de glucoprotenas que modulan la adherencia celular y median en la calcificacin de la matriz orgnica para regular la entrada de las clulas que expresan
factores solubles como las protenas morfogenticas (BMPs), protegiendo y facilitando su liberacin segn los requerimientos. Su funcin es proporcionar dureza y
resistencia a las fuerzas compresivas que recibe el hueso.1,2,4-6
PROCESO DE REMODELACIN SEA
Las clulas mesenquimatosas pluripotenciales se diferencian directamente en el
seno del tejido conjuntivo en clulas formadoras de hueso (osteoblastos) en respuesta a las molculas de adhesin y los factores solubles de seal. Este tipo de
formacin sea directa es lo que caracteriza el desarrollo del hueso intramembranoso (osificacin intramembranosa).
Existe tambin el proceso de osificacin endocondral, en el cual las clulas
mesenquimticas siguen un camino hacia la estirpe celular condrognica en lugar de hacerlo hacia la osteognica; el motivo tampoco est bien identificado,
pero se especula que las BMPs y la sntesis local de factores angiognicos o
angiogenticos como el factor bsico de crecimiento fibroblstico (bFGF), actan en esas localizaciones, modulando la expresin del fenotipo celular hacia
esta lnea condrognica.
Donde se hace ms evidente este proceso es en los centros de osificacin
primaria de los huesos largos, entre la epfisis y la metfisis. En la metfisis,
los condrocitos en diferentes estadios de evolucin se disponen ordenadamente
en forma de columnas longitudinales, lo que permite el crecimiento del hueso
en longitud a travs de los centros de osificacin secundaria cuando los osteoblastos provenientes del pericondrio invaden los espacios dejados por los condrocitos degenerados e inician la formacin sea.1,2,7
Independientemente de la ruta de la histognesis sea, no existe ninguna diferencia bioqumica, morfolgica o funcional entre el hueso endocondral y el intramembranoso, y durante la reparacin sea del esqueleto en el adulto tambin
responde a los mismos factores. Las diferencias entre estos huesos de distinto
origen se encuentran en la carga funcional y la vascularizacin. Por ejemplo, el
hueso intramembranoso tiene una vascularizacin mayor que el de las extremidades, lo que puede ser un factor determinante en cuanto a permitir una mayor
concentracin de BMPs a nivel local.
www.medigraphic.com
173
Ortho-tips Vol. 4 No. 3 2008
La transformacin de hueso esponjoso en hueso compacto se debe al aumento de espesor de las trabculas con la progresiva invasin de los espacios
medulares por parte del tejido mineralizado que causa una reduccin dimensional de las cavidades preexistentes. El hueso que llena estas cavidades se forma de una manera ms lenta, tiene una disposicin ms ordenada y los haces
de colgena se encuentran paralelos entre s constituyendo unas formaciones
denominadas osteonas o sistemas haversianos.
Cuando se produce una fractura, las clulas y las molculas de seal aparecen en el sitio de la lesin para repararla de la misma manera que en el proceso embriognico. En el momento inicial de la fractura se desencadena una respuesta inflamatoria con activacin del complemento y rotura de vasos; la
degradacin proteoltica de la matriz extracelular aporta factores quimiotcticos
para los monocitos y los macrfagos y una vez que stos se activan liberan el
factor de crecimiento de los fibroblastos (FGF) que estimula a las clulas endoteliales a expresar el activador del plasmingeno y la procolagenasa. La sangre
extravasada forma un cogulo, y las plaquetas que lo integran tienen una funcin dual: la hemostasia y la liberacin de factores moduladores para el proceso de reparacin (l PDGF, TGF-, y el FGF).
La zona daada presenta una hipoxia debido a la rotura de los vasos sanguneos y como consecuencia se produce una disminucin del pH, condiciones
necesarias para que acten los macrfagos y los leucocitos polimorfonucleares
que eliminan los detritus celulares, a la vez que secretan factores que promueven la quimiotaxis y la mitognesis.
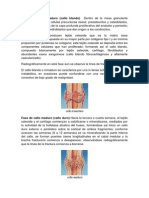
Despus de tres a cinco das de la fractura, se constituye un tejido de
granulacin consistente en vasos, colgeno y clulas. El colgeno ser el sustrato que contenga los factores a los que sern sensibles las clulas y constituir el lugar al que ellas se anclarn cuando lleguen a travs de los vasos, del
periostio, del endostio y de la mdula sea, diferencindose posteriormente en
osteoblastos y condroblastos. La maduracin del tejido de granulacin se produce en varias semanas hasta que se forma el callo seo que ms tarde ser
sustituido por hueso fibroso inmaduro y posteriormente por hueso lamelar. El
papel del callo seo es estabilizar los fragmentos de la fractura, ya que si existe movilidad este proceso no puede llevarse a cabo, con lo que el tejido que
predominar ser de tipo cartilaginoso.
El ltimo proceso que ocurre en la cascada de fenmenos de reparacin sea
es el remodelado, se trata de un proceso de activacin-reabsorcin-formacin,
donde los osteoclastos se activan produciendo las lagunas de Howship, que sern repobladas por osteoblastos que expresan osteoide, y cuando ste se calcifica se restaura la morfologa sea. Este equipo de clulas se denomina unidad
bsica multicelular.
El proceso, activacin-reabsorcin-formacin en los humanos se produce en
un periodo de tiempo comprendido entre 3 y 6 meses; el proceso de remodelado en hueso cortical se lleva a cabo por los osteoclastos que labran un tnel
que posteriormente se repuebla de osteoblastos. A esta unidad funcional que
constituyen ambas clulas se le denomina cono de corte. El cono de corte ac-
www.medigraphic.com
174
Gutirrez Gmez J. El proceso de remodelacin sea
ta en la matriz como una especie de taladro, acompaado por las estructuras
vasculares que crecen a medida que avanza su actividad erosiva. A cierta distancia del frente de erosin se alinean los osteoblastos, bordeando las paredes
erosionadas de la matriz, que se disponen en forma progresiva para cerrar el tnel creado por los osteoblastos pero sin llegar a obliterarlo. El resultado final de
todo este proceso ser un conducto de Havers.1,2,5,7
HISTOGNESIS POR DISTRACCIN
La tcnica de histognesis por distraccin fue descrita por el Doctor Ilizarov en
1951, quien dise el primer mecanismo de fijacin externa que permiti alargar y
transportar el hueso.
Ilizarov descubri que si un hueso se fractura en una zona sana y se empuja
para separarlo, el cuerpo llena el vaco desarrollando nuevo tejido seo, lo que
efectivamente alarga el hueso. El nuevo hueso es tan fuerte como el original
desarrollado en la niez (Hall, 1998). A este tipo de consolidacin sea se le
denomina histognesis por distraccin.
El fijador original propuesto por Ilizarov est formado bsicamente por dos
anillos
metlicos puestos
alrededor POR
de laMEDIGRAPHIC
pierna, alambres o agujas que aseguESTE DOCUMENTO
ES ELABORADO
ran los anillos al hueso y guas, colocadas en paralelo con el hueso, que unen
a los anillos; estas guas se pueden alargar como un telescopio (McDonald y
otros, 1996) (Figura 4).
La distraccin por histognesis se refiere a la produccin de nuevo hueso,
que se forma de manera gradual. Es requerida una
operacin para aplicar este mtodo; primero se insertan las agujas o clavos a travs de la piel y los
msculos hasta llegar al hueso para ser alargado o
corregido; despus se aseguran los anillos a la distancia adecuada uno del otro a travs de las guas y
seguidamente se realiza una pequea incisin a travs de la cual se corta el hueso (osteotoma).
El alargamiento o la transportacin, segn se requiera, comienza generalmente una semana despus, que suele ser el tiempo necesario para la formacin del callo seo (McDonald y otros, 1996); en
ese momento se aplica una fuerza que hace que
ambas partes del hueso seccionado se separen a
razn de un milmetro por da aproximadamente;
este proceso se llama distraccin. Aunque inicialmente Ilizarov describi el proceso de histognesis
precisamente en forma similar al prrafo anterior,
descubri con la prctica que en vez de realizar una
osteotoma, era preferible hacer una corticotoma en
el hueso sano. La defini como corte de baja energa que preserva el aporte sanguneo en el periostio.
Figura 4. Fijador Ilizarov.
www.medigraphic.com
175
Ortho-tips Vol. 4 No. 3 2008
Es decir, propuso la vascularizacin en toda la superficie del hueso; aunque es difcil, claramente provee de mayor volumen de masa sea entre el espacio de la distraccin (Figura 5).8,9
CONCLUSIONES
La homeostasis esqueltica, tambin llamada homeostasis mineral del organismo, est regulada por interacciones entre rganos, clulas, factores de seal, hormonas y factores de crecimiento que actan a nivel intra
y extracelular, regulando a este nivel el metabolismo del
calcio, fisiolgicamente fundamental para la formacin
y el remodelado seo a lo largo de la vida.
Los iones: calcio, fosfato y magnesio responden a
la accin de la vitamina D3, la Hormona Paratiroidea
(PTH) y la calcitonina. La vitamina D3 aumenta la reabsorcin de calcio a nivel intestinal, la PTH la reabsorcin a nivel renal, adems activa los osteoclastos
y la calcitonina y desactiva los osteoblastos, facilitanFigura 5. Fijador externo
do la restauracin del nivel basal de calcio. sta ser
que permite alargamiento
la base de todo el proceso de cicatrizacin.
seo.
El conocimiento de las bases a ms de ser y entender una serie de mecanismos complejos dentro del proceso de la reparacin
sea es de vital importancia en el entorno de la realizacin de procedimientos
como las elongaciones seas, dando hoy da una serie de xitos en su mayora, pero previendo tambin las posibilidades de fracaso si no tomamos en
cuenta los factores que pueden influir para no llevar a efecto el proceso limpio
de la reparacin.
BIBLIOGRAFA
1.
2.
3.
4.
5.
6.
7.
8.
9.
Sun JS, Wu SY, Lin FH. The role of muscle-derived stem cells in bone tissue engineering.
Biomaterials 2005; 26(18): 3953-60.
Barn ZK, Reyes-Snchez A. Injertos seos en ciruga ortopdica. MG Cir Ciruj 2006; 74(3): 217-22.
Arpornmaeklong P, Kochel M, Depprich R, Kbler NR, Wrzler KK. Influence of platelet-rich
plasma PRP on osteogenic differentiation of rat bone marrow stromal cells: an in vitro study. Int
J Oral Maxillofac Surg 2004; 33(1): 60-70.
Becerra A. Advances in skeletal reconstruction using bone morphogenetic proteins, Ed. T. S.
Lindholm. World Scientific Publishing Co., 2002; 2: 147-53.
Urist MR. Bone formation by autoinduction. Science 1965; 150(698): 893-9.
Boden SD, Zdeblick TA, Sandhu HS, Heim SE. The use of rhBMP-2 in interbody fusion cages.
Definitive evidence of osteoinduction in humans: a preliminary report. Spine 2000; 25(3): 376-81.
Hanamura H, Higuchi Y, Nakagawa M, Iwata H, Nogami H, et al. Solubilized bone morphogenetic
protein (BMP) from mouse osteosarcoma and rat demineralized bone matrix. Clin Orthop Relat
Res 1980; (148): 281-90.
De Biase P, Capanna R. Clinical applications of BMPs. Injury 2005; 36 Supp 3: S43-46.
Doblar M, Garca JM, Gmez MJ. On the modelling bone tissue fracture and healing of the bone
tissue. Acta Cient Venez 2003; 54(1): 105-19.
www.medigraphic.com
176
Вам также может понравиться
- Rejuvenecer Con El Plasma Sanguíneo De Los JóvenesОт EverandRejuvenecer Con El Plasma Sanguíneo De Los JóvenesРейтинг: 5 из 5 звезд5/5 (1)
- "Factores de Señalización" Pilares Fundamentales en Regeneración Ósea.Документ7 страниц"Factores de Señalización" Pilares Fundamentales en Regeneración Ósea.nugget1012Оценок пока нет
- Cell To Cell Communication in Guided Bone RegenerationДокумент5 страницCell To Cell Communication in Guided Bone RegenerationKaren HamameОценок пока нет
- Taller ComunicCelularДокумент8 страницTaller ComunicCelularMaría Victoria Navarro croswhiteОценок пока нет
- Regeneración ósea guiadaДокумент108 страницRegeneración ósea guiadaHugoRicardoОценок пока нет
- RTG - MembranasДокумент61 страницаRTG - MembranasHugoRicardoОценок пока нет
- Células Madre Mesenquimales: Una Alternativa para La Regeneración ÓseaДокумент8 страницCélulas Madre Mesenquimales: Una Alternativa para La Regeneración Óseaestefany vanessa galvis hoyosОценок пока нет
- Bases Fisiologicas de La Reparacion Osea 1Документ5 страницBases Fisiologicas de La Reparacion Osea 1Sergio Gajardo OcampoОценок пока нет
- Bases Fisiológicas de La Regeneración Ósea IIДокумент6 страницBases Fisiológicas de La Regeneración Ósea IIvictor bustilloОценок пока нет
- Biología Del Hueso y Curación ÓseaДокумент35 страницBiología Del Hueso y Curación ÓseaWendy Alejandra NarvaezОценок пока нет
- CIRUGIAДокумент7 страницCIRUGIALeonardo MataОценок пока нет
- Consolidación ósea: fases y factores que modifican el proceso reparativoДокумент16 страницConsolidación ósea: fases y factores que modifican el proceso reparativoJonathan Reyes100% (2)
- Osteoblasto PDFДокумент7 страницOsteoblasto PDFmagaetcОценок пока нет
- Histología y Fisiología Del Tejido ÓseoДокумент7 страницHistología y Fisiología Del Tejido ÓseoDiego PadillaОценок пока нет
- Reparación Del Tejido Óseo en El Envejecimiento 2020Документ11 страницReparación Del Tejido Óseo en El Envejecimiento 2020Thalia RamirezОценок пока нет
- Factores de CrecimientoДокумент25 страницFactores de CrecimientoDanielPortillaОценок пока нет
- LibroBM2011 Cap1Документ16 страницLibroBM2011 Cap1ISABELLA RINCON OÑATEОценок пока нет
- 04 Factores de La Resorcion Osea PDFДокумент16 страниц04 Factores de La Resorcion Osea PDFlizeth velaОценок пока нет
- MARCO CONCEPTUAL Con ReferenciasДокумент9 страницMARCO CONCEPTUAL Con Referenciaswilliam cОценок пока нет
- Buco 2Документ10 страницBuco 2Giovanni ArticaОценок пока нет
- Artículo - Acoplamiento Entre Osteoclasto y OsteoblastoДокумент3 страницыArtículo - Acoplamiento Entre Osteoclasto y OsteoblastoPaoloОценок пока нет
- Practica de Tejidos BiologiaДокумент12 страницPractica de Tejidos BiologiaAnghely Gianella Alicia Gomez MergildoОценок пока нет
- Consolidacion Osea y Defecto de Cicatrizacion Del HuesoДокумент55 страницConsolidacion Osea y Defecto de Cicatrizacion Del HuesopaoОценок пока нет
- Dispositivas Fases de Consolidación OseaДокумент17 страницDispositivas Fases de Consolidación Oseacarlos sanchezОценок пока нет
- CIRUGIA - Cicatrizacion OseaДокумент4 страницыCIRUGIA - Cicatrizacion OseaGuillaume MichiganОценок пока нет
- Biología ósea y fisiología enДокумент11 страницBiología ósea y fisiología enBîłłý Řôğěř100% (1)
- Factores Reguladores de La Resorción ÓseaДокумент16 страницFactores Reguladores de La Resorción ÓseaADRIANA PASTRANAОценок пока нет
- Fase de Callo InmaduroДокумент2 страницыFase de Callo InmaduroFercho AndradeОценок пока нет
- Regeneración Ósea DR IvanДокумент62 страницыRegeneración Ósea DR IvanGeovanny Alejandro Solari AcevedoОценок пока нет
- 2A Contextualización Del ProblemaДокумент10 страниц2A Contextualización Del ProblemaRegina LizárragaОценок пока нет
- Células óseas: osteoprogenitoras, osteoblastos, osteocitos y osteoclastosДокумент3 страницыCélulas óseas: osteoprogenitoras, osteoblastos, osteocitos y osteoclastosAdvancedangela123Оценок пока нет
- Estructura y Características Del Tejido ÓseoДокумент5 страницEstructura y Características Del Tejido ÓseoBryan Andres Smith DiazОценок пока нет
- Resumen de Remodelación Ósea y La Función Del RANK, RANKL y OPGДокумент8 страницResumen de Remodelación Ósea y La Función Del RANK, RANKL y OPGNikolai FernandezОценок пока нет
- Envejecimiento Sistema OseoДокумент33 страницыEnvejecimiento Sistema OseoRicardo Andres RuizОценок пока нет
- Consolidacion Osea 1Документ19 страницConsolidacion Osea 1Jonathan Mindiola SantanaОценок пока нет
- Ensayo Osteoclastos Luis Eli Marquez GonzalezДокумент5 страницEnsayo Osteoclastos Luis Eli Marquez GonzalezLuis Eli Márquez GonzálezОценок пока нет
- Fisiopatologia de La FracturaДокумент2 страницыFisiopatologia de La Fracturasebastian gutierrez alvarezОценок пока нет
- BiologiaenreparaciondefracturasДокумент51 страницаBiologiaenreparaciondefracturasOlgaPatyDíazBalcázarОценок пока нет
- Bryan Sarango TejidosДокумент29 страницBryan Sarango Tejidosbry scarlotОценок пока нет
- Consolidacion OseaДокумент16 страницConsolidacion OseaAny Jara MoralesОценок пока нет
- Consolidacion OseaДокумент16 страницConsolidacion Osealibra_81Оценок пока нет
- Fisiopatología ÓseaДокумент1 страницаFisiopatología ÓseaTraumatología y Ortopedia HGQОценок пока нет
- REPARACIÓN DE FRACTURASДокумент219 страницREPARACIÓN DE FRACTURASsilviac95Оценок пока нет
- Citología Del HuesoДокумент11 страницCitología Del HuesoKaren Lossio AricochéОценок пока нет
- Consolidacion Osea1 1204654412503494 4Документ16 страницConsolidacion Osea1 1204654412503494 4Roxana PinedaОценок пока нет
- Crecimiento ÓseoДокумент11 страницCrecimiento Óseoamelia mamaniОценок пока нет
- Osteoblastos y OsteocitosДокумент5 страницOsteoblastos y Osteocitosbarrid24Оценок пока нет
- Tejido ÓseoДокумент7 страницTejido ÓseoSofía Cueva Cruz (Sofi)Оценок пока нет
- Medicina Legal- consolidación óseaДокумент7 страницMedicina Legal- consolidación óseaNataly Jorquera CopaivaОценок пока нет
- Células óseas y su regulaciónДокумент9 страницCélulas óseas y su regulaciónCarlos Petit LorussoОценок пока нет
- Bases Fisiológicas de La Regeneración Ósea II. El Proceso de RemodeladoДокумент7 страницBases Fisiológicas de La Regeneración Ósea II. El Proceso de RemodeladomeraguzmanОценок пока нет
- 1 Óseo TejidosДокумент5 страниц1 Óseo TejidosGuille RubinoОценок пока нет
- Patología ÓseaДокумент150 страницPatología ÓseaSantyagoAriasОценок пока нет
- Apuntes Tejido ÓseoДокумент19 страницApuntes Tejido ÓseoMaximiliano León PizarroОценок пока нет
- Evolucion Del Callo OseoДокумент10 страницEvolucion Del Callo OseojanaОценок пока нет
- Reparación ÓseaДокумент6 страницReparación ÓseaMonica Leyvas100% (1)
- Endo Estructura Bacteriana - Liz HuitronДокумент98 страницEndo Estructura Bacteriana - Liz HuitronEmmanuel CieloОценок пока нет
- Para Tocar - Serrat 2 PDFДокумент18 страницPara Tocar - Serrat 2 PDFEmmanuel Cielo100% (1)
- AnuarioДокумент11 страницAnuarioEmmanuel CieloОценок пока нет
- Endodontología II 2019-2020 - 0 PDFДокумент20 страницEndodontología II 2019-2020 - 0 PDFEmmanuel CieloОценок пока нет
- Im ProntaДокумент10 страницIm ProntaEmmanuel CieloОценок пока нет
- Poster Perio AMIC 2019Документ1 страницаPoster Perio AMIC 2019Emmanuel CieloОценок пока нет
- Articulo Cientifico PDFДокумент6 страницArticulo Cientifico PDFNeider Jose Campo HernandezОценок пока нет
- Cerámicas DentalesДокумент11 страницCerámicas DentalesMani ChioОценок пока нет
- Cerámicas dentales: clasificación y criterios de selecciónДокумент2 страницыCerámicas dentales: clasificación y criterios de selecciónEmmanuel CieloОценок пока нет
- Microbiota de La Cavidad BucalДокумент48 страницMicrobiota de La Cavidad BucalEmmanuel CieloОценок пока нет
- Caso #2Документ3 страницыCaso #2Emmanuel CieloОценок пока нет
- Cuestionarios y Escalas de ActitudesДокумент16 страницCuestionarios y Escalas de ActitudesRonaldHS100% (1)
- Caso 3Документ7 страницCaso 3Emmanuel CieloОценок пока нет
- Cerámicas DentalesДокумент2 страницыCerámicas DentalesEmmanuel CieloОценок пока нет
- Emociones BásicasДокумент32 страницыEmociones BásicasEmmanuel CieloОценок пока нет
- 1 Introducción y Conceptos Básicos - Estadistica NegocioДокумент20 страниц1 Introducción y Conceptos Básicos - Estadistica NegocioEmmanuel CieloОценок пока нет
- RayadoДокумент3 страницыRayadoEmmanuel CieloОценок пока нет
- FlautaДокумент1 страницаFlautaEmmanuel CieloОценок пока нет
- Examen de Ojo Oido y GlándulasДокумент5 страницExamen de Ojo Oido y GlándulasEmmanuel CieloОценок пока нет
- ManualdediseccionesanatomiaДокумент27 страницManualdediseccionesanatomiaEmmanuel CieloОценок пока нет
- Mucosa OralДокумент10 страницMucosa OralAna María AramayoОценок пока нет
- MorfofisiologiaschДокумент33 страницыMorfofisiologiaschEmmanuel CieloОценок пока нет
- HolocaustoДокумент18 страницHolocaustoEmmanuel Cielo0% (1)
- Tabla de Escala de Atitudes.Документ3 страницыTabla de Escala de Atitudes.Emmanuel CieloОценок пока нет
- Divorcio y NINIS.Документ24 страницыDivorcio y NINIS.Emmanuel CieloОценок пока нет
- Ley de La Conservación de La MasaДокумент8 страницLey de La Conservación de La MasaEmmanuel CieloОценок пока нет
- Sistema Musculo Esquelético ResumenДокумент5 страницSistema Musculo Esquelético ResumenEmmanuel CieloОценок пока нет
- Semblanza de Martín CortésДокумент3 страницыSemblanza de Martín CortésEmmanuel CieloОценок пока нет
- Sistema EsqДокумент1 страницаSistema EsqEmmanuel CieloОценок пока нет
- 3000chistes 003Документ56 страниц3000chistes 003fjrb1960Оценок пока нет
- Cómo Cambiar Tu Vida A Través de Las PalabrasДокумент105 страницCómo Cambiar Tu Vida A Través de Las PalabrasSaul Ajorí0% (1)
- Villa ElisaДокумент47 страницVilla ElisaMarialis SchreiberОценок пока нет
- Efectos Toxicos de Plomo y El Zinc en Artemia FranciscanaДокумент10 страницEfectos Toxicos de Plomo y El Zinc en Artemia FranciscanaJose Antonio Martinez VillalbaОценок пока нет
- Ergonomía TP4Документ8 страницErgonomía TP4Lourdes ZapataОценок пока нет
- Aspectos IntroductoriosДокумент10 страницAspectos IntroductoriosgarnerОценок пока нет
- Plantilla de Test Neuropsicologicos II BДокумент53 страницыPlantilla de Test Neuropsicologicos II BAna SousaОценок пока нет
- Boletín Oficial Del Principado de AsturiasДокумент12 страницBoletín Oficial Del Principado de AsturiasNeftali BlancoОценок пока нет
- Agenda de Plan AlimentarioДокумент1 страницаAgenda de Plan AlimentarioJohon Cesar Cornejo PariОценок пока нет
- Regulación coordinada de la fosforilación oxidativa y rutas metabólicasДокумент17 страницRegulación coordinada de la fosforilación oxidativa y rutas metabólicasLiss ContrerasОценок пока нет
- Parásitos humanos y sus características morfológicasДокумент33 страницыParásitos humanos y sus características morfológicaseorgalionОценок пока нет
- Clindamín BiozooДокумент3 страницыClindamín BiozooannygiacoОценок пока нет
- Memoria Practica 3Документ9 страницMemoria Practica 3lososaitОценок пока нет
- MARCO INSTITUCIONAL SOCIAL Y TEORICO CPC ENVIAR Nuevas CorreccionesДокумент6 страницMARCO INSTITUCIONAL SOCIAL Y TEORICO CPC ENVIAR Nuevas CorreccionesLaura GARCIA VINCOS100% (1)
- Presentacion Ejecutiva SubsidiosДокумент69 страницPresentacion Ejecutiva SubsidiosRaphielys M. Canela PeñaОценок пока нет
- La Desobediencia A Dios Causas y ConsecuenciasДокумент117 страницLa Desobediencia A Dios Causas y ConsecuenciasMissionario Gilberto RamosОценок пока нет
- Aplicación de Métodos Combinados para ElДокумент341 страницаAplicación de Métodos Combinados para ElJaime Alberto Sanchez CardonaОценок пока нет
- Adolescencia, madurez y vejezДокумент11 страницAdolescencia, madurez y vejezLuis JaraОценок пока нет
- Solución de EjerciciosДокумент13 страницSolución de EjerciciosKatalina Muñoz100% (1)
- Titularización de CarteraДокумент16 страницTitularización de CarteraLucía Romero UrdialesОценок пока нет
- Características y clasificación de la carne de vacunoДокумент161 страницаCaracterísticas y clasificación de la carne de vacunomaria gabinoОценок пока нет
- Universidad Estatal Península de Santa ElenaДокумент3 страницыUniversidad Estatal Península de Santa ElenaKevin BarzolaОценок пока нет
- Denuncias Aqp AmbientalesДокумент14 страницDenuncias Aqp AmbientalesFIORELLA MARJORIE GONZALES RODRIGUEZОценок пока нет
- ANAFILAXIAДокумент8 страницANAFILAXIAMarisol López HernándezОценок пока нет
- Capítulo 5 HarperДокумент3 страницыCapítulo 5 HarperMARIANA ESCOBAR RIVERAОценок пока нет
- TD 1 Limpieza y LubricaciónДокумент8 страницTD 1 Limpieza y Lubricaciónsebastian villegasОценок пока нет
- FundetecДокумент6 страницFundetecJose david Julio berrioОценок пока нет
- Sectores EconomicosДокумент7 страницSectores EconomicosLuis PalominoОценок пока нет
- Hoja de Vida Cindy Castro .Документ3 страницыHoja de Vida Cindy Castro .Alejandra Castro MontanezОценок пока нет
- Cuadro SinopticoДокумент2 страницыCuadro SinopticoJessica Aide Ledesma NavaОценок пока нет