Академический Документы
Профессиональный Документы
Культура Документы
Informe Calorimetria
Загружено:
Oliver ZambranoОригинальное название
Авторское право
Доступные форматы
Поделиться этим документом
Поделиться или встроить документ
Этот документ был вам полезен?
Это неприемлемый материал?
Пожаловаться на этот документАвторское право:
Доступные форматы
Informe Calorimetria
Загружено:
Oliver ZambranoАвторское право:
Доступные форматы
1
CALORIMETRIA
I.
INTRODUCCION
El calor es una forma de energa. La temperatura de un sistema es una
propiedad del mismo que determina si que-dar o no en equilibrio trmico
cuando se pone en contacto con cualquier otro sistema. Supngase que el
sistema A, a temperatura superior a la de B, es puesto en contacto con este.
Una vez alcanzado el equilibrio trmico, se encuentra que A ha
experimentado una disminucin y B un aumento de temperatura. De esta
manera decimos que entre dos cuerpos que se encuentran en estas
condiciones existe un flujo de energa, a la que llamamos calor. Entonces
tenemos que el calor es la energa trasferida entre dos sistemas y que est
exclusivamente relacionada con la diferencia de temperatura existente entre
ellos. Esta prctica trata de la calorimetra, por eso debemos saber que es
calorimetra. Una definicin sencilla dice que la calorimetra se encarga de
medir el calor en una reaccin qumica o un cambio fsico usando un
calormetro. La calorimetra indirecta calcula el calor que los organismos
vivos producen a partir de la produccin de dixido de carbono y de
nitrgeno (urea en organismos terrestres), y del consumo de oxgeno.
El calor especfico es una propiedad intensiva de la materia, por lo que es
representativo de cada sustancia; por el contra-rio, la capacidad calorfica
es una propiedad extensiva representativa de cada cuerpo o sistema
particular. Cuanto mayor es el calor especfico de las sustancias, ms
energa calorfica se necesita para incrementar la temperatura. Por ejemplo,
se requiere ocho veces ms energa para incrementar la temperatura de un
lingote de magnesio que ara un lingote de plomo de la misma masa.
CALORIMETRIA
II.
RESUMEN
La calorimetra se encarga de medir el calor en una reaccin qumica o un
cambio fsico usando un calormetro. La calorimetra indirecta calcula el
calor que los organismos vivos producen a partir de la produccin de
dixido de carbono y de nitrgeno (urea en organismos terrestres), y del
consumo de oxgeno. Para determinar el calor especfico de una sustancia
cualquiera debemos saber con qu facilidad sta intercambia calor con el
medio que le rodea. El medio debe estar bajo condiciones controladas para
poder cuantificar el intercambio de calor del cuerpo en estudio y para ello
dispondremos de un sistema aislado del medio ambiente, en otras palabras,
le crearemos un pequeo ambiente al objeto estudiado de tal manera que
se encuentre libre de interaccin con la atmsfera, tal ambiente es el
Thermo o Calormetro quien idealmente no debiera intercambiar nada de
calor con el medio, sin embargo sabemos que esto no ocurre, sin embargo,
para intervalos de tiempo no muy extensos es el thermo una buena
aproximacin a lo idealmente requerido
III.
OBJETIVOS:
Determinar el equivalente en agua del calormetro
IV.
MARCO TEORICO:
CALOR.
El calor es la transferencia de energa entre diferentes cuerpos o diferentes
zonas de un mismo cuerpo que se encuentran a distintas temperaturas. Este
flujo siempre ocurre desde el cuerpo de mayor temperatura hacia el cuerpo de
menor temperatura, ocurriendo la transferencia de calor hasta que ambos
cuerpos se encuentren en equilibrio trmico. El calor puede ser transferido por
diferentes mecanismos, entre los que cabe resear la radiacin, la conduccin
y la conveccin, aunque en la mayora de los procesos reales todos se
encuentran presentes en mayor o menor grado.
CAPACIDAD CALORFICA.
La capacidad calorfica de define como la cantidad de calor que hay que
suministrar a toda la extensin de una sustancia para elevar su temperatura en
una unidad (kelvin o grado Celsius). Se la representa con la letra
(mayscula).Para medir la capacidad calorfica bajo unas determinadas
condiciones es necesario comparar el calor absorbido por una sustancia (o un
CALORIMETRIA
sistema) con el incremento de tempera-tura resultante. La capacidad calorfica
viene dada por:
= lim
T 0
Q
T
Donde:
C = Es la capacidad Calorfica, que en general ser funcin de
las variables de estado
Q = Es la calor absorbido por el sistema.
T = La variacin de temperatura
Julios
La Capacidad calorfica se mide en unidades del SI(
)
K
o tambin en (
cal
C )
La capacidad calorfica (C) de un sistema fsico depende dela cantidad de
sustancia o masa de dicho sistema. Para un sistema formado por una sola
sustancia homognea se define adems el calor especfico o capacidad
calorfica especfica c a partir de la relacin:
c=
Q
c=
m
m T
Donde:
c = Es el calor especifico o capacidad calorfica especifica
m = La masa de Sustancia considerada
De las anteriores relaciones es fcil inferir que al aumentarla masa de una
sustancia, se aumenta su capacidad calorfica ya que aumenta la inercia
trmica, y con ello aumenta la dificultad de la sustancia para variar su
temperatura. Un ejemplo de esto se puede apreciar en las ciudades costeras
donde el mar acta como un gran termostato regulando las variaciones de
temperatura
CALOR ESPECFICO.
El calor especfico es una magnitud fsica que se define como la cantidad de
calor que hay que suministrar a la unidad de masa de una sustancia o sistema
termodinmico para elevar su temperatura en una unidad (kelvin o grado
Celsius). En general, el valor del calor especfico depende de dicha
temperatura inicial. Se la representa con la letra c (minscula).Por lo tanto el
calor especfico es la capacidad calorfica especfica y se expresa de la
siguiente manera:
CALORIMETRIA
c=
Q
mT
El calor especfico es una propiedad intensiva de la materia, por lo que es
representativo de cada sustancia; por el contrario, la capacidad calorfica es
una propiedad extensiva representativa de cada cuerpo o sistema particular.
Cuanto mayor es el calor especfico de las sustancias, ms energa calorfica
se necesita para incrementar la temperatura. Por ejemplo, se requiere ocho
veces ms energa para incrementar la temperatura de un lingote de magnesio
que para un lingote de plomo de la misma masa.
El trmino "calor especfico" tiene su origen en el trabajo del fsico Joseph
Black, quien realiz variadas medidas calorimtricas y us la frase capacidad
para el calor. En esa poca la mecnica y la termodinmica se consideraban
ciencias independientes, por lo que actualmente el trmino podra parecer
inapropiado; tal vez un mejor nombre podra ser transferencia de energa
calorfica especfica, pero el trmino est demasiado arraigado para ser
reemplazado
CANTIDAD DE CALOR.
La experiencia pone de manifiesto que la cantidad de calor tomada (o cedida)
por un cuerpo es directamente proporcional a su masa y al aumento (o
disminucin) de temperatura que experimenta. La expresin matemtica de
esta relaciones la ecuacin calorimtrica.
Q=mc T
Donde:
Q = es la transferencia de energa en forma calorfica entre el sistema y su
entorno u otro sistema,
m = es la masa del sistema (se usa una n cuando se trata del calor especfico
molar)
T = es el incremento de temperatura que experimenta el sistema
CALORIMETRO
Los componentes del calormetro (fig. 1) son un vaso aislante (de vidrio o
plstico), vaso medidor interno de paredes delgadas (vidrio plateado o metal),
tapa con termmetro y agitador
CALORIMETRIA
Fig. 1: Partes de un calormetro
Aun si el aislamiento de calor de nuestro calormetro es satisfactorio, calentara
y enfriara respectivamente en el curso de las operaciones de equilibrio de calor.
EQUIVALENTE EN AGUA (V)
Es la cantidad de agua con la cual podemos reemplazar el vaso medidor el
termmetro y el agitador. El valor numrico est dado por la cantidad de calor
requerida para elevar la temperatura del calormetro en 1C. El equivalente en
agua se refiere al conjunto: vaso medidor, termmetro y agitador, por ello, este
valor es diferente para cada calormetro.
Si se coloca en un vaso calormetro una masa de agua m a (100 gramos por
ejemplo) a la temperatura ambiente, se medir en el termmetro la temperatura
ta. Aadimos a esta otra masa de agua calentada m c (150 gramos por ejemplo)
a la temperatura de tc de 40 C o 50C y despus de agitar cuidadosamente se
conseguir la temperatura de equilibrio de la mescla t.
El calor perdido por el agua caliente ser
Q C =m c c (t c t)
La cantidad de calor ganado por el agua a la temperatura ambiente y por el
calormetro ser:
Qa=ma c (tt a )
Q a=V ( t t a )
En consecuencia, el equivalente en agua del calormetro es:
V =mc
t c t
ma
tt a
CALORIMETRIA
V.
METODOLOGIA Y TECNICAS
1. EQUIPO Y MATERIALES:
Termo(Calormetro de Aluminio)
Termmetro
Vaso de Precipitados
Jeringa
Balanza
Agua
Hornilla
Trapo
2. PROCEDIMIENTO
VI.
Se pes el calormetro vaco( termo) Pc
Se ech agua a la temperatura ambiente aproximadamente 100
g para esto determinar la masa se pes 100ml de agua que
equivale a 100 gramos
Luego se agito con mucho cuidado y se ley la temperatura
ambiente(ta)
Por consiguiente se ech agua caliente y se determin la
temperatura de agua caliente tc 93C y la masa de 202 gramos.
Luego se agito cuidadosamente y se ley la temperatura de
equilibrio( t )
Finalmente se calcul el equivalente en agua del calormetro
RESULTADOS
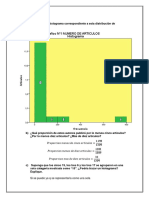
Tabla N 01
N
1
ma
mc
ta
tc
200 g
202 g
22C
93C
53C
60.65
Por formula
t t
V =mc c ma
tt a
CALORIMETRIA
Se tiene
V =202 g
( 9353 ) C
200 g
( 5322 ) C
V = 60.6451613
VII.
CONCLUCIONES
De la ecuacin anterior concluimos que (v) es la masa de agua con una
capacidad calorfica igual a la del calormetro.
Adems No puede ser negativo porque una masa negativa no tiene sentido
fsico; por lo tanto la masa del calormetro como su calor especfico son
positivos, al igual que el calor especifico del agua.
Su valor depende, de la masa del calormetro y de su calor especfico
Cuando ya conocemos el equivalente de agua de un calormetro, ya es posible
calcular el calor especfico por gramo (slido) del cuerpo en cuestin a partir de
las masas y temperaturas determinadas experimentalmente y as determinar de
manera ms precisa el valor del calor especfico de un slido.
VIII.
BIBLIOGRAFIA
UNIVERSIDAD DEL CAUCA. (2010). Calorimetra. Julio 2016, de
departamento
de
fsica
Sitio
web:
https://es.scribd.com/doc/38486076/Calorimetria-Informe-de-laboratorio
UNIVERSIDAD AUTONOMA DE MADRID. (2005). Calor especifico. 1807-2016,
de
Laboratorio
de
Fsica
Genera,
Sitio
web:
CALORIMETRIA
https://www.uam.es/personal_pdi/ciencias/rdelgado/docencia/FISICA_ITI
/PRACTICAS/Calor-Esp.pdf
Ing. Sandra Silvester e Ing. Rubn Sarges Guerra. (2012).
EQUIVALENTE EN AGUA DE UN CALORIMETRO. 2016, de
Departamento de Materias Bsicas Unidad Docente Bsica de Fsica
Sitio
web:
http://www.frro.utn.edu.ar/repositorio/catedras/basicas/fisica2/files/EQUIV
ALENTE_EN_AGUA_CALORIMETRO.pdf
Вам также может понравиться
- Cortes de La TerneraДокумент4 страницыCortes de La TerneraOliver ZambranoОценок пока нет
- Práctica de AulaДокумент14 страницPráctica de AulaOliver ZambranoОценок пока нет
- Esta Di SticaДокумент8 страницEsta Di SticaOliver ZambranoОценок пока нет
- Informe de FisicaДокумент15 страницInforme de FisicaOliver ZambranoОценок пока нет
- Examen de Fluidos 2Документ22 страницыExamen de Fluidos 2Oliver Zambrano100% (1)
- REGRESIONДокумент12 страницREGRESIONOliver ZambranoОценок пока нет
- Condiciones Termicas (39220)Документ11 страницCondiciones Termicas (39220)Fatima Bbtuby100% (1)
- U1251-2B Users Guide MultimetroДокумент171 страницаU1251-2B Users Guide MultimetroLuis GarcíaОценок пока нет
- Ficha Técnica 35670Документ2 страницыFicha Técnica 35670benjaguerrОценок пока нет
- Caldera de TermofluidoДокумент14 страницCaldera de TermofluidoEdison Paul Tierra TierraОценок пока нет
- VidrioДокумент107 страницVidrioCh IrivinОценок пока нет
- Problemas de Calor y TemperaturaДокумент7 страницProblemas de Calor y TemperaturaGerman Montero100% (1)
- Laboratorio Conductividad TermicaДокумент21 страницаLaboratorio Conductividad TermicaMateo RuizОценок пока нет
- Sintesis de Nanofibras de CarbonoДокумент90 страницSintesis de Nanofibras de Carbonovipllenger0% (1)
- Introduccion A La Termodinamica Con Aplicaciones de Ingenieria2 PDFДокумент100 страницIntroduccion A La Termodinamica Con Aplicaciones de Ingenieria2 PDFJennifer NajleОценок пока нет
- Propiedades Reológicas de FluidosДокумент21 страницаPropiedades Reológicas de FluidosTahic P100% (1)
- Teoria de Los EscapesДокумент6 страницTeoria de Los Escapesczr89100% (1)
- Norma Asme b31.4Документ111 страницNorma Asme b31.4Roque MatienzoОценок пока нет
- TEMA 04 I.R.agentes de DeterioroДокумент23 страницыTEMA 04 I.R.agentes de DeterioroSusana Rodríguez MartínОценок пока нет
- Ficha de Odorante PDFДокумент20 страницFicha de Odorante PDFrandhyalejandroОценок пока нет
- Indice de Polarizacion (Ip) en Motores ElectricosДокумент5 страницIndice de Polarizacion (Ip) en Motores Electricosfrinesi0% (1)
- NRF 208 Pemex 2009 Relevado de EsfuerzosДокумент45 страницNRF 208 Pemex 2009 Relevado de Esfuerzosjerrymcfly100% (5)
- Riesgo Neumatico - HidraulicoДокумент113 страницRiesgo Neumatico - HidraulicoCursos IngproserОценок пока нет
- Permisos de Trabajo Certificación 07Документ55 страницPermisos de Trabajo Certificación 07Ruben Orlando Carazo Jarava100% (4)
- Los Aislantes SólidosДокумент22 страницыLos Aislantes SólidosLarry Ivan100% (1)
- 2 - Acondicionamiento Ambiental II - Sistemas Pasivo de EnfriamientoДокумент60 страниц2 - Acondicionamiento Ambiental II - Sistemas Pasivo de EnfriamientoGeral Dali Sulca Urbano100% (1)
- Calor Latente de Fusion Del HieloДокумент7 страницCalor Latente de Fusion Del HieloeliasrtОценок пока нет
- Demostración Del Confort Térmico en El Interior de Dos Viviendas Antiguas en La Ciudad de San Francisco de CampecheДокумент18 страницDemostración Del Confort Térmico en El Interior de Dos Viviendas Antiguas en La Ciudad de San Francisco de Campechecrissl_1Оценок пока нет
- CalorДокумент8 страницCalorJohann Fidel CarhuaypiñaОценок пока нет
- Ejercicios de AutomatizacionДокумент11 страницEjercicios de AutomatizacionJordan Arrazola PaterninaОценок пока нет
- Ejemplo Carga Terrmica Camara FrigorificaДокумент4 страницыEjemplo Carga Terrmica Camara FrigorificaCarlosHernández100% (1)
- Auditoria Propiamente Dicha Procesos CarnicosДокумент72 страницыAuditoria Propiamente Dicha Procesos Carnicoskmotillo9012Оценок пока нет
- Guía de Secadores Solares de CafeДокумент14 страницGuía de Secadores Solares de CafeLeopoldo Jose Dominguez BuesoОценок пока нет
- Practica 2 Condiciones AtmosfericasДокумент11 страницPractica 2 Condiciones AtmosfericasAndrea JoaquinОценок пока нет
- Compresion en GasesДокумент22 страницыCompresion en Gasesyesi1188100% (1)
- Taller Fenomenos de TransferenciaДокумент2 страницыTaller Fenomenos de TransferenciaJuliethPatiñoОценок пока нет