Академический Документы
Профессиональный Документы
Культура Документы
GuiaTematica quimicaOrganicaI
Загружено:
Liiz PinedaОригинальное название
Авторское право
Поделиться этим документом
Поделиться или встроить документ
Этот документ был вам полезен?
Это неприемлемый материал?
Пожаловаться на этот документАвторское право:
GuiaTematica quimicaOrganicaI
Загружено:
Liiz PinedaАвторское право:
UNIVERSIDAD AUTNOMA METROPOLITANA
Dr. Salvador Vega y Len
Rector General
Mtro. Norberto Manjarrez lvarez
Secretario General
UNIDAD IZTAPALAPA
Dr. Jos Octavio Nateras Domnguez
Rector de Unidad
Dr. Miguel ngel Gmez Fonseca
Secretario de Unidad
Dra. Edith Ponce Alquicira
Directora de la Divisin de Ciencias Biolgicas y de la Salud
Dra. Milagros Huerta Coria
Coordinadora de Extensin Universitaria
Lic. Adrin Felipe Valencia Llamas
Jefe de la Seccin de Produccin Editorial
Primera Impresin 2015
UNIVERSIDAD AUTNOMA METROPOLITANA
UNIDAD IZTAPALAPA
Av. San Rafael Atlixco No. 186, Col. Vicentina,
Del. Iztapalapa, C.P 09340, Mxico D.F. Tel.: 5804 4600
Impreso y hecho en Mxico/Printed in Mexico
Gua Temtica para el Curso de Qumica Orgnica I
ndice
Prlogo
. . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 5
Introduccin
. . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 7
Tema 1. Formulacin y nomenclatura de los compuestos orgnicos . . . . . . . . . . . . . . . . . . . . . . . . . 9
Tema 2. El enlace qumico en los compuestos orgnicos. . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 21
Tema 3. Alcanos . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 33
Tema 4. Alquenos. . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 39
Tema 5. Resonancia . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 57
Tema 6. Alcoholes . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 77
Tema 7. Haluros de alquilo y arilo . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 91
Tema 8. Estereoqumica. . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 105
Tema 9. Mecanismos de reaccin SN y E . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 113
Tema 10. Fenoles. . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 117
Tema 11. teres . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 121
Bibliografa
. . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 127
Gua Temtica para el Curso de Qumica Orgnica I
Prlogo
Esta obra contiene la descripcin esquemtica del contenido sinttico del Programa de Estudios de la Unidad de Enseanza
Aprendizaje (UEA) de formacin bsica Qumica Orgnica I correspondiente a los nuevos planes de estudio aprobados para las
Licenciaturas en Ingeniera de los Alimentos e Ingeniera Bioqumica Industrial que ofrece la Divisin de Ciencias Biolgicas y
de la Salud desde el trimestre 13-I (enero del 2013) ya que esta UEA fue aprobada por el Colegio Acadmico en la sesin 344
celebrada el 19 de abril de 2012 con los Acuerdos 344.4 y 344.5.
Esta obra est elaborada como una herramienta adicional de enseanza de los elementos de aprendizaje tradicionales tales
como los libros de texto tanto para los alumnos como para los profesores con base en la descripcin de los elementos bsicos
que debe de contener cada tema y subtema del Programa de Estudios de Qumica Orgnica I.
Los temas del texto estn ordenados segn el Programa de Estudios de la Unidad de Enseanza Aprendizaje y cada Tema
est dividido en subtemas que corresponden a cada punto del Contenido Sinttico. En algunos subtemas se presentan ejemplos
de reacciones y estructuras moleculares para ilustrar el punto a desarrollar. No se presentan ejercicios o problemas en cada
captulo de la obra ya que no es un libro de texto.
Jefe de Departamento
Francisco Cruz Sosa/Jorge Armando Haro Castellanos/Ignacio Lpez y Celis/Sergio Alatorre Santamara
Gua Temtica para el Curso de Qumica Orgnica I
Introduccin
El objetivo central de esta obra es ser una gua esquemtica del Contenido Sinttico de la Unidad de Enseanza Aprendizaje del
primer curso de Qumica Orgnica de las licenciaturas en Ingeniera de los Alimentos e Ingeniera Bioqumica Industrial, con el
objetivo de que en cada tema y subtema los alumnos sepan lo que deben estudiar y aprender y los profesores tengan un apoyo
didctico para impartir en cada sesin del curso.
Tomando en cuenta que todos los profesores ensean de manera diferente la Qumica Orgnica y que los alumnos la
aprenden de manera heterognea entonces se pens en elaborar esta gua esquemtica para auxiliar en el proceso de enseanza
y aprendizaje, como material adicional a los libros tradicionales de Qumica Orgnica tanto para los profesores como para los
alumnos. Adems de que como cada profesor puede dar menor o mayor nfasis en cada tema del contenido sinttico segn
vaya avanzado en el curso, por lo tanto en esta gua temtica de Qumica Orgnica I los alumnos pueden revisar cuales temas
han cubierto con el profesor y cuales pueden adelantar, cubrir o reforzar fuera de clase.
En cada uno de los once temas del contenido sinttico del Programa de Qumica Orgnica I se han elaborado cuadros
verticales que representan de manera esquemtica los subtemas de cada tema para que los usuarios obtengan la informacin
bsica sobre la nomenclatura, formulacin, sntesis, reacciones, usos y aplicaciones de los compuestos orgnicos. La bibliografa
es comn para todos los once temas y est basada en los libros de texto ms comunes y utilizados por los profesores que imparten los cursos de Qumica Orgnica, los alumnos pueden consultar estos libros de texto en las bibliotecas si es que no pueden
adquirir algn ejemplar del texto solicitado por el profesor del curso o del autor de su preferencia.
Los autores esperan que esta obra sea de utilidad para todos los involucrados en la enseanza y en el aprendizaje de la
Qumica Orgnica y agradecen al Ilustrador Fredy Rodrguez Jimnez por el arte y diseo grfico que ilustra el inicio de cada tema
y por las imgenes, frmulas o reacciones que estn al final de algunos esquemas.
Los autores
Francisco Cruz Sosa/Jorge Armando Haro Castellanos/Ignacio Lpez y Celis/Sergio Alatorre Santamara
Gua Temtica para el Curso de Qumica Orgnica I
Tema 1
Formulacin y nomenclatura de los compuestos orgnicos
1.1 Alcanos, alquenos, alquinos, compuestos aromticos, haluros de alquilo y de arilo, alcoholes, aldehdos, cetonas, cidos
carboxlicos, steres, aminas y amidas.
CH3
C
CH3
NH2
H2C
O
H
C
CH3
CH2
CH4
OCH3
O
CH3
CH3
OH
Cl
Cl
O
C
CH3
CH3
O
C
CH3
Francisco Cruz Sosa/Jorge Armando Haro Castellanos/Ignacio Lpez y Celis/Sergio Alatorre Santamara
Universidad Autnoma Metropolitana /Unidad Iztapalapa/Divisin de Ciencias Biolgicas y de la Salud
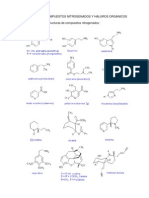
Esquema 1.1 Compuestos Orgnicos. Clasificacin
Clasificacin de los compuestos orgnicos
Compuestos orgnicos oxigenados, nitrogenados y halogenados
Hidrocarburos C, H
Alifticos
Saturados
Aromticos
Insaturados
Alcanos
Lineales
o
Acclicos
Nitrogenados
Oxigenados
C, H, O
alcoholes
Alquenos
Cclicos
Alquinos
C, H, N
C, H, N, O
C, H, X
aminas
amidas
haluros
de alquilo
aldehdos
cetonas
Cclicos
y Acclicos
cidos
carboxlicos
haluros
de arilo
steres
H H H H
HCCCCH
H H H H
C == C
eteno
hidrocarburos
H
H
NCC
CH2
O
OH
H3C N
10
tirosina
Tema 1. Formulacin y nomenclatura de los compuestos orgnicos
O
O
CH3
OH
triclorometano
H H
butano
Halogenados
C, H, X
cocana
Gua Temtica para el Curso de Qumica Orgnica I
Esquema 1.2 Alcanos. Formulacin y nomenclatura
Alcanos lineales
Nombre
Frmula condensada
Frmula semidesarrollada
Alcanos C 1 a C 6
CnH2n+2
Serie homloga
metano
CH4
CH4
etano
C 2 H6
CH 3 - CH3
propano
C 3 H8
CH 3 - CH2 - CH3
butano
C 4 H10
CH 3 - CH2 - CH2 - CH3
pentano
C 5 H12
CH 3 - CH2 - CH2 - CH2 - CH3
hexano
C 6 H14
CH 3 - CH2 - CH2 - CH2- CH2 - CH3
Alcanos C 10 a C 12
CnH2n+2
Serie homloga
decano
C 10 H22
CH 3 - (CH2)8 - CH3
undecano
C 11 H 24
CH 3 - (CH2)9 - CH3
dodecano
C 12 H26
CH 3 - (CH2)10 - CH3
Alcanos C 20 a C 22
CnH2n+2
Serie homloga
eicosano
C 20 H42
CH 3 - (CH2)18 - CH3
heneicosano
C 21 H 44
CH 3 - (CH2)19 - CH3
docosano
C 22 H46
CH 3 - (CH2)20 - CH3
butano
Francisco Cruz Sosa/Jorge Armando Haro Castellanos/Ignacio Lpez y Celis/Sergio Alatorre Santamara
11
Universidad Autnoma Metropolitana /Unidad Iztapalapa/Divisin de Ciencias Biolgicas y de la Salud
Esquema 1.3 Alcanos, alquenos, alquinos, compuestos aromticos: Formulacin y nomenclatura
Hidrocarburos C, H
Familia
Grupo Funcional
alcanos
- CH2 - CH2 -
CnH2n+2
alquenos
- CH = CH -
CnH2n
alquinos
- C C-
cicloalcanos
Ejemplos
Frmula General
CH4
metano
CH 3 - CH3
etano
H2C = CH2
H2C = CH - CH3
eteno propeno
etileno
propileno
H-C C-H
etino
acetileno
CnH2n-2
CnH2n
ciclohexano
cicloalquenos
ciclopenteno 1, 4-ciclohexadieno
aromticos
benceno
H
H
benceno
12
CH2CH3
H
1-buteno
Tema 1. Formulacin y nomenclatura de los compuestos orgnicos
Gua Temtica para el Curso de Qumica Orgnica I
Esquema 1.4 Nomenclatura de grupos alquilo y arilo
Grupo alquilo y arilo
Metano
metilo
CH3-
metileno
-CH2-
metino
H-C-
Etano
Propano
etilo CH3 - CH2-
n-propilo CH3 - CH2 -CH2 1-metiletilo CH3 - CH isopropilo
CH3
Pentano
Butano
n-butilo CH3 - CH2- CH2- CH22-metilpropilo CH3 - CH- CH2isobutilo
CH3
Eteno
etenilo
vinilo
CH2 = CH -
etilideno CH3 - CH =
CH3 - CH - CH 1-metilpropilo
sec-butilo
CH3
1, 1-dimetiletilo
tert-butilo
n-pentilo CH3 - CH2- CH2- CH2-CH2-
CH3
CH3 - C --
3-metilbutilo CH3 - CH - CH2- CH2isopentilo
CH3
CH3
Arilo
Propeno
1-propenilo CH3 - C = CH 2-propenilo
CH2 = CH - CH2alilo
propilideno CH3 - CH 2 - CH =
fenilo
C6 H5 CH2 -
bencilo C6 H5 - CH2 -
Francisco Cruz Sosa/Jorge Armando Haro Castellanos/Ignacio Lpez y Celis/Sergio Alatorre Santamara
13
Universidad Autnoma Metropolitana /Unidad Iztapalapa/Divisin de Ciencias Biolgicas y de la Salud
Esquema 1.5 Alcoholes, aldehdos, cetonas, cidos carboxlicos, steres. Formulacin y nomenclatura
Hidrocarburos oxigenados C, H, O
Familia
alcoholes
Grupo Funcional
grupo hidroxilo - OH
Ejemplos
Frmula
R - OH
CH4 - OH
metanol
alcohol metlico
CH 3 - CH2- OH
etanol
alcohol etlico
CHO
aldehdos
grupo carbonilo
unido a un
hidrgeno
R - CHO
CH3 - CHO
etanal
acetaldehdo
propanona
cetonas
grupo carbonilo
unido a
carbonos
R - CO - R
dimetil cetona
acetona
cidos carboxilicos
grupo carboxilo
R - COOH
CH 3 - COO H
cido etanoico
cido actico
steres
14
grupo alcoxicarbonilo
R - COOR
benzaldehdo
O
CH 3 - C- CH 3
COOH
cido benzoico
O
etanoato de metilo
acetato de metilo CH 3 - C- OCH 3
Tema 1. Formulacin y nomenclatura de los compuestos orgnicos
Gua Temtica para el Curso de Qumica Orgnica I
Esquema 1.6 Alcoholes. Formulacin y nomenclatura
Alcoholes
Alcoholes Primarios
metanol
alcohol metlico
etanol
alcohol etlico
CH 3 - OH
CH3 - CH2 - OH
propan-1-ol
CH3 - CH2 - CH2 - OH
1-propanol
alcohol n-proplico
butan-1-ol
CH3 - CH2 - CH2 -CH2 - OH
1-butanol
alcohol n-butlico
2-metil-propan-1-ol CH3 - CH - CH2 - OH
2-metil-1-propanol
alcohol isobutlico
CH3
CH3 - CH - OH
CH3
propan-2-ol
2-propanol
alcohol isoproplico
alcohol isoproplico
2-metilpropan-2-ol
2-metil-2-propanol
alcohol tert-butlico
CH3
CH3 - C- OH
CH3
OH
CH3
1-metilciclohexanol
CH3 - CH2 - CH - OH
CH3
Polialcoholes
butan-2-ol
2-butanol
alcohol sec-butlico
OH
CH2 - OH
alcohol benclico
Alcoholes Terciarios
Alcoholes Secundarios
ciclohexanol
ciclohexanol
dioles
trioles
CH2 - CH2
CH2 - OH
OH OH
etano-1, 2-diol
1, 2-etanodiol
etilenglicol
CH - OH
CH2- OH
propano-1, 2, 3-triol
1, 2, 3-propanotriol
glicerol o glicerina
1,2-etanodiol
Francisco Cruz Sosa/Jorge Armando Haro Castellanos/Ignacio Lpez y Celis/Sergio Alatorre Santamara
15
Universidad Autnoma Metropolitana /Unidad Iztapalapa/Divisin de Ciencias Biolgicas y de la Salud
Esquema 1.7 Aminas, amidas. Formulacin y nomenclatura
Hidrocarburos nitrogenados C, H, N
Familia
aminas
Grupo Funcional
Frmula
grupo amino
metanamina
metilamina
grupo alquilamino
N-metiletanamina
dimetilamina
grupo dialquilamino
amidas
Ejemplos
N,N-dimetilmetanamina
trimetilamina
etanamida
acetamida
grupo carboxamida
grupo N-alquilcarboxamida
N-metiletanamida
grupo N,N-dialquilcarboxamida
N,N-dimetiletanamida
metanfetamina
16
Tema 1. Formulacin y nomenclatura de los compuestos orgnicos
Gua Temtica para el Curso de Qumica Orgnica I
Esquema 1.8 Aminas. Formulacin y nomenclatura
Aminas
Alifticas
Alquilaminas
Aromticas
Heterociclos
Primarias
Heterociclos
Arilaminas
Primarias
metanamina
metilamina
etanamina
etilamina
azolidina
pirrolidina
ciclohexilamina
azol
pirrol
bencenamina
anilina
fenilamina
Secundarias
azina
piridina
Secundarias
N-metilmetanamina
dimetilamina
perhidroazina
piperidina
N-metilanilina
N-metiletanamina
etilmetilamina
indol
Terciarias
Terciarias
N,N-dimetilmetanamina
trimetilamina
butan-1,4-diamina
(putrescina)
N, N-dimetilanilina
luminol
Francisco Cruz Sosa/Jorge Armando Haro Castellanos/Ignacio Lpez y Celis/Sergio Alatorre Santamara
17
Universidad Autnoma Metropolitana /Unidad Iztapalapa/Divisin de Ciencias Biolgicas y de la Salud
Esquema 1.9 Haluros de alquilo y arilo. Formulacin y nomenclatura
Hidrocarburos halogenados C, H, X
Familia
haluros de alquilo
Frmula General
Grupo Funcional
grupo haluro
R-X
Ejemplos
clorometano
cloruro de metilo
bromoetano
bromuro de etilo
haluros de arilo
grupo haluro
Ar - X
bromobenceno
2-bromopropano
18
Tema 1. Formulacin y nomenclatura de los compuestos orgnicos
iodobenceno
Gua Temtica para el Curso de Qumica Orgnica I
Esquema 1.10 Haluros de alquilo y arilo. Formulacin y nomenclatura
Hidrocarburos Halogenados
Aliftico
Aromtico
metano halogenado (cloro)
benceno monohalogenado
clorometano
cloruro de metilo
diclorometano
cloruro de metileno
clorobenceno
triclorometano
cloroformo
bromobenceno
benceno dihalogenado
tetraclorometano
tetracloruro de carbono
haluro de alquilo: carbono primario
1-bromopropano
bromuro de propilo
orto-dibromobenceno meta-dibromobenceno para-dibromobenceno
benceno trihalogenado
1-bromo-2-metilpropano
bromuro de isobutilo
haluro de alquilo: carbono secundaro
1, 3, 5-tribromobenceno
2-bromopropano
bromuro de isopropilo
haluro de alquilo: carbono terciario
2-bromo-2-metilpropano
bromuro de tert-butilo
clorobenceno
Francisco Cruz Sosa/Jorge Armando Haro Castellanos/Ignacio Lpez y Celis/Sergio Alatorre Santamara
19
Gua Temtica para el Curso de Qumica Orgnica I
Tema 2
El enlace qumico en los compuestos orgnicos
2.1 El enlace inico, enlace covalente y enlace covalente coordinado
2.2 Polaridad de enlace y su efecto sobre las propiedades qumicas de los compuestos
2.3 Rompimiento del enlace covalente: homlisis y heterlisis
2.3.1 Homlisis. Formacin de radicales libres; su estructura y reactividad. Factores que catalizan la homlisis. Efecto de los
radicales libres sobre los organismos vivos
2.3.2 Heterlisis. Formacin de iones. Produccin de carbocationes y carbaniones
CH3
CH2
O
O -
H
N
CH2
CH3
Esquema 2.1 Nmero y tipos de enlaces en el tomo de carbono
Carbono
Enlace doble
Enlaces sencillos
Enlace triple
Hibridacin: sp3
Hibridacin: sp2
Hibridacin: sp
geometra: tetradrica
geometra: trigonal planar
geometra: lineal
metano CH4
enlaces
C
etano
etileno
H2C = CH2
enlace
C
enlaces
En la hibridacin tetradrica hay cuatro orbitales sp3 idnticos. Los orbitales
sp3 forman cuatro enlaces sencillos ()
con ngulos de 109 28 y estn dirigidos hacia los vrices de un tetraedro.
etino
HC CH
acetileno
En la hibridacin trigonal hay tres orbitales sp2 idnticos y un electrn en
un orbital puro 2p. Los orbitales sp2
forman tres enlaces sencillos () con
ngulos de 120 y estn dirigidos hacia
los vrtices de forma planar triangular.
El orbital puro 2p forma el enlace .
enlace
C
enlaces
C
enlace
En la hibridacin lineal hay dos orbitales sp idnticos y dos electrones, cada
uno en un orbital puro 2p. Los orbitales sp forman dos enlaces sencillos ()
con ngulos de 180. Los dos orbitales
puros 2p forma dos enlaces .
Francisco Cruz Sosa/Jorge Armando Haro Castellanos/Ignacio Lpez y Celis/Sergio Alatorre Santamara
21
Universidad Autnoma Metropolitana /Unidad Iztapalapa/Divisin de Ciencias Biolgicas y de la Salud
Enlace sencillo carbono - carbono
El enlace covalente sencillo est conformado por la unin de dos tomos de carbono mediante la comparticin de dos electrones
en un orbital molecular sigma (). Los electrones corresponden uno a cada tomo que forma la unin.
Enlace entre dos tomos de carbono: Localizacin de la densidad electrnica
Enlace doble carbono - carbono
El enlace doble est conformado por un enlace covalente y un enlace covalente . El primero () es un orbital molecular que
se forma con un par de electrones ubicados originalmente en orbitales atmicos sp2 y el segundo (), tambin es un orbital
molecular, pero a diferencia del anterior, ste est compuesto por un par de electrones de orbitales atmicos p.
Enlace triple carbono - carbono
El enlace covalente triple est conformado por un enlace y dos enlaces , se forma cuando se comparten un par de electrones ubicados en orbitales atmicos sp dando lugar al orbital molecular y dos pares de electrones originalmente ubicados en
orbitales atmicos p dando como resultado dos orbitales moleculares , uno por arriba y abajo en el plano, y el otro adelante
y atrs del plano.
22
Tema 2. El enlace qumico en los compuestos orgnicos
Gua Temtica para el Curso de Qumica Orgnica I
Esquema 2.2 Nmero y tipos de enlaces en el tomo de oxgeno
Oxgeno
Enlace doble
Enlaces sencillos
Hibridacin: sp3
geometra: tetradrica
Hibridacin: sp2
geometra: trigonal planar
etanol
propanona
acetona
alcohol etlico
par de electrones
sin compartir
enlace
par de electrones
sin compartir
enlaces
enlace
En la geometra planar trigonal el oxgeno tiene
un enlace y uno . Para el orbital , el oxgeno
contribuye con un electrn de un orbital hbrido sp
y para el enlace contribuye con un electrn en un
orbital p puro; y dos orbitales sp2 tienen c/u un par
de electrnes sin compartir. Los ngulos que forman
los orbitales son de 120.
En la hibridacin tetradrica hay cuatro orbitales
sp3 idnticos. Dos orbitales sp3 forman dos enlaces
sencillos () y dos orbitales sp3 tienen cada uno
un par de eletrones sin compartir. Los ngulos de
los enlaces sigma son de 108 9 y estan dirigidos
hacia los vrtices de un tetradro.
Esquema 2.3 Nmero y tipos de enlaces en el tomo de nitrgeno
Nitrgeno
Enlaces sencillos
Hibridacin: sp3
geometra: tetradrica
metanamina
metilamina
par de electrones
sin compartir
Enlace doble
Enlace triple
Hibridacin: sp2
geometra: tetradrica planar
etanonitrilo
acetonitrilo
metil imina de la acetona
(base de Schiff)
par de electrones
sin compartir
par de electrones
sin compartir
enlace
enlaces
enlaces
En la hibridacin tetradrica hay cuatro
orbitales sp3 idnticos. Tres orbitales
sp3 forman tres enlaces sencillos
() y un orbital sp3 tiene un par de
electrones sin compartir. Los ngulos
de los enlaces sp3 son de 109.5 y
estn dirigidos hacia los vrices de un
tetraedro.
Hibridacin: sp
geometra: lineal
En la hibridacin trigonal hay tres orbitales
sp2 idnticos y un electrn en un orbital
puro 2p. Los tres orbitales sp2, dos forman
enlaces sencillos () y el otro orbital sp2
tiene un par de electrones sin compatir,
los orbitales sp2 tienene ngulos de 120 y
estn dirigidos hacia los vrtices de forma
planar triangular. El orbital puro 2p forma
el enlace .
enlaces
enlace
En la hibridacin lineal hay dos
orbitales sp idnticos y dos electones,
cada uno en un orbital puro 2p. Un
orbital sp forma un enlace sencillo ()
y el otro orbiltal sp tiene un par de
electrones sin compartir, los orbitales
sp tienen ngulos de 180. Los dos
orbitales puros 2p forma dos enlaces .
Francisco Cruz Sosa/Jorge Armando Haro Castellanos/Ignacio Lpez y Celis/Sergio Alatorre Santamara
23
Universidad Autnoma Metropolitana /Unidad Iztapalapa/Divisin de Ciencias Biolgicas y de la Salud
cido cianhdrico
(cianuro de hidrgeno)
amoniaco
adenina
2.1.1 Enlace Inico
En un enlace inico la diferencia en los valores de electronegatividad entre los dos tomos que forman el enlace es alta (mayor
a 1.7) formndose iones positivos (tomos que pierden su electrn) adems de iones negativos (tomos que ganan el electrn).
Esquema 2.4 Valores de electronegatividad de los elementos ms comunes en qumica orgnica. La electronegatividad es la
capacidad de un tomo de atraer a los electrones del enlace en una molcula.
Electronegatividad
1A
Valores de electronegatividad de los
elementos ms comunes en qumica
orgnica (Escala de Pauling)
3A
B
2.0
4A
C
2.5
5A
6A
7A
N
3.0
O
3.5
F
4.0
P
2.1
S
2.5
Cl
3.0
H
2.1
2A
Li
1.0
Be
1.5
Na
0.9
Mg
1.2
Br
2.8
K
0.8
Ca
1.0
I
2.5
Al
1.5
Esquema 2.5 El enlace inico
Enlace inico
Sales de alcoholes
Sales de fenoles
etanoato
de sodio
acetato
de sodio
metxido de sodio
etxido de potasio
Sales de cidos carboxlicos
fenxido de sodio
Diferencia en electronegatividad
Sales de aminas
bromuro de
tetrametilamonio
benzoato
de potasio
Enlace inico diferencia
Enlace O - Na (3.5 - 0.9 = 2.6) = enlace inico
cloruro de piridinio
Enlace O - K (3.5 - 0.8 = 2.7) = enlace inico
O
Enlace O - Mg (3.5 - 1.2 = 2.3) = enlace inico
24
ftalato de magnesio
Tema 2. El enlace qumico en los compuestos orgnicos
Gua Temtica para el Curso de Qumica Orgnica I
2.1.2 Enlace covalente
En un enlace covalente la diferencia en los valores de electronegatividad entre los dos tomos que forman el enlace es baja
(menor a 1.7) formndose un enlace en el cual los dos tomos comparten uno o ms pares de electrones para estabilizar la
unin entre los tomos.
Esquema 2.6 El enlace covalente
Enlace covalente
Covalente no polar
Hidrocarburos
etano
Diferencia en electronegatividad
Enlace covalente no polar
diferencia inferior a 0.4
Enlace C - C (2.5 - 2.5 = 0)
eteno
etileno
Enlace H - H (2.1 - 2.1 = 0)
etino
acetileno
ciclohexano
fenol
dimetilter
ter dimetlico
Enlace covalente polar
diferencia entre 1.7 y 0.4
etanal
acetaldehdo
propanona
dimetil cetona
acetona
Enlace N - C (3.0 - 2.5 = 0.5)
Enlace N - H (3.5 - 2.1 = 0.9)
Enlace O - H (3.5 - 2.1 = 1.4)
benceno
metanol
alcohol metilico
Enlace C - H (2.5 - 2.1 = 0.4)
Enlace O - C (3.5 - 2.5 = 1.0)
ciclohexeno
Covalente polar
Enlace Cl - C (3.0 - 2.5 = 0.5)
cido etanoico
cido actico
metanamina
metilamina
triclorometano
cloroformo
ciclohexano
benceno
cloroformo
Francisco Cruz Sosa/Jorge Armando Haro Castellanos/Ignacio Lpez y Celis/Sergio Alatorre Santamara
25
Universidad Autnoma Metropolitana /Unidad Iztapalapa/Divisin de Ciencias Biolgicas y de la Salud
2.1.3 Enlace covalente coordinado
En un enlace covalente coordinado los dos tomos que forman el enlace no dependen de la electronegatividad si no de un
tomo que aporte un par de electrones y de otro tomo que aporte un orbital vaco, dando como resultado un ion positivo y
un ion negativo.
Esquema 2.7 El enlace covalente coordinado
Enlace covalente coordinado
Compuestos con nitrgeno
Compuestos con oxgeno
Compuestos oxigenados
Compuestos nitrogenados
Enlaces covalentes = 2
Enlaces covalentes = 3
Enlace covalente coordinado = 1
Enlace covalente coordinado = 1
ion alquil oxonio
enlaces
covalentes
enlace
covalente
coordinado
ion amonio
enlaces
covalentes
alcohol ettilco protonado
ion etil hidronio
ion dialquil oxonio
enlaces
covalentes
bromuro de
metilamonio
enlace
covalente
coordinado
ter protonado
ion dietil oxonio
26
cloruro de
anilinio
Tema 2. El enlace qumico en los compuestos orgnicos
enlace
covalente
coordinado
Gua Temtica para el Curso de Qumica Orgnica I
2.2 Polaridad de enlace y su efecto sobre las propiedades qumicas de los compuestos
La polaridad de un enlace entre dos tomos depende de que un tomo tenga una electronegatividad mayor a la del otro por lo
que el desplazamiento de la nube electrnica ser hacia el tomo ms electronegativo que tendr un carga parcial negativa, delta
negativa (-), mientras que el otro tomo tendr una carga parcial positiva, delta positiva (+).
Esquema 2.8 Polaridad del enlace y de molculas
Polaridad del enlace y de molculas
Polaridad del enlace
Polaridad en molculas
Momentos dipolares de enlace
Momentos dipolares moleculares
enlaces
sencillos
momento dipolar
en enlace (debye)
molculas
asimtricas
momento dipolar
en enlace (debye)
0.22
1.9
0.86
1.0
1.51
2.3
1.56
2.9
1.48
1.29
3.9
0.3
1.5
1.31
1.9
1.53
enlace
doble
momento dipolar
en enlace (debye)
molculas
simtricas
momento dipolar
en enlace (debye)
2.4
enlace
triple
momento dipolar
en enlace (debye)
3.6
Francisco Cruz Sosa/Jorge Armando Haro Castellanos/Ignacio Lpez y Celis/Sergio Alatorre Santamara
27
Universidad Autnoma Metropolitana /Unidad Iztapalapa/Divisin de Ciencias Biolgicas y de la Salud
Molculas polares
Una caracterstica importante de los compuestos polares es la interaccin dipolo-dipolo, por ejemplo: entre molculas de clorometano se presenta una orientacin en las molculas, debido a las fuerzas atractivas de las cargas positivas en la regin de los
hidrgenos (menos electronegativos) con las negativas en la regin del tomo de cloro (ms electronegativo).
Molculas apolares
Las molculas apolares o no polares estn conformadas por enlaces entre tomos con igual o similar electronegatividad, por lo
que la densidad electrnica se distribuye de forma simtrica en la molcula y no se crean cargas, por ejemplo en la molcula de
hidrgeno los tomos tienen la misma electronegatividad y por lo tanto su enlace es apolar o no polar.
Los alcanos son molculas no polares, ya que poseen tomos con electronegatividad similar.
Las molculas simtricas estn conformadas por tomos que tienen diferente electronegatividad, pero por su arreglo geomtrico
hace que se anule esta polaridad, ejemplos de este tipo de compuestos no polares es el tetracloruro de carbono (CCl4) y el
dixido de carbono (CO2).
tetracloruro de carbono
28
dixido de carbono
Tema 2. El enlace qumico en los compuestos orgnicos
Gua Temtica para el Curso de Qumica Orgnica I
2.3 Rompimiento del enlace covalente: homlisis y heterlisis.
Esquema 2.9 Rompimiento del enlace covalente
Rompimiento del enlace covalente
Roptura heteroltica
Roptura homoltica
Reacciones de homlisis
Formacin de radicales libres
Reacciones de heterlisis
Formacin de carbocationes
bromuro de tert-butilo
carbocatin
terciario
ion
bromuro
Formacin de carbaniones
cloroformo
carbanin
ion
terciario hidrgeno
Francisco Cruz Sosa/Jorge Armando Haro Castellanos/Ignacio Lpez y Celis/Sergio Alatorre Santamara
29
Universidad Autnoma Metropolitana /Unidad Iztapalapa/Divisin de Ciencias Biolgicas y de la Salud
2.3.1 Homlisis es la ruptura de un enlace covalente en el que los dos tomos que lo forman tienen la misma
o similar electronegatividad por lo que cada tomo retiene su electrn que comparta y esto da lugar a la
formacin de dos radicales libres, los cuales pese a no tener carga son muy reactivos debido al electrn que
queda desapareado.
Formacin de radicales libres; su estructura y reactividad. Factores que catalizan la homlisis. Efecto de los radicales libres sobre
los organismos vivos.
Esquema 2.10 Radicales libres: estructura y reactividad
Radicales libres: estructura y reactividad
Radiales libres y no radicales
Efecto de radicales libres en organismos
Especies reativas de oxgeno
Los radicales libres son muy reactivos pueden
reaccionar con lpidos, ADN protenas y carbohidratos.
Son radicales libres
Esctructura
radical anin
superxido
Agentes exgenos que pueden producir
radicales libres
Contaminacin por automotores
radical
hidroxilo
Contaminacin ambiental
Excesiva exposicin a la radiacin solar
xido de
nitrogeno II
Fumar cigarros: humo del tabaco
Especies reactivas de oxgeno
No son radicales libres
Esctructura
perxido de
hidrogeno
Alimentos que pueden producir
radicales libres
Dietas ricas en grasas, en especial: ingesta de
aceites vegetales sometidos a altas temperaturas
(aceite requemado) y cidos grasos trans.
Estado anmico del organismo ante
situaciones externas reales o imaginarias
ozono
El stres puede causar: obesidad, sobrepeso, prdida
de cabello depresin, acn, insomnio, lceras,
enfermedades cardacas, reduccin del deseo sexual.
peroxinitrto
Especies reactivas de oxgeno (ROS)
El efecto de especies reactivas de oxgeno (ROS) en los organismos vivos produce el deterioro del ADN y la modificacin de la
estructura de las protenas, adems del proceso de peroxidacin lipdica que lleva a la degradacin y destruccin de la membrana
celular; dando como consecuencia la modificacin de las caractersticas estructurales y funcionales en un tejido vivo.
Los alimentos como el aguacate contienen antioxidantes, que son compuestos que inhiben la actividad (oxidacin) de las
especies reactivas de oxgeno.
Antioxidante
Antioxidante
neutraliza a
radical libre
30
Tema 2. El enlace qumico en los compuestos orgnicos
Gua Temtica para el Curso de Qumica Orgnica I
Esquema 2.11 Estabilidad de radicales libre del carbono
Estabilidad de radicales libre del carbono
Estabilidad
metilo
radical libre
terciario
radical libre tert-butilo
radical libre
primario
radical libre
secundario
radical libre isopropilo
radical libre etilo
radical libre metilo
Radical libre metilo
2.3.2 La heterlisis es la ruptura de un enlace covalente muy polarizado, en donde el tomo que presenta
mayor electronegatividad se lleva el par de electrones del enlace formando iones negativos llamados
carbaniones, y por otra parte se forman los iones positivos conocidos como carbocationes o iones carbonio.
Francisco Cruz Sosa/Jorge Armando Haro Castellanos/Ignacio Lpez y Celis/Sergio Alatorre Santamara
31
Universidad Autnoma Metropolitana /Unidad Iztapalapa/Divisin de Ciencias Biolgicas y de la Salud
Esquema 2.12 Estabilidad de carbocationes y carbaniones
Estabilidad
Carbaniones
Carbocationes
metilo
vinilo
fenilo
carbocatin
terciario
carbocatin
bencilo
carbocatin
secundario
carbanin
metilo
carbanin
primario
carbocatin
alilo
carbocatin
primario
carbocatin
metilo
carbanin
secundario
carbanin
terciario
carbocatin
vinilo
32
metilo
carbocatin
fenilo
Tema 2. El enlace qumico en los compuestos orgnicos
Gua Temtica para el Curso de Qumica Orgnica I
Tema 3
Alcanos
3.1 El metano como alcano tpico; su estructura y tipo de enlace. La hibridacin sp3 caracterstica
de los alcanos. Orbitales sigma y sus propiedades
3.2 Reacciones de alcanos
3.2.1 Sustitucin por radicales libres; ejemplo: halogenacin
3.2.2 Pirlisis (Cracking)
3.2.3 Combustin
3.1 El metano como alcano tpico; su estructura y tipo de enlace. La hibridacin sp3 caracterstica de
los alcanos. Orbitales sigma y sus propiedades
El metano es el hidrocarburo saturado ms sencillo, el tomo de carbono presenta hibridacin sp3 la cual consiste en la combinacin del orbital 2s con los tres orbitales 2p para generar cuatro orbitales hbridos sp3, los cuales forman enlaces sencillos sigma
con los 4 tomos de hidrgeno para formar una estructura tetradrica.
Orbital hbrido sp3
Estructura tetradrica del metano
Esquema 3.1 Metano
Metano
Frmula empirica de los alcanos
metano
frmula molecular
frmula desarrollada
Configuracin electrnica del carbono
estado fundamental del carbono
promocin de un electrn del
orbital 2s al orbital 2p
hibridacin sp3 del carbono
estructura qumica
(geometra tetradrica)
4 orbitales hbridos sp3
4 enlaces sencillos ()
Francisco Cruz Sosa/Jorge Armando Haro Castellanos/Ignacio Lpez y Celis/Sergio Alatorre Santamara
33
Universidad Autnoma Metropolitana /Unidad Iztapalapa/Divisin de Ciencias Biolgicas y de la Salud
3.2 Reacciones de alcanos
3.2.1 Sustitucin por radicales libres; ejemplo: halogenacin
La halogenacin de los alcanos es un proceso qumico mediante el cual se van a sustituir los tomos de hidrgeno por los halgenos (F, Cl, Br y I). El halgeno ms comnmente usado para este tipo de reacciones es el cloro (Cl2), que se emplea en forma
de gas, en presencia de luz y a temperatura ambiente. La bromacin requiere de luz y temperatura (125 C), la reaccin con flor
requiere condiciones especiales, ya que es explosiva y con iodo es endotrmica.
Esquema 3.2 Sustitucin por radicales libres: halogenacin
Sustitucin por radicales libres
Halogenacin de alcanos
Monocloracin del etano
Reaccin de monocloracin del metano
radical libre etilo
mecanismo
etapa 1: iniciacin
cloruro de etilo
etapa 2: propagacin
monocloracin del propano
radical n-propilo
radical isopropilo
cloruro de metilo
clorometano
etapa 3: terminacin
1-cloropropano
cloruro de n-propilo
(45%)
cloruro de metilo
clorometano
etano
34
Tema 3. Alcanos
2-cloropropano
cloruro de isopropilo
(55%)
Gua Temtica para el Curso de Qumica Orgnica I
Cloruro de metilo (CH3-Cl). Es un hidrocarburo que se comercializa como gas licuado comprimido, se emplea en la fabricacin del sellador de silicn y en la fabricacin de metil celulosa, entre otros productos.
Sustituciones adicionales en el cloruro de metilo
cloruro de metilo
(clorometano)
cloruro de metileno
(diclorometano)
cloroformo
triclorometano
cloroformo
triclorometano
cloruro de metileno
(diclorometano)
tetracloruro de carbono
El cloruro de metileno o diclorometano es un lquido incoloro, tiene mltiples usos como disolvente, se usa en la limpieza
de equipo de cmputo entre otras aplicaciones. El cloroformo se utiliza como materia prima en la industria qumica y como
disolvente mientras que el tetracloruro de carbono actualmente, ya no se utiliza debido a su toxicidad.
Monocloracin de alcanos
n-butano
2-metilpropano
isobutano
1-clorobutano (28%)
1-cloro-2-metilpropano
cloruro de isobutilo (64%)
2-clorobutano (72%)
2-cloro-2-metilpropano
cloruro de tert-butilo (36%)
Francisco Cruz Sosa/Jorge Armando Haro Castellanos/Ignacio Lpez y Celis/Sergio Alatorre Santamara
35
Universidad Autnoma Metropolitana /Unidad Iztapalapa/Divisin de Ciencias Biolgicas y de la Salud
La bromacin es una reaccin ms regioselectiva que la cloracin, por lo que se pueden formar ismeros constitucionales,
en donde uno de ellos predomina ms que otro de una manera significativa. Por ejemplo: la bromacin del propano se realiza
a 330 C en fase vapor para dar un 97% de bromuro de isopropilo y 3% de bromuro de n-propilo.
Esquema 3.3 Monobromacin de alcanos
Monobromacin de alcanos
n-propano
n-butano
2-metilpropano
isobutano
1-bromopropano
bromuro de n-propilo (3%)
2-bromopropano
bromuro de isopropilo (97%)
1-bromobutano
bromuro de n-butilo (2%)
1-bromo-2-metilpropano
bromuro de isobutilo (1%)
2-bromobutano
bromuro de sec-butilo (98%)
2-bromo-2-metilpropano
bromuro de tert-butilo (99%)
2-bromopropano
36
Tema 3. Alcanos
Gua Temtica para el Curso de Qumica Orgnica I
3.2.2 Pirlisis o cracking se define como la descomposicin de un compuesto orgnico originada por calor
en ausencia de oxgeno. Cuando se hace pasar un alcano a travs de una cmara de calentamiento con
temperatura entre 400-600C se produce la fragmentacin de estas molculas en alcanos de peso molecular
menor y en alquenos.
Esquema 3.4 Pirlisis de alcanos
Pirlisis (Cracking) de alcanos
Alcanos
pirlisis
Alcanos menores
Alquenos
400 - 600 C, catalizador
Francisco Cruz Sosa/Jorge Armando Haro Castellanos/Ignacio Lpez y Celis/Sergio Alatorre Santamara
37
Universidad Autnoma Metropolitana /Unidad Iztapalapa/Divisin de Ciencias Biolgicas y de la Salud
3.2.3 Combustin de Alcanos
La combustin es un proceso de las molculas orgnicas, en la cual los tomos de carbono de la molcula se combinan con el
oxgeno convirtindose en molculas de dixido de carbono y los tomos de hidrgeno en agua. La combustin es una reaccin
exotrmica, el calor desprendido se llama calor de combustin.
Esquema 3.5 Combustin de alcanos
Combustin de alcanos
Alcanos
exceso de O2
Exceso de O2
Llama (fuego)
calor
= calor de combustin
= - 211 Kcal/mol
calor
= - 368 kal/mol
calor
= - 526 Kcal/mol
calor
= - 687 Kcal/mol
calor
= - 845 Kcal/mol
calor
38
Productos
Tema 3. Alcanos
Gua Temtica para el Curso de Qumica Orgnica I
Tema 4
Alquenos
4.1 Estructura. La hibridacin sp2 y la formacin del enlace en los alquenos
4.2 Caractersticas de los enlaces . Rigidez, isomera, polarizacin, efecto inductivo
4.3 Isomera cis-trans y E-Z: reacciones de adicin caracterstica de los alquenos
4.3.1 Adicin de haluros de hidrgeno
4.3.2 Adicin de cido sulfrico
4.3.3 Adicin de halgenos
4.3.4 Hidratacin de alquenos catalizada por cidos
4.3.5 Hidrogenacin de alquenos
4.3.6 Polimerizacin de alquenos. Obtencin de polietileno: Polimerizacin catinica y polimerizacin por radicales libres,
su aplicacin en la industria
4.4 Oxidacin de alquenos: Reacciones con permanganato, cido ntrico y ozono
4.5 Obtencin de alquenos a partir de compuestos halogenados
4.6 Identificacin de alquenos
4.7 Dienos acumulados, dienos conjugados y dienos aislados
Francisco Cruz Sosa/Jorge Armando Haro Castellanos/Ignacio Lpez y Celis/Sergio Alatorre Santamara
39
Universidad Autnoma Metropolitana /Unidad Iztapalapa/Divisin de Ciencias Biolgicas y de la Salud
4.1 Estructura. La hibridacin sp2 y la formacin del enlace en los alquenos
Los alquenos u olefinas son hidrocarburos insaturados que contienen uno o ms dobles enlaces carbono-carbono. El alqueno
ms simple es el eteno o etileno, es una molcula coplanar debido a que los ncleos de sus tomos se encuentran en el mismo
plano. El etileno se usa en la industria para la obtencin de polmeros (polietileno). Se considera una hormona vegetal en la
maduracin de ctricos (limones, naranjas) y de algunas frutas como pltanos.
Eteno (etileno)
Esquema 4.1 Formacin del enlace en los alquenos e hibridacin sp2
Alquenos
Configuracin electrnica del carbono
Frmula empirica de los alquenos
estructura del doble enlace
carbono - carbono
estado fundamental del carbono
enlace
enlaces
enlaces
promocin de un electrn del
orbital 2s al orbital 2p
enlace
hibridacin sp2 del carbono
3 orbitales hbridos sp2
+ un orbital p
3 enlaces sencillos ()
+ un enlace
40
Tema 4. Alquenos
Gua Temtica para el Curso de Qumica Orgnica I
4.2 Caractersticas de los enlaces . Rigidez, isomera, polarizacin, efecto inductivo.
Los enlaces moleculares se forman por el traslape de los orbitales atmicos p en la hibridacin sp2. El enlace es ms dbil
(ms reactivo) que el enlace s. La isomera cis - trans o isomera geomtrica es una caracterstica de los alquenos, en el ismero
cis los sustituyentes estn en el mismo lado del doble enlace y en el ismero trans, se encuentran en lados opuestos, ambos
tienen la misma frmula condensada pero diferente arreglo en el espacio y presentan diferentes propiedades fsicas y qumicas.
Esquema 4.2 Enlace
Caractersticas del enlace
Isometra geomtrica
Enlace sencillo carbono - carbono
libre rotacin del enlace sencillo
gira
cis-2-buteno
trans-2-buteno
ismero (Z) con grupos de mayor
prioridad del mismo lado
enlace doble carbono - carbono
no hay rotacin del enlace doble
ismero (E) con grupos de mayor
prioridad en lados opuestos
rigido
rigido
No gira
(Z)-1-bromo-1-cloropropeno
(E)-1-bromo-1-cloropropeno
efecto inductivo electro-atrayente del oxgeno: polarizacin del doble enlace carbono-oxgeno
densidad
electrnica
negativa en
el oxgeno
densidad
electrnica
positiva en
el carbono
cis-2-buteno
trans-2-buteno
Francisco Cruz Sosa/Jorge Armando Haro Castellanos/Ignacio Lpez y Celis/Sergio Alatorre Santamara
41
Universidad Autnoma Metropolitana /Unidad Iztapalapa/Divisin de Ciencias Biolgicas y de la Salud
4.3 Reacciones de adicin caracterstica de los alquenos
Los alquenos tienen una caracterstica importante, la posicin de los electrones p; estos se encuentran alejados de los ncleos
de los tomos del enlace carbono-carbono y por lo tanto son retenidos con menor fuerza, por lo que estn expuestos a sufrir un
ataque por un electrfilo (molcula o grupo con carga parcial o formal positiva), para formar un enlace y un carbocatin que
puede tener afinidad por un nuclofilo. Un nuclefilo es una especie qumica que contiene un par de electrones o una carga
negativa que puede ceder o compartir con un electrfilo, el cual puede aceptar un par de electrones para formar un enlace.
Nuclefilos fuertes
Nuclefilos moderados
Nuclefilos dbiles
Esquema 4.3 Adicin electroflica al doble enlace carbono - carbono
Adicin electroflica al doble enlace carbono - carbono
Reaccin General
enlace
enlace
nuevos
enlaces
sencillos
()
electrfilo nuclefilo
enlace
Mecanismo general de la adicin electroflica a alquenos
carbocatin
etapa 1
etapa 2
42
Tema 4. Alquenos
Gua Temtica para el Curso de Qumica Orgnica I
4.3.1 Adicin de haluros de hidrgeno
Los alquenos reaccionan con reactivos simtricos como el hidrgeno (H-H) o un halgeno (X-X) o con molculas asimtricas
como el cido clorhdrico (HCl). Cuando los carbonos del doble enlace tienen sustituyentes iguales y/o el reactivo de adicin
es simtrico, tambin la adicin es simtrica, pero cuando los sustituyentes de los carbonos del doble enlace son diferentes y
el reactivo es asimtrico, la adicin es asimtrica. La regla de Markovnikov indica que cuando un reactivo asimtrico como el
HCl reacciona con un alqueno, el tomo de hidrgeno se acopla al carbono con el mayor nmero de tomos de hidrgeno y el
halgeno al carbono ms sustituido, es decir en esta adicin ocurre la formacin del carbocatin ms estable.
Esquema 4.4 Adicin de haluros de alquilo
Adicin de haluros de alquilo HX
Adicin simtrica
2-buteno
Adicin asimtrica
Regla de Markovinikov
2-metil-2-buteno
producto principal
2-bromo-2-metibutano
2-bromobutano
Mecanismo de reaccin: adicin asimtrica
etapa 1: producto principal, formacin del carbocatin terciario
producto secundario
2-bromo-3-metibutano
etapa 1: producto secundario, formacin del carbocatin secundario
etapa 2: producto principal, ataque del ion bromuro al carbocatin principal
2-bromo-2-metibutano
etapa 2: producto secundario, ataque del ion bromuro al carbocatin secundario
2-bromo-3-metibutano
Francisco Cruz Sosa/Jorge Armando Haro Castellanos/Ignacio Lpez y Celis/Sergio Alatorre Santamara
43
Universidad Autnoma Metropolitana /Unidad Iztapalapa/Divisin de Ciencias Biolgicas y de la Salud
4.3.2 Adicin de cido sulfrico
Los alquenos reaccionan con el cido sulfrico concentrado y fro formando sulfatos cidos de alquilo, los cuales se producen por
adicin de un tomo de hidrgeno a un carbono del enlace p y la adicin del in bisulfato, al otro carbono del mismo enlace p.
Estos compuestos tambin se conocen como steres del cido sulfrico, los cuales pueden convertirse a alcoholes al reaccionar
en caliente con agua.
Esquema 4.5 Adicin de cido sulfrico
Adicin de cido sulfrico H2SO4
Adicin asimtrica
Regla de Markovinikov
sulfato cido de alquilo
2-metil-2-buteno
Mecanismo de reaccin: adicin asimtrica
etapa 1: formacin del carbocatin terciario
etapa 2: ataque del ion bisulfato al carbocatin
conversion del sulfato de alquilo a un alcohol
2-metil-2-butanol
44
Tema 4. Alquenos
Gua Temtica para el Curso de Qumica Orgnica I
4.3.3 Adicin de halgenos
La halogenacin de alquenos se efecta principalmente con cloro y bromo para dar como producto un dihalogenuro vecinal.
Esquema 4.6 Adicin de halgenos
Adicin de halgenos X2
Mecanismo de reaccin: adicin anti
etapa 1: formacin del ion bromonio (halogenonio)
dihalogenuro vecinal
etapa 2: ataque del ion bromuro (halogenuro) desde el lado opuesto
trans-1, 2-dibromociclohexano
cis-2-buteno
()-treo-2, 3-dibromobutano
enantimeros: mezcla racmica
cis-2-buteno
eritro-2,3-dibromobutano
meso-2, 3-dibromobutano
trans-2-buteno
Bromacin del 2-buteno
Francisco Cruz Sosa/Jorge Armando Haro Castellanos/Ignacio Lpez y Celis/Sergio Alatorre Santamara
45
Universidad Autnoma Metropolitana /Unidad Iztapalapa/Divisin de Ciencias Biolgicas y de la Salud
4.3.4 Hidratacin de alquenos catalizada por cidos
Los alquenos reaccionan con el agua en presencia de cidos como catalizadores, dando como producto alcoholes, esta es una
reaccin de adicin que sigue la regla de Markovnikov.
Esquema 4.7 Hidratacin de alquenos catalizada por cidos
Reaccin de hidratacin de alquenos en medio cidos
Adicin simtrica
2-buteno
Adicin asimtrica
Regla de Markovnikov
2-butanol
2-metil-2-butano
producto principal
2-metil-2-butanol
Mecanismo de reaccin: adicin asimtrica
etapa 1: producto principal, formacin del carbocatin terciario
producto secundario
3-metil-2-butanol
etapa 1: producto secundario, formacin del carbocatin secundario
etapa 2: producto principal, ataque nucleofilico del H2O
etapa 2: producto secundario, ataque nucleofilico del H2O
Contina esquema
46
Tema 4. Alquenos
Gua Temtica para el Curso de Qumica Orgnica I
etapa 3: producto principal, perdida del protn
etapa 3: producto secundario, perdida del protn
etano
etanol
Adicin de H2O al eteno en medio cido (adicin simtrica)
isobuteno
alcohol tert-butlico
Adicin de H2O al isobuteno en medio cido (adicin asimtrica)
Francisco Cruz Sosa/Jorge Armando Haro Castellanos/Ignacio Lpez y Celis/Sergio Alatorre Santamara
47
Universidad Autnoma Metropolitana /Unidad Iztapalapa/Divisin de Ciencias Biolgicas y de la Salud
4.3.5 Hidrogenacin de alquenos
La hidrogenacin es la adicin de hidrgeno al doble enlace carbono carbono (enlace ), para la obtencin de alcanos, utilizando como catalizadores platino, paladio o nquel, en donde el paladio se encuentra en forma de polvo adsorbido en carbn
(Pd/C).
Esquema 4.8 Hidrogenacin de alquenos
Hidrogenacin de alquenos
catalizador = (Pt, Pd, Ni)
catalizador
Alcano
mecanismo de hidrogenacin cataltica
alquenos adsorbido
en la superficie del
catalizador
tomos de H
adsorbidos en
la superficie
del catalizador
superficie del catalizador metlico
un tomo de H es
transferido al alqueno
un segundo tomo
de H es trasnferido al
alqueno
catalizador regenerado
el producto de reaccin es un alcano ya que dos
tmos de H se han aadido doble enlace del mismo
lado, dando un producto de adicin syn
48
Tema 4. Alquenos
Gua Temtica para el Curso de Qumica Orgnica I
4.3.6 Polimerizacin de alquenos. Obtencin de polietileno: Polimerizacin catinica y Polimerizacin por
radicales libres, su aplicacin en la industria
En la produccin de polietileno, un aspecto importante es utilizar etileno puro, se requiere de un reactor de alta presin, para
llevar a cabo la polimerizacin rpida y tener un equipo para la comprensin, para trabajar a 1000 atm bajo un control estricto
de la temperatura, ya que la reaccin es exotrmica. La polimerizacin se efecta en presencia de catalizadores que producen
radicales libres. El polietileno se utiliza en la fabricacin de bolsas, botellas, aislantes para cables, tubera de riego, envases industriales entre otros.
Esquema 4.9 Polimerizacin de alquenos
Polimerizacin de alquenos
alqueno
catalizador
polmero
Francisco Cruz Sosa/Jorge Armando Haro Castellanos/Ignacio Lpez y Celis/Sergio Alatorre Santamara
49
Universidad Autnoma Metropolitana /Unidad Iztapalapa/Divisin de Ciencias Biolgicas y de la Salud
Esquema 4.10 Polimerizacin de alquenos: etileno
Hidrogenacin de alquenos
etileno
catalizador
polietileno
etapa 1: formacin del radicales libres, perxido de benzoilo y adicin al doble enlace
calor
radical carboxilo
etapa 2: propagacin, se repite cientos o miles de veces
etapa 3: terminacin
polietileno
50
Tema 4. Alquenos
Gua Temtica para el Curso de Qumica Orgnica I
Polimerizacin Catinica. Etapas
Iniciacin: Se adiciona un cido en donde los electrones del alqueno atrapan al protn, generndose de esta manera un
carbocatin.
Propagacin: El carbocatin formado ataca a los electrones de la otra molcula, formndose un nuevo carbocatin y as
continua la reaccin.
Terminacin: La cadena deja de crecer y en ese momento el carbocatin reacciona con el anin.
Esquema 4.11 Polimerizacin de alquenos: polimerizacin catinica
Polimerizacin catinica
Catalizador = H2SO4 BF3
catalizador
isobutileno
Mecanismo de reaccin
poliisobutileno
etapa 1: protonacin del doble enlace, formacin del carbocatin
cation terbutilo
etapa 2: ataque nucleofilico del alqueno al catin terbutilo
etapa 3: propagacin, se repite el ataque nucleofilico del alqueno al carbocatin formado
etapa 4: terminacin, se repite cientos o miles de veces al ataque nucleofilico del alqueno al carbocatin formado
poliisobutileno
Francisco Cruz Sosa/Jorge Armando Haro Castellanos/Ignacio Lpez y Celis/Sergio Alatorre Santamara
51
Universidad Autnoma Metropolitana /Unidad Iztapalapa/Divisin de Ciencias Biolgicas y de la Salud
4.4 Oxidacin de alquenos: Reacciones con permanganato, cido ntrico y ozono
Esquema 4.12 Oxidacin de alquenos
Oxidacin de alquenos
Ozonlisis O3
Permanganato de potasio KMNO4
carbono
secundario
carbono
terminal
calor
moloznido
Mecanismo de reaccin
oznido
carbono
secundario
carbono
secundario
carbono
terciario
carbono
secundario
calor
calor
carbono carbono
cuaternario terciario
El permanganato de potasio (KMnO4) es un agente oxidante fuerte, que se utiliza en la oxidacin de alquenos en medio cido
o bsico y calentamiento, los alquenos son transformados en aldehdos pero la reaccin continua hasta la formacin de cidos
carboxlicos. Los alquenos terminales en su proceso de oxidacin con permanganato de potasio liberan dixido de carbono y la
formacin del cido carboxlico.
Oxidacin del 1-penteno con KMnO4 en medio cido y calor
Ozonlisis reductiva
El ozono en presencia de un alqueno asimtrico (un carbono cuaternario y un carbono terciario formando el doble enlace carbonocarbono) da como producto de reaccin un moloznido, especie qumica inestable, que inmediatamente sufre un rearreglo
para dar una molcula ms estable llamado oznido, y este en presencia de agua da dos productos: una cetona y un aldehdo.
Como subproducto de la reaccin se forma el perxido de hidrgeno que tambin es un agente oxidante (H2O2) transformando
al aldehdo en cido carboxlico, para evitar esta oxidacin se agrega Zn metlico para detener la oxidacin.
H 2 O2 + Zn
52
Tema 4. Alquenos
Zn(O H) 2
Gua Temtica para el Curso de Qumica Orgnica I
Molculas de ozono
4.5 Obtencin de alquenos a partir de compuestos halogenados
Los halogenuros de alquilo se comportan como electrfilos debido al enlace polar que forman el carbono-halgeno, reaccionan
fcilmente con bases fuertes para producir alquenos.
Esquema 4.13 Obtencin de alquenos a partir de compuestos halogenados
Obtencin de alquenos a partir de R-X
Deshidrohalogenacin de R-X
Solventes polares
E1 R-X 3 y 2
Bases fuertes E2
R-X CH 3 , 1 y 2
Eliminacin E2
Eliminacin E1
CH
CH
Br
H 2O
CH
C
CH
CH
CH
+ H 3O
CH
- CH
- Br
KO H
CH
CH
CH 3 -O H
+ KB r + H 2 O
bromuro de tert-butilo
2-bromo-2-metilpropano
isobuteno
2-metilpropeno
bromuro de etilo
bromoetano
etileno
eteno
Francisco Cruz Sosa/Jorge Armando Haro Castellanos/Ignacio Lpez y Celis/Sergio Alatorre Santamara
53
Universidad Autnoma Metropolitana /Unidad Iztapalapa/Divisin de Ciencias Biolgicas y de la Salud
Esquema 4.14 Mecanismo E1 y E2
Mecanismo E1 y E2
Mecanismo E1
base
Mecanismo E2
base
fuerte
base
etanol
calor
carbocatin
terciario
estado de transicin
base - H
base - H
4.6 Identificacin de alquenos
Esquema 4.15 Identificacin de alquenos
Identifica cin de al quenos
Reactivo de Baeyer
Ensayo con bromo
color
rojo
color
violeta
incoloro
Diol
color caf
propeno
color
rojo
1,2-dibromopropano
propeno
color
violeta
1,2-dihidroxipropano
(incoloro)
color caf
54
Tema 4. Alquenos
Gua Temtica para el Curso de Qumica Orgnica I
4.7 Dienos acumulados, dienos conjugados y dienos aislados
Esquema 4.16 Dienos
Dienos acumulados, conjugados y aislados
Dienos acumulados
(dobles enlaces juntos o alenos)
Dienos conjugados
(dobles enlaces alternados con
enlaces sencillos)
Dienos aislados
(dobles enlaces separados por
ms de un enlace sencillo)
1, 3-butadieno
propadieno
1, 4-pentadieno
Esquema 4.17 Estabilidad de dienos
Calores de hidrogenacin de alquenos y dienos
alquenos
H medido
-30.3
dienos
H calculado
-60.6
diferencia
-3.5
-54.1
-57.7
-3.6
-60.2
-60.2
-0.0
1, 3-butadieno
1-buteno
-30.1
1, 3-pentadieno
1-penteno
-27.6
2-penteno
H medidos
-57.3
1, 4-pentadieno
Energa de resonancia o energa de deslocalizacin o energa de conjugacin
El valor medido para el 1,3-pentadieno es de -54.1Kcal/mol y el valor calculado es de -57.7 Kcal/
mol lo que da una diferencia de -3.6 Kcal/mol, lo que indica que un doble enlace conjugado es
aproximadamente 3.6 Kcal/mol ms estable de lo esperado. A diferencia del 1,4-pentadieno en el
cual el valor medido y el esperado son iguales (doble enlace aislado).
Francisco Cruz Sosa/Jorge Armando Haro Castellanos/Ignacio Lpez y Celis/Sergio Alatorre Santamara
55
Universidad Autnoma Metropolitana /Unidad Iztapalapa/Divisin de Ciencias Biolgicas y de la Salud
Esquema 4.18 Reaccin de Diels-Alder
Reaccin de Diels-Alder
Mecanismo de la reaccin de Diels-Alder
Reaccin de Diels-Alder
1,3-butadieno
3-buten-2-ona
calor
estado de transicin cclico
3-ciclohexenil metil cetona
isopreno
56
Tema 4. Alquenos
Gua Temtica para el Curso de Qumica Orgnica I
Tema 5
Resonancia
5.1 Definicin. Ejemplos: La adicin 1,4 de los dienos explicada en funcin de la resonancia. Resonancia del ion carbonato.
Resonancia de los sistemas conjugados
5.2 Reglas de resonancia
5.3 Aplicacin de la teora de la resonancia
5.4 El benceno y su resonancia
5.5 Estabilidad y energa de resonancia
5.6 Aromaticidad: coplanaridad, alternancia y regla de Hckel
5.7 Compuestos aromticos heterocclicos: pirrol, furano, piridina
5.8 Sustitucin electroflica en el benceno, mecanismos: nitracin, halogenacin, sulfonacin, alquilacin y acilacin
5.9 Efecto de los sustituyentes sobre la sustitucin electroflica en el benceno
5.1 Definicin. Ejemplos: La adicin 1,4 de los dienos explicada en funcin de la resonancia. La
resonancia describe la deslocalizacin de electrones en un sistema en el cual los electrones se
encuentran en ms de dos tomos.
Los dienos presentan resonancia. Son compuestos relativamente estables, pero muy reactivos en presencia de radicales libres y
sufren reacciones de adicin (1-2) y (1-4).
doble enlace parcial
pequeo traslape
Francisco Cruz Sosa/Jorge Armando Haro Castellanos/Ignacio Lpez y Celis/Sergio Alatorre Santamara
57
Universidad Autnoma Metropolitana /Unidad Iztapalapa/Divisin de Ciencias Biolgicas y de la Salud
Esquema 5.1 Adicin 1,4 de los dienos
Adicin 1,4 en dienos conjugados
Adicin 1,4
Adicin 1,2
3-bromo-1-buteno
1-bromo-2-buteno
1,3-butadieno
etapa 1: adicin electrfilica
Mecanismo de reaccin
etapa 2: adicin del nuclefilo
3-bromo-1-buteno
1-bromo-2-buteno
Control cintico y control termodinmico en la adicin de HBr al 1,3-butadieno. En la adicin electroflica del cido bromhdrico al 1,3-butadieno a -80 C, el producto principal formado es el 3-bromo-1-buteno con un 80% adicin (1-2) y el 20% de
1-bromo-2-buteno por adicin (1-4). Si la reaccin anterior se efecta calentando a 40 C, el producto que predomina es de la
adicin (1-4) con un porcentaje del 85%.
3-bromo-1-buteno
producto 1,2 (80%)
1-bromo-2-buteno
producto 1,4 (20%)
1,3-butadieno
3-bromo-1-buteno
producto 1,2 (15%)
58
Tema 5. Resonancia
1-bromo-2-buteno
producto 1,4 (85%)
Gua Temtica para el Curso de Qumica Orgnica I
Los porcentajes de cada ismero estn en funcin de la temperatura de reaccin, el producto de control cintico (formacin
ms rpida) es el producto 1,2 y el producto de control termodinmico (producto ms estable) es el producto 1,4.
carbocatin allico
energa
3-bromo-1-buteno
producto 1,2 menos estable
1-bromo-2-buteno
producto 1,4 ms estable
transcurso de la reaccin
La adicin 1,2 tiene menor energa de activacin que la adicin 1,4 y se lleva a cabo con mayor rapidez (a todas las temperaturas);
aunque el producto 1,2 se forma con ms rapidez tambin revierte con ms rapidez al carbocatin allico intermedio. A 40C se
establece un equilibrio y la concentracin de los productos se determina por sus estabilidades relativas. A 40oC el producto 1,4
es el ms estable y es el que predomina (85%).
5.1 (Continuacin) Resonancia del ion carbonato. Resonancia de los sistemas conjugados
La determinacin experimental de la longitud de los tres enlaces carbono-oxgeno da como resultado que tiene la misma
longitud (1.31 ) por lo tanto, se puede concluir que la estructura es un hbrido en resonancia, en donde la carga negativa esta
deslocalizada entre los tres tomos de oxgenos.
Esquema 5.2 Resonancia
Resonancia
Resonancia del ion carbonato
estructura de resonancia
del ion carbonato
Resonancia de sistemas conjugados
estructura de resonancia
del 1,3-butadieno
Francisco Cruz Sosa/Jorge Armando Haro Castellanos/Ignacio Lpez y Celis/Sergio Alatorre Santamara
59
Universidad Autnoma Metropolitana /Unidad Iztapalapa/Divisin de Ciencias Biolgicas y de la Salud
5.2 Reglas de resonancia
1. En las estructuras resonantes el movimiento de electrones se realiza desde posiciones adyacentes. Solo constituye la distribucin de electrones, no hay cambios de posiciones de los tomos.
2. Los tomos que poseen su octeto completo, contribuyen ms al hbrido de resonancia que los que no tienen.
3. Las estructuras que presentan la mnima separacin de carga, sern las ms importantes.
4. Las estructuras ms importantes son aquellas en donde el tomo ms electronegativo tiene la carga negativa y la carga
positiva se encuentra en el tomo ms electropositivo.
Esquema 5.3 Reglas de resonancia
Resonancia
1. En las estructuras de resonancia se
mueven electrones No tomos
2. Las estructuras de resonancias del hbrido deben
tener el mismo nmero de electrones apareados
propeno
ion carboxilo
3. Las estructuras con ms enlaces contribuyen ms
a la resonancia que las que tienen menos enlaces
4. Las estructuras con carga negativa en el tomo ms
electronegativo (EN) contribuyen ms que las que tienen
carga negativa en el tomo menos EN
contribuye ms
contribuye menos
contribuye
menos
Grupo
carbonilo
contribuye
ms
60
Tema 5. Resonancia
contribuye
medianamente
Gua Temtica para el Curso de Qumica Orgnica I
Resonancia
Formacin resonante
Representacin combinada
(hbrido de resonancia)
Equilibrio
cido actico
Todos los tomos con octetos
completos, no hay separacin de
cargas (contribuyente mayor)
resonancia
in acetato
Carbono sin ncleo completo
separcin de cargas
(contribuyente menor)
Momento dipolar
5.3 Aplicacin de la teora de la resonancia
La molcula de ozono se representa por dos estructuras resonantes, en donde los oxgenos terminales son equivalentes debido
a la hibridacin de la molcula. La carga queda repartida entre los tomos externos (-1/2), y el ngulo que forman entre ellos
es de 116.8.
Francisco Cruz Sosa/Jorge Armando Haro Castellanos/Ignacio Lpez y Celis/Sergio Alatorre Santamara
61
Universidad Autnoma Metropolitana /Unidad Iztapalapa/Divisin de Ciencias Biolgicas y de la Salud
Esquema 5.4 Teora de la resonancia
Aplicacin de la teora de la resonancia
Explica la manera en que unen los tomos y como se distribuyen
los electrones como una respuesta teorica a datos experimentales
que la teora estructural no puede explicar por s misma.
Oxgeno (dos pares de electrones sin
compartir)
Carbono (No tiene
pares de electrones
sin compartir)
ozono
Nitrgeno (un par
de electrones sin
compartir)
nitrometano
estracturas resonantes o contribuyentes
hbrido de resonancia
estructuras resonantes o contribuyentes
hbrido de resonancia
5.4 El benceno y su resonancia
El benceno es un hidrocarburo aromtico con frmula molecular C6H6 y con una estructura hexagonal regular, en donde cada
vrtice est ocupado por un tomo de carbono con hibridacin sp2 y la sobreposicin de los orbitales atmicos p permite la
deslocalizacin de los electrones . La longitud del enlace carbono-carbono en el benceno es igual para todos los enlaces 139
pm (picmetros), contrastando con la longitud en un enlace simple carbono-carbono de 154 pm, y con la longitud en un enlace
carbono-carbono de un alqueno que es de 133 pm por lo tanto los enlaces en el benceno son de una longitud intermedia.
Esquema 5.5 Benceno y su resonancia
El benceno y su resonancia
Benceno C6 H6
Densidad electrnica del enlace pi del benceno
estructuras resonantes o contribuyentes
hbrido de resonancia
62
Tema 5. Resonancia
Gua Temtica para el Curso de Qumica Orgnica I
5.5 Estabilidad y energa de resonancia
La estabilidad del benceno se debe a la energa de resonancia que presenta por la deslocalizacin de los electrones en el
anillo, formando la densidad electrnica representada por un hbrido de resonancia. La energa de resonancia se define como
la diferencia de energa (calor liberado en la hidrogenacin) entre el 1,3,5-ciclohexatrieno (hipottico) y el benceno (real)
como se puede observar en el esquema 5.6.
Esquema 5.6 Estabilidad del benceno y energa de resonancia
Estabilidad del benceno y energa de resonancia
Estabilidad del benceno
KMnO4
OH
H 2O
OH
KMnO4
No hay
reaccin
HO
Energa de resonancia: La diferencia de energa (calor
liberado en la hidrogenacin) entre el 1,4-ciclohexadieno
y el 1,3-ciclohexadieno o entre el compuesto hipottico
(1,3,5-ciclohexatrieno) y el benceno.
compuesto
hipottico
Estabilidad del benceno
(solo se xida la cadena lateral)
CH 3
-36.0
COOH
-1.8
KMnO4
Energa
H2 O
CH 2 OH
COOH
-55.4 -85.8
-49.8
-28.6 -57. 2
K2 Cr 2O 7
H2SO4
calores de hidrogenacin Kcal/mol
Francisco Cruz Sosa/Jorge Armando Haro Castellanos/Ignacio Lpez y Celis/Sergio Alatorre Santamara
63
Universidad Autnoma Metropolitana /Unidad Iztapalapa/Divisin de Ciencias Biolgicas y de la Salud
5.6 Aromaticidad: coplanaridad, alternancia y regla de Hckel
La regla de Hckel define cuando una molcula es aromtica, si cumple con el criterio 4n+2. El valor de 4n+2 debe ser igual al
nmero de electrones deslocalizados, en donde n es siempre un nmero entero 0, 1, 2, 3, 4, etc.
Esquema 5.7 Aromaticidad
Aromaticidad
Regla de Hckel 4n + 2
Condiciones para la aromaticidad
1) El compuesto debe tener estructura cclica y dobles enlaces
+ electrones libres alternados
nmero de electrones en el ciclo
2) Todos los tomos de carbono del ciclo deben de tener
hibridacin sp2
0
1
2
3
4
etc.
4X0+2=2
4X1+2=6
4 X 2 + 2 = 10
4 X 3 + 2 = 14
4 X 4 + 2 = 18
3) Tener una estructura plana y casi plana para el solapamiento
de los orbitales p
4) Cumplir con la regla de Hckel: el nmero de electrones de
ciclo debe ser 4n + 2 siendo n = Nmero enero (0, 1, 2, 3, 4, etc.)
catin ciclopropenilo benceno
2 electrones
6 electrones
naftaleno
10 electrones
antraceno
14 electrones
[18] anuleno
18 electrones
5.7 Compuestos aromticos heterocclicos: pirrol, furano, piridina
Esquema 5.8 Compuestos aromticos heterocclicos
Compuestos aromticos heterocclicos
pirrol
furano
piridina
4 electrones + 2 electrones r
4 electrones + 2 electrones r
6 electrones
2 enlaces dobles = 4 electrones
2 enlaces dobles = 4 electrones
un par de
electrones
sin compartir
del nitrgeno
estructuras resonantes del pirrol
64
3 enlaces dobles = 6 electrones
sin compartir
del oxgeno
el par de electrones sin compartir
del nitrgeno no interviene para la
suma de los 6 electrones
estructuras resonantes del furano
estructuras resonantes de la piridina
un par de
electrones
Tema 5. Resonancia
Gua Temtica para el Curso de Qumica Orgnica I
El tomo de nitrgeno en el pirrol presenta una hibridacin sp3, y cuando aporta su par de electrones no enlazantes al anillo se
convierte en sp2, as como los tomos de carbono participan con cuatro electrones de los enlaces p para que la molcula cumpla
con la regla de Hckel.
De la misma forma que el nitrgeno en el pirrol, el tomo de oxgeno en el furano aporta un par de electrones al anillo para
darle el carcter aromtico a la molcula.
Tambin el tomo de azufre en el tiofeno aporta un par de electrones al anillo para formar el sexteto de electrones.
El tomo de nitrgeno en la piridina tiene una hibridacin sp2, pero debido a que ya est formando un enlace p en el anillo, no
aporta el par de electrones no enlazantes puesto que no se encuentran el plano del anillo aromtico.
Francisco Cruz Sosa/Jorge Armando Haro Castellanos/Ignacio Lpez y Celis/Sergio Alatorre Santamara
65
Universidad Autnoma Metropolitana /Unidad Iztapalapa/Divisin de Ciencias Biolgicas y de la Salud
5.8 Sustitucin electroflica en el benceno, mecanismos: nitracin, halogenacin, sulfonacin,
alquilacin y acilacin
En la sustitucin electroflica aromtica un electrfilo reacciona con un par de electrones p del anillo para formar un enlace s.
En algunas ocasiones se requiere de un cido de Lewis; al final existe la prdida de un tomo de hidrgeno en el anillo para
que la molcula recupere su aromaticidad. Cuando el electrfilo se une al anillo se forma un carbocatin (complejo sigma) que
es estabilizado por resonancia. Este tipo de reacciones son importantes en la sntesis de compuestos para la industria qumica.
Esquema 5.9 Sustitucin electroflica aromtica
Sustitucin electroflica aromtica en el benceno
Mecanismo General
E = electrfilo
etapa 1: adicin del electrfilo
complejo sigma estabilizado por resonancia
etapa 2: prdida del protn
carbocatin estabilizado
por deslocalizacin de la
carga positiva
66
producto sustituido
aromtico
Tema 5. Resonancia
Gua Temtica para el Curso de Qumica Orgnica I
5.8 Sustitucin electroflica en el benceno, mecanismos: nitracin
La nitracin del benceno se realiza con cido ntrico concentrado caliente, esta reaccin presenta algunos inconvenientes importantes a considerar, es lenta y el uso de cidos ntrico caliente puede causar una explosin. Existe un procedimiento ms
seguro, el uso de una mezcla de los cidos sulfrico y ntrico, en donde el cido sulfrico acta como un catalizador acelerando la
reaccin y permitiendo que la temperatura empleada en el proceso sea menor. El benceno reacciona con una mezcla sulfontrica
que genera iones nitronio (NO2+), los cuales se adicionan al benceno formando un complejo sigma, y luego pierde un protn
para dar el nitrobenceno.
El nitrobenceno se usa en la fabricacin de aceite lubricante para los motores y en la maquinaria industrial adems de manufactura de pesticidas, colorantes y medicamentos.
Esquema 5.10 Nitracin
Nitracin
Reaccin
Mecanismo de reaccin
nitrobenceno
benceno
benceno
complejo sigma
electrfilo
nitrobenceno
in nitronio
Francisco Cruz Sosa/Jorge Armando Haro Castellanos/Ignacio Lpez y Celis/Sergio Alatorre Santamara
67
Universidad Autnoma Metropolitana /Unidad Iztapalapa/Divisin de Ciencias Biolgicas y de la Salud
5.8 Sustitucin electroflica en el benceno, mecanismos: halogenacin
El benceno reacciona con los halgenos moleculares (Cl2, Br2, I2 y F2) en presencia de cidos de Lewis. Los ms usados son cloro
y bromo, ya que reaccionan de forma similar con el benceno. La reaccin con yodo es muy lenta y el manejo de la reaccin con
el flor es difcil. El bromo benceno es un lquido incoloro de olor caracterstico, se utiliza como solvente y aditivo de aceites de
motor.
El mecanismo de halogenacin se realiza en dos etapas: Etapa 1. El catalizador (cido de Lewis), interacciona con la molcula del halgeno, polarizando el enlace y as uno de los halgenos adquiere una carga positiva permitiendo ser atacado por el
benceno. Etapa 2. Recuperacin de la aromaticidad del anillo cuando este pierde un protn.
Esquema 5.11 Halogenacin
Halogenacin
Cloracin
Bromacin
clorobenceno
benceno
benceno
electrfilo
electrfilo
mecanismo de reaccin
benceno
complejo sigma
mecanismo de reaccin
benceno
complejo sigma
bromobenceno
clorobenceno
68
bromobenceno
Tema 5. Resonancia
Gua Temtica para el Curso de Qumica Orgnica I
5.8 Sustitucin electroflica en el benceno, mecanismos: sulfonacin
El benceno reacciona con trixido de azufre disuelto en cido sulfrico, la reaccin procede en dos etapas: Etapa 1. Reaccin del
benceno con el trixido de azufre Etapa 2. Recuperacin de la aromaticidad por prdida de un protn.
La sulfonacin del benceno es una reaccin reversible, en donde el grupo sulfnico (SO3H) posteriormente puede ser
removido por medio de una reaccin con cido sulfrico acuoso. Esta propiedad se puede emplear para proteger posiciones del
benceno con el grupo sulfnico (SO3H) en la sntesis de compuestos con mayor complejidad.
Esquema 5.12 Sulfonacin
Sulfonacin
Reaccin
benceno
cido bencensulfnico
Mecanismo de reaccin
benceno
complejo sigma
electrfilo
electrfilo
desulfonacin
cido
bencensulfnico
estructuras de resonancia del trixido de azufre
cido
bencensulfnico
calor
benceno
Francisco Cruz Sosa/Jorge Armando Haro Castellanos/Ignacio Lpez y Celis/Sergio Alatorre Santamara
69
Universidad Autnoma Metropolitana /Unidad Iztapalapa/Divisin de Ciencias Biolgicas y de la Salud
5.8 Sustitucin electroflica en el benceno, mecanismos: alquilacin
En la alquilacin de Friedel-Crafts un tomo de hidrgeno del anillo aromtico es sustituido por un alquilo. La reaccin procede
cuando el halogenuro de alquilo primario y el cido de Lewis forman un aducto (R-X-AlX3) generndose la formacin de una carga parcial positiva (+) sobre el carbono que se encuentra unido al halgeno lo cual le proporciona un carcter electroflico. Los
halogenuros de alquilo secundarios y terciarios reaccionan con AlX3 para formar carbocationes y el anin AlX4-. Los catalizadores
comnmente utilizados son haluros de aluminio (AlX3) o de hierro (FeX3).
Cloruro de metilo. Formacin de aducto
En la alquilacin de Friedel-Crafts del benceno hay polisustitucin de grupos alquilo al anillo, debido a que el grupo entrante lo
vuelve ms nuclefilo.
Esquema 5.13 Alquilacin
Alquilacin
Reaccin
Mecanismo de reaccin
benceno
benceno
complejo sigma
electrfilo
carbocatin
alquilbenceno
70
Tema 5. Resonancia
Gua Temtica para el Curso de Qumica Orgnica I
La transposicin de un carbocatin primario a uno secundario o terciario, debido a la estabilidad de los mismos, puede dar como
resultado productos no deseados.
Esquema 5.14 Alquilacin con y sin transposicin
Alquilacin
Alquilacin sin rearreglo
benceno
Alquilacin con rearreglo
etilbenceno
electrfilo
propilbenceno
benceno
carbocatin primario
mecanismo
isopropilbenceno
electrfilo
carbocatin primario
benceno
complejo sigma
carbocatin secundario
etilbenceno
benceno
rearreglo
propilbenceno
El rendimiento
depende de la
temperatura de
reaccin
benceno
isopropilbenceno
Francisco Cruz Sosa/Jorge Armando Haro Castellanos/Ignacio Lpez y Celis/Sergio Alatorre Santamara
71
Universidad Autnoma Metropolitana /Unidad Iztapalapa/Divisin de Ciencias Biolgicas y de la Salud
5.8 Sustitucin electroflica en el benceno, mecanismos: acilacin
En la acilacin de Friedel-Crafts del benceno un tomo de hidrgeno es sustituido por un grupo acilo. El mecanismo de la reaccin procede en varias etapas:
Etapa 1.- Reaccin del cloruro de acilo y el cido de Lewis como catalizador para la preparacin del catin acilonio.
Etapa 2.- Reaccin del benceno con el catin generado y formacin del complejo s.
Etapa 3.- Recuperacin de la aromaticidad por prdida de un protn para la obtencin de una cetona.
Esquema 5.15 Acilacin
Acilacin
Reaccin
Mecanismo de reaccin
benceno
benceno
cetona
complejo sigma
electrfilo
catin acilo
sntesis de la acetofenona
resonancia del ion acilo
benceno
72
complejo sigma
acetofenona
Tema 5. Resonancia
Gua Temtica para el Curso de Qumica Orgnica I
5.9 Efecto de los sustituyentes sobre la sustitucin electroflica en el benceno
Cuando el benceno reacciona con una mezcla sulfontrica da como producto el nitrobenceno, este sustituyente ser el que determine donde suceder el ataque de otro sustituyente como en el caso de la nitracin del mismo compuesto, obtenindose tres
productos en proporciones diferente, el meta-dinitrobenceno (93%), orto-dinitrobenceno (6%) y para-dinitrobenceno (0.7%).
Esquema 5.16 Nitracin del benceno y del tolueno
Efecto de los sustiuyentes en la SEA (Sustitucin electroflica aromtica)
Nitracin del benceno
Nitracin del tolueno
nitrobenceno
(un producto)
orto-nitrotolueno
para-nitrotolueno meta-nitrotolueno
38%
58%
4%
Esquema 5.17 Nitracin del benceno y del nitrotolueno
Efecto de los sustiuyentes en la SEA
Nitracin del benceno
nitrobenceno
(un producto)
Nitracin del nitrobenceno
meta-nitrotolueno
93%
orto-nitrotolueno para-nitrotolueno
6%
0.7%
Francisco Cruz Sosa/Jorge Armando Haro Castellanos/Ignacio Lpez y Celis/Sergio Alatorre Santamara
73
Universidad Autnoma Metropolitana /Unidad Iztapalapa/Divisin de Ciencias Biolgicas y de la Salud
Esquema 5.18 Grupos activantes y grupos desactivantes
Efecto de los sustiuyentes en la SEA
grupos activantes orto y para
grupos desactivantes orientadores meta
Activantes fuertes
Grupo nitro
Anilinas
Fenxidos
Fenoles
Nitrobenceno
Activantes moderados
Anilidas
Grupo ciano
cido
bencensulfnico
Benzonitrilo
Grupo carbonilo
teres
Activantes dbiles
Grupo sulfnico
solfnico
Benzaldehdo
Grupo carboxilo
Acetofenona
Grupo ster
Sal de amonio 4
Alquilbencenos
Efectos de los sustituyentes en las sustitucin electrofilica aromtica
Sustituyente
reactividad
orientacin
efecto inductivo
efecto de resonancia
-OH
-NH2
activante
orto, para
debil
atrayente de
electrones
fuerte
donante de
electrones
-CH3
activante
orto, para
debil
donante de
electrones
ninguno
-F, -Cl
-Br, -l
desactivante
orto, para
fuerte
atrayente de
electrones
debil
donante de
electrones
-CHO, -COOCH3
desactivante
meta
fuerte
atrayente de
electrones
fuerte
atrayente de electrones
-N(CH3)3
desactivante
meta
fuerte
atrayente de
electrones
ninguno
-NO2 -C N
-COCH3 -COOH
74
Tema 5. Resonancia
Gua Temtica para el Curso de Qumica Orgnica I
Un grupo activante es una especie qumica que le confiere al anillo aromtico la capacidad de realizar la sustitucin electroflica aromtica (SEA) con una velocidad de reaccin mayor o bin realizar la reaccin en menor tiempo. La razn es que este
grupo activante tiene la propiedad de estabilizar a un carbocatin de un sistema aromtico por medio de un efecto inductivo o
por resonancia. La activacin por efecto inductivo, es una caracterstica de los grupos alquilo, pero son clasificados como dbiles,
un ejemplo es el tolueno.
La activacin por efecto de resonancia se presenta cuando los sustituyentes tienen electrones no compartidos y los pueden
ceder al anillo, como se puede observar en la resonancia que presenta la anilina.
Un grupo desactivante es una especie qumica que disminuye la reactividad y la velocidad de reaccin del sistema aromtico,
debido a la sustraccin de electrones del anillo por parte del sustituyente como en el caso del cido benzoico.
Francisco Cruz Sosa/Jorge Armando Haro Castellanos/Ignacio Lpez y Celis/Sergio Alatorre Santamara
75
Universidad Autnoma Metropolitana /Unidad Iztapalapa/Divisin de Ciencias Biolgicas y de la Salud
Los halgenos contienen electrones no enlazantes que pueden aportar al anillo, pero debido a su electronegatividad, pueden
atraer a la nube de electrones , por lo tanto son desactivantes dbiles, sin embargo orientan a orto y para la entrada de un
electrfilo.
Esquema 5.19 Halgenos
Halgenos: desactivantes y orientadores o y p
Halgenos: efectos inductivo negativo (atrae electrones)
desactiva el ciclo aromtico, por lo que en el efecto
inductivo predomina la reactividad
Enlace carbono - halgeno
polarizado con el extremo positivo
en el tomo de carbono y el
extremo negativo en el tomo de
halgeno
Halgenos: resonancia (introduce electrones)
el efecto de la resonancia predomina en
la orientacin. El ataque en orto y para da
estructuras resonantes ms estables que en meta
Ataque
oro
Ataque
meta
Ataque
para
76
Tema 5. Resonancia
Gua Temtica para el Curso de Qumica Orgnica I
Tema 6
Alcoholes
6.1 Estructura
6.2 Propiedades fsicas
6.3 Alcohol etlico: importancia qumica y fisiolgica
6.4 Obtencin de alcoholes
6.5 Alcoholes como cidos y bases
6.6 Reacciones de sustitucin y de eliminacin en los alcoholes
6.7 Oxidacin de alcoholes
6.8 Polioles. Glicerol. Accin del peryodato sobre los vic-dioles (diol vecinal)
6.1 Estructura
Esquema 6.1 Alcoholes
Alcoholes
Metilo
Secundarios
Terciarios
metanol
alcohol metlico
Primarios
etanol
alcohol etlico
propan-1-ol
1-propanol
alcohol n-proplico
propan-2-ol
2-propanol
alcohol isoproplico
2-metilpropan-2-ol
2-metil-2-propanol
alcohol tert-butlico
butan-2-ol
2-butanol
alcohol sec-butlico
Francisco Cruz Sosa/Jorge Armando Haro Castellanos/Ignacio Lpez y Celis/Sergio Alatorre Santamara
77
Universidad Autnoma Metropolitana /Unidad Iztapalapa/Divisin de Ciencias Biolgicas y de la Salud
ngulos de enlace del agua, metanol y ter dimetlico, en donde se observa la influencia de los sustituyentes: En el metanol el
ngulo del enlace C-O-H es de 108.9, mayor al ngulo conformado por los tomos de hidrgeno en el agua que es de 104.5,
esto se debe que en el metanol el grupo metilo es ms voluminoso que el hidrgeno.
Asociacin por enlace de hidrgeno
6.2 Propiedades fsicas
Solubilidad
Los alcoholes pueden ser lquidos o slidos dependiendo de su peso molecular, debido a la presencia del grupo hidroxilo y a su
polaridad pueden formar puentes de hidrgeno con el agua facilitado su solubilidad. Cuando los alcoholes tienen peso molecular elevado, estos sern solubles en solventes no polares (benceno, tolueno, xileno, ciclohexano, etc.).
Punto de Ebullicin
Los alcoholes presentan puntos de ebullicin ms elevados que los alcanos con peso molecular similar, esto se debe a que los
alcoholes pueden formar puentes de hidrgeno entre s, requirindose mayor cantidad de energa para romperlos. Mientras
mayor sea la cadena el punto de ebullicin se va elevando y disminuye cuando estos presentan ramificaciones, esto se debe a la
presencia de las fuerzas de Van der Waals.
Esquema 6.2 Propiedades fsicas
Propiedades fsicas
Solubilidad
Enlaces
Solubles en agua
polarizados
grupo
hidrofbico
Punto de ebullicin
Compuestos con PM similares
grupo
hidroflico
Puente de hidrgeno
Alcano
(propano)
gas
Poco solubres en agua
ter
(ter dimetlico)
Alcohol
(etanol)
Insolubres en agua
78
Tema 6. Alcoholes
gas
lquido
Gua Temtica para el Curso de Qumica Orgnica I
6.3 Alcohol etlico: importancia qumica y fisiolgica
El alcohol etlico reacciona fcilmente con cidos carboxlicos para obtener steres, que son utilizados como aditivos en jugos,
refrescos, jarabes, perfumes, aromatizantes ambientales y en bebidas alcohlicas. El alcohol etlico es utilizado como un aditivo
en la gasolina. En la industria qumica se utiliza para la sntesis del acetato de etilo que sirve como disolvente para pegamentos
y pinturas.
Acetato de etilo
Los efectos del alcohol etlico en la fisiologa humana, han demostrado que el abuso en el consumo de este producto es txico
para los tejidos del organismo. Algunas de las enfermedades ms frecuentes son la cirrosis heptica, cncer de hgado y la afectacin del sistema nervioso central, entre otras.
Esquema 6.3 Etanol
Etanol
Importancia fisiolgica
Importancia qumica
Sntesis
Bebida alcohlica
steres
(acetato de etilo)
enzimas de
glucosa
teres
(ter dietlico)
Mecanismo de accin (efecto bifsico)
1. Etapa de euforia: relajacin y alegra
Combustible
chispa
Aplicaciones:
Disolvente, desinfectante, anticongelante
Excipiente en:
Medicamentos, cosmticos, perfumes
levaduras
Tasa de alcoholemia permitida: lmite mximo
energa
0.8 g/L en sangre 0.4 g/mL de aire espirado
Equivalente de 2 a 5 copas por hora
2. Etapa de emocin: confusin y problemas de coordinacin
Tasa de alcoholemia no permitida
mayor a 0.9 g/L en sangre .5 g/mL de aire espirado
Equivalente de 4 a 7 copas por hora
Francisco Cruz Sosa/Jorge Armando Haro Castellanos/Ignacio Lpez y Celis/Sergio Alatorre Santamara
79
Universidad Autnoma Metropolitana /Unidad Iztapalapa/Divisin de Ciencias Biolgicas y de la Salud
6.4 Obtencin de alcoholes
Hidratacin de alquenos
Los alquenos realizan reacciones de adicin electroflica (AE), en donde los electrones actan como base atrapando protones,
permitiendo as la formacin de carbocationes siguiendo la regla de Markovnikov. Los alquenos reaccionan con el agua en presencia de cido sulfrico (H2SO4 al 50%) que acta como catalizador, obtenindose como producto alcoholes.
Los halogenuros de alquilo se comportan como electrfilos por la presencia del halgeno unido a un carbono (C-X) haciendo a ste, un enlace polar. Las reacciones de halogenuro de alquilo con hidrxido proceden mediante el mecanismo de
sustitucin nucleoflica (SN) de primer orden SN1 o de segundo orden SN2.
Esquema 6.4 Obtencin de alcoholes: hidratacin y reaccin SN
Obtencin de alcoholes
A partir de Halogenuros de alquilo
Hidratacin de alquenos
Reaccin de sustitucin nucleoflica (SN)
Reaccin de adicin electrfilica
Reaccin SN2: R-X Me, 1 y 2
Adicin Markovnikov
Reaccin SN1: R-X, 3 y 2
propeno
80
propan-2-ol
2-propanol
alcohol isoproplico
2-cloro-2-metipropano
cloruro de tert-butilo
Tema 6. Alcoholes
2-metilpropan-2-ol
2-metil-2-propanol
alcohol tert-butlico
Gua Temtica para el Curso de Qumica Orgnica I
Reduccin de Aldehdos y Cetonas
Los aldehdos y cetonas se reducen con NaBH4 (borohidruro de sodio) o LiAlH4 (hidruro de litio y aluminio) transformndose
en alcoholes primarios y secundarios debido a la presencia del grupo carbonilo. El NaBH4 es un agente reductor suave, mientras
que el LiAlH4 es muy fuerte.
etanol
acetaldehdo
1) LiAIH4 , ter dietlico
2) H , H2O
ciclohexanol
ciclohexanona
Reaccin de aldehdos y cetonas con el reactivo de Grignard
El reactivo de Grignard es un compuesto organometlico con frmula molecular R-MgX, en donde R es un grupo alquilo y X un
halgeno, la presencia del carbono del grupo alquilo frente al magnesio le da una caracterstica de reaccionar rpidamente con
electrfilos.
1)
ter dietlico
2)
MgBr
ter
Francisco Cruz Sosa/Jorge Armando Haro Castellanos/Ignacio Lpez y Celis/Sergio Alatorre Santamara
81
Universidad Autnoma Metropolitana /Unidad Iztapalapa/Divisin de Ciencias Biolgicas y de la Salud
Esquema 6.6 Obtencin de alcoholes: reduccin y reactivo de Grignard
Obtencin de alcoholes
Adicin del reactivo de Grignard
Reduccin de compuestos carbonilcos
Reduccin de aldehdos: Alcoholes primarios
Reduccin de cetonas: Alcoholes secundarios
Adicin a formaldehdo: Alcohol primario
ter
Reduccin de cidos carboxilicos:
Alcoholes primarios
Adicin a aldehdos: Alcoholes secundarios
ter
Adicin a cetonas: Alcoholes terciarios
ter
ter dietlico
propan-2-ol
etanal
butanona
butanal
etanol
2-butanol
etanol
1-butanol
ter dietlico
ciclopentilmetanol
ciclopentilmetanal
ter dietlico
ciclohexanona
82
ciclohexanol
Tema 6. Alcoholes
Gua Temtica para el Curso de Qumica Orgnica I
6.5 Alcoholes como cidos y bases
Los alcoholes pueden comportarse como cidos o bases, debido al dipolo que forma el grupo hidroxilo. Al reaccionar con una
base fuerte como NaH (hidruro de sodio) se forma un grupo alcoxi, debido a que el alcohol pierde su protn formndose alcxido de sodio y desprendindose hidrgeno molecular. Los alcoholes se comportan como bases, debido a la presencia de los
electrones no enlazantes del oxgeno, captando protones de cidos fuertes como el H2SO4 (cido sulfrico). Los alcoholes terciarios, son menos cidos que los secundarios y que los primarios, debido al impedimento estrico producido por sus sustituyentes
que impiden la substraccin del in hidrgeno de manera efectiva.
La acidez de un alcohol se puede establecer cualitativamente
observando la estabilidad del ion alcxido correspondiente
CH3OH > primario > secundario > terciario
Ms cido
Acidez creciente
Menos cido
CH3O > primario > secundario > terciario
Ms estable
Estabilidad creciente
Menos estable
Esquema 6.7 Alcoholes como cidos y bases
Obtencin de alcoholes
Basicidad en alcoholes
Acidez en alcoholes
alcohol protonado
Deshidratacin del etanol
Base fuerte
Base
Etanol
alcohol etlico
Etanol
alcohol etlico
etxido de sodio
Etanol
protonado
eteno
2-metilpropan-2-ol
2-metil-2-propanol
alcohol tert-butlico
tert-butxido de potasio
Francisco Cruz Sosa/Jorge Armando Haro Castellanos/Ignacio Lpez y Celis/Sergio Alatorre Santamara
83
Universidad Autnoma Metropolitana /Unidad Iztapalapa/Divisin de Ciencias Biolgicas y de la Salud
6.6 Reacciones de sustitucin en los alcoholes
Los alcoholes reaccionan con HCl o con HBr para dar como productos halogenuros de alquilo y agua. Los alcoholes primarios
y secundarios reaccionan con HCl en presencia de ZnCl2 y calentamiento, los alcoholes terciarios como el alcohol tert-butlico
reacciona rpidamente sin calentar.
El orden de reactividad de los alcoholes es: 3 > 2 > 1
Esquema 6.8 Reacciones de sustitucin. Con HBr
Reacciones de sustitucin
84
Reacciones de sustitucin nucleoflica S N1
Reacciones de sustitucin nucleoflica SN 2
Reacciones con HBr
Reacciones con HBr
Alcoholes 3 y 2 mecanismo SN1
Alcoholes 1 mecanismo SN2
Tema 6. Alcoholes
Gua Temtica para el Curso de Qumica Orgnica I
6.6 Reacciones de sustitucin en los alcoholes
Los alcoholes pueden identificarse mediante el reactivo de Lucas, este consiste en una disolucin de ZnCl2 en HCl concentrado.
El reactivo de Lucas reacciona con alcoholes primarios, secundarios y terciarios a diferentes velocidades de reaccin para formar
sus respectivos cloruros de alquilo.
Alcoholes primarios: no presentan turbidez (mecanismo SN2)
Alcoholes secundarios: aparicin de la turbidez entre 3 a 5 minutos (mecanismo SN1)
Alcoholes terciarios: aparicin de turbidez inmediata (mecanismo SN1)
Esquema 6.9 Reacciones de sustitucin: reactivo de Lucas
Reacciones de sustitucin
Reacciones de sustitucin nucleoflica S N1
Reacciones con HCl/ZnCl2 (Reactivo de Lucas)
Alcoholes 3 y 2 mecanismo SN1
Reacciones de sustitucin nucleoflica S N2
Reacciones con HCl/ZnCl2 (Reactivo de Lucas)
Alcoholes 1 mecanismo SN2
Francisco Cruz Sosa/Jorge Armando Haro Castellanos/Ignacio Lpez y Celis/Sergio Alatorre Santamara
85
Universidad Autnoma Metropolitana /Unidad Iztapalapa/Divisin de Ciencias Biolgicas y de la Salud
6.6 Reacciones de eliminacin en los alcoholes
Esquema 6.10 Reacciones de eliminacin
Reacciones de eliminacin
Reaccin general
Reacciones de Eliminacin (E1)
Sin rearreglo
Reacciones de Eliminacin (E1)
con rearreglo
but-1-eno
1-buteno
but-2-eno
2-buteno
Mecanismo de reaccin
Mecanismo de reaccin
ciclohexanol
Producto secundario
alqueno monosustituido
rearreglo
carbocatin 1
carbocatin 2
ciclohexeno
Producto principal
alqueno disustituido
carbocatin 2
pero nada de
3,3-Dimetil-2-butanol
Alcohol neopentlico
2-Cloro-2,3-dimetibutano
2-Cloro-2-metibutano
Cuando hay transposicin del grupo alquilo
86
Tema 6. Alcoholes
Gua Temtica para el Curso de Qumica Orgnica I
6.6 Reacciones de eliminacin en los alcoholes. Regla de Saytzeff
Los alcoholes secundarios y terciarios reaccionan con facilidad con cido sulfrico para formar iones alquil-oxonio, los cuales al perder
agua producen carbocationes estables, capaces de atraer electrones y formar dobles enlaces con la consiguiente prdida de protn.
Esquema 6.11 Reacciones de eliminacin
Reacciones de eliminacin
Regla de Saytzeff
En la deshidratacin, en cuanto ms estable sea
un alqueno, ms rpido se formar
Facilidad de formacin de alquenos
Estabilidad de alquenos
calor
butan-2-ol
2-butanol
1-metilciclohexanol
but-1-eno
1-buteno
compuesto minoritario
alqueno monosustituido
but-2-eno
2-buteno
compuesto mayoritario
alqueno disustituido
metilenciclohexano
compuesto minoritario
alqueno disustituido
1-metilciclohexeno
compuesto mayoritario
alqueno trisustituido
calor
Francisco Cruz Sosa/Jorge Armando Haro Castellanos/Ignacio Lpez y Celis/Sergio Alatorre Santamara
87
Universidad Autnoma Metropolitana /Unidad Iztapalapa/Divisin de Ciencias Biolgicas y de la Salud
Reacciones
1. Desidratacin de Alcoholes
ion alquil-oxnio
minoritario
mayoritario
6.7 Oxidacin de alcoholes
Alcoholes primarios
Se oxidan de manera selectiva a aldehdos (R-CHO), en presencia de clorocromato de piridinio (PCC) o el dicromato de piridinio
(PDC). Para obtener cidos carboxlicos a partir de alcoholes primarios, los aldehdos obtenidos debern reaccionar con agua
para formar hidratos de aldehdo [R-CH(OH)2] y despus continuar con la oxidacin a cidos carboxlicos. Los alcoholes primarios pueden oxidarse directamente a cidos carboxlicos utilizando permanganato de potasio (KMnO4) o dicromato de potasio
K2Cr2O7.
Aldehdo
Alcohol
primario
Hidrato de
aldehdo
Alcoholes secundarios
Se pueden oxidar para la obtencin de cetonas, el reactivo ms comn es el cido crmico H2CrO4.
1-Feniletanol
1-feniletanona l
88
Feniletanona
Acetofenona
Fenilmetilcetona
(72%)
Tema 6. Alcoholes
cido
carboxilico
Gua Temtica para el Curso de Qumica Orgnica I
Los alcoholes terciarios.
Estos generalmente no sufren oxidacin.
Esquema 6.12 Reacciones de oxidacin
Oxidacin de alcoholes
Oxidacin de alcoholes 1
a aldehdos
Oxidacin de alcoholes 2
a cetonas
Oxidacin de alcoholes 1
a cidos carboxilicos
etanol
alcohol etlico
etanol
alcohol etlico
piridina
ciclohexanol
etanal
acetaldehdo
ciclohexanona
cido etanoico
cido actico
Oxidacin de los Alcoholes
Los alcoholes primarios pueden tambin oxidarse a aldehdos con K2Cr2O7, los cuales deben ser separados
rpidamente de la reaccin para que no sigan oxidndose hasta cidos carboxlicos.
Aldehido
cido
carboxlico
Cetona
No hay reaccin
o
Francisco Cruz Sosa/Jorge Armando Haro Castellanos/Ignacio Lpez y Celis/Sergio Alatorre Santamara
89
Universidad Autnoma Metropolitana /Unidad Iztapalapa/Divisin de Ciencias Biolgicas y de la Salud
6.8 Polioles. Glicerol. Accin del peryodato sobre los vic-dioles
Esquema 6.12 Polioles
Polioles
Dioles
Trioles
etano-1,2-diol
1,2-etanodiol
etilenglicol
propano-1,2,3-triol
1,2,3-propanotriol
glicerol
hexano-2,4-diol
Accin del peryodato sobre los vic-dioles
vic-diol: es un diol con dos grupos hidroxilo en posiciones vecinales, es
decir, unidos a tomos de carbono adyacentes. Ejemplo: etilenglicol
ruptura ruptura
cetona
2,4-dimetilhexano-2,3,4,5-tetraol
acetona
cido
carboxlico
cido
frmico
aldehdo
cido
acetaldehdo
actico
Por cada ruptura C-C se forma un nuevo elace C-O para cada carbono.
90
Tema 6. Alcoholes
Gua Temtica para el Curso de Qumica Orgnica I
Tema 7
Haluros de Alquilo y Arilo
7.1 Estructura y nomenclatura
7.2 Obtencin
7.3 Reacciones de sustitucin nucleoflica y reacciones de eliminacin en los haluros de alquilo
7.4 Importancia de los haluros de alquilo en la sntesis de compuestos orgnicos
7.5 Obtencin de compuestos rgano metlicos. Reactivos de Grignard y reactivos de litio
7.6 Uso de compuestos de Grignard en sntesis orgnica
7.7 Estabilidad de los haluros de alquilo, toxicidad
Tefln (politetrafluoroetileno)
7.1 Estructura y nomenclatura
Los haluros de alquilo tienen la formula general (R-X) en donde R representa un grupo alquilo y X un halgeno (F, Cl, Br, I),
la diferencia entre la electronegatividad de los tomos proporciona la polaridad al enlace carbonohalgeno. Los haluros de
alquilo se clasifican en primarios, secundarios y terciarios segn el nmero de tomos de carbono unidos al carbono enlazado
al halgeno.
Primario
(1)
Secundario
(2)
Terciario
(3)
Francisco Cruz Sosa/Jorge Armando Haro Castellanos/Ignacio Lpez y Celis/Sergio Alatorre Santamara
91
Universidad Autnoma Metropolitana /Unidad Iztapalapa/Divisin de Ciencias Biolgicas y de la Salud
Esquema 7.1 Haluros de alquilo y de arilo
Haluros de alquilo y de arilo
Haluros de Alquilo
Haluros de Arilo
donde
donde
Monohalogenados
clorometano
cloruro de metilo
Monohalogenados
bromoetano
bromuro de etilo
Dihalogenados
diclorometano
cloruro de metileno
fluorobenceno clorobenceno
bromobenceno
Dihalogenados
1,2-dibromoetano
Trihalogenados
triclorometano
cloroformo
o-diclorobenceno
m-dibromobenceno
p-diiodobenceno
2,2,3-tribromobutano
Trihalogenados
tetrahalogenados
tetraclorometano
tetracloruro de carbono
Ciclicos
1,2,4-triclorobenceno
clorociclohexano
92
1,2-diclorociclohexano
Tema 7. Haluros de Alquilo y Arilo
1,3,5-tribromobenceno
Gua Temtica para el Curso de Qumica Orgnica I
7.2 Obtencin
Esquema 7.2 Obtencin de haluros de alquilo y de arilo
Obtencin
Haluros de alquilo
Haluros de arilo
a partir de alcanos
a partir de benceno
cloracin del benceno
donde
a partir de alquenos
bromacin del benceno
donde
a partir de alcoholes terciarios
yodacin del benceno
donde
a partir de alcoholes secundarios y primarios
a partir de anilina
otro reactivo para clorar:
otro reactivo para bromar:
anilina
sal de diazonio
Francisco Cruz Sosa/Jorge Armando Haro Castellanos/Ignacio Lpez y Celis/Sergio Alatorre Santamara
93
Universidad Autnoma Metropolitana /Unidad Iztapalapa/Divisin de Ciencias Biolgicas y de la Salud
Los haluros de alquilo pueden obtenerse por halogenacin de alcanos va el mecanismo de formacin de radicales, que
puede involucrar la obtencin de una mezcla de haluros debido a la inestabilidad de los radicales alquilo formados.
terciario > secundario > primario > metilo
luz
45%
55%
Los haluros de alquilo tambin pueden obtenerse por medio de la reaccin de un alqueno en presencia de cido clorhdrico
o cido bromhdrico.
Los alquenos reaccionan con cloro y bromo para formar 1,2- dihaloalcanos, con halgenos vecinales.
Los cloruros de alquilo se pueden obtener a partir de alcoholes primarios y secundarios utilizando cloruro de tionilo (SOCl2)
en presencia de piridina.
Los cloruros de alquilo se pueden obtener mediante la reaccin de alcoholes en presencia de cido clorhdrico. Este procedimiento se emplea principalmente con alcoholes terciarios, ya que estos forman carbocationes estables y reaccionan instantneamente. Se les adiciona ZnCl2 a los alcoholes secundarios y primarios para que reaccionen con una velocidad adecuada.
94
Tema 7. Haluros de Alquilo y Arilo
Gua Temtica para el Curso de Qumica Orgnica I
7.2 Obtencin. Adicin Markovnikov y antiMarkovnikov (Karash-Mayo)
Esquema 7.3 Adicin de haluros de hidrgeno a alquenos
Adicin de haluros de hidrgeno a alquenos
Adicin Markovnikov
Adicin anti Markovnikov (karash-Mayo)
mecanismo inico
mecanismo por radicales libres
1. formacin de carbocationes
1. iniciacin: radicales libres del perxido
carbocatin secundario
2. propagacin: radical libre reacciona con HX
radical libre reacciona con el alqueno
carbocatin primario
2. adicin del ion X
radical libre reacciona con HX
carbocatin secundario
producto mayoritario
carbocatin primario
producto minoritario
3. terminacin
orientacin tipo Markovnikov
2-cloro-propano
cloruro de isopropilo
orientacin tipo anti Markovnikov
producto mayoritario
1-bromopropano
Francisco Cruz Sosa/Jorge Armando Haro Castellanos/Ignacio Lpez y Celis/Sergio Alatorre Santamara
95
Universidad Autnoma Metropolitana /Unidad Iztapalapa/Divisin de Ciencias Biolgicas y de la Salud
7.3 Reacciones de sustitucin nucleoflica y reacciones de eliminacin en los haluros de alquilo
Reacciones de Sustitucin Nucleoflica en haluros de alquilo primario
Los haluros de alquilo primarios reaccionan con nuclefilos mediante el mecanismo de sustitucin nucleoflica bimolecular (SN2),
la reaccin se caracteriza por la formacin de un estado de transicin y no hay formacin de carbocationes. En la reaccin del
bromuro de etilo con una base fuerte, el in bromuro saliente es desplazado por el nuclefilo, el cual aporta un par de electrones para formar un nuevo enlace y el in bromuro se lleva el par de electrones del enlace s. Este tipo de ruptura es llamada
heteroltica.
Reaccin de sustitucin nucleoflica en haluros de alquilo secundario y terciario
Los halogenuros de alquilo secundarios y terciarios reaccionan con nuclefilos mediante el mecanismo de sustitucin nucleoflica
unimolecular (SN1), la reaccin involucra la formacin de un carbocatin promovido al aplicar calor a la reaccin. En la reaccin
del bromuro de tert-butilo se ioniza en presencia del nuclefilo.
La reaccin SN1 tiene lugar en tres etapas:
Etapa 1. Formacin de un carbocatin tert- butilo al salir el halgeno (anin bromuro). Esta etapa es lenta.
Etapa 2. La etapa 2 es rpida, se realiza por el ataque del nuclefilo al carbocatin.
Etapa 3. Es la eliminacin de un protn sustraido por el agua que actua como base, obtenindose un alcohol y un ion oxonio.
96
Tema 7. Haluros de Alquilo y Arilo
Gua Temtica para el Curso de Qumica Orgnica I
Reaccin de Eliminacin E1
La eliminacin unimolecular o E1 se realiza en los haluros de alquilo secundarios y terciarios, esta reaccin se efecta en dos
etapas.
Etapa 1. Formacin de un carbocatin, promovido por la salida del haluro.
Etapa 2. Prdida de un protn sustrado por una base y formacin de un enlace .
Reaccin de Eliminacin E2
La eliminacin bimolecular o E2 es un mecanismo concertado, en donde un protn es sustrado por una base fuerte y de manera
simultnea se efecta la salida del grupo saliente, dando lugar a la formacin de un enlace .
Estereoqumica de la eliminacin E 2
geometra antiperiplanar, hidrgeno y halgeno estn en lados opuestos de la molcula
estado de transicin
Francisco Cruz Sosa/Jorge Armando Haro Castellanos/Ignacio Lpez y Celis/Sergio Alatorre Santamara
97
Universidad Autnoma Metropolitana /Unidad Iztapalapa/Divisin de Ciencias Biolgicas y de la Salud
Esquema 7.4 Reacciones de sustitucin nucleoflica (SN) y eliminacin (E)
Reacciones de Sustitucin Nucleoflica y Eliminacin
Reacciones de Sustitucin Nucleofilica
Reacciones de Eliminacin
Base
sustitucin nucleofilica sin rearreglo
eliminacin sin isomera geomtrica
base
fuerte
base
fuerte
regla se Saytzeff: obencin del alqueno ms sustituido
sustitucin nucleofilica con rearreglo
base
fuerte
carbocatin primario
base
fuerte
2-clorobutano
cloruro de sec-butilo
eliminacin con isomera geomtrica
base
fuerte
o
+ H-base
base
dbil
carbocatin secundario
alcohol primario
alcohol secundario
producto mayoritario
cis
98
but-2-eno
1-buteno
producto mayoritario
Tema 7. Haluros de Alquilo y Arilo
trans
Gua Temtica para el Curso de Qumica Orgnica I
7.4 Importancia de los haluros de alquilo en la sntesis de compuestos orgnicos
La caracterstica principal de los haluros de alquilo es el halgeno, que es el que determina las propiedades de la molcula y
a ste se le llama grupo funcional. En los haluros de alquilo el halgeno est unido a un tomo de carbono, y de acuerdo a la
diferencia de electronegatividad entre estos dos tomos la molcula es polar, y es el carbono en donde se efectan las reacciones
con los diferentes nuclefilos, dando como producto una gran variedad de compuestos de importancia comercial.
Esquema 7.5 Reacciones de sustitucin nucleoflica (SN)
Haluros de alquilo en la sntesis orgnica
Producto
Nuclefilo
alcoholes
alcoholes
teres
alquinos
yoduros de alquilo
nitrilos
steres
amina primaria
amina secudnaria
amina terciaria
Alcohol bencilico
Francisco Cruz Sosa/Jorge Armando Haro Castellanos/Ignacio Lpez y Celis/Sergio Alatorre Santamara
99
Universidad Autnoma Metropolitana /Unidad Iztapalapa/Divisin de Ciencias Biolgicas y de la Salud
7.5 Obtencin de compuestos rgano metlicos. Reactivos de Grignard y reactivos de litio
El reactivo de Grignard se prepara por medio de la reaccin entre magnesio metlico y un halogenuro de alquilo y tiene la
frmula R-Mg-X. El halgeno puede ser (Cl, Br o I) y el halogenuro de alquilo empleado puede ser 1, 2, 3 o arilo (fenilo).
ter anhidro
Reactivo
de Grignard
Esquema 7.6 Reactivo de Grignard y reactivos de litio
Obtencin de compuestos rgano metlico
Reactivo de alquil litio
Reactivo de Grignard
ter o
haluro
de alquilo, donde
THF
haluro
de alquilo, donde
haluro de
alquilo magnesio
Algunas reacciones del reactivo de alquil litio
Algunas reacciones del reactivo de Grignard
alcano
alcano
alcano
alcano
dialquil
cuprato
de litio
+ alcano
cido carboxilicos
grupo carbonilo
alcano
alcoholes
ter Anhidro
Cloruro de etilo
Cloruro de etil magnesio
(Reactivo de Grignard)
ter Anhidro
tano
Cloruro de etil magnesio
Obtencin de etano
100
alquil litio
Tema 7. Haluros de Alquilo y Arilo
Gua Temtica para el Curso de Qumica Orgnica I
1er paso:
ter Anhidro
Yoduro de propilmagnesio
(Reactivo de Grignard)
Yoduro de propilo
Yoduro de propilmagnesio
Propano
Metanol
Obtencin de propano
Obtencin de cidos carboxlicos.
Un aldehdo o una cetona
Un alcohol
Obtencin de alcoholes
(CH3)2CuLi + I (CH2)9CH3
CH3 (CH2 )9CH3 + LiI + CH3Cu
Reaccin del dimetilcuprato de litio en presencia de 1-iododecano, obtenindose como productos el undecano,
ioduro de litio y metilcobre
Francisco Cruz Sosa/Jorge Armando Haro Castellanos/Ignacio Lpez y Celis/Sergio Alatorre Santamara
101
Universidad Autnoma Metropolitana /Unidad Iztapalapa/Divisin de Ciencias Biolgicas y de la Salud
7.6 Uso de compuestos de Grignard en sntesis orgnica
Un mtodo de obtencin de alcoholes es la reaccin de aldehdos o cetonas con el reactivo de Grignard. Debido a los valores de
electronegatividad del Mg (1.2) y del C (2.5), el enlace entre estos dos tomos es polar con la mayor densidad electrnica ubicada
en el carbono (ya que es el ms electronegativo), por lo cual tiene la capacidad para llevarse el par de electrones de enlace con
el Mg en la ruptura heteroltica. Esto hace que acte como carbanin para atacar como nuclefilo tanto a carbonilos de cetonas o
aldehidos, como a dixido de carbono y a oxiranos, entre otros, para producir los compuestos que se aprecian en el esquema 7.7.
Esquema 7.7 Compuesto de Grignard en sntesis orgnica
Uso de compuestos de Grignard en sntesis orgnica
formacin de alcoholes primarios
Formacin de alcoholes terciarios
metanal
formaldehdo
cetona
xido
de etileno
Formacin de alcoholes secundarios
Formacin de cidos carboxilicos
aldehdo
102
Tema 7. Haluros de Alquilo y Arilo
Gua Temtica para el Curso de Qumica Orgnica I
7.7 Estabilidad de los haluros de alquilo, toxicidad
Los halogenuros de alquilo son compuestos txicos, utilizados en la agricultura como plaguicidas e insecticidas, pero su uso se
est restringido debido al dao que causa al medio ambiente y a los humanos. La toxicidad de los halogenuros de alquilo se
debe a la capacidad de estos para reaccionar con grupos amino o mercapto de enzimas, dando productos alqulicos txicos.
Esquema 7.8 Estabilidad y toxicidad
Estabilidad de haluros de alquilo, toxicidad
Compuestos organoclorados
Compuestos organoclorados
Haluros de alquilo: caractersticas
Haluros de arilo: caractersticas
Enlace fuerte C - Cl
Enlace fuerte C - Cl
Compuestos hidrofbicos
Compuestos hidrofbicos
Ejemplo: insecticidas
Ejemplo: insecticidas
lindano
1,2,3,4,5,6-hexaclorociclohexano
DDT
dicloro difenil tricloroetano
1,1,1-tricloro-2,2-bis (4-clorofenil) etano
Uso: en la agricultura, en las semillas antes de
sembrarlas
Uso: contra mosquitos, piojos, pulgas
Cloroformo
Tetracloruro de carbono
Tetrafluoroetileno
Clorofluorocarburos
(freones)
Francisco Cruz Sosa/Jorge Armando Haro Castellanos/Ignacio Lpez y Celis/Sergio Alatorre Santamara
103
Gua Temtica para el Curso de Qumica Orgnica I
Tema 8
Estereoqumica
8.1 Ismeros estructurales y estereoismeros
8.2 Enantimeros y molculas quirales
8.3 Nomenclatura de enantimeros. El sistema D-L y el sistema R-S
8.4 Propiedades de enantimeros
8.5 Separacin de enantimeros. Trabajos de Pasteur
8.6 Molculas quirales que no poseen centro quiral
8.7 Isomera cis-trans. Sistema E-Z para designar diastermeros de alquenos
Francisco Cruz Sosa/Jorge Armando Haro Castellanos/Ignacio Lpez y Celis/Sergio Alatorre Santamara
105
Universidad Autnoma Metropolitana /Unidad Iztapalapa/Divisin de Ciencias Biolgicas y de la Salud
8.1 Ismeros estructurales y estereoismeros
Esquema 8.1 Ismeros estructurales y estereoismeros
Ismeros estructurales y estereoismeros
Ismeros estructurales o constitucionales
Ismeros de cadena
n-butano
Estereoismeros
Enantimeros: un carbono quiral
2-clorobutano
(S)-2-clorobutano
(R)-2-clorobutano
2-metilpropano
Ismeros de posicin
enantimetros:
dos carbonos quirales
1-butanol
espejo
Diastermeros
2-butanol
Ismeros de funcin
1-butanol
cido D-tartrico
dietil ter
cido L-tartrico
cido mesotartrico
Ismeros geomtricos
Tautomera ceto-enol
cis-2-buteno
acetona
99.9999999 %
propen-2-ol
1 X 10-7 %
isomero (Z) con grupos de mayor isomero (E) con grupos de mayor
prioridad en lados opuestos
prioridad el mismo lado
(Z)-1-bromo-1-cloropropeno
106
trans-2-buteno
Tema 8. Estereoqumica
(E) -1-bromo-1-cloropropeno
Gua Temtica para el Curso de Qumica Orgnica I
8.2 Enantimeros y molculas quirales
Esquema 8.2 Enantimeros y molculas quirales
Enantimeros y molculas quirales
Enantimeros: imgenes especulares no
superponibles con uno o ms tomos
de carbono quirales (que tienen cuatro
sustituyentes diferentes).
Molculas quirales
solo existe un compuesto con frmula
solo existe un compuesto con frmula
espejo
carbono quiral
para la frmula CHXYZ existen dos compuestos no
superponibles con diferente actividad ptica: un ismero
desvia el plano de la luz polarizada a la derecha mientras
que el otro ismero lo desvia a la izquierda.
espejo
2-butanol
espejo
Francisco Cruz Sosa/Jorge Armando Haro Castellanos/Ignacio Lpez y Celis/Sergio Alatorre Santamara
107
Universidad Autnoma Metropolitana /Unidad Iztapalapa/Divisin de Ciencias Biolgicas y de la Salud
8.3 Nomenclatura de enantimeros. El sistema D-L y el sistema R-S
Esquema 8.3 Nomenclatura de enantimeros
Nomenclatura de enantimeros
Sistema D - L
Sistema (R) (S)
Proyeccin de Fischer. La cadena de carbonos en posicin
vertical (la ms oxidada hacia arriba y la ms reducida
hacia abajo). Los sustituyentes que no forman parte de la
cadena de carbonos se situan en la lnea horizonal.
Reglas de prioridad de Cahn-Ingold-Prelog La
prioridad se asigna con base en el nmero
atmico unido al carbono quiral y cuando son
iguales se toman en cuenta los subsecuentes.
Gliceraldehdo
Gliceraldehdo
Posicin
Grupo funcional {-OH}
hacia la derecha
hacia la izquierda
Prioridad
hacia adelante del plano
tomo unido al carbono quiral
-OH
-CHO
-CH2-OH
-H
hacia atras del plano
D-Gliceraldehdo
L-Gliceraldehdo
(R)-Gliceraldehdo
108
Tema 8. Estereoqumica
(S)-Gliceraldehdo
Gua Temtica para el Curso de Qumica Orgnica I
8.4 Propiedades de enantimeros
Esquema 8.4 Propiedades de enantimeros
Propiedades de los enantimeros
Propiedades fsicas
El par de enantimeros tiene las misma
propiedades fsicas excepto la interaccin con la luz
polarizada en un plano.
cido (+) - lactico
Rotacin
especfica
(R) - (+) - limoneno
Rotacin
especfica
olor a limn
Propiedades qumicas
El par de enantimeros tiene las mismas
propiedades qumicas excepto si reaccionan
con diferentes molculas quirales.
cido () - lactico
Rotacin
especfica
(S) - () - limoneno
Rotacin
especfica
olor a pino
(R) - () - adrenalina
(S) - (+) - adrenalina
La adrenalina natural es el estereoismeto (R)-(-)
siendo ms potente que el estereoismero (S)-(+)
(R) - (+) - talidomida
(S) - () - talidomida
El estereoismero (R)-(+) de la tolidomida tiene efectos
sedantes mientras que el estereoismero (S)-(-) tiene
efectos teratognicos.
Francisco Cruz Sosa/Jorge Armando Haro Castellanos/Ignacio Lpez y Celis/Sergio Alatorre Santamara
109
Universidad Autnoma Metropolitana /Unidad Iztapalapa/Divisin de Ciencias Biolgicas y de la Salud
8.5 Separacin de enantimeros. Trabajos de Pasteur
Esquema 8.5 Separacin de enantimeros
Separacin de enantimeros
Trabajos de Pasteur
Forma recmica del tartrato sdico amnico cristales
distingibles y separables (par d + l)
Mtodo general de separacin de mezclas
recmicas (par d + l)
compuestos (+)-B + compuesto (-)-B
agente de resolucin 2 (+)-A
Separacin por
mezcla de
cristalizacin
diastermeros
cromatografa
Separacin mecnica
compuestos
(+)-B - (+)-A
separacin
con un
reactivo
apropiado
compuestos (+)-B
Soluble
en
cido D(-)-tartrico
110
Soluble
en
Enantimero
separado
cido L(+)-tartrico
Tema 8. Estereoqumica
compuestos
(-)-B - (+)-A
separacin
con un
reactivo
apropiado
compuestos (-)-B
Enantimero
separado
Gua Temtica para el Curso de Qumica Orgnica I
8.6 Molculas quirales que no poseen centro quiral
Esquema 8.6 Molculas que no poseen centro quiral
Molculas que no poseen centro quiral
Alenos. Cumulenos. No contienen un centro
quiral sino un eje quiral de frmula
abC = C = Cab donde a es diferente de b
Bifenilos de frmula
ismero cis
Donde a es diferente de b y
c es diferente de d
hacia atrs
ismero trans
perpendicualar
al otro anillo
aromtico
cis 1,3-dicloroaleno
hacia adelante
conformacin escalonada (quiral)
No hay conversin
trans 1,3-dicloroaleno
compuestos meso: son estereoismeros que carecen de actividad
ptica a pesar de tener centros estereognicos,
contienen un plano de simetra que divide a la
molcula en dos partes iguales.
diastermeros:
conformacin escalonada (quiral)
son estereoismeros que no son imagen
en el espejo, contienen dos o ms centros
estereognicos
Francisco Cruz Sosa/Jorge Armando Haro Castellanos/Ignacio Lpez y Celis/Sergio Alatorre Santamara
111
Universidad Autnoma Metropolitana /Unidad Iztapalapa/Divisin de Ciencias Biolgicas y de la Salud
8.7 Isomera cis-trans. Sistema E-Z para designar diastermeros de alquenos
Esquema 8.7 Isomera cis trans, sistema E - Z
Diastermeros de alquenos
Sistema cis - trans
Sistema E-Z
Alquenos de frmula abC = Cab
donde a es diferente de b
Alquenos de frmula abC = Ccd
donde a es diferente de b y c es
diferente de d.
ismero cis
ismero trans
se asigna la
prioridad (1)
al tomo con
mayor nmero
atmico
ismero Z
cis-2-buteno
trans-2-buteno
(Z)-1-bromo-1-cloropropeno
112
ismero E
Tema 8. Estereoqumica
(E)-1-bromo-1-cloropropeno
Gua Temtica para el Curso de Qumica Orgnica I
Tema 9
Mecanismos de reaccin SN y E
9.1 Sustitucin nucleoflica en carbono saturado
9.2 Molecularidad de las reacciones de sustitucin nucleoflica. Cintica de la reaccin
9.3 Estereoqumica y mecanismos de las reacciones SN1 y SN2. Factores que afectan su velocidad
9.4 Reacciones de eliminacin. Mecanismos de la reaccin E1 y E2
9.5 Sustitucin vs. Eliminacin
9.1 Sustitucin nucleoflica en carbono saturado
Esquema 9.1 Sustitucin nucleoflica
Sustitucin nucleoflica en carbono saturado
nuclofilo
Carbono saturado (R) + grupos saliente (L)
Especie neutra o anin que es rica
en electrones
R L
Sustrato
Reaccin general de sustitucin nucleoflica
Nuclofilo mediante
su par de electrones
reemplaza en el
sustrato R - L
ion hidroxilo
R es el
electrfilo
al grupo
saliente
bromuro de metilo
Producto de
reaccin
metanol
El grupo saliente (L) se lleva el
par de electrones
ion bromuro
Francisco Cruz Sosa/Jorge Armando Haro Castellanos/Ignacio Lpez y Celis/Sergio Alatorre Santamara
113
Universidad Autnoma Metropolitana /Unidad Iztapalapa/Divisin de Ciencias Biolgicas y de la Salud
9.2 Molecularidad de las reacciones de sustitucin nucleoflica. Cintica de la reaccin
Esquema 9.2 Cintica de reaccin
Cintica de la reaccin de sustitucin nuceloflica
Sustrato metlico
Sustrato con carbono secundario
rapidez =
rapidez =
SN2 Reaccin bimolecular, participan dos
molcula en el complejo activado que
molculas
determina la velocidad de la reaccin
SN2 Reaccin bimolecular, participan dos
molculas en el complejo activado que
determina la velocidad de la reaccin
rapidez =
Sustrato con carbono primario
SN1 Reaccin unimolecular, participa una
molculas en el complejo activado que
determina la velocidad de la reaccin
rapidez =
SN2 Reaccin bimolecular, participan dos
molculas en el complejo activado que
determina la velocidad de la reaccin
Sustrato con carbono terciario
rapidez =
Sustrato con carbono primario SN1 con rearreglo del
carbocatin primario a carbocatin terciario
SN1 Reaccin unimolecular, participa una
molcula en el complejo activado que
determina la velocidad de la reaccin
rapidez =
SN1 Reaccin unimolecular, participan una
molcula en el complejo activado que
determina la velocidad de la reaccin
rearreglo
R-X primario
114
carbocatin primario
carbocatin terciario
Tema 9. Mecanismos de reaccin SN y E
Gua Temtica para el Curso de Qumica Orgnica I
9.3 Estereoqumica y mecanismos de las reacciones SN1 y SN2. Factores que afectan su velocidad
Esquema 9.3 Estereoqumica
Estereoqumica y mecanismos de las reacciones SN1 y SN2
Estereoqumica de la reaccin SN1
1
disolvente
polar
Estereoqumica de la reaccin SN2
ataque por la parte
posterior al grupo
saliente
2
3
R - X terciario
1
2
carbocatin
R - X secundario
ataque desde la
parte superior
1
3
2
retencin de la
configuracin
1
ataque desde la
parte inferior
3
2
Intermediario: se
forma el enlace
Nu - C y el enlace
C - L se rompe
1
2
carbocatin (R3C )
en un plano
inversin de la
configuracin
inversin de la
configuracin
mezcla recmica: mezcla de dos enantimeros en la
relacin 1:1 de una sola molcula
Francisco Cruz Sosa/Jorge Armando Haro Castellanos/Ignacio Lpez y Celis/Sergio Alatorre Santamara
115
Universidad Autnoma Metropolitana /Unidad Iztapalapa/Divisin de Ciencias Biolgicas y de la Salud
9.4 Reacciones de Eliminacin. Mecanismos de la reaccin E1 y E2
Esquema 9.4 Reacciones de Eliminacin
Mecanismos de la reaccin E1 y E2
Reaccin de Eliminacin
base
alqueno
sustrato R - X
Reaccin E1
Reaccin E2
base
fuerte
sustrato R - X
carbocatin
base
dbil
+ H - Base
alqueno
alqueno
+ H - base + x
base + HX
9.5 Sustitucin vs. Eliminacin
Esquema 9.5 Sustitucin vs. Eliminacin
Sustitucin vs. Eliminacin
Eliminacin
Sustitucin
R-X
CH3 - X
R - X primario
base dbil
H2O / R-OH
SN2
no hay reaccin
Nota: Hay reaccin cuando
el carbocatin primario
sufre un rearreglo a un
carbocatin ms estable
R - X secundario
SN1
R - X terciario
SN1
116
base fuerte
RO / OH / CN
SN2
base dbil
H2O / R-OH
base fuerte
RO / OH / CN
no hay reaccin
E2
R - X secundario
E1
E2
R - X terciario
E1
E2
R-X
R - X primario
SN2
no hay reaccin
Tema 9. Mecanismos de reaccin SN y E
Gua Temtica para el Curso de Qumica Orgnica I
Tema 10
Fenoles
10.1 Diferencia entre un alcohol y un fenol y su aplicacin en la industria
10.2 Acidez de fenoles
10.3 Efecto de los sustituyentes sobre la acidez de los fenoles
10.4 Formacin de teres a partir de fenoles
10.5 Oxidacin de fenoles
10.1 Diferencia entre un alcohol y un fenol y su aplicacin en la industria
Esquema 10.1 Diferencia entre un alcohol y un fenol
Diferencia entre un alcohol y un fenol
Alcoholes R - OH
reaccin con una base fuerte
Fenoles
no hay reaccin
reaccin con una base fuerte
reaccin de nitracin
ster
reaccin de oxidacin
reaccin de nitracin
alcohol primario
aldehdo
alcohol primario
cido carboxlico
reaccin de oxidacin
alcohol secundario
cetona
no hay reaccin
fenoles
quinonas
alcohol terciario
Francisco Cruz Sosa/Jorge Armando Haro Castellanos/Ignacio Lpez y Celis/Sergio Alatorre Santamara
117
Universidad Autnoma Metropolitana /Unidad Iztapalapa/Divisin de Ciencias Biolgicas y de la Salud
10.2 Acidez de fenoles
Esquema 10.2 Acidez de fenoles
Acidez de fenoles
Alcoholes R - OH
Fenoles
Acidez en alcoholes pKa 16 - 18
Acidez en fenoles pKa = 8 - 10
alcohol
ion alcxido
Formas resonantes del ion fenxido
Acidez comparativa de los fenoles
Ka
pKa
-3
-5
3- 5
-8
-10
8 - 10
cidos carboxlicos 10 a 10
fenoles
10 a 10
agua
10 -14
14
alcoholes
10-16 a 10-18
16 - 18
Acidez relativa de los fenoles comparada con
cidos carboxlicos y alcoholes
No hay reaccin
No hay reaccin
No hay reaccin
118
Tema 10. Fenoles
Gua Temtica para el Curso de Qumica Orgnica I
10.3 Efecto de los sustituyentes sobre la acidez de los fenoles
Esquema 10.3 Efecto de los sustituyentes sobre la acidez de los fenoles
Efecto de los sustituyentes: Acidez de los fenoles
Grupos activantes: disminuyen al acidez
Grupos desactivantes: aumentan al acidez
Fenol
10.4 Formacin de teres a partir de fenoles
Esquema 10.4 Formacin de teres a partir de fenoles
Formacin de teres a partir de fenoles
Sntesis de Williamson
teres fenlicos
Fenol
Fenxido
de sodio
Fenxido de sodio
teres fenlicos
Sntesis de Williamson
Sntesis del anisol
Fenol
Fenxido
de sodio
Fenxido de sodio
Anisol
Francisco Cruz Sosa/Jorge Armando Haro Castellanos/Ignacio Lpez y Celis/Sergio Alatorre Santamara
119
Universidad Autnoma Metropolitana /Unidad Iztapalapa/Divisin de Ciencias Biolgicas y de la Salud
10.5 Oxidacin de fenoles
Esquema 10.5 Oxidacin de fenoles
Oxidacin de fenoles
Fenoles sustituidos
Difenoles
catecol
m-cresol
p-aminofenol
120
o-benzoquinona
2-metil-1, 4-benzoquinona
p-benzoquinona
hidroquinona
Tema 10. Fenoles
p-benzoquinona
Gua Temtica para el Curso de Qumica Orgnica I
Tema 11
teres
11.1 Estructura y nomenclatura de teres
11.2 Propiedades fsicas
11.3 Preparacin de teres. Sntesis de Williamson
11.4 Reacciones de los teres. Rompimiento por cidos
11.5 teres cclicos. Epxidos
11.1 Estructura y nomenclatura de teres
Esquema 11.1 Estructura y nomenclatura de teres
Estructura y nomenclatura de teres
teres dialqulicos R - O - R
teres fenil alqulicos Ar - O - R
teres difenlicos Ar - O - Ar
ter dimetlico
dimetil ter
ter dietlico
dietil ter
ter difenlico
difenil ter
anisol
ter fenil metlico
ter fenil isoproplico
ter etil metlico
metiletil ter
Heterociclos alifticos
tetrahidrofurano
1,4-dioxano
Heterociclos aromticos
furano
Francisco Cruz Sosa/Jorge Armando Haro Castellanos/Ignacio Lpez y Celis/Sergio Alatorre Santamara
121
Universidad Autnoma Metropolitana /Unidad Iztapalapa/Divisin de Ciencias Biolgicas y de la Salud
11.2 Propiedades fsicas
Esquema 11.2 Propiedades fsicas
Propiedades fsicas de teres
Polaridad (alcoholes vs teres)
densidad
densidad
electrnica
electrnica
positiva
negativa
Punto de ebullicin (alcoholes vs teres)
P. eb. alcoholes
P. eb. teres
densidad
electrnica
positiva
alcoholes solvatan a
cationes y/o aniones
anin (-)
teres solvatan
solo a cationes
catin (+)
catin (+)
disolventes
menos polares
diclorometano
n-hexano
benceno
ter dietilico
ms polares
acetato
de etilo
agua
metanol
cloroformo
122
etanol
acetona
Tema 11. teres
Gua Temtica para el Curso de Qumica Orgnica I
11.3 Preparacin de teres. Sntesis de Williamson
Esquema 11.3 Preparacin de teres. Sntesis de Williamson
Propiedades fsicas de teres
Sntesis de teres dialqulicos
Sntesis de teres fenlicos
ter etil metlico
Sntesis de Wiliamson intramolecular
Sntesis de teres cicloalqulicos
ter fenil etlico
tetrahidrofurano
ter ciclohexil metlico
Francisco Cruz Sosa/Jorge Armando Haro Castellanos/Ignacio Lpez y Celis/Sergio Alatorre Santamara
123
Universidad Autnoma Metropolitana /Unidad Iztapalapa/Divisin de Ciencias Biolgicas y de la Salud
11.4 Reacciones de los teres. Rompimiento por cidos
Esquema 11.4 Reacciones de los teres. Rompimiento por cidos
Reacciones de los teres. Rompimiento por cidos
teres no cclicos simtricos
teres no cclicos no simtricos: mezcla de productos
Mecanismo de reaccin
ter etil metlico
etanol
yoduro
de etilo
etanol
teres cclicos (epxidos)
xido de etileno
etilenglicol
Mecanismo de reaccin
124
Tema 11. teres
yoduro
de metilo
yoduro
de etilo
metanol
Gua Temtica para el Curso de Qumica Orgnica I
11.5 teres cclicos (epxidos)
Esquema 11.5 teres cclicos
Heterociclos oxigenados
oxirano
xido de etileno
oxetano
xido de
ciclohexano
oxetano
dioxanos
furano y pirano
tetrahidrofurano
tetrahidropirano
2-etil-3-metiloxetano
furano
pirano
1,2-dioxano
1,3-dioxano
1,4-dioxano
dibenzodioxina (dioxina)
Francisco Cruz Sosa/Jorge Armando Haro Castellanos/Ignacio Lpez y Celis/Sergio Alatorre Santamara
125
Gua Temtica para el Curso de Qumica Orgnica I
Bibliografa
Libros de Texto
Bruice, Paula Yurkanis Qumica Orgnica Pearson Educacin Mxico 5 Edicin Mxico 2008.
& Carey, Francis A. Qumica Orgnica Mc. Graw-Hill Interamericana 6 Edicin Mxico 2006.
& Fox, Marye Anne, Whitesell James K. Qumica Orgnica Addison Wesley Longman 2 Edicin Mxico 2000.
& McMurry, John Qumica Orgnica Thomson Paraninfo 7 Edicin Mxico 2009.
& Morrison, Robert T., Boyd, Robert N. Qumica Orgnica Pearson Addison Wesley 5 Edicin Mxico 1998.
& Solomons, Graham T.W. Qumica Orgnica Editorial Limusa, S.A. de C.V. 2 Edicin Mxico 1999.
& Wade, L.G. Jr. Qumica Orgnica Volumen 1 y Volumen 2 Pearson Educacin 7 Edicin Mxico 2011.
Francisco Cruz Sosa/Jorge Armando Haro Castellanos/Ignacio Lpez y Celis/Sergio Alatorre Santamara
127
Gua Temtica para el Curso de Qumica Orgnica I
Se termin de imprimir en diciembre de 2015,
con un tiraje de 200 ejemplares, ms sobrantes para reposicin.
Вам также может понравиться
- Qui MicaДокумент40 страницQui MicaZuly Maricela Davila Maura100% (2)
- Hidrocarburos CíclicosДокумент18 страницHidrocarburos Cíclicoscarlos300106Оценок пока нет
- Pruebas de Susceptibilidad A La Caries Dental y Su Relación Con La Clínica Del NiñoДокумент8 страницPruebas de Susceptibilidad A La Caries Dental y Su Relación Con La Clínica Del NiñoLiiz PinedaОценок пока нет
- Quimica Organica NomenclaturaДокумент66 страницQuimica Organica NomenclaturaMariel Martinez100% (1)
- Pka de FarmacosДокумент6 страницPka de FarmacosIsidro Santiago Sanchez83% (12)
- Hidratacion y Adicion de AcidoДокумент18 страницHidratacion y Adicion de AcidoJose Luis PachecoОценок пока нет
- QumicaheterociclДокумент505 страницQumicaheterocicleduardo63k100% (1)
- Acidos y BasesДокумент35 страницAcidos y BasesLaura Alejandra Sandoval MontoyaОценок пока нет
- EstandarizaciÓn de Disoluciones Valorantes.Документ12 страницEstandarizaciÓn de Disoluciones Valorantes.shia2makaОценок пока нет
- Aplicacion de La Calidad en El Medicamento PDFДокумент50 страницAplicacion de La Calidad en El Medicamento PDFluisОценок пока нет
- Modelos Epistémicos de La Lectura en Estudiantes Universitarios MexicanosДокумент30 страницModelos Epistémicos de La Lectura en Estudiantes Universitarios MexicanosLiiz PinedaОценок пока нет
- Guide ABC of Easy Titration ES LOWДокумент40 страницGuide ABC of Easy Titration ES LOWMiguel Angel Lupaca BernalesОценок пока нет
- Fitoquimica Preeliminar de Algunas Plantas Superiores de ColombiaДокумент7 страницFitoquimica Preeliminar de Algunas Plantas Superiores de ColombiaLiiz PinedaОценок пока нет
- Grupos Protectores en Química OrgánicaДокумент40 страницGrupos Protectores en Química Orgánicafernandopessoa25Оценок пока нет
- Acidos y BasesДокумент35 страницAcidos y BasesLaura Alejandra Sandoval MontoyaОценок пока нет
- Sintesis OrganicaДокумент131 страницаSintesis OrganicaSugey AОценок пока нет
- Sintesis OrganicaДокумент131 страницаSintesis OrganicaSugey AОценок пока нет
- Defensor Del PuebloДокумент3 страницыDefensor Del PuebloLiiz PinedaОценок пока нет
- Manual de AntropometriaДокумент30 страницManual de AntropometriaElywhtGrandBarОценок пока нет
- Experimento Miller-UreyДокумент2 страницыExperimento Miller-UreyLiiz PinedaОценок пока нет
- Tejido Inmune1Документ38 страницTejido Inmune1Liiz PinedaОценок пока нет
- EcologiaДокумент108 страницEcologiarishyxОценок пока нет
- Geometría y TrigonometríaДокумент16 страницGeometría y TrigonometríaLiiz PinedaОценок пока нет
- Q S HistДокумент1 страницаQ S HistLiiz PinedaОценок пока нет
- MATEMATICAS 3 UnamДокумент12 страницMATEMATICAS 3 UnamLiiz PinedaОценок пока нет
- Preparación Del Paciente TecnicasДокумент8 страницPreparación Del Paciente TecnicasLiiz PinedaОценок пока нет
- FisiologiaДокумент5 страницFisiologiaLiiz PinedaОценок пока нет
- BIOLOGIA LiizДокумент23 страницыBIOLOGIA LiizLiiz PinedaОценок пока нет
- ALQUENOS Y ALQUINOSFEr.Документ53 страницыALQUENOS Y ALQUINOSFEr.FernandoОценок пока нет
- Hidrocarburos AlcanosДокумент31 страницаHidrocarburos AlcanosValeria OlmedoОценок пока нет
- Muchas de Las Reacciones de Los Alquinos SonДокумент13 страницMuchas de Las Reacciones de Los Alquinos SonFrank Pitalua BarbosaОценок пока нет
- Taller H GRUPO 3Документ8 страницTaller H GRUPO 3Orozco Andrés FelipeОценок пока нет
- Cap. 2 Tabla 2Документ19 страницCap. 2 Tabla 2Juan daniel Torrez vidaurreОценок пока нет
- Guia Alquenos 2021Документ14 страницGuia Alquenos 2021Karol Michell Reyes ValenciaОценок пока нет
- Clase 2 Qca Org Nomenclatura 1Документ85 страницClase 2 Qca Org Nomenclatura 1Victor RuedaОценок пока нет
- Sintesis y Reacciones de AlquenosДокумент12 страницSintesis y Reacciones de AlquenosWilliams Reynaldo Arce DelgadoОценок пока нет
- Ejercicios Clase 10 de NoviembreДокумент6 страницEjercicios Clase 10 de Noviembrefelipe jaraОценок пока нет
- Tarea de QuimicaДокумент11 страницTarea de QuimicaAngelica SorianoОценок пока нет
- Quimica Organica I 2020 - Manual de PrácticasДокумент34 страницыQuimica Organica I 2020 - Manual de PrácticasModesto CopiasОценок пока нет
- Reacciones de Los Compuestos Orgánicos 1Документ22 страницыReacciones de Los Compuestos Orgánicos 1SilvanaSeguiОценок пока нет
- Asignatura: Química Grado: 11° NOMBREДокумент9 страницAsignatura: Química Grado: 11° NOMBREvanessa carolina maestre mendozaОценок пока нет
- Qui MicaДокумент20 страницQui Micacarmennino0102Оценок пока нет
- Practica de Jesus QuimicaДокумент4 страницыPractica de Jesus QuimicaJualdi Tejada MarizanОценок пока нет
- QuimicaДокумент18 страницQuimicaRodriguez Ramos ArevaloОценок пока нет
- CARBONOДокумент72 страницыCARBONODionne BeckОценок пока нет
- Determinación de Dobles Enlaces, Alcoholes y FenolesДокумент6 страницDeterminación de Dobles Enlaces, Alcoholes y FenolesMilena Paulette Valarezo AlvarezОценок пока нет
- Manual Nomenclatura OrganicaДокумент36 страницManual Nomenclatura Organicamariana ossa ortegaОценок пока нет
- Informe Nro 6 Quimica Organica RevisadoДокумент13 страницInforme Nro 6 Quimica Organica RevisadoJuan Diego Cahuana Vasquez100% (1)
- Alquinos 1561739585Документ9 страницAlquinos 1561739585J̶a̶s̶m̶a̶n̶y̶A̶t̶i̶e̶n̶c̶i̶a̶ȜȝОценок пока нет
- Hidrocarburos InsaturadosДокумент14 страницHidrocarburos InsaturadosAntonio Holin100% (1)
- Quimica OrganicaДокумент42 страницыQuimica Organicaevild7400Оценок пока нет
- Exposicion Alcanos y Alquenos de Quimica IiДокумент12 страницExposicion Alcanos y Alquenos de Quimica IiCamilo andres Acuña sierraОценок пока нет
- Quimica Orgànica 1Документ34 страницыQuimica Orgànica 1Andrea BustamanteОценок пока нет
- CUESTIONARIO OrgДокумент31 страницаCUESTIONARIO OrgcristinaguizarulloaОценок пока нет