Академический Документы
Профессиональный Документы
Культура Документы
Texto Guia de Laboratorio de Microbiología UPV Última Actualización PDF
Загружено:
Sebastian Montecinos ValenzuelaОригинальное название
Авторское право
Доступные форматы
Поделиться этим документом
Поделиться или встроить документ
Этот документ был вам полезен?
Это неприемлемый материал?
Пожаловаться на этот документАвторское право:
Доступные форматы
Texto Guia de Laboratorio de Microbiología UPV Última Actualización PDF
Загружено:
Sebastian Montecinos ValenzuelaАвторское право:
Доступные форматы
MANUAL DE LABORATORIO DE
MICROBIOLOGA
TEXTO GUA PARA EL ALUMNO
Carrera de Medicina
MEDI 4032
UNIVERSIDAD PEDRO DE VALDIVIA
Carlos Ivovic Oddo
Tecnlogo Mdico
Profesor de Microbiologa
FACULTAD DE CIENCIAS MDICAS
Manual de Laboratorio de Microbiologa
NDICE DE CONTENIDOS
Tema
UNIDAD 1:
Pgina
BIOSEGURIDAD
Definiciones
Simbologa
Categoras del Riesgo
Gestin de Riesgos
Normas de Bioseguridad
Bioseguridad en la Prctica Mdica
Origen de las Amenazas en Bioseguridad Mdica
Reduccin de Riesgos en Bioseguridad
Medidas de Contencin
Bioseguridad en el Laboratorio de Microbiologa
Niveles de Bioseguridad
Accidentes de Bioseguridad en Microbiologa
Ejercicios de aplicacin de contenidos (bioseguridad)
Actividad de laboratorio n 1 y 2 (bioseguridad)
Desinfeccin y antisepsia
El efecto de los agentes qumicos sobre los microrganismos
Efecto de factores fsicos sobre los microrganismos
Efecto de la temperatura
Efecto de las radiaciones, Luz Ultravioleta
Efecto de las radiaciones, Radiacin Gamma
Esterilizacin
Ejercicios de aplicacin de contenidos (antisepsia, desinfeccin y esterilizacin)
UNIDAD 2:
TOMA DE MUESTRAS Y CULTIVO PRIMARIO
Actividad de Laboratorio n3 al 5 (aislamiento de bacterias)
Actividad de Laboratorio n6: observacin macroscpica de cultivos
Actividad de Laboratorio n7: observacin microscpica de cultivos
UNIDAD 3:
4
4-5
6
7
8
8
9
10
11
12
12-13
14
14-15
16-17
18-19
20-21
22
22-25
25-28
28
29-33
34
36-39
40-41
42-44
IDENTIFICACIN DE BACTERIAS
Fundamentos de identificacin de enterobacterias mediante pruebas bioqumicas
Fundamentos de identificacin de Cocceas Gram positivas aerobias
Aspectos taxonmicos generales
Prueba de la catalasa, primera etapa en la marcha de identificacin
Identificacin de Cocceas Gram (+) aerobias o facultativas, con catalasa negativa
Pruebas de Identificacin para Streptococcus pneumoniae
Actividad de Laboratorio n8: identificacin de bacilos
Actividad de Laboratorio n9: determinacin de catalasa
Actividad de Laboratorio n10: identificacin de cocceas Gram positivas I
Actividad de Laboratorio n11: Identificacin de cocceas Gram positivas II
45-50
51-53
51
54
55
56
60-61
62
63
64
2
FACULTAD DE CIENCIAS MDICAS
Manual de Laboratorio de Microbiologa
UNIDAD 4:
PRUEBAS DE SUSCEPTIBILIDAD A LOS ANTIMICROBIANOS
Aspectos generales
La Concentracin Inhibitoria Mnima y Bactericida Mnima
Interpretacin de las Pruebas: susceptibilidad o resistencia
El antibiograma por mtodo de difusin en agar
Ejercicios de aplicacin de contenidos
Actividad de Laboratorio n12: el antibiograma por difusin
Tablas de determinacin de la susceptibilidad mediante difusin en agar
65-66
66-67
67-68
68-72
72
73
74-75
FACULTAD DE CIENCIAS MDICAS
Manual de Laboratorio de Microbiologa
UNIDAD 1
BIOSEGURIDAD
Definiciones y simbologas
Podemos definir la BIOSEGURIDAD como el conjunto de las medidas, normas y procedimientos
fijados por una organizacin para minimizar y/o controlar el riesgo de ocurrencia de un accidente
con agentes biolgicos.
De acuerdo a esta definicin, se hace necesario precisar que el RIESGO es el grado de
vulnerabilidad de lo que nos interesa proteger, en otras palabras implica la existencia de una
posibilidad de que le ocurra un dao a lo que debemos proteger.
El riesgo de accidentes con cualquier agente (qumico, fsico o biolgico) est siempre
presente, pero se hace cuantitativamente menor o mayor dependiendo del grado de control de las
circunstancias que determinan la ocurrencia del accidente. Para dar una dimensin objetiva al
riesgo, podemos darle una categora de valor bajo, medio o alto.
La existencia de estos distintos agentes, o los acontecimientos que los liberan o desencadenan son
llamados AMENAZAS.
De acuerdo a las condiciones de ocurrencia que desencadenan a las amenazas, podemos
distinguir dos clases:
1. Amenazas Dirigidas: aquellas que actan por INTENCIN, es decir actos
premeditados y dirigidos con el objeto de causar dao.
2. Amenazas No Dirigidas: son las que ocurren en forma aleatoria, impredecible o
accidental.
El grado de dao que una determinada Amenaza es capaz de infligir sobre lo protegido
puede ser categorizado (como magnitud) y medido (como probabilidad). A la asociacin de estas
categoras de magnitud y probabilidad la llamaremos PELIGRO.
Este es el smbolo internacional que indica la existencia de un
agente peligroso (amenaza), que tiene la posibilidad de causarnos dao
severo o mortal. No se especifica cul es la amenaza, pero si el nivel de
dao que no puede causar. Lo podemos observar en las etiquetas de los
reactivos qumicos, a veces asociados a otros smbolos.
Ejemplos:
Cianuro de Potasio.
Acetato de Talio (veneno rodenticida)
Fluoruro de Sodio (anticoagulante usado para la toma de muestras para medicin de
niveles de glucosa).
Oxido de Etileno (agente esterilizante).
Formaldehdo (agente conservador de tejidos y esterilizante).
FACULTAD DE CIENCIAS MDICAS
Manual de Laboratorio de Microbiologa
Los agentes que representan una amenaza para la bioseguridad
se identifican internacionalmente con este smbolo, el que debe
considerarse como una ADVERTENCIA:
En este caso no se hace mencin al nivel de peligro, por
lo que el dao causado por el supuesto agente puede ser de cualquier
magnitud.
No se especifica el tipo de agente biolgico, este puede ser
una muestra para anlisis de laboratorio, una sustancia
contaminada con agentes biolgicos, un extracto de origen biolgico, un agente biolgico aislado
desconocido, o un agente biolgico aislado. La simbologa no hace distincin entre tipos de
agentes: virus, bacterias, hongos, parsitos, su estado estructural ni respecto de su actividad vital.
Es posible observar este smbolo en contenedores de transporte de muestras para anlisis:
orina, sangre, secreciones, deposiciones, biopsias o partes para estudio anatomopatolgico sin
tratamiento con fijadores. Contenedores con deshechos quirrgicos, de salas de hospitalizacin o
de laboratorios clnicos, muestras o cultivos en trnsito, partes de seres vivos o seres de
naturaleza no bien comprendida deben rotularse con este smbolo, adems de las etiquetas que
especifiquen contenido.
Existe una detallada descripcin de las especificaciones aceptadas internacionalmente
para el transporte de sustancias biolgicas que implican riesgo de bioseguridad. En nuestro pas
esta actividad esta regulada por el Instituto de Salud Pblica de Chile, puedes consultar la
normativa vigente en www.ispch.cl/sites/default/.../normativa_Transp_Sust_Infecciosas.pdf
Otros smbolos de advertencia de riesgos son:
Sustancia Inflamable
Sustancia Nociva, irritante
Material Explosivo
Material radiactivo
Sustancia Corrosiva
Sustancia daina
para el ambiente
FACULTAD DE CIENCIAS MDICAS
Manual de Laboratorio de Microbiologa
Categoras de Riesgo:
Una forma prctica de objetivar el nivel de riesgo y a la vez establecer un criterio comn
de valor entre las personas que ven expuestas a diversas amenazas es asignar categoras de riesgo.
Para categorizar el riesgo en bioseguridad (y en otros mbitos) deben establecerse
mediante consenso valores arbitrarios para las probabilidades de que se manifiesten las amenazas
presentes y los peligros latentes que stas implican. Para esto es necesario previamente constituir
grupos de profesionales idneos y realizar un anlisis de riesgo, el que arrojara un resultado
semejante a este:
Valores arbitrarios para la probabilidad de amenaza o para el dao resultante en la
exposicin:
1.- amenaza insignificante, ningn dao o dao insignificante.
2.- Nivel bajo o menor.
3.- Nivel medio
4.- Nivel alto
Como ahora tenemos asignados valores a las amenazas y sus correspondientes daos,
podemos asociarlos mediante una matriz de numrica, que representa una relacin matemtica
entre el nivel de la amenaza y su dao resultante (peligrosidad)
Categora de Riesgo:
MAGNITUD DEL DAO X PROBABILIDAD DE AMENAZA
Valores 1 a 6: riesgo bajo
Valores 8 a 9: riesgo medio
Valores 12 a 16 riesgo alto
Una vez establecidas estas categoras es posible efectuar MANEJO O GESTION DE RIESGO a
nivel institucional.
Gestin de Riesgos:
La Gestin de Riesgos es un proceso analtico, multidisciplinario y dinmico que tiende a
conocer el estado de control de amenazas de un sistema, en otras palabras a determinar la
probabilidad de ocurrencia de daos y sus causas.
La gestin de riesgos es una de las herramientas ms eficaces en la contencin de
amenazas, apreciacin de fortalezas y debilidades, mediadas de reduccin y control de riesgos y
reduccin de costos implcitos en problemas de bioseguridad. De la gestin de riesgos emana
6
FACULTAD DE CIENCIAS MDICAS
Manual de Laboratorio de Microbiologa
como resultado el conjunto de NORMAS DE BIOSEGURIDAD, que cada institucin adopta para la
seguridad de sus profesionales (equipo mdico) y trabajadores, de las personas beneficiarias de la
organizacin (pacientes), y del medio en el que est inserta (ambiente y sociedad).
En el proceso de Gestin de Riesgos se describen varias etapas que lo componen, y se
suceden en forma cclica o se implementan segn la necesidad:
1.- Evaluacin del Riesgo:
- constituir el grupo de estudio
- definicin de amenazas
- definicin de daos por exposicin a las amenazas
- definicin de prioridades
- recopilacin de informacin
2.- Clasificacin de Riesgos segn categoras.
- Asignar valores arbitrarios a las amenazas identificadas
- Asignar valores arbitrarios a los daos resultantes
- Categorizar el riesgo en alto medio bajo nulo.
3.- Determinar medidas de reduccin de riesgos
- Desplazamiento de personas
- Capacitacin
- Modificacin de la planta fsica del establecimiento
- Programas de mantenimiento
- Disposicin de desechos hospitalarios
- Instalacin de Servicio de esterilizacin
- Uso de medidas de barrera
4.- Control de riesgos
- Formacin de Comit de Infeccin Intrahospitalaria
- Vigilancia epidemiolgica
- Control de vectores
- Auditoras de cumplimiento de normativas
- Anlisis de fallos en cumplimientos de normas.
Normas de Bioseguridad
Las Normas de Bioseguridad son el conjunto de disposiciones establecidas mediante el
proceso de Gestin de Riesgos, que tienen como finalidad PROTEGER AL INDIVIDUO, LA
COMUNIDAD Y EL AMBIENTE, del contacto con agentes biolgicos potencialmente nocivos.
En general, estas normas permiten establecer mecanismos de barrera que impidan la
propagacin de todo tipo de agentes biolgicos en mbitos tan diversos como la atencin de
salud, la produccin industrial de alimentos, medicamentos, biotecnologas, la investigacin
cientfica o policial forense, y la proteccin del medio ambiente.
7
FACULTAD DE CIENCIAS MDICAS
Manual de Laboratorio de Microbiologa
Cada institucin donde se manejen sustancias potencialmente infecciosas, seres vivos o
derivados de estos, es responsable de fijar sus propias normas de bioseguridad,
independientemente del deber de cumplir con las disposiciones que la Autoridad Sanitaria
determine para este efecto. En nuestro pas estas normas son establecidas por el Instituto de
Salud Pblica de Chile como organismo tcnico del Ministerio de Salud, y el Instituto Nacional de
Normalizacin (INN).
Existen muchas normas de bioseguridad disponibles, algunas de alcance muy especfico
relacionadas con el manejo de agentes como el Virus HANTA, Micobacterium tuberculosis, Virus
de la Inmunodeficiencia Humana (VIH), etc.
A modo de ejemplo puedes consultar el Manual de Normas de Bioseguridad de Conicyt
2008 en Investigacin.uach.cl/archivos/manual_bioseguridad_2008.pdf
Bioseguridad en la prctica de la Medicina:
Los accidentes biolgicos en la prctica de la Medicina tienen directa relacin con la
exposicin a agentes infecciosos mediante la atencin de pacientes o por contacto con sus fluidos
y tejidos. Este contacto origina una contaminacin que puede tener como consecuencia:
Contagio: la instalacin de agente biolgico que
Implica un proceso infeccioso en el profesional
Estado de portador sano
Simple transmisin del agente, sea directa o indirecta
La ocurrencia de una infeccin por contacto accidental va a
depender de la concomitancia de varios factores, adems de las medidas
de barrera que el profesional debe emplear, en esto debemos considerar
el grado de susceptibilidad del infectado, las puertas de entrada y el mecanismo de infeccin, la
cantidad de microrganismo infectante y sus caractersticas biolgicas (mecanismos de patogenia).
El ambiente tambin puede condicionar la ocurrencia de la infeccin (humedad, ventilacin,
temperatura ambiental).
Como en cualquier proceso infeccioso, ocurre una alteracin del equilibrio de la Trada
Ecolgica en la que se relaciona AMBIENTE AGENTE HOSPEDERO.
FACULTAD DE CIENCIAS MDICAS
Manual de Laboratorio de Microbiologa
Origen de las Amenazas a la Bioseguridad en Medicina:
Las fuentes de amenazas en los ambientes mdicos estn vinculadas a acciones del pblico
que recibe atencin, sus acompaantes, servicios de apoyo interno o externo, servicios informales,
acciones del equipo de salud y personal administrativo. La alta concurrencia al servicio hospitalario
y la gran variedad de acciones que all se verifican especialmente cuando existe desorganizacin y
falta de medidas de control facilitan la ocurrencia de amenazas a la bioseguridad.
En este caso, las fuentes de amenazas podemos categorizarlas como:
GENERADORES: Todo individuo que mediante acciones, condicin
de salud, ejecutante de tcnicas o misiones, puede generar,
transmitir o eliminar agentes biolgicos potencialmente
peligrosos al ambiente hospitalario. Un generador puede ser
considerado adems RESERVORIO de agentes infecciosos.
TRANSMISORES: Todo individuo que forma parte de una cadena
de acciones en la que se manipulan objetos contaminados o
muestras de pacientes que pueden contener agentes infecciosos.
De esta forma, los pacientes con estados infecciosos y la disposicin de residuos biolgicos
representan una importante fuente de amenazas a la bioseguridad.
Entre los residuos biolgicos peligrosos derivados de la atencin mdica destacan:
Residuos provenientes de zonas de aislamiento.
Cultivos de agentes infecciosos.
Sangre humana, sus derivados y objetos que la contengan.
Residuos orgnicos diversos (orina, deposiciones, secreciones)
Residuos materiales contaminados provenientes de ciruga y autopsias.
Residuos materiales contaminados de laboratorio.
Instrumentos cortopunzantes usados.
Residuos de unidades de dilisis.
Cadveres de animales de laboratorio.
Residuos provenientes de Establecimientos geritricos.
Residuos Provenientes de Comunidades teraputicas o Centros de Rehabilitacin
psicofsica donde se realice el tratamiento de adicciones.
La forma adecuada de mantener estas amenazas bajo control es una adecuada Gestin de Riesgos.
FACULTAD DE CIENCIAS MDICAS
Manual de Laboratorio de Microbiologa
Reduccin de Riesgos en Bioseguridad:
El proceso exitoso de Gestin de Riesgos debe tener como resultado la generacin de
Normas de Bioseguridad y Medidas de Control. En este sentido la direccin del establecimiento de
salud, o las respectivas jefaturas de servicio pueden determinar una gran variedad de normas y
medidas destinadas a disminuir el riesgo de accidentes relacionados con la bioseguridad, como
pueden ser:
Programas de capacitacin del personal
Vigilancia de la adecuada aplicacin de tcnicas mdicas
Uso de medidas de barrera
Vigilancia epidemiolgica
Organizacin del desplazamiento de personas
Programas de mantenimiento permanente de la planta fsica
Gestin de Riesgos permanente
Inmunizaciones, cuando la naturaleza del agente lo determine
Control del estado de salud del personal mdico y administrativo
Control de manipuladores de alimentos
Control de vectores
CONCIENCIA DEL RIESGO Y RESPONSABILIDAD PERSONAL
La responsabilidad y el AUTOCUIDADO son los pilares fundamentales del control de riesgos
en bioseguridad. El compromiso personal de cada integrante del equipo de salud en mantener su
integridad y en observar las normas de bioseguridad es la mejor forma de garantizar la
disminucin de riesgos. De lo contrario, cualquier esfuerzo en este sentido puede ser estril.
Las medidas de autocuidado pueden verse reflejadas en documentos como las
PRECAUCIONES UNIVERSALES o PRECAUCIONES STANDARD, normas de consenso para el
trabajo con pacientes y sus fluidos corporales destinadas a minimizar el riesgo de transmisin de
infecciones entre pacientes y el personal y vice-versa, por contacto con fluidos de alto riesgo,
especialmente la sangre y sus derivados.
Se consideran fluidos de alto riesgo en bioseguridad:
Sangre
Semen
Secreciones Vaginales
Leche Materna
Lquido de cavidades cerradas
Lquido Cefalorraqudeo
Lquido Pleural
Lquido Sinovial
Y todos los otros fluidos que tengan sangre visible
10
FACULTAD DE CIENCIAS MDICAS
Manual de Laboratorio de Microbiologa
Todas las muestras o fluidos corporales provenientes de pacientes deben considerarse
siempre como potencialmente infectantes, independiente del motivo de consulta o de diagnstico
de ingreso, por lo que su manipulacin implica la observacin permanente de las Precauciones
Universales.
Puedes revisar documentos relacionados a estas Precauciones Universales en:
http://www.enfermeriajw.cl/pdf/GUIACLINICAIIHPrevenciondeExposicionesaSangreymanejoPostexposicion_RES_793_06_09_04.pdf
www.ssvaldivia.cl/hospital/acredita/...iih/04%20NORMA%206.doc
En todo caso, el LAVADO DE MANOS antes de la jornada,
entre pacientes, y al final de la jornada, representa el mejor
ejemplo de una efectiva y sencilla medida de barrera de transmisin
de enfermedades.
Medidas de Contencin
Corresponden a la aplicacin de las medidas resultantes de la etapa 3. Y 4. De la Gestin
de Riesgos, es decir las Normas de Bioseguridad y Medidas de Control mencionadas anteriormente
en la pgina 6.
Podemos clasificar las Medidas de Contencin en dos grandes grupos dependiendo del
objetivo de aplicacin:
Medidas de Contencin Primaria: estn dirigidas al accionar de las personas, en
mbitos como la proteccin de la salud, el manejo adecuado de pacientes y las
condiciones del ambiente de trabajo en el establecimiento de salud. En este grupo
podemos mencionar (entre otras) la accin del Comit de Infeccin
Intrahospitalaria, la adecuada gestin de abastecimiento en insumos de seguridad,
capacitacin especfica en bioseguridad, etc.
Medidas de Contencin Secundarias: estn dirigidas a la proteccin del ambiente,
y se relacionan con el diseo y la calidad de la planta fsica del establecimiento, y
de la prestacin de servicios externos (extraccin de basuras, disposicin de
residuos hospitalarios).
11
FACULTAD DE CIENCIAS MDICAS
Manual de Laboratorio de Microbiologa
Bioseguridad en el Laboratorio de Microbiologa
El Laboratorio Clnico, y especialmente la Seccin de Microbiologa es una importante
fuente generadora de amenazas, debido a la actividad propia de esta unidad asistencial. Por esta
razn, la adecuada capacitacin del personal, la descripcin de mtodos y procedimientos, la
auditora de normas, los protocolos de accin frente a accidentes, y el diseo de la planta fsica
son de vital importancia en el control de amenazas.
Al interior de un Laboratorio de Microbiologa podemos observar varias medidas de
contencin primaria, como lo son:
los insumos de seguridad personal (pecheras, guantes, antiparras, mascarillas)
soluciones de desinfeccin
contenedores de material cortopunzante
protocolos de reaccin frente a accidentes
filtros de aire de alta eficiencia (HEPA)
lmparas de luz UVC
mechero
tapas de contencin de aerosoles (centrfugas)
gabinetes de bioseguridad
o CLASE I: otorga proteccin para el ambiente y equipos
o CLASE II: otorga proteccin para el ambiente, equipos y muestras
o CLASE III: proteccin de alto nivel, aislamiento para el trabajo con agentes
altamente peligrosos.
Niveles de Bioseguridad en Laboratorios de Microbiologa:
El conjunto de medidas de contencin primarias y secundarias que se han implementado
en un Laboratorio de Microbiologa determinan el NIVEL DE BIOSEGURIDAD de esta dependencia,
es decir el grado de seguridad instalada para el trabajo con agentes biolgicos. A mayor peligro
representado por los agentes, mayor nivel de bioseguridad.
Podemos distinguir cuatro niveles de bioseguridad para un laboratorio de microbiologa:
NIVEL 1:
Instalaciones adecuadas para trabajar con agentes no infecciosos o
que no afectan a personas adultas sanas. Corresponden a laboratorios de
docencia, laboratorios clnicos de baja complejidad o de instalaciones bsicas.
Pueden manejarse microrganismos como Escherichia coli, Bacillus subtilis,
Streptococcus viridans por ejemplo.
12
FACULTAD DE CIENCIAS MDICAS
Manual de Laboratorio de Microbiologa
NIVEL 2:
Las instalaciones deben poseer gabinetes de bioseguridad de
acuerdo al tipo de agentes que se pretende manejar. Debe existir control de
acceso. Se hace necesario el
contar con protocolos y
aparatos necesarios para la
descontaminacin. Corresponde
al diseo de laboratorios de
microbiologa clnica o de
investigacin, donde se trabaja
con muestras de origen humano,
animal o ambiental, donde es
posible manipular agentes
como Salmonella, Vibrio,
Neisseria gonorrhoeae, muestras para serologa viral (Hepatitis B, VIH, Virus
Hepstein Barr).
NIVEL 3:
Estos laboratorios estn preparados para el trabajo con
microrganismos transmisibles por va area, y tienen potencial para causar
enfermedades graves. Las barreras de contencin deben ser suficientemente
fuertes para proteger a los trabajadores al interior, en reas contiguas, ambiente y
comunidad. Es necesaria la instalacin de lmparas UVC, filtros HEPA y gabinetes
de bioseguridad clase II o III. Las instalaciones deben estar preparadas para el
trabajo con agentes como Micobacterias y Micoplasmas.
NIVEL 4:
Las instalaciones del laboratorio estn preparadas para el trabajo
con agentes extremadamente peligrosos, para los que no existen tratamientos o
vacunas disponibles. Todo tipo de trabajo se realiza al interior de gabinetes de
bioseguridad de Clase III, con ropas o trajes de aislamiento. La planta fsica tiene
aislamiento total del ambiente y el acceso alto nivel de control. Los agentes que
all se manejan son generalmente virales (virus de fiebres hemorrgicas).
Podemos plantear la existencia de un quinto nivel de bioseguridad para el
almacenamiento y estudio de agentes creados por la ingeniera gentica, agentes biolgicos
destinados a uso blico, agentes de biologa desconocida o agentes que han sido erradicados de la
vida libre, para los cuales no se han descrito tratamientos de ningn tipo y que podran tener
efectos catastrficos en la humanidad.
13
FACULTAD DE CIENCIAS MDICAS
Manual de Laboratorio de Microbiologa
Accidentes de bioseguridad en el laboratorio de microbiologa:
Los accidentes de bioseguridad que originan contaminacin del ambiente o de nuestro
cuerpo pueden ocurrir generalmente por falta de conocimiento o destreza, no usar medidas de
barrera, mantenimiento deficiente de aparatos o gabinetes, falta de capacitacin, y relajacin en
las medidas de control.
Las vas de infeccin en este tipo de accidentes son por inhalacin, ingestin o percutnea.
Acciones como el trabajar sin guantes al manipular muestras o cultivos, pipeterar directamente
con la boca, olfatear cultivos, no usar mechero para generar un rea protegida, pasarse los
guantes usados por la piel, el pelo o la ropa, comer en el laboratorio, no lavarse las manos al
terminar la actividad, constituyen un riesgo de contaminacin y eventualmente de infeccin con
agentes biolgicos, tanto para el alumno como para la comunidad.
En el caso de ocurrir cualquiera de estos accidentes que implique contacto con agentes
biolgicos, el alumno DEBE AVISAR DE INMEDIATO AL PROFESOR. NO ACTUAR POR INICIATIVA
PROPIA.
Ejercicios de Aplicacin de Contenidos
1.- Un sujeto liber el contenido de un frasco con caldo de cultivo de Vibrio cholerae en un
canal de regado de hortalizas. Responde lo siguiente:
Seala dos amenazas evidentes en este hecho:
Qu clases de amenazas son, de acuerdo a los hechos?
2.- La cepa de Vibrio cholerae result no poseer el gen que codifica la enterotoxina. De
acuerdo a los hechos y antecedentes, asigna un valor objetivo y una categora al riesgo (alto,
medio, bajo). Da dos fundamentos para tu respuesta:
3.- El profesor le entreg a los alumnos del ramo de microbiologa unas placas de cultivo
con Escherichia coli, Streptococcus pyogenes y Neisseria meningitidis.
Averigua respecto del potencial patgeno de estos agentes y ordnalos segn peligro de la
amenaza, de menor a mayor.
-
14
FACULTAD DE CIENCIAS MDICAS
Manual de Laboratorio de Microbiologa
4.- Aparte de los microrganismos, hay otras amenazas latentes en el enunciado, disctelas
con otros alumnos y responde cules son.
5.- Cul es la categora de riesgo que asignaras a un grupo de escolares que tiene a un
compaero de curso con meningitis meningoccica, el que ha sido diagnosticado como caso
ndice?
Anota tus fundamentos.
6.- La cepa de Neisseria meningitidis del caso anterior ha sido aislada y referida al Instituto
de Salud Pblica (ISP) mediante protocolo de notificacin obligatoria. Cul ser la categora de
riesgo para el microbilogo del ISP que trabaja con esta cepa, si est en un laboratorio de Nivel III?
Dale valor numrico al riesgo y fundamenta.
7.- Averigua un poco antes de responder, luego propone un nivel de bioseguridad para
trabajar con los siguientes agentes o muestras:
- Determinacin de anticuerpos anti VIH
- Urocultivo
- Micobacterium avium
- Vibrio cholerae biotipo El Tor
- Virus EBOLA
- Bacillus pumilus
- Variola virus
- Alternaria solani
8.- Hoy recibiste el honor de ser nombrado Jefe del Comit de Infeccin Intrahospitalaria.
La Enfermera Jefe del establecimiento te ha solicitado una medida urgente para evitar los
desplazamientos innecesarios del pblico dentro del establecimiento por el riesgo de introduccin
de agentes infecciosos. Qu medida propones, cmo la implementas? Seguramente ya estuviste
en algn hospital y viste la aplicacin, trata de acordarte.
Soy una amenaza permanente, no lo olvides.
15
FACULTAD DE CIENCIAS MDICAS
Manual de Laboratorio de Microbiologa
Ejercicios de Laboratorio
Actividad n1:
El ambiente y las personas como generadores de riesgo biolgico
Objetivos:
Observar la existencia de agentes microbianos en el ambiente
Determinar la importancia de la manipulacin en la transmisin de
agentes infecciosos
Valorar el lavado de manos como medida de barrera
Determinar la importancia de la mascarilla como medida de
barrera.
Material y Mtodo:
36 Placas Petri con Agar Sangre en Base Columbia, mascarillas, jabn y agua.
Trabajar en tres grupos de cinco personas.
El mtodo de trabajo es por simple exposicin de material estril o mediante contacto
con material estril.
Grupo 1: Exponer una placa de agar al ambiente, sobre el mesn, durante diez
minutos. Colocar los dedos suavemente sobre el agar durante 30 segundos. Cerrar y
rotular.
Grupo 2: Dos alumnos deben realizar lo siguiente: manipular objetos durante tres
minutos, luego colocar suavemente los dedos sobre el agar.
En seguida, el mismo deber lavarse las manos con el jabn disponible durante tres
minutos, luego debe dejar secar al aire. Colocar suavemente los dedos sobre el agar.
Cerrar y rotular.
Grupo 3: Un alumno deber leer un texto en voz alta frente a una placa abierta,
durante dos minutos. Otro repetir lo mismo utilizando mascarilla.
Cerrar y rotular.
Incubar 48 hrs a 30C, atmsfera aerobia. Refrigerar y observar los resultados en el
paso prctico siguiente.
Discute los resultados con el profesor y tus compaeros.
Anota tus conclusiones:
16
FACULTAD DE CIENCIAS MDICAS
Manual de Laboratorio de Microbiologa
Actividad n2:
Las manos, una eficaz forma de transmitir enfermedades.
Objetivos:
Evaluar la cantidad de bacterias que portamos en nuestras manos.
Comprender el riesgo de transmisin de microrganismos mediante
manipulacin.
Valorar el lavado de las manos como medida de barrera.
Material y Mtodo:
500 mL de Caldo Peptonado estril, envasado en recipientes de boca ancha.
Pipetas estriles
Placas Petri estriles, sin medio de cultivo
Agar Nutritivo standard, envasado en tubos para fundir.
Gradillas.
El mtodo de trabajo consiste en obtener una muestra de un enjuague de manos y
realizar un recuento de las bacterias aerbicas mesfilas viables, luego calcular el nmero
total de bacterias en la mano.
Cada grupo de cinco alumnos trabaja de la siguiente forma:
1. Introducir toda la mano en el recipiente de Caldo
Peptonado estril, realizar friccin con los dedos durante 1 minuto. Retirar
"Todo lo que aqu se
la mano y dejar esta preparacin en reposo por 10 minutos al ambiente,
hace me parece muy
intil; los
con el recipiente tapado.
fallecimientos se
suceden de la forma
2. Fundir dos tubos con Agar Nutritivo Standard en un
ms simple. Se
vaso
de
pp.
con
agua corriente mediante ebullicin. Una vez fundido,
contina operando,
sin embargo, sin
retirar del calor y esperar a que se tempere a la temperatura que soporta
tratar de saber
verdaderamente por
la mano (40 a 45C).
qu tal enfermo
3. Con una pipeta estril, tomar una muestra de 0,5 mL
sucumbe antes que
otros en casos
del
Caldo
Peptonado
en que hicimos el lavado de manos, y colocarlo en el
idnticos".
centro de la placa de Petri. Repite en otra placa.
Ignacio Felipe
4. Agregar cuidadosamente a las dos placas el Agar
Semmelweis
(1818 -1865)
Nutritivo fundido y mezclar con las muestras mediante movimientos
rotarios suaves. Dejar solidificar en la superficie del mesn sin mover.
5. Una vez slido rotular e incubar por 48 hrs. a
temperatura ambiente. Refrigerar hasta el paso prctico siguiente.
6. Con un lpiz marcador permanente, dividir las placas
en cuatro cuadrantes por el lado del agar. Contar el nmero de colonias
presentes en todos los cuadrantes. Cuenta la otra placa y promedia. Esto
representa la cantidad de bacterias vivas en la muestra de 0,5 mL.
7. Calcula ahora la cantidad de bacterias en la mano, plantea una frmula
matemtica de estimacin del total y disctela con tus compaeros.
8. Registra tus resultados, plantea un debate con estas observaciones.
17
FACULTAD DE CIENCIAS MDICAS
Manual de Laboratorio de Microbiologa
Desinfeccin y Antisepsia
Bien lo estableci Ignacio Semmelwies (1818-1865) al observar que el uso de ciertos
agentes qumicos para sanitizar las manos poda reducir las tasas de infecciones asociadas a la
atencin mdica, en tanto que Joseph Lister (1827-1912) demuestra que el tratamiento trmico
aplicado a instrumentales es una medida eficaz para disminuir las infecciones post quirrgicas. En
esta poca, Louis Pasteur (1822-1895) recin est demostrando la presencia de microrganismos en
el ambiente, capaces de producir putrefaccin y asocindolos a la ocurrencia de enfermedades
infecciosas.
Queda claro entonces, que la accin de agentes fsicos y qumicos es til en la contencin
de las enfermedades infecciosas. De esta afirmacin se desprenden los conceptos de
DESINFECCION Y ANTISEPSIA.
Llamaremos DESINFECCIN a la simple descontaminacin de un objeto o superficie de
algo, de la que eliminaremos casi todas las formas vegetativas. Es importante recordar que
pueden existir microrganismos con diversos grados de resistencia a los agentes qumicos
empleados, que el efecto de estos depender de factores como la concentracin, el tiempo de
exposicin, la naturaleza qumica del agente, la temperatura, y finalmente la existencia de
mecanismos de latencia en los microrganismos (esporas bacterianas).
ANTISEPSIA son todos los procedimientos encaminados a reducir al mximo la presencia
de microrganismos sobre los tejidos vivos (piel, algunas mucosas) que estn en contacto con el
ambiente, aplicando mtodos fsicos o qumicos. El propsito de la antisepsia es conseguir la
ASEPSIA, o ausencia de microrganismos.
Los mtodos fsicos o qumicos empleados para la desinfeccin y antisepsia tienen
diferencias fundamentales: el dao estructural (en los mtodos fsicos) y la toxicidad (en los
mtodos qumicos). Un antisptico no debe ser txico ni daar la integridad de los tejidos.
Los efectos de los Desinfectantes y Antispticos pueden ser de dos tipos:
Bacteriostticos:
si slo detienen la proliferacin microbiana,
Bactericidas:
si producen la muerte de los microrganismos.
De acuerdo a los efectos observados, podemos clasificar a estos agentes qumicos como de ALTO
NIVEL, NIVEL INTERMEDIO O BAJO NIVEL.
18
FACULTAD DE CIENCIAS MDICAS
Manual de Laboratorio de Microbiologa
Los microrganismos presentan distintos grados de resistencia a estos agentes, siendo los
ms resistentes Priones y los ms susceptibles Virus con manto o envoltura.
El efecto de cualquier
antisptico o desinfectante puede
verse alterado por la presencia de
suciedad o restos orgnicos. Es
imprescindible retirar todo exceso
de suciedad antes de la aplicacin.
La persistencia de tierra,
restos de alimentos, sangre, pus,
secreciones puede implicar el
aumento de la concentracin o del
tiempo de exposicin al agente
qumico.
La eleccin del desinfectante a usar tiene relacin con el objeto que nos interesa
tratar. Existe una categorizacin de los objetos de uso clnico de acuerdo al riesgo de transmitir
una infeccin mediante su uso.
El efecto desinfectante
deber ser mayor cuando se aplique a
objetos crticos, al punto de lograr la
esterilizacin.
Los agentes qumicos
Que pueden ser usados con efecto
esterilizante sobre objetos crticos son
por ejemplo:
GLUTARALDEHIDO AL 2%
GAS OXIDO DE ETILENO
PEROXIDO DE HIDROGENO
ACIDO PER ACETICO AL 2%
El uso de los materiales tratados con estos agentes qumicos no puede ser
inmediato debido a su elevada toxicidad, por lo que el proceso de preparacin considera un
tiempo de disipacin.
19
FACULTAD DE CIENCIAS MDICAS
Manual de Laboratorio de Microbiologa
El efecto de los agentes qumicos sobre los microrganismos:
Los agentes qumicos empleados con fines de desinfeccin y antisepsia, como tambin los
empleados con fines teraputicos (antimicrobianos), actan sobre los micro organismos con la
finalidad de producir una disminucin de la carga bacteriana mediante la eliminacin de las formas
vegetativas (bactericidas), impidiendo la multiplicacin bacteriana (bacteriostticos) o
definitivamente eliminando toda tipo de forma de vida microbiana (esterilizantes).
El efecto bactericida, bacteriosttico o esterilizante depender de los siguientes factores:
Tipo de agente qumico empleado:
o Alcoholes: etanol o isopropanol al 70%
o Alquilantes: Formaldehdo, xido de etileno
o Halogenantes: Hipoclorito, Yoduros
o Surfactantes: compuestos de amonio cuaternario, jabones, triclosn.
o Oxidantes: xido de etileno, perxido de hidrgeno, cido peractico.
o Compuestos fenlicos:
Hexaclorofeno, Clorhexidina.
Concentracin y Tiempo de accin:
o La eficacia de un agente qumico
aumenta con la concentracin y el
tiempo de exposicin.
Naturaleza del microrganismo:
o Los virus sin envoltura son ms resistentes que los con envoltura.
o Los micro organismos Gram negativos tienden a ser ms resistentes que
los Gram positivos a los agentes qumicos,
o Son especialmente resistentes las bacterias que forman endosporas.
o A mayor cantidad de micro organismo, mayor necesidad de concentracin
o tiempo de exposicin del agente qumico.
Objeto u objetivo de aplicacin:
o Los desinfectantes se pueden aplicar sobre objetos o superficies
inanimadas, la concentracin y el tiempo de exposicin dependern de la
resistencia al efecto corrosivo.
o Los antispticos son por definicin de baja toxicidad, y se aplican sobre
tejidos vivos (piel y algunas mucosas) en concentraciones bajas y por
tiempo limitado.
20
FACULTAD DE CIENCIAS MDICAS
Manual de Laboratorio de Microbiologa
Temperatura de aplicacin
o En general, los efectos sobre una poblacin microbiana aumenta con la
temperatura
pH de la solucin
o El pH adecuado depender de la naturaleza aninica o catinica del
agente qumico. En general, el efecto del pH se relaciona con la capacidad
de ionizacin tanto del agente qumico como de las envolturas celulares
de los micro organismos, por facilitacin del transporte de iones en
solucin acuosa a travs de las estructuras de envoltura.
Presencia de sustancias interferentes:
o Los desinfectantes pueden perder su eficacia por contacto con materia
orgnica contaminante: sangre, secreciones, deposiciones, restos de
alimentos, xidos.
o Los antispticos tambin pierden eficacia si se aplican sobre la piel sucia.
Los efectos de estos agentes qumicos se verifican sobre las estructuras de las protenas
funcionales y estructurales de los microrganismos, y sobre los cidos nucleicos. Lo anterior implica
alteraciones en la funcin metablica, en la estructura y permeabilidad de la membrana celular, y
en la replicacin del material gentico.
De acuerdo a su eficacia,
podemos categorizar a estos
agentes qumicos en tres niveles de
accin.
Los agentes de bajo nivel
tienen efecto limitado, y no
garantizan
una
adecuada
sanitizacin. Pueden encontrarse al
alcance del pblico como jabones o
soluciones germicidas de venta
libre.
Los agentes de nivel intermedio tienen mejor efecto, pero no logran la eliminacin de
esporas. Se encuentran en este grupo a los alcoholes, los derivados fenlicos, los halogenantes
como el cloro y yodo, y el perxido de hidrgeno en baja concentracin.
Los agentes qumicos de alto nivel son muy txicos, por lo que no se usan como
antispticos sino como desinfectantes o esterilizantes dependiendo de su concentracin o
toxicidad. En este grupo podemos citar al glutaraldehido, cido peractico, xido de etileno,
plasma de perxido de hidrgeno.
21
FACULTAD DE CIENCIAS MDICAS
Manual de Laboratorio de Microbiologa
Caballeros, yo pudiera sealar a ese lquido [estril] y decirles: He tomado mi
gota de agua de la inmensidad de la creacin, y la he tomado llena de los
elementos convenientes para el desarrollo de seres inferiores. Y espero, observo,
inquiero de ella, suplicndole que comience de nuevo para m el hermoso
espectculo de la primera creacin. Pero est muda... muda desde el mismo
comienzo de estos experimentos hace varios aos; est muda porque la he
mantenido alejada de la nica cosa que el hombre no puede producir de los
grmenes que se alimentan en el aire de la vida, porque la vida es un germen y
un germen es vida. Nunca se recobrar la doctrina de la generacin espontnea
del golpe mortal de este sencillo experimento.
Louis Pasteur. 18221822-1895
Efectos de factores de orden fsico sobre los microrganismos
La actividad biolgica tambin puede verse alterada por efecto de factores de orden fsico.
La simple accin mecnica de arrastre, la abrasin, la desecacin y el efecto de la luz solar actan
en forma natural sobre los microrganismos.
No obstante lo anterior, la humanidad ha desarrollado tecnologas que permiten manejar
los factores fsicos para aprovecharlos con el objeto de descontaminar y esterilizar. En este
sentido, son conocidas las aplicaciones de temperaturas (especialmente calor), presin y
radiaciones (luz ultravioleta de onda corta, radiacin gamma).
Los factores de orden fsico tienen los siguientes efectos sobre los microrganismos:
1.- Efecto de la temperatura:
El fro por lo general tiene efecto bacteriosttico, por lo que muchas bacterias pueden
recuperar su actividad si se les regresa a su temperatura vital ptima. En muchas de las especies
bacterianas se observa alguna capacidad de tolerar el congelamiento, resistiendo a la formacin
de cristales de hielo en el citoplasma. Esta capacidad de resistencia aumenta cuando estos
organismos se encuentran en un medio rico en protenas o carbohidratos.
Por el contrario, los efectos del calor pueden ser bactericidas ya que se verifican sobre las
protenas estructurales o funcionales de los microrganismos. En la medida que aumentamos la
exposicin al calor por sobre los rangos de tolerancia vital de una especie bacteriana, comienza a
ocurrir alteracin irreversible de la arquitectura proteica, lo que implica un colapso estructural y
funcional. En las bacterias de importancia mdica las formas vegetativas, es decir, las que son
aptas para el metabolismo y reproduccin resultan destruidas con la exposicin a temperaturas
22
FACULTAD DE CIENCIAS MDICAS
Manual de Laboratorio de Microbiologa
cercanas al punto de ebullicin del agua, condicin que solo pueden resistir las esporas
bacterianas.
Efecto del aumento de la temperatura sobre una
poblacin bacteriana.
El aumento de la temperatura por sobre el ptimo
necesario para actividad vital (rango trmico)
conduce a un rpido colapso biolgico.
Diferentes bacterias a distintas temperaturas:
A travs de la evolucin las bacterias han desarrollado adaptaciones para la vida a diversas
temperaturas, por lo que podemos clasificarlas como:
Bacterias msfilas, si su actividad vital se desarrolla a temperaturas entre 25 y
45C, lo que incluye a las patgenas para el ser humano.
Bacterias psicrfilas, si mantienen actividad entre los 0 y 20C. En este grupo se
encuentran microrganismos capaces de descomponer alimentos durante la
refrigeracin. Algunos patgenos mesfilos pueden tolerar este rango de
temperatura (Staphylococcus aureus y Listeria monocytogenes). Un subgrupo
capaz de tolerar temperaturas algo mas altas son denominadas psicrotrofas.
Bacterias termfilas, si viven entre 50 y 70C. Un subgrupo denominado
hipertermfilas es capaz de sobrevivir a temperaturas tan altas como 70 a 110C.
De acuerdo a esta clasificacin, cada especie bacteriana es capaz de vivir en un margen de
temperatura denominado RANGO TRMICO, que tiene una amplitud cercana a 35C.
Margen de crecimiento para distintos
grupos bacterianos
En Staphylococcus aureus y Listeria
monocytogenes estos mrgenes tienen
mayor amplitud.
23
FACULTAD DE CIENCIAS MDICAS
Manual de Laboratorio de Microbiologa
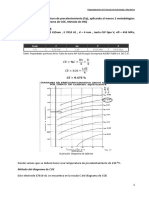
El tiempo en el que se verifica el efecto letal del calor sobre una poblacin bacteriana
tiene relacin inversa con la cantidad de calor aplicada. En otras palabras, para un efecto ms
rpido se requiere mayor temperatura.
A este valor de tiempo se le llama TIEMPO DE
REDUCCIN DECIMAL (D), y corresponde al tiempo
necesario para dejar solo el 10% de sobrevivientes de
una especie bacteriana al aplicarle un tratamiento
bactericida fsico o qumico.
En este grfico, para una especie bacteriana x,
se logra dejar el 10% viable en 12 minutos a 60C. Si se
contina a la misma temperatura, el 0,1% sobrevive a
los 40 minutos.
Si fijamos la temperatura, el valor D es dependiente de la especie bacteriana: Si tratamos
a una especie bacteriana x a 60C obtenemos un valor D de 12 minutos, si aplico el mismo
tratamiento a la bacteria y puedo obtener un valor D diferente.
Esto introduce dos nuevas definiciones:
TIEMPO TRMICO MORTAL, que es el tiempo mnimo necesario para inactivar el 100% de
una poblacin bacteriana dada a una temperatura constante.
PUNTO TRMICO MORTAL, que es la temperatura mnima necesaria para inactivar
totalmente una poblacin bacteriana en un tiempo fijo de 10 minutos.
Con estos tres conceptos se definen las condiciones ideales para la esterilizacin mediante
calor, o del tratamiento de alimentos para la mxima reduccin de la carga bacteriana sin
alteracin de sus propiedades.
Si nos fijamos en el cuadro anterior, existen especies bacterianas que requieren
tratamientos trmicos por sobre la temperatura de ebullicin del agua, ya que poseen esporas. La
mejor forma de lograr el efecto de inactivacin de estos microrganismos sin alterar los materiales
es combinar calor, agua y presin, en un sistema cerrado y controlado que conocemos como
AUTOCLAVE.
24
FACULTAD DE CIENCIAS MDICAS
Manual de Laboratorio de Microbiologa
La aplicacin calor y vapor bajo
presin realizada en el autoclave es uno
de los procedimientos de esterilizacin
ms utilizados en la preparacin de
materiales para la medicina, ya que
asegura en forma eficiente la eliminacin
de formas vegetativas y de resistencia
(esporas) de todo tipo de microrganismos,
a la vez que destruye virus y priones.
Este proceso es fcil de controlar, es rpido
y eficaz.
Esporas de Bacillus anthracis, Tincin de Gram 1500x
En general, los materiales a tratar mediante autoclavado se exponen durante 15 minutos a
121C, sin embargo este standard puede variar en funcin del volumen de materiales a tratar o de
la naturaleza de estos, de modo que siempre se debe considerar el tiempo necesario para que el
ncleo de los paquetes de materiales alcance la exposicin necesaria, o para que los agentes
microbianos alcancen el tiempo trmico mortal.
2.- Efectos de las radiaciones:
La radiacin es una propagacin de energa en forma de ondas electromagnticas de
distinta longitud. Llamaremos longitud de onda a la distancia que hay entre dos puntos mximos
o mnimos de ella (ver figura). De acuerdo a las distintas longitudes de onda de las radiaciones,
estas se agrupan en el ESPECTRO ELECTROMAGNETICO de emisin/absorcin.
En este ordenamiento podemos situar en
el extremo de ondas ms largas a la
radiacin infrarroja caracterizada por la
emisin
de
calor,
y
en
el
extremo de ondas ms cortas a los rayos
csmicos. Entre este amplio rango de
frecuencias podemos encontrar a la luz
visible, los rayos X y los rayos gamma.
25
FACULTAD DE CIENCIAS MDICAS
Manual de Laboratorio de Microbiologa
Amplitud del espectro electromagntico
La aplicacin de calor con fines bactericidas es esencialmente una forma de aplicacin de
radiacin, no obstante tenemos otras alternativas de aplicaciones bactericidas de las ondas
electromagnticas, tales como la luz ultravioleta (UV) de onda corta (Luz UVC) y la radiacin
gamma.
La cantidad de energa transmitida por la onda es directamente proporcional a su longitud,
y esta cantidad de energa es capaz de producir cambios en los cuerpos que la absorben. De esta
forma, las ondas de baja energa como la luz visible y UV provocan cambios qumicos NO
IONIZANTES. En la medida que aumentamos la energa en la radiacin esta se hace ms
penetrante y los efectos se tornan IONIZANTES, capaces de causar la muerte celular.
La Luz Ultravioleta (UV):
Con una longitud de onda un poco ms corta que la luz visible, se sita en este espectro a
la luz ultravioleta (UV). Todos hemos sentido los efectos de la luz UV de onda larga UVA cuando
nuestra piel se expone a la luz solar y se broncea; con algo ms de energa la luz UVB la exposicin
prolongada es capaz de causarnos dao en la piel, y eventualmente alteraciones celulares.
Afortunadamente la atmsfera con su capa de ozono nos protege de los mortales rayos de la luz
UVC que proviene del sol, ya que estos poseen una mayor capacidad de penetracin y de dao por
ionizacin.
Todos los compuestos qumicos tienen la propiedad de absorber energa en forma de
alguna determinada longitud de onda relacionada con su estructura molecular. Este principio
permite utilizar a la luz UVC con fines bactericidas debido a que la longitud de onda de esta luz
26
FACULTAD DE CIENCIAS MDICAS
Manual de Laboratorio de Microbiologa
(283 a 200 nm) es coincidente con el mximo de absorcin de la molcula de ADN y ARN (260 nm)
y con los mximos de absorcin de las protenas (280 y 230 nm).
Los fotones de alta energa emitidos por una
fuente de luz UVC son capaces de romper enlaces de
las bases nitrogenadas pirimdicas (Citosina C, y Timina
T) del ADN bacteriano, generando FOTOPRODUCTOS
qumicos que imposibilitan la correcta replicacin o
transcripcin de la informacin gentica, por ejemplo,
dmeros anmalos de T-T o C-C.
En las protenas, estos fotoproductos se originan por la alteracin de aminocidos
aromticos (Triptofano, fenilalanina, tirosina), o por ruptura de los enlaces peptdicos. Ambos
efectos causan alteraciones de la estructura y funcionalidad proteica.
De esta forma, la energa de los fotones UVC causa efectos mutagnicos secundarios o
efectos letales por inactivacin del material gentico. A pesar de esto, existen bacterias con la
capacidad de reparar los efectos de la luz UVC mediante mecanismos enzimticos inducibles.
Aplicaciones de la Luz UVC:
La luz UVC tiene aplicaciones bactericidas eficaces en la esterilizacin del aire, agua y
superficies, siempre y cuando la dosis de energa que reciben las bacterias sea la adecuada.
Debemos recordar que la cantidad de energa disminuye con respecto al cuadrado de la distancia
de la fuente de emisin, y que la cantidad de energa emitida depende de la potencia de la fuente.
Una lmpara UVC de Hg de 40 W de potencia es eficaz a un metro de distancia, en tiempos de
exposicin de segundos, inactivando cerca del 99% de las formas vegetativas bacterianas.
Dosis de energa de Luz UVC para efecto letal en algunos agentes infecciosos
Microorganismo
Esporas de Bacillus subtilis
Legionella pneumophyla
Virus de la Hepatitis A
Salmonella typhi
Staphylococcus aureus
Escherichia coli
Virus de la Influenza
Streptococcus sp.
Dosis letal en W/cm
22.000
12.300
8.000
7.000
6.600
6.600
6.600
3.800
Podemos instalar una fuente de emisin de luz UVC asociada a sistemas de purificacin de
agua, o de purificacin de aire filtrado o acondicionado, como medida de barrera para mejorar la
calidad sanitaria del ambiente. Ejemplo de esto es la aplicacin de luz UVC para la inactivacin de
27
FACULTAD DE CIENCIAS MDICAS
Manual de Laboratorio de Microbiologa
Legionella pneumophila en sistemas de acondicionamiento de aire, ya que este patgeno tiene
como reservorio el agua de condensacin que se forma en estos equipos.
La luz UVC es invisible al ojo humano, las
fuentes de emisin UVC se ven iluminadas
con una luz celeste a o luz parsita de
mayor que corresponde a solo el 2 a 5%
de la emisin.
Equipo de aire acondicionado con trampa de Luz UVC
Por lo anterior, las fuentes de emisin UVC
son peligrosas, capaces de provocar
quemaduras en la piel y dao irreversible
en los ojos.
La Radiacin Gamma:
La radiacin gamma es un tipo de energa electromagntica caracterizada por la emisin
de fotones producto de la desintegracin de elementos radiactivos (isotopos) como Co60 y Cs137.
Esta radiacin es muy penetrante debido a su alto nivel de energa, y sus efectos son IONIZANTES.
La radiacin gamma realiza su accin mediante el choque de los fotones de alta energa
con los tomos del material que los recibe.
Los efectos de la ionizacin de la radiacin gamma pueden alterar significativamente el
material gentico, causando la muerte celular. Estos efectos pueden ser de tres tipos:
Efecto letal directo: ruptura de enlaces de bases nitrogenadas y entrecruzamiento
de las hebras de ADN. Ocurre con exposicin a altas dosis de radiacin.
Efecto letal indirecto, por ionizacin de las molculas de agua (radiolisis del agua).
Este efecto libera grandes cantidades de H+ y grupos hidroxilo OH-. Los radicales
OH- pueden combinarse con el ADN o con el oxgeno libre para generar perxidos
(H2O2) que actan oxidando los componentes de la estructura bacteriana.
Efecto mutagnico: causado por dosis menores de radiacin, genera alteraciones
en el ordenamiento del ADN bacteriano y originando replicaciones y
transcripciones alteradas.
Los efectos sern mayores dependiendo del aumento de la dosis de radiacin. La radiacin
absorbida se mide en unidades RADS o Gigaray (Gy). La capacidad de las bacterias para soportar la
radiacin puede ser muy variable, pero bastante mayor que la del ser humano. La dosis letal de
radiacin para un humano adulto es cercana a los 10 Gy, en tanto que para las bacterias vara
entre 200 Gy y 3000 Gy. Existen especies bacterianas capaces de soportar niveles de radiacin de
5000 o ms Gy (5000 Gy es 5 kGy).
28
FACULTAD DE CIENCIAS MDICAS
Manual de Laboratorio de Microbiologa
Esterilizacin:
Como ya hemos visto, existen varios procesos que pueden afectar la viabilidad de los
microrganismos. Podemos distinguir aquellos destinados a disminuir la carga microbiana como lo
son la desinfeccin o antisepsia si es por mtodos qumicos, y la pasteurizacin si es por mtodos
fsicos mediante tratamiento trmico. La esterilizacin en cambio tiene efectos letales sobre toda
forma de vida.
Se entiende por esterilizacin todos los procesos fsicos, qumicos (o combinaciones de
stos) que tienen como propsito erradicar toda forma de vida, incluyendo esporas, virus y
priones. La esterilizacin es esencialmente un concepto radical.
Cualquiera sea el proceso que elijamos para tratar nuestros materiales, debe tener como
requisito la eliminacin de las formas ms resistentes de vida (ver pgs. 18-23-27), sin alterar la
estructura o las propiedades de los materiales. Por lo tanto, la esterilizacin es el RESULTADO
FINAL DEL PROCESO, y no la mera exposicin a los agentes qumicos o fsicos. En este proceso se
cuentan adems una serie de etapas previas tendientes a asegurar el xito, tales como
descontaminacin, inspeccin, preparacin y empaque de materiales, exposicin al proceso,
almacenaje y despacho de estos.
Procesos qumicos de esterilizacin:
Consisten en la aplicacin de agentes qumicos como gas Oxido de etileno (ETO), vapores
de formaldehido, o gas-plasma de perxido de hidrgeno asociados a bajas temperaturas (50a
60C) en una cmara de tratamiento de control automtico. Los objetos a tratar son plsticos con
capacidad de resistir algo de temperatura, ltex, gomas o polmeros, o instrumentos sensibles a
altas temperaturas y humedad. Ejemplos de materiales a tratar son: sondas, endoscopios diversos.
Parmetros de esterilizacin para Gas de ETO:
Temperatura
35C
55C
Tiempo una vez alcanzada la temperatura, humedad
sobre el 40% y presin del gas entre 450 y 740 mg./lt.
5 hrs.
2,5 hrs.
Algunos agentes qumicos pueden aplicarse como solucin. El glutaraldehido al 2%
aplicado durante 20 a 30 minutos y el cido peractico al 0.2% durante 15 minutos a 55C, luego
de enjuagado con agua estril permite la esterilizacin de plsticos y gomas termosensibles, y
metales sensibles al calor.
29
FACULTAD DE CIENCIAS MDICAS
Manual de Laboratorio de Microbiologa
Procesos fsicos de esterilizacin:
Estos procesos emplean factores como la exposicin a calor o radiaciones.
Destaca en este tipo de procesos el AUTOCLAVADO, tratamiento de materiales resistentes
al calor mediante la exposicin a vapor a alta presin. Los materiales que pueden someterse a este
proceso son por ejemplo: ropas, gasas, vendas, plsticos resistentes al calor, instrumental
quirrgico, vidrio, y algunas soluciones.
El standard de tratamiento es de 15 minutos a 121C, pero puede variar en funcin de la
carga de materiales en el autoclave, de la naturaleza de stos y del tamao de los paquetes. Un
paquete de gran volumen requiere mayor tiempo de exposicin para lograr que el ncleo del
material alcance la temperatura durante el tiempo necesario. Es posible reducir el tiempo de
tratamiento aumentando la temperatura en el proceso. Observa la tabla siguiente, que relaciona
tiempo, temperatura y presin:
Tiempo desde que alcanza temperatura y
presin
15 minutos
10 minutos
3 minutos
Temperatura
Presin
121C
126C
134C
1,5 Atm.
2,0 Atm.
2,9 Atm.
En la siguiente tabla podrs observar distintas modalidades de procesos de esterilizacin:
Material
Lquidos
Algodones
Artculos de goma
o ltex
Algodn y gasas
Siliconas
Plsticos
Acero inoxidable
Aluminio
Maderas
Vidrios
Aceites y
petrolatos
Mtodo de
esterilizacin
Parmetros de
esterilizacin
Autoclave
Autoclave
Autoclave
134 o 135 C
134 o 135 C
121C
Autoclave
Autoclave
Oxido de etileno
Plasma Formaldehdo
Formaldehdo
134 o 135 C
121C
37 - 55C
50C
Autoclave
Estufa por calor seco
Autoclave
Estufa por calor seco
Autoclave
Autoclave
Estufa por calor seco
Estufa a calor seco
50 60C
134 o 135C
180C
134 o 135C
180C
134 o 135C
134C
160 180C
180C
Consideraciones
Equipo con ciclo de lquidos
De preferencia utilizar
soluciones estriles de
fbrica
30
FACULTAD DE CIENCIAS MDICAS
Manual de Laboratorio de Microbiologa
La esterilizacin mediante vapor a alta presin es un proceso seguro y rpido, que adems
implica menor consumo de energa.
Otra alternativa de tratamiento trmico para lograr la esterilizacin es la exposicin a calor
seco, para lo que se utiliza el equipo comnmente conocido como PUPINEL, que puede funcionar
mediante conveccin de aire caliente, sea de tipo gravitatoria o mecnica. En este tipo de equipo,
el standard de aplicacin del proceso consiste en elevar la temperatura de la cmara hasta 180C,
luego un perodo de exposicin mnimo de 30 minutos y finalmente un tiempo de enfriado. Con
todo, este proceso puede tener un ciclo total de unas tres horas y consume gran cantidad de
energa elctrica. Igualmente, el tiempo de exposicin es dependiente de la temperatura:
Temperatura
180C
170C
Tiempo desde que se alcanza la
temperatura
30 minutos
60 minutos
160C
150C
140C
121C
120 minutos
150 minutos
180 minutos
360 minutos
Los materiales que pueden esterilizarse mediante calor seco son polvos (talco), aceites,
petrolato, vaselina, los que no son aptos para tratamiento en autoclave. Este tipo de tratamiento
daa el templado del acero quirrgico y puede provocar carbonizacin en textiles.
Control de los procesos y aseguramiento de calidad:
Desde el punto de vista de la bioseguridad, los procesos de esterilizacin deben ser sujetos
de certificacin. Esta condicin implica poder auditar y trazar toda la aplicacin del proceso, desde
la recepcin de los materiales hasta el usuario final, de modo de poder garantizar la inocuidad de
los materiales sometidos a esterilizacin.
Para efecto del control del proceso, se aplican INDICADORES DE ESTERILIZACIN:
Indicadores Fsicos
En cada ciclo de Esterilizacin
Indicadores Qumicos
Indicadores Biolgicos
En cada paquete a esterilizar.
1.- Semanal en todos los equipos de
esterilizacin
2.- En todas las cargas que contienen
implantes
3.- Despus de cada reparacin del
equipo
Los indicadores fsicos son los manmetros, termmetros, higrmetros y registros
emanados de los equipos, y no estn a la vista del usuario final de los materiales.
31
FACULTAD DE CIENCIAS MDICAS
Manual de Laboratorio de Microbiologa
Los Indicadores qumicos pueden observarse en todos los paquetes de materiales
sometidos a esterilizacin, deben estar siempre a la vista del usuario quin debe observar el viraje
del indicador a modo de control visual.
Estos indicadores son sustancias que
cambiarn de color cuando se alcance la
temperatura de tratamiento, o la concentracin
del agente esterilizante. En ningn caso garantizan
el cumplimiento del proceso completo.
Los indicadores biolgicos son la garanta ms segura
de la eficacia del proceso, ya que consisten en dispositivos que
contienen bacterias vivas seleccionadas para el control de
esterilizacin, las que deben resultar inactivadas. El usuario de
materiales estriles no tendr a la vista este tipo de controles,
pero puede consultar la validacin del proceso mediante certificados.
Como conducta segura antes de utilizar un material supuestamente estril, debemos
observar que el envoltorio (envase) est siempre indemne, que tenga la fecha de aplicacin del
proceso y de vencimiento, y que el viraje de los indicadores qumicos sea categrico.
Ernst von Bergmann
(1836 -1907)
En 1896, el cirujano alemn Ernst von
Bergmann, creador del concepto de asepsia
quirrgica, introduce el uso del autoclave,
aparato que utiliz en forma permanente para
aplicar calor bajo presin en el tratamiento de
la ropa para ciruga.
32
FACULTAD DE CIENCIAS MDICAS
Manual de Laboratorio de Microbiologa
Eleccin del proceso adecuado:
Como hemos visto, existe una gran variedad de procesos posibles para lograr la
esterilizacin, la eleccin del ms adecuado depender del tipo de materiales a tratar, de la
toxicidad residual, de la eficacia del proceso y de la economa de su aplicacin. A modo de gua
comparativa puedes observar la siguiente tabla (se excluye la radiacin ionizante):
Ventajas y limitaciones de los distintos mtodos de esterilizacin
Mtodo
Autoclave a vapor
Calor seco
Ventajas
Ciclos ms cortos.
Menor costo de operacin.
Efectivo frente a la eliminacin
de priones.
No presenta toxicidad para el
personal ni para el ambiente.
Certificable.
Equipamiento de menor costo
que el autoclave
Facilidad de operacin de los
equipos
Oxido de etileno
Permite la esterilizacin de
material termosensible
Certificable
Buena penetracin
Plasma
Baja temperatura.
Ciclos de corta duracin.
No txico para las personas ni
para el ambiente.
No requiere instalaciones
especiales
Rpido
Efectivo en la esterilizacin
de endoscopios y
laparoscopios
Equipo automtico
estandarizado
No contamina al medio
ambiente
Baja temperatura.
Ciclos de corta duracin.
Certificable
Acido peractico
lquido
Formaldehdo
Limitaciones
Mtodo no compatible con
Material termosensible.
No elimina pirgenos.
No esteriliza sustancias oleosas ni polvos.
Dao del material por exposicin a
temperaturas elevadas.
Tiempos de exposicin prolongados en
comparacin con la esterilizacin a vapor.
Dificultad en la certificacin del mtodo.
Costos de operacin elevados.
No hay informacin respecto a su
efectividad contra priones
Requieren perodos prolongados de
proceso y aireacin.
No es un mtodo efectivo contra priones
Txico para el personal, pacientes y
ambiente
Incompatibilidad con algunos materiales.
Controversia respecto a su utilizacin en
artculos con lmenes largos entre 1 y 2 mt.
y angostos (entre 1 y 3mm).
No elimina priones
Slo puede ser utilizado para material
sumergible
Esteriliza un solo contenedor por ciclo por
lo que no puede ser utilizado para
cantidades mayores de material
No elimina priones
Debe ser utilizado en forma inmediata
Incompatibilidad con algunos materiales.
Mtodo no aprobado para su utilizacin en
USA
No elimina priones
Puedes obtener mayor informacin en:
www.enfermeraspabellonyesterilizacion.cl/trabajos/plasma.pdf
juridico1.minsal.cl/RESOLUCION_1665_01.doc
33
FACULTAD DE CIENCIAS MDICAS
Manual de Laboratorio de Microbiologa
Ejercicios de Aplicacin de Contenidos
1.- Si para el lavado de manos usas un jabn germicida con amonio cuaternario, Qu nivel
de accin germicida tiene?
2.- Dado el uso mdico del objeto y su riesgo de transmitir agentes infecciosos, Cmo
clasificas a un termmetro?, Cmo lo desinfectas?
3.- Qu agente qumico utilizaras para desinfectar un endoscopio?, Qu nivel de
desinfeccin debe obtenerse?
4.- Un trabajador agrcola debe someterse a hidratacin parenteral urgente. Cul sera la
secuencia de acciones ms correcta al instalar el tratamiento? Nombra los agentes qumicos a
usar.
5.- Qu precauciones deben tomarse antes de usar objetos esterilizados con xido de
etileno?
6.- Qu mtodo de esterilizacin fsico es adecuado aplicar a materiales plsticos
sensibles al calor?
7.- En un evento de intoxicacin alimentaria se determin la presencia de Staphylococcus
aureus en una partida de queso que se mantena en una vitrina refrigerada de un supermercado.
Si la cadena de frio es adecuada, Cul puede ser el generador o reservorio en este evento?,
Qu caractersticas especiales tiene Staphylococcus aureus?
8.- Describe por qu razn el tratamiento standard de esterilizacin por vapor bajo presin
considera una exposicin de materiales durante 15 minutos a 121C y 15 lb de presin.
9.- Explica como la accin de los rayos gamma sobre las molculas de agua afecta
indirectamente a las bacterias.
10.- Explica cul sera tu mtodo de eleccin para la esterilizacin de ropa quirrgica de
algodn.
34
FACULTAD DE CIENCIAS MDICAS
Manual de Laboratorio de Microbiologa
UNIDAD 2
TOMA DE MUESTRAS Y CULTIVO PRIMARIO
35
FACULTAD DE CIENCIAS MDICAS
Manual de Laboratorio de Microbiologa
Ejercicios de Laboratorio
Actividad n3:
Objetivos:
Aislamiento de bacterias a partir de muestras mdicas I.
Practicar la toma de muestra farngea.
Practicar la metodologa de siembra de muestras microbiolgicas
en medios de cultivo slidos.
Reconocer materiales y estrategias de cultivo.
Practicar juego de roles mdico paciente.
Materiales y mtodo: Toma de muestras y siembra de secrecin farngea sobre Agar
Sangre en base Columbia.
Disponer de trulas estriles para toma de muestras, baja lenguas,
guantes, portaobjetos, placas de agar sangre Columbia.
Formar un grupo de trabajo de cinco alumnos.
Toma de muestras:
Explique a su paciente que procedimiento le va a hacer. Use
guantes.
Pdale que abra bien la cavidad bucal y saque la lengua.
Deprima la lengua con un baja lenguas y observe el estado de la
cavidad oro farngea. Busque sitios con signos inflamatorios o la
presencia de pus, especialmente cerca de las amgdalas.
Mientras mantiene la boca abierta y la lengua deprimida, con una
trula estril tome una muestra de secrecin farngea en forma
rpida y precisa, sin daar a su paciente. El procedimiento puede
ser algo molesto.
Siembra:
Disponga de una placa de Agar Sangre Columbia y rote la trula en
un punto perifrico. Luego dibuje una estra sobre el agar con la
misma trula. Descarte la trula en un recipiente con solucin
clorada. Identifique la siembra con el nombre de su paciente y
luego incube a 35 a 37C por 24 horas.
Observe el desarrollo de distintas colonias bacterianas, ponga
atencin a los efectos del desarrollo bacteriano sobre la sangre.
Examen directo:
Este procedimiento es parte integral del examen microbiolgico de
la faringe y es de mucha utilidad, ya que le permitir mediante Tincin de Gram y evaluar
el estado inflamatorio y la presencia de bacterias patgenas. Tome otra muestra farngea
de acuerdo a lo descrito y colquela en el centro de un portaobjetos limpio, mediante
rotacin suave. Reserve para realizar la actividad n 7.
36
FACULTAD DE CIENCIAS MDICAS
Manual de Laboratorio de Microbiologa
Ejercicios de Laboratorio
Actividad n4:
Objetivos:
Aislamiento de bacterias a partir de muestras mdicas II.
Practicar la metodologa de siembra de muestras microbiolgicas
en medios de cultivo slidos.
Reconocer materiales y estrategias de cultivo.
Practicar juego de roles mdico paciente.
Intentar el diagnstico del estado de portador nasal de
Staphylococcus aureus.
Materiales y mtodo: Toma de muestras y siembra de secrecin nasal sobre Agar Sangre
en base Columbia. Los materiales son los mismos de la actividad
n3.
Toma de Muestras:
Explique a su paciente el procedimiento. Use guantes.
Pida al paciente que incline la cabeza ligeramente hacia atrs.
Con una trula estril frote el piso y las paredes de la ventana
nasal. Prepare una lmina para el examen directo.
Siembra:
Tome otra muestra nasal y siembre una placa de Agar sangre
Columbia de acuerdo a lo descrito en la actividad n3. Identifique
con el nombre del paciente y luego incube por 24 horas a 35
37C
Observe el desarrollo de distintas colonias bacterianas, ponga
atencin a los efectos del desarrollo bacteriano sobre la sangre,
especialmente aquellas que presentan pigmento dorado y que
causan aclaramiento (hemolisis) alrededor.
Actividad
hemoltica
(beta
hemolisina)
Staphylococcus aureus sobre Agar sangre Columbia.
de
Los agares sangre sin otros aditivos son
medios de cultivo nutritivos de uso general, y
permiten el desarrollo de la mayora de las
bacterias que no tienen requerimientos
nutricionales especiales. Soportan bin el
crecimiento de las bacterias de la microbiota
normal y de la gran mayora de los patgenos para
el ser humano. Son ejemplos:
Agar sangre en base Columbia
Agar sangre en base Soya Tripticasa
Agar sangre en base Infusin.
37
FACULTAD DE CIENCIAS MDICAS
Manual de Laboratorio de Microbiologa
Ejercicios de Laboratorio
Actividad n5:
Objetivos:
Aislamiento de bacterias a partir de muestras mdicas III.
Practicar la metodologa de siembra de muestras de deposiciones
sobre medios de cultivo slidos.
Reconocer materiales y estrategias de cultivo.
Observar el desarrollo de enterobacterias y su actividad
metablica.
Materiales y mtodo: Toma de muestras en medio de transporte y siembra de
deposiciones sobre Agar MacConkey o Agar XLD (Xilosa-LisinaDesoxicolato).
Toma de muestras:
Siembra:
Use guantes. Tome una muestra de deposiciones con trula estril
y luego introdzcala en un medio de transporte Cary Blair.
Siembre con la trula un punto perifrico sobre Agar MacConkey o
Agar XLD. Vuelva la trula a su envase.
Prepare una lmina para el examen directo, segn lo descrito en la
actividad 3. Cuide de no contaminar.
Esterilice un asa de siembra por incineracin. Espere a que se
enfre y luego realice la siembra SUAVEMENTE de acuerdo a la
figura de la actividad 3.
Identifique con el nombre del paciente e incube 24 horas a 3537C. Despus observe el desarrollo de colonias y comente.
Cultivo de Escherichia coli sobre Agar
MacConkey. Las colonias se observan
rosadas por efecto de la fermentacin de
la lactosa contenida en el medio de cultivo.
El halo de precipitacin que rodea las
colonias se forma por efecto del pH cido
sobre las sales biliares que contiene la
frmula.
38
FACULTAD DE CIENCIAS MDICAS
Manual de Laboratorio de Microbiologa
Cultivo de Escherichia coli sobre Agar XLD.
Las colonias se observan amarillas por
efecto de la fermentacin de la Xilosa,
lactosa y sacarosa. El halo de precipitacin
ocurre por accin del pH cido sobre el
desoxicolato.
Se observan cuatro colonias negras,
productoras de H2S, que pueden
corresponder Proteus sp.
Salmonella typhimurium sobre Agar XLD.
Las colonias se observan negras por la produccin de H2S.
Las especies de Salmonella degradan el aminocido Lisina
(Lisina decarboxilasa), por lo que se produce elevacin del
pH y viraje hacia el rojo.
Los Medios de cultivo Agar MacConkey y Agar XLD son selectivos
para enterobacterias, (Gram negativas que habitan en el intestino)
ya que su composicin contiene sales biliares que inhiben el desarrollo
de bacterias Gram positivas. El Agar XLD tiene mayor concentracin de sales biliares, por lo que su
efecto inhibidor es mayor, y permite una mejor recuperacin selectiva de enteropatgenos como
lo son Salmonella sp. y Shigella sp.
Existen muchas frmulas de medios de cultivo selectivos, la mayora tiene por objeto
facilitar la recuperacin de agentes patgenos por inhibicin de la flora acompaante, por lo que
pueden usarse para la siembra primaria, es decir directamente de la muestra.
Algunos ejemplos de medios selectivos son:
Agar TCBS:
Agar SS:
Agar Thayer Martin:
Agar Baird Parker:
cultivo de Vibrio cholerae
cultivo de Salmonellas y Shigellas
cultivo de Neisseria gonorrhoeae y N. meningitidis
cultivo de Staphylococcus aureus
39
FACULTAD DE CIENCIAS MDICAS
Manual de Laboratorio de Microbiologa
Ejercicios de Laboratorio
Actividad n6:
Objetivos:
Observacin macroscpica de un cultivo y aislamiento de cepas.
Observar la morfologa colonial.
Observar los efectos del desarrollo bacteriano sobre el medio de cultivo
(bioqumica, accin de hemolisinas).
Apreciar la diversidad de la microbiota y sus diferencias.
Practicar el aislamiento a partir de un cultivo de fase slida, mediante asa.
Materiales y mtodo: Use sus cultivos de la actividad n5.
Placas de Agar sangre (cualquier frmula base)
Asas de siembra.
Bioseguridad:
Trabaja con bacterias no identificadas aisladas de humanos, no est
descartada la presencia de patgenos en los cultivos.
No olfatear los cultivos.
Use guantes, mechero encendido.
No exponga los cultivos innecesariamente.
Desarrollo:
- Observe atentamente el cultivo y registre las caractersticas segn la
tabla adjunta.
- Con un lpiz marcador, divida en dos con una lnea central una placa de
agar sangre.
- En su cultivo, elija dos colonias diferentes que le parezcan interesantes.
- Con el asa estril y fra, toque una de ellas y luego siembre un sector del
agar sangre. Esterilice el asa, enfre, y repita con la otra colonia en el otro
sector. Incubar 24 horas entre 35 y 37C. Identifique siempre sus cultivos.
Morfologa colonial bacteriana
40
FACULTAD DE CIENCIAS MDICAS
Manual de Laboratorio de Microbiologa
MORFOLOGA COLONIAL
ASPECTO DE LA COLONIA COLONIA 1 COLONIA 2
Tamao:
Grande
Mediano
Pequeo
Superficie:
Plana
Planoconvexa
Convexa
Acuminada
Umbilicada
Papilada
Lisa
Rugosa
Forma:
Puntiforme
Circular
Filamentosa
Irregular
Rizoide
Fusiforme
Cerebriforme
Borde:
redondeado (entero)
Ondulado
Lobulado
Espiculado
Filamentoso
Rizoide
Brillo:
Opaco
Brillante
Consistencia:
Hmeda
Seca
Cremosa
Pigmento (Color):
Propio
Difusible
Hemolisinas:
Alfa hemoltica
Beta hemoltica
Gamma hemoltica
La observacin de la morfologa colonial es
el primer paso orientativo a la identificacin de
especies bacterianas.
En la medida que el bacterilogo adquiere
experiencia, esta etapa del cultivo le permite
tomar decisiones respecto de la marcha de
identificacin, a la vez que apreciar las
proporciones en las que se desarrollan las
distintas especies, y la carga microbiana de la
muestra.
La presencia de colonias pigmentadas es
orientativa de algunos patgenos como
Staphylococcus
aureus,
Pseudomonas
aeruginosas, Serratia rubidea y el anaerobio
Prevotella melaninogenica.
La accin de las hemolisinas tambin es un
ndice de mecanismos de accin patgena.
Muchas cepas de Staphylococcus aureus son beta
hemolticas (Hemolisis total), as como tambin
Streptococcus pyogenes (Streptococcus beta
hemoltico del grupo B).
La consistencia cremosa nos orienta hacia
levaduras, como Candida albicans. Si la colonia
tiene una consistencia mucosa, con tendencia a
escurrir o a filamentar, podemos estar en
presencia de alguna bacteria capsulada, como
Klebsiella pneumoniae.
Los hongos miceliados producen grandes
colonias filamentosas, con centros pigmentados de verde, negro o caf, debido a la presencia de
sus mecanismos de reproduccin asexuada (esporas fngicas). Esta descripcin es consistente con
especies de los gneros Penicillium, Aspergillus o Alternaria respectivamente.
41
FACULTAD DE CIENCIAS MDICAS
Manual de Laboratorio de Microbiologa
Ejercicios de Laboratorio
Actividad n7:
Objetivos:
Observacin microscpica de cultivos.
Conocer los fundamentos y practicar la Tincin de Gram.
Observar la morfologa bacteriana mediante microscopa.
Observar alteraciones estructurales de las bacterias.
Materiales y Mtodo: Utilice los cultivos de la actividad n6.
Portaobjetos
Kit de Tincin de Gram.
Asas de siembra
Placas de agar sangre (cualquier frmula).
Microscopio.
Bioseguridad:
Trabaja con bacterias no identificadas aisladas de humanos, no est
descartada la presencia de patgenos en los cultivos.
No olfatear los cultivos.
Use guantes, mechero encendido.
No exponga los cultivos innecesariamente.
Desarrollo:
-
A partir de la bacteria seleccionada en la actividad n6, prepare una lmina
para teir:
Con un asa de siembras tome una pequea gota de agua destilada y depostela en
el centro de un portaobjetos.
Esterilice el asa en el mechero y enfrela.
Con el asa toque un punto de la periferia de una colonia y luego llvela al agua del
portaobjetos. Haga una emulsin con movimientos circulares.
Fijacin: Con el asa extienda la emulsin sobre el
portaobjetos y squelo usando suavemente el
calor del mechero. No caliente en exceso para
evitar daos en la estructura bacteriana.
Tincin de Gram: Cubra la fijacin con colorante cristal violeta por 60 segundos.
Lave bajo chorro de agua.
Cubra ahora con lugol por 60 segundos. Lave.
Cubra con alcohol-acetona por 15 segundos, agite suavemente y lave. Repita hasta
22que ya no salga ms colorante.
Cubra con safranina por 30 segundos. Lave.
Secar al aire.
42
FACULTAD DE CIENCIAS MDICAS
Manual de Laboratorio de Microbiologa
Observar en el microscopio con aumento de 1000X.
Realice un nuevo cultivo sobre agar sangre para mantener la bacteria que
investiga y cultive por 24 horas a 35-37C. Identifique su siembra.
Etapas de la Tincin de Gram
La diferenciacin entre Gram Positivos y Gram Negativos ocurre durante el tratamiento con
alcohol acetona. Los Gram Negativos pierden el complejo cristal violeta-lugol (violeta) en la
decoloracin y luego se tien con la contratincin de safranina (rojo)
Cocceas Gram positivas en Diplo (1000X)
Cocceas Gram positivas en cadena (1000X)
43
FACULTAD DE CIENCIAS MDICAS
Manual de Laboratorio de Microbiologa
Otras posibles imgenes de bacterias teidas con el mtodo de Christian Gram:
Corynebacterium diphtheriae (1000X), bacilo Gram positivo,
aerobio, inmvil, no capsulado, ligeramente curvado y de
forma irregular. Posee una disposicin caracterstica en forma
de letras chinas. Agente causal de la difteria mediante toxina
lisognica.
Bacillus anthracis en tejido esplnico (1000X). Bacilo Gram
positivo aerbico y formador de esporas, capsulado e inmvil.
Su reservorio natural es el suelo y los cadveres de animales, es
capaz de producir toxinas tan potentes que pueden usarse
como arma biolgica con efectos devastadores.
Salmonella entrica serotipo typhimurium o Salmonella
typhimurium (1000X), bacilo Gram negativo de metabolismo
facultativo, enterobacteria causante de infecciones alimentarias.
La serovar typhi es la responsable del sndrome conocido como
fiebre tifodea. La morfologa de este agente mediante la tincin
de Gram es indistinguible de otras enterobacterias comunes.
Neisseria meningitidis, Tincin de Gram en sedimento de lquido
cefalorraquideo (1000X). Se observa su caracterstica disposicin
en diplo, en el exterior e interior de los leucocitos
polimorfonucleares.
Agente etiolgico de la meningitis meningoccica.
Candida albicans observada en secrecin vaginal (1000X).
Esta es una levadura, se reproduce asexuadamente mediante
yemacin y forma pseudomicelios, especialmente cuando
adquiere rol patgeno. Agente causal de vulvovaginitis.
44
FACULTAD DE CIENCIAS MDICAS
Manual de Laboratorio de Microbiologa
UNIDAD 3
IDENTIFICACION DE BACTERIAS
FUNDAMENTOS DE ALGUNOS METODOS DE ESTUDIO BIOQUIMICO PARA LA IDENTIFICACION DE
ENTEROBACTERIAS:
La aplicacin de pruebas bioqumicas mediante distintos medios de cultivo diferenciales
nos permite obtener una gran cantidad de informacin respecto del metabolismo bacteriano, lo
que es un reflejo de la gentica de gneros y especies, y por lo tanto una forma econmica y
segura de identificar una especie bacteriana.
Las combinaciones de estas pruebas se conocen como bateras de pruebas de
identificacin, las que se eligen de acuerdo al tipo de bacteria en estudio. Podemos concebir
bateras de pruebas para identificar enterobacterias, bacilos no fermentadores, cocceas Gram
positivas, entre otras.
Para la actividad n8, en la que se pretende identificar enterobacterias, los fundamentos
de las reacciones son los siguientes:
1- AGAR TSI:
Principio:
En el Agar TSI se determina la capacidad de un microorganismo para
atacar los hidratos de carbono GLUCOSA, LACTOSA y/o SACAROSA presentes en la frmula, con
produccin o no de gases (CO2), junto con la produccin o no de cido sulfhdrico (H2S). El agar
TSI tiene rojo de fenol como indicador de pH el cual vira al color amarillo en presencia de acidez y
al color rojo en presencia de alcalinidad. El medio de cultivo tiene como fuente de azufre el
tiosulfato de Na, que puede ser degradado por las bacterias productoras de H2S. Como indicador
de esta actividad, el medio de cultivo contiene sulfato de amonio ferroso el cual reacciona con el
H2S produciendo un precipitado negro e insoluble de sulfuro ferroso. Para que se produzca H2S, se
requiere de un medio neutro o alcalino por lo que dicha reaccin generalmente est limitada al
fondo del medio, y se observa con bacterias que no fermentan la sacarosa (Salmonella), pero que
si fermentan glucosa. Por esta razn, un fondo negro debe leerse como A (cido), aunque el color
amarillo est tapado por el color negro.
Interpretacin:
Se efecta despus de 18 a 24 horas de incubacin a 37C. Se anotan las
reacciones como una fraccin de nmeros: la reaccin ocurrida en la superficie del medio
corresponde al numerador (parte aerobia) y la reaccin ocurrida en la profundidad del medio
corresponde al denominador (parte anaerobia). La acidez se denomina con la letra A (color
amarillo) y la alcalinidad con la letra K (color rojo).
En este medio de cultivo se pueden ver las siguientes reacciones bioqumicas:
Fermentacin de la glucosa solamente: (K/A).
Fermentacin de glucosa, lactosa y/o sacaros: (A/A)
No fermentacin de los carbohidratos: (K/K), la bacteria no utiliza los hidratos de carbono
mediante fermentacin, produciendo aminas que alcalinizan el fondo y la superficie del medio.
45
FACULTAD DE CIENCIAS MDICAS
Manual de Laboratorio de Microbiologa
Algunas bacterias no fermentadoras solamente atacan la peptona aerbicamente dando
un TSI K/N, es decir superficie alcalina y no hay cambio en el fondo del tubo.
Adems, podemos observar
Produccin de gas: ruptura del medio con formacin de burbujas.
Produccin de H2S: ennegrecimiento de la columna del medio de cultivo.
De izquierda a derecha:
1.- TSI A/A, +/(-): cido sobre cido, gas positivo y H2S negativo.
Este patrn de resultados puede obtenerse con Escherichia coli,
Klebsiella pneumoniae, Enterobacter aergenes, entre otras.
2.- TSI K/A, (+)w/(-): alcalino sobre cido, gas escaso con
incubacin prolongada, H2S negativo. Patrn sugerente de
Shigella sp.
3.- TSI K/A, (-)/+: alcalino sobre cido, gas negativo y H2S positivo, sugiere Salmonella,
posiblemente Salmonella enteritidis.
4.- TSI K/N, (-)/(-): alcalino sobre neutro, sin produccin de gas ni H2S, patrn caracterstico
de algunos bacilos no fermentadores como Pseudomonas aeruginosa o Acinetobacter bawmanii.
2- AGAR LIA:
Principio:
En agar LIA (Lysine Iron Agar) se determina la capacidad de una bacteria
para atacar el aminocido lisina mediante descarboxilacin o desaminacin, la fermentacin de
glucosa, la produccin o no de gases (CO2), junto con la produccin o no de cido sulfhdrico (H2S).
Interpretacin:
Se efecta despus de 18 a 24 horas de incubacin (48 horas si es
necesario) a 37C. Igualmente se registran las reacciones como en el Agar TSI. La acidez se
denomina con la letra A (color amarillo) y la alcalinidad con la letra K (color prpura).
En este medio se observan las siguientes reacciones bioqumicas:
Fermentacin de la glucosa (K/A), la bacteria no ataca el aminocido y solo fermenta la
glucosa.
Descarboxilacin de la lisina: (K/K)
Desaminacin de la lisina: (R/A) se ve como rojo/ amarillo.
Produccin de gas: ruptura del medio.
Produccin de H2S: ennegrecimiento del medio de cultivo.
El indicador del pH del medio es prpura de bromocresol, el cual en acidez vira al color
amarillo y en alcalinidad al color prpura. Por contener pequea cantidad de Glucosa (1 g/ L) la
fermentacin se observa al fondo del tubo (amarillo), con la superficie alcalina.
46
FACULTAD DE CIENCIAS MDICAS
Manual de Laboratorio de Microbiologa
Muchas bacterias poseen descarboxilasas que atacan el aminocido lisina, con formacin
de cadaverina de reaccin alcalina y con produccin de CO2. Para que acten las descarboxilasas
se requiere pH cido, el que se obtiene por la fermentacin de la glucosa presente en el medio.
La desaminacin de la lisina es un proceso oxidativo que se manifiesta por la aparicin de
color rojo en el tendido, siendo el fondo del tubo amarillo por fermentacin de la glucosa. Tiene
como fuente de azufre el Tiosulfato de Na, necesario para que las bacterias puedan producir H2S.
La reaccin ocurre solo en ambiente cido y se observa como como produccin de color negro
(sulfuro ferroso), por esta razn el fondo negro implica la presencia de cido (A).
LIA K/K, (-)/(-): descarboxilacin de lisina, sin gas ni
H2S, sugiere Escherichia coli, Klebsiella sp. o
Salmonella sp.
LIA K/A, +/(-): descarboxilacin negativa, hay gas
pero no H2S, sugiere Escherichia coli, Enterobacter
o Klebsiella. Shigella sp. no dara gas.
R/A, +/(-): desaminacin positiva, con gas sin H2S,
es predictivo de Morganella morganii.
K/A, +w/+: descarboxilacin de lisina, hay produccin de gas y mucho H2S. Resultados sugerentes
de Salmonella, Citrobacter o Edwardsiella.
3- AGAR CITRATO DE SIMMONS:
Principio:
En el agar Citrato de Simmons se determina la capacidad de un
microorganismo de emplear el citrato como nica fuente de carbono.
El metabolismo del citrato es una fase previa de los cidos tricarboxlicos
para entrar en el ciclo de Krebs. Un organismo capaz de utilizar el citrato como nica fuente de
carbono tambin es capaz de utilizar las sales de amonio como nica fuente de nitrgeno. El
medio de cultivo contiene adems sales de amonio inorgnicas que se desdoblan en amoniaco
(NH4) con la consiguiente alcalinidad del medio. El indicador de pH es el azul de bromotimol el cual
en presencia de alcalinidad vira al color azul indicando que la prueba es POSITIVA. Cuando no hay
cambio de color ni crecimiento bacteriano se dice que la prueba es NEGATIVA.
Interpretacin:
Se efecta despus de 18 a 24 horas de incubacin (48 horas s es
necesario) a37C. Viraje a azul con desarrollo: positivo. Sin cambios: negativo.
47
FACULTAD DE CIENCIAS MDICAS
Manual de Laboratorio de Microbiologa
Entre las enterobacterias con caracterstica citrato (+) se
observan los siguientes gneros:
Enterobacter sp, Klebsiella pneumoniae, Serratia
sp, Citrobacter sp. y algunas especies de Salmonella.
Sin embargo, Escherichia, Shigella, Salmonella typhi y son
citrato negativas.
4- AGAR UREA:
Principio:
En el agar Urea de Christensen se determina la capacidad de una bacteria
para producir ureasa y degradar la urea, formando dos molculas de amoniaco. La ureasa es una
enzima bacteriana constitutiva (no requiere presencia de sustrato para que la bacteria la
produzca), por lo que es un excelente marcador gentico. Bacterias del gnero Proteus producen
gran cantidad de ureasa, Klebsiella sp. tambin es productora de ureasa, pero en cantidades
menores. El medio de cultivo contiene rojo de fenol como indicador de pH y una pequea cantidad
de glucosa para mejorar la diferencia entre el resultado positivo y negativo. Cuando una bacteria
posee ureasa el pH se torna bsico por efecto del amonio y el indicador cambia a rojo. Si la
reaccin es negativa, la fermentacin de glucosa cambia el pH hacia cido y el color pasa a
amarillo.
Interpretacin:
Se efecta despus de 18 a 24 horas de incubacin a 37C.
Izquierda: Agar urea de Christensen positivo, Proteus vulgaris
Centro: Medio de cultivo sin inocular.
Derecha: Agar urea de Christensen negativo, Escherichia coli
La accin de la ureasa en los Proteus puede alcalinizar
rpidamente el medio de cultivo, en tanto que con Klebsiellas los
resultados positivos pueden observarse tras 24 a 48 horas de
incubacin.
Reaccin de la ureasa:
C=O(NH2)2 + H++ 2H2O
HCO3- + 2NH4+
48
FACULTAD DE CIENCIAS MDICAS
Manual de Laboratorio de Microbiologa
5- MEDIO M.I.O:
Principio:
En Medio MIO (Motilidad, Indol, Ornitina) se determina la motilidad de un
microrganismo (presencia de flagelos), la capacidad de producir indol a partir de triptofano y la
capacidad de degradar la ornitina (ornitina decarboxilasa).
Interpretacin:
Se efecta despus de 18 a 24 horas de incubacin a 37C.
La primera caracterstica a observar es la motilidad bacteriana, la que se
aprecia observando desarrollo bacteriano (turbidez) fuera de la lnea de inoculacin, pudiendo
ocupar la totalidad del medio de cultivo. Si la motilidad es negativa, el desarrollo bacteriano se
observa solo en la lnea de inoculacin. Para lograr esta observacin, el medio de cultivo es
semislido.
La segunda caracterstica observable es la decarboxilacin de la ornitina,
en la que el aminocido pierde el grupo carboxilo por accin de la ornitina decarboxilasa y se
transforma en un compuesto alcalino: la putrescina. Como consecuencia el medio se alcaliniza, y el
indicador prpura de bromocresol cambia hacia prpura. La reaccin es similar a la
decarboxilacin de la lisina en el medio LIA:
El medio MIO posee una pequea cantidad de glucosa fermentable, para
distinguir los resultados negativos de los positivos. Cuando las bacterias no son productoras de
ornitina decarboxilasa, la fermentacin de glucosa produce cido y el indicador cambia a amarillo.
La tercera caracterstica observable mediante el Medio MIO es la
formacin de indol a partir del aminocido Triptofano presente en grandes cantidades en la
peptona triptena. El triptfano es degradado en una cadena de reacciones donde participa la
enzima triptofanasa, donde pierde el grupo amino produciendo finalmente indol, cido pirvico y
amonio.
49
FACULTAD DE CIENCIAS MDICAS
Manual de Laboratorio de Microbiologa
El indol es reconocido agregando gotas de Reactivo de Kovacs, con la
formacin de un anillo de color rojo sobre el medio de cultivo. El indol se extrae con butanol o
alcohol amlico y luego reacciona con el componente p-dimetilamino benzaldehdo para originar
rosindol (rojo) en medio fuertemente cido:
Bacterias Indol positivas: Escherichia coli, Proteus vulgaris.
Bacterias Indol negativas: Klebsiella pneumoniae, Proteus mirabilis.
Existe una gran variedad de pruebas que pueden ser de utilidad en la identificacin de
enterobacterias. Mediante fermentacin de carbohidratos especficos es posible distinguir entre
miembros de un mismo gnero, la produccin de metabolitos terminales como acetilmetilcarbinol
permite caracterizar grupos bacterianos, y la prueba de oxidasa nos permite diferenciar entre
bacterias fermentadoras u oxidativas de los carbohidratos.
50
FACULTAD DE CIENCIAS MDICAS
Manual de Laboratorio de Microbiologa
FUNDAMENTOS DE ALGUNOS METODOS DE ESTUDIO PARA LA IDENTIFICACION DE COCCEAS
GRAM POSITIVAS AEROBIAS:
Aspectos taxonmicos generales:
Existe una gran variedad de bacterias cocceas Gram positivas, por lo que su clasificacin
taxonmica resulta compleja. En general, tratamos de ordenar este conjunto de bacterias de
acuerdo a su metabolismo (aerbico, facultativo o anaerobio estricto), a su disposicin
caracterstica (grupos, cadenas, pares, cubos) y mediante algunas caractersticas fenotpicas de
importancia (catalasa, hemolisinas). Varios gneros de estas bacterias pertenecen al Phylum
Firmicutes, que engloba a muchas de las bacterias Gram positivas. Los firmicutes pueden
pertenecer a tres clases, y situamos a las cocceas Gram positivas en la clase Bacilli. No obstante lo
anterior, podemos encontrar cocceas Gram positivas en otros Phylum (Actinobacteria).
El rden taxonmico de los gneros ms representativos es entonces:
Dominio:
Phylum:
Clase:
Orden Bacillales:
Familia Staphylococcaceae:
Orden Lactobacillales:
Familia Streptococcaceae:
Familia Enterococcaceae:
Bacteria
Firmicutes
Bacilli
Gnero Staphylococcus
Gnero Streptococcus
Gnero Enterococcus
El gnero Staphylococcus contiene varias especies, entre las cuales destacan S. aureus, S.
epidermidis, S. saprophyticus y S. lugdunensis por haber reportado participacin en casos clnicos.
Otras especies de este gnero podra aparecer como patgenos emergentes.
Las familias Streptococcaceae y Enterococcaceae estn estrechamente relacionadas, en
ellas se encuentran patgenos de reconocida importancia y otras especies que forman parte de
nuestra microbiota, algunas de las cuales adquieren rol patgeno como oportunistas o en funcin
de su caracterstica gentica (cepa patgena).
Podemos categorizar al gnero Streptococcus por su actividad hemoltica en alfa, beta o
gamma hemolticos. Estas caractersticas pueden observarse en varios grupos afines de
Streptococcus. Es importante destacar que el tipo de actividad hemoltica no es privativo de
alguno de los grupos de Lancefield, determinados segn la respuesta inmune frente al polisacrido
capsular, por lo que podemos observar la existencia de especies de Streptococcus alfa hemolticos
pertenecientes al grupo A y Streptococcus beta hemolticos tambin pertenecientes al grupo A de
Lancefield, y otras asociaciones hemlisis/polisacrido capsular.
51
FACULTAD DE CIENCIAS MDICAS
Manual de Laboratorio de Microbiologa
1.- Streptococcus alfa hemolticos (hemlisis viridans o incompleta), grupo heterogneo que
habita normalmente en la orofarnge y puede adquirir rol patgeno oportunista, incluye varios
subgrupos.
Grupo mitis: asociado a endocarditis y caries dentales, especies de importancia clnica:
Streptococcus mitis
Streptococcus oligofermentans
Streptococcus oralis
Streptococcus gordoni
Streptococcus cristatus
Streptococcus infantis
Streptococcus peroris
Streptococcus australis
Streptococcus pneumoniae
Grupo anginosus: asociados a abscesos subcutneos y de rganos, infecciones del tracto
urogenital y respiratorio, especies de importancia clnica:
Streptococcus anginosus: infecciones urogenitales, abscesos de tejidos blandos,
abdominales, cuello y cabeza.
Streptococcus constellatus ssp. constellatus
Streptococcus constellatus ssp. pharingis : infecciones respiratorias
Streptococcus intermedius : asociado a abscesos cerebrales y hepticos.
Algunas especies del grupo anginosus pueden exhibir hemolisis alfa o beta, incluso cepas no
hemolticas. Algunas especies pertenecientes a este grupo se denominan informalmente como
Streptococcus milleri, nominacin que puede observarse a veces en literatura mdica, pero no
corresponde a una especie demostrada.
Grupo mutans: asociados a caries dentales y endocarditis, especies de importancia
clnica:
Streptococcus mutans: principal agente de la placa bacteriana dental, asociado a
endocarditis, bacteremia y caries dental.
Streptococcus sobrinus: agente secundario de caries dentales.
Streptococcus criceti
Streptococcus ratti
Streptococcus downei
Streptococcus macacae
Streptococcus ferus
Grupo salivarius: asociado a caries dentales y endocarditis, especies importantes:
Streptococcus salivarius: bacteremia, endocarditis, meningitis
Streptococcsu vestibularis
Streptococcus termophylus
Streptococcus hyointestinalis
52
FACULTAD DE CIENCIAS MDICAS
Manual de Laboratorio de Microbiologa
Grupo bovis: agentes de endocarditis y de infeccin del tracto biliar y urinario, asociado a
cncer de colon:
Streptococcus infantarius ssp. infantarius
Streptococcus infantarius ssp. coli
Streptococcus alactolyticus
Streptococcus equinus/bovis: cncer de colon
Streptococcus gallolyticus ssp. gallolyticus: cncer gastrointestinal
Streptococcus gallolyticus ssp. pasteurianus: meningitis
Streptococcus gallolyticus ssp. Macedonicus
Grupo sanguis/sanguinis: aislados de casos de bacteremia:
Streptococcus sanguis, biotipos 1, 2 y 3
Streptococcus parasanguis
Streptococcus gordonii
Streptococcus sinensis
2.- Streptococcus beta hemolticos (hemolisis completa), comprende el Grupo Piognico y en
Grupo No Piognico. Se destacan las especies de inters mdico
Grupo piognico: contiene especies patgenas primarias, se observan involucrados en una
gran variedad de casos clnicos:
Streptococcus pyogenes (beta hemoltico grupo A)
Streptococcus agalactiae (beta hemoltico grupo B)
Streptococcus equi ssp. Equi
Streptococcus equi ssp. Zooepidermicus
Streptococcus dysgalactiae ssp. Dysgalactiae
Streptococcus dysgalactiae ssp. Equisimilis (beta hemoltico grupos A, C, G)
Streptococcus canis
Streptococus iniae
Streptococcus porcinus
Streptococcus phoaceae
Streptococcus didelphis
Streptococcus urinalis
Grupo No Piognico: sus especies forman colonias pequeas, pueden poseer
carbohidratos de pared de los grupos A, C, G, F. Se observan ocasionalmente involucrados
en abscesos, infecciones del SNC, infecciones pulmonares y bacteremias.
Streptococcus anginosus (cepas hemolticas grupos A, C, G, F)
Streptococcus constellatus (cepas hemolticas grupos A, C, F)
Streptococcus intermedius (cepas hemolticas grupo F)
Puedes revisar un caso clnico en: http://www.scielo.cl/scielo.php?pid=S0716-10182004000300019&script=sci_arttext . Empiema
pleural por Streptococcus grupo anginosus en un preescolar y revisin de la literatura Paola Pidal M., Javiera Basaure O., Priscilla Prado
D. y Pedro Alarcn L. Hospital Padre Alberto Hurtado: Unidad de Laboratorio Clnico (PPM, PAL), Unidad de Gestin Clnica del Nio
(JBO, PPD). Rev Chil Infect 2004; 21 (3): 248-253.
53
FACULTAD DE CIENCIAS MDICAS
Manual de Laboratorio de Microbiologa
Prueba de la Catalasa, primera etapa en la marcha de identificacin:
La enzima catalasa es una enzima muy comn entre los organismos vivos, tiene por
funcin transformar el perxido de hidrgeno en agua y oxgeno:
2 H2O2
2 H2O + O2
El perxido de H es un producto residual del metabolismo celular, especialmente en
organismos aerobios o facultativos. La acumulacin de perxido puede provocar un estado celular
oxidativo, lo que disminuye la eficiencia en los mecanismos de transporte de electrones. La
presencia de catalasa en las bacterias est ntimamente ligada con las reacciones metablicas que
determinan la condicin aerbica o anaerbica. Podemos observar actividad de catalasa en
muchos tipos de bacterias.
La determinacin de esta enzima adems de la observacin de la disposicin de las clulas
bacterianas es el primer paso en la marcha de identificacin:
Cocceas Gram positivas
(aerobia, microaerfila, o anaerobia facultativa)
Catalasa (+)
Gneros
Catalasa (-)
Staphylococcus
Micrococcus
Otros gneros
Streptococcus
Enterococcus
Otros gneros
Actividad de Catalasa y Citocromo oxidasa asociada al
tipo de disposicin celular
Gnero
Staphylococcus
Micrococcus
Stomatococcus
Streptococcus
Globicatella
Enterococcus
Lactococcus
Vagococcus
Leuconostoc
Aerococcus
Alloicoccus
Gemella
Pediococcus
Tetragenococcus
Helcococcus
Oxidasa
+
+
+
-
Catalasa
+
+
w
+
w
+
-
Disposicin
grupos
grupos
grupos
Cadenas
Cadenas
Cadenas
Cadenas
Cadenas
Cadenas
Pares o ttradas
Pares o ttradas
Pares o ttradas
Pares o ttradas
Pares o ttradas
Pares o ttradas
+: reaction positiva, -: reaccin negativa, +w: reaccin dbil.
CLINICAL M ICROBIOLOGY REVIEWS, Oct. 1995, p. 479495 Vol. 8, No. 4
0893-8512/95/$04.0010 Copyright q 1995, American Society for Microbiology
54
FACULTAD DE CIENCIAS MDICAS
Manual de Laboratorio de Microbiologa
La reaccin de la catalasa, segn se describe en la actividad de laboratorio n 9 (pag. 58) se
observa como una efervescencia fuerte, y permite diferenciar claramente los gneros
Staphylococcus y Micrococcus de las otras cocceas Gram positivas. Los gneros Aerococcus y
Alloicoccus tienen una disposicin celular diferente y dan una reaccin dbil, mediante la accin
de una enzima peroxidasa que puede actuar sobre el perxido de H, adems estos gneros no
contienen enzimas de citocromo. Todos los gneros de cocceas Gram positivas con disposicin en
cadena no dan reaccin de catalasa.
Identificacin de Cocceas Gram positivas aerobias o facultativas, con catalasa negativa
Si la reaccin de catalasa es negativa, es imprescindible observar la disposicin celular
mediante una tincin de Gram, realizada a partir de un cultivo en fase lquida (Caldo Tioglicolato,
por ejemplo). Las bacterias con disposicin en cadenas pueden clasificarse de acuerdo al patrn
hemoltico para decidir en base a este las pruebas de confirmacin. Es importante recordar que
esta estrategia de estudio si bien es prctica y rpida, puede ser inexacta especialmente en
aquellas especies con cepas de distinto comportamiento hemoltico, como los Streptococcus del
grupo anginosus.
La marcha de identificacin con respecto al patrn hemoltico y de disposicin es:
Cocceas Gram (+), catalasa (-), en pares o cadenas
Alfa hemolticas
Pares
beta hemolticas
Cadenas
Reaccin de
Quellung (+)
Bilis esculina
Susceptibilidad a
(-)
Bacitracina (+)
Streptococcus
Bilis esculina
pyogenes
Bacitracina (-)
Bilis esculina (-)
Test de Camp
Otras especies de
Bilis esculina (+)
Streptococcus
(+)
(+)
Optoquina (+)
Solubilidad en
Bilis (+)
gamma hemolticas
Otras especies de
Grupo D (-)
Streptococcus
Grupo D (+)
agalactiae
(-)
Otras especies de
Streptococcus beta hemolticos
Streptococcus viridans
Otros gneros
NaCl 6.5% (-)
NaCl 6.5% (+)
Grupo D (+)
Grupo D (-)
Streptococcus pneumoniae
Streptococcus
Equis/bovis
(Grupo D no enterococo)
Enterococcus sp.
NaCl 6.5% (-)
55
FACULTAD DE CIENCIAS MDICAS
Manual de Laboratorio de Microbiologa
Pruebas de identificacin para Streptococcus pneumoniae:
Streptococcus pneumoniae es una especie anaerobia
facultativa, capnfila (crece en atmsfera con 8 a 10% de CO2),
genticamente relacionada con el grupo mitis de los Streptococcus
viridans. Sus colonias son pequeas (1 a 3 mm), mucosas, con centro
deprimido (umbilicadas) por efecto de la autolisis, no pigmentadas y
de reaccin alfa hemoltica. Sus clulas son capsuladas, de 0.5 a 1.2 m,
dispuestas en pares y de forma oval lanceolada.
Las pruebas de identificacin son sencillas y seguras:
Solubilidad en bilis: Los Streptococcus pneumoniae se lisan en una solucin de
desoxicolato de Na al 10%. La prueba debe hacerse contra un control negativo.
Susceptibilidad a la Optoquina (clorhidrato de etilhidrocuprena, disco de 5g):
Streptococcus pneumoniae no tolera la optoquina, ya que
sus membranas celulares son sensibles al compuesto.
La prueba se realiza mediante la siembra de una suspensin
de bacterias en caldo Mueller Hinton y luego siembra sobre
agar sangre. Si la zona de inhibicin es ayor a 14 mm, la
prueba es positiva.
Algunos investigadores reportan hasta un 4% de cepas con
resistencia a la optoquina.
Reaccin de Quellung: Al tratar las cepas de Streptococcus
pneumoniae con antisueros especficos, se puede observar
mediante microscopa un engrosamiento de la cpsula.
56
FACULTAD DE CIENCIAS MDICAS
Manual de Laboratorio de Microbiologa
Identificacin de Streptococcus viridans:
Descartando la presencia de Streptococcus pneumoniae, resulta conveniente ahora
investigar si estamos frente a una especie del complejo Streptococcus equis/bovis, antes de
abordar la identificacin de los otros Streptococcus alfa hemolticos:
57
FACULTAD DE CIENCIAS MDICAS
Manual de Laboratorio de Microbiologa
58
FACULTAD DE CIENCIAS MDICAS
Manual de Laboratorio de Microbiologa
59
FACULTAD DE CIENCIAS MDICAS
Manual de Laboratorio de Microbiologa
Actividad n8:
Objetivos:
Identificacin de Bacilos Gram negativos
Conocer los fundamentos metodolgicos de la identificacin de
enterobacterias.
Reconocer medios de cultivo diferenciales y practicar siembra en ellos.
Practicar la identificacin bacteriana mediante pruebas bioqumicas.
Materiales y mtodo: Los alumnos dispondrn de tres enterobacterias incgnitas para realizar la
identificacin. Cada grupo de cinco alumnos trabaja con una cepa.
Medios de cultivo diferenciales:
Agar TSI (Agar Hierro y tres azcares)
Agar Citrato de Simmons
Agar LIA (Agar Hierro y Lisina)
Medio MIO (Medio de Motilidad, Indol y Ornitina)
Agar Urea de Christensen.
Bioseguridad:
Trabaja con bacterias incgnitas. Pueden incluirse enterobacterias
patgenas o de infeccin oportunista.
Use guantes. Mechero encendido.
No olfatee ni exponga innecesariamente los cultivos. No coma.
En caso de derrame o contacto avise al profesor. No acte por iniciativa
propia.
Lvese las manos antes de dejar el laboratorio.
Desarrollo:
- Prepare en una gradilla una serie con los medios de cultivo citados
(batera de identificacin) en el mismo orden de secuencia. Identifique el
primer tubo con el n del incgnito y su grupo de trabajo.
- Esterilice el asa de siembra y enfrela.
- Tome una pequea porcin de cultivo y realice la siembra de tubos de la
siguiente forma (puede recargar el asa entre tubo y tubo):
- Agar TSI: sembrar en estra de superficie y picada profunda.
- Agar Citrato: sembrar en estra de superficie.
- Agar LIA: sembrar en estra de superficie y picada profunda.
Fig.2.12.
- Medio MIO: sembrar en picada vertical central y profunda, sin
desplazamientos laterales. Fig.2.11
- Agar Urea: sembrar en estra de superficie.
- Cultivar durante 24 horas a 35 a 37C. Luego realizar la lectura e
interpretacin de resultados mediante la tabla adjunta en la pgina 51.
- Para la interpretacin de cada tubo de pruebas bioqumicas utilice la
pauta de fundamentos que se incluyen en la pgina 45 a 50.
60
FACULTAD DE CIENCIAS MDICAS
Manual de Laboratorio de Microbiologa
Tabla de Identificacin de bacterias
(uso restringido a actividad de docencia)
Resultados de las pruebas:
+ : Positivo en ms del 90% de los casos.
(-): Positivo en menos del 10% de los casos.
V: Resultados variables, positivos entre el 10% y 90% de los casos.
La presente tabla de identificacin tiene como objeto ejemplificar el uso combinado de la
informacin obtenida mediante pruebas bioqumicas de identificacin bacteriana, no debe aplicarse como
pauta de trabajo en microbiologa clnica porque contiene informacin restringida.
61
FACULTAD DE CIENCIAS MDICAS
Manual de Laboratorio de Microbiologa
Actividad n9:
Objetivos:
Determinacin de Catalasa.
Valorar la prueba de catalasa para diferenciar grandes grupos bacterianos.
Practicar la identificacin de bacterias de acuerdo a la catalasa.
Materiales y mtodo: Los alumnos dispondrn de tres bacterias incgnitas su identificacin.
Cada grupo de cinco alumnos trabaja con una cepa (no intercambiar).
Lminas portaobjetos
Asas de siembra
Agar sangre
Solucin de perxido de hidrgeno al 20% (Agua oxigenada)
Bioseguridad:
Trabaja con bacterias incgnitas. Pueden incluirse bacterias patgenas o
de infeccin oportunista.
Use guantes. Mechero encendido.
No olfatee ni exponga innecesariamente los cultivos. No coma.
En caso de derrame o contacto avise al profesor. No acte por iniciativa
propia.
Lvese las manos antes de dejar el laboratorio.
Descarte el material contaminado en solucin de hipoclorito.
Desarrollo:
- Prepare una serie de tres portaobjetos limpios con una gota de perxido
de hidrgeno en el centro.
- Esterilice el asa de siembra y enfrela.
- Coloque el asa en el perxido y observe si hay desprendimiento de gas.
- Tome una pequea porcin de agar sangre sin cultivar y realice la misma
operacin en otro portaobjetos. Hay desprendimiento de gas?
- Esterilice el asa y enfrela. Tome una pequea cantidad de cultivo y
repita en el tercer portaobjetos. Registre los resultados. Descarte en
solucin de hipoclorito.
- Catalasa negativo: sin cambios. Catalasa positivo: emisin de burbujas.
Si la bacteria da catalasa positivo, contine en la actividad 10.
Si la bacteria da catalasa negativo, contine en la actividad 11.
62
FACULTAD DE CIENCIAS MDICAS
Manual de Laboratorio de Microbiologa
Actividad n10:
Objetivos:
Identificacin de Cocceas Gram positivas catalasa positivas.
Conocer los fundamentos metodolgicos de la identificacin de Cocceas
Gram positivas aerobias.
Reconocer medios de cultivo selectivos y diferenciales y practicar siembra
en ellos.
Practicar la identificacin bacteriana mediante pruebas bioqumicas.
Materiales y mtodo: Los alumnos dispondrn de una bacteria incgnita para su identificacin.
Cada grupo de cinco alumnos trabaja con una cepa.
Medios de cultivo diferenciales:
Agar Manitol sal
Agar DNAsa
Agar Telurito de K
Agar sangre de cordero
Bioseguridad:
Trabaja con bacterias incgnitas. Pueden incluirse bacterias patgenas o
de infeccin oportunista.
Use guantes. Mechero encendido.
No olfatee ni exponga innecesariamente los cultivos. No coma.
En caso de derrame o contacto avise al profesor. No acte por iniciativa
propia.
Lvese las manos antes de dejar el laboratorio.
Desarrollo:
- Identifique los materiales con el n del incgnito y su grupo de trabajo.
- Esterilice el asa de siembra y enfrela.
- Tome una pequea porcin de cultivo y realice la siembra en cada medio
de cultivo de la siguiente forma (puede recargar el asa entre cada medio):
- Agar Manitol sal: sembrar en estra de superficie.
- Agar DNAsa: sembrar en estra de superficie. (abundante)
- Agar Telurito de K: sembrar en estra de superficie
- Agar sangre: sembrar en superficie, poco inculo.
- Cultivar durante 24 horas a 35 a 37C. Luego realizar la lectura e
interpretacin de resultados mediante la tabla adjunta.
- Para la interpretacin de cada tubo de pruebas bioqumicas utilice la
pauta de fundamentos que se incluyen en la pgina
63
FACULTAD DE CIENCIAS MDICAS
Manual de Laboratorio de Microbiologa
Actividad n11:
Objetivos:
Identificacin de Cocceas Gram positivas catalasa negativas.
Conocer los fundamentos metodolgicos de la identificacin de Cocceas
Gram positivas aerobias.
Reconocer medios de cultivo selectivos y diferenciales y practicar siembra
en ellos.
Practicar la identificacin bacteriana mediante pruebas bioqumicas.
Materiales y mtodo: Los alumnos dispondrn de dos bacterias incgnitas para su identificacin.
Cada grupo de cinco alumnos trabaja con una cepa. No intercambiar
Medios de cultivo diferenciales:
Agar Sal
Agar Bilis esculina
Agar Telurito de K
Agar sangre de cordero
Bioseguridad:
Trabaja con bacterias incgnitas. Pueden incluirse bacterias patgenas o
de infeccin oportunista.
Use guantes. Mechero encendido.
No olfatee ni exponga innecesariamente los cultivos. No coma.
En caso de derrame o contacto avise al profesor. No acte por iniciativa
propia.
Lvese las manos antes de dejar el laboratorio.
Desarrollo:
- Identifique los materiales con el n del incgnito y su grupo de trabajo.
- Esterilice el asa de siembra y enfrela.
- Tome una pequea porcin de cultivo y realice la siembra en cada medio
de cultivo de la siguiente forma (puede recargar el asa entre cada medio):
- Agar sal: sembrar en estra.
- Agar Bilis esculina: sembrar en estra.
- Agar Telurito de K: sembrar en estra.
- Agar sangre: sembrar en superficie, poco inculo.
- Cultivar durante 24 horas a 35 a 37C. Luego realizar la lectura e
interpretacin de resultados mediante la tabla adjunta en la pgina
64
FACULTAD DE CIENCIAS MDICAS
Manual de Laboratorio de Microbiologa
UNIDAD 4
PRUEBAS DE SUSCEPTIBILIDAD A LOS ANTIMICROBIANOS
El uso de diversos agentes qumicos para la prevencin y el tratamiento de personas
afectadas por agentes infecciosos, basado en fundamentos cientficos, comienza a mediados del
siglo XIX. En esa poca las recomendaciones de Ignacio Semmelweis (lavado de manos con cloruro
de Ca), y de Joseph Lister en 1865 (uso del fenol para la antisepsia y desinfeccin) son ejemplos
representativos de la utilidad de estas prcticas. Este conocimiento incipiente dio un salto de
efectos insospechados con el descubrimiento de la penicilina por Alexander Fleming en 1928, y la
produccin y purificacin de esta sustancia por Norman Heatley, Ernst Chain y Howard Florey
entre 1939 y 1941. A partir de este momento histrico, a los antimicrobianos de origen qumico
artificial (quimioterpicos), se suman sustancias de origen natural: los antibiticos.
Una vez comprobada la eficacia de estas nuevas sustancias en el tratamiento de
enfermedades infecciosas, se hizo adems evidente el fracaso en muchos casos. La necesidad de
entender el fallo en el uso de estas sustancias determin intensas investigaciones en la
comprensin de la estructura bacteriana, los sitios diana donde se verifica la accin de los
antimicrobianos y los mecanismos de resistencia desarrollados por los microrganismos. Estas
lneas de investigacin han determinado en la actualidad un uso ms racional y responsable de los
antimicrobianos, aspecto fundamental para asegurar el xito de la terapia, evitar las
complicaciones y disminuir el tiempo de hospitalizacin. En este marco de accin, se incluyen las
pruebas de susceptibilidad a los antimicrobianos.
Aspectos generales:
Los mtodos de determinacin de la susceptibilidad a los antimicrobianos son pruebas
realizadas in vitro bajo condiciones estandarizadas, y tienen como propsito fundamental
determinar la condicin de susceptible o resistente de un microrganismo aislado, frente a una
determinada sustancia de utilidad teraputica. Este tipo de pruebas se realiza frente a bacterias
que no tienen susceptibilidad predecible, con el objeto de asegurar el xito del tratamiento. Para
este propsito existen varios mtodos, que se explican a continuacin:
Mtodo por difusin en agar (antibiograma):
Es el mtodo ms utilizado, es relativamente econmico y de fcil estandarizacin, usado
frente a los agentes infecciosos comunes. Se realiza sobre Agar Mueller Hinton II de acuerdo al
mtodo descrito por Kirby y Bauer, bsicamente es una difusin del antimicrobiano desde discos
de papel en condiciones estandarizadas. Ver detalles ms adelante.
Mtodo por dilucin en agar (determinacin de concentracin inhibitoria mnima
o CIM):
El mtodo consiste en preparar una serie de dilucin de un antimicrobiano, la que se
agrega al agar, para luego sembrar una carga constante de microrganismo y determinar en que
65
FACULTAD DE CIENCIAS MDICAS
Manual de Laboratorio de Microbiologa
dilucin (concentracin) ocurre la inhibicin del crecimiento. Es el mtodo de referencia para
determinar la CIM.
Mtodo por dilucin en caldo (determinacin de CIM):
Es un mtodo similar al anterior, pero la fase es lquida (caldo). Tambin permite la
determinacin de la CIM. Puede realizarse en tubos o en pocillos (microplacas).
E-Test o Epsilon test (determinacin de CIM mediante difusin en agar):
Es un mtodo realizado en fase slida (agar) mediante difusin, en este
caso se usan tiras impregnadas con concentraciones decrecientes de
antimicrobiano, desde 256 g hasta 0.016 g. Es el mtodo ms sencillo y
econmico de conocer la CIM, y resulta de gran utilidad para conocer la
susceptibilidad de bacterias como Haemophilus influenzae, Streptococcus
pyogenes y Streptococcus pneumoniae.
Mtodos automticos (cintica de crecimiento frente al antimicrobiano):
Mtodos rpidos que permiten determinar la inhibicin del crecimiento mediante
turbidimetra o fluorometra en fase lquida. Son tiles para el estudio de bacterias de desarrollo
rpido, como enterobacterias.
La Concentracin Inhibitoria Mnima (CIM) y Concentracin Bactericida Mnima (CBM):
La Concentracin Inhibitoria Mnima (CIM) es la concentracin ms baja de un
antimicrobiano, necesaria para producir una inhibicin visible del desarrollo bacteriano in vitro,
bajo condiciones estandarizadas. Las condiciones de estandarizacin de estas pruebas son
establecidas por un organismo internacional: CLSI (Clinical Laboratory Standads Institute). Es
importante destacar que la CIM se determina mediante observacin visual, por lo que es posible
que algunos clones de la bacteria que se investiga puedan soportar an la concentracin que logra
inhibir a la mayora.
La Concentracin Bactericida Mnima (CBM) corresponde a la concentracin ms baja
posible de un antimicrobiano, necesaria para inhibir todos los microrganismos en un subcultivo
realizado en medios exentos de inhibidores. Esta determinacin puede usarse como complemento
a la CIM, ya que es posible que algunos clones necesiten dosis ms altas de antimicrobiano para
lograr prevenir la multiplicacin.
Observando el siguiente diagrama se puede comprender mejor este hecho: Si probamos
una bacteria frente a una serie de dilucin del antibitico X la CIM que se obtiene es 2.0 g/mL, ya
que no observamos ms desarrollo en concentraciones mayores. Para comprobar la CIM,
realizamos un cultivo en medios libres de inhibidores, y observamos que an se obtiene desarrollo
en concentraciones de 4.0 g/mL, lo que se debe a la presencia de clones que soportan una
concentracin ms alta del antibitico X.
66
FACULTAD DE CIENCIAS MDICAS
Manual de Laboratorio de Microbiologa
MIC: Concentracin Inhibitoria Mnima, MBC: Concentracin Bactericida Mnima.
Interpretacin de las Pruebas, Susceptibilidad o Resistencia:
En la interpretacin de resultados de cualquiera de estos mtodos, las bacterias se
consideran como susceptibles, medianamente susceptibles (susceptibilidad intermedia) o
resistentes a los antimicrobianos.
Susceptible (S): esta condicin del microrganismo significa que puede tratarse la
infeccin con las dosis habitualmente recomendadas.
Susceptibilidad intermedia (I): significa que el agente responde a dosis mayores
del antimicrobiano, cercanas a la concentracin plasmtica. En esta condicin la
respuesta a la terapia puede ser deficiente, pero puede mejorar con dosis mayores
o en sitios donde el antimicrobiano se concentra (como las quinolonas en la orina).
Resistente (R): el agente infeccioso tiene mecanismos de resistencia contra el
antimicrobiano, o el agente se encuentra fuera del espectro de accin del
antimicrobiano. En este caso, el microrganismo no sera inhibido durante la
terapia.
La caracterstica de S, I o R de un agente infeccioso frente a un antimicrobiano se
determina con proyeccin a la concentracin plasmtica mxima alcanzada por la dosis del
antimicrobiano. En otras palabras, no puede considerarse susceptible a un microrganismo si la CIM
es mayor que la alcanzada en el plasma.
Como la CIM es un antecedente que no siempre se adjunta al resultado de la prueba de
susceptibilidad, se hace necesario establecer un consenso o punto de corte para establecer la
condicin S, I, o R que finalmente aparecer en el informe de resultados. En el caso de las pruebas
por difusin en agar, el punto de corte es la medida del dimetro del halo de inhibicin, en
milmetros, lo que es una medida indirecta de la CIM. El el caso de los mtodos por dilucin, el
punto de corte corresponde a la misma CIM. Puedes ver un ejemplo de los puntos de corte en la
tabla de susceptibilidad adjunta en las pginas 60 y 61.
67
FACULTAD DE CIENCIAS MDICAS
Manual de Laboratorio de Microbiologa
Como regla general, en una condicin teraputica la concentracin plasmtica del
antimicrobiano debe ser entre dos y cuatro veces ms alta que la CIM, para asegurar la eficacia
clnica del tratamiento. La siguiente imagen describe cmo los niveles plasmticos de un
antimicrobiano exceden el valor de la CIM y disminuyen con el tiempo entre dosis.
El paciente tendr una dosis de cobertura
del antimicrobiano hasta que la concentracin
plasmtica caiga bajo la CIM, momento en el que
puede ser necesario administrar otra dosis.
El antibiograma por Mtodo de Difusin en Agar:
La forma ms usada, rpida y sencilla de conocer el espectro de susceptibilidad de un
agente infeccioso es el antibiograma por difusin en agar descrito por Kirby y Bauer. En este caso,
se trata de una prueba in vitro estandarizada, til para el estudio de bacterias poco exigentes de
rpido desarrollo y con identidad que implica una susceptibilidad poco predecible, capaces de
desarrollar resistencia. No obstante lo anterior, existen muchos agentes bacterianos que an
poseen susceptibilidad predecible y permiten la instalacin de terapias empricas, pero no se
descarta para ellos la aparicin de resistencia por lo que podran someterse a este tipo de prueba.
Adems, este tipo de estudios puede aplicarse como screening epidemiolgico para
evaluar la resistencia a los antimicrobianos en la comunidad, y para la bsqueda de nuevos
agentes inhibidores que podran tener uso teraputico.
Esta prueba con algunas modificaciones puede ser aplicada para otros microrganismos de
mayor exigencia. Las condiciones de estandarizacin se evalan permanentemente por el CLSI. La
recomendacin general es realizar el cultivo primario y seleccionar una colonia del agente
sospechoso para el estudio. No es aconsejable el estudio de ms de un agente simultneamente.
El estudio de susceptibilidad por siembra directa de muestras primarias debe dejarse solo para
aquellos casos de extrema urgencia, donde la tincin Gram demuestra la presencia de un solo
microrganismo (en muestras de lquidos biolgicos normalmente estriles, o en orina). En este
caso, la prueba debe posteriormente repetirse a modo de confirmacin con el agente ya aislado
mediante cultivo.
68
FACULTAD DE CIENCIAS MDICAS
Manual de Laboratorio de Microbiologa
El fundamento bsico de la prueba consiste en la difusin pasiva de antimicrobianos
cargados en discos de papel en concentraciones fijas (potencia del disco), la que se produce en un
medio de cultivo slido (Agar Mueller Hinton II) donde se ha sembrado la bacteria en estudio. Tras
un perodo de incubacin de 12 a 18 horas, es posible observar los efectos de los antimicrobianos
como halos de inhibicin del desarrollo bacteriano.
La medida del dimetro de los halos es
una representacin indirecta de la CIM, la
concentracin del antimicrobiano es menor a
mayor distancia del disco. En otras palabras, si
el dimetro es muy grande, la CIM es muy baja.
Los discos de antimicrobianos se eligen
de acuerdo al agente microbiano, el sitio de la
infeccin y los antecedentes del paciente. De esta
forma podemos concebir antibiogramas para agentes Gram negativos aislados de orina, de
secreciones, para Gram positivos, para bacilos no fermentadores, etctera.
De acuerdo a lo anterior, en el informe de un antibiograma tipo deberamos encontrar
informacin respecto de los siguientes antimicrobianos (la siguiente tabla no constituye una
norma sino una orientacin):
Enterobacteriaceas
Ampicilina
Cefazolina o
cefalotina
Gentamicina
Amikacina
Amoxicilina ac. Clavulnico o
Ampicilina sulbactam o
Trimetoprim sulfametoxazol
Ciprofloxacino
Cefoperazona o
Cefoxitina
Imipenem o
Meropenem
Cefotaxima o
Ceftriaxona
Antibiograma para bacterias comunes
Pseudomonas
Staphylococcus sp.
aeurginosa
Piperacilina o
Penicilina
Ticarcilina o
Mezlocilina
Ceftazidima
Oxacilina
Gentamicina
Amikacina
Cefoperazona
Cefepime
Ciprofloxacino
Aztreonam
Enterococcus sp.
Penicilina
Ampicilina
Eritromicina o
Claritromicina o
Azitromicina
Vancomicina
Linezolid
Clindamicina
Linezolid
Trimetoprim
sulfametoxazol
Quinupristia/Dalfopristina
Vancomicina
Imipenem o
Meropenem
Tobramicina
69
FACULTAD DE CIENCIAS MDICAS
Manual de Laboratorio de Microbiologa
Antibiograma para bacterias comunes, suplementario para uropatgenos
Enterobacteriaceas
Pseudomonas
Staphylococcus sp.
Enterococcus sp.
aeurginosa
Nitrofurantona
Carbenicilina
Nitrofurantona
Nitrofurantona
Lomefloxacino o
Levofloxacino o
Ciprofloxacino o
Norfloxacino
Norfloxacino
Levofloxacino o
Norfloxacino
Ceftixozima
Tetraciclina
Tetraciclina
El primer grupo de antimicrobianos (celdas azules) debiera aparecer en un antibiograma
tipo para los agentes esta tabla. El segundo grupo de antimicrobianos (verde), tambin se agrega
a la prueba de susceptibilidad, pero se incluyen en forma selectiva (ejemplo: para Escherichia coli,
se informar Cefotaxima o Ceftriaxona, para Staphylococcus aureus se informar Eritromicina o
Claritromicina o Azitromicina). Es pusible inclur otros antimicrobianos suplementarios en la
prueba.
En el caso de bacterias aisladas de orina, a los dos primeros grupos de antimicrobianos se
pueden sumar algunos adecuados para el tratamiento de infecciones del tracto urinario.
Factores que afectan la calidad de los resultados del antibiograma por difusin:
A pesar de tratarse de un mtodo muy bien estandarizado, existen varios factores que
pueden alterar los resultados, lo que puede llevar a errores de interpretacin con efectos en el
xito del tratamiento.
Valor del pH: El pH del medio de cultivo debe situarse en un rango de 7,2 a 7,4. Valores
fuera de rango puedan aumentar o disminuir la potencia del antimicrobiano. Los
aminoglucsidos, quinolonas y macrlidos disminuyen su potencia en pH cido, en tanto
que la Tetraciclina aumenta.
Humedad:
El exceso de humedad, por mala absorcin del inculo o por efecto de
agua de condensacin sobre el agar, pueden provocar una alteracin en la difusin del
antimicrobiano, generando halos de inhibicin imprecisos o de tamaos aumentados.
Concentracin de Timina y Timidina: Una cantidad aumentada de timina y timidina en el
medio de cultivo puede impedir la accin inhibitoria del Trimetoprim y las Sulfonamidas,
generando halos de inhibicin pequeos o anulndolos. Esta condicin podra generar un
informe de falsa resistencia a esos antimicrobianos. La prueba de calidad para este
aspecto se realiza con una cepa de Enterococcus faecalis ATCC 29212 o ATCC 33186, las
que deben dar un halo de inhibicin superior a 20 mm.
70
FACULTAD DE CIENCIAS MDICAS
Manual de Laboratorio de Microbiologa
Concentracin de Cationes divalentes: La concentracin de Ca++ y de Mg++ puede afectar
la potencia de los aminoglucsidos y tetraciclina. Una baja concentracin de estos
cationes genera halos de inhibicin de mayor tamao, y lo contrario ocurre con las altas
concentraciones. La prueba de calidad se realiza con Pseudomonas aeruginosa ATCC
27853, que debe dar un halo de inhibicin entre 16 y 21 mm.
Conservacin de los sensidiscos:
La potencia de los sensidiscos est estandarizada,
para mantenerla es necesario conservar los sensidiscos en refrigeracin, congelando el
stock de reserva. La potencia est garantizada solo hasta la fecha de expiracin indicada
por el fabricante.
Concentracin del inculo:
Para realizar la prueba de susceptibilidad por difusin es
necesario sembrar una suspensin estandarizada de la bacteria en toda la superficie el
agar. La suspensin del agente se prepara en Caldo Mueller Hinton o Caldo Soya tripticasa,
con una cantidad de bacterias que determine una turbidez equivalente al Standard
MacFarland 0.5, o a su equivalente medido por turbidimetra (absorbancia de 0.08 a 0.10 a
625 nm). La cantidad de bacterias que se obtiene es aproximadamente 1 a 2x108 UFC/mL.
Inculos ms concentrados pueden saturar la prueba y originar halos imprecisos o ms
pequeos. Inculos ms diluidos producen halos de bordes indefinidos.
Siembra del agar:
La siembra debe cubrir la totalidad de la superficie, y debe ser
homognea. Esto genera halos de bordes definidos que facilitan la lectura
Profundidad del agar: La difusin ocurre en todos los sentidos desde el disco impregnado
con antimicrobiano. Si la capa de agar es muy gruesa hay mayor difusin hacia el fondo y
menor hacia la periferia, lo que genera halos ms pequeos. Lo contrario ocurre con agar
muy delgado, donde se producen halos muy grandes. El espesor ideal del medio de cultivo
es de 5.0 +/- 0.3 mm. Este aspecto es de alta importancia, porque toda la prueba se ve
afectada, generando falsos susceptibles o resistentes si el agar es muy delgado o grueso
respectivamente.
Distancia entre los discos:
Los discos deben tener una distancia de unos 2.5 cm entre
ellos, para asegurar que los halos de inhibicin no se sobrepongan. Para una placa Petri de
90 mm es aconsejable hasta seis discos, y para una de 140 mm hasta 10 discos. La difusin
ocurre desde el primer contacto con el agar, por lo que los discos no se deben relocalizar.
Frmula del medio de cultivo y caractersticas biolgicas del agente: El Agar Mueller
Hinton II es un medio de cultivo con pocos nutrientes, donde las bacterias comunes
(enterobacterias, Staphylococcus) se desarrollan sin problemas. Para realizar el
71
FACULTAD DE CIENCIAS MDICAS
Manual de Laboratorio de Microbiologa
antibiograma contra bacterias fastidiosas es necesario suplementar la frmula o utilizar
otros medios de cultivo:
- Agar Mueller Hinton con sangre de cordero: Streptococcus pneumoniae,
Streptococcus beta hemolticos, Streptococcus sp. Viridans.
- Agar Mueller Hinton Chocolate: Neisserias patgenas, Haemophilus sp.
- Agar HTM: Haemophilus sp.
Si quieres ms datos de este tema: http://www.ispch.cl/lab_sal/doc/manual_susceptibilidad.pdf Prueba de
Susceptibilidad Antimicrobiana por Difusin en Agar. Instituto de Salud Pblica de Chile.
Ejercicios de Aplicacin de Contenidos
1.- Un paciente presenta una infeccin de herida operatoria causada por Enterococcus faecalis,
Qu antibiticos no deben faltar en el estudio de susceptibilidad de este agente? Para este caso
clnico, cul te parece el ms importante?
2.- En una infeccin urinaria se aisla Escherichia coli que se prueba
frente a Ciprofloxacino, con un halo de inhibicin de 14 mm. Si el
pH del Agar Mueller Hinton es 6.3, cul sera la condicin S, I, o R
del agente?, cmo lo confirmaras?.
3.- A un paciente febril se le asla Streptococcus pneumoniae de
una toma seriada de hemocultivos, en qu medio de cultivo se
debe hacer el antibiograma por difusin?
Hay reglas sencillas para el
uso de la Penicilina:
Usarla slo para los microbios
que sean vulnerables a ella,
aplicar la dosis indicada y que
el tratamiento dure lo
suficiente para eliminar la
infeccin; siguiendo estas
reglas, todos quedarn
satisfechos; de lo contrario, el
resultado ser decepcionante.
Alexander Fleming (1881 1955)
Premio Nobel de Medicina 1945
4.- Para el caso anterior, si quieres usar Penicilina, cul sera el
mtodo ms recomendado para determinar la susceptibilidad de
Streptococcus pneumoniae frente a ese antibitico? Para una
excelente respuesta consulta la referencia:
http://www.scielo.cl/pdf/rci/v17n2/art11.pdf Recomendaciones para el estudio de
susceptibilidad in vitro de Streptococcus pneumoniae
5.- Explica por qu una concentracin alta de timina y timidina en
el Agar Mueller Hinton origina halos reducidos con el
antimicrobiano Trimetoprim sulfametoxazol.
72
FACULTAD DE CIENCIAS MDICAS
Manual de Laboratorio de Microbiologa
Actividad n12:
Determinacin de la susceptibilidad a los antimicrobianos mediante
difusin en agar. Mtodo de Kirby-Bauer en Agar Mueller Hinton.
Objetivo:
Conocer y practicar la determinacin de susceptibilidad mediante el
mtodo de Kirby-Bauer.
Materiales y mtodo: Los alumnos pueden realizar la determinacin con una de las tres bacterias
de la actividad n8.
Se requiere de Agar Mueller Hinton y Caldo Mueller Hinton.
Trulas estriles.
Multidisco de antimicrobianos (calibrado).
Mechero.
Regla milimetrada.
Tablas de susceptibilidad (pgina 57 y 58).
Bioseguridad:
Use guantes. Mechero encendido.
No olfatee ni exponga innecesariamente los cultivos. No coma.
En caso de derrame o contacto avise al profesor. No acte por iniciativa
propia.
Lvese las manos antes de dejar el laboratorio.
Desarrollo:
- Con el asa de siembras estril y fra, tome una cantidad pequea de la
bacteria a probar, y prepare una suspensin muy suave en Caldo Mueller
Hinton.
- Impregne una trula estril con la suspensin microbiana, y cubra con sta
toda la superficie del Agar Mueller Hinton. No debe dejar ningn espacio sin
siembra. Espere a que la superficie est seca.
- Coloque un multidisco de antimicrobianos (los discos de papel en contacto
con el agar) de forma centrada en la placa. Presione ligeramente para
asegurar el contacto.
- Incubar 24 horas a 35 a 37C.
- Mida el dimetro de los halos de inhibicin y compare las medias con la
tabla de susceptibilidad que se adjunta.
- Informe la susceptibilidad para cada antimicrobiano: S (susceptible) o R
(resistente).
Antibiograma por el mtodo de difusin en
agar segn Kirby-Bauer.
73
FACULTAD DE CIENCIAS MDICAS
Manual de Laboratorio de Microbiologa
PUNTOS DE CORTE
HALOS DE INHIBICION ESTANDARES (segn N. C. C. L. S.)*
REVISION ENERO 2004 ,M100-S14 VOL.24 N 1
AGENTE ANTIMICROBIANO
SIGLA
POTENCIA
RESISTENCIA
SUSCEPTIBLE
AMIKACINA
AK
30 mcg
AMPICILINA
10 mcg
14 mm
13 mm
17 mm
17 mm
AMPICILINA-SULBACTAM
SAM
10/10 mcg
AMOXICILINA
AX
25 mcg
AMOX- AC.CLAVULANICO
AMC
20/10 mcg
ACIDO NALIDIXICO
30 mcg
ACIDO OXOLINICO
2 mcg
ACIDO PIPEMIDICO
PI
20 mcg
AZITROMICINA
AZT
15 mcg
AZTREONAM
AZ
30 mcg
CEFADROXILO
CPH
30 mcg
CEFALEXINA
CN
30 mcg
CEFALOTINA
CF
30 mcg
CEFAZOLINA
CEZ
30 mcg
CEFAMANDOL
CMA
30 mcg
CEFEPIME
CPM
30 mcg
CEFIXIMA
CFM
5 mcg
CEFOPERAZONA
CFP
75 mcg
CEFOTAXIMA
CTX
30 mcg
CEFOXITINA
CXA
CEFPROZIL
CEFRADINA
(28)*(18)H(16)E(23)Sb
(29)*(22)H(17)E(24)Sb
11 mm (19)H
11 mm
13 mm (19)* (19)H
13 mm
10 mm
13 mm
13 mm (11)H
15 mm (25)H
14 mm
14 mm
14 mm
14 mm
14 mm
14 mm
15 mm (20)H
14 mm
18 mm (20)*(20) H
19 mm
11 mm
19 mm
18 mm (12)H
22 mm (26)H
18 mm
18 mm
18 mm
18 mm
18 mm
18 mm
(30)N(25)H(23)Sb(21)Sv
(31)N(26)H(24)Sb(24)Sv
15 mm (20)H(30)N
15 mm
14 mm
19 mm (21)H(31)N
21 mm
23 mm
30 mcg
(25)H(30)N(23)Sb(25)Sv
14 mm (23)N
(26)H(31)N(24)Sb(28)Sv
18 mm (28)N
CPR
30mcg
14mm
CD
30 mcg
CEFTAZIDIMA
CAZ
30 mcg
14 mm
14 mm
18mm
18 mm
18 mm (26)H(31)N(21)B
CEFTRIAXONA
CTR
30 mcg
13 mm
(25)H(30)N(17)B
CEFUROXIMA i v
CXM
30 mcg
CIPROFLOXACINO
CIP
5 mcg
CLARITROMICINA
CLR
15 mcg
CLINDAMICINA
2 mcg
CLORANFENICOL
30 mcg
CLOXACILINA
CX
1 mcg
COLISTIN
CL
10 mcg
21 mm
(25)H(24)Sv(23)Sb(34)N
(26)H(27)Sv(24)Sb(35)N
14 mm (16)H(25)N
15 mm (20)H(27)N
13 mm
18 mm (20)H(31)N
21 mm (21)H(41)N
18 mm (13)H(21)$(21)
(10)H(16)$(16)S
14 mm (15)S(15)$
12 mm
21 mm (19)S(19)$
18 mm (21)S(29)H(21)$
(17)S(25)H(20)$
DICLOXACILINA
DX
1mcg
DOXICICLINA
DXS
30mcg
ENOXACINO
10 mcg
10 mm
8 mm
10 mm
12 mm
14 mm (31)N
13 mm
11 mm
13mm
16 mm
18 mm (36)N
74
FACULTAD DE CIENCIAS MDICAS
Manual de Laboratorio de Microbiologa
ERITROMICINA
EM
15 mcg
ESTREPTOMICINA
10 mcg
FOSFOMICINA
FO
200 mcg
FLEROXACINO
FLX
5 mcg
FURAZOLIDONA
FZ
100 mcg
GENTAMICINA
GE
10 mcg
KANAMICINA
30 mcg
LEVOFLOXACINO
LVX
5 mcg
LINCOMICINA
2 mcg
LINEZOLID
LZD
30 mcg
MEROPENEM
MRP
10 mcg
MOXIFLOXACINO
MXF
5 mcg
NEOMICINA
30 mcg
NITROFURANTOINA
NIT
300 mcg
NORFLOXACINO
NOR
10 mcg
OFLOXACINO
FLX
5 mcg
OXACILINA
OX
1 mcg
PENICILINA
10 UOF
PIPERACILINA
PE
100 mcg
PIPERAC/TAZOBACTAM
TZ
100/10 MCG
RIFAMPICINA
5 mcg
ROXITROMICINA
RXT
15 mcg
SULFATRIMETOPRIM
SX
25 mcg
SULFONAMIDA
SF
250 mcg
SULPERAZONA
SFP
30/75 mcg
TEICOPLANINA
TEI
TETRACICLINA
13 mm (15)S(15)$
11 mm
12 mm
15 mm (18)H(28)N
14 mm
12 mm
13 mm
13 mm (16)H
16 mm
20 mm
13 mm (19)H(15)B
15 mm (17)H(14)$
12 mm
14 mm
12 mm
12 mm(24)N
19 mm$ (10)*(17)**
19 mm (28)*(26)N
23 mm (21)S(21)$
15 mm
16 mm
19 mm (19)H(35)N
17 mm
15 mm
18mm
17 mm
21 mm
21 mm (23)E
16 mm(20)H(20)B
19mm (18)HS$
17 mm
17 mm
17 mm
16 mm(31)N
20 mm$(13)*(18)**
20 mm
(14)E(23)Sb
$(29)*(47)N(15)E(24)Sb
17 mm
17 mm
16 mm
13 mm
10 mm (15)$
12 mm
15 mm
21 mm (18)P
21 mm (18)P(18)*
20 mm(19)$
23 mm
16 mm (19)$
17 mm
21 mm
30 mcg
<10 mm
>14 mm
30 mcg
14 mm
19 mm
(18)S(18)$(30)N(25)H
(23)S(23)$(38)N(29)H
TOBRAMICINA
TB
10 mcg
TRIMETOPRIM
TMP
5 mcg
VANCOMICINA
VA
30 mcg
* Staphylococcus sp.
** Staphylococcus coagulasa (-)
P Ps. aeruginosa
E Enterococcus sp.
S Streptococcus sp.
Sv Streptococcus sp. Viridans
$ Streptococcus pneumoniae
B B. Cepacia
12 mm
15 mm
10 mm
16 mm
16 mm(14)*(14)E(14)S 17 mm$(15)*(15)S
H Haemophilus sp.
N Neisseria gonorrhoeae
Sb Streptococcus Beta Hemoliticos
*National Committee for Clinical Laboratory Standards.
Esta tabla de determinacin de susceptibilidad se incluye con fines didcticos, para efectos de uso clnico deben consultarse los
manuales actualizados por el CLSI (Clinical Laboratory Standards Institute). Los puntos de corte de susceptibilidad y resistencia se
revisan anualmente.
75
Вам также может понравиться
- Informe de BioseguridadДокумент16 страницInforme de BioseguridadRAUL ESCOBAR RAMIREZОценок пока нет
- (Texto Guia de Laboratorio de Microbiología UPV) PDFДокумент39 страниц(Texto Guia de Laboratorio de Microbiología UPV) PDFJuan Volta BellamyОценок пока нет
- BioseguridadДокумент4 страницыBioseguridadlautaroagustin440Оценок пока нет
- Bioseguridad Segun La Oms OpsДокумент47 страницBioseguridad Segun La Oms OpsSaarato ZerefОценок пока нет
- Bioseguridad en HospitalesДокумент92 страницыBioseguridad en HospitalesMargarita Torres0% (1)
- Preguntas BioseguridadДокумент3 страницыPreguntas BioseguridadrxnlrОценок пока нет
- Metodología para La Evaluación Del Riesgo Biológico.Документ9 страницMetodología para La Evaluación Del Riesgo Biológico.Cesar MayorgaОценок пока нет
- Bioseguridad Segun La Oms OpsДокумент47 страницBioseguridad Segun La Oms OpsMilagros Alfaro MendivelОценок пока нет
- IportanteДокумент21 страницаIportanteVictor Hugo Díaz SandovalОценок пока нет
- Riesgos químicos y biológicos en el trabajoДокумент17 страницRiesgos químicos y biológicos en el trabajosteffany cardenasОценок пока нет
- Informe de BioquiДокумент11 страницInforme de BioquiNIDWARD JUAN AGUILAR ESTANAОценок пока нет
- A1T3 - Luis Vásquez Javier ArturoДокумент26 страницA1T3 - Luis Vásquez Javier ArturoJAVIER ARTURO LUIS VASQUEZОценок пока нет
- Normas bioseguridad laboratorio químicaДокумент29 страницNormas bioseguridad laboratorio químicaSteep Junior Rodriguez LeonОценок пока нет
- NTP - 739 Inspecciones de Bioseguridad en LaboratoriosДокумент5 страницNTP - 739 Inspecciones de Bioseguridad en LaboratoriosDALTONОценок пока нет
- 1.1.8 Guía de BioseguridadДокумент13 страниц1.1.8 Guía de BioseguridadJulio H. Nuñez A.Оценок пока нет
- Manual de Bioseguridad-BacteДокумент12 страницManual de Bioseguridad-BacteLuisa FandiñoОценок пока нет
- 5 - Reactivos y BioseguridadДокумент36 страниц5 - Reactivos y BioseguridadEliana Alegria gonzalezОценок пока нет
- Objetivos:: Prácticas Microbiología MEHU-UPAOДокумент12 страницObjetivos:: Prácticas Microbiología MEHU-UPAOVictoriaJamancaAstoОценок пока нет
- Modelo de InformeДокумент12 страницModelo de InformeMaría CVОценок пока нет
- Procedimiento de Identificacion de Peligros y Evaluacion de Riesgos 2020Документ12 страницProcedimiento de Identificacion de Peligros y Evaluacion de Riesgos 2020BLANCA100% (2)
- BIOSEGURIDADДокумент5 страницBIOSEGURIDADhailingomez202044988Оценок пока нет
- Gestion de Riesgo BiologicoДокумент19 страницGestion de Riesgo BiologicoAlina Torres MateoОценок пока нет
- Informe de Bioseguridad en Un LaboratorioДокумент10 страницInforme de Bioseguridad en Un LaboratorioROSABELL RODRIGUEZ GUTIERREZОценок пока нет
- Bioseguridad Rodo 2Документ42 страницыBioseguridad Rodo 2coroscopОценок пока нет
- BIOSEGURIDAD EN EL LABORATORIO Trabajo Final Subir DriveДокумент18 страницBIOSEGURIDAD EN EL LABORATORIO Trabajo Final Subir DriveJandy LoyolaОценок пока нет
- Resumen BioseguridadДокумент3 страницыResumen BioseguridadANA PAOLA HERNANDEZ AGUILARОценок пока нет
- Analisis de RiesgoДокумент60 страницAnalisis de RiesgoNoemí RodríguezОценок пока нет
- GENERALIDADES DE LA BIOSEGURIDAD Romero FloresДокумент5 страницGENERALIDADES DE LA BIOSEGURIDAD Romero FloresDavid G. C VОценок пока нет
- BIOSEGURIDADДокумент26 страницBIOSEGURIDADRobinson Mora AngaritaОценок пока нет
- OMS Manual de Bioseguridad en EspañolДокумент12 страницOMS Manual de Bioseguridad en EspañolInmunoBlog100% (1)
- Laboratorio y BioseguridadДокумент34 страницыLaboratorio y BioseguridadAngie PamelaОценок пока нет
- Actividad 3 - Epidemiologia y Medicina LaboralДокумент10 страницActividad 3 - Epidemiologia y Medicina LaboralSOFFI TATIANA RODRIGUEZ MARTINEZОценок пока нет
- Resumen-Crítica-Bibliografía (GRUPO 6-Biología Teoría)Документ2 страницыResumen-Crítica-Bibliografía (GRUPO 6-Biología Teoría)MARCELA MARISOL VENTURA CASTILLOОценок пока нет
- Curso Seguridad y PrevenciónДокумент10 страницCurso Seguridad y PrevenciónJose Juan Gómez RamosОценок пока нет
- Semana 2 Asistencia en InmunizacionesДокумент22 страницыSemana 2 Asistencia en InmunizacionesFranklin De La CruzОценок пока нет
- Matriz de Riesgos TrabajoДокумент10 страницMatriz de Riesgos Trabajosebastian acostaОценок пока нет
- Vallejos Flores - PRUEBA ESCRITA, PRINCIPIOS GENERALES DE BIOSEGURIDADДокумент4 страницыVallejos Flores - PRUEBA ESCRITA, PRINCIPIOS GENERALES DE BIOSEGURIDADCARLA VALERIA VALLEJOS FLORESОценок пока нет
- InocuidadДокумент5 страницInocuidadAlexandra García RomeroОценок пока нет
- PGTH 03Документ7 страницPGTH 03Ortiz DaicyОценок пока нет
- Trabajo de BioseguridadДокумент15 страницTrabajo de BioseguridadAndrea Cecilia Escobar TrocheОценок пока нет
- BioseguridadДокумент36 страницBioseguridadJudith Paz VillegasОценок пока нет
- CLASEДокумент5 страницCLASEAnderson MorenoОценок пока нет
- Ingenieria Ambiental Y SaneamientoДокумент4 страницыIngenieria Ambiental Y SaneamientoJL FavОценок пока нет
- Tarea 1Документ5 страницTarea 1Jasmin Janeth Quintero MonrroyОценок пока нет
- Unidad1 - Fae1 - Preguntas Orientadoras - Juliancorral - Grupo - 151054 - 22Документ11 страницUnidad1 - Fae1 - Preguntas Orientadoras - Juliancorral - Grupo - 151054 - 22Julian CorralОценок пока нет
- Bioseguridad en La FarmaciaДокумент10 страницBioseguridad en La FarmaciaLau TarifaОценок пока нет
- Gestión del riesgo biológicoДокумент30 страницGestión del riesgo biológicoJessica AndreaОценок пока нет
- Manual Bioseguridad ISPCHДокумент46 страницManual Bioseguridad ISPCHJoão José Damian Salazar100% (1)
- Bioseguridad Segun La Oms, OpsДокумент47 страницBioseguridad Segun La Oms, OpsAlfa Johanny Santos71% (77)
- TEMA 18 Agentes Biológicos PDFДокумент10 страницTEMA 18 Agentes Biológicos PDFNaTy SierraОценок пока нет
- 1.nonografia de Bioseguridad en El LaboratorioДокумент19 страниц1.nonografia de Bioseguridad en El LaboratorioJhon Aguilar MarrerosОценок пока нет
- Identificación de Los Peligros y La Valoración de Los Riesgos en Seguridad y Salud OcupacionalДокумент14 страницIdentificación de Los Peligros y La Valoración de Los Riesgos en Seguridad y Salud OcupacionalMilena MedinaОценок пока нет
- IPERДокумент20 страницIPERcallojacqueline100% (1)
- Bioseguridad en EnfermeríaДокумент22 страницыBioseguridad en EnfermeríaArmando Carhuatocto100% (2)
- Bioseguridad Concepto de BioseguridadДокумент2 страницыBioseguridad Concepto de Bioseguridadputa materiaОценок пока нет
- Bio SeguridadДокумент5 страницBio SeguridadWillian Vasquez RuizОценок пока нет
- Anexo 17 Sve BiologicoДокумент14 страницAnexo 17 Sve BiologicoDiana RincónОценок пока нет
- Seguridad y medio ambiente en planta química. QUIE0108От EverandSeguridad y medio ambiente en planta química. QUIE0108Рейтинг: 5 из 5 звезд5/5 (1)
- Identificación de los productos y medios empleados para el control de plagas. SEAG0110От EverandIdentificación de los productos y medios empleados para el control de plagas. SEAG0110Оценок пока нет
- Nanociencia y biotecnologia. analisis de riesgo ambientalОт EverandNanociencia y biotecnologia. analisis de riesgo ambientalОценок пока нет
- Citación Asamblea Ordinaria N°3 06 11 22xДокумент1 страницаCitación Asamblea Ordinaria N°3 06 11 22xSebastian Montecinos ValenzuelaОценок пока нет
- Estimacion CRFДокумент1 страницаEstimacion CRFSebastian Montecinos ValenzuelaОценок пока нет
- Capacitación React Redux - Clase1Документ15 страницCapacitación React Redux - Clase1Sebastian Montecinos ValenzuelaОценок пока нет
- Instalación y uso básico de MongoDBДокумент12 страницInstalación y uso básico de MongoDBSebastian Montecinos ValenzuelaОценок пока нет
- Norma Tecnica 02032006pablaДокумент100 страницNorma Tecnica 02032006pablapabladonosoОценок пока нет
- Recursos A Descargar Capacitación React Módulo IIIДокумент1 страницаRecursos A Descargar Capacitación React Módulo IIISebastian Montecinos ValenzuelaОценок пока нет
- React Native ClaseДокумент1 страницаReact Native ClaseSebastian Montecinos ValenzuelaОценок пока нет
- Texto Guia de Laboratorio de Microbiología UPV Última Actualización PDFДокумент75 страницTexto Guia de Laboratorio de Microbiología UPV Última Actualización PDFSebastian Montecinos ValenzuelaОценок пока нет
- Informe Diseño Estructural Ptar Guacheta - v3Документ60 страницInforme Diseño Estructural Ptar Guacheta - v3Jhon CajicáОценок пока нет
- Taller - Minerales-Rocas IgneasДокумент4 страницыTaller - Minerales-Rocas IgneasAlejandro RodríguezОценок пока нет
- Et Pinturas MaritimasДокумент14 страницEt Pinturas MaritimasasproingenieriaОценок пока нет
- CIRANO - PLUS Hoja de SeguridadДокумент8 страницCIRANO - PLUS Hoja de Seguridadgerardo antonio cortes garciaОценок пока нет
- Deber Soldabilidad 201720 1Документ5 страницDeber Soldabilidad 201720 1Marilyn CoroОценок пока нет
- Determinación de Microorganismos en Los AlimentosДокумент34 страницыDeterminación de Microorganismos en Los AlimentosDaniel AguileraОценок пока нет
- DestilaciionДокумент8 страницDestilaciionupanafrayОценок пока нет
- Unidades de AlbañileríaДокумент129 страницUnidades de AlbañileríaYonatan Florian Alcantara100% (1)
- Resumen Guía Del Usuario Gre2016Документ14 страницResumen Guía Del Usuario Gre2016jesus2567% (3)
- Especificaciones Técnicas Trapa RascadoresДокумент40 страницEspecificaciones Técnicas Trapa RascadoresLuis ManuelОценок пока нет
- HS-049 Jabon Líquido Spray KCДокумент10 страницHS-049 Jabon Líquido Spray KCHAYDEEPEREZLOPEZОценок пока нет
- Defensa Exposición Procesos SedimentariosДокумент6 страницDefensa Exposición Procesos SedimentariosAlexandra ArteagaОценок пока нет
- Triptico La DrogadicciónДокумент2 страницыTriptico La DrogadicciónBraulio Quispe CaritaОценок пока нет
- Cocona DoДокумент141 страницаCocona DoDaliaParraPalaciosОценок пока нет
- Movimiento y control del humo en incendiosДокумент10 страницMovimiento y control del humo en incendiosclothyklОценок пока нет
- Gas SarinДокумент6 страницGas Sarinraul.ben.2020Оценок пока нет
- Un Metal de Interés Tecnológico - El AluminioДокумент3 страницыUn Metal de Interés Tecnológico - El AluminiolujulОценок пока нет
- Certificado de Calidad Chema PDFДокумент38 страницCertificado de Calidad Chema PDFCatherine Hinostroza100% (1)
- PCI Análisis Instrumental 2019Документ53 страницыPCI Análisis Instrumental 2019Luis alejandro Perez mercadoОценок пока нет
- Verificación pavimentación-checklistДокумент5 страницVerificación pavimentación-checklistMiguel Meza AlfaroОценок пока нет
- Copia de Procedimiento de Mandrilado General S-NДокумент16 страницCopia de Procedimiento de Mandrilado General S-NGerman DiBaccoОценок пока нет
- Cómo abrir una farmacia: guía paso a pasoДокумент101 страницаCómo abrir una farmacia: guía paso a pasoherbert14100% (1)
- Desacople PIB y Energía EspañolДокумент19 страницDesacople PIB y Energía EspañolmasanegraОценок пока нет
- Trabajo Fuerza Motriz T.Документ18 страницTrabajo Fuerza Motriz T.paulОценок пока нет
- Colaplex Goold MSDSДокумент11 страницColaplex Goold MSDSXavi PuigОценок пока нет
- Perfil HepáticoДокумент18 страницPerfil HepáticoMiriam Villanueva100% (1)
- Catálogo Gral LoctiteДокумент32 страницыCatálogo Gral LoctitepepopetaОценок пока нет
- Informe CalorДокумент4 страницыInforme CalorMauricio Andres Taborda MontañoОценок пока нет
- Abmg PDFДокумент18 страницAbmg PDFCinthia Padilla GallegosОценок пока нет
- Guia de Calor y Conduccion Termica 1 2018Документ3 страницыGuia de Calor y Conduccion Termica 1 2018Baruch_PrialeОценок пока нет