Академический Документы
Профессиональный Документы
Культура Документы
Lab Ley de Boyle
Загружено:
Isabella Rovira0 оценок0% нашли этот документ полезным (0 голосов)
78 просмотров2 страницыley de boyle
Авторское право
© © All Rights Reserved
Доступные форматы
DOCX, PDF, TXT или читайте онлайн в Scribd
Поделиться этим документом
Поделиться или встроить документ
Этот документ был вам полезен?
Это неприемлемый материал?
Пожаловаться на этот документley de boyle
Авторское право:
© All Rights Reserved
Доступные форматы
Скачайте в формате DOCX, PDF, TXT или читайте онлайн в Scribd
0 оценок0% нашли этот документ полезным (0 голосов)
78 просмотров2 страницыLab Ley de Boyle
Загружено:
Isabella Roviraley de boyle
Авторское право:
© All Rights Reserved
Доступные форматы
Скачайте в формате DOCX, PDF, TXT или читайте онлайн в Scribd
Вы находитесь на странице: 1из 2
Introduccin Impacto Social
Definicin de la Ley Boyle Un pequeo ejemplo de como la ley
de Boyle est presente en nuestro da
El volumen es inversamente
a da: Las llantas de los automviles
proporcional a la presin: Si la
deben mantener el aire a una presin
presin aumenta, el volumen
muy por encima de a presin
disminuye. Si la presin disminuye, el
atmosfrica para que puedan resistir
volumen aumenta.
el peso del vehculo. Cuando se
Por qu ocurre esto? pincha una llanta se escapa el aire
dentro de la llanta hasta que la
Al aumentar el volumen, las partculas presin interna es igual a la
(tomos o molculas) del gas tardan atmosfrica. La relacin cuantitativa
ms en llegar a las paredes del entre el volumen y la presin de una
recipiente y por lo tanto chocan menos muestra gaseosa se resume en la
veces por unidad de tiempo contra Ley de Boyle que dice: a temperatura
ellas. Esto significa que la presin ser constante, el volumen de una
menor ya que sta representa la muestra gaseosa varia inversamente
frecuencia de choques del gas contra con la presin ejercida sobre el gas.
las paredes. Cuando disminuye el
volumen la distancia que tienen que
recorrer las partculas es menor y por
Materiales
tanto se producen ms choques en
cada unidad de tiempo: aumenta la Ladrillos (4)
presin. Lo que Boyle descubri es Soporte
que si la cantidad de gas y la Jeringuillas de 50 mL
temperatura permanecen constantes,
el producto de la presin por el
volumen siempre tiene el mismo valor. Cuestionario
Como hemos visto, la expresin
matemtica de esta ley es: 1. Cmo afecta la presin la
PV = k (el producto de la presin por el densidad de los gases?
volumen es constante) Supongamos R: Segn la Ley de Boyle, el
que tenemos un cierto volumen de gas volumen de un gas mantenido a
V1 que se encuentra a una presin P1 temperatura constante, es
al comienzo del experimento. Si inversamente proporcional a la
variamos el volumen de gas hasta un presin. En palabras ms
nuevo valor V2, entonces la presin claras, a mayor presin menos
cambiar a P2, y se cumplir: volumen, y como la densidad
es masa entre volumen
P1V1 = P2V2 que es otra manera de llegamos a la conclusin de que
expresar la ley de Boyle. si la presin aumenta la
densidad aumenta.
2. Si deseas duplicar el ausencia de presin no dejara
volumen de n gas a de existir el volumen de una
temperatura constante, muestra.
Cmo modificara usted la
presin? 6. Compara la masa obtenida
R: A mayor presin menor por los clculos con el de la
volumen, entonces, se debe balanza
disminuir en un 50% la presin, R: Los ladrillos utilizados en el
para que suba el volumen. laboratorio traan su peso
escrito, por lo tanto no los
3. 3) Sin colocar materiales pesamos con la balanza.
sobre el embolo Cul es la
presin ejercida sobre el
gas? .
R: La Presin que se ejerce
sobre el embolo de la
inyectadora es la presin de 1
atm lo cual es igual a 753mmHg
4. Cuntos ladrillos se
necesitan para reducir el
volumen a la mitad?
R: Se necesitan 4 ladrillos para
reducir el volumen a la mitad.
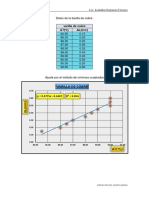
5. Analizando los grficos a
qu conclusin se puede
llegar?
R: -Grafica de presin contra
volumen:
Se puede observar la
comprensibilidad de los gases,
en este caso del aire, pues al
aplicar una fuerza que se
traduce a presin por la
definicin de esta (P=F/A) se
puede ver que sin molculas no
hay volumen, es decir, el
volumen es directo al nmero
de molculas.
-Grafica de presin contra 1/V:
La lnea de esta grafica no pasa
por el origen, ya que la
Вам также может понравиться
- Proyecto Final - Métodos Numéricos - RM, IRДокумент7 страницProyecto Final - Métodos Numéricos - RM, IRIsabella RoviraОценок пока нет
- M3 Programación Lineal IN A Actividad 3 Proyecto ModularДокумент8 страницM3 Programación Lineal IN A Actividad 3 Proyecto ModularEduardo Bertaud CastañedaОценок пока нет
- 1 Introducción Al Análisis de CircuitosДокумент24 страницы1 Introducción Al Análisis de CircuitosIsabella RoviraОценок пока нет
- Tema 6. Control Charts de ShewhartДокумент35 страницTema 6. Control Charts de ShewhartIsabella RoviraОценок пока нет
- Tema 9. Interpretación y Causas de InestabilidadДокумент13 страницTema 9. Interpretación y Causas de InestabilidadIsabella RoviraОценок пока нет
- Codigo y Circuito Proyecto FinalДокумент4 страницыCodigo y Circuito Proyecto FinalIsabella RoviraОценок пока нет
- Distribución Muestral de La VarianzaДокумент13 страницDistribución Muestral de La VarianzaIsabella RoviraОценок пока нет
- Proyecto Final - Instrumentación - Ac, Ir, AvДокумент14 страницProyecto Final - Instrumentación - Ac, Ir, AvIsabella RoviraОценок пока нет
- FitoprotecciónДокумент12 страницFitoprotecciónIsabella RoviraОценок пока нет
- Examen SEMESTRAL 2021Документ4 страницыExamen SEMESTRAL 2021Isabella RoviraОценок пока нет
- Investigación - Parcial 2 - MC, JG, KG, JJ, IrДокумент18 страницInvestigación - Parcial 2 - MC, JG, KG, JJ, IrIsabella RoviraОценок пока нет
- Anteproyecto Física IIДокумент5 страницAnteproyecto Física IIIsabella RoviraОценок пока нет
- Asignación #1 LaboratorioДокумент5 страницAsignación #1 LaboratorioIsabella RoviraОценок пока нет
- Asignación #2 Tabla de Las 14 Redes de BravaisДокумент4 страницыAsignación #2 Tabla de Las 14 Redes de BravaisIsabella Rovira0% (1)
- Asignación Nº3 Cristales CerámicosДокумент6 страницAsignación Nº3 Cristales CerámicosIsabella RoviraОценок пока нет
- Laboratorio Mecanica de Materiales GraficasДокумент9 страницLaboratorio Mecanica de Materiales GraficasIsabella RoviraОценок пока нет
- Formato para Entrega de Informes (Industrial)Документ7 страницFormato para Entrega de Informes (Industrial)Isabella RoviraОценок пока нет
- Guía 1. Matemáticas 6°Документ5 страницGuía 1. Matemáticas 6°Archivo CenturyОценок пока нет
- Laboratorio 01 Fisica-Dilatación Terminado UnschДокумент6 страницLaboratorio 01 Fisica-Dilatación Terminado UnschjersonОценок пока нет
- Quimica4 U1 Cap10 PDFДокумент14 страницQuimica4 U1 Cap10 PDFgisela frolaОценок пока нет
- Verificación de Instrumentos para Pesar de Alto Alcance De.Документ9 страницVerificación de Instrumentos para Pesar de Alto Alcance De.lizarazojavierОценок пока нет
- Representacion Del ProcesoДокумент5 страницRepresentacion Del ProcesoNatalia AmayaОценок пока нет
- Informe CONAMIN 2018Документ13 страницInforme CONAMIN 2018César EstrellaОценок пока нет
- Ejemplos de Diagramas de Ishikawa y ParetoДокумент7 страницEjemplos de Diagramas de Ishikawa y ParetoMarleny Guerra Huanchi100% (1)
- Procedimiento Basico para Estadistica DescriptivaДокумент3 страницыProcedimiento Basico para Estadistica DescriptivaAngelicaОценок пока нет
- Evau Madrid 2018. Matemáticas II. Opción A.Документ6 страницEvau Madrid 2018. Matemáticas II. Opción A.fvd71Оценок пока нет
- Geometria y TrigonometriaДокумент24 страницыGeometria y TrigonometriaOsvaldo CortesОценок пока нет
- Tema 1 - Determinantes TeoriaДокумент8 страницTema 1 - Determinantes TeoriaJuan daniel Torrez vidaurreОценок пока нет
- Clase 5 - Fundamentos de Geometría DescriptivaДокумент30 страницClase 5 - Fundamentos de Geometría DescriptivaLeonardo Concha RodriguezОценок пока нет
- Ejercicios de ModelamientoДокумент2 страницыEjercicios de ModelamientoAlejandra SilvaОценок пока нет
- Manual de Autocad IIДокумент64 страницыManual de Autocad IIKaty RomeroОценок пока нет
- Actividad 4 Cuadro ComparativoДокумент4 страницыActividad 4 Cuadro ComparativoValeria ChavezОценок пока нет
- Jimenez Jasso Julio César Sistema de Ecuaciones LinealesДокумент7 страницJimenez Jasso Julio César Sistema de Ecuaciones Linealessnake jimenezОценок пока нет
- U11 Cuerpos GeométricosДокумент54 страницыU11 Cuerpos GeométricosMerche Auñon VillarОценок пока нет
- Clase 4 Medidas de Posicion Central - 1362 - 0Документ23 страницыClase 4 Medidas de Posicion Central - 1362 - 0José DuarteОценок пока нет
- Importancia de La Investigación CientíficaДокумент21 страницаImportancia de La Investigación CientíficaCarlos Mario OrtizОценок пока нет
- 2 GADE - Matematicas II - Tema 1Документ33 страницы2 GADE - Matematicas II - Tema 1Miguel PalaciosОценок пока нет
- Razonamiento AproximadoДокумент9 страницRazonamiento AproximadoXianju Yiang LiОценок пока нет
- Informe N°02 de Fisica IiДокумент14 страницInforme N°02 de Fisica IiALBERT JEREMY BRIONES PRADOОценок пока нет
- Informe de Laboratorio - Ley de Boyle - MariotteДокумент4 страницыInforme de Laboratorio - Ley de Boyle - MariotteDavid PeñaОценок пока нет
- Informe Doc1 AbejasДокумент33 страницыInforme Doc1 AbejasAaronОценок пока нет
- Hojas de Apoyo - CascarasДокумент19 страницHojas de Apoyo - CascarasAlejandro Flores PazОценок пока нет
- 4° Medio Matemática Medidas de Tendencia Central y de Posición Datos Agrupados EjemploДокумент9 страниц4° Medio Matemática Medidas de Tendencia Central y de Posición Datos Agrupados EjemploKenia HernandezОценок пока нет
- 05CALДокумент4 страницы05CALhectorhmath5346Оценок пока нет
- GuíaExBachExamenAdmision ESДокумент12 страницGuíaExBachExamenAdmision EScesaga0075102Оценок пока нет
- De Donde Vengo, Quien Soy y Hacia Donde Voy - Ricardo CentenoДокумент13 страницDe Donde Vengo, Quien Soy y Hacia Donde Voy - Ricardo CentenoRicardo Centeno GuevaraОценок пока нет