Академический Документы
Профессиональный Документы
Культура Документы
Ejercicios Fqi
Загружено:
Ricardo Arias CОригинальное название
Авторское право
Доступные форматы
Поделиться этим документом
Поделиться или встроить документ
Этот документ был вам полезен?
Это неприемлемый материал?
Пожаловаться на этот документАвторское право:
Доступные форматы
Ejercicios Fqi
Загружено:
Ricardo Arias CАвторское право:
Доступные форматы
1.
Se tiene un cilindro horizontal con dos mbolos mviles, de los cuales el de la izquierda
se mueve libremente y el de la derecha tiene un rozamiento equivalente de r = 0,2 bar.
Tanto el cilindro como los mbolos son adiabticos y con una seccin de A = 1 m2. Las
condiciones iniciales del gas son n = 10 mol de gas ideal con g = 1,4 , P1 = 1 bar, T1 = 300
K y presin atmosfrica P0 = 1 bar. A partir de este estado 1 se va a llegar un estado 2 y
despus a un estado 3 caracterizados por (a) Se comprime lentamente el gas empujando el
mbolo de la izquierda. Calcular las variables termodinmicas P T y V y la energa interna,
Q y W hasta que el mbolo de la derecha comience a moverse.
(b) Se continua comprimiendo lentamente el gas empujando el mbolo de la izquierda hasta
que se desplaza 0,5 m respecto a la posicin del estado 2. Calcular las variables
termodinmicas P T y V y la energa interna ,Q y W.
2. A partir de los siguientes datos
S(rmbico) + O2(g) SO2(g) Hreaccin= -296.06 kJ
S(monoclnico) + O2(g) SO2(g) Hreaccin= -296.36 kJ
Calcule el cambio de entalpia para la transformacin
S(rmbico) S(monoclnico)
3. Los valores para el agua del volumen molar y la capacidad calorfica molar a presin
constante son 18'0 cc/mol y 75'3 J K -1 mol-1, respectivamente. Adems = 2'07 . 10-4 K-1.
Calcular la disminucin de temperatura que se produce si el agua a 25'0C y 1000'0 atm se
lleva reversible y adiabticamente a 1'00 atm de presin. Suponer que es nulo
4. Se mezclan adiabticamente y a presin constante 10'0 gr. de hielo a -10'0C y 50'0 gr. de
agua a 30'0C. Cual es la temperatura final del sistema?. Para el agua lquida, C p es 1'00
cal/(K gr). Para el hielo Cp es 0'500 cal/(K gr) a 0'00C , H de fusin es 80'0 cal/gr a
0'00C. b) Si tenemos 50'0 gr de hielo a -10'0C y 50'0 gr de agua a 30'0C, Cual ser la
temperatura final? Habr hielo en el sistema?.
6. Para la reaccin 2 Hg (g) + O 2 (g) <==> 2 HgO (s) a 600K, Ho = - 71'5 Kcal e So = -
91'9 cal K-1 mol-1. Los Cp (molares) de O2 y HgO (s) corresponden a las ecuaciones,
respectivamente, 6'31 + 0'0023 T y 6'24 + 0'016 T cal K -1 mol-1 . Si consideramos los gases
como ideales: enuncia cuanto vale Cp (molar) para el Hg.
7. Un mol de un G.I. se expande isotermicamente desde (P1,V1, T) hasta (P2,V2,T) en una
etapa, frente a una P de oposicin constante e igual a P2. Si P1= 10 at, P2=5 at y T=300K,
Cul es el trabajo realizado por el sistema?
8. Si se lleva a cabo la misma expansin isotrmica, pero en 2 etapas, (P1,V1,T)
(P,V,T) (P2,V2,T), formular la expresin para el trabajo producido en trminos de T,
P1, P2 y P. Para qu valor de P es mximo el trabajo de expansin que se puede obtener
en estas dos etapas? Si el estado inicial y final del sistema es el mismo que en el problema
anterior, Cul es el trabajo mximo producido?
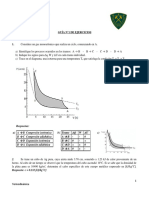
9. Un mol de un gas ideal monoatmico recorre el ciclo indicado en la figura segn las
etapas 1, 2 y 3 e implicando los estados A, B y C. Suponiendo que todas las etapas son
reversibles y que CV= 3/2R. Calcular Q, W, Uy H para cada proceso y para el ciclo.
10. El poder calorfico de los alimentos puede ser determinado midiendo el calor
producido al quemarse una cantidad de muestra del alimento en una bomba calorimtrica a
V constante. El calor desprendido en la combustin de 1gr (3.10-3 moles) de una muestra
grasa de pollo fue 10.000 cal a 37C. Calclese el poder calorfico en cal/gr a 37C y P
constante, sabiendo que la reaccin puede representarse por la ecuacin:
C20H32O2 (s) + 27 O2 (g) 20 CO2 (g) + 16 H2O (l)
11. Dados los calores de formacin y de combustin siguientes, y sabiendo que el calor de
vaporizacin del H2O a 298 K es de 10,5 Kcal/mol. Calcular el H y U para la reaccin a
298K:
CH3-COOH (l) + C2H5OH (l)CH3COOC2H5 (l) + H2O (l)
Hcombustion(CH3COOC2H5 (l)) = -536,9 Kcal/mol
Hf (CH3COOH (l)) = 116,7 Kcal/mol Hf (C2H5OH (l)) = 66,3 Kcal/mol
Hf (CO2 (g)) = -94,0 Kcal/mol Hf (H2O(g)) = -57,8 Kcal/mol
Вам также может понравиться
- Taller FQ Exam30f5Документ2 страницыTaller FQ Exam30f5Bryan BeleñoОценок пока нет
- Taller FisicoДокумент4 страницыTaller FisicoAndres MorenoОценок пока нет
- Ejercicios Capitulo 1 y 2Документ4 страницыEjercicios Capitulo 1 y 2jhanrataОценок пока нет
- Termodinámica problemas gases idealesДокумент2 страницыTermodinámica problemas gases idealesMiguel A. Aguilar VeraОценок пока нет
- Examen TermoДокумент19 страницExamen TermoDora A. ParraguezОценок пока нет
- TermodinamicsДокумент11 страницTermodinamicsJose Palomo0% (1)
- TallerДокумент4 страницыTallerYireth Beleño OrtizОценок пока нет
- Taller TermodinamicaДокумент5 страницTaller Termodinamicaapi-241769574Оценок пока нет
- Segunda Ley y Entropia TallerДокумент2 страницыSegunda Ley y Entropia TallerLaura Cristina BrandОценок пока нет
- PROBLEMAS I UnidadДокумент3 страницыPROBLEMAS I UnidadJorge VillegasОценок пока нет
- Tema 1.problemas Primer Principio (2016-2017)Документ4 страницыTema 1.problemas Primer Principio (2016-2017)Raquel Suárez López100% (1)
- Ejercicios Capitulo 1 y 2Документ4 страницыEjercicios Capitulo 1 y 2Julii TrochezОценок пока нет
- Guias FQI 2019 6 A 9 v2Документ12 страницGuias FQI 2019 6 A 9 v2Christian Iván Silva GarcíaОценок пока нет
- Fisica Quimica. Ejercicios Practico 16 y 17Документ3 страницыFisica Quimica. Ejercicios Practico 16 y 17Josse BPОценок пока нет
- Guía Termodinámica ProblemasДокумент8 страницGuía Termodinámica ProblemasyoshiwisОценок пока нет
- Problemas Bis 2013Документ3 страницыProblemas Bis 2013Emanuel TejadaОценок пока нет
- Segunda y tercera ley termodinámicaДокумент3 страницыSegunda y tercera ley termodinámicaeutectic1992Оценок пока нет
- Primera ley termodinámica: ejercicios de calor, trabajo y energía internaДокумент7 страницPrimera ley termodinámica: ejercicios de calor, trabajo y energía internaOleggValVilОценок пока нет
- Problemas Tema 2Документ2 страницыProblemas Tema 2José Rafael GuillénОценок пока нет
- Practica No 3 Calor Temperatura Termodinamica 1 - 2019Документ4 страницыPractica No 3 Calor Temperatura Termodinamica 1 - 2019Wilver VasquezОценок пока нет
- Unidad 2 - Termodinámica - EjerciciosДокумент10 страницUnidad 2 - Termodinámica - Ejerciciosʙʀᴀɴᴅᴏɴ ᴀᴅᴜᴠɪʀɪОценок пока нет
- Ejerccios Fisicoquimica Taller 1ra LeyДокумент2 страницыEjerccios Fisicoquimica Taller 1ra LeyBielka Pérez ʚïɞОценок пока нет
- 02 +primer+principio +calor,+trabajo+y+energía +reversibilidadДокумент5 страниц02 +primer+principio +calor,+trabajo+y+energía +reversibilidadMARÍA ISABEL PEREYRA TELLADOОценок пока нет
- Ejercicios 2do Principio Termodinámica 2019-IДокумент2 страницыEjercicios 2do Principio Termodinámica 2019-IRai Delgado Torres100% (1)
- Ejercicios Segunda Ley 2020-IIДокумент2 страницыEjercicios Segunda Ley 2020-IIStefany Elizabeth Crisostomo QuispeОценок пока нет
- Ejercicios Segunda Ley 2020-IIДокумент2 страницыEjercicios Segunda Ley 2020-IIStefany Elizabeth Crisostomo QuispeОценок пока нет
- Termoquimica y Primera Ley de La TermodinamicaДокумент4 страницыTermoquimica y Primera Ley de La TermodinamicaMariel :vОценок пока нет
- Ejercicios de Termo Exmaen 2 ParcialДокумент10 страницEjercicios de Termo Exmaen 2 ParcialerubielОценок пока нет
- Practica 1 Fisqca UcbДокумент4 страницыPractica 1 Fisqca UcbalexofigurinОценок пока нет
- Boletin n1Документ2 страницыBoletin n1ImaneОценок пока нет
- Cálculos de rendimiento y cambios de entropía para procesos termodinámicosДокумент6 страницCálculos de rendimiento y cambios de entropía para procesos termodinámicosDaniel NoreñaОценок пока нет
- Practico 2° y 3° LeyДокумент14 страницPractico 2° y 3° LeyBritney Nina arganaОценок пока нет
- Guía Fisicoquímica IДокумент3 страницыGuía Fisicoquímica ITania GachusОценок пока нет
- Problemas Propuestos para El Segundo ExamenДокумент5 страницProblemas Propuestos para El Segundo ExamenVictor V IeОценок пока нет
- Problem As MinasДокумент17 страницProblem As MinasDaniel GaeteОценок пока нет
- Gua N1 Termodinmica 2015Документ9 страницGua N1 Termodinmica 2015Elías Raphael Rubilar BugueñoОценок пока нет
- Guía 8 de Balance de Masa y EnergíaДокумент2 страницыGuía 8 de Balance de Masa y EnergíaJUAN ANDRÉS SANDOVAL HERRERA0% (1)
- Trabajo - Termodinamica PDFДокумент2 страницыTrabajo - Termodinamica PDFExamenesPorWhatsappОценок пока нет
- Enunciados Ejercicios Entregados en Clase Examen 1Документ6 страницEnunciados Ejercicios Entregados en Clase Examen 1Jennifer YataОценок пока нет
- Guía de TermodinámicaДокумент9 страницGuía de TermodinámicaJavier CortésОценок пока нет
- Ejercicios Tema 6 - 2016Документ3 страницыEjercicios Tema 6 - 2016Jack AnasagastiОценок пока нет
- Guia Numero 4Документ7 страницGuia Numero 4eutectic19920% (1)
- 03 Ejercicios de Sistemas Termodinámicos. Primera Ley de La Termodinámica y Tipos de Procesos TermodinámicosДокумент6 страниц03 Ejercicios de Sistemas Termodinámicos. Primera Ley de La Termodinámica y Tipos de Procesos TermodinámicosLuis Fernando Jeri Guillén40% (5)
- Ejercicios Intro TermodinamicaДокумент2 страницыEjercicios Intro TermodinamicaJohn AranzalesОценок пока нет
- Guía 1 PDFДокумент3 страницыGuía 1 PDFDaniel Andres Roa UmañaОценок пока нет
- Guía de Ejercicios Tema 3Документ4 страницыGuía de Ejercicios Tema 3Kleidder ZacariasОценок пока нет
- Guia de Problemas - Capitulo 5Документ17 страницGuia de Problemas - Capitulo 5Víctor Vázquez0% (1)
- 1o LeyДокумент4 страницы1o LeyneedformaxОценок пока нет
- Guia2 1 Ley TDДокумент5 страницGuia2 1 Ley TDCis FranОценок пока нет
- Problemas de Termotecnia sobre sistemas cerrados y abiertos con agua y gases idealesДокумент17 страницProblemas de Termotecnia sobre sistemas cerrados y abiertos con agua y gases idealesClaudio Pincheira RozasОценок пока нет
- Problemas Ingenieria QuimicaДокумент66 страницProblemas Ingenieria Quimicaelcazador_047Оценок пока нет
- Parcial4 Publicar PDFДокумент3 страницыParcial4 Publicar PDFJesus AguilarОценок пока нет
- Ejerccios Fisicoquímica - Taller 1ra Ley - FarmaciaДокумент3 страницыEjerccios Fisicoquímica - Taller 1ra Ley - FarmaciasaraОценок пока нет
- 3 TermodinamicaДокумент6 страниц3 TermodinamicaJordi López ClaràОценок пока нет
- Ingeniería química. Soluciones a los problemas del tomo IОт EverandIngeniería química. Soluciones a los problemas del tomo IОценок пока нет
- Teoría Del Gas Real: La Relación Exacta Para Gases RealesОт EverandTeoría Del Gas Real: La Relación Exacta Para Gases RealesОценок пока нет
- Informe Laboratorio Co2Документ7 страницInforme Laboratorio Co2Ricardo Arias CОценок пока нет
- Taller Clasificacion PDFДокумент1 страницаTaller Clasificacion PDFRicardo Arias CОценок пока нет
- Juzgados YopalДокумент1 страницаJuzgados YopalRicardo Arias CОценок пока нет
- Juzgados YopalДокумент1 страницаJuzgados YopalRicardo Arias CОценок пока нет
- Informe Laboratorio #2 WinogradskyДокумент12 страницInforme Laboratorio #2 WinogradskyRicardo Arias CОценок пока нет
- Clase de Ing Economica (ENVIAR A COMPAÑEROS)Документ13 страницClase de Ing Economica (ENVIAR A COMPAÑEROS)Ricardo Arias CОценок пока нет
- Informe Laboratorio Co2Документ7 страницInforme Laboratorio Co2Ricardo Arias CОценок пока нет
- Informe TopograficoДокумент15 страницInforme TopograficoRicardo Arias CОценок пока нет
- Microcompostaje en BotellaДокумент9 страницMicrocompostaje en BotellaRicardo Arias CОценок пока нет
- Taller Cambio ClimáticoДокумент8 страницTaller Cambio ClimáticoRicardo Arias CОценок пока нет
- Taller Ciclos BiogeoquimicosДокумент5 страницTaller Ciclos BiogeoquimicosRicardo Arias CОценок пока нет
- Mediciones ElectricasДокумент21 страницаMediciones ElectricasJosi SQueaОценок пока нет
- Informe 2023Документ7 страницInforme 2023Yenaro IzquierdoОценок пока нет
- IncrustacionesДокумент6 страницIncrustacionesValentina Gonzalez CabreraОценок пока нет
- Fichas TerminadasДокумент9 страницFichas TerminadasJHOMAR QUIROZОценок пока нет
- Listado de TesisДокумент5 страницListado de TesisOscar Enrique Andia MatosОценок пока нет
- NTC3384Документ55 страницNTC3384Arley Muñoz OrtizОценок пока нет
- UnidadIEstabilidadquimica 22162Документ13 страницUnidadIEstabilidadquimica 22162Morales LeónОценок пока нет
- Trabajo Domiciliario de Consolidacion 2019 CorregidoДокумент3 страницыTrabajo Domiciliario de Consolidacion 2019 CorregidoAnonymous 03TLwlОценок пока нет
- Ensayo Charpy IzodДокумент7 страницEnsayo Charpy IzodAntonio100% (9)
- Practica 1Документ12 страницPractica 1VladyОценок пока нет
- Control mamparas materialesДокумент2 страницыControl mamparas materialesFRANKОценок пока нет
- Evidencia 6 Proyecto Plan de Manejo Ambiental (PMA)Документ13 страницEvidencia 6 Proyecto Plan de Manejo Ambiental (PMA)Michael ToroОценок пока нет
- TUBERIA SprinklerДокумент4 страницыTUBERIA SprinklerNicolas CardonaОценок пока нет
- Balance energía etapa 5 ejercicios calorДокумент8 страницBalance energía etapa 5 ejercicios calorPaolita Carvajal FajardoОценок пока нет
- Hoja de seguridad sulfato ácido de sodioДокумент6 страницHoja de seguridad sulfato ácido de sodioVale Prado VargasОценок пока нет
- Procedimiento de Corte y Biselado de Planchas Por PlasmaДокумент6 страницProcedimiento de Corte y Biselado de Planchas Por PlasmaWaldomiroCanoОценок пока нет
- Nodo de AgregacionДокумент5 страницNodo de AgregacionDaniella HernándezОценок пока нет
- Tabla de Detracciones PDFДокумент1 страницаTabla de Detracciones PDFPablo Alejandro Martinez SilvaОценок пока нет
- Sistema de AlimentacionДокумент203 страницыSistema de AlimentacionJazmínAR100% (1)
- Gutierrez Alvarez AnaДокумент98 страницGutierrez Alvarez AnaCrippioОценок пока нет
- Alotropia QuimicaДокумент3 страницыAlotropia QuimicaGianpierre de la CruzОценок пока нет
- Gestión integral residuos sólidos Cuenca Matanza RiachueloДокумент15 страницGestión integral residuos sólidos Cuenca Matanza RiachueloNatiWallNutОценок пока нет
- Limpieza de superficies y mobiliarioДокумент77 страницLimpieza de superficies y mobiliarioFabiola ValentinОценок пока нет
- Tipos de rocas y minerales que las formanДокумент7 страницTipos de rocas y minerales que las formanReynaCarrilloОценок пока нет
- Catalogo Assa Abloy 2018Документ22 страницыCatalogo Assa Abloy 2018Juan Yovani Parada ArenasОценок пока нет
- El Cemento Dental de Este SigloДокумент9 страницEl Cemento Dental de Este SigloDayanaCastilloОценок пока нет
- Practica N°4 ChanzapaaДокумент5 страницPractica N°4 ChanzapaaGABY GAMES YTОценок пока нет
- Prelosas CeДокумент61 страницаPrelosas CemgОценок пока нет
- Alimentador SpaДокумент24 страницыAlimentador SpaCHRISTIAN ZAVALAОценок пока нет
- Proceso Frasch EXPOДокумент34 страницыProceso Frasch EXPOEdgar SilvaОценок пока нет
- El Arco EléctricoДокумент11 страницEl Arco EléctricoOriental EstereoОценок пока нет