Академический Документы
Профессиональный Документы
Культура Документы
Aporte - 1, Boris
Загружено:
Luis Carlos Zuñiga0 оценок0% нашли этот документ полезным (0 голосов)
13 просмотров6 страницОригинальное название
Aporte_1, boris.doc
Авторское право
© © All Rights Reserved
Доступные форматы
DOC, PDF, TXT или читайте онлайн в Scribd
Поделиться этим документом
Поделиться или встроить документ
Этот документ был вам полезен?
Это неприемлемый материал?
Пожаловаться на этот документАвторское право:
© All Rights Reserved
Доступные форматы
Скачайте в формате DOC, PDF, TXT или читайте онлайн в Scribd
0 оценок0% нашли этот документ полезным (0 голосов)
13 просмотров6 страницAporte - 1, Boris
Загружено:
Luis Carlos ZuñigaАвторское право:
© All Rights Reserved
Доступные форматы
Скачайте в формате DOC, PDF, TXT или читайте онлайн в Scribd
Вы находитесь на странице: 1из 6
UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA UNAD
Escuela de Ciencias Bsicas, Tecnologa e Ingeniera
Trabajo de Reconocimiento del curso Curso Bioqumica 201103
FORMATO PARA LA PRESENTACIN DE APORTES
Trabajo: Actividad 4: Trabajo Colaborativo 1
Nombre: BORIS LEON OSSA
Actividad a desarrollar: Pruebas cualitativas para la caracterizacin de
aminocidos en el laboratorio
Objetivo: Identificar los grupos funcionales en los aminocidos que ayudan a
reaccionar en la pruebas de caracterizacin en el laboratorio.
Contenido del aporte:
Leu-Lys-His-Asn-Met-Trp-Tyr
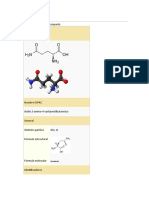
Estructura de cada aminocido que conforma el pptido. Indique el tipo de
aminocido que es de acuerdo a: s es cido, bsico, polar o apolar y de la
explicacin del por qu.
Leucina: Se clasifica dentro del grupo de aminocidos apolares, ya que el grupo
de su cadena lateral R se caracteriza por ser hidrofobico, es decir, repelente al
agua, por lo que el agua no la solvata con facilidad, se caracteriza tambin por
tener muchos enlaces C-C y C-H.
Lisina: Pertenece al grupo de los aminocidos bsicos, ya que su cadena lateral
esta protonada a pH fisiolgico.
UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA UNAD
Escuela de Ciencias Bsicas, Tecnologa e Ingeniera
Trabajo de Reconocimiento del curso Curso Bioqumica 201103
Histidina: Este aminocido se clasifica dentro del grupo de los aminocidos
bsicos, ya que su caracterstica se debe a que su cadena lateral tiene un grupo
nitrogenado.
Asparagina: Se clasifica dentro del grupo de aminocidos polares, ya que
contiene grupos amido que participan en la formacin d puentes de hidrogeno.
Metionina: Este aminocido pertenece al grupo Apolar, ya que en su cadena
lateral posee la caracterstica de hidrofobico debido a su grupo azufrado.
UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA UNAD
Escuela de Ciencias Bsicas, Tecnologa e Ingeniera
Trabajo de Reconocimiento del curso Curso Bioqumica 201103
Triptfano: Pertenece al grupo de los aminocidos Apolares los cuales son
hidrofobicos en su cadena lateral, y este aminocido tiene esa caracterstica por
su radical hidrocarburado.
Tirosina: Este aminocido se clasifica dentro del grupo de aminocidos polares,
debido a su grupo hidroxilo.
La reaccin implicada en la reaccin de reconocimiento.
- REACION DE NINHIDRINA Porque reacciona con todos los A.A a un pH
4-8. Formando compuesto de color purpura.
UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA UNAD
Escuela de Ciencias Bsicas, Tecnologa e Ingeniera
Trabajo de Reconocimiento del curso Curso Bioqumica 201103
- REACCION XANOPROTEICA Porque reacciona con el A.A. aromticos
como el Triptfano que est presente en el pptido formando
nitroderivados de color naranja.
- REACCION DE MILLON Porque reacciona con A.A. fenlicos como la
Tirosina presente en el pptido. Formando compuestos rojos.
- REACCION DE ACIDO GLIOXILICO PARA TRIPTOFANO Porque
reacciona con el triptfano, A.A. presente en el pptido, forma compuesto
color purpura
- PRUEBA DE PAULYPorque reacciona con las Aminas de la Lisina,
fenoles como Tirosina, imidazoles como la Histidina dando compuestos
fuertemente coloreados.
- REACCION DE EHRLICHPorque este reacciona con compuestos como
ndoles y aminas aromticas como Triptfano, dando compuestos
coloreados.
1b. Para el pptido dado: Caractersticas acido-bsicas
- Esquematizar la estructura, resaltando la formacin de las uniones
peptdicas.
- Extremo N-terminal y C-terminal
- Encierre en un crculo los grupos ionizables pptido y frente a cada una de
estos grupos coloque el valor de pK.
UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA UNAD
Escuela de Ciencias Bsicas, Tecnologa e Ingeniera
Trabajo de Reconocimiento del curso Curso Bioqumica 201103
- Presenten las diferencias que hay entre la forma de calcular el punto
isoelctrico de un aminocido individual y el punto isoelctrico de pptidos.
PUNTO ISOELECTRICO PUNTO ISOELECTRICO
AMINOACIDO PEPTIDOS
El punto Isoelctrico pI es el pH que Conocer el valor de cada uno de los
est en medio de los valores de pKs pKa de los N y C terminales, analizar
de ambos lados de In Zwiterin los que aminocido tiene grupos
cuales se suman y se dividen por ionizables en su cadena lateral y
dos tanto para A.A. Polares y No anotar pKa de la cadena R, se suma
Polares. y se divide por el nmero de valores
de pKs
2. En un experimento de laboratorio Usted completo un estudio de cintica
enzimtica, obteniendo los siguientes datos: Utilizando la metodologa de
Lineweaver- Burk.
El valor de Km y su debida interpretacin.
El valor de Vmx y Vmx/2 y su debida interpretacin.
UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA UNAD
Escuela de Ciencias Bsicas, Tecnologa e Ingeniera
Trabajo de Reconocimiento del curso Curso Bioqumica 201103
Conclusin: Con el desarrollo de este aporte se puede concluir que cada
aminocido posee caractersticas estructurales que permiten que se manifiesten
ante un medio de manera distinta, es decir cada aminocido se pude comportar
conforme este compuesto su cadena radical o grupo funcional, es esta la que
realmente le da el carcter y la clasificacin inica al aminocido.
Referencia bibliogrfica
Gerardo Prez, Yolanda Navarro. Universidad Nacional Abierta y a
Distancia. Duitama, 1992.
Saber es practico. 2014.
http://www.saberespractico.com/estudios/universidad/quimica/los-20-
aminoacidos-naturales-o-estandar/ (ltimo acceso: 27 de Marzo de 2014).
Mdulo Bioqumica 201103, Golda Meyer Torres Vargas (Directora
Nacional), Alberto Garca Jerez (Acreditador), Duitama enero de 2013,
Universidad Nacional Abierta y a Distancia UNAD.
Вам также может понравиться
- Apuntes de Logica Matematica-Razonamientos y DemostracionesДокумент27 страницApuntes de Logica Matematica-Razonamientos y DemostracionesLeire SaldivarОценок пока нет
- Manual Corel Draw X5Документ322 страницыManual Corel Draw X5jorgemosquete57% (7)
- Presupuesto Jarly PintoДокумент3 страницыPresupuesto Jarly PintoLuis Carlos ZuñigaОценок пока нет
- Guía de Actividades y Rúbrica de Evaluación - Fase 1 - Trabajo Estructura de La Materia y Nomenclatura PDFДокумент17 страницGuía de Actividades y Rúbrica de Evaluación - Fase 1 - Trabajo Estructura de La Materia y Nomenclatura PDFDayanita MartinezОценок пока нет
- Presupuesto Jarly PintoДокумент3 страницыPresupuesto Jarly PintoLuis Carlos ZuñigaОценок пока нет
- Actividad Unidad I Grupo201102 277Документ21 страницаActividad Unidad I Grupo201102 277Luis Carlos ZuñigaОценок пока нет
- Final Delitos IonformaticosДокумент2 страницыFinal Delitos IonformaticosLuis Carlos ZuñigaОценок пока нет
- Protocolo 3Документ1 страницаProtocolo 3Luis Carlos ZuñigaОценок пока нет
- Trabajo Quimica 1Документ11 страницTrabajo Quimica 1Jazmin Avella ChaparroОценок пока нет
- Presupuesto Jarly PintoДокумент12 страницPresupuesto Jarly PintoLuis Carlos ZuñigaОценок пока нет
- Presupuesto Jarly PintoДокумент12 страницPresupuesto Jarly PintoLuis Carlos ZuñigaОценок пока нет
- JeanetteCamacho REDES CCNA2 I 2018 LetterДокумент1 страницаJeanetteCamacho REDES CCNA2 I 2018 LetterLuis Carlos ZuñigaОценок пока нет
- Angel Ramos Aporte DiapoДокумент5 страницAngel Ramos Aporte DiapoLuis Carlos ZuñigaОценок пока нет
- William Hernan Rios Grupo12 Actividad 4Документ10 страницWilliam Hernan Rios Grupo12 Actividad 4Luis Carlos ZuñigaОценок пока нет
- Identificación de Modelos de Orden Reducido A Partir de La Curva de Reacción Del ProcesoДокумент20 страницIdentificación de Modelos de Orden Reducido A Partir de La Curva de Reacción Del ProcesoJorge GarciaОценок пока нет
- InstruccionesДокумент1 страницаInstruccionesLuis Carlos ZuñigaОценок пока нет
- Mi Ambiente FormativoДокумент4 страницыMi Ambiente FormativoLuis Carlos ZuñigaОценок пока нет
- Ple GablesДокумент2 страницыPle GablesLuis Carlos ZuñigaОценок пока нет
- Ejercicio Fase 2, Corresponde Al Numero 3Документ1 страницаEjercicio Fase 2, Corresponde Al Numero 3Luis Carlos ZuñigaОценок пока нет
- InstruccionesДокумент2 страницыInstruccionesMatías Farías OyarzúnОценок пока нет
- 1er Aporte MyrianДокумент2 страницы1er Aporte MyrianLuis Carlos ZuñigaОценок пока нет
- 1er Aporte Jose Luis RodriguezДокумент3 страницы1er Aporte Jose Luis RodriguezLuis Carlos ZuñigaОценок пока нет
- Jose Luis Rodriguez-Etapa1Документ9 страницJose Luis Rodriguez-Etapa1Luis Carlos ZuñigaОценок пока нет
- InstruccionesДокумент1 страницаInstruccionesLuis Carlos ZuñigaОценок пока нет
- 2.3.2.3 Lab - Configuring Rapid PVST William RiosДокумент15 страниц2.3.2.3 Lab - Configuring Rapid PVST William RiosLuis Carlos ZuñigaОценок пока нет
- PERFIL OCUPACIONAL Técnico en Análisis de SistemasДокумент1 страницаPERFIL OCUPACIONAL Técnico en Análisis de SistemasLuis Carlos ZuñigaОценок пока нет
- 3246 Cotizaciones Instituto Tecnico SasДокумент2 страницы3246 Cotizaciones Instituto Tecnico SasLuis Carlos ZuñigaОценок пока нет
- Ejercicio 1 Unidad 2 - Nombre Del EstudianteДокумент3 страницыEjercicio 1 Unidad 2 - Nombre Del EstudianteLuis Carlos ZuñigaОценок пока нет
- Fondos VideeosДокумент1 страницаFondos VideeosLuis Carlos ZuñigaОценок пока нет
- Acuerdo 34Документ9 страницAcuerdo 34henrychtОценок пока нет
- QUÍMICA ANALÍTICA I Intercambio IónicoДокумент9 страницQUÍMICA ANALÍTICA I Intercambio IónicoScott Thomas WeilandОценок пока нет
- Aminoácidos EsencialesДокумент33 страницыAminoácidos EsencialesEdde PalenciaОценок пока нет
- 20 Aminoacidos BiologiaДокумент8 страниц20 Aminoacidos BiologiaBrittany CorralesОценок пока нет
- Enzimas LipolíticasДокумент21 страницаEnzimas LipolíticasMadelaine DuffautОценок пока нет
- Seminario #1Документ7 страницSeminario #1Pedro Osvaldo Vigabriel100% (1)
- A - Protocolo No 2 - Aminoácidos - BioquímicaДокумент27 страницA - Protocolo No 2 - Aminoácidos - BioquímicaJenifer LópezОценок пока нет
- Síntesis de Aminoácidos Esenciales y No EsencialesДокумент15 страницSíntesis de Aminoácidos Esenciales y No Esencialesmariela100% (1)
- ProteínasДокумент4 страницыProteínasNelly MosqueraОценок пока нет
- DETERMINACIÓN de Proteína Total Mediante EspectrofotometríaДокумент10 страницDETERMINACIÓN de Proteína Total Mediante EspectrofotometríaLisbeth Pilar Cornetero DiazОценок пока нет
- PescadoДокумент25 страницPescadoAda Arevalo LlatasОценок пока нет
- GlutaminaДокумент24 страницыGlutaminaJose MoranОценок пока нет
- Serotonina Histamina EicosanoidesДокумент69 страницSerotonina Histamina EicosanoidesAndres JimboОценок пока нет
- Discusion Complementaria 2Документ14 страницDiscusion Complementaria 2Perla León100% (1)
- Metabolismo de Los Aminoácidos Ii. Síntesis de Los AminoácidosДокумент36 страницMetabolismo de Los Aminoácidos Ii. Síntesis de Los AminoácidosJuana EstudianteОценок пока нет
- HISTATINASДокумент5 страницHISTATINASrosseОценок пока нет
- AminoácidosДокумент6 страницAminoácidosEdwardОценок пока нет
- PescadoДокумент27 страницPescadotanyОценок пока нет
- Tipos de Aminoácidos EsencialesДокумент9 страницTipos de Aminoácidos EsencialesYOUR SUPPORTОценок пока нет
- 1.2 Aminoácidos y Estructura PrimariaДокумент45 страниц1.2 Aminoácidos y Estructura PrimariaLiZz LaraОценок пока нет
- Aminoacidos Esenciales.Документ19 страницAminoacidos Esenciales.Valentiinee Guzmán67% (3)
- Actividad 5Документ30 страницActividad 5johannaОценок пока нет
- Acido UrocanicoДокумент3 страницыAcido UrocanicoMauro GonzalezОценок пока нет
- El Analisis de Histamina en El Pescado Por Que Es Necesario - SiggoДокумент8 страницEl Analisis de Histamina en El Pescado Por Que Es Necesario - SiggoWilliamОценок пока нет
- Método Molecular para La Detección de Bacterias Productoras de Aminas Biógenas en AlimentosДокумент6 страницMétodo Molecular para La Detección de Bacterias Productoras de Aminas Biógenas en AlimentosYADIRA ABIGAIL ASENCIOS ARIZAОценок пока нет
- CARPETA RECUPERACIÓ C.T. 4to SEC-2023Документ42 страницыCARPETA RECUPERACIÓ C.T. 4to SEC-2023RobertОценок пока нет
- Cuadro de AminoacidosДокумент3 страницыCuadro de AminoacidosDiegoVasquezОценок пока нет
- Taller Bioquimica 2Документ5 страницTaller Bioquimica 2jalvarez7693Оценок пока нет
- Titulacion de AminoacidosДокумент24 страницыTitulacion de Aminoacidosvladimir alvarezОценок пока нет
- Aminoácidos Esenciales y No Esenciales PDFДокумент23 страницыAminoácidos Esenciales y No Esenciales PDFEvelyn RuízОценок пока нет
- 20 Aminoacidos FuncionesДокумент6 страниц20 Aminoacidos FuncionesVizcaino Rojas JosèОценок пока нет