Академический Документы
Профессиональный Документы
Культура Документы
Ejemplos Verano 2.3 2018a
Загружено:
Javier G Zapiain SalinasОригинальное название
Авторское право
Доступные форматы
Поделиться этим документом
Поделиться или встроить документ
Этот документ был вам полезен?
Это неприемлемый материал?
Пожаловаться на этот документАвторское право:
Доступные форматы
Ejemplos Verano 2.3 2018a
Загружено:
Javier G Zapiain SalinasАвторское право:
Доступные форматы
Térmodinámica
Verano 2018
Unidad II: Propiedades de los Fuidos Puros
Ejemplo Unidad 3
Leyes y Ecuaciones de los Gases no Ideales.
Resuelva los siguientes problemas:
1. Calcule vb y Z para el hexa‡oruro de azufre a 75 C y 15 bar mediante las ecuaciones
siguientes:
Ecuacion de gases ideales.
La ecuación virial truncada, con los valores experimentales siguientes de los coe…cientes
viriales: B = 194 cm3 mol 1 C = 15300 cm6 mol 2
2. Calcule vb y Z para el benceno a 300 C y 12 bar mediante las ecuaciones siguientes:
Ecuacion de gases ideales.
La ecuación de Van der Waals
La ecuación de Redlich-Kwong
3. Determine vb y Z para el vapor de agua a 250 C y 1800 kPa a partir de lo siguiente:
Ecuación de los gases ideales.
Mediante la ecuación virial truncada con los valore experimentales siguientes de los
coe…cientes viriales: B = 152:5 cm3 mol 1 C = 5800 cm6 mol 2
Mediante tablas de vapor.La ecuación de Van der Waals
La ecuación de Redlich-Kwong
4. Cuando la ecuación del virial se trunca a cuatro terminos, describe con exactitud la
información volumétrica para el gas metano a 0 C con:
B= 53:4 cm3 mol 1
C = 2620 cm6 mol 2
D = 5000 cm9 mol 3
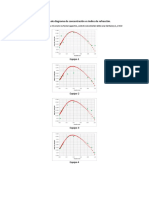
Use esta información para preparar una grá…ca de Z en función de P para metáno a 0
C de 0 a 200 bar. Considere que:
Z = 1 + B 0 P + C 0 P 2 + D0 P 3
con:
B = RT B 0
C = (RT )2 C 0 + B 02
D = (RT )3 D0 + 3B 0 C 0 + B 03
Вам также может понравиться
- 2 Da PRACTICA DIRIGIDAДокумент3 страницы2 Da PRACTICA DIRIGIDAFernandoОценок пока нет
- Serie 2 - Gases Reales UTN INSPTДокумент3 страницыSerie 2 - Gases Reales UTN INSPTDeb iiОценок пока нет
- 7 - 10 Gases RealesДокумент5 страниц7 - 10 Gases RealesEduardo Quispe VillarrealОценок пока нет
- Termodinamica - Taller Capitulo 3 PropiedДокумент16 страницTermodinamica - Taller Capitulo 3 Propied北本健人0% (1)
- TermodinamicaДокумент11 страницTermodinamicaJender AlexanderОценок пока нет
- Gases RealesДокумент35 страницGases RealesAlma EscobarОценок пока нет
- Ecuaciones de estado de van der Waals y propiedades termodinámicas de gasesДокумент5 страницEcuaciones de estado de van der Waals y propiedades termodinámicas de gasesJhonatan HualiОценок пока нет
- 3 TermodinamicaДокумент6 страниц3 TermodinamicaJordi López ClaràОценок пока нет
- Guia 2Документ3 страницыGuia 2Francisco Javier Retamal SotoОценок пока нет
- Examen Sustitutorio 2020-1Документ3 страницыExamen Sustitutorio 2020-1owen ricardo llacsahuanga vegasОценок пока нет
- Informe 03 Lab FQДокумент3 страницыInforme 03 Lab FQJDОценок пока нет
- Correlaciones de ViscosidadДокумент13 страницCorrelaciones de Viscosidaddalila_agueroОценок пока нет
- Crupo - 1-Fenomenos II Cap.10Документ24 страницыCrupo - 1-Fenomenos II Cap.10Alexa Pino Valdivia0% (1)
- GasesRealesBB 3478Документ2 страницыGasesRealesBB 3478José PulloquingaОценок пока нет
- Ejercicios de gases reales según modelos de Van der Waals, Beattie-Bridgeman y Estados CorrespondientesДокумент3 страницыEjercicios de gases reales según modelos de Van der Waals, Beattie-Bridgeman y Estados CorrespondientesAndres Guisberth ApazaОценок пока нет
- Gases RealesДокумент3 страницыGases RealesAnai Gutierres FuentesОценок пока нет
- Final Tema 5 en BloqueДокумент2 страницыFinal Tema 5 en Bloquejudith QuincheОценок пока нет
- Examen 2â Eval DistanciaДокумент5 страницExamen 2â Eval DistanciaDaniela 05Оценок пока нет
- Quimica 100 PPP1Документ6 страницQuimica 100 PPP1JOGA BONITOОценок пока нет
- Ejercicios Ec EstadoДокумент8 страницEjercicios Ec EstadoAllenОценок пока нет
- Primer ExamenДокумент9 страницPrimer Examenjvalencia_196986Оценок пока нет
- Desviación del comportamiento del gas ideal: Ecuación de Van der WaalsДокумент1 страницаDesviación del comportamiento del gas ideal: Ecuación de Van der WaalsGabriel Andres Gomez CallaОценок пока нет
- Final Tema 2 2C 2018 - 1er LlamadoДокумент2 страницыFinal Tema 2 2C 2018 - 1er LlamadoEster Leaños QuentaОценок пока нет
- Intento 2Документ9 страницIntento 2LAURA ESTER ROMERO NUÑEZОценок пока нет
- Problemas de Gases Ideales PreguntasДокумент11 страницProblemas de Gases Ideales PreguntasAnderson Toribio AlbertoОценок пока нет
- Problemas de Gases Ideales PREGUNTASДокумент11 страницProblemas de Gases Ideales PREGUNTASIng Ronald PortalesОценок пока нет
- Termod - Capitulo Iii-Ecuaciones de Estado (2014 I)Документ32 страницыTermod - Capitulo Iii-Ecuaciones de Estado (2014 I)ErickОценок пока нет
- Termod - Capitulo-Ecuaciones de EstadoДокумент32 страницыTermod - Capitulo-Ecuaciones de EstadoDennis Elias TaipeОценок пока нет
- Chemical Reaction EngineeringДокумент9 страницChemical Reaction EngineeringMedaJrArellanoОценок пока нет
- Ecuación de EstadoДокумент27 страницEcuación de EstadoRogelio DíazОценок пока нет
- Prob1 2008Документ2 страницыProb1 2008Rosa100% (1)
- Clase EquilibrioДокумент49 страницClase EquilibrioLluvia Linnett Martínez ReséndizОценок пока нет
- Lab 03 - Humedad RelativaДокумент12 страницLab 03 - Humedad Relativaanais zambranoОценок пока нет
- Quima090 s3 Guia2Документ9 страницQuima090 s3 Guia2LuisОценок пока нет
- Práctica de Gases Reales 2022Документ19 страницPráctica de Gases Reales 2022Axel Daril Alfredo AzañeroОценок пока нет
- Pauta PS22Документ7 страницPauta PS22Paula FierroОценок пока нет
- Termodinamica Taller Capitulo 3 PropiedaДокумент16 страницTermodinamica Taller Capitulo 3 PropiedaF5LucasОценок пока нет
- Problemas de Termodinámica IIДокумент2 страницыProblemas de Termodinámica IIEdgar Enrique Muños CastroОценок пока нет
- Unidad. 1Документ78 страницUnidad. 1erick sanchezОценок пока нет
- Termodinamica 2 - Clase 4Документ13 страницTermodinamica 2 - Clase 4Edwin Angel Solis Vitor100% (3)
- Separata de Gases RealesДокумент6 страницSeparata de Gases Realesluis DQОценок пока нет
- Ejercicios ResueltosДокумент8 страницEjercicios ResueltosCristian ArámbulaОценок пока нет
- Gases RealesДокумент3 страницыGases RealesdarioОценок пока нет
- Problemas de Termodinámica FundamentosДокумент24 страницыProblemas de Termodinámica FundamentosSebastian Andres De Oro0% (1)
- Práctica #3 - Termodinámica de Mezclas - 540332: Tema: Cómputo Generalizado Del Equilibrio Líquido-VaporДокумент3 страницыPráctica #3 - Termodinámica de Mezclas - 540332: Tema: Cómputo Generalizado Del Equilibrio Líquido-Vapormaria lopezОценок пока нет
- Aplicación Del Cálculo Numérico, Ejercicios ResueltosДокумент6 страницAplicación Del Cálculo Numérico, Ejercicios ResueltosandrefernandezОценок пока нет
- Determinación de constantes de Van der WaalsДокумент10 страницDeterminación de constantes de Van der WaalsJhon Alvarado ArceОценок пока нет
- Ejercicios de Fenomenos de Transporte de BirdДокумент34 страницыEjercicios de Fenomenos de Transporte de BirdChen Bao ZhuОценок пока нет
- 1er Set MN 2020Документ3 страницы1er Set MN 2020CN Kenyu AlexОценок пока нет
- LeyCosenosTriángulosДокумент3 страницыLeyCosenosTriángulosVICTOR MANUEL LUNA HERNANDEZОценок пока нет
- Guia 1Документ8 страницGuia 1Junior Benjamin Castro FloresОценок пока нет
- Ejercicios Estado GaseosoДокумент12 страницEjercicios Estado GaseosoAldair Stephano AresteguiОценок пока нет
- PRÁCTICA - Angulos CuadrantalesdДокумент1 страницаPRÁCTICA - Angulos CuadrantalesdNabel Guerra HuarancaОценок пока нет
- Química: Ejercicios de reacciones químicas y cálculos estequiométricosДокумент2 страницыQuímica: Ejercicios de reacciones químicas y cálculos estequiométricosAlanBlitzerОценок пока нет
- Problemas de Reactores PDFДокумент6 страницProblemas de Reactores PDFYohary De PazОценок пока нет
- Problemas resueltos de Hidráulica de CanalesОт EverandProblemas resueltos de Hidráulica de CanalesРейтинг: 4.5 из 5 звезд4.5/5 (7)
- Ingeniería química. Soluciones a los problemas del tomo IОт EverandIngeniería química. Soluciones a los problemas del tomo IОценок пока нет
- Actividades Tema III 2020aДокумент1 страницаActividades Tema III 2020aJavier G Zapiain SalinasОценок пока нет
- Examen Tema I Simulacion 2020Документ2 страницыExamen Tema I Simulacion 2020Javier G Zapiain SalinasОценок пока нет
- Problemario 2.1Документ2 страницыProblemario 2.1Javier G Zapiain SalinasОценок пока нет
- Problemario SP 1.1Документ1 страницаProblemario SP 1.1Javier G Zapiain SalinasОценок пока нет
- Problemario 1.3Документ2 страницыProblemario 1.3Javier G Zapiain SalinasОценок пока нет
- Actividades Tema I 2020aДокумент1 страницаActividades Tema I 2020aJavier G Zapiain SalinasОценок пока нет
- Problemario SP 1.2Документ1 страницаProblemario SP 1.2Javier G Zapiain SalinasОценок пока нет
- Actividades Tema II 2020aДокумент1 страницаActividades Tema II 2020aJavier G Zapiain SalinasОценок пока нет
- Problemario 4.1Документ1 страницаProblemario 4.1Javier G Zapiain SalinasОценок пока нет
- Problemario 2.2Документ2 страницыProblemario 2.2Javier G Zapiain SalinasОценок пока нет
- Problemario 3.1Документ2 страницыProblemario 3.1Javier G Zapiain SalinasОценок пока нет
- Datos DiezcolumnasДокумент1 страницаDatos DiezcolumnasJavier G Zapiain SalinasОценок пока нет
- Problemario 2.1 MCPPДокумент2 страницыProblemario 2.1 MCPPJavier G Zapiain SalinasОценок пока нет
- Metodo de Tiscareño Jimez Costo de ColumnasДокумент3 страницыMetodo de Tiscareño Jimez Costo de ColumnasJavier G Zapiain SalinasОценок пока нет
- Practica 4Документ1 страницаPractica 4Javier G Zapiain SalinasОценок пока нет
- Problema 8-4 y 8-5Документ1 страницаProblema 8-4 y 8-5Javier G Zapiain SalinasОценок пока нет
- Practica 1Документ1 страницаPractica 1Javier G Zapiain SalinasОценок пока нет
- Problemario 1.2Документ1 страницаProblemario 1.2Javier G Zapiain SalinasОценок пока нет
- Benceno-Tolueno 1 AtmДокумент1 страницаBenceno-Tolueno 1 AtmJavier G Zapiain SalinasОценок пока нет
- Coevaluacion 2019bДокумент29 страницCoevaluacion 2019bJavier G Zapiain SalinasОценок пока нет
- Encuadre 1Документ1 страницаEncuadre 1Javier G Zapiain SalinasОценок пока нет
- Triptico Sintesis y Optimizacion de ProcesosДокумент2 страницыTriptico Sintesis y Optimizacion de ProcesosJavier G Zapiain SalinasОценок пока нет
- Problemario 1.1 MCPPДокумент2 страницыProblemario 1.1 MCPPJavier G Zapiain SalinasОценок пока нет
- Triptico Laboratorio Integral II 2019 BДокумент2 страницыTriptico Laboratorio Integral II 2019 BJavier G Zapiain SalinasОценок пока нет
- Datos Minimos de PortadaДокумент1 страницаDatos Minimos de PortadaJavier G Zapiain SalinasОценок пока нет
- Problemario 1.1 SyOДокумент2 страницыProblemario 1.1 SyOJavier G Zapiain SalinasОценок пока нет
- Triptico Mejora de La Calidad de Procesos y Productos 2019Документ2 страницыTriptico Mejora de La Calidad de Procesos y Productos 2019Javier G Zapiain SalinasОценок пока нет
- Síntesis y Optimización de Procesos PDFДокумент9 страницSíntesis y Optimización de Procesos PDFr2rovbОценок пока нет
- Graficas Del Factor de CompresibilidadДокумент3 страницыGraficas Del Factor de CompresibilidadJavier G Zapiain SalinasОценок пока нет