Академический Документы
Профессиональный Документы
Культура Документы
4 Cartel
Загружено:
Alex RomeroИсходное описание:
Оригинальное название
Авторское право
Доступные форматы
Поделиться этим документом
Поделиться или встроить документ
Этот документ был вам полезен?
Это неприемлемый материал?
Пожаловаться на этот документАвторское право:
Доступные форматы
4 Cartel
Загружено:
Alex RomeroАвторское право:
Доступные форматы
¿SE PUEDE DETERMINAR EL PUNTO ISOELECTRICO DE GELATINA Y CASEINA POR PRECIPITACIÓN?
EQUIPO 3
INTRODUCCIÓN
DISCUSIÓN DE RESULTADOS
CONCLUSIÓN
Proteínas
Son biomacromoleculas formadas por cadenas de aminoácidos unidos por enlaces peptídicos y con un peso molecular mayor o igual a 5000 g/mol. Se descubrieron en 1838 y hoy se sabe que OBJETIVOS
Determinar el pI de diferentes proteínas RESULTADOS
son los componentes principales de las células y representan más del 50% del peso seco de la misma. El termino proteína deriva del griego proteios que significa primero.
Observar el efecto del alcohol como agente precipitante
Clasificación de proteínas
Por su composición MATERIAL REACTIVOS
Simples: Son aquellas que al hidrolizarse solo liberan aminoácidos 2 Gradilla Acetato de sodio 0.1N
Conjugadas: Son aquellas que al hidrolizarse liberan aminoácidos y otro compuesto que recibe el nombre de grupo prostético (átomo o molécula) 18 tubos de ensaye Alcohol etílico 𝐶1 𝑉1 = 𝐶2 𝑉2 CASEINA Tubos 5 al 9
Vaso de precipitados Agua destilada
NOMBRE GRUPO PROSTÉTICO 2 Pipetas graduadas (1ml, 10ml) Gelatina 1%
𝐶1 𝑉1 (0.1𝑁)(1𝑚𝑙) 0.01𝑁
Metaloproteinas Iónes metálicos 1 pizeta Ácido acético 0.01N, 0.1N, 1N = 𝐶2 = 0.01𝑁 𝒑𝑯 = 4.76 + 𝑙𝑜𝑔 = 4.76
𝑉2 10𝑚𝑙 0.01𝑁
Lipoproteínas
Cromoproteínas
Lípidos
Algún pigmento
Perilla Caseinato de sodio 0.01N
Nucleoproteínas Ácido nucleico
Glicoproteínas Carbohidratos [𝑏𝑎𝑠𝑒]
𝑝𝐻 = 𝑝𝐾 + 𝑙𝑜𝑔 [á𝑐𝑖𝑑𝑜] Tubos 1 al 4
Por su solubilidad ÁCIDO ACÉTICO (CH3 COOH) No. CAS: 64‐19‐7
(0.1𝑁)(2𝑚𝑙) 0.01𝑁
NOMBRE SOLUBLES EN
DATOS IMPORTANTES
(0.01𝑁)(0.62𝑚𝑙) 0.01𝑁 = 0.02𝑁 𝒑𝑯 = 4.76 + 𝑙𝑜𝑔 = 4.45
ESTADO FÍSICO, ASPECTO EFECTOS DE EXPOSICIÓN DE CORTA DURACIÓN
= 6.2𝑥10−4 𝑁 𝒑𝑯 = 4.76 + 𝑙𝑜𝑔 = 5.96 10𝑚𝑙 0.02𝑁
Albuminas Agua y soluciones salinas Líquido transparente, olor picante.
PELIGROS QUÍMICOS
La sustancia es corrosiva para los ojos, la piel y el tracto respiratorio. Corrosivo por ingestión. La inhalación puede causar edema
pulmonar, pero sólo tras producirse los efectos corrosivos iniciales en los ojos o las vías respiratorias.
10𝑚𝑙 6.2𝑥10−4 𝑁
Globulinas Soluciones salinas isotónicas La sustancia es un ácido débil. Reacciona violentamente con oxidantes fuertes originando peligro de incendio y explosión. EFECTOS DE EXPOSICIÓN PROLONGADA
Histonas Soluciones salinas Reacciona violentamente con bases fuertes, ácidos fuertes y muchos otros compuestos. Ataca a algunos tipos de plásticos, caucho El contacto prolongado o repetido con la piel puede producir dermatitis. Los pulmones pueden resultar afectados tras exposiciones
y revestimientos. prolongadas o repetidas a un aerosol de esta sustancia. Riesgo de erosión de los dientes tras exposiciones prolongadas o repetidas al
Prolaminas Etanol 70 u 80% LÍMITES DE EXPOSICIÓN aerosol de esta sustancia.
Glutelinas En ácidos y bases diluidos TLV: 10 ppm como TWA; 15 ppm como STEL (ACGIH 2010). LEP UE: 10 ppm; 25 mg/m³ como TWA (EU 1991). MEDIDAS DE PRECAUCIÓN
VÍAS DE EXPOSICIÓN Utilice gafas protectoras apropiadas, almacenar en recipientes bien cerrados. En local bien ventilado. Alejado de fuentes de ignición y
Escleroproteinas Insolubles en agua Efectos locales graves calor. Temperatura ambiente.
(0.1𝑁)(4𝑚𝑙) 0.01𝑁
Por su forma RIESGO DE INHALACIÓN
Por evaporación de esta sustancia a 20°C se puede alcanzar bastante rápidamente una concentración nociva en el aire.
EN CASO DE CONTACTO
Inhalación: Trasladar a la persona al aire libre. En caso de que persista el malestar, pedir atención (0.01𝑁)(1.25𝑚𝑙) 0.01𝑁 = 0.04𝑁 𝒑𝑯 = 4.76 + 𝑙𝑜𝑔 = 4.15
= 1.25𝑥10−3 𝑁 𝒑𝑯 = 4.76 + 𝑙𝑜𝑔 = 5.66 10𝑚𝑙 0.04𝑁
médica.
Fibrosas: Son aquellas que parecen enrollarse a lo largo de un eje común. Generalmente efectúan funciones de sostén Ingestión: Beber agua abundante. Evitar el vómito (existe riesgo de perforación). Pedir inmediatamente 10𝑚𝑙 1.25𝑥10−3 𝑁
atención médica. No neutralizar.
Globulares: Son aquellas que presentan plegamientos que les dan apariencia esférica. Asociadas a funciones dinámicas
Piel: Lavar abundantemente con agua. Quitarse las ropas contaminadas.
Ojos: Lavar los ojos con abundante agua por lo menos durante 20 minutos, manteniendo los párpados
Por su función separados. Conseguir la atención médica inmediatamente.
Estructurales, Reserva, Hormonas, Catalizadoras, Toxinas, Inmunoglobulinas, Transportadoras PROPIEDADES FÍSICAS (0.1𝑁)(8𝑚𝑙) 0.01𝑁
Niveles estructurales Punto de ebullición: 118°C Densidad relativa de la mezcla vapor/aire a 20°C (aire = 1): 1.02 (0.1𝑁)(0.25𝑚𝑙) 0.01𝑁 = 0.08𝑁 𝒑𝑯 = 4.76 + 𝑙𝑜𝑔 = 3.85
Punto de fusión: 16.7°C Punto de inflamación: 39°C c.c. = 2.5𝑥10−3 𝑁 𝒑𝑯 = 4.76 + 𝑙𝑜𝑔 = 5.36 10𝑚𝑙 0.08𝑁
Densidad relativa (agua = 1): 1.05 Temperatura de autoignición: 485°C 10𝑚𝑙 2.5𝑥10−3 𝑁
NIVEL REPRESENTA ENLACES CARACTERISTICOS Solubilidad en agua: miscible.
Presión de vapor, kPa a 20°C: 1.5
Primario Tipo, cantidad y secuencia de aminoácidos Enlace peptídico Densidad relativa de vapor (aire = 1): 2.1
Secundario Orientacion geométrica (parcial) de la Puentes de hidrogeno
cadena
Terciario Orientacion espacial de la cadena, Enlaces no covalentes como: ionicos y puentes de hidrogeno (1𝑁)(1.6𝑚𝑙) 0.01𝑁
ETANOL (C2H6O) No. CAS: 64-17-5 (0.1𝑁)(0.5𝑚𝑙) 0.01𝑁 = 0.16𝑁 𝒑𝑯 = 4.76 + 𝑙𝑜𝑔 = 3.55
presentan actividad biológica entre radicales, efecto hidrofóbico. Covalentes lábiles como = 5𝑥10−3 𝑁 𝒑𝑯 = 4.76 + 𝑙𝑜𝑔 = 5.06 10𝑚𝑙 0.16𝑁
puente disulfuro 10𝑚𝑙 5𝑥10−3 𝑁
DATOS IMPORTANTES
Cuaternario Asociacion de varias cadenas que se Enlaces no covalentes como: ionicos y puentes de hidrogeno
encuentran en nivel terciario. Actividad entre radicales. Covalentes lábiles como puente disulfuro
ESTADO FÍSICO, ASPECTO EFECTOS DE EXPOSICIÓN DE CORTA DURACIÓN
biologica Líquido incoloro, de olor característico. La sustancia irrita los ojos. La inhalación de altas concentraciones del vapor puede originar irritación de los ojos y del tracto
respiratorio. La sustancia puede afectar al sistema nervioso central.
PELIGROS FÍSICOS EFECTOS DE EXPOSICIÓN PROLONGADA PROCEDIMIENTO
El vapor se mezcla bien con el aire, formándose fácilmente mezclas explosivas. El líquido desengrasa la piel. La sustancia puede afectar al tracto respiratorio superior y al sistema nervioso central, dando lugar a
PELIGROS QUÍMICOS irritación, dolor de cabeza, fatiga y falta de concentración.
Reacciona lentamente con hipoclorito cálcico, óxido de plata y amoníaco originando peligro de incendio y explosión. MEDIDAS DE PRECAUCIÓN
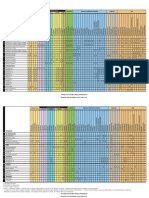
Reacciona violentamente con oxidantes fuertes tales como ácido nítrico, nitrato de plata, nitrato de mercurio o perclorato Separado de oxidantes fuertes. REACTIVOS (mL) 1 2 3 4 5 6 7 8 9
CASEÍNA magnésico, originando peligro de incendio y explosión. EN CASO DE CONTACTO
VÍAS DE EXPOSICIÓN Inhalación: Aire limpio, reposo.
La sustancia se puede absorber por inhalación del vapor y por ingestión. Ingestión: Enjuagar la boca. Proporcionar asistencia médica.
RIESGO DE INHALACIÓN Piel: Quitar las ropas contaminadas. Aclarar y lavar con agua y jabón. Agua destilada 8.38 7.75 8.75 8.5 8 7 5 1 7.4
Por evaporación de esta sustancia a 20°C se puede alcanzar bastante lentamente una concentración nociva en el aire. Ojos: Enjuagar con agua abundante durante varios minutos (quitar las lentes de contacto si puede hacerse
En la leche hay tres clases de proteínas: caseína, lacto albúminas y lacto globulinas (todas globulares). La caseína es una proteína con facilidad), después proporcionar asistencia médica.
DETERMINACIÓN DEL PUNTO ISOELÉCTRICO DE LA CASEÍNA.
conjugada de la leche del tipo fosfoproteína que se separa de la leche por acidificación y forma una masa blanca. Las fosfoproteinas Ac. Acético 0.01 N 0.62 1.25 - - - - - - -
son un grupo de proteínas que están químicamente unidas a una sustancia que contiene ácido fosfórico. En la caseína la mayoría de
Ac. Acético 0.1 N - - 0.25 0.5 1 2 4 8 - Preparamos 9 tubos como indica la tabla. Agitamos los tubos y agregamos 1 mL de sln de
los grupos fosfato están unidos por los grupos hidroxilo de los aminoácidos serina y treonina. La caseína en la leche se encuentra en caseína. Agitar los tubos inmediatamente. Observar los enturbamientos que se producen
después de agitar, esperar 15 minutos.
forma de sal cálcica (caseinato cálcico). La caseína representa cerca del 77% al 82% de las proteínas presentes en la leche y el 2,7% PROPIEDADES FÍSICAS Ac. Acético 1.0 N - - - - - - - - 1.6
en composición de la leche líquida. La caseína está formada por alpha(s1), alpha(s2)-caseína, ß-caseína, y kappa-caseína formando Punto de ebullición: 79°C Punto de fusión: -117°C Densidad relativa (agua = 1): 0,8 Solubilidad en agua: miscible Densidad relativa de la mezcla vapor/aire a 20°C (aire = 1): 1,03 Punto de inflamación: 13°C c.c. Temperatura de autoignición: 363°C
una micela o unidad soluble. Ni la alfa ni la beta caseína son solubles en la leche, solas o combinadas. Si se añade la kappa caseína
a las dos anteriores o a cada una de ellas por separado se forma un complejo de caseína que es solubilizado en forma de micela.
Esta micela está estabilizada por la kappa caseína mientras que las alfa y beta son fosfoproteínas que precipitan en presencia de REACTIVOS (mL) 1 2 3 4 5 6 7 8 9
Acetato de sodio 0.1 N 2 2 2 2 2 2 2 2 2
iones calcio. ACETATO DE SODIO NO. CAS 127-09-3
DATOS IMPORTANTES
ESTADO FÍSICO, ASPECTO MEDIDAS DE PRECAUCIÓN
Polvo cristalino higroscópico, blanco. Oxidante fuerte. Gases inflamables y tóxicos se forman a temperaturas elevadas >280ºC debido a la descomposición térmica (amoníaco, Ac. Acético 0.1 N 0.12 0.25 0.5 1 2 4 - - -
DETERMINACIÓN DEL PUNTO ISOELÉCTRICO DE LA GELATINA.
óxidos de azufre, óxidos de nitrógeno).
La kappa caseína, sin embargo, tiene pocos grupos fosfato y un alto contenido de carbohidratos unidos a ella. También tiene todos sus residuos de serina y treonina con sus correspondientes PELIGROS
La sustancia se descompone al calentarla intensamente y en EN CASO DE CONTACTO
grupos hidroxilo, así como los carbohidratos dispuestos en una sola cara de su superficie por lo que esta parte exterior es fácilmente soluble en agua gracias a los grupos polares que posee. La contacto con ácidos fuertes produciendo vapores de ácido Inhalación: Aire limpio, reposo. Ac. Acético 1.0 N - - - - - - 0.8 1.6 3.2
Mezclar bien el contenido de los tubos y desechar la mitad de cada uno, al tubo no. 5 añadir de 5 a 8
acético. Reacciona violentamente con oxidantes fuertes. La Piel: Aclarar y lavar la piel con agua y jabón.
otra parte de su superficie se une fácilmente a las alfa y beta caseína insolubles, lo que da lugar a la formación de la micela. disolución en agua es una base débil. Ojos: Enjuagar con agua abundante durante varios minutos (quitar las lentes de contacto si puede hacerse mL de alcohol etílico hasta producir una tenue nebulosidad, adicionar a los demás tubos la misma
con facilidad), después proporcionar asistencia médica.
VÍAS DE EXPOSICIÓN Ingestión: Reposo. Agua destilada 3.88 3.75 3.5 3 2 - 3.2 2.4 0.8 cantidad de alcohol que la añadida al tubo no. 5. Anote los resultados de la misma forma que para la
La sustancia se puede absorber por ingestión. caseína.
La propiedad característica de la caseína es su baja solubilidad a pH 4,6. El pH de la leche es 6,6 aproximadamente, estando a ese pH la caseína cargada negativamente y solubilizada como sal RIESGO DE INHALACIÓN
No se puede indicar la velocidad con que se alcanza una Gelatina al 1% 2 2 2 2 2 2 2 2 2
concentración nociva de esta sustancia en el aire.
cálcica. Si se añade ácido a la leche, la carga negativa de la superficie de la micela se neutraliza (los grupos fosfato se protonan) y la proteína neutra precipita.
GELATINA
PROPIEDADES FÍSICAS
Punto de fusión: 328°C
Densidad: 1,5 g/cm
CUESTIONARIO
La gelatina está compuesta en un 85% o 90% de colágeno proveniente de materias primas animales y entre 1% y 2% de sales minerales; el porcentaje restante es agua. No contiene Solubilidad en agua, g/100 ml a 20°C: 46,5
conservantes ni otros aditivos y está libre de colesterol y de purinas (compuestos con ácido úrico).
1. Defina pl de una proteína.
FUNDAMENTOS
El cambio de pH de la solución en que se encuentra la proteína promueve cambio en las cargas de los residuos y por lo tanto un cambio de carga total de la proteína. Cuando el número
de cargas positivas se iguala con el número de cargas negativas se dice que la proteína se encuentra en su pH isoeléctrico (punto isoeléctrico) y presenta el mínimo de solubilidad ya
Solubilidad de las proteínas que no hay repulsión electroestática entre las moléculas. Se puede separar proteínas usando precipitación por su punto isoeléctrico ya que cada proteína tiene un valor específico.
pH Además, las proteínas presentan su conformación nativa y es posible solubilizarlas en una solución con el pH adecuado.
El cambio de pH de la solución en que se encuentra la proteína promueve cambio en las cargas de los residuos y por lo tanto un cambio de carga total de la proteína. Cuando el número de
cargas positivas se iguala con el número de cargas negativas se dice que la proteína se encuentra en su pH isoeléctrico (punto isoeléctrico) y presenta el mínimo de solubilidad ya que no hay
repulsión electroestática entre las moléculas. Se puede separar proteínas usando precipitación por su punto isoeléctrico ya que cada proteína tiene un valor específico. Además, las proteínas
presentan su conformación nativa y es posible solubilizarlas en una solución con el pH adecuado.
2. Escriba la ecuación de Henderson Hasselbach.
Propiedades dieléctricas del disolvente
La constante dieléctrica se define como la capacidad de mantener separados a iones de diferente carga, en este sentido el agua presenta la mayor constante dieléctrica lo que permite mantener
en solución a las proteínas. La adición de solventes de menor capacidad de separación de iones hace que las proteínas precipiten. Se usan como agentes precipitantes solventes miscibles con el
agua como acetona y etanol. Se debe trabajar a temperatura baja para evitar la desnaturalización de la proteína.
Temperatura
3. ¿Por qué el alcohol actúa como agente precipitante de la gelatina?
El rango de temperatura que permite la solubilización de proteínas se encuentra entre 0°C y 40°C. La mayoría de las proteínas a temperaturas mayores de 45°C-60°C sufren desnaturalización
debido a la ruptura de puentes de hidrogeno y fuerzas de Van Der Waals. Algunas proteínas recobran su conformación al bajar la temperatura, a esto se le llama renaturalización.
La gelatina es una mezcla heterogénea de proteínas de alto peso molecular. Éstas son proteínas solubles en agua, y el agua está incorporada dentro de las moléculas individuales de los
Desnaturalización proteica: Proceso o serie de procesos en el que se altera la disposición espacial de las cadenas polipeptidicas dentro de la molécula, transformándose la estructura típica de la aminoácidos, lo que hace su carácter de gel. Al agregar el alcohol etílico, se rompen las uniones de las moléculas, pues el agua es miscible con el alcohol etílico, y las proteínas
proteína en otra más desordenada. precipitan, además de no ser solubles en alcohol.
REFERENCIAS BIBIOGRAFÍCAS
García L. et al. (2017). Ayudas didácticas. Bioquímica I. Departamento de Bioquímica-Alimentos. Facultad de Ciencias Químicas. Benemérita Universidad Autónoma de
Puebla.
Instituto Nacional de Seguridad e Higiene en el Trabajo: Fichas internacionales de seguridad química. Consultado el 18 de enero de 2018, de INSHT. Sitio web:
http://www.insht.es/.
Mathews, C , Van Holde, K. y Ahern K. (2002).Bioquímica. 3° ED. Pearson Educación. Madrid
Universidad Pablo de Olavide. Extracción de la caseína y determinación del punto Isoeléctrico. Disponible en:
https://www.upo.es/depa/webdex/quimfis/docencia/biotec_FQbiomol/Practica3FQB.pdf
Вам также может понравиться
- Cartel 4Документ1 страницаCartel 4David GarciaОценок пока нет
- Cartel 4 Bioquimica 1 1Документ1 страницаCartel 4 Bioquimica 1 1ChincoyaF100% (2)
- Evidencia 2 PDFДокумент2 страницыEvidencia 2 PDFManuel MAОценок пока нет
- Ejercicios BioquímicaДокумент4 страницыEjercicios BioquímicavaudevilleeОценок пока нет
- Infografia 3 BiocaДокумент1 страницаInfografia 3 BiocaJossue MolinaОценок пока нет
- Taller Metabolismo de AminoacidosДокумент4 страницыTaller Metabolismo de AminoacidosMilene PonceОценок пока нет
- Entrega y Reposicion de EppsДокумент13 страницEntrega y Reposicion de Eppscesar alcides pezo borreroОценок пока нет
- AINESДокумент1 страницаAINESASTRID PINOОценок пока нет
- Reproducción CelularДокумент7 страницReproducción CelularSAHILPREET SINGHОценок пока нет
- Glucogénesis y GlicólisisДокумент1 страницаGlucogénesis y GlicólisisEmОценок пока нет
- Clasificación de Las EnzimasДокумент10 страницClasificación de Las EnzimasRuben GomezОценок пока нет
- Reporte 3Документ1 страницаReporte 3Karla HernandezОценок пока нет
- Entrega Epp 2023Документ2 страницыEntrega Epp 2023Juan SalazarОценок пока нет
- Interpretacion PesticidasДокумент4 страницыInterpretacion PesticidasAle OosaОценок пока нет
- Mapa Conceptual de Ácidos NucleicosДокумент1 страницаMapa Conceptual de Ácidos NucleicosGhost eng3lОценок пока нет
- Desnaturalización de Las ProteínasДокумент8 страницDesnaturalización de Las ProteínasRamos KarenОценок пока нет
- Ubs Arrastre Hidraulico Pozo de Percolacion Viviendas-Inst. Hidraulica - ElectricasДокумент1 страницаUbs Arrastre Hidraulico Pozo de Percolacion Viviendas-Inst. Hidraulica - ElectricasRosa NavarroОценок пока нет
- SET-SST-121-entrega - y - Reposicion - de EPPSДокумент8 страницSET-SST-121-entrega - y - Reposicion - de EPPSJose Marin AguilarОценок пока нет
- Turbocharger (Turbocharger) - ALLDATA RepairДокумент14 страницTurbocharger (Turbocharger) - ALLDATA Repairmemo velascoОценок пока нет
- Requerimientos Nutricionales de Cabras Lecheras - 202193 - 154929Документ2 страницыRequerimientos Nutricionales de Cabras Lecheras - 202193 - 154929LIZBETH CAROLINA JACOME CONTRERASОценок пока нет
- Mapa ICB.Документ1 страницаMapa ICB.Dani BackalОценок пока нет
- ANEXO #13 (Seguimiento METAX-ZOON) - 1Документ4 страницыANEXO #13 (Seguimiento METAX-ZOON) - 1Deivitd CardenasОценок пока нет
- PresentacionCLASE - PepH Acido Ascorbico 2673Документ14 страницPresentacionCLASE - PepH Acido Ascorbico 2673Esmeralda PalaciosОценок пока нет
- Patokinesis de Artroplastia de CaderaДокумент1 страницаPatokinesis de Artroplastia de CaderaHiguera Diaz Sandra MilenaОценок пока нет
- Practica 1 Caracteristicas de AminoacidosДокумент9 страницPractica 1 Caracteristicas de AminoacidosLilimon PlayОценок пока нет
- E-0020-4130-ELE-DTL-001 - 1 - Área 4130. Molienda. Plano Detalles Tap-Off Línea 23 KVДокумент1 страницаE-0020-4130-ELE-DTL-001 - 1 - Área 4130. Molienda. Plano Detalles Tap-Off Línea 23 KVAlex Labraña RojoОценок пока нет
- Profesiograma ProducciónДокумент1 страницаProfesiograma ProducciónCONFIA SSTОценок пока нет
- IPERC - Construccion de Cocina de Nuevo Campamento ACP - 2022Документ10 страницIPERC - Construccion de Cocina de Nuevo Campamento ACP - 2022wilson alexis zaquinaula bancesОценок пока нет
- Biosintesis de Acidos GrasosДокумент26 страницBiosintesis de Acidos GrasosBryaan MLokoo100% (1)
- Enzimas APUNTESДокумент6 страницEnzimas APUNTESmarОценок пока нет
- Plano de Drenajes, OficinasДокумент1 страницаPlano de Drenajes, Oficinaspereiracris095Оценок пока нет
- Profesiograma para Desarrollo de Evaluaciones Médicas OcupacionalesДокумент18 страницProfesiograma para Desarrollo de Evaluaciones Médicas Ocupacionalessalud ocupacionalОценок пока нет
- Ácidos Nucleicos y Enzimas Asociadas ApuntesДокумент32 страницыÁcidos Nucleicos y Enzimas Asociadas ApuntesSandra MorillasОценок пока нет
- Estructuras - ClinicaДокумент13 страницEstructuras - ClinicaAlexander Orbegoso VillavicencioОценок пока нет
- Función de NutricionДокумент1 страницаFunción de NutricionAnonimusОценок пока нет
- Soluciones Amortiguadoras 222Документ14 страницSoluciones Amortiguadoras 222Juliana SánchezОценок пока нет
- Agentes Químicos Mecanismo de Resistencia A Los AntibioticosДокумент1 страницаAgentes Químicos Mecanismo de Resistencia A Los AntibioticosJHERICO YHURAK HUAMAN CERNAОценок пока нет
- HIDROCARBUROS AROMÁTICOS GUIA 2do MEDIO 14-11-19Документ3 страницыHIDROCARBUROS AROMÁTICOS GUIA 2do MEDIO 14-11-19anon_777624809Оценок пока нет
- Reporte 5 - Lab BioquímicaДокумент1 страницаReporte 5 - Lab BioquímicaZempoalteca Tellez AshleyОценок пока нет
- Atb 1Документ2 страницыAtb 1YureОценок пока нет
- Poster Hofmeister SeriesДокумент1 страницаPoster Hofmeister SeriesFranco BonaféОценок пока нет
- Mapa Mental de LípidosДокумент1 страницаMapa Mental de LípidosGhost eng3lОценок пока нет
- Laboratorio #2 NitroacetanilidaДокумент7 страницLaboratorio #2 NitroacetanilidaRicardo Romero0% (1)
- INICIA 2ESO FISQUIM LA LessonДокумент1 страницаINICIA 2ESO FISQUIM LA LessonPau Bon FillgassoОценок пока нет
- Is - Grupo 3 - Incendio - 16-12Документ1 страницаIs - Grupo 3 - Incendio - 16-12api-520954620Оценок пока нет
- Profesiograma y Matriz de Exámenes Ocupacionales - CasactivaДокумент6 страницProfesiograma y Matriz de Exámenes Ocupacionales - CasactivaAraque AraqueОценок пока нет
- Filosofía Económica - Tarea 3Документ2 страницыFilosofía Económica - Tarea 3Alexander David Lopez EscobedoОценок пока нет
- Anexo 1 Distancias Rev - 0Документ9 страницAnexo 1 Distancias Rev - 0Sebastian DuarteОценок пока нет
- La Homeostasis PDFДокумент1 страницаLa Homeostasis PDFjuansebastianОценок пока нет
- E-0020-4130-ELE-DTL-001 - 2 - Área 4130. Molienda. Plano Detalles Tap-Off Línea 23 KVДокумент1 страницаE-0020-4130-ELE-DTL-001 - 2 - Área 4130. Molienda. Plano Detalles Tap-Off Línea 23 KVAlex Labraña RojoОценок пока нет
- Ubs Arrastre Hidraulico - Zanja de Percolacion-Inst. Sanitarias A-1Документ1 страницаUbs Arrastre Hidraulico - Zanja de Percolacion-Inst. Sanitarias A-1joanОценок пока нет
- Mapa de Calor Educacion Fisica 2023 RosuloДокумент11 страницMapa de Calor Educacion Fisica 2023 RosuloYhon Eduardo Camacho ArrateaОценок пока нет
- DG - 01, Distribucion GeneralДокумент1 страницаDG - 01, Distribucion Generalluis telloОценок пока нет
- N14ms03-I1-221570-200es-00001 Plano MuroДокумент1 страницаN14ms03-I1-221570-200es-00001 Plano Muromarco astrogaОценок пока нет
- Seguimiento de Planes Biologicos - 07OCT2022Документ124 страницыSeguimiento de Planes Biologicos - 07OCT2022javier pachecoОценок пока нет
- Ciencias Sociales (1a)Документ1 страницаCiencias Sociales (1a)Michael HernándezОценок пока нет
- ExportacionДокумент1 страницаExportacionLuis Manuel Gonzalez BalarezoОценок пока нет
- Tema 4Документ19 страницTema 4Loreto BlancoОценок пока нет
- Hpc-Eb-Rb-Pl-02 - Detalles PlafonesДокумент1 страницаHpc-Eb-Rb-Pl-02 - Detalles PlafoneslayiОценок пока нет
- ChlamydiaДокумент4 страницыChlamydiaAlex Romero100% (1)
- Practica 6 FisioДокумент4 страницыPractica 6 FisioAlex RomeroОценок пока нет
- MolibdenoДокумент6 страницMolibdenoAlex RomeroОценок пока нет
- AlveolosДокумент10 страницAlveolosAlex RomeroОценок пока нет
- Destilacion Por Arrastre de VaporДокумент5 страницDestilacion Por Arrastre de VaporAlex RomeroОценок пока нет
- Absorbancia 1.1Документ5 страницAbsorbancia 1.1Alex RomeroОценок пока нет
- Factores Fisiológicos Que Influyen en La Producción de Las Pasturas: Temperatura, Luz, Humedad.Документ4 страницыFactores Fisiológicos Que Influyen en La Producción de Las Pasturas: Temperatura, Luz, Humedad.juanОценок пока нет
- Bioelementos y BiomoleculasДокумент6 страницBioelementos y BiomoleculasBetty DguezОценок пока нет
- ANTIMICROBIANOSДокумент25 страницANTIMICROBIANOSCesar Alfonso Zarate AsmatОценок пока нет
- Desarollo Syllabus NutriДокумент84 страницыDesarollo Syllabus Nutripilincho111279Оценок пока нет
- Tarea 2 - 201103 - 2Документ9 страницTarea 2 - 201103 - 2Luisa fer AriasОценок пока нет
- Tipos de CoagulacionДокумент10 страницTipos de CoagulacionBrissa Vera SanchezОценок пока нет
- EstimacionvalornutricionalДокумент39 страницEstimacionvalornutricionalJuan Carlos Jones GiraldoОценок пока нет
- Uso de La Amonificacion para Mejorar La Calidad Del Heno. AlimentacionДокумент5 страницUso de La Amonificacion para Mejorar La Calidad Del Heno. AlimentacionVenezuelaGanadera.comОценок пока нет
- Preinforme AmicoácidosДокумент16 страницPreinforme Amicoácidosandres9410Оценок пока нет
- Aminoácidos ModificadosДокумент2 страницыAminoácidos ModificadosGabo Bernal Oceguera100% (1)
- PROMEXICO Presentacion-BiotecnologiaДокумент81 страницаPROMEXICO Presentacion-BiotecnologiaElena MendozaОценок пока нет
- Acordeon BIOQUIMICA - Docx 1443395676337Документ12 страницAcordeon BIOQUIMICA - Docx 1443395676337Anonymous ExcNQWv7PОценок пока нет
- Guia Digital Extractos Naturales 1Документ38 страницGuia Digital Extractos Naturales 1Luis Ramos100% (1)
- PUEM GyOДокумент11 страницPUEM GyOZaniru Raúl Marín MartínezОценок пока нет
- Guia 4 Sintesis de Proteinas-Grado Noveno Ii PeriodoДокумент4 страницыGuia 4 Sintesis de Proteinas-Grado Noveno Ii Periodorocio menaОценок пока нет
- 10 - Proteínas 2Документ5 страниц10 - Proteínas 2HectorPalaciosCarballidoОценок пока нет
- Informe de Manjar BlancoДокумент33 страницыInforme de Manjar BlancoGR0910S0% (1)
- Fórmulas de Nutrición Enteral en Pediatría - Consuelo Pedrón, Víctor NavasДокумент111 страницFórmulas de Nutrición Enteral en Pediatría - Consuelo Pedrón, Víctor NavasDanilo GalarzaОценок пока нет
- Divulgacion 5a43b790138f4Документ124 страницыDivulgacion 5a43b790138f4SoyGuada0% (1)
- Compuestos Orgánicos Nitrogenados y Oxigenados, Carbohidratos y ProteínasДокумент8 страницCompuestos Orgánicos Nitrogenados y Oxigenados, Carbohidratos y ProteínasPatrick SulkОценок пока нет
- Sobre Germinados - MANUEL LARA DELGADO PDFДокумент157 страницSobre Germinados - MANUEL LARA DELGADO PDFCELESTE0% (1)
- Caso Clinico GeriatriaДокумент5 страницCaso Clinico GeriatriaWendy GómezОценок пока нет
- Dieta Macros Jesus GallegoДокумент28 страницDieta Macros Jesus GallegoJhonny Gabriel TorrezОценок пока нет
- Plantas Alimenticias No ConvencionalesДокумент19 страницPlantas Alimenticias No ConvencionalesallanОценок пока нет
- Clase Practica 9 Kenya Gil SДокумент4 страницыClase Practica 9 Kenya Gil SKenya SantacruzОценок пока нет
- Tratamientos Previos Al Procesamiento de Productos HidrobiologicosДокумент56 страницTratamientos Previos Al Procesamiento de Productos HidrobiologicosKARENXITAVS100% (6)
- Triptico Dos PDFДокумент2 страницыTriptico Dos PDFJuan LuisОценок пока нет
- Informe LactoscanДокумент6 страницInforme LactoscanJuan MorochoОценок пока нет
- Determinación de Proteínas Mediante El Método KjeldahlДокумент5 страницDeterminación de Proteínas Mediante El Método KjeldahlStiven BravoОценок пока нет
- 04 CuidadosPaliativosenEnfermeriaДокумент401 страница04 CuidadosPaliativosenEnfermeriaelucazОценок пока нет