Академический Документы
Профессиональный Документы
Культура Документы
Análisis de alcoholes
Загружено:
Danilo JaramilloИсходное описание:
Оригинальное название
Авторское право
Доступные форматы
Поделиться этим документом
Поделиться или встроить документ
Этот документ был вам полезен?
Это неприемлемый материал?
Пожаловаться на этот документАвторское право:
Доступные форматы
Análisis de alcoholes
Загружено:
Danilo JaramilloАвторское право:
Доступные форматы
SISTEMA DE GESTIÓN DE TÉCNICA DE LABORATORIO
LABORATORIOS FACULTAD DE ELABORADO POR: JONNATHAN PILAMALA
CIENCIAS
FECHA: ABRIL 2017
REVISADO: DRA. PATRICIA LAYEDRA
APROBADO: DRA. JENNY MORENO
FECHA: ABRIL 2017
QUÍMICA DE ALCOHOLES EDICIÓN : PRIMERA
Página de Página 1 de 7
INFORME N° 2
QUÍMICA DE ALCOHOLES
1. Objetivos:
1.1. General:
Identificar las propiedades químicas y físicas de los alcoholes
1.2. Específicos: (Mínimo tres)
2. Marco Teórico y Referencial:
2.1. Marco Referencial:
2.2. Marco teórico:
3. Parte Experimental:
3.1. Sustancias y Reactivos:
Metanol
Etanol
2-Propanol
Ácido Sulfúrico
Reactivo de Lucas
Dicromato de Potasio
Alcohol t-amílico
Sal común
3.2. Materiales y Equipos:
12 tubos de ensayo
Gradilla
Reverbero
LABORATORIO QUÍMICA ORGÁNICA
SISTEMA DE GESTIÓN DE TÉCNICA DE LABORATORIO
LABORATORIOS FACULTAD DE ELABORADO POR: JONNATHAN PILAMALA
CIENCIAS
FECHA: ABRIL 2017
REVISADO: DRA. PATRICIA LAYEDRA
APROBADO: DRA. JENNY MORENO
FECHA: ABRIL 2017
QUÍMICA DE ALCOHOLES EDICIÓN : PRIMERA
Página de Página 2 de 7
Corchos de tubos
Pipetas 10 ml
Espátula
Vidrio de reloj
2 vaso de Precipitación de 250 ml
Pinza para tubos de ensayo
Fósforos o Fosforera
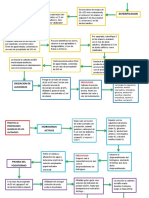
3.3. Desarrollo experimental:
Solubilidad En Agua
En 3 tubos de ensayo colocar 1 ml de
(etanol, 2-propanol, alcohol t-amílico)
Agregar con una pipeta unas cuantas
gotas de agua destilada
Tapando el tubo de ensayo en cada
adición
Esperar hasta que se produzca
enturbiamiento persistente
Reactivo De Lucas en Alcoholes
LABORATORIO QUÍMICA ORGÁNICA
SISTEMA DE GESTIÓN DE TÉCNICA DE LABORATORIO
LABORATORIOS FACULTAD DE ELABORADO POR: JONNATHAN PILAMALA
CIENCIAS
FECHA: ABRIL 2017
REVISADO: DRA. PATRICIA LAYEDRA
APROBADO: DRA. JENNY MORENO
FECHA: ABRIL 2017
QUÍMICA DE ALCOHOLES EDICIÓN : PRIMERA
Página de Página 3 de 7
Anotar el tiempo
necesario para
Colocar el tapón que en cada tubo
de corcho y dejar se produzca
emulsión
Agregar 1ml de reposar
(etanol, 2-butanol,
En 3 tubos de alcohol t-amílico)
ensayo colocar en cada uno
1ml e reactivo de
Lucas
Oxidación De Alcoholes con Dicromato de Potasio.
En 3 tubos de ensayo se coloca 1ml de (etanol, 2-propanol, alcohol t-amílico
Adicionar 1ml de una solución de dicromato de potasio al 5% en cada tubo
Adicionar 1ml de ácido sulfúrico (gota a gota) por las paredes de cada tubo
Agitar y observar si hay (aumento de temperatura o cambio de coloración)
Calentar a baño maría y observar si se producen cambios
Formación De Esteres
LABORATORIO QUÍMICA ORGÁNICA
SISTEMA DE GESTIÓN DE TÉCNICA DE LABORATORIO
LABORATORIOS FACULTAD DE ELABORADO POR: JONNATHAN PILAMALA
CIENCIAS
FECHA: ABRIL 2017
REVISADO: DRA. PATRICIA LAYEDRA
APROBADO: DRA. JENNY MORENO
FECHA: ABRIL 2017
QUÍMICA DE ALCOHOLES EDICIÓN : PRIMERA
Página de Página 4 de 7
En 1 tubo de ensayo Al percibir un olor
colocar 1ml de Calentar la mezcla agradable de acetato
(etanol, Ac. acético cuidadosamente a de etilo, dejar enfriar
glacial) y 2ml de baño maría la solución por
ácido sulfúrico debajo de los 20 0C
Adicionar 5ml de
Observar
solución de sal común
Análisis cualitativo de metanol y etanol.
Encender los 2 líquidos con una astilla
En 2 vidrio reloj dejar caer 5l de etanol
de madera encendida a la par con una
y 5 ml de metanol
pequeña cantidad de bórax
4. Reacciones y Resultados:
LABORATORIO QUÍMICA ORGÁNICA
SISTEMA DE GESTIÓN DE TÉCNICA DE LABORATORIO
LABORATORIOS FACULTAD DE ELABORADO POR: JONNATHAN PILAMALA
CIENCIAS
FECHA: ABRIL 2017
REVISADO: DRA. PATRICIA LAYEDRA
APROBADO: DRA. JENNY MORENO
FECHA: ABRIL 2017
QUÍMICA DE ALCOHOLES EDICIÓN : PRIMERA
Página de Página 5 de 7
4.1. Reacciones:
4.2. Resultados:
SOLUBILIDAD EN AGUA.
OBSERVAR TURBIDEZ
1ml de etanol Gotas de agua destilada
1ml de 2-propanol Gotas de agua destilada
1ml de alcohol t-amílico Gotas de agua destilada
REACCIÓN DE LUCAS.
ANOTAR TIEMPO
EMULSIÓN
1ml de etanol 1ml React. De Lucas
1ml de 2-propanol 1ml React. De Lucas
1ml de alcohol t-amílico 1ml React. De Lucas
OXIDACIÓN CON DICROMATO DE POTASIO. (En baño maría hirviente)
ANOTAR CAMBIO DE COLOR
Y TEMPERATURA
1ml de etanol 1ml sol 1 ml H2SO4
LABORATORIO QUÍMICA ORGÁNICA
SISTEMA DE GESTIÓN DE TÉCNICA DE LABORATORIO
LABORATORIOS FACULTAD DE ELABORADO POR: JONNATHAN PILAMALA
CIENCIAS
FECHA: ABRIL 2017
REVISADO: DRA. PATRICIA LAYEDRA
APROBADO: DRA. JENNY MORENO
FECHA: ABRIL 2017
QUÍMICA DE ALCOHOLES EDICIÓN : PRIMERA
Página de Página 6 de 7
Dicromato
1ml de 2-propanol 1ml sol 1 ml H2SO4
Dicromato
1ml alcohol t-amílico 1ml sol 1 ml H2SO4
Dicromato
FORMACIÓN DE ÉSTERES.
En un tubo de ensayo colocar 3 ml de etanol y adicionar 2 ml de ácido acético y 1 ml de
ácido sulfúrico. Calentar a baño maría y percibir el olor, dejar enfriar y añadir 5 ml de
solución de cloruro de sodio. Anotar resultados.
ANÁLISIS CUALITATIVO DE METANOL Y ETANOL
ANOTAR
0.5 ml. etanol Encender bórax
0.5 ml. metanol Encender bórax
5. Conclusiones y Recomendaciones:
5.1. Conclusiones:
5.2. Recomendaciones:
6. Referencias Bibliográficas:
6.1. Citas:
6.2. Bibliografía:
LABORATORIO QUÍMICA ORGÁNICA
SISTEMA DE GESTIÓN DE TÉCNICA DE LABORATORIO
LABORATORIOS FACULTAD DE ELABORADO POR: JONNATHAN PILAMALA
CIENCIAS
FECHA: ABRIL 2017
REVISADO: DRA. PATRICIA LAYEDRA
APROBADO: DRA. JENNY MORENO
FECHA: ABRIL 2017
QUÍMICA DE ALCOHOLES EDICIÓN : PRIMERA
Página de Página 7 de 7
6.3. Internet:
7. Cuestionario:
7.1 ¿Cómo se diferencia metanol del etanol en el laboratorio?
7.2 ¿Al aumentar el número de carbonos como varían las propiedades físicas de los alcoholes?
7.3 ¿Cómo se obtiene alcohol industrialmente, detalle el esquema o mecanismo?
7.4 ¿Tabla propiedades físicas de los alcoholes?
7.5 ¿usos del alcohol en la industria?
8. Anexos:
8.1. Esquema del equipo
RESUMEN (150 palabras)
DESCRIPTORES
LABORATORIO QUÍMICA ORGÁNICA
Вам также может понравиться
- Grandes Obras de Manualidades. El perfume: Los secretos de la elaboración del perfumeОт EverandGrandes Obras de Manualidades. El perfume: Los secretos de la elaboración del perfumeОценок пока нет
- Prácticas Tecnología EnzimáticaДокумент21 страницаPrácticas Tecnología EnzimáticaAndro SalasОценок пока нет
- Acuarios para dummies (guía de iniciación a la acuariofilia)От EverandAcuarios para dummies (guía de iniciación a la acuariofilia)Оценок пока нет
- Practica 2 Eq6 5im15Документ16 страницPractica 2 Eq6 5im15Cassy JuVaz100% (1)
- Guia Extraccion de TaninosДокумент6 страницGuia Extraccion de TaninosManuel PetinsОценок пока нет
- Alquinos InformeДокумент15 страницAlquinos InformeCristina Paez100% (2)
- Técnica de Laboratorio Química de AlcoholesДокумент6 страницTécnica de Laboratorio Química de AlcoholesItati GaiborОценок пока нет
- Acetil Salicilico CorrДокумент11 страницAcetil Salicilico CorrAntonii CarrascoОценок пока нет
- Práctica N. 1. Síntesis de Cloruro de T AmiloДокумент10 страницPráctica N. 1. Síntesis de Cloruro de T AmiloErika LalònОценок пока нет
- Obtención e identificación de eteno a partir de etanolДокумент8 страницObtención e identificación de eteno a partir de etanolLuis Córdova CoxОценок пока нет
- Técnicas de Laboratorio - Destilación SimpleДокумент3 страницыTécnicas de Laboratorio - Destilación SimpleFRANS ROMOОценок пока нет
- Informe 7Документ22 страницыInforme 7Jared AcostaОценок пока нет
- Compendio de La Química Organica Iii 1521 2024-1Документ49 страницCompendio de La Química Organica Iii 1521 2024-1Ilse SaenzОценок пока нет
- Practica 2 de AlcoholesДокумент4 страницыPractica 2 de AlcoholesJavier Cruz AtiОценок пока нет
- Obtención de HMF a partir de fructosaДокумент40 страницObtención de HMF a partir de fructosaAzul HernándezОценок пока нет
- Ensayo de QuimicaДокумент5 страницEnsayo de QuimicaJosé SantosОценок пока нет
- Flujograma de AlquinosДокумент2 страницыFlujograma de AlquinosDianitaBonilla100% (1)
- Toxicologia Indice de Toxidez de La HiguerillaДокумент15 страницToxicologia Indice de Toxidez de La HiguerillaJhon Jairo Intriago CabreraОценок пока нет
- Técnicas de Laboratorio - Obtención e Identificación de AlquinosДокумент3 страницыTécnicas de Laboratorio - Obtención e Identificación de AlquinosSantiago PérezОценок пока нет
- Pratica 6Документ11 страницPratica 6Arturo Perez GuzmanОценок пока нет
- Equilibrio Químico CorregidoДокумент9 страницEquilibrio Químico CorregidodavidОценок пока нет
- Práctica Iv Equilibrio QuímicoДокумент7 страницPráctica Iv Equilibrio QuímicoVivi Mar CSiОценок пока нет
- Propiedades y reactividad de compuestos aromáticosДокумент3 страницыPropiedades y reactividad de compuestos aromáticosGeraldine HdezОценок пока нет
- Diagrama de FlujoДокумент3 страницыDiagrama de FlujoDömë IñiguezОценок пока нет
- Informe 1Документ14 страницInforme 1Cristina PaezОценок пока нет
- PROYECTO Sintesis AspirinaДокумент3 страницыPROYECTO Sintesis AspirinaNancy Belträn RdzОценок пока нет
- Solubilidad de Pares LiquidosДокумент5 страницSolubilidad de Pares LiquidosErick SalinasОценок пока нет
- Guía Lab Química Orgánica I 17-18Документ13 страницGuía Lab Química Orgánica I 17-18Yadi UgenioОценок пока нет
- Práctica 2 AlcoholesДокумент5 страницPráctica 2 AlcoholesalexandraОценок пока нет
- Practica de AlcoholesДокумент4 страницыPractica de AlcoholesRichard SchОценок пока нет
- COMPENDIO Prácticas de Química Orgánica 0067 Completo 2023-2Документ34 страницыCOMPENDIO Prácticas de Química Orgánica 0067 Completo 2023-2CARMEN SCARLETT ORTIZ CORTESОценок пока нет
- Informe #2 Permeabilidad de La Membrana PDFДокумент15 страницInforme #2 Permeabilidad de La Membrana PDFLuisa Herrera LopezОценок пока нет
- Lab 5 Transaminación PDFДокумент5 страницLab 5 Transaminación PDFmxrfОценок пока нет
- Fuerzas intermolecularesДокумент4 страницыFuerzas intermolecularesparra rubio juan diegoОценок пока нет
- Practica 1 Halogenuros de AlquiloДокумент4 страницыPractica 1 Halogenuros de AlquiloJavier Cruz AtiОценок пока нет
- Practica 3 Aldehidos y CetonasДокумент4 страницыPractica 3 Aldehidos y CetonasAndy Lyyzz0% (1)
- Manual Quim Org III QFB 201901Документ20 страницManual Quim Org III QFB 201901joseОценок пока нет
- PracticaДокумент8 страницPracticaalarandi-fernan-2000Оценок пока нет
- Informe 4 Actividad de EnzimasДокумент10 страницInforme 4 Actividad de Enzimasslendy sofia100% (1)
- CainaДокумент4 страницыCainaEvelynОценок пока нет
- Manual practicasDROE02Документ25 страницManual practicasDROE02Juan Manuel Campos NavarroОценок пока нет
- NITRITOSДокумент2 страницыNITRITOSEdwin Estiben Perilla SalgadoОценок пока нет
- Las Enzimas y AdnДокумент4 страницыLas Enzimas y AdnNicolasОценок пока нет
- Técnicas de Laboratorio - Destilación SimpleДокумент3 страницыTécnicas de Laboratorio - Destilación SimpleJared AcostaОценок пока нет
- Equilibrio-Químico Grupo 4Документ14 страницEquilibrio-Químico Grupo 4Maicol SerranoОценок пока нет
- Diagrama Practica 2Документ2 страницыDiagrama Practica 2AlexОценок пока нет
- Práctica 2. Pruebas de Caracterización de Haluros de Alquilo y AlcoholesДокумент5 страницPráctica 2. Pruebas de Caracterización de Haluros de Alquilo y AlcoholesYeimy Andrea Ocampo GilОценок пока нет
- RanitidinaДокумент5 страницRanitidinaLiceniaMontañezОценок пока нет
- Laboratorio 6Документ5 страницLaboratorio 6david Sierra gaonaОценок пока нет
- Practicasquimica4modifporplanestudios 160721163151 PDFДокумент18 страницPracticasquimica4modifporplanestudios 160721163151 PDFMaría Carolina RieraОценок пока нет
- Informe de Laboratorio - EnzimasДокумент17 страницInforme de Laboratorio - Enzimasbrayan avilez100% (1)
- Manual Lab - Qorg.i IQДокумент24 страницыManual Lab - Qorg.i IQSuleima JiménezОценок пока нет
- Reconocimiento de La CalatasaДокумент1 страницаReconocimiento de La CalatasajohnОценок пока нет
- Metodo de Cristalizacion SimpleДокумент3 страницыMetodo de Cristalizacion SimpleGerardo SotoОценок пока нет
- Equilibrio Químico Corregido-1Документ11 страницEquilibrio Químico Corregido-1Edison GusñayОценок пока нет
- Liceo Campestre Thomas de Iriarte: Guía de laboratorio de identificación de compuestos carbonílicos y pruebas de solubilidadДокумент3 страницыLiceo Campestre Thomas de Iriarte: Guía de laboratorio de identificación de compuestos carbonílicos y pruebas de solubilidadkingcarmilorОценок пока нет
- Practica 4 FerneyДокумент1 страницаPractica 4 FerneyJose EspinelОценок пока нет
- Guía Propiedades Físicas y QuímicasДокумент7 страницGuía Propiedades Físicas y QuímicasCristian camilo Cano ColoradoОценок пока нет
- Presentación - Compuestos de Metales Alcalinos y AlcalinoterreosДокумент1 страницаPresentación - Compuestos de Metales Alcalinos y AlcalinoterreosDanilo JaramilloОценок пока нет
- Tren de Rodaje 2020Документ2 страницыTren de Rodaje 2020Danilo JaramilloОценок пока нет
- AminoacidosДокумент13 страницAminoacidosDanilo JaramilloОценок пока нет
- Presentación - Compuestos de Metales Alcalinos y AlcalinoterreosДокумент1 страницаPresentación - Compuestos de Metales Alcalinos y AlcalinoterreosDanilo JaramilloОценок пока нет
- Jorge 2Документ5 страницJorge 2Danilo JaramilloОценок пока нет
- Taller Aminoácidos y PéptidosДокумент2 страницыTaller Aminoácidos y PéptidosDanilo JaramilloОценок пока нет
- Plan de contingencia académico de Tren de RodajeДокумент4 страницыPlan de contingencia académico de Tren de RodajeDanilo Jaramillo100% (1)
- Propiedades de los metales alcalinos y alcalinotérreosДокумент15 страницPropiedades de los metales alcalinos y alcalinotérreosDanilo JaramilloОценок пока нет
- Resultados Practica 5Документ6 страницResultados Practica 5Danilo JaramilloОценок пока нет
- GUÍA No.06 MEDICIÓN DE PHДокумент1 страницаGUÍA No.06 MEDICIÓN DE PHDanilo JaramilloОценок пока нет
- Tren de Rodaje 2020Документ2 страницыTren de Rodaje 2020Danilo JaramilloОценок пока нет
- Formato AnexosДокумент2 страницыFormato AnexosDanilo JaramilloОценок пока нет
- 2004 Jorge VillegasДокумент2 страницы2004 Jorge VillegasDanilo JaramilloОценок пока нет
- 2004 Jorge VillegasДокумент2 страницы2004 Jorge VillegasDanilo JaramilloОценок пока нет
- Villegas 2323Документ5 страницVillegas 2323Danilo JaramilloОценок пока нет
- Villegas 2323Документ5 страницVillegas 2323Danilo JaramilloОценок пока нет
- Reaccion y Resultados Info 2Документ4 страницыReaccion y Resultados Info 2Danilo JaramilloОценок пока нет
- GUÍA No.04 OBTENCIÓN DE HIDRÓGENO Y OXÍGENOДокумент3 страницыGUÍA No.04 OBTENCIÓN DE HIDRÓGENO Y OXÍGENODanilo JaramilloОценок пока нет
- GUÍA No. 03 SOLUBILIDAD Y CONDUCTIVIDADДокумент5 страницGUÍA No. 03 SOLUBILIDAD Y CONDUCTIVIDADDanilo JaramilloОценок пока нет
- El Agua, BiologiaДокумент4 страницыEl Agua, BiologiaDanilo JaramilloОценок пока нет
- Tren Jorge Villegas 15 2020Документ5 страницTren Jorge Villegas 15 2020Danilo Jaramillo100% (1)
- Unidad III-RUC y COMPROBANTES DE VENTA PDFДокумент38 страницUnidad III-RUC y COMPROBANTES DE VENTA PDFDanilo JaramilloОценок пока нет
- TrombopeniaДокумент9 страницTrombopeniaDanilo JaramilloОценок пока нет
- Trastorn o Scre Cimiento CelularДокумент64 страницыTrastorn o Scre Cimiento Celularlau_mönzter_1Оценок пока нет
- Guía de LaboratorioДокумент18 страницGuía de Laboratoriokathy vasconezОценок пока нет
- Ecuacion de ValorДокумент10 страницEcuacion de ValorDanilo JaramilloОценок пока нет
- Alcano Más Permanganato de PotasioДокумент2 страницыAlcano Más Permanganato de PotasioDanilo Jaramillo100% (1)
- Preoyecto de OrganicaДокумент17 страницPreoyecto de OrganicaDanilo JaramilloОценок пока нет
- Materia de TipsДокумент10 страницMateria de TipsDanilo JaramilloОценок пока нет
- Informe de MicrobiologiaДокумент52 страницыInforme de Microbiologiadirce823Оценок пока нет
- Diseño y Funcionamiento de Lagunas de EstabilizacionДокумент36 страницDiseño y Funcionamiento de Lagunas de EstabilizacionOrlando Herrera ValdiviaОценок пока нет
- Seleccion de CablesДокумент6 страницSeleccion de CablesboredeОценок пока нет
- Proyecto RayonДокумент13 страницProyecto RayonRosa LeonОценок пока нет
- Información Práctica Sobre Elaboración de Vino: Glicerol Y VinificaciónДокумент40 страницInformación Práctica Sobre Elaboración de Vino: Glicerol Y VinificaciónANA BELINDA SOSA ARDONОценок пока нет
- Metabolismo de La Célula AnimalДокумент15 страницMetabolismo de La Célula AnimalWENDOLIN ALEXANDRA CUAMATZI HERNANDEZОценок пока нет
- Programa de Formulación Al Mínimo Costo MixitДокумент5 страницPrograma de Formulación Al Mínimo Costo MixitDesarrollosgj Cca100% (1)
- Analisis Elemental Cualitativo de HalogenosДокумент13 страницAnalisis Elemental Cualitativo de HalogenosEDWIN_JUGADOR80% (5)
- ChalconasДокумент5 страницChalconasmilukr100% (1)
- Conclusiones, Sugerencias y TerminologiaДокумент2 страницыConclusiones, Sugerencias y TerminologiaAida Navarrete RodriguezОценок пока нет
- Determinación de loratadina en tabletas comerciales y genéricasДокумент17 страницDeterminación de loratadina en tabletas comerciales y genéricasMishell Karolina Machado Valle100% (1)
- Laboratorio de Biologia Humana Uta Aplic. Met. Cientifico PDFДокумент4 страницыLaboratorio de Biologia Humana Uta Aplic. Met. Cientifico PDFVane ButrónОценок пока нет
- FenilaminaДокумент7 страницFenilaminaNestor ChavezОценок пока нет
- Plasticos Tipos PDFДокумент8 страницPlasticos Tipos PDFDavidFuicaRojasОценок пока нет
- Calorías en Sardina, Tabla e Información Nutricional para Pescado Azul - Pescados y Derivados - DietasДокумент8 страницCalorías en Sardina, Tabla e Información Nutricional para Pescado Azul - Pescados y Derivados - DietasEdwin Ernesto Pereira AlenОценок пока нет
- Práctica 1 AMBIENTADORДокумент3 страницыPráctica 1 AMBIENTADORG'nesiis AndreiitapОценок пока нет
- Los Diferentes Grupos Funcionales Ordenados de Mayor A Menor ImportanciaДокумент5 страницLos Diferentes Grupos Funcionales Ordenados de Mayor A Menor ImportanciaYhoneyder Delrio MejiaОценок пока нет
- PRACTICA NRO 2 BIOQUIMICA Determinacion de GlucosaДокумент15 страницPRACTICA NRO 2 BIOQUIMICA Determinacion de GlucosaSait Huaman IngaОценок пока нет
- Identificación de Termoplásticos Por PirólisisДокумент6 страницIdentificación de Termoplásticos Por Pirólisismilagros adco0% (1)
- Identificación de proteínas en laboratorio bioquímicaДокумент13 страницIdentificación de proteínas en laboratorio bioquímicaMarlyn DuranОценок пока нет
- BiologiaДокумент43 страницыBiologiaDdvQsОценок пока нет
- Curso Division de ColoniasДокумент11 страницCurso Division de Coloniasrods2003Оценок пока нет
- Estructuras de Kekule OrganicaДокумент5 страницEstructuras de Kekule OrganicaAracelyGomez100% (1)
- Informe LipidosДокумент11 страницInforme LipidosJeanОценок пока нет
- Cicloalcanos y aromáticosДокумент3 страницыCicloalcanos y aromáticosELIANAОценок пока нет
- AlcoholesДокумент31 страницаAlcoholesMarcelo Orozco CorralesОценок пока нет
- Práctica 7 - Extracción y Análisis de Líídos de Yema de HuevoДокумент13 страницPráctica 7 - Extracción y Análisis de Líídos de Yema de HuevoUsui TakumiОценок пока нет
- Plan de Area Quimica - OnceДокумент20 страницPlan de Area Quimica - OnceMayerlis Gomez100% (1)
- Diseño y Montaje de Una Planta para La Obtencion de QuitinaДокумент11 страницDiseño y Montaje de Una Planta para La Obtencion de QuitinamarcosotbОценок пока нет
- Investigacion Previa Quimica Organica 1 Practica 1 Diels-AlderДокумент5 страницInvestigacion Previa Quimica Organica 1 Practica 1 Diels-AlderGuillermo RTОценок пока нет