Академический Документы
Профессиональный Документы
Культура Документы
Oxidacion
Загружено:
Jonatan Goicochea BaconОригинальное название
Авторское право
Доступные форматы
Поделиться этим документом
Поделиться или встроить документ
Этот документ был вам полезен?
Это неприемлемый материал?
Пожаловаться на этот документАвторское право:
Доступные форматы
Oxidacion
Загружено:
Jonatan Goicochea BaconАвторское право:
Доступные форматы
OXIDACIÓN - CIENCIAS DE LOS MATERIALES II
UNIVERSIDAD NACIONAL DE INGENIERIA
Facultad de Ingeniería Mecánica
OXIDACION Y CORROSION
Curso : Ciencia de los Materiales II “B”
Profesor : Ing. LUIS SOSA
Alumnos : GOICOCHEA BACON JONATAN 20160263D
2017-II
FACULTAD DE INGENIERÍA MECÁNICA Página 1
OXIDACIÓN - CIENCIAS DE LOS MATERIALES II
Índice
Objetivo ….………………...............................................................3
Descripción de equipos utilizados ...................................................3
Fundamento Teórico……...............................................................5
Descripción del procedimiento….................................................. 6
Cálculos y resultados………..........................................................7
Conclusiones y recomendaciones................................................9
bibliografia……………..................................................................10
FACULTAD DE INGENIERÍA MECÁNICA Página 2
OXIDACIÓN - CIENCIAS DE LOS MATERIALES II
OXIDACIÓN
1.- OBJETIVO
Analizar la morfología del material después de que se realice el proceso de
oxidación en él y compararlo con la morfología del material sin el proceso de
oxidación.
Observar las reacciones de oxidación y reducción de algunos metales o iones
metálicos.
Conociendo los resultados comprender el análisis de lo que es el poder relativo
del agente oxidante y el poder relativo de los iones metálicos como agentes
oxidante.
FACULTAD DE INGENIERÍA MECÁNICA Página 3
OXIDACIÓN - CIENCIAS DE LOS MATERIALES II
2.- DESCRIPCIÓN DE LOS EQUIPOS UTILIZADOS
2.1.- MÁQUINAS
a) HORNO ELÉCTRICO
b) ELEMENTOS DE SEGURIDAD (GUANTES, PINZA Y CASCO)
FACULTAD DE INGENIERÍA MECÁNICA Página 4
OXIDACIÓN - CIENCIAS DE LOS MATERIALES II
c) BALANZA ELECTRONICA
d) VERNIER CALIPER
e) PROBETA DE ACERO Y COBRE
FACULTAD DE INGENIERÍA MECÁNICA Página 5
OXIDACIÓN - CIENCIAS DE LOS MATERIALES II
3.- FUNDAMENTO TEÓRICO
La oxidación térmica es una manera de producir una capa delgada de óxido
(generalmente dióxido de silicio ) en la superficie de una oblea . La técnica de las
fuerzas de un agente oxidante que se difunden en la oblea a alta temperatura y
reaccionar con él. La tasa de crecimiento del óxido con frecuencia predicha por el
modelo de Deal-Grove . La oxidación térmica se puede aplicar a diferentes materiales
La oxidación térmica del silicio generalmente se realiza a una temperatura entre 800
y 1200 ° C , lo que resulta en la llamada capa de óxido de alta temperatura (OTA).
Se puede utilizar el vapor de agua (vapor) o molecular de oxígeno como oxidante, en
consecuencia, es llamado oxidación en húmedo o seco. La reacción es uno de los
siguientes:
El ambiente oxidante también puede contener varios puntos porcentuales de ácido
clorhídrico (HCl). El cloro elimina los iones de metal que se pueden producir en el
óxido.
Óxido térmico incorpora silicio utilizado en el sustrato y el oxígeno suministrado por el
ambiente. Por lo tanto, crece tanto hacia abajo en la oblea y hasta fuera de ella. Por
cada unidad de espesor de consumo de silicio, 2,27 la unidad espesores de óxido
aparecerá. Por el contrario, si una superficie de silicio desnudo se oxida, el 46% del
espesor de óxido estará por debajo de la superficie original, y el 54% por encima de
ella.
Deal-Grove modelo
De acuerdo con el uso común Deal-Grove modelo, el tiempo t necesario para crecer
un óxido de espesor X o, a una temperatura constante, en una superficie de silicio
desnudo, es la siguiente:
FACULTAD DE INGENIERÍA MECÁNICA Página 6
OXIDACIÓN - CIENCIAS DE LOS MATERIALES II
donde las constantes A y B encapsular las propiedades de la reacción y la capa de
óxido, respectivamente.
Si una oblea que ya contiene óxido se coloca en un ambiente oxidante, esta ecuación
debe ser modificado mediante la adición de un término correctivo τ, el tiempo que
habría sido necesario para hacer crecer el óxido de pre-existentes en las condiciones
actuales. Este término se puede encontrar usando la ecuación de t por encima.
Al resolver la ecuación cuadrática de los rendimientos de X o:
4.- DESCRIPCIÓN DEL PROCEDIMIENTO
A. Se obtuvieron muestras del material en estudio.
B. Hacer el desbaste de las muestras con ayuda de las lijas.
C. Realizar el proceso de pulido de las muestras con ayuda del pulidor mecánico.
D. Atacar químicamente las muestras del material en estudio con el Ácido Nítrico
al 70%.
E. Llevar las muestras al horno durante tiempos de 30min, 60min y 90min.
F. Analizar su morfología
FACULTAD DE INGENIERÍA MECÁNICA Página 7
OXIDACIÓN - CIENCIAS DE LOS MATERIALES II
5.- CÁLCULOS Y RESULTADOS
cObre
Volumen Tiempo
Diámetro Altura Densidad Área Espesor
inicial
mm Mm cm3 gr/cm3 cm2 um min
12,715 17.98 2.283 8.742 9.7217 12.34 36
12,645 17.405 2.1858 8.8872 9.4259 12.57 34
12,675 15.065 1.9009 8.7986 8.5224 15.323 32
12,655 13.275 1.6697 8.8297 7.7933 18.2703 26
bronce
Volumen Tiempo
Diámetro Altura Densidad Área Espesor
inicial
mm Mm cm3 gr/cm3 cm2 um min
12.73 21.035 2.6773 8.392 10.9579 7.0466 36
12.725 19.775 2.5149 8.4021 10.4489 8.2239 34
12.74 17.975 2.2914 8.357 9.5518 14.1811 32
12.675 16.36 2.0643 8.4371 9.0381 25.2441 26
ACERO
Volumen Tiempo
Diámetro Altura Densidad Área Espesor
inicial
mm mm cm3 gr/cm3 cm2 Um min
12.475 25.11 3.0691 7.8946 12.2855 22.085 36
12.6 20.145 2.5119 7.7791 10.468 33.5987 34
12.825 23.865 3.0829 7.4993 12.1991 25.589 32
12.57 18.575 2.3051 7.8026 9.8172 27.1933 26
FACULTAD DE INGENIERÍA MECÁNICA Página 8
OXIDACIÓN - CIENCIAS DE LOS MATERIALES II
Para una temperatura de 700°C se tiene las siguientes graficas:
COBRE
20
18 y = 0.0654x + 9.1304
16
14
Espesor(um)
12
10
0
0 20 40 60 80 100 120 140
Tiempo(min)
BRONCE
30
25
Espesor(um)
y = 0.0031x2 - 0.3084x + 14.326
20
15
10
0
0 20 40 60 80 100 120 140
Tiempo(min)
FACULTAD DE INGENIERÍA MECÁNICA Página 9
OXIDACIÓN - CIENCIAS DE LOS MATERIALES II
ACERO
Valores Y
40
y = 0.0002x3 - 0.0413x2 + 3.3572x - 52.554
Espesor(um)
35
30
25
20
15
10
0
0 20 40 60 80 100 120 140
Tiempo(min)
FACULTAD DE INGENIERÍA MECÁNICA Página 10
OXIDACIÓN - CIENCIAS DE LOS MATERIALES II
7.- CONCLUSIONES Y RECOMENDACIONES
La oxidación de metales a alta temperatura es en particular importante en el
diseño de ingeniería de turbinas de gas, motores de cohetes y equipo
petroquímico de alta temperatura.
El coeficiente de Pilling-Bedworth es el cociente entre el volumen de oxido
formado y el volumen del metal consumido por la oxidación.
La película de oxido que se forma en el metal puede ser protectora o no protectora
depende del coeficiente de Pilling-Bedworth
La palabra corrosión en una frase corta es “Destrucción de un material”. Esta
destrucción puede presentarse por vía química, electro-química o metalúrgica.
La corrosión es un proceso muy lento dependiendo del tipo de corrosión y del
material.
La corrosión causa grandes gastos empresariales por descuido de los
encargados, principalmente en las maquinas y estructuras de las empresas.
Dependiendo del lugar en que se encuentre va a ser diferente el tipo de corrosión
que se presente.
La corrosión no la podemos evitar al 100% pero si controlarla, una vez encontrada
la corrosión la podemos evitar de muchas maneras dependiendo del material.
FACULTAD DE INGENIERÍA MECÁNICA Página 11
OXIDACIÓN - CIENCIAS DE LOS MATERIALES II
CUESTIONARIO
1. ¿En qué casos la oxidación presenta un comportamiento de tipo lineal?
Se presenta un comportamiento lineal cuando se dan las condiciones isotérmicas y una
presión de oxigeno constante, se da generalmente en los metales alcalinos, alcalinotérreos
y tierras raras. El oxígeno puede atravesar la capa de óxido (discontinua), y atacar
directamente el metal
Este comportamiento lineal es típico de materiales cuya capa de óxido es porosa, o cuya
relación P.B. es muy diferente de 1, es decir en materiales en que la velocidad de
oxidación no se ve influida por la presencia de la capa de óxido, ya que éste se agrieta o
se desprende.
2. El hierro por encima de los 500 ºC presenta un oxido complejo, debido a sus varias
valencias. Sabiendo que se forman los óxidos: FeO, Fe2O3 y Fe3O4, indicar
esquemáticamente sus ubicaciones en una capa de óxido.
FACULTAD DE INGENIERÍA MECÁNICA Página 12
OXIDACIÓN - CIENCIAS DE LOS MATERIALES II
En el hierro la oxidación compleja se da debido a la pérdida de los electrones por lo que en
el FeO el hierro pierde +2 electrones, en el Fe3O4 es de +8/3 y en el Fe2O3 es de +3,por
lo cual las ubicaciones en una capa de óxido es de la siguiente manera:
3. Un cilindro metálico sólido con un diámetro inicial de 12.65 mm, una altura de 18.58
mm y una masa inicial de 20.5798 gramos es introducido en un horno a 850 ºC
durante tres horas. Su masa final es de 19.6932 gramos. Determinar el espesor del
material perdido por oxidación.
SOLUCION
DATOS: -Hallando el volumen de la masa inicial:
𝜋
D0 =12.65 mm *A0 = (12.65)2=125.6776 𝑚𝑚2
4
h0 =18.58 mm *V0 =A0 . h0= (125.6776)(18.58)=2335.0898 𝑚𝑚3 |
m0 =20.5798 gr -Hallando la 𝜌 :
m 20.5798 gr gr
m𝑓 =19.6932 gr * 𝜌 = V0 = =8.813 x10−3
0 2335.0898 𝑚𝑚 3 𝑚𝑚3
h𝑓 = ¿? -Ahora: V𝑓 = ¿?
m𝑓 19.6932 gr 3
e =h𝑜 - h𝑓 V𝑓 = = gr =2.234.56 𝑚𝑚
𝜌 8.813 x10−3 𝑚𝑚3
-Se considera: A0 =A𝑓
V𝑓 =2234.56=A𝑓 . h𝑓 → h𝑓 =17.78 mm
→e=h𝑜 - h𝑓 =18.58 mm -17.78 mm
→e=0.8
FACULTAD DE INGENIERÍA MECÁNICA Página 13
OXIDACIÓN - CIENCIAS DE LOS MATERIALES II
4. Un depósito abierto de acero que contiene un electrolito corrosivo sufre una pérdida
de material de 2 gramos/metro cuadrado por día. Calcule la perdida expresada en
mdd. 1 mdd = 1 miligramo/decímetro cuadrado por día. Calcule el sobre espesor de
las paredes y fondo de dicho depósito para que dure sin perforarse al menos 10
años. Considerar la densidad del acero 7,87 gr/cm3.
-Calculando la pérdida en mdd.
𝑔 103 𝑚𝑔
2 = 2 = 20 𝑚𝑑𝑑
𝑚2 . 𝑑𝑖𝑎 100𝑑𝑚2 . 𝑑𝑖𝑎
-Calculando el espesor en 10 años.
𝑔𝑟 365𝑑𝑖𝑎
∆𝑚 2𝑚2 𝑥 𝑑𝑖𝑎 𝑥 𝑎ñ𝑜𝑠
e= = = 927.573 x10−6 m ≈ 1𝑚𝑚
𝜌.A0 (7.87gr/m3)x106
5. Se quiere utilizar un determinado tipo de acero para la fabricación de tanques que
almacenaran un líquido corrosivo. Para ello se expusieron probetas de este acero a
la acción de este líquido corrosivo y se observó una pérdida media de 30
miligramos/decímetro cuadrado por día. Determinar si el acero seleccionado es el
adecuado. Un material se considera bastante resistente y puede utilizarse si su
velocidad de corrosión es menor o igual a 1 mm/año.
Considerando una superficie de 1 m^2
30
30𝑚𝑔
= 1000 𝑔 = 1.095 𝑔 = 1.095𝑘𝑔
𝑑𝑚2 𝑑𝑖𝑎 1 2
10000 𝑚 𝑑𝑖𝑎
El volumen de esta masa será
𝑚 𝑚
V= = = 1,38. 10−4 𝑚3
𝜌 𝜌
𝑉 1,38. 10−4 𝑚3 𝑚𝑚
e= = 2
= 0,138
𝐴 1𝑚 𝑎ñ𝑜
𝑚𝑚 𝑚𝑚
0,138 <1
𝑎ñ𝑜 𝑎ñ𝑜
Entonces es bastante resistente por lo tanto se puede utilizar.
FACULTAD DE INGENIERÍA MECÁNICA Página 14
OXIDACIÓN - CIENCIAS DE LOS MATERIALES II
8.- BIBLIOGRAFÍA
Corrosión. Nilthon Zavaleta Gutierrez. Editado por CONCYTEC. La
Libertad, Perú. 2012
Ciencia de Materiales – Selección y Diseño. Pat L. Mangonon.
Ed.Pearson Educación. México. 2001.
Corrosion for Everybody. A. Groysman. Ed. Springer. 2010
Fundamento de Ciencia de los Materiales: Cuaderno de clases prácticas.
J. Cembrero. Universidad Politécnica de Valencia, Servicio de
Publicaciones. 1997.
FACULTAD DE INGENIERÍA MECÁNICA Página 15
Вам также может понравиться
- Informe 5: Oxidación y CorrosiónДокумент13 страницInforme 5: Oxidación y CorrosiónDavid Malaver DiazОценок пока нет
- Laboratorio 5 Oxidación y Corrosión 2016 1Документ20 страницLaboratorio 5 Oxidación y Corrosión 2016 1Carlos AlanyaОценок пока нет
- Estimacion de Recursos InformeДокумент13 страницEstimacion de Recursos InformeFreddy Calderon Vela tortisОценок пока нет
- 0TP DifusionДокумент3 страницы0TP DifusionAgustina ZapataОценок пока нет
- Traccion Del Acero Acabado FinalДокумент14 страницTraccion Del Acero Acabado FinalMonik PaulisОценок пока нет
- Tesis 3Документ13 страницTesis 3Gonzalo Escobar CainaОценок пока нет
- PRÁCTICA 4 y 5. Tratamientos TermoquímicosДокумент11 страницPRÁCTICA 4 y 5. Tratamientos TermoquímicosMoises RiveraОценок пока нет
- Clase 2 (25 de Agossto)Документ7 страницClase 2 (25 de Agossto)Luis Arturo Muñoz JorqueraОценок пока нет
- Ingeniería ambiental examen finalДокумент2 страницыIngeniería ambiental examen finalBryan BravoОценок пока нет
- Quiz de FundiciónДокумент2 страницыQuiz de Fundicióndiego joseОценок пока нет
- INFORME #006 Niquelado BrillanteДокумент7 страницINFORME #006 Niquelado BrillanteNoemi Quispe VillacortaОценок пока нет
- Bib2 U1 A2 PaghДокумент4 страницыBib2 U1 A2 Paghpaulina guerrero hernandezОценок пока нет
- Informe 6 Perdidas PrimariasДокумент19 страницInforme 6 Perdidas PrimariasCristian BarriaОценок пока нет
- Oxidación y CorrosiónДокумент12 страницOxidación y CorrosiónMartinОценок пока нет
- Cesar - Torres Tarea 8Документ7 страницCesar - Torres Tarea 8César Torres100% (1)
- Labo n1 Ensayo de JominyДокумент15 страницLabo n1 Ensayo de JominyJIMYJJJHHHОценок пока нет
- Lem 3 Primer ReporteДокумент6 страницLem 3 Primer ReporteVíctor Manuel Pérez HernándezОценок пока нет
- S8 - Tarea Resistencia de MaterialesДокумент6 страницS8 - Tarea Resistencia de Materialesjohn anthony lucero mirandaОценок пока нет
- Práctica de DesgasteДокумент7 страницPráctica de DesgasteDaniel CBОценок пока нет
- Propiedades Fisicas Y Quimicas de Recubrimientos TiO2 PDFДокумент8 страницPropiedades Fisicas Y Quimicas de Recubrimientos TiO2 PDFDiego PeñaОценок пока нет
- Pract 1 ElectroДокумент5 страницPract 1 ElectroSara Flores CasarrubiasОценок пока нет
- Cinética de cementación de cobre con zincДокумент7 страницCinética de cementación de cobre con zincJean Harrison Briceño ChihuanОценок пока нет
- Informe de LaboratorioДокумент7 страницInforme de LaboratorioVictorMiguelPalominoAvilaОценок пока нет
- Practica 2 Materiales de Ingeniería ESPOLДокумент11 страницPractica 2 Materiales de Ingeniería ESPOLPsycosiado DivertidoОценок пока нет
- Oxidación y corrosión de metales: Estudio comparativo del bronce, cobre y aceroДокумент16 страницOxidación y corrosión de metales: Estudio comparativo del bronce, cobre y aceroJordy Robinson Caichihua VergaraОценок пока нет
- Informe Técnico Diseño de Lixiviación Por BateaДокумент14 страницInforme Técnico Diseño de Lixiviación Por BateaPedro CortesОценок пока нет
- Taller 7.procesos Activados Por Temperatura y Difusion de SolidosДокумент9 страницTaller 7.procesos Activados Por Temperatura y Difusion de SolidosJenyfer Ardila BolañoОценок пока нет
- Examen final de Tecnología de MaterialesДокумент2 страницыExamen final de Tecnología de MaterialesJuan Carlos Aguilar SandovalОценок пока нет
- Tarea 8Документ7 страницTarea 8Alexis Varas Moreno100% (1)
- LAB3 Feno 2Документ6 страницLAB3 Feno 2Delfino Qquehue MaccapaОценок пока нет
- Memoria de Calculo E-SpДокумент20 страницMemoria de Calculo E-Spcarlos mejiaОценок пока нет
- Cuestionario Unidad Ii P1Документ7 страницCuestionario Unidad Ii P1manuel navaОценок пока нет
- Calculo Resistividad de TerrenoДокумент11 страницCalculo Resistividad de TerrenoRicardo Gómez MОценок пока нет
- Determinación de la conductividad térmica de materiales aislantesДокумент7 страницDeterminación de la conductividad térmica de materiales aislantesMilton HuamanchoqueОценок пока нет
- D 42168 Desbloqueado PDFДокумент171 страницаD 42168 Desbloqueado PDFPaulina FerrerОценок пока нет
- Plantilla - Tarea Semana 8Документ6 страницPlantilla - Tarea Semana 8jose muñozОценок пока нет
- Deterioro ambiental materialesДокумент6 страницDeterioro ambiental materialesjose muñozОценок пока нет
- Lab 3 - Fuertes NamoДокумент10 страницLab 3 - Fuertes NamoBRYAN RAFAEL FUERTES NAMOОценок пока нет
- Difusión del CarbonoДокумент13 страницDifusión del CarbonoMiguel ArguzОценок пока нет
- Grupo N°8 - PR4 - S3P4Документ15 страницGrupo N°8 - PR4 - S3P4Josue OrtizОценок пока нет
- Tarea 8 Iacc Resistencia MaterialesДокумент6 страницTarea 8 Iacc Resistencia MaterialesIgnacio Carvajal CortésОценок пока нет
- Practica 10 - DistribucionДокумент39 страницPractica 10 - DistribucionKevin Celis100% (1)
- Formato de Incorporacion de PartidaДокумент1 страницаFormato de Incorporacion de Partidarosver chinoОценок пока нет
- Informe Labo 1 PDFДокумент18 страницInforme Labo 1 PDFDUWAL EUDOCIO VARILLAS PRINCIPEОценок пока нет
- Pc2-Domiciliaria 2Документ6 страницPc2-Domiciliaria 2EDYLTHONОценок пока нет
- Ensayo JominyДокумент18 страницEnsayo JominyEd LCОценок пока нет
- Tecnología del Concreto I (EC 612-H) – Práctica de Aula N°1Документ2 страницыTecnología del Concreto I (EC 612-H) – Práctica de Aula N°1Pedro GarciaОценок пока нет
- Corrosión de placa de zinc a altas temperaturasДокумент7 страницCorrosión de placa de zinc a altas temperaturasPierre NeiraОценок пока нет
- Lab 3 TrefilaciónДокумент15 страницLab 3 TrefilaciónTomásОценок пока нет
- Informe de Reducción de MineralesДокумент12 страницInforme de Reducción de MineralesSilvia HernandezОценок пока нет
- Laboratorio Fluidos (1) (Autoguardado)Документ11 страницLaboratorio Fluidos (1) (Autoguardado)Cristian alexiss Gonzales pabloОценок пока нет
- Laboratorio 2 FINALДокумент15 страницLaboratorio 2 FINALCesar BolañosValenciaОценок пока нет
- Corrosión y protección de materialesДокумент24 страницыCorrosión y protección de materialesJose Fernando Rubio ValleОценок пока нет
- Informe Practica 1Документ14 страницInforme Practica 1Andres PerozoОценок пока нет
- Endurecimiento Por LlamaДокумент5 страницEndurecimiento Por LlamaHANS EVERT ANCO HUAMANОценок пока нет
- Informe LixiviacionДокумент5 страницInforme LixiviacionCHRISTIAN COLLAZOS PARDAVEОценок пока нет
- Resistencia de materiales - Corrosión y degradaciónДокумент6 страницResistencia de materiales - Corrosión y degradaciónJosafat Benavides Núñez100% (2)
- Obras de TomaДокумент87 страницObras de TomaAnonymous z78OXVGz9IОценок пока нет
- Recopilacion de Informacion Final Con Mapa PDFДокумент15 страницRecopilacion de Informacion Final Con Mapa PDFKevin PadillaОценок пока нет
- Tarea 6 HumanidadesДокумент2 страницыTarea 6 HumanidadesJonatan Goicochea BaconОценок пока нет
- Distancias de Los TKsДокумент1 страницаDistancias de Los TKsJonatan Goicochea BaconОценок пока нет
- FitEngineLA25ACO GДокумент1 страницаFitEngineLA25ACO GJonatan Goicochea BaconОценок пока нет
- 01 Bombeo de Agua1Документ16 страниц01 Bombeo de Agua1Jonatan Goicochea BaconОценок пока нет
- Rly IJBДокумент4 страницыRly IJBJonatan Goicochea BaconОценок пока нет
- Estado de ArteДокумент1 страницаEstado de ArteJonatan Goicochea BaconОценок пока нет
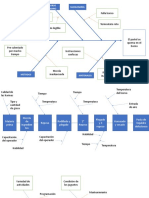
- Mala Receta Falla Horno: Medio Ambiente Recurso Humano MaquinariaДокумент6 страницMala Receta Falla Horno: Medio Ambiente Recurso Humano MaquinariaJonatan Goicochea BaconОценок пока нет
- Rly IJBДокумент4 страницыRly IJBJonatan Goicochea BaconОценок пока нет
- Diagrama - Causa-Efecto 2018Документ10 страницDiagrama - Causa-Efecto 2018FCELISОценок пока нет
- MC612 Taller 12 - Descripción de Sistemas, Subsistemas, Componentes y PartesДокумент1 страницаMC612 Taller 12 - Descripción de Sistemas, Subsistemas, Componentes y PartesJonatan Goicochea BaconОценок пока нет
- Plan de TesisДокумент10 страницPlan de TesisJonatan Goicochea BaconОценок пока нет
- Basilio Oscar Sistema Vision Control PesosДокумент81 страницаBasilio Oscar Sistema Vision Control PesosJonatan Goicochea BaconОценок пока нет
- T01 M377 TДокумент210 страницT01 M377 TCarlos Mallqui MuñozОценок пока нет
- (M3) Goicochea Bacon Jonatan NДокумент1 страница(M3) Goicochea Bacon Jonatan NJonatan Goicochea BaconОценок пока нет
- Gestion de La Calidad Tercera Práctica Calificada 2020 1Документ3 страницыGestion de La Calidad Tercera Práctica Calificada 2020 1Jonatan Goicochea BaconОценок пока нет
- Taller No 2 Apli. de Planf. y Prog de ProyectosДокумент7 страницTaller No 2 Apli. de Planf. y Prog de ProyectosJonatan Goicochea BaconОценок пока нет
- Monografía de RodamientosДокумент16 страницMonografía de RodamientosVeilSide VeilSidesОценок пока нет
- Soluciones climatización contra Covid-19Документ20 страницSoluciones climatización contra Covid-19Jonatan Goicochea BaconОценок пока нет
- MC612 Taller 13 - Construcción Experimental, Analisis de Pronóstico y Modificación Del ProyectoДокумент1 страницаMC612 Taller 13 - Construcción Experimental, Analisis de Pronóstico y Modificación Del ProyectoJonatan Goicochea BaconОценок пока нет
- Wps Especificacion Del Procedimiento de SoldaduraДокумент1 страницаWps Especificacion Del Procedimiento de SoldaduraJonatan Goicochea BaconОценок пока нет
- Solución ErroresДокумент1 страницаSolución ErroresRicardo Espindola RamosОценок пока нет
- MC612 Taller 11 - Preparación para El ProyectoДокумент1 страницаMC612 Taller 11 - Preparación para El ProyectoJonatan Goicochea BaconОценок пока нет
- Pro Yec To IngenieriaДокумент7 страницPro Yec To IngenieriaJonatan Goicochea BaconОценок пока нет
- Wps EjemploДокумент1 страницаWps EjemploJonatan Goicochea BaconОценок пока нет
- Modulo de Lecturas1Документ95 страницModulo de Lecturas1Fernando CortezОценок пока нет
- Lab 1b.-Modelo Matem Sistema DinamcoДокумент10 страницLab 1b.-Modelo Matem Sistema DinamcoJonatan Goicochea BaconОценок пока нет
- Tecnologia de La Soldadura PQR Wps WPQДокумент2 страницыTecnologia de La Soldadura PQR Wps WPQWilmer Zavaleta HuamanyauriОценок пока нет
- Soluciones climatización contra Covid-19Документ20 страницSoluciones climatización contra Covid-19Jonatan Goicochea BaconОценок пока нет
- Perfil Airlan PerúДокумент1 страницаPerfil Airlan PerúJonatan Goicochea BaconОценок пока нет
- Matriz de Identificacion de Peligros y Evaluacion de RiesgoДокумент4 страницыMatriz de Identificacion de Peligros y Evaluacion de RiesgoVictor Jesus Rios0% (1)
- 1° CienciasДокумент3 страницы1° CienciasCristian Flores BustamanteОценок пока нет
- Control de motores eléctricos con botones pulsadores de arranque y paroДокумент7 страницControl de motores eléctricos con botones pulsadores de arranque y parorafael salas munosОценок пока нет
- Como Convertir Un Archivo PDF A Word para EditarДокумент2 страницыComo Convertir Un Archivo PDF A Word para EditarBrandonОценок пока нет
- Incumplimiento InvoluntarioДокумент13 страницIncumplimiento InvoluntarioDionimar PereiraОценок пока нет
- Reseña Historica Mision CulturaДокумент2 страницыReseña Historica Mision CulturaAbraham HernandezОценок пока нет
- Radio CognitivaДокумент17 страницRadio CognitivaMoisesClintonSonccoHuisaОценок пока нет
- Trabajo 2 Corte - Tatiana QuinteroДокумент8 страницTrabajo 2 Corte - Tatiana Quinterotatiana quinteroОценок пока нет
- ParafinaДокумент3 страницыParafinakurtОценок пока нет
- Primer Momento C H M de 4Документ3 страницыPrimer Momento C H M de 4Ayelen MarquezОценок пока нет
- Motivación: de Los Conceptos A Las AplicacionesДокумент5 страницMotivación: de Los Conceptos A Las AplicacionesAndrea RenneeОценок пока нет
- Calibración de Material Volumétrico - Práctica 1 HarrisДокумент14 страницCalibración de Material Volumétrico - Práctica 1 HarrisJuan Luis Ramírez Agudelo100% (2)
- Trabajo 2 Fisica IiiДокумент2 страницыTrabajo 2 Fisica Iiikathy garciaОценок пока нет
- Guía PrácticaElSecretoLeydeAtraccionДокумент15 страницGuía PrácticaElSecretoLeydeAtraccionAlberto MarpezОценок пока нет
- Derecho de Peticion 3542992022 OkДокумент9 страницDerecho de Peticion 3542992022 OkFelix Armando Celis ValenciaОценок пока нет
- Presentacion Placas HuellasДокумент15 страницPresentacion Placas Huellasdaka59012Оценок пока нет
- TallerДокумент9 страницTallerPaola OlivosОценок пока нет
- Tecnicas de Negociacion Del Modulo N. 5 de La Universidad Tecnológica de Honduras UTHДокумент7 страницTecnicas de Negociacion Del Modulo N. 5 de La Universidad Tecnológica de Honduras UTHjojse alvarenga100% (2)
- TR1 Derecho EmpresarialДокумент4 страницыTR1 Derecho Empresarialbryan santiago leiva mozombiteОценок пока нет
- Cuestionario Estructuras de ConcretoДокумент67 страницCuestionario Estructuras de ConcretoJonatan RamosОценок пока нет
- Crucigrama Métodos de Separación - 1Документ2 страницыCrucigrama Métodos de Separación - 1Raul SánchezОценок пока нет
- Cartilla ADElante ABC SINDICAL - ESCUELA SINDICAL ADEДокумент30 страницCartilla ADElante ABC SINDICAL - ESCUELA SINDICAL ADEגאָרנישט גאָרנישטОценок пока нет
- Planta Alcaraván MBBRДокумент26 страницPlanta Alcaraván MBBRing_andreaОценок пока нет
- Mod 4 BTH para Llenar1Документ104 страницыMod 4 BTH para Llenar1Jhiamil Negretty Romero100% (1)
- Icat 16Документ86 страницIcat 16carmusic97Оценок пока нет
- INFORMEДокумент29 страницINFORMEcarlosmorgadohdzОценок пока нет
- Modulo de Fisica Grado 10Документ35 страницModulo de Fisica Grado 10YRDZ TUTOSОценок пока нет
- Mejorar aprendizaje matemáticasДокумент3 страницыMejorar aprendizaje matemáticasDiego Guitrón100% (2)
- Escala CUVE Agresion Escolar PDFДокумент10 страницEscala CUVE Agresion Escolar PDFDeborah L. Sievens FigueroaОценок пока нет
- Diseño OrganizacionalДокумент8 страницDiseño OrganizacionalCarlos RomeroОценок пока нет