Академический Документы
Профессиональный Документы
Культура Документы
Inflamación
Загружено:
tedarpe0 оценок0% нашли этот документ полезным (0 голосов)
20 просмотров3 страницыОригинальное название
Inflamación.docx
Авторское право
© © All Rights Reserved
Доступные форматы
DOCX, PDF, TXT или читайте онлайн в Scribd
Поделиться этим документом
Поделиться или встроить документ
Этот документ был вам полезен?
Это неприемлемый материал?
Пожаловаться на этот документАвторское право:
© All Rights Reserved
Доступные форматы
Скачайте в формате DOCX, PDF, TXT или читайте онлайн в Scribd
0 оценок0% нашли этот документ полезным (0 голосов)
20 просмотров3 страницыInflamación
Загружено:
tedarpeАвторское право:
© All Rights Reserved
Доступные форматы
Скачайте в формате DOCX, PDF, TXT или читайте онлайн в Scribd
Вы находитесь на странице: 1из 3
Inflamación
Cuando se produce una lesión tisular, ya sea debida a bacterias, traumatismos,
sustancias químicas, calor o cualquier otro fenómeno, los tejidos lesionados liberan
múltiples sustancias que dan lugar a cambios secundarios espectaculares en los tejidos
vecinos no lesionados. Este complejo de cambios tisulares se llama inflamación.
La inflamación se caracteriza por:
1) la vasodilatación de los vasos sanguíneos locales, con el consiguiente exceso de flujo
sanguíneo local.
2) el aumento de la permeabilidad de los capilares, lo que permite la fuga de grandes
cantidades de líquido hacia los espacios intersticiales.
3) a menudo la coagulación del líquido en los espacios intersticiales por un aumento en
las cantidades de fibrinógeno y otras proteínas que salen de los capilares.
4) la migración de un gran número de granulocitos y monocitos al tejido.
5) la tumefacción de las células tisulares. Algunos de los muchos productos tisulares que
provocan estas reacciones son la histamina, la bradicinina, la serotonina, las
prostaglandinas, varios productos de reacción diferentes del sistema del complemento,
los productos de reacción del sistema de coagulación de la sangre y múltiples sustancias
llamadas linfocinas, que liberan los linfocitos T sensibilizados. Varias de estas sustancias
activan con fuerza el sistema macrofágico y en pocas horas los macrófagos comienzan
a devorar los tejidos destruidos. Pero, a veces, los macrófagos también lesionan las
células tisulares que están todavía vivas.
Efecto «tabicador» de la inflamación.
Uno de los primeros resultados de la inflamación es «aislar» la zona lesionada del resto
de los tejidos. Los espacios tisulares y los linfáticos de la zona inflamada se bloquean
con coágulos de fibrinógeno de manera que durante algún tiempo apenas fluye líquido a
través de los espacios. Este proceso de tabicación retrasa la diseminación de bacterias
y productos tóxicos.
La intensidad del proceso inflamatorio suele ser proporcional al grado de lesión tisular.
Por ejemplo, cuando los estafilococos invaden los tejidos, liberan toxinas celulares muy
tóxicas. Como resultado de ello se produce una inflamación rápidamente (de hecho
mucho más rápido que la velocidad con la que los propios estafilococos se multiplican y
propagan). Luego la infección estafilocócica local se tabica muy rápidamente, lo que evita
su diseminación por el cuerpo. Los estreptococos, por el contrario, no producen este tipo
de destrucción tisular local intensa. Por eso el proceso de tabicación se desarrolla
lentamente a lo largo de varias horas, mientras muchos estreptococos se reproducen y
migran.
Respuestas del macrófago y el neutrófilo durante la inflamación
El macrófago tisular es la primera línea de defensa contra la infección. A los pocos
minutos de comenzar la inflamación, los macrófagos ya presentes en los tejidos, ya sean
histiocitos en los tejidos subcutáneos, macrófagos alveolares en los pulmones, microglia
en el encéfalo u otros, comienzan de inmediato sus acciones fagocíticas. Cuando se
activan por los productos de la infección y de la inflamación, el primer efecto es el
aumento de tamaño rápido de cada una de estas células. Después, muchos de los
macrófagos previamente sésiles pierden sus inserciones y se hacen móviles, formando
la primera línea de defensa frente a la infección durante la primera hora o más. El número
de estos macrófagos movilizados no es a menudo grande, pero puede salvar la vida.
La invasión por neutrófilos de la zona inflamada es una segunda línea de defensa.
Alrededor de la primera hora siguiente a la infección, un gran número de neutrófilos
comienza a invadir la zona inflamada desde la sangre. Esto se debe a citocinas
inflamatorias (p. ej., TNF, IL-1) y otros pro- ductos bioquímicos producidos por tejidos
inflamados que inician las siguientes reacciones:
1. Provocan una mayor expresión de moléculas de adhesión, como selectinas y molécula
de adhesión intracelular 1 (ICAM-1) en la superficie de las células endoteliales en los
capilares y las vénulas. Estas moléculas de adhesión, que reaccionan con moléculas de
integrina complementarias en los neutrófilos, hacen que estos se peguen a las paredes
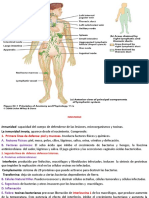
de los capilares y las vénulas de la zona inflamada. Este efecto se denomina marginación
y se muestra en la figura 33-2 y, con más detalle, en la figura 33-6.
2. Hacen también que las uniones intercelulares entre las células endoteliales de los
capilares y las vénulas pequeñas se aflojen, lo que deja aberturas suficientemente
grandes para que los neutrófilos avancen por diapédesis directa- mente desde la sangre
hacia los espacios tisulares.
3. Provocan la quimiotaxia de los neutrófilos hacia los tejidos lesionados, como se explicó
antes. De este modo, varias horas después de que comience la lesión tisular, la zona
está bien suplida de neutrófilos. Debido a que los neutrófilos sanguíneos ya son células
maduras, ya están preparados para comenzar de inmediato sus funciones de limpieza
matando bacterias y eliminando materiales extraños.
Aumento rápido del número de neutrófilos en la sangre: «neutrofilia».
También a los pocos minutos de empezar una inflamación aguda e intensa, el número
de neutrófilos en la sangre aumenta a veces cuatro a cinco veces: desde una cifra normal
de 4.000-5.000 a 15.000-25.000 neutrófilos por microlitro. A esto se le llama neutrofilia,
que significa aumento del número de neutrófilos en la sangre. La neutro- filia se debe a
los productos de la inflamación que entran en el torrente sanguíneo, llegan a la médula
ósea y allí actúan sobre los neutrófilos almacenados para movilizarlos hacia la sangre
circulante. Esto deja incluso más neutrófilos disponibles para la zona tisular inflamada.
La segunda invasión de macrófagos del tejido inflamado es una tercera línea de defensa.
Junto a la invasión de los neutrófilos, los monocitos procedentes de la sangre entran en
el tejido inflamado y aumentan de tamaño hasta convertirse en macrófagos. Pero el
número de monocitos en la sangre circulante es bajo: además, la reserva de monocitos
en la médula ósea es mucho menor que la de neutrófilos. Luego el aumento de
macrófagos en la zona del tejido inflamado es mucho más lento que el de los neutrófilos
y necesita varios días para ser eficaz. Además, incluso después de invadir el tejido
inflamado, los monocitos todavía son células inmaduras que necesitan 8h o más para
adquirir tamaños mucho mayores y desarrollar cantidades tremendas de lisosomas; sólo
entonces adquieren la capacidad plena de los macrófagos tisulares para la fagocitosis.
Después de varios días o semanas, los macrófagos dominan finalmente las células
fagocitarias de la zona inflamada por la mayor producción en la médula ósea de nuevos
monocitos, como se explica más adelante.
Como ya se ha señalado, los macrófagos pueden fagocitar muchas más bacterias (unas
cinco veces más) y partículas mucho más grandes, incluidos los propios neutrófilos y
grandes cantidades de tejido necrótico, que los neutrófilos. Además, los macrófagos
desempeñan una función importante en el inicio del desarrollo de los anticuerpos.
La mayor producción de granulocitos y monocitos en la médula ósea es una cuarta
línea de defensa.
La cuarta línea de defensa es una mayor producción de granulocitos y monocitos en la
médula ósea. Esto se debe a la estimulación de las células precursoras de granulocitos
y monocitos en la médula. Pero transcurren 3-4 días antes de que los granulocitos y
monocitos recién formados alcancen la fase de dejar la médula ósea. Si el estímulo
procedente del tejido inflamado continúa, la médula ósea puede continuar produciendo
estas células en cantidades tremendas durante meses e incluso años, a veces 20-50
veces con respecto a lo normal.
Вам также может понравиться
- Resumen Inflamacion Patologia RobbinsДокумент8 страницResumen Inflamacion Patologia RobbinsDennisse Pinto100% (4)
- Fisiopatología de La InflamaciónДокумент33 страницыFisiopatología de La InflamaciónVanessa Infante Liranzo71% (7)
- Cadena de FríoДокумент61 страницаCadena de Fríoauroritax100% (2)
- Inflamación J Reparacion Celular y CicatrizaciónДокумент80 страницInflamación J Reparacion Celular y CicatrizaciónElian Cruz100% (1)
- Clinica VacunacionДокумент11 страницClinica VacunacionLuciana Celín100% (1)
- Inmunoglobulinas 2010Документ36 страницInmunoglobulinas 2010Esteban J Higuera-LizcanoОценок пока нет
- Inflamación Aguda y CrónicaДокумент6 страницInflamación Aguda y CrónicaFernando Villavicencio100% (1)
- Inflamacion y Reparacion - Patologia - RobbinsДокумент14 страницInflamacion y Reparacion - Patologia - Robbinslidia chambi zelaОценок пока нет
- Inflamación aguda y crónicaДокумент18 страницInflamación aguda y crónicaYanina Pdv90% (10)
- Temario y Calendario Curso Dr. Prieto 2018-2019Документ46 страницTemario y Calendario Curso Dr. Prieto 2018-2019Carlos FajardoОценок пока нет
- Capitulo 33Документ5 страницCapitulo 33Fernanda Muñoz SotoОценок пока нет
- INFLAMACIÓNДокумент5 страницINFLAMACIÓNAimara FerreiraОценок пока нет
- 1 . - Leucocitos y Resistencia Del Cuerpo A La Infección.Документ13 страниц1 . - Leucocitos y Resistencia Del Cuerpo A La Infección.deeppurple.478Оценок пока нет
- 1 B . - Leucocitos y Resistencia Del Cuerpo A La InfecciónДокумент27 страниц1 B . - Leucocitos y Resistencia Del Cuerpo A La Infeccióndeeppurple.478Оценок пока нет
- LEUCOCITOSДокумент5 страницLEUCOCITOSAnkelly CeballoОценок пока нет
- Inmunidad innata: Primera línea de defensa contra la infecciónДокумент59 страницInmunidad innata: Primera línea de defensa contra la infecciónMaria Celeste Ajanel OsorioОценок пока нет
- Segundo Momento EvaluativoДокумент1 страницаSegundo Momento Evaluativofabianalora00Оценок пока нет
- Sistema InmunitarioДокумент11 страницSistema InmunitarioJoaquin Biglia AvanciniОценок пока нет
- Ciclo vital leucocitos: defensa inmunológicaДокумент3 страницыCiclo vital leucocitos: defensa inmunológicaAlicia VanegasОценок пока нет
- Macrófagos: defensas celulares del sistema inmuneДокумент14 страницMacrófagos: defensas celulares del sistema inmuneJavier Santos Molina OliveraОценок пока нет
- Fisioterapia InflamacionДокумент17 страницFisioterapia InflamacionCristobal Hernandez MadridОценок пока нет
- P13. Inmunidad. Miguel Vereau. 202120Документ57 страницP13. Inmunidad. Miguel Vereau. 202120GESU PIERO LOPEZ MEJIAОценок пока нет
- Mecanismos de Producción Del Proceso de InflamaciónДокумент22 страницыMecanismos de Producción Del Proceso de InflamaciónJunior ValdiviezoОценок пока нет
- Inflamación 1Документ7 страницInflamación 1Anny SolisОценок пока нет
- Lpaper Cat 2ectura-INFLAMACI-NДокумент2 страницыLpaper Cat 2ectura-INFLAMACI-NFer Aravena ToledoОценок пока нет
- 06 LeucocitosДокумент15 страниц06 LeucocitosKaren RamosОценок пока нет
- INFLAMACIONДокумент23 страницыINFLAMACIONSandra chopinОценок пока нет
- INFLAMACIONДокумент21 страницаINFLAMACIONZoOledad D'MatsumotoОценок пока нет
- Informacion InflamacionДокумент3 страницыInformacion InflamacionPaulo Valentin Arevalo ChumОценок пока нет
- Capitulo 34-SebastiansanchezДокумент2 страницыCapitulo 34-SebastiansanchezSebastian Sanchez MayaОценок пока нет
- Inflamación: respuesta protectora fundamentalДокумент7 страницInflamación: respuesta protectora fundamentalSadi danielaОценок пока нет
- Bacterias Gram PositivasДокумент6 страницBacterias Gram PositivasOmar ArnoldОценок пока нет
- Trabajo InmunidadДокумент11 страницTrabajo InmunidadalejandralumiereОценок пока нет
- 3.aspectos Fisiopatológicos Del Proceso InflamatorioДокумент19 страниц3.aspectos Fisiopatológicos Del Proceso InflamatorioJosefina Sepulveda OrtizОценок пока нет
- InmudidadДокумент34 страницыInmudidadFabrizzio RomeroОценок пока нет
- Resistencia Del Organismo A La InfecciónДокумент4 страницыResistencia Del Organismo A La InfecciónMayki QuintanaОценок пока нет
- Exposición - Equipo 9 LLДокумент13 страницExposición - Equipo 9 LLÁngel LagunasОценок пока нет
- Resumen Inflamacion Patologia RobbinsДокумент7 страницResumen Inflamacion Patologia RobbinsLorena Vera UbillúsОценок пока нет
- INMUNOLOGДокумент27 страницINMUNOLOGortiz1081Оценок пока нет
- Inflamación y reparación: procesos y mediadoresДокумент74 страницыInflamación y reparación: procesos y mediadoresChiara PereiraОценок пока нет
- Resumen Inflamacion Patologia RobbinsДокумент8 страницResumen Inflamacion Patologia RobbinsNicolas MuñozОценок пока нет
- LupusДокумент14 страницLupusKarla EscotoОценок пока нет
- Inflamación y reparación tisularДокумент17 страницInflamación y reparación tisularJuan Pablo LagosОценок пока нет
- Cuestionario Unidad VIДокумент3 страницыCuestionario Unidad VIKatherine YisselОценок пока нет
- Tarea Fisiopatología (Inflamación)Документ7 страницTarea Fisiopatología (Inflamación)Lucas MartinezОценок пока нет
- Barrera SecundariaДокумент5 страницBarrera SecundariaDereck AlayoОценок пока нет
- 13 Resistencia Del Organismo A La InfecciónДокумент37 страниц13 Resistencia Del Organismo A La InfecciónDANNA SADITH GUERRERO DELGADOОценок пока нет
- Las fases de la cicatrización: inflamación, proliferación y maduraciónДокумент2 страницыLas fases de la cicatrización: inflamación, proliferación y maduraciónTitanes Samaniego NarОценок пока нет
- Inflamación FisiopatologiaДокумент19 страницInflamación FisiopatologiaAimee ConcepcionОценок пока нет
- Barreras Naturales de La DefensaДокумент15 страницBarreras Naturales de La DefensaRaed OrtizОценок пока нет
- Sistema inmunológico: definición, tipos de defensa, antígeno y anticuerposДокумент12 страницSistema inmunológico: definición, tipos de defensa, antígeno y anticuerposJuan Ignacio D'AversaОценок пока нет
- Respuesta Del Macrofago y Neutrofilo Durante La InflamcionДокумент7 страницRespuesta Del Macrofago y Neutrofilo Durante La InflamcionIrvin SalgadoОценок пока нет
- Semiología Parte 2Документ30 страницSemiología Parte 2romiiirauqueОценок пока нет
- Respuesta InflamatoriaДокумент9 страницRespuesta Inflamatoriaclara baezОценок пока нет
- Inmuno Temas 1-4Документ34 страницыInmuno Temas 1-4marinachocolateblanco.negroОценок пока нет
- Inflamación y Reparación TisularДокумент7 страницInflamación y Reparación Tisulardailymarquez2606Оценок пока нет
- 2.-Resistencia Del Organismo A La InfecciónДокумент3 страницы2.-Resistencia Del Organismo A La InfecciónBeto HerreraОценок пока нет
- Inflamación aguda y crónica: causas, mecanismos y efectosДокумент36 страницInflamación aguda y crónica: causas, mecanismos y efectospersy dafneОценок пока нет
- Participación de Los Fagocitos en La Inflamación PDFДокумент7 страницParticipación de Los Fagocitos en La Inflamación PDFKamila Mendoza ArteagaОценок пока нет
- 4 InflamacionДокумент5 страниц4 Inflamaciongusmar5380100% (7)
- INFLAMACIÓNДокумент37 страницINFLAMACIÓNNatalia FrancoОценок пока нет
- Fuerza de TorsiónДокумент5 страницFuerza de TorsiónSebastian CondeОценок пока нет
- Culpable Porque Se Levanta TardeДокумент15 страницCulpable Porque Se Levanta TardeSebastian CondeОценок пока нет
- Cuáles Son Los Alimentos Con Bajo Índice GlicémicoДокумент3 страницыCuáles Son Los Alimentos Con Bajo Índice GlicémicoSebastian CondeОценок пока нет
- 631recomendaciones Tecnicas Cultivo AguacateДокумент55 страниц631recomendaciones Tecnicas Cultivo AguacateJuan GDОценок пока нет
- Control nervioso de la degluciónДокумент2 страницыControl nervioso de la degluciónSebastian CondeОценок пока нет
- Apoyo Internacional Del 911Документ2 страницыApoyo Internacional Del 911Sebastian CondeОценок пока нет
- Ac Monoclonales TereapeuticaДокумент37 страницAc Monoclonales TereapeuticaEverlyn WgОценок пока нет
- IntroducciónДокумент136 страницIntroducciónGybran VargasОценок пока нет
- Obste III - CLASE 3 SISTEMA INMUNEДокумент8 страницObste III - CLASE 3 SISTEMA INMUNESheila Constanza Araya TorresОценок пока нет
- 38 Octubre2014Документ80 страниц38 Octubre2014Eduardo RomeroОценок пока нет
- Aplicación de La Citometría A Flujo Al Diagnóstico de Las IDPДокумент2 страницыAplicación de La Citometría A Flujo Al Diagnóstico de Las IDPChristhopher TorresОценок пока нет
- Historia de La Vacuna - Fun - BiologicosДокумент16 страницHistoria de La Vacuna - Fun - BiologicosJuana Iris Rosales EscobarОценок пока нет
- Leucocitos, Neutrófilos y Fagocitosis.Документ10 страницLeucocitos, Neutrófilos y Fagocitosis.Luis Castillo CORTESОценок пока нет
- Capítulo 1 - Introducción A La Fisiología HumanaДокумент18 страницCapítulo 1 - Introducción A La Fisiología HumanaJessica Izchel Velasco BarajasОценок пока нет
- Salud Mental - Primer Examen DepartamentalДокумент24 страницыSalud Mental - Primer Examen DepartamentalJose Gregorio jr Flores CorderoОценок пока нет
- UD2. Técnicas Inmunológicas Basadas en Reacciones Antígeno Anticuerpo Secundarias o IndirectasДокумент24 страницыUD2. Técnicas Inmunológicas Basadas en Reacciones Antígeno Anticuerpo Secundarias o IndirectasVerónicaОценок пока нет
- 7 Hierbas Que Mejoran La Autofagia y La Curación CelularДокумент25 страниц7 Hierbas Que Mejoran La Autofagia y La Curación CelularConce Ramirez100% (3)
- Barreras EpitelialesДокумент4 страницыBarreras EpitelialesSilvia ArchiboldОценок пока нет
- Esta Filo Cocos IsДокумент9 страницEsta Filo Cocos Isjohn alderОценок пока нет
- Fisiopatologia Upao 3Документ23 страницыFisiopatologia Upao 3Marcos Israel Morales PiscoyaОценок пока нет
- Planificación Semanas 5-9 OctavoДокумент8 страницPlanificación Semanas 5-9 OctavoCristian NuñezОценок пока нет
- Inmunizaciones ResumenДокумент5 страницInmunizaciones Resumenydelisa felizОценок пока нет
- Manifestaciones Bucales de Enfermedades HematológicasДокумент27 страницManifestaciones Bucales de Enfermedades HematológicasJulio Cesar Rivera CazaresОценок пока нет
- Cuestionario Capitulos 7 y 8Документ17 страницCuestionario Capitulos 7 y 8Paúl sdetomateОценок пока нет
- Cómo Afectan Las Emociones Al Sistema InmunológicoДокумент8 страницCómo Afectan Las Emociones Al Sistema Inmunológicoandreamt123Оценок пока нет
- Estructura Informe de Indagación Científica (Con Hipótesis) (1) AlonzoДокумент11 страницEstructura Informe de Indagación Científica (Con Hipótesis) (1) AlonzoAlonzo Castillo100% (2)
- CAPÍTULO 287 - AsmaДокумент25 страницCAPÍTULO 287 - Asmaa180767Оценок пока нет
- 2941-HABILIDADES DEL PENSAMIENTO CIENTÍFICO-4-BM Egresados-7Документ10 страниц2941-HABILIDADES DEL PENSAMIENTO CIENTÍFICO-4-BM Egresados-7sanquimicoОценок пока нет
- Simulacro 2 Con RespuetasДокумент36 страницSimulacro 2 Con Respuetasavengersrm 2019Оценок пока нет
- Ganglios y Vasos LinfaticosДокумент21 страницаGanglios y Vasos LinfaticosSarmiento S PaОценок пока нет
- U1 y 2 Psicopato 2019 PDFДокумент180 страницU1 y 2 Psicopato 2019 PDFFl 24Оценок пока нет
- Temario TERCER MÓDULO - Arturo OvidioДокумент17 страницTemario TERCER MÓDULO - Arturo OvidiogustavoОценок пока нет