Академический Документы
Профессиональный Документы
Культура Документы
Estado Gaseoso Practica Experimental 2013
Загружено:
Gabriel RiosОригинальное название
Авторское право
Доступные форматы
Поделиться этим документом
Поделиться или встроить документ
Этот документ был вам полезен?
Это неприемлемый материал?
Пожаловаться на этот документАвторское право:
Доступные форматы
Estado Gaseoso Practica Experimental 2013
Загружено:
Gabriel RiosАвторское право:
Доступные форматы
UNIVERSIDAD TÉCNICA DE ORURO - FACULTAD NACIONAL DE INGENIERÍA - DPTO.
DE QUIMICA - ORURO-BOLIVIA
1. INTRODUCCION.
Se sabe que la materia se presenta en tres estados físicos o estado de generación molecular: sólido líquido y
gaseoso. De ellos el mas simple para estudiar es el estado gaseoso, por su baja agregación molecular, es decir
por la presencia de moléculas muy dispersa en todo un sistema. La diferencia entre los tres estados,
atendiendo su agregación molecular, radica principalmente a que en los gases las moléculas son individuales,
tiene una baja densidad por tanto ocupan un volumen muy grande, tienen una baja viscosidad esto les
permite fluir muy fácilmente con una diferencia de presión muy baja. Finalmente debido a la gran cantidad de
espacio vació entre gran cantidad de espacio entre moléculas de gas, un sistema de gas se puede someter a un
proceso de compresión y expansión en las funciones de las variables de estado. (T, P, V).
PROPIEDADES DEL ESTADO GASEOSO.-
Los gases, igual que los líquidos, no tienen forma fija pero, a diferencia de éstos, su volumen tampoco es fijo.
También son fluidos, como los líquidos.
En los gases, las fuerzas que mantienen unidas las partículas son muy pequeñas. En un gas el número de
partículas por unidad de volumen es también muy pequeño.
Las partículas se mueven de forma desordenada, con choques entre ellas y con las paredes del recipiente que
los contiene. Esto explica las propiedades de expansibilidad y compresibilidad que presentan los gases: sus
partículas se mueven libremente, de modo que ocupan todo el espacio disponible. La compresibilidad tiene un
límite, si se reduce mucho el volumen en que se encuentra confinado un gas éste pasará a estado líquido.
Al aumentar la temperatura las partículas se mueven más deprisa y chocan con más energía contra las paredes
del recipiente, por lo que aumenta la presión.
Aprovechando la baja agregación molecular del estado gaseoso.
Dibujar el diagrama P. T. para representar procesos.
Determinar procesos físicos y químicos.
2. OBJETIVOS.
Efectuar lecturas de presión y volumen a temperatura constante, para dibujar el diagrama P. V. y
calcular la constante de Boyle.
Efectuar medidas de volumen de gas a distintas temperaturas y presión constante para determinar el
coeficiente de expansión térmica 𝛼𝑜 . De un gas.
Determinar la densidad de un gas y explicar su comportamiento en función de la temperatura,
efectuando una reacción química solido-liquido.
3. FUNDAMENTO TEORICO.
LABORATORIO QMC-1206“B” - ESTADO GASEOSO - ING. MARIO HUANCA IBANEZ - PAGINA 1
UNIVERSIDAD TÉCNICA DE ORURO - FACULTAD NACIONAL DE INGENIERÍA - DPTO. DE QUIMICA - ORURO-BOLIVIA
Un gas se dice que tiene comportamiento ideal cuando en una mezcla no forma compuestos químicos, al ser
sometido a presiones relativamente altas y a temperatura relativamente bajas. Es cuando sus moléculas se
encuentran individuales, cuyo volumen es despreciable frente al volumen de todo un sistema, donde se
encuentra la masa del gas.
Un gas de campo.
𝑃
n = Cte.
𝑉
PROCESOS.
A B
T1
Proceso
𝑇𝑂
P1
𝑃𝑂
𝑉1
𝑉𝑂
Estado inicial Estado final
LEY DE BOYLE.
La Ley de Boyle-Mariotte (o Ley de Boyle), formulada por Robert Boyle y Edme Mariotte, es una de las leyes de
los gases ideales que relaciona el volumen y la presión de una cierta cantidad de gas mantenida a temperatura
constante. La ley dice que el volumen es inversamente proporcional a la presión:
(𝑃𝑉) 𝑇 = 𝐾
LEY DE CHARLES.
La Ley de Charles y Gay-Lussac, o simplemente Ley de Charles, es una de las leyes de los gases ideales.
Relaciona el volumen y la temperatura de una cierta cantidad de gas ideal, mantenido a una presión
constante, mediante una constante de proporcionalidad directa.
LABORATORIO QMC-1206“B” - ESTADO GASEOSO - ING. MARIO HUANCA IBANEZ - PAGINA 2
UNIVERSIDAD TÉCNICA DE ORURO - FACULTAD NACIONAL DE INGENIERÍA - DPTO. DE QUIMICA - ORURO-BOLIVIA
En esta ley, Jacques Charles dice que para una cierta cantidad de gas a una presión constante, al aumentar la
temperatura, el volumen del gas aumenta y al disminuir la temperatura el volumen del gas disminuye. Esto se
debe a que la temperatura está directamente relacionada con la energía cinética (debido al movimiento) de las
moléculas del gas. Así que, para cierta cantidad de gas a una presión dada, a mayor velocidad de las moléculas
(temperatura), mayor volumen del gas.
𝑉
( ) =𝐾
𝑇 𝑃
COEFICIENTE DE EXPANSIÓN TÉRMICA.
1 𝜕𝑉
𝛼𝑜 = ( )
𝑉𝑜 𝜕𝑇 𝑃
Densidad de un gas.
𝑚
𝑃𝑉 = 𝑅𝑇
𝑚
𝑃𝑀
𝜌=
𝑅𝑇
4. PROCEDIMIENTO EXPERIMENTAL.
LEY DE BOYLE.
Disponer del aparato montado como se muestra en la figura 1. Se dejan como unos 15 ml de la mezcla
de gases en el tubo neumometrico y se nivela el agua en ambas columnas, luego se cierra la llave del
tubo (se utiliza con este fin una bureta). Es importante que no existan fugas de gas o ingreso de aire al
aparato.
LABORATORIO QMC-1206“B” - ESTADO GASEOSO - ING. MARIO HUANCA IBANEZ - PAGINA 3
UNIVERSIDAD TÉCNICA DE ORURO - FACULTAD NACIONAL DE INGENIERÍA - DPTO. DE QUIMICA - ORURO-BOLIVIA
Déjese el aparato en un estado estacionario hasta que el agua adquiera la temperatura ambiente.
Seguidamente, elévese la ampolla a cuatro diferentes alturas y regístrese las variaciones de volúmenes
para cada altura. Repítanse las operaciones en otras seis posiciones anotándose sus volúmenes
respectivos. Regístrese la temperatura del medio ambiente y la presión atmosférica del medio.
LEY DE CHARLES.
Una vez instalado el aparato que se muestra en la figura 2, primeramente se efectúa la lectura en el
baño María y del volumen de gas contenido en el balón, la manguera y la parte de la bureta hasta
donde llega el nivel de agua, este nivel de referencia es el de importancia.
Es necesario revisar que no existan fugas de gas en el aparato, sobre todo en las conexiones.
Luego se procede al suministro de calor desde la fuente del regulador de voltaje, para calentar el baño
María a distintas temperaturas (de manera ascendente). A cada temperatura incrementada le
corresponde un incremento de volumen. Los incrementos de temperatura se deben efectuar con
intervalos de 2 ó 3 grados centígrados, con aproximaciones de 0.1℃.
LABORATORIO QMC-1206“B” - ESTADO GASEOSO - ING. MARIO HUANCA IBANEZ - PAGINA 4
UNIVERSIDAD TÉCNICA DE ORURO - FACULTAD NACIONAL DE INGENIERÍA - DPTO. DE QUIMICA - ORURO-BOLIVIA
APLICACIÓN DE LA ECUACION DE ESTADO.
Disponga del aparato que se muestra en la figura 3, efectué la reacción en el matraz de succión de
aproximadamente 0.33 gramos de mármol (𝐶𝑎𝐶𝑂3 ), con exceso de acido clorhídrico diluido, para la
producción de gas hidrogeno, del cual se desea determinar su densidad en condiciones determinadas
de presión y temperatura.
Se deben registrar la temperatura, el volumen de gas hidrogeno, la diferencia de altura de agua entre
el nivel de agua en el vaso y la probeta.
Repítase este procedimiento para seis temperaturas diferentes, en este caso la temperaturas fueron a
15.5, 25, 35, 45, 55 y 65℃.
5. DATOS Y RESULTADOS.
Para la prueba basada en la ley de R. Boyle debemos registrar los datos de volumen y altura de líquido
manométrico a temperatura ambiente, el cual debe considerarse una constante, en este caso
realizamos con dos grupos del aula el experimento pero solo tómanos de un solo grupo.
En cambio para la prueba basada en la Ley de Charles debemos registrar los datos de la temperatura
de forma ascendente y medir los volúmenes para determinar el coeficiente de expansión térmica,
para este experimento realizaron este proceso tres grupos del aula solo se tomo uno solo grupo Para
determinar el coeficiente de expansión térmica.
Para el tercer proceso de experimentación realizaron tres grupos del aula cada uno realizo a dos
temperaturas diferentes y se midió las alturas para determinar la densidad del gas.
LABORATORIO QMC-1206“B” - ESTADO GASEOSO - ING. MARIO HUANCA IBANEZ - PAGINA 5
UNIVERSIDAD TÉCNICA DE ORURO - FACULTAD NACIONAL DE INGENIERÍA - DPTO. DE QUIMICA - ORURO-BOLIVIA
DATOS DE LA PRUEBA Nº 1
𝑵º 𝑽 (𝒎𝒍) h ( cm)
1 12.5 +h3 186.0
2 15.0 +h2 96.0
3 17.4 +h1 43.0
4 19.4 0 0.0
5 20.0 -hi 68.5
6 27.6 -h2 117.0
7 30.5 -h3 152.0
DATOS DE LA PRUEBA Nº 2
𝑵º 𝑻 (℃) 𝑽 (𝒎𝒍)
1 18 321.6
2 22 326.0
3 25 329.5
4 28 333.3
5 32 337.7
6 35 340.0
7 38 343.7
8 41 349.9
9 44 353.1
10 47 359.1
DATOS DE LA PRUEBA Nº 3
𝑵º 𝑻 (℃) 𝒉 (𝒄𝒎)
1 15.5±1.0 18.3
2 25.0±1.0 17.2
3 35.0±1.0 15.2
4 45.0±1.0 13.5
5 55.0±1.0 12.5
6 65.0±1.0 11.7
Los cálculos para cada prueba se realizaran en la parte del apéndice.
LABORATORIO QMC-1206“B” - ESTADO GASEOSO - ING. MARIO HUANCA IBANEZ - PAGINA 6
UNIVERSIDAD TÉCNICA DE ORURO - FACULTAD NACIONAL DE INGENIERÍA - DPTO. DE QUIMICA - ORURO-BOLIVIA
6. DISCUSIONES Y CONCLUSIONES.
Bueno se pudo observar claramente que en el primer experimento existe cierto error como se puede
ver en la figura 4 donde tuve ciertos problemas para hallar la presión.
Ahora en el segundo experimento se pudo ver que el coeficiente de expasion termica se pudo hallar
sin mayores problemas.
Para el tercer experimento se realizo sin mayores problemas para hallar la densidad del gas donde
son relativamente bajas y esto nos indica que nuestros cálculos están relativamente bien hechas o
bien calculadas.
7. BIBLIOGRAFIA.
Guía de Practicas En Laboratorio De Fisicoquímica
Ing. Mario Huanca Ibáñez
www.wikipedia.com
I) APENDICE.
Los cálculos realizados y las tablas mostradas son cálculos de el primer experimento realizado en el curso por
dos grupos diferentes.
TABLA Nº 1
𝑵º 𝑽 (𝒎𝒍) h ( cm)
1 12.5 +h3 186.0
2 15.0 +h2 96.0
3 17.4 +h1 43.0
4 19.4 0 0.0
5 20.0 -hi 68.5
6 27.6 -h2 117.0
7 30.5 -h3 152.0
TABLA Nº 1.1
Nº V (ml) h (cm) V*V h*h v*h Y=a+bx
1 12,5 186 156,25 34596 2325 1897,775
2 15 96 225 9216 1440 1736,57
3 17,4 43 302,76 1849 748,2 1581,8132
4 19,4 0 376,36 0 0 1452,8492
5 20 68,5 400 4692,25 1370 1414,16
6 27,6 117 761,76 13689 3229,2 924,0968
7 30,5 152 930,25 23104 4636 737,099
∑ 142,4 662,5 3152,38 87146,25 13748,4 9744,3632
z
LABORATORIO QMC-1206“B” - ESTADO GASEOSO - ING. MARIO HUANCA IBANEZ - PAGINA 7
UNIVERSIDAD TÉCNICA DE ORURO - FACULTAD NACIONAL DE INGENIERÍA - DPTO. DE QUIMICA - ORURO-BOLIVIA
TABLA Nº 1.2
Nº 𝑽 (𝒎𝒍) 𝑷 (𝒎𝒎 𝑯𝒈)
1 12,5 2126,3
2 15 1773,3
3 17,4 1528,73
4 19,4 1371,84
5 20 1109,26
6 27,6 963,07
7 30,5 871,84
Diagrama presion volumen
2500
P (mmHg)
2000
1500
1000
Series1
500
0
0 10 20 30 40
V (ml)
Los siguientes cálculos son del segundo experimento realizado en el aula de fisicoquímica y en este caso nos
pide determinar el coeficiente de expansión térmica de un gas.
TABLA Nº 2
𝑵º 𝑻 (℃) 𝑽 (𝒎𝒍)
1 18 321.6
2 22 326.0
3 25 329.5
4 28 333.3
5 32 337.7
6 35 340.0
7 38 343.7
8 41 349.9
9 44 353.1
10 47 359.1
LABORATORIO QMC-1206“B” - ESTADO GASEOSO - ING. MARIO HUANCA IBANEZ - PAGINA 8
UNIVERSIDAD TÉCNICA DE ORURO - FACULTAD NACIONAL DE INGENIERÍA - DPTO. DE QUIMICA - ORURO-BOLIVIA
1 𝜕𝑉
𝛼𝑜 = ( )
𝑉𝑂 𝜕𝑇
1 4.4
𝛼1 = ( ) = 0.00342
321.6 4
1 3.5
𝛼2 = ( ) = 0.00358
326.0 3
1 3.8
𝛼3 = ( ) = 0.00384
329.5 3
1 4.4
𝛼4 = ( ) = 0.00330
333.3 4
1 2.3
𝛼5 = ( ) = 0.00227
337.7 3
1 3.7
𝛼6 = ( ) = 0.00363
340.0 3
1 6.2
𝛼7 = ( ) = 0.00601
343.7 3
1 3.2
𝛼8 = ( ) = 0.00304
349.9 3
1 6
𝛼9 = ( ) = 0.00566
353.1 3
𝛼𝑝𝑟𝑜𝑚𝑒𝑑𝑒𝑖𝑜 = 0.00386
1 37.5
𝛼𝑝𝑟𝑜𝑚𝑒𝑑𝑖𝑜 = ( ) = 0.00403
321.6 29
Cálculos realizados para determinar la densidad del gas estos datos son del tercer experimento realizado en el
aula por tres grupos diferentes.
TABLA Nº 3
𝑵º 𝑻 (℃) 𝒉 (𝒄𝒎)
1 15.5±1.0 18.3
2 25.0±1.0 17.2
3 35.0±1.0 15.2
4 45.0±1.0 13.5
5 55.0±1.0 12.5
6 65.0±1.0 11.7
LABORATORIO QMC-1206“B” - ESTADO GASEOSO - ING. MARIO HUANCA IBANEZ - PAGINA 9
UNIVERSIDAD TÉCNICA DE ORURO - FACULTAD NACIONAL DE INGENIERÍA - DPTO. DE QUIMICA - ORURO-BOLIVIA
Determinamos la densidad del gas ideal pero para realizar el calculo se debe realizar la conversión de la
temperatura de ℃ 𝑎 𝐾.
𝑔𝑟
𝑀𝐶𝑎𝐶𝑂3 = 100.0878 𝑙𝑎 𝑜𝑡𝑟𝑎 𝑚𝑎𝑠𝑎 𝑒𝑠 𝑑𝑒 0.33 𝑔𝑟 𝑢𝑠𝑎𝑑𝑎 𝑒𝑛 𝑒𝑙 𝑒𝑥𝑝𝑒𝑟𝑖𝑚𝑒𝑛𝑡𝑜
𝑚𝑜𝑙
𝑅 = 0.0821 𝑎𝑡𝑚 𝐿⁄𝐾 𝑚𝑜𝑙
𝑃𝑂𝑟𝑢𝑟𝑜 = 0.64 𝑎𝑡𝑚
𝑷𝑴
𝝆=
𝑹𝑻
0.64 𝑎𝑡𝑚 ∗ 100.0878 𝑔𝑟⁄𝑚𝑜𝑙
𝜌1 = = 2.704 𝑔𝑟⁄𝐿
0.0821 𝑎𝑡𝑚 𝐿⁄º𝐾 𝑚𝑜𝑙 ∗ 288.5 º𝐾
0.64 𝑎𝑡𝑚 ∗ 100.0878 𝑔𝑟⁄𝑚𝑜𝑙
𝜌2 = = 2.618 𝑔𝑟⁄𝐿
0.0821 𝑎𝑡𝑚 𝐿⁄º𝐾 𝑚𝑜𝑙 ∗ 298 º𝐾
0.64 𝑎𝑡𝑚 ∗ 100.0878 𝑔𝑟⁄𝑚𝑜𝑙
𝜌3 = = 2.533 𝑔𝑟⁄𝐿
0.0821 𝑎𝑡𝑚 𝐿⁄º𝐾 𝑚𝑜𝑙 ∗ 308 º𝐾
0.64 𝑎𝑡𝑚 ∗ 100.0878 𝑔𝑟⁄𝑚𝑜𝑙
𝜌4 = = 2.453 𝑔𝑟⁄𝐿
0.0821 𝑎𝑡𝑚 𝐿⁄º𝐾 𝑚𝑜𝑙 ∗ 318 º𝐾
0.64 𝑎𝑡𝑚 ∗ 100.0878 𝑔𝑟⁄𝑚𝑜𝑙
𝜌5 = = 2.378 𝑔𝑟⁄𝐿
0.0821 𝑎𝑡𝑚 𝐿⁄º𝐾 𝑚𝑜𝑙 ∗ 328 º𝐾
0.64 𝑎𝑡𝑚 ∗ 100.0878 𝑔𝑟⁄𝑚𝑜𝑙
𝜌6 = = 2.308 𝑔𝑟⁄𝐿
0.0821 𝑎𝑡𝑚 𝐿⁄º𝐾 𝑚𝑜𝑙 ∗ 338 º𝐾
0.64 𝑎𝑡𝑚 ∗ 100.0878 𝑔𝑟⁄𝑚𝑜𝑙
𝜌𝑝𝑟𝑜𝑚𝑒𝑑𝑖𝑜 = = 2.492 𝑔𝑟⁄𝐿
0.0821 𝑎𝑡𝑚 𝐿⁄º𝐾 𝑚𝑜𝑙 ∗ 313.083 º𝐾
TABLA Nº 3.1
𝑵º T (K) 𝒈𝒓
𝝆 ( ⁄𝑳)
1 288.5 2.704
2 298 2.618
3 308 2.533
4 318 2.453
5 328 2.378
6 338 2.308
LABORATORIO QMC-1206“B” - ESTADO GASEOSO - ING. MARIO HUANCA IBANEZ - PAGINA 10
UNIVERSIDAD TÉCNICA DE ORURO - FACULTAD NACIONAL DE INGENIERÍA - DPTO. DE QUIMICA - ORURO-BOLIVIA
Comportamiento del gas ideal
2.8
en funcion de la temperatura
d (gr/
2.7
2.6
2.5
Series1
2.4
L)
y = -0.008x + 5.0029 Linear (Series1)
2.3
R² = 0.9979
2.2
280 300 320 340 360
T (ºK)
0.64 𝑎𝑡𝑚 ∗ 0.33 𝑔𝑟
𝜌1 = = 0.00892 𝑔𝑟⁄𝐿 𝑚𝑜𝑙
0.0821 𝑎𝑡𝑚 𝐿⁄º𝐾 𝑚𝑜𝑙 ∗ 288.5 º𝐾
0.64 𝑎𝑡𝑚 ∗ 0.33 𝑔𝑟
𝜌2 = = 0.00863 𝑔𝑟⁄𝐿 𝑚𝑜𝑙
0.0821 𝑎𝑡𝑚 𝐿⁄º𝐾 𝑚𝑜𝑙 ∗ 298 º𝐾
0.64 𝑎𝑡𝑚 ∗ 0.33 𝑔𝑟
𝜌3 = = 0.00835 𝑔𝑟⁄𝐿 𝑚𝑜𝑙
0.0821 𝑎𝑡𝑚 𝐿⁄º𝐾 𝑚𝑜𝑙 ∗ 308 º𝐾
0.64 𝑎𝑡𝑚 ∗ 0.33 𝑔𝑟
𝜌4 = = 0.00809 𝑔𝑟⁄𝐿 𝑚𝑜𝑙
0.0821 𝑎𝑡𝑚 𝐿⁄º𝐾 𝑚𝑜𝑙 ∗ 318 º𝐾
0.64 𝑎𝑡𝑚 ∗ 0.33 𝑔𝑟
𝜌5 = = 0.00784 𝑔𝑟⁄𝐿 𝑚𝑜𝑙
0.0821 𝑎𝑡𝑚 𝐿⁄º𝐾 𝑚𝑜𝑙 ∗ 328 º𝐾
0.64 𝑎𝑡𝑚 ∗ 0.33 𝑔𝑟
𝜌6 = = 0.00761 𝑔𝑟⁄𝐿 𝑚𝑜𝑙
0.0821 𝑎𝑡𝑚 𝐿⁄º𝐾 𝑚𝑜𝑙 ∗ 338 º𝐾
0.64 𝑎𝑡𝑚 ∗ 0.33 𝑔𝑟
𝜌𝑃𝑟𝑜𝑚𝑒𝑑𝑖𝑜 = = 0.00822 𝑔𝑟⁄𝐿 𝑚𝑜𝑙
0.0821 𝑎𝑡𝑚 𝐿⁄º𝐾 𝑚𝑜𝑙 ∗ 313.083 º𝐾
En este caso utilizamos la masa usada en el experimento y luego hicimos una comparación para ver el
comportamiento del gas con ambas masas.
LABORATORIO QMC-1206“B” - ESTADO GASEOSO - ING. MARIO HUANCA IBANEZ - PAGINA 11
UNIVERSIDAD TÉCNICA DE ORURO - FACULTAD NACIONAL DE INGENIERÍA - DPTO. DE QUIMICA - ORURO-BOLIVIA
TABLA Nº 3.2
𝑵º T (K) 𝒈𝒓
𝝆 ( ⁄𝑳)
1 15,5 0,00892
2 25 0,00863
3 35 0,00835
4 45 0,00809
5 55 0,00784
6 65 0,00751
Comportamiento del gas en funcion
de la temperatura
0.009
d (gr/L)
0.0088
0.0086
0.0084
0.0082
Series1
0.008
0.0078 Linear (Series1)
0.0076 y = -3E-05x + 0.0093
R² = 0.9985
0.0074
0 20 40 60 80
T (K)
Bueno después de realizar el cálculo de la densidad con ambas masas se pudo obtener que el comportamiento
sea el mismo.
CUESTIONARIO.
a) Explique con diagramas el comportamiento de las dos primeras pruebas y que nombres reciben estos
diagramas.
LABORATORIO QMC-1206“B” - ESTADO GASEOSO - ING. MARIO HUANCA IBANEZ - PAGINA 12
UNIVERSIDAD TÉCNICA DE ORURO - FACULTAD NACIONAL DE INGENIERÍA - DPTO. DE QUIMICA - ORURO-BOLIVIA
Diagrama presion volumen
2500
P (mmHg)
2000
1500
1000
Series1
500
0
0 10 20 30 40
V (ml)
b) ¿Cuál es la temperatura y presión para la licuación de un gas y que nombres reciben estas variables de
estado? Explíquese el proceso de licuación con la ayuda de una grafica.
Licuación de los gases
El paso por el cual un gas se convierte a líquido se llama condensación. (Licuación de vapores).
Todos los gases se pueden licuar. Antiguamente se creía en la existencia de gases permanentes, porque era
imposible licuarlos, no obstante que eran sometidos a presiones de hasta 3000 atmósferas (oxígeno,
nitrógeno, hidrógeno, etc) Por los trabajos de Andrews (1875), se conoció la necesidad de una temperatura
determinada para efectuar la licuación de los gases.
Se denomina temperatura crítica a la temperatura límite para la licuación de un gas. Por encima de esta
temperatura es imposible licuar a un gas, aunque se le someta a enormes presiones.
Se llama presión crítica, a la presión que se necesita para licuar un gas cuando éste se encuentra en su
temperatura crítica.
SUSTANCIAS T. crítica P. crítica
Agua 356°C --
Anhídrido Sulfuroso 175°C 78 at.
Amoníaco 132°C 112 at.
Anhídrido carbónico 31°C 73 at.
Oxígeno -119°C 50 at.
Nitrógeno -147°C 34 at.
Eter -194°C --
Hidrógeno -240°C 13 at.
c)
LABORATORIO QMC-1206“B” - ESTADO GASEOSO - ING. MARIO HUANCA IBANEZ - PAGINA 13
Вам также может понравиться
- 1° Cuestionario 2020 QMC 1200Документ2 страницы1° Cuestionario 2020 QMC 1200Sergio Martin Huanca CondoriОценок пока нет
- 13Документ11 страниц13steve oliverОценок пока нет
- FISICAДокумент15 страницFISICAPaula MamaniОценок пока нет
- Primer Parcial (Enunciados) PDFДокумент4 страницыPrimer Parcial (Enunciados) PDFAilec GuarayoОценок пока нет
- Lab 9 AcabadoДокумент22 страницыLab 9 AcabadoGustavo CondarcoОценок пока нет
- Lab Nro 11 Fis 1200 F 1-2021 Relacion de Carga A Masa Del ElectronДокумент12 страницLab Nro 11 Fis 1200 F 1-2021 Relacion de Carga A Masa Del ElectronDiego Raul Barreta VillcaОценок пока нет
- CafeinaДокумент3 страницыCafeinaJesús Munayco FloresОценок пока нет
- LAB10 Cinetica Quimica - para CombinarДокумент19 страницLAB10 Cinetica Quimica - para CombinarEnrique Belzu RiosОценок пока нет
- Estado Gaseoso IДокумент18 страницEstado Gaseoso IRosmery Ramos ManriqueОценок пока нет
- Lab 5Документ9 страницLab 5andreaОценок пока нет
- Lab Nº6 de QMC 1206Документ10 страницLab Nº6 de QMC 1206Dennis Gutierrez RiojaОценок пока нет
- Lab #12 de QMC 1206Документ4 страницыLab #12 de QMC 1206Sady MarazОценок пока нет
- Practica de Laboratorio de AlquenosДокумент15 страницPractica de Laboratorio de Alquenosestefania vidarte juaniasОценок пока нет
- INFORME FIS 4 GBCДокумент10 страницINFORME FIS 4 GBCgabriel bautista cruzОценок пока нет
- Informe AlcoholesДокумент16 страницInforme AlcoholesCarla FloresОценок пока нет
- Lab 1 de TermodianmicaДокумент7 страницLab 1 de TermodianmicaYara VargasОценок пока нет
- Extraccion Cafec3adnaДокумент6 страницExtraccion Cafec3adnaFránkitóó Fèèstt ʚïɞОценок пока нет
- Laboratorio 2 ProductividadДокумент6 страницLaboratorio 2 ProductividadAdriana aguilar tercerosОценок пока нет
- Índice Adiabático de GasesДокумент11 страницÍndice Adiabático de GasesAngie Aliaga LeroОценок пока нет
- Laboratorio 4Документ7 страницLaboratorio 4Carla FloresОценок пока нет
- QMC 1400 Lab 6Документ10 страницQMC 1400 Lab 6naydaОценок пока нет
- Practica#1.Lab de Ope2Документ28 страницPractica#1.Lab de Ope2Andry Bohorquez100% (1)
- Calor Especifico de Líquidos Sólidos SolucionesДокумент10 страницCalor Especifico de Líquidos Sólidos SolucionesGabriel Rios100% (1)
- EJERCICIOS PRACTICA No 5 FIS 1102 CДокумент9 страницEJERCICIOS PRACTICA No 5 FIS 1102 Cwiltion cruzitoОценок пока нет
- Masa Molar de Gases FisicoquímicaДокумент10 страницMasa Molar de Gases FisicoquímicaMichael Waldo100% (1)
- Estado GaseosoДокумент12 страницEstado GaseosoandreaОценок пока нет
- Clase ELTДокумент3 страницыClase ELTEsther Rodriguez ChoqueОценок пока нет
- Relacion de Capacidades CalorificasДокумент11 страницRelacion de Capacidades CalorificasAlvaro Marcelo Gonzales Rodriguez100% (1)
- Metrologia Informe 1 MCI I G2Документ5 страницMetrologia Informe 1 MCI I G2LuisGerardОценок пока нет
- Termodinamica de Las Reacciones QuimicasДокумент11 страницTermodinamica de Las Reacciones QuimicasV Mendizabal JocelynОценок пока нет
- Tratamiento de Datos ExperimentalesДокумент8 страницTratamiento de Datos ExperimentalesMiguel Angel LopezОценок пока нет
- Estado GaseosoДокумент18 страницEstado GaseosoFlavia TercerosОценок пока нет
- Lab 2 TermodinamicaДокумент12 страницLab 2 TermodinamicaMarcos YaviОценок пока нет
- Examenes Parciales Fisicoquimica QMC 1206 PDFДокумент2 страницыExamenes Parciales Fisicoquimica QMC 1206 PDFAilec GuarayoОценок пока нет
- Informe N7Документ16 страницInforme N7Yojann Lopez VillcaОценок пока нет
- Analisis Minig SPECTROLAB PDFДокумент0 страницAnalisis Minig SPECTROLAB PDFtitohemanОценок пока нет
- Lab-1 QMC 1206Документ14 страницLab-1 QMC 1206Angie Aliaga Lero100% (1)
- PRQ 3257 Primer ParcialДокумент1 страницаPRQ 3257 Primer ParcialJacquelineОценок пока нет
- Laboratorio de TERMODINAMICAДокумент4 страницыLaboratorio de TERMODINAMICARolando0% (1)
- Fis 102 GammaДокумент3 страницыFis 102 GammaMaik Bladi MamaniОценок пока нет
- Lab 4 CAPACITOR DE PLACAS PLANAS PARALELASДокумент7 страницLab 4 CAPACITOR DE PLACAS PLANAS PARALELASJoseph EscobarОценок пока нет
- Ejercicios Resueltos QMC 1206 IIДокумент7 страницEjercicios Resueltos QMC 1206 IIAna Luisa Garnica SalgadoОценок пока нет
- Cinetica Quimica 11Документ24 страницыCinetica Quimica 11jacqueline sauce canazaОценок пока нет
- 2273 P4 ElectrotermiaДокумент2 страницы2273 P4 ElectrotermiaJose Luis Lopez Huarachi100% (1)
- Eteres 12Документ3 страницыEteres 12Luis CarlosОценок пока нет
- Practica 4 Tecnica de Analisis de Circuitos, Teorema de TheveninДокумент3 страницыPractica 4 Tecnica de Analisis de Circuitos, Teorema de TheveninCarlosОценок пока нет
- Exp4Qmc1206 22020Документ5 страницExp4Qmc1206 22020Armando Ibarra FernandezОценок пока нет
- Inv. 6 Medidor de ConcentricidadesДокумент4 страницыInv. 6 Medidor de ConcentricidadesPiter WellsОценок пока нет
- Lab 7 de QMC1206Документ7 страницLab 7 de QMC1206AllenWalkerОценок пока нет
- Laboratorio de Electronica 1 (Practica 1)Документ33 страницыLaboratorio de Electronica 1 (Practica 1)Luis AguilarОценок пока нет
- Laboratorio N9 3ley Termodinamica 1Документ31 страницаLaboratorio N9 3ley Termodinamica 1Dany Guzman100% (1)
- Lab 3 PicnometrosДокумент15 страницLab 3 PicnometrosVictor Alfredo Rios ChoqueОценок пока нет
- Lab 12 QMC 1206Документ19 страницLab 12 QMC 1206Gabriel Illanes MamaniОценок пока нет
- .Mat 1105 F Practica#3 Gutierrez G Diego D.Документ6 страниц.Mat 1105 F Practica#3 Gutierrez G Diego D.Diego GutierrezОценок пока нет
- Informe N - 1 FisicoquimicaДокумент14 страницInforme N - 1 FisicoquimicaHector Pocomucha ParragaОценок пока нет
- Practica 1QAPДокумент7 страницPractica 1QAPUriel García HernándezОценок пока нет
- Ley de BoyleДокумент17 страницLey de BoyleJuan Pablo Moran CaballeroОценок пока нет
- Practica7 SoriaVegaEdgarBenjaminДокумент23 страницыPractica7 SoriaVegaEdgarBenjaminBenjamin SoriaОценок пока нет
- Psicometría. Principios básicos y protocolos experimentales diversosОт EverandPsicometría. Principios básicos y protocolos experimentales diversosОценок пока нет
- Practica 1 RaulДокумент2 страницыPractica 1 RaulGabriel RiosОценок пока нет
- Formulario de Teoria de ColasДокумент2 страницыFormulario de Teoria de ColasGabriel RiosОценок пока нет
- EJEMPLO Manufactura SincrónicaДокумент2 страницыEJEMPLO Manufactura SincrónicaGabriel RiosОценок пока нет
- Proyecto Toma de DecisionesДокумент1 страницаProyecto Toma de DecisionesGabriel Rios100% (1)
- Diagrama de GozintoДокумент4 страницыDiagrama de GozintoGabriel RiosОценок пока нет
- Resumen Libro de Krajewski Y RitzmanДокумент93 страницыResumen Libro de Krajewski Y RitzmanGabriel RiosОценок пока нет
- Teoria de Inventarios ProyectoДокумент21 страницаTeoria de Inventarios ProyectoGabriel Rios100% (1)
- Tema 7 Primera Ley de La TermodinamicaДокумент22 страницыTema 7 Primera Ley de La TermodinamicaGabriel RiosОценок пока нет
- SIMULACIONДокумент26 страницSIMULACIONGabriel RiosОценок пока нет
- Practica 2 1-2018Документ20 страницPractica 2 1-2018Gabriel RiosОценок пока нет
- Relacion de Capacidades Calorificas de Los GasesДокумент11 страницRelacion de Capacidades Calorificas de Los GasesGabriel RiosОценок пока нет
- Laboratorio Fis-1100 #2Документ4 страницыLaboratorio Fis-1100 #2Gabriel RiosОценок пока нет
- Laboratorio # 9Документ9 страницLaboratorio # 9Gabriel RiosОценок пока нет
- Informe de LevasДокумент4 страницыInforme de LevasGabriel RiosОценок пока нет
- Masa Molar de Un Gas IdealДокумент8 страницMasa Molar de Un Gas IdealGabriel RiosОценок пока нет
- Calor de HidrataciónДокумент6 страницCalor de HidrataciónGabriel RiosОценок пока нет
- Calor Especifico de Líquidos Soluciones y SolidosДокумент13 страницCalor Especifico de Líquidos Soluciones y SolidosGabriel RiosОценок пока нет
- La Teoría de La Viscosidad de Los LíquidosДокумент10 страницLa Teoría de La Viscosidad de Los Líquidosjorge luisОценок пока нет
- Planta TermicaДокумент21 страницаPlanta TermicaAnthony HuhoОценок пока нет
- Bfde U3 A2 Brje PDFДокумент5 страницBfde U3 A2 Brje PDFJesús BuenoОценок пока нет
- Diagramas PsicrométricoДокумент11 страницDiagramas PsicrométricoKevin O. SangabrielОценок пока нет
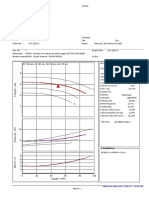
- Curva Bba. Nowa 5013 - para 50 m3-h - 3 BarДокумент2 страницыCurva Bba. Nowa 5013 - para 50 m3-h - 3 BarDiego palomino vittorОценок пока нет
- Vasos ComunicantesДокумент23 страницыVasos Comunicantesbaudilio utreraОценок пока нет
- Clase 20-06-2022Документ3 страницыClase 20-06-2022Eriica MendozaОценок пока нет
- Analisis de La Sensibilidad de Los Parametros Que Influyen en La Transferencia de Calor en Gasoductos PDFДокумент140 страницAnalisis de La Sensibilidad de Los Parametros Que Influyen en La Transferencia de Calor en Gasoductos PDFJuan Sebastian CamachoОценок пока нет
- Plantilla Trabajo Investigacion (Fisica-Chiclayo)Документ5 страницPlantilla Trabajo Investigacion (Fisica-Chiclayo)ROMERO TUÑOQUE ALDHAIRОценок пока нет
- CLASE VII-flujo de Fluidos en TuberiasДокумент75 страницCLASE VII-flujo de Fluidos en TuberiasDavid Palomino ParionaОценок пока нет
- 2.1 Composición Multifásica Del SueloДокумент9 страниц2.1 Composición Multifásica Del SueloYESSICA NAYIBE ROSERO YELAОценок пока нет
- Finales BiofisicaДокумент164 страницыFinales BiofisicaWendi RochaОценок пока нет
- Lab2 - BFI02A - 2019-1 (Autoguardado)Документ11 страницLab2 - BFI02A - 2019-1 (Autoguardado)Nicolle GonzalesОценок пока нет
- Ejercicios de Transferencia de CalorДокумент70 страницEjercicios de Transferencia de CalorMigdalia Coromoto Parejo Martinez100% (1)
- Curso Turbomáquinas I 2014-1 SGCH (Semana 6 y 7) PDFДокумент13 страницCurso Turbomáquinas I 2014-1 SGCH (Semana 6 y 7) PDFrarocerОценок пока нет
- Actividad 3-2 ProblemarioДокумент3 страницыActividad 3-2 ProblemarioKenia SegoviaОценок пока нет
- Operación Unitaria. Mezcla de LíquidosДокумент23 страницыOperación Unitaria. Mezcla de Líquidoskarla rosasОценок пока нет
- Ejercicios-Resueltos-Ciclo RankineДокумент3 страницыEjercicios-Resueltos-Ciclo RankineJosé ChintemiОценок пока нет
- Taller de Mecanica de Fluidos 20 PreguntasДокумент6 страницTaller de Mecanica de Fluidos 20 PreguntasKristian OliverosОценок пока нет
- Ej. Desarrollado en Clase PPTERMICAДокумент7 страницEj. Desarrollado en Clase PPTERMICARUTHОценок пока нет
- Ondas 2Документ12 страницOndas 2Maca PradesОценок пока нет
- Clase Temperatura y Dilatación Térmica Mecanica de Fluidos y TermodinámicaДокумент36 страницClase Temperatura y Dilatación Térmica Mecanica de Fluidos y TermodinámicaMario Leviguan Del RioОценок пока нет
- Practica de Determinación de Punto de FusiónДокумент8 страницPractica de Determinación de Punto de FusiónManuela CárdenasОценок пока нет
- Syllabus de Resistencia de Materiales PDFДокумент5 страницSyllabus de Resistencia de Materiales PDFDiego CabreraОценок пока нет
- Cristian Roco Tarea5Документ9 страницCristian Roco Tarea5rokacioОценок пока нет
- JB77-142 - Small Bolter 77Документ480 страницJB77-142 - Small Bolter 77Rene Ramos MenesesОценок пока нет
- Tablas de EmisividadДокумент5 страницTablas de EmisividadAndres0% (1)
- Trabajo Final Fisica IIДокумент14 страницTrabajo Final Fisica IIEstiven PeñaОценок пока нет
- TP FuegoДокумент7 страницTP FuegoJeremias GuibelaldeОценок пока нет