Академический Документы
Профессиональный Документы
Культура Документы
Practica 3"EXTRACCIÓN SÓLIDO-LÍQUIDO DE LOS COMPONENTES"
Загружено:
Ángel M. Rodriguez MИсходное описание:
Оригинальное название
Авторское право
Доступные форматы
Поделиться этим документом
Поделиться или встроить документ
Этот документ был вам полезен?
Это неприемлемый материал?
Пожаловаться на этот документАвторское право:
Доступные форматы
Practica 3"EXTRACCIÓN SÓLIDO-LÍQUIDO DE LOS COMPONENTES"
Загружено:
Ángel M. Rodriguez MАвторское право:
Доступные форматы
Instituto Tecnológico de Orizaba Ingeniería de Procesos Alimentarios
PRACTICA No. 3
“EXTRACCIÓN SÓLIDO-LÍQUIDO DE LOS COMPONENTES”
Fecha de realización: ______________
COMPETENCIAS A ADQUIRIR
Al alumno conoce los principios que rigen en el de extracción solido-liquido y su
aplicación en los alimentos.
Explica cómo afecta el tamaño de partícula y la temperatura la velocidad de extracción
solido-líquido durante el proceso.
INTRODUCCIÓN
En el laboratorio y en muchas industrias se llevan a cabo un sinfín de extracciones, pero en particular
la de sólido-líquido, la cual será la trabajada en esta práctica y será por contacto directo en este caso.
EXTRACCIÓN SÓLIDO-LÍQUIDO
La extracción sólido-líquido o lixiviación es una operación para separar los constituyentes solubles de
un sólido inerte con un solvente.
El proceso completo de la extracción suele comprender la recuperación por separado del solvente y el
soluto. La extracción sólido-líquido tiene gran importancia en un gran número de procesos industriales.
En metalurgia en la extracción de: cobre con ácido sulfúrico, oro con cianuro, etc.
Muchos productos orgánicos naturales se separan de sus estructuras originales mediante lixiviación.
Por ejemplo, el azúcar se separa por lixiviación de la remolacha con agua caliente; los aceites vegetales
se recuperan a partir de semillas, como las de soya y algodón mediante lixiviación con disolventes
orgánicos; el tanino se disuelve a partir de raíces y hojas de plantas. El té y el café se preparan mediante
técnicas y equipos similares a los utilizados en las verdaderas operaciones de lixiviación. Además los
precipitados químicos con frecuencia se lavan de sus aguas madres adheridas mediante técnicas y
equipos muy similares a los utilizados en las verdaderas operaciones de lixiviación, como el lavado de
licor de sosa caustica del carbonato de calcio precipitado después de la reacción entre el óxido de calcio
y el carbonato de sodio.
LIXIVIACIÓN Y EXTRACCIÓN EN LA INDUSTRIA QUÍMICA
Los sólidos se cargan en un tanque, se rocían con disolvente hasta reducir su contenido de soluto a un
valor económicamente mínimo y luego se vacían. En algunos casos la velocidad de disolución es tan
rápida que es suficiente en un solo paso del disolvente a través del material, pero es más frecuente
utilizar flujo en contracorriente del disolvente a través de una batería de tanques. En este método, el
Elaboró: M.A Justina Ocampo Linares
Instituto Tecnológico de Orizaba Ingeniería de Procesos Alimentarios
disolvente fresco se introduce en el tanque que contiene el sólido ya tratado, fluye a través de varios
tanques en serie y finalmente se retira del tanque por el que se carga la alimentación de sólido. Una
serie de tanques de este tipo recibe el nombre de batería de extracción. El sólido contenido en cualquiera
de los tanques es estacionario hasta que se extrae completamente. Las conexiones de las tuberías se
disponen de tal forma que tanto el disolvente fresco como la disolución concentrada se pueden introducir
y retirar respectivamente, de cualquier tanque, lo que permite cargar y descargar a la vez un tanque. Los
demás tanques de la batería se mantienen en operación en contracorriente, avanzando los tanques de
entrada y descarga a medida que se carga y se retira el material. Tal proceso se llama a veces proceso
Shanks.
En algunos casos de lixiviación el disolvente es volátil, siendo preciso utilizar recipientes cerrados
operados a presión. También se requiere presión para forzar el paso del disolvente a través del lecho
en el caso de sólidos poco permeables. Una serie de estos tanques de presión operados con flujo de
disolvente en contracorriente recibe el nombre de batería de difusión.
LIXIVIACIÓN DE SEMILLAS VEGETALES.
Las semillas de algodón, soya, semillas de lino, cacahuates, salvado ricino y muchos otros productos
similares, con frecuencia sufren la acción de lixiviación o extracción, con disolventes orgánicos que
separan los aceites vegetales que los contienen.
Las semillas generalmente deben prepararse en forma especial para obtener la mejor lixiviación; esto
puede emitir el descascarar, precocinar, el ajuste de contenido de la humedad (agua) y el prensado o
formación de hojuelas. Algunas veces, una parte del aceite se elimina inicialmente en forma mecánica
mediante expulsión o prensado. Generalmente, los disolventes de lixiviación son naftas de petróleo, para
muchos aceites una fracción muy cercana al hexano; los hidrocarburos clorados dejan un residuo
demasiado toxico para el alimento lixiviado y no puede utilizarse para la alimentación animal.
VELOCIDAD DE EXTRACCIÓN
La velocidad de extracción es afectada por los siguientes factores:
Temperatura
Concentración del solvente
Tamaño de partícula
Porosidad
Agitación
Al aumentar la temperatura se aumenta la velocidad porque la solubilidad es mayor, el aumento de
temperatura es muy usado en procesos de reacción química. La temperatura máxima para cada sistema
está limitada por: el punto de ebullición del solvente, solubilidad de impurezas y por economía.
Elaboró: M.A Justina Ocampo Linares
Instituto Tecnológico de Orizaba Ingeniería de Procesos Alimentarios
La concentración del solvente es importante para soluciones acuosas, debido a la saturación y a la
existencia de reacciones químicas, es de poca importancia cuando la extracción es controlada por
difusión.
La reducción de partículas tiene gran importancia, porque aumenta el área de contacto y disminuye el
tiempo necesario para la extracción, sobre todo para sólidos de baja porosidad.
La porosidad permite que el líquido penetre a través de los canales formados por lo9s poros dentro del
sólido, aumentando así el área activa para la extracción.
La agitación da una mayor eficiencia en la extracción debido a que disminuye la película de fluido que
cubre la superficie de los sólidos en reposos y que actúa como una resistencia a la difusión.
GENERALIDADES:
La lixiviación es una operación de transferencia de masa por lo que es indispensable que exista un
contacto íntimo entre el solvente y el soluto contenido en el sólido.
Factores a controlar en una lixiviación:
1) Tipo de solvente a utilizar
2) Temperatura del proceso
3) Tamaño de partícula del sólido
1) Selección del Solvente a utilizar:
El solvente empleado debe solubilizar al soluto
(agua azúcar; alcohol pectina y gomas; solventes orgánicos grasas y aceites)
El solvente ideal es el agua (bajo costo, no tóxica, no inflamable, no corrosiva), sin embargo no
siempre tiene una capacidad de extracción adecuada
El solvente empleado debe tener el mayor coeficiente de transferencia de masa posible
Elaboró: M.A Justina Ocampo Linares
Instituto Tecnológico de Orizaba Ingeniería de Procesos Alimentarios
2) La Temperatura del Proceso
Al aumentar la temperatura del proceso:
Aumenta la solubilidad del soluto en el solvente
Aumenta el coeficiente de difusión del solvente en las partículas de sólido
Lo que provoca una mayor velocidad de extracción Sin embargo, temperaturas muy
elevadas pueden deteriorar el producto o provocar la evaporación del solvente Se debe
encontrar la temperatura más adecuada para cada caso en particular
MATERIAL:
MATERIAL Y EQUIPO SUSTANCIA
Etiquetas Agua purificada
Guantes de carnaza Hojas de Jamaica
Termómetro
Gradilla metálica
4 vasos de pp. De 500ml.
Pipeta graduada de 10 ml
20 tubos de ensaye
Potenciómetro
Balanza analítica
Licuadora eléctrica
Parilla Eléctrica
PROCEDIMIENTO:
1) De una muestra de flor de Jamaica se toman 5gr. Se divide en dos. La primera se lleva a molienda
(2.5 g) , la segunda permanece en tamaño natural (2.5 g).
2) Se divide nuevamente en proporciones iguales ambas muestras (1.25 g).
3) Se agregan a los vasos de precipitado 300 ml de agua purificada a cada uno y se mantienen 2 a
una temperatura de 50°C y otros 2 a una temperatura de 90°C en una estufa.
4) 5 tubos de ensaye se destinaran para la muestra de la extracción de tamaño de partícula fina a
50°C, y otros 5 para la temperatura de 90°C, siendo tomados a 0, 2, 5, 10 y 15 min las muestras,
una vez iniciada la extracción.
5) De igual forma se procederá con la Jamaica “no molida (Entera)”.
6) Una vez alcanzada la temperatura constante de los vasos, se procede a la inmersión de la
Jamaica a cada uno de sus vasos respectivos, se toma una muestra en el instante de inmersión
(tiempo cero).
7) Habiendo terminado la toma de muestra, estas deben dejarse reposar para que disminuyan su
temperatura hasta la temperatura ambiente.
8) Se calibra el potenciómetro con agua destilada a pH=7 (puede utilizarse una solución buffer para
el mismo fin). Se procede a tomar la lectura del pH para cada uno de los 20 tubos. Anotar
resultados.
Elaboró: M.A Justina Ocampo Linares
Instituto Tecnológico de Orizaba Ingeniería de Procesos Alimentarios
OBSERVACIONES Y RESULTADOS
I) OBSERVACIONES
La materia prima principal para la realización de la practica fueron hojas de Jamaica
(Hibiscus sabdariffa)seca la cual se obtuvo del mercado Zapata ubicado en Oriente
9 A, Emiliano Zapata, 94320 Orizaba, Ver.
Se tomaron 5 g de materia prima la cual se dividió en dos partes igual, la primera se
lleva a molienda* (2.5 g) a esta se le nombro como parte “Molida” , la segunda
permanece en tamaño natural (2.5 g) a esta se le nombro como parte “Entera” ambas
partes se pesaron en una balanza analítica de la marca Adventurer TM OHAUS
*Para la molienda se utilizó una licuadora de la marca Osterizer, se trituraron 2.5 g de
modo que esta no fuera muy fina (polvo), lo cual basto unos pocos segundos en la
licuadora.
º
Posteriormente las dos partes divididas anteriormente se volvieron a dividir en dos
partes iguales lo cual nos resultarían 4 partes cada una con un peso igual de 1.25 g
Se tomaron 4 vasos de pp de 300 ml y se agrego agua purificada a cada uno de ellos. 2
vasos de precipitado se mantuvieron a una temperatura de 50 ºC y los otros 2 a una
temperatura de 90 ºC esto se logró utilizando termómetros de mercurio y una parrilla
eléctrica.
Se tomaron 10 tubos de ensaye para la “Parte Molida” de los cuales 5 tubos de ensaye
fueron destinados para la temperatura 50°C, y otros 5 para la temperatura de 90°C.
Parte Molida – Temperatura de 50 ºC
10 ml :
1.5 g
Cuando llegamos a la temperatura
deseada (50ºC), continuamos con
inmersión de la muestra, agregamos
los 1.5 g de muestra Molida, y a partir
de ahí tomamos alícuotas de 10 ml con
intervalos de tiempo de 0, 2, 5, 10, 15
minutos y los depositamos en cada tuvo
previamente etiquetado.
Esto lo repetimos con la temperatura de
90 ºC.
Elaboró: M.A Justina Ocampo Linares
Instituto Tecnológico de Orizaba Ingeniería de Procesos Alimentarios
Estos pasos se repitieron pero ahora con la parte “Entera”
Los tubos de ensaye se dejaron reposar para que
alcanzara la temperatura ambiente, pero para
hacer más ágil el proceso se puso un ventilador
pequeño para que la transferencia de calor fuera
mas rápido.
Y Para Finalizar se finalizar se tomó el pH conLO
un
Potenciómetro de la marca HANNA INSTRUMENT
HI 8314 y se anotaron los resultados
II) RESULTADOS
En la siguiente Tabla se encuentran los resultados obtenidos de las mediciones de pH de
Jamaica.
Tabla de resultados de mediciones de pH
Temperatura Tiempo pH Jamaica
(ºC) ( Minutos) Entera Molida
0 3.94 3.65
2 3.91 3.43
50 5 3.45 3.3
10 3.14 3.19
15 2.98 3.0
0 4.1 3.91
2 3.21 3.49
90 5 2.94 3.04
10 2.80 2.96
15 2.75 2.95
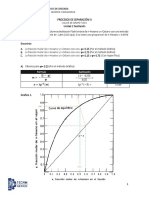
En la siguiente grafica se muestra la medición de pH con respecto al tiempo para temperatura
de 50 y 90 ºC.
Elaboró: M.A Justina Ocampo Linares
Instituto Tecnológico de Orizaba Ingeniería de Procesos Alimentarios
Mediciones de pH a 50 º C Mediciones de pH a 90 º C
4.5 4.5
4 4
3.5 3.5
pH - Jamaica
pH - Jamaica
3 3
2.5 2.5
2 2
1.5 1.5
1 1
0.5 0.5
0 0
0 5 10 15 20 0 5 10 15 20
Tiempo ( minutos ) Tiempo (minutos)
Entera ( 50º) Entera 90 º C Molida 90 º C
CUESTIONARIO
1.- Menciones dos procesos de la industria alimentaria donde se aplica la extracción solido-
liquido.
Las aplicaciones importantes de la extracción sólido-líquido en la industrias alimenticias son:
Los aceites vegetales se recuperan a partir de semillas, como los de soja y de algodón
mediante la lixiviación con disolventes orgánicos como: éter de petróleo, hexano, etc.
Extracción de colorantes a partir de materias sólidas por lixiviación con alcohol o soda.
Obtención de azúcar se separa por lixiviación de la remolacha con agua caliente.
Fabricación de té y café instantáneo.
2.- ¿Que es la extracción?
La extracción es la técnica empleada para separar un producto orgánico de una mezcla de reacción o
para aislarlo de sus fuentes naturales. Puede definirse como la separación de un componente de una
mezcla por medio de un disolvente.
En la práctica es muy utilizada para separar compuestos orgánicos de las soluciones o suspensiones
acuosas en las que se encuentran. El procedimiento consiste en agitarlas con un disolvente orgánico
inmiscible con el agua y dejar separar ambas capas. Los distintos solutos presentes se distribuyen entre
las fases acuosas y orgánica, de acuerdo con sus solubilidades relativas.
De este modo, las sales inorgánicas, prácticamente insolubles en los disolventes orgánicos más
comunes, permanecerán en la fase acuosa, mientras que los compuestos orgánicos que no forman
puentes de hidrógeno, insolubles en agua, se encontrarán en la orgánica.
Elaboró: M.A Justina Ocampo Linares
Instituto Tecnológico de Orizaba Ingeniería de Procesos Alimentarios
3.- ¿Cómo afecta la temperatura el grado de extracción?
Generalmente un aumento de temperatura aumenta la viscosidad (sabiendo que se da mejor extracción
a baja viscosidad) y coeficiente de reparto.
Un aumento de la temperatura favorece la solubilidad y aumentan los coeficientes de transferencia de
materia. El límite superior se fija atendiendo a criterios de calidad del producto, criterios económicos y
de seguridad con respecto al disolvente.
4.- ¿Cómo afecta el tamaño de partícula el grado de extracción?
Cualquiera que sea el método de extracción empleado, generalmente la materia prima (sólido) que
contiene al soluto debe acondicionarse (corte, trituración, molienda) para propiciar el contacto con el
solvente y facilitar su extracción.
Las partículas pequeñas crean una mayor área interfacial entre el sólido y el líquido y una
distancia más corta para que el soluto se difunda a través de la partícula y alcance la superficie.
Pero si el tamaño de partícula es demasiado pequeño, se forman conglomerados que impiden la
circulación de solvente entre las partículas y dificultan su separación del solvente provocando
que las partículas de sólido puedan ser arrastradas con el solvente.
CONCLUSIÓN
La extracción solido - liquido o lixiviación es una operación importante para separar las partes solubles
de un solido inerte con un solvente, por eso es importante manejar este proceso a la perfección en el
laboratorio de alimentos , También debemos saber que a medida que cambia la temperatura y pasa el
tiempo la extracción de nuestra muestra se va ver afectada por el pH, mientras mayor sea el tiempo de
extracción mayor va ser la concentración.
BIBLIOGRAFÍA
http://www.quimicaorganica.net/extraccion.html
https://www.slideshare.net/flordemariahs/extraccin-solidoliquido-lixiviacion
https://es.wikipedia.org/wiki/Hibiscus_sabdariffa
http://sgpwe.izt.uam.mx/files/users/uami/mlci/lixiv_introd.pdf
Elaboró: M.A Justina Ocampo Linares
Instituto Tecnológico de Orizaba Ingeniería de Procesos Alimentarios
Elaboró: M.A Justina Ocampo Linares
Вам также может понравиться
- Práctica #1 - Evaporador de Película AscendenteДокумент15 страницPráctica #1 - Evaporador de Película AscendenteDiana R SanchezОценок пока нет
- Torre de Absorción.Документ15 страницTorre de Absorción.tocinopОценок пока нет
- Ejemplos de ProcesosДокумент27 страницEjemplos de ProcesosEsme VidalОценок пока нет
- Laboratorio Integral II Ecuacion de ArrheniusДокумент14 страницLaboratorio Integral II Ecuacion de ArrheniusJose Alfredo Vargas25% (4)
- Pract-6-Evaporador de Pelicula AscendenteДокумент14 страницPract-6-Evaporador de Pelicula AscendenteJulio BarrancoОценок пока нет
- Articulo Importancia de Los Reactores PDFДокумент6 страницArticulo Importancia de Los Reactores PDFCamilo Cortés100% (1)
- Procesos de Separacion 3Документ7 страницProcesos de Separacion 3Jonathan Contreras0% (1)
- Ejercicios de ClaseДокумент5 страницEjercicios de Clase'Marhiamszz' SrZz100% (1)
- Laboratorio Practica de SecadorДокумент8 страницLaboratorio Practica de SecadorJulio BarrancoОценок пока нет
- Guia EvaporadoresДокумент3 страницыGuia EvaporadoresNerak QuelaliОценок пока нет
- Cuestionario IntroДокумент3 страницыCuestionario IntroFANYОценок пока нет
- Cristalizacion Ope .Документ52 страницыCristalizacion Ope .vinibenalОценок пока нет
- Practica 1 (Completa) - DifusionДокумент22 страницыPractica 1 (Completa) - DifusionLlovll Maywood100% (3)
- Práctica 6. Evaporador de Pelicula AcendenteДокумент8 страницPráctica 6. Evaporador de Pelicula AcendenteDaniel Zebadua ZentenoОценок пока нет
- Extraccion Liquido-LiquidoДокумент38 страницExtraccion Liquido-LiquidonanyОценок пока нет
- Práctica 9 (Centrifuga de Canasta)Документ9 страницPráctica 9 (Centrifuga de Canasta)Lupita CoronaОценок пока нет
- Tipos de Empaques. Operaciones de Transferencia de Calor y Momentum.Документ7 страницTipos de Empaques. Operaciones de Transferencia de Calor y Momentum.Leonel QuintalОценок пока нет
- Práctica 11. Coeficiente de Difusión en Fase GaseosaДокумент10 страницPráctica 11. Coeficiente de Difusión en Fase GaseosaItzel Daniela Solis TinocoОценок пока нет
- Teoria de Los Reactores No IdealesДокумент21 страницаTeoria de Los Reactores No IdealesLesly GelacioОценок пока нет
- 15 Eficacia de Murphree PDFДокумент47 страниц15 Eficacia de Murphree PDFKevin Cabistán Calderón100% (2)
- Reactores HeterogeneosДокумент6 страницReactores HeterogeneosNataly OsorioОценок пока нет
- Destilacion Op3Документ106 страницDestilacion Op3luceroОценок пока нет
- Cuestionario 1-9Документ6 страницCuestionario 1-9Joel Machaca G100% (3)
- Trabajo Destilacion FraccionadaДокумент25 страницTrabajo Destilacion Fraccionadamarieladelabarra100% (1)
- Actividad 2 - Parametros de Diseño de Evaporadores.Документ4 страницыActividad 2 - Parametros de Diseño de Evaporadores.Ruben PachecoОценок пока нет
- Clase 6. DesactivaciónДокумент69 страницClase 6. DesactivaciónAndrea SánchezОценок пока нет
- 3.3 Reacción CatalizadaДокумент16 страниц3.3 Reacción CatalizadaJORDIОценок пока нет
- Método MickleyДокумент3 страницыMétodo MickleyAnonymous 1iU7GjRNdОценок пока нет
- Consideraciones de Diseño en Columnas EmpacadasДокумент6 страницConsideraciones de Diseño en Columnas Empacadas042696673410% (1)
- Destilacion RepentinaДокумент9 страницDestilacion Repentinavictor JavierОценок пока нет
- Calculos en HumidificacionДокумент62 страницыCalculos en Humidificacionleslye floressОценок пока нет
- Torres de RellenoДокумент14 страницTorres de RellenoVanessa FV75% (4)
- Problemas Humidificación y Enfriamiento de Agua1Документ3 страницыProblemas Humidificación y Enfriamiento de Agua1conker4Оценок пока нет
- 2.3 Metodos para La Determinación de La Velocidad de ReacciónДокумент20 страниц2.3 Metodos para La Determinación de La Velocidad de ReacciónJORDIОценок пока нет
- Unidad 2Документ56 страницUnidad 2Yennifer Giselle Martinez100% (1)
- Diseño Termodinámico de Un Intercambiador de CalorДокумент10 страницDiseño Termodinámico de Un Intercambiador de CalorFUMARROLA33% (3)
- Modelo Matematico de Torre de DestilacionДокумент16 страницModelo Matematico de Torre de DestilacionMarinely OviedoОценок пока нет
- Practica 10 Cinetica Química de Una RX CatalizadaДокумент49 страницPractica 10 Cinetica Química de Una RX CatalizadaDanny GarcíaОценок пока нет
- Diseño de SecadoresДокумент19 страницDiseño de SecadoresChilamBalamОценок пока нет
- Practica 3. Lechos FluidizadosДокумент13 страницPractica 3. Lechos FluidizadosAndrea Castillo0% (1)
- Caída de Presión en Lechos FluidizadosДокумент7 страницCaída de Presión en Lechos FluidizadosGilberto Ontiveros100% (1)
- AdsorcionДокумент4 страницыAdsorcionJanelly TejedaОценок пока нет
- Platos Perforados Patentados y Con BajanteДокумент39 страницPlatos Perforados Patentados y Con BajanteCarlos ArenasОценок пока нет
- Platos de VálvulaДокумент10 страницPlatos de Válvulaluis sanchez100% (1)
- Tipos de Columnas EmpacadasДокумент3 страницыTipos de Columnas EmpacadasJessica Romero Fontalvo100% (2)
- Equipos de EvaporacionДокумент14 страницEquipos de EvaporacionLuisSaavedraFlores100% (1)
- PRACTICA #10 ElectroquimicaДокумент9 страницPRACTICA #10 ElectroquimicaMiriam Vasquez Bravo100% (1)
- Tipos de Equipos de EvaporacionДокумент37 страницTipos de Equipos de Evaporacionromero3194Оценок пока нет
- Laboratorio Integral 3. - Práctica 9. - Extracción Sólido-LíquidoДокумент9 страницLaboratorio Integral 3. - Práctica 9. - Extracción Sólido-LíquidoDavidHerreraОценок пока нет
- Equipos de HumidificacionДокумент9 страницEquipos de HumidificacionIsabella Quevedo100% (2)
- TALLER Ingeniería de Las Reacciones Químicas 1 PDFДокумент4 страницыTALLER Ingeniería de Las Reacciones Químicas 1 PDFAndres LlorenteОценок пока нет
- Equipo 4 SedimentacionДокумент43 страницыEquipo 4 SedimentacionDensin Velazquez del Valle0% (1)
- Taller Extracción Liquido - LiquidoДокумент7 страницTaller Extracción Liquido - LiquidoAndrea Rojas VargasОценок пока нет
- Informe de Lixiviacion Ing 2Документ21 страницаInforme de Lixiviacion Ing 2bcampos0% (1)
- Extraccion de Colorante de Pepa de Palta - UNT Lozano Ayala DanielДокумент25 страницExtraccion de Colorante de Pepa de Palta - UNT Lozano Ayala Danieldelozaya100% (12)
- Métodos de ExtracciónДокумент6 страницMétodos de ExtracciónDan MárquezОценок пока нет
- Informe de Lixiviacion Ing 2Документ19 страницInforme de Lixiviacion Ing 2Edwincito FloresОценок пока нет
- LixiviacionДокумент16 страницLixiviacionArturo PeraltaОценок пока нет
- Actividad Proceso de Extraccion de ColorantesДокумент14 страницActividad Proceso de Extraccion de ColorantesLuis Barriga MonteroОценок пока нет
- Extraccion de Colorante de Pepa de Palta UNT Lozano Ayala DanielДокумент26 страницExtraccion de Colorante de Pepa de Palta UNT Lozano Ayala DanielFanyta FanytaОценок пока нет
- Problema 2.2 - Matlab SoluciónДокумент3 страницыProblema 2.2 - Matlab SoluciónÁngel M. Rodriguez MОценок пока нет
- Deshidratación SecadoДокумент33 страницыDeshidratación SecadoÁngel M. Rodriguez MОценок пока нет
- Problema 2.6 Montgomey 2013 y 1991Документ9 страницProblema 2.6 Montgomey 2013 y 1991Ángel M. Rodriguez MОценок пока нет
- Diseño de Una Columna Flash en AspenДокумент4 страницыDiseño de Una Columna Flash en AspenÁngel M. Rodriguez MОценок пока нет
- ADSORCIÓN ExposiciónДокумент13 страницADSORCIÓN ExposiciónÁngel M. Rodriguez MОценок пока нет
- 02 - Tipos de PlatosДокумент8 страниц02 - Tipos de PlatosÁngel M. Rodriguez MОценок пока нет
- Examen de Secado/Preguntas/Unidad 5.Документ10 страницExamen de Secado/Preguntas/Unidad 5.Ángel M. Rodriguez M100% (1)
- 1000 Frases en InglesДокумент33 страницы1000 Frases en InglesUlises Novoa100% (1)
- Cortes de VegetalesДокумент11 страницCortes de VegetalesSebastianОценок пока нет
- Pensum Ing. de Alimentos Universidad de La SalleДокумент1 страницаPensum Ing. de Alimentos Universidad de La SallesdmorenorОценок пока нет
- Gastronomía de La Costa Del Golfo de MéxicoДокумент18 страницGastronomía de La Costa Del Golfo de MéxicoIrving OchoaОценок пока нет
- Bienestar Animal para Operarios en Rastros de BovinosДокумент58 страницBienestar Animal para Operarios en Rastros de BovinosAnonymous tBJwSUSjОценок пока нет
- 06 Ejercicios PQ-ABC SolДокумент8 страниц06 Ejercicios PQ-ABC SolNelva SilviaОценок пока нет
- 3 - Evaluacion Del AtletaДокумент47 страниц3 - Evaluacion Del AtletaCОценок пока нет
- Norma CodexДокумент9 страницNorma CodexDvonne HartОценок пока нет
- PROYECTO - DE - INVERSION - PALETERIA NДокумент18 страницPROYECTO - DE - INVERSION - PALETERIA NMillén PincayОценок пока нет
- Verbos ModalesДокумент5 страницVerbos ModalesJudith MataОценок пока нет
- Citopreparación e HistoquímicaДокумент22 страницыCitopreparación e HistoquímicaAtenea Garcia RiveroОценок пока нет
- Resumen Caperucita en ManhattanДокумент5 страницResumen Caperucita en Manhattanmiki.treppiedi12Оценок пока нет
- Formato 03 - Plan de Trabajo - AlpayanAAA PDFДокумент4 страницыFormato 03 - Plan de Trabajo - AlpayanAAA PDFNolan Diaz NureñaОценок пока нет
- En La Industria CerveceraДокумент2 страницыEn La Industria CerveceraAnonymous 3OEeCYUJb100% (1)
- Siglo21 20150720Документ36 страницSiglo21 20150720Anonymous Hov228VОценок пока нет
- Encuestas AgronomiaДокумент5 страницEncuestas AgronomiaMoises Asto Caceres100% (2)
- Efecto de Tres Tipos de Biol y Dos Densidades de Siembra en El Cultivo de LechugaДокумент186 страницEfecto de Tres Tipos de Biol y Dos Densidades de Siembra en El Cultivo de LechugaRuben SierraОценок пока нет
- TRABAJODEABASДокумент7 страницTRABAJODEABASSarina Alexandra Siña GarciaОценок пока нет
- FYF Semana4 Paleo S7Документ50 страницFYF Semana4 Paleo S7Rita Arrieta HerreraОценок пока нет
- Organigrama y PropuestaДокумент2 страницыOrganigrama y PropuestaClau ArbillaОценок пока нет
- Recetas Master Class CuscoДокумент58 страницRecetas Master Class CuscoJavier CorreaОценок пока нет
- Los Trastornos Alimenticios Impiden La Absorción de NutrientesДокумент2 страницыLos Trastornos Alimenticios Impiden La Absorción de NutrientesNicolás Romero RuizОценок пока нет
- Foda BimboДокумент3 страницыFoda BimboAnonymous yMn6VLwOEОценок пока нет
- Industria Carnica PDFДокумент48 страницIndustria Carnica PDFalbtotoОценок пока нет
- Menu KokolaДокумент2 страницыMenu KokolaAída Rodríguez JiménezОценок пока нет
- Anexo 1. Sesión 1 Elaboración de Mezcla de Alimento (ALTERNA)Документ7 страницAnexo 1. Sesión 1 Elaboración de Mezcla de Alimento (ALTERNA)Edinson Padilla PajaroОценок пока нет
- Singani de LuribayДокумент6 страницSingani de LuribayCarola GuzmánОценок пока нет
- Mod. 3 Proteínas (Bis)Документ12 страницMod. 3 Proteínas (Bis)laialhpОценок пока нет
- Pss Mex Suma EdenДокумент2 страницыPss Mex Suma EdenFrank ZambranoОценок пока нет
- Catálogo Petunia Repostería Con Alma WP PDFДокумент6 страницCatálogo Petunia Repostería Con Alma WP PDFMateo Penilla AlzateОценок пока нет