Академический Документы
Профессиональный Документы
Культура Документы
Determinacion de La Pureza de Vinagre Por Titulacion Potenciometrica
Загружено:
Luis Fernando Muñuico CardenasАвторское право
Доступные форматы
Поделиться этим документом
Поделиться или встроить документ
Этот документ был вам полезен?
Это неприемлемый материал?
Пожаловаться на этот документАвторское право:
Доступные форматы
Determinacion de La Pureza de Vinagre Por Titulacion Potenciometrica
Загружено:
Luis Fernando Muñuico CardenasАвторское право:
Доступные форматы
UNIVERSIDAD NACIONAL DEL ALTIPLANO
FACULTAD DE INGENERIA QUIMICA
DETERMINACION DE LA PUREZA DE VINAGRE POR TITULACION
POTENCIOMETRICA
I. OBJETIVOS
Determinar la pureza de la sustancia problema
Realizar curvas potenciometricas
Analizar y dar resultado a los cálculos presentes
II. FUNDAMENTO TEORICO
Existen muchos sistemas químicos y biológicos en los que aparecen
ácidos débiles o bases débiles, cuya concentración es necesario
determinar en muchas ocasiones. Para ello se recurre a realizar una
valoración ácido-base, utilizando un agente valorante, que es una
disolución de concentración bien conocida, que se hace reaccionar
con una muestra problema, hasta alcanzar el punto de equivalencia,
que puede determinarse mediante un indicador ácido-base o por una
técnica instrumental.
Valoraciones ácido-base. Los estudios cuantitativos de las
reacciones de estequiometría conocida se llevan a cabo de modo
conveniente por medio de un procedimiento llamado valoración.
En el experimento de valoración, una disolución de concentración
conocida exactamente (reactivo valorante) se agrega de forma
gradual a otra disolución de concentración desconocida (reactivo
a valorar) hasta que la reacción química entre las dos disoluciones sea
completa. Si se conocen los volúmenes de las dos disoluciones y la
concentración de una de ellas, se puede calcular la concentración
de la otra disolución. También puede valorarse una disolución de
composición de concentración desconocida midiendo el volumen
necesario para reaccionar por completo con una cantidad conocida de
reactivo valorante (que puede estar en estado sólido) en el matraz y
midiendo el volumen de disolución de composición desconocida
necesario para producir la reacción completa entre ambos.
Los métodos volumétricos se basan en el hecho de que la
concentración del reactivo valorante es conocida dentro del grado
de precisión requerido. En este sentido, hay reactivos con los
cuales es posible preparar disoluciones de concentración conocida
y estable con el tiempo. Estos reactivos se llaman patrones
primarios. Típicamente, un patrón primario es una especie de elevada
pureza, químicamente estable, no higroscópica, de peso equivalente
alto, y que tras ser disuelto, da lugar a especies en disolución
químicamente estables, es decir, que no sufren cambios químicos por
el contacto con la luz, el aire, etc., con lo cual, tras su disolución
y enrase a un volumen conocido es posible determinar su
concentración con precisión. Por el contrario, un reactivo sólido
como el hidróxido sódico no es un patrón primario porque, además
de su difícil manipulación, es higroscópico y tiende a carbonatarse
en contacto con el CO2 del aire; todo ello origina un error en la
pesada que impide la obtención de datos fiables de concentración,
por ello es necesario factorar esta disolución previamente con un
patrón primario como el ftalato ácido de potasio.
LUIS MUÑUICO CARDENAS 1
UNIVERSIDAD NACIONAL DEL ALTIPLANO
FACULTAD DE INGENERIA QUIMICA
Acido acético.
El ácido acético (también llamado ácido metilcarboxílico o ácido etanoico)
puede encontrarse en forma de ion acetato. Se encuentra en el vinagre, y es el
principal responsable de su sabor y olor agrios. Su fórmula es CH3-COOH
(C2H4O2). De acuerdo con la IUPAC, se denomina sistemáticamente ácido
etanoico.
Es el segundo ácido carboxílico más simple después del ácido fórmico o
metanoico, que solo tiene un carbono, y antes del ácido propanoico, que ya tiene
una cadena de tres carbonos.
El punto de fusión es 16,6 °C y el punto de ebullición es 117,9 °C.
En disolución acuosa, puede perder el protón del grupo carboxilo para dar
su base conjugada, el acetato. Su pKa es de 4,8 a 25 °C, lo cual significa, que al
pH moderadamente ácido de 4,8, la mitad de sus moléculas se habrán
desprendido del protón. Esto hace que sea un ácido débil y que, en
concentraciones adecuadas, pueda formar disoluciones tampón con su base
conjugada. La constante de disociación a 20 °C es Ka = 1,75·10−5.
Es de interés para la química orgánica como reactivo, para la química
inorgánica como ligando, y para la bioquímica como metabolito (activado
como acetil-coenzima A). También se utiliza como sustrato, en su forma
activada, en reacciones catalizadas por las enzimas conocidas
como acetiltransferasas y, en concreto, histona acetiltransferasas.
Hoy día, la vía natural de su obtención es a través de la carbonilación (reacción
con CO) de metanol. Antaño se producía por oxidación
de etileno en acetaldehído, el cual se oxidaba posteriormente para obtener,
finalmente, el ácido acético
III. MATERIALES Y REACTIVOS
bureta agitador magnético
Magneto Pipeta
LUIS MUÑUICO CARDENAS 2
UNIVERSIDAD NACIONAL DEL ALTIPLANO
FACULTAD DE INGENERIA QUIMICA
Pizetas Potenciómetro
Matraz erlenemeyer Vaso de precipitado
Matraz aforado vinagre
Agua destilada Hidróxido de sodio
IV. PARTE EXPERIMENTAL
Cargar la bureta con solución de NaOH previamente preparada.
Medir con la pipeta 3mL de vinagre y diulir en 100mL de agua
destilada
Colocar en el vaso de precipitado de 250mL una alícuota de 20mL
de solución de vinagre y luego completar con agua destilada a
100mL
LUIS MUÑUICO CARDENAS 3
UNIVERSIDAD NACIONAL DEL ALTIPLANO
FACULTAD DE INGENERIA QUIMICA
Colocar el vaso precipitado bajo la bureta, introducir el pH-metro
dentro de la solución de vinagre, anotar valores de pH
Añadir con agitación constante la solución básica de NaOH con
incrementos de 0,5mL, reportar el valor del pH a medida que se
añada el álcali.
Agregar solución de NaOH hasta llegar a pH “12”.
Calcular la pureza de vinagre
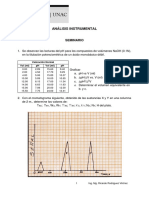
V. RESULTADOS
Tabulacion de datos y/o interpolación
mL de NaOH pH
0 4.32
0.5 4.42
1 4.54
1.5 4.66
2 4.80
2.5 4.94
3 5.12
3.5 5.30
4 5.49
4.5 5.69
5 5.92
5.5 6.19
6 6.48
6.5 6.97
7 8.22
7.5 8.98
8 9.31
8.5 9.58
9 9.79
9.5 10.03
10 10.25
Colores azules valores a tomar.
Aplicando segunda derivada y primera derivada a los datos tenemos la
siguiente tabla:
mL NaOH pH ΔpH/ ΔV ΔpH2/ ΔV2
5.5 6.19 0.29 0.2
6 6.48 0.49 0.76
6.5 6.97 1.25 -0.49
7 8.22 0.76 -0.43
7.5 8.98 0.33
8 9.31
Datos a interpolar de color rojo tenemos lo siguiente:
LUIS MUÑUICO CARDENAS 4
UNIVERSIDAD NACIONAL DEL ALTIPLANO
FACULTAD DE INGENERIA QUIMICA
𝑥 − 6.5 0 − 0.76
=
7 − 6.5 −0.49 − 0.76
𝑥 = 6.80
pH
12
10
8
Axis Title
0
0 2 4 6 8 10 12
Axis Title
Hallando porcentaje de ácido acetico:
6.80𝑚𝐿 . 0.0969𝑁 . 0.060𝑚𝑒𝑞
%𝐴𝑐. 𝑎𝑐𝑒𝑡𝑖𝑐𝑜 = 𝑥 100
1.5𝑔
%𝐴𝑐. 𝑎𝑐𝑒𝑡𝑖𝑐𝑜 = 2.63%
VI. CONCLUSIONES
Se puede concluir que la practica fue un éxito al demostrar la curva de la
primera derivada y de los datos obtenidos
Se concluye que la variación del pH con respecto al volumen es muy
variado ya que 1mL puede generar gran diferencia al momento de superar
su punto de equilibrio al momento de elevar su pH.
LUIS MUÑUICO CARDENAS 5
Вам также может понравиться
- Seminario de Problemas para Examen Final PDFДокумент4 страницыSeminario de Problemas para Examen Final PDFCarlos Baca SanchezОценок пока нет
- Error Fotométrico.Документ5 страницError Fotométrico.BernardoFelipeVelez0% (1)
- Fuentes de Error en Las Prácticas 1 y 2 de La Química II ExperimentalДокумент3 страницыFuentes de Error en Las Prácticas 1 y 2 de La Química II ExperimentalFelipe GomezОценок пока нет
- Practica Lab 4,5,6,7Документ16 страницPractica Lab 4,5,6,7DANNERI LEZAMA GALLEGOSОценок пока нет
- Informe 1 Refractometría de Etanol en Ron - Santiago Acosta, Yuliana BarretoДокумент8 страницInforme 1 Refractometría de Etanol en Ron - Santiago Acosta, Yuliana BarretoOscar BarretoОценок пока нет
- Acidimetria y AlcalimetriaДокумент32 страницыAcidimetria y AlcalimetriathonyОценок пока нет
- INFORME - VALORACIÓN ÁCIDO BASE - SIMULADOR - Rev 3Документ2 страницыINFORME - VALORACIÓN ÁCIDO BASE - SIMULADOR - Rev 3Nehuen MartinoОценок пока нет
- Informe Práctica #1 Qa IДокумент10 страницInforme Práctica #1 Qa IAldair Orozco UlloaОценок пока нет
- Reporte Voltametria y PolarografiaДокумент46 страницReporte Voltametria y Polarografiadiogenes2011Оценок пока нет
- Ejercicios Resueltos Espectrofotometría 2017Документ5 страницEjercicios Resueltos Espectrofotometría 2017Diana Dominguez AquinoОценок пока нет
- POTENCIOMETRIAДокумент1 страницаPOTENCIOMETRIALauraRosasОценок пока нет
- Tema 10 y 11Документ65 страницTema 10 y 1148456971100% (1)
- Metodos de Mohr y VolhardДокумент4 страницыMetodos de Mohr y VolhardJavier FuenmayorОценок пока нет
- PRACTICA #6-QUIMICA ANALITICA-VOLUMETRÍA de PRECIPITACION - Determinación de La Concentraciòn de Cloruros en El Agua PotableДокумент8 страницPRACTICA #6-QUIMICA ANALITICA-VOLUMETRÍA de PRECIPITACION - Determinación de La Concentraciòn de Cloruros en El Agua PotableCynthia GonzalesОценок пока нет
- UNSCH-PRACT04 (Autoguardado)Документ18 страницUNSCH-PRACT04 (Autoguardado)Gray D L LeoОценок пока нет
- Conductimetria Conceptos TeoricosДокумент4 страницыConductimetria Conceptos TeoricosPilar BalverdiОценок пока нет
- Proyecto 2019 Algas Ulva LactucaДокумент57 страницProyecto 2019 Algas Ulva LactucaDaryenis Güipe0% (1)
- Marcha Analítica Cationes - Grupo 4Документ34 страницыMarcha Analítica Cationes - Grupo 4kelvin hairo gonzales muñoz100% (1)
- Determinación de Hierro (Iii), Oxido de Aluminio, Densidad Aparente, Materia Insoluble, y Humedad en Muestra de BauxitaДокумент6 страницDeterminación de Hierro (Iii), Oxido de Aluminio, Densidad Aparente, Materia Insoluble, y Humedad en Muestra de BauxitaDiana HernándezОценок пока нет
- Práctica 3 - ConductimetríaДокумент3 страницыPráctica 3 - ConductimetríaEsteban CortesОценок пока нет
- PerganmanometríaДокумент5 страницPerganmanometríaLuis GutiierezОценок пока нет
- Cinética de Oxidación de Etano Con CromoДокумент11 страницCinética de Oxidación de Etano Con CromoLauraRodriguezОценок пока нет
- FOTÓLISISДокумент29 страницFOTÓLISISMaxRománCiprianoValeroОценок пока нет
- Ibeth Mamani Parillo PolarografiaДокумент12 страницIbeth Mamani Parillo PolarografiaDavid JosueОценок пока нет
- Prac. 05 Determinación de Calcio en Cenizas de Productos Fitógenos, Zoógenos, Suelos y AguaДокумент12 страницPrac. 05 Determinación de Calcio en Cenizas de Productos Fitógenos, Zoógenos, Suelos y AguaELMER ELI CHUQUIMANGO CUEVA100% (1)
- 2015 BДокумент3 страницы2015 BFrank Estrella RuizОценок пока нет
- Potencimetria Directa FluorДокумент6 страницPotencimetria Directa Fluormaman100% (1)
- Práctica 3. Biología MolecularДокумент11 страницPráctica 3. Biología MolecularCelia Paola Gutiérrez ArandaОценок пока нет
- Informe LevaduraДокумент4 страницыInforme LevaduraSteven Agredo SánchezОценок пока нет
- Informe Analítica - Permanganometría - M.AlfaroДокумент14 страницInforme Analítica - Permanganometría - M.AlfaroJaviera Alfaro VicencioОценок пока нет
- Practica de LipidosДокумент5 страницPractica de LipidosEsther SoledadОценок пока нет
- Adsorcion Del Acido Acetico Sobre Carbon ActivadoДокумент10 страницAdsorcion Del Acido Acetico Sobre Carbon ActivadoLicet CadilloОценок пока нет
- Potenciometría y ConductimetríaДокумент30 страницPotenciometría y ConductimetríaAxel TuyubОценок пока нет
- Preparacion de Cloruros Por El Metodo de MORHДокумент15 страницPreparacion de Cloruros Por El Metodo de MORHJEAN CAMILO PORRAS RICO100% (1)
- Volumetría de Oxido - Reducción IДокумент10 страницVolumetría de Oxido - Reducción IingrossОценок пока нет
- Determinación de Peróxidos en Agua OxigenadaДокумент15 страницDeterminación de Peróxidos en Agua OxigenadaMarlen AlarcónОценок пока нет
- INFORME 8 PotenciometricaДокумент10 страницINFORME 8 PotenciometricaHelen DayelyОценок пока нет
- Determinación Cualitativa de Aminoácidos Por ElectroforesisДокумент3 страницыDeterminación Cualitativa de Aminoácidos Por ElectroforesisKarenОценок пока нет
- Practica No. 3 Titulacion PotenciometricДокумент3 страницыPractica No. 3 Titulacion Potenciometricsussel badayОценок пока нет
- Acidez de Compuestos OrgánicosДокумент3 страницыAcidez de Compuestos OrgánicosKatherineОценок пока нет
- ANÁLISIS COULOMBIMÉTRICOlaboДокумент26 страницANÁLISIS COULOMBIMÉTRICOlaboJose Arin DiazLopez100% (1)
- Práctica Análisis Cualitativo Observación CristalesДокумент5 страницPráctica Análisis Cualitativo Observación CristalesRakel MontenegroОценок пока нет
- El Poder Amortiguador de Los AminoácidosДокумент7 страницEl Poder Amortiguador de Los Aminoácidosnicolas guzman0% (1)
- Cuantificacion Potenciometrica de Hierro (III) PDFДокумент9 страницCuantificacion Potenciometrica de Hierro (III) PDFJose Emmanuel ChemaОценок пока нет
- Informe-Gravimetría v.Документ5 страницInforme-Gravimetría v.Adriana LeónОценок пока нет
- Practica #03 HIDROCARBUROS PDFДокумент2 страницыPractica #03 HIDROCARBUROS PDFtanyОценок пока нет
- BIOLOGÍA GENERAL Lab. - Acidos Nucleicos UnalmДокумент8 страницBIOLOGÍA GENERAL Lab. - Acidos Nucleicos UnalmXIWXIОценок пока нет
- Práctica - Determinación de Cloruros en El Agua Mediante GravimetríaДокумент8 страницPráctica - Determinación de Cloruros en El Agua Mediante GravimetríaJuan José González MenéndezОценок пока нет
- Determinación de Constante de EstabilidadДокумент5 страницDeterminación de Constante de EstabilidadGICELAОценок пока нет
- Metodo JobДокумент5 страницMetodo Jobeduardohk18Оценок пока нет
- Cromatografia Liquido Solido PDFДокумент14 страницCromatografia Liquido Solido PDFluna713Оценок пока нет
- Valoración Ácido-Base ConductimétricaДокумент3 страницыValoración Ácido-Base ConductimétricaFede SalasОценок пока нет
- Experimento 4 Determinación Gravimétrica de NíquelДокумент5 страницExperimento 4 Determinación Gravimétrica de NíquelBrandon CaballeroОценок пока нет
- Previo - Polimerización de AldehídosДокумент8 страницPrevio - Polimerización de AldehídosKarla García100% (1)
- Informe de Analisis Quimico 7Документ24 страницыInforme de Analisis Quimico 7Lucero Gomez CabreraОценок пока нет
- Informe Cuanti II Informe 6 Argentometria Parte IIДокумент5 страницInforme Cuanti II Informe 6 Argentometria Parte IIMishelle ParraОценок пока нет
- Conductividad de Soluciones ElectroliticasДокумент12 страницConductividad de Soluciones ElectroliticasKaren Andrade MoralesОценок пока нет
- Determinacion de La Pureza de Acido Cítrico Por Titulación PotenciometricaДокумент4 страницыDeterminacion de La Pureza de Acido Cítrico Por Titulación PotenciometricaLuis Fernando Muñuico CardenasОценок пока нет
- Info-9-Fisico MARCO TEORICOДокумент7 страницInfo-9-Fisico MARCO TEORICOBryan LópezОценок пока нет
- Calidad del agua para estudiantes de ciencias ambientalesОт EverandCalidad del agua para estudiantes de ciencias ambientalesОценок пока нет
- Formato Informe 1. Calibración de Material Volumétrico y Preparacion de SolucionesДокумент8 страницFormato Informe 1. Calibración de Material Volumétrico y Preparacion de SolucionesJUAN DIEGO ZABALA NAVARROОценок пока нет
- Método de MohrДокумент13 страницMétodo de MohrAngelica CastroОценок пока нет
- Conceptos TeoricosДокумент69 страницConceptos TeoricoshelenОценок пока нет
- Guia de Laboratorio FQ2Документ16 страницGuia de Laboratorio FQ2nadia123Оценок пока нет
- Carbón Activado para La Purificación de GasesДокумент13 страницCarbón Activado para La Purificación de GasesCarlos BarriosОценок пока нет
- SOLUCIONES Guía de Ejercicios Titulación y Neutralización AF-BFДокумент6 страницSOLUCIONES Guía de Ejercicios Titulación y Neutralización AF-BFDallit's Sagredo Oyarce88% (16)
- Analisis 7 8 InformeДокумент21 страницаAnalisis 7 8 InformeDante MontañezОценок пока нет
- NMX B 449 FerroaleacionesДокумент67 страницNMX B 449 Ferroaleacioneswero1526Оценок пока нет
- Analisis de Yodo en SalДокумент4 страницыAnalisis de Yodo en SallbtorioОценок пока нет
- Info 2Документ6 страницInfo 2Ali ArellanoОценок пока нет
- Práctica 02. Determinación de Concentraciones y Las Diversas Maneras de ExpresarlaДокумент9 страницPráctica 02. Determinación de Concentraciones y Las Diversas Maneras de ExpresarlaEmmanuel BonillaОценок пока нет
- Práctica Número 1 Métodos Ácido - BaseДокумент18 страницPráctica Número 1 Métodos Ácido - BaseOscar Abraham Ibarra RochaОценок пока нет
- Curvas de Titulación-TallerДокумент6 страницCurvas de Titulación-TallerAndres GuerreroОценок пока нет
- Práctica 3Документ6 страницPráctica 3jhordanogomezОценок пока нет
- LABoratorio Analisis Quimico UNIДокумент26 страницLABoratorio Analisis Quimico UNIKenny SalazarОценок пока нет
- Determinacion de La ProteinaДокумент11 страницDeterminacion de La ProteinaAnonymous OPokBZAFОценок пока нет
- Nom 132-1998Документ17 страницNom 132-1998americabig99Оценок пока нет
- TP0351 Calcio y Magnesio en Agua Con EDTA Por VolumetríaДокумент10 страницTP0351 Calcio y Magnesio en Agua Con EDTA Por VolumetríasaphkielОценок пока нет
- BQAN - Act. 4 - U2 - SAGFДокумент7 страницBQAN - Act. 4 - U2 - SAGFSandy Mayra GuadarramaОценок пока нет
- M-S-Lc-I016 Instructivo de Ensayo Demanda Química de OxígenoДокумент12 страницM-S-Lc-I016 Instructivo de Ensayo Demanda Química de OxígenoYenny OstosОценок пока нет
- Practicas de EdafologiaДокумент11 страницPracticas de EdafologiaFanyMariluTiradoCernaОценок пока нет
- Estandarizacion de HCL y Alcalinidad Total en MezclasДокумент7 страницEstandarizacion de HCL y Alcalinidad Total en MezclasPreuzОценок пока нет
- Cómo Elaborar Un Póster de Investigación Una Guía para EstudiantesДокумент1 страницаCómo Elaborar Un Póster de Investigación Una Guía para EstudiantesTania GachusОценок пока нет
- Analiza Muestras de Alimentos y Bebidas Con Métodos FisicoquímicosДокумент8 страницAnaliza Muestras de Alimentos y Bebidas Con Métodos FisicoquímicosMARTINEZ MARTINEZ HAROLD EMIRОценок пока нет
- Nom 021 Recnat 2000 As 07 Co y MoДокумент4 страницыNom 021 Recnat 2000 As 07 Co y MoMelanie LopezОценок пока нет
- P4. Puntos CríticosДокумент13 страницP4. Puntos CríticosRomina AguileraОценок пока нет
- ACALINIDADДокумент8 страницACALINIDADRubenEliasMorenoVegaОценок пока нет
- CLORUROSДокумент5 страницCLORUROSrriondarОценок пока нет
- Practica 14Документ9 страницPractica 14JORGE LEONARDO FRASSER QUIÑONESОценок пока нет
- NTC5557 Ácido en MorteroДокумент12 страницNTC5557 Ácido en MorterodaucОценок пока нет