Академический Документы
Профессиональный Документы
Культура Документы
Analise Cloreto
Загружено:
Rafamizuta0 оценок0% нашли этот документ полезным (0 голосов)
738 просмотров16 страницEste documento descreve métodos para análise de cloreto em tecidos vegetais, incluindo os métodos de Mohr, mercurimétrico e potenciométrico. Ele discute a preparação da amostra, extração do cloreto, reagentes e procedimentos para cada método. O método de Mohr envolve a titulação do cloreto com nitrato de prata, enquanto o método mercurimétrico usa nitrato de mercúrio e um indicador.
Исходное описание:
Оригинальное название
analise cloreto
Авторское право
© Attribution Non-Commercial (BY-NC)
Доступные форматы
PDF, TXT или читайте онлайн в Scribd
Поделиться этим документом
Поделиться или встроить документ
Этот документ был вам полезен?
Это неприемлемый материал?
Пожаловаться на этот документEste documento descreve métodos para análise de cloreto em tecidos vegetais, incluindo os métodos de Mohr, mercurimétrico e potenciométrico. Ele discute a preparação da amostra, extração do cloreto, reagentes e procedimentos para cada método. O método de Mohr envolve a titulação do cloreto com nitrato de prata, enquanto o método mercurimétrico usa nitrato de mercúrio e um indicador.
Авторское право:
Attribution Non-Commercial (BY-NC)
Доступные форматы
Скачайте в формате PDF, TXT или читайте онлайн в Scribd
0 оценок0% нашли этот документ полезным (0 голосов)
738 просмотров16 страницAnalise Cloreto
Загружено:
RafamizutaEste documento descreve métodos para análise de cloreto em tecidos vegetais, incluindo os métodos de Mohr, mercurimétrico e potenciométrico. Ele discute a preparação da amostra, extração do cloreto, reagentes e procedimentos para cada método. O método de Mohr envolve a titulação do cloreto com nitrato de prata, enquanto o método mercurimétrico usa nitrato de mercúrio e um indicador.
Авторское право:
Attribution Non-Commercial (BY-NC)
Доступные форматы
Скачайте в формате PDF, TXT или читайте онлайн в Scribd
Вы находитесь на странице: 1из 16
ANÁLISE DE CLORETO EM TECIDO VEGETAL
ENILSON DE BARROS SILVA1
FRANCISCO DIAS NOGUEIRA2
PAULO TÁCITO GONTIJO GUIMARÃES3
INTRODUÇÃO
O átomo de cloro (Cl) é um micronutriente não metálico, pertencente
ao grupo 7A, halogênio, juntamente com o iodo, bromo e flúor. O cloro pos-
sui sete elétrons na camada de valência; portanto, tende a ganhar um elétron,
adquirindo a configuração de um gás nobre e formando o íon cloreto, que é a
forma mais comumente encontrada na natureza. Na forma elementar, o gás
Cl é verde-claro, de fórmula molecular Cl2, ocorrendo, naturalmente, como
ânion cloreto (Raij, 1991).
As pesquisas evidenciam que o Cl é um micronutriente essencial na
vida vegetal (Broyer et al., 1954 e Johnson et al., 1957), sendo absorvido por
algumas espécies de plantas em quantidades muito elevadas. O interesse dos
fisiólogos em relação ao Cl- se dirige menos para os problemas relativos à
sua eventual deficiência do que para as modificações metabólicas provocadas
por sua presença, em concentrações demasiadamente elevadas, no meio nu-
tritivo (Marschner, 1986, Tisdale, Nelson e Beaton, 1986 e Mengel e Kirkby,
1987). Mas, o Cl- tem uma função importante como cofator, junto com
manganês, na evolução do oxigênio, no fotossistema II na fotossíntese
(Broyer et al., 1954; Gouny, 1973; Marschner, 1986; Mengel e Kirkby, 1987
e Malavolta, Vitti e Oliveira, 1989).
1. Engenheiro Agrônomo, M.Sc., Pesquisador da EPAMIG/Doutorando Departa-
mento de Ciência do Solo/UNIVERSIDADE FEDERAL DE LAVRAS/UFLA,
Caixa Postal 37 – 37.200-000 - Lavras, MG
2. Engenheiro Agrônomo, D.Sc., Pesquisador EMBRAPA/EPAMIG/CRSM, La-
vras, MG.
3. Engenheiro Agrônomo, D.Sc., Pesquisador da EPAMIG/CRSM, Lavras, MG.
6
O Cl é um micronutriente ímovel , com baixa redistribuição das folhas
para outros órgãos da planta. Geralmente, ele se acumula nas folhas da
planta com o tempo e há poucas evidências do movimento desse nutriente
dos tecidos velhos para os novos (Eaton, 1966). A toxidez de Cl- manisfesta-
se pela queima da extremidade e margens das folhas, com bronzeamento
prematuro e abscisão das folhas (Eaton, 1966; Gouny, 1973; Snoeck,
N’Goran e Snoeck, 1986; Malavolta, Vitti e Oliveira, 1989; N’Goran, 1990).
O ânion cloreto (Cl-) pode ser determinado por métodos gravimétri-
cos, volumétricos, potenciométricos e colorimétricos. Os métodos volumé-
tricos, como os métodos de Mohr e de Volhard, são extensivamente utiliza-
dos em análise de cloreto em plantas e foram desenvolvidos no século XVII
(Gaines, Parker e Gascho, 1984). O método de Mohr é a determinação direta
do íon cloreto e o de Volhard é a determinação indireta (Ohlweiler, 1968ab e
Jeffery et al., 1992). O método de Volhard envolve a titulação do íon prata
em meio ácido com solução padrão de tiocianato de potássio, após a preci-
pitação do íon cloreto, em presença do indicador, que é uma solução satura-
da de sulfato de amônio e ferro III.
A mercurimetria, um outro método volumétrico, pode ser utilizada na
determinação de cloreto inorgãnico. O método baseia-se na titulação do clo-
reto com solução padrão de nitrato de mercúrio(II). O ponto final da titula-
ção é determinado com o auxílio de indicadores, como por exemplo, nitro-
prussiato de sódio ou difenilcarbazona, os quais produzem respectivamente
uma turvação causada pela formação de um precipitado branco de nitroprus-
siato de mercúrio e um complexo azul-violeta, que é afetado pela concentra-
ção do indicador. No caso da difenilcarbazona, os melhores resultados são
obtidos com 5 a 10 gotas desse indicador (Ohlweiler, 1974).
A análise potenciométrica é a mais difundida, sendo esse, o método
oficial da Association of Official Analytical Chemists (AOAC), para determi-
nação de cloreto em tecido vegetal (AOAC, 1970). Esse método tem elevada
precisão, mas necessita de muito tempo por tratar-se de titulação manual (Gilli-
am, 1971; Adriano, Pratt e Holtzclaw, 1973 e Gaines, Parker e Gascho, 1984).
A titulação potenciométrica envolve a medida da diferença de poten-
cial entre dois eletrodos, sendo um, o indicador. O potencial é avaliado em
7
função da concentração do íon a ser determinado, utilizando-se um eletrodo
de referência de potencial constante. O ponto de equivalência será revelado
por uma abrupta alteração da diferença de potencial (Ohlweiller, 1968b e
Jeffery et al., 1992).
Existe um certo interesse pelo conhecimento dos efeitos do cloreto
nas plantas, e o desenvolvimento da análise instrumental tem contribuído
para a utilização de métodos mais precisos e práticos para a quantificação
desse micronutriente em análise de rotina.
PREPARO DA AMOSTRA
As amostras do material vegetal são identificadas, lavadas, secas,
moídas e acondicionadas em frascos de vidro. A lavagem do material vegetal
é realizada para remover partículas de solo, poeira e resíduos industriais,
de defensivos e de fertilizantes. As amostras são lavadas com água de
torneira e em seguida lavadas com água destilada. Logo após a lavagem,
são colocadas em sacos de papel e transferidas para estufa a 65-700C,
com forçada circulação de ar, durante um período de 48 horas ou até peso
constante. Depois de secas, as amostras são moídas em moinho mecânico
com peneira de 1 mm de diâmetro e armazenadas em frascos de vidro de 50
ml com tampa plástica.
DESCRIÇÃO DOS MÉTODOS
1. MÉTODO DE MOHR
A determinação de cloreto foi adaptada, tomando como base os tra-
balhos de Lacroix, Keeney e Walsh (1970) e Malavolta, Vitti e Oliveira
(1989).
8
1.1. PRINCÍPIO DO MÉTODO
O cloro extraído pela solução de nitrato de cálcio (Ca(NO3)2.4H2O),
na forma de íon cloreto, é titulado com solução padronizada de nitrato de
prata (AgNO3), na presença de cromato de potássio (K2CrO4) como indica-
dor. O ponto final da titulação é identificado pela coloração vermelha, resul-
tante da formação de cromato de prata depois de toda a precipitação do clo-
reto (AgCl), pois, o cromato de prata é mais solúvel que o cloreto de prata.
1.2. EXTRAÇÃO DE CLORETO
Para a extração do cloreto, proceder do seguinte modo:
a) pesar 1 g de matéria seca (MS) em erlenmeyer de 125 ml;
b) adicionar 100 ml de solução de Ca(NO3)2.4H2O a 0,085 mol.l-1;
c) agitar em agitador horizontal por 15 minutos;
d) filtrar o extrato em papel de filtro e recolher o filtrado em frasco
com tampa.
1.3. APARELHOS E REAGENTES
O preparo da solução e a vidraria utilizada é descrita a seguir:
a) solução extratora de Ca(NO3)2.4H2O a 0,085 mol.l-1: dissolver 20
g de Ca(NO3)2.4H2O e completar o volume para 1000 ml com água destilada
deionizada em balão volumétrico de 1000 ml;
b) padrão de nitrato de prata 0,0282 mol.l-1: dissolver 4,791 g de
AgNO3, e completar o volume para 1000 ml com água destilada e deionizada
em balão volumétrico de 1000 ml. Portanto, 1 ml dessa solução, equivale a 1
mg de cloreto. Em seguida, padronizar essa solução e colocar em um er-
lenmeyer: 50 ml de água destilada deionizada, 25 ml de NaCl 0,030 mol.l-1 e
9
1 ml da solução indicadora de K2CrO4 a 0,258 mol.l-1 e titular com nitrato de
prata até o aparecimento da cor vermelha clara.
c) solução indicadora de cromato de potássio (K2CrO4) a 0,258 mol.l-1:
dissolver 5 g de K2CrO4 em aproximadamente 50 ml de água destilada e dei-
onizada.
1.4. MARCHA ANALÍTICA
Na marcha analítica, propriamente dita, proceder como o descrito a
seguir:
a) tomar uma alíquota de 10 ml do extrato (1 g de MS/100 ml de
solução de Ca(NO3)2.4H2O) e transferir para um erlenmeyer de 125 ml;
b) adicionar 1 ml (micropipeta de 1 ml) á solução de K2CrO4, indica-
dor, no momento da titulação, para não ocorrer oxidação do extrato pelo
cromato;
c) titular com a solução padrão de nitrato de prata até formação de
coloração vermelha, anotando-se o volume gasto (V1);
d) fazer prova em branco, titulando-se 10 ml da solução de
Ca(NO3)2.4H2O e anotar o volume de AgNO3 gasto (V0);
e) utilizar 3 repetições das amostras preparadas.
1.5. CÁLCULOS
Após a titulação, calcular a porcentagem de cloreto no material ve-
getal pela fórmula abaixo:
% Cl- = (V1 - V0) * fc
V1 = Volume gasto de AgNO3 na titulação da amostra, em ml;
V0 = Volume gasto na titulação da prova em branco, em ml;
fc = fator de correção da solução de AgNO3.
10
2. MÉTODO MERCURIMÉTRICO
A determinação de cloreto descrita foi uma adaptação das metodolo-
gias propostas por Lacroix, Keeney e Walsh (1970), Ohlweiler (1981) e
Malavolta, Vitti e Oliveira (1989).
2.1. PRINCÍPIO DO MÉTODO
O princípio de determinação é baseada na reação do íon mercúrico
para formar cloreto mercúrico solúvel, e quando íon mercúrico for adiciona-
do em excesso, o indicador difenilcarbazona torna-se azul-violeta, mostrando
o ponto final da titulação.
2.2. EXTRAÇÃO DO CLORETO
A extração do cloreto foi semelhante àquela descrito para o método
de Mohr.
2.3. APARELHOS E REAGENTES
O preparo da solução é descrita a seguir:
a) indicador difenilcarbazona: dissolver 100 mg de difenilcarbazona
em 100 ml de álcool a 95% e guardar em frasco escuro na geladeira;
b) solução de nitrato de mercúrio II (0,0071 mol.L-1): dissolver 2,66
g de Hg(NO3)2.H2O em 20 ml de água destilada deionizada, tratados com
0,25 ml de ácido nítrico concentrado e diluir para volume de 1000 ml; de-
terminar a concentração exata dessa solução em relação a 10 ml da solução
padrão de NaCl 0,0141 mol.l-1 diluída a 100 ml, com água destilada e deioni-
zada. Portanto, 1 ml de Hg(NO3)2.H2O, eqüivale a 1 mg de cloreto.
11
2.4. MARCHA ANALÍTICA
O procedimento químico deve seguir os passos abaixo:
a) tomar uma alíquota de 10 ml do extrato (1 g de MS/100 ml de
solução de Ca(NO3)2.4H2O) e a passar para erlenmeyer de 125 ml;
b) adicionar 10 gotas de difenilcarbazona com uma pipeta de 2 ml;
c) titular com nitrato de mercúrio (II) até formar uma coloração azul
violeta, ou seja, a cor desenvolvida devido ao excesso de Hg(NO3)2.H2O,
que reage com a difenilcarbazona, e anotar o volume gasto (V1);
d) fazer a prova em branco titulando-se 10ml da solução de
Ca(NO3)2.4H2O a 0,085 mol.l-1 e anotar, em seguida, o volume de
Hg(NO3)2.H2O gasto (V0);
e) utilizar 3 repetições das amostras preparadas.
2.5. CÁLCULOS
Após a titulação, calcular a porcentagem de cloreto no material ve-
getal pela fórmula abaixo:
% Cl- = (V1 - V0) * fc
V1 = Volume gasto de Hg(NO3)2.H2O na titulação da amostra, em
ml;
V0 = Volume gasto na titulação da prova em branco, ml;
fc = fator de correção da solução de Hg(NO3)2.H2O.
3. MÉTODO DE VOLHARD
A determinação de cloreto baseou-se no método de Volhard (Kol-
thoff e Sandell, 1952) em suas linhas gerais, com as adaptações necessárias á
sua aplicação, em material vegetal, feitas por Catani, Moraes e Bergamin
(1969).
12
3.1. PRINCÍPIO DO MÉTODO
O método envolve a titulação do íon prata residual em meio ácido com
solução padrão de tiocianato de potássio, após a precipitação do íon cloreto, em
presença do indicador solução saturada de sulfato de amônio e ferro III.
3.2. EXTRAÇÃO DO CLORETO
Para a extração do cloreto, proceder da seguinte forma:
a) incinerar 1 g do material seco (MS) a 500-550o C em cápsula de
porcelana de 50 ml;
b) adicionar 20 ml de solução de HNO3 0,2 mol.L-1 e homogeneizar;
c) filtrar em frasco de vidro de 100 ml, lavar o resíduo com 2 porções
de 10 ml de solução de HNO3 0,2 mol.L-1.
3.3. MARCHA ANALÍTICA
O procedimento químico deve seguir os passos abaixo:
a) adicionar 10 ml (V1) de solução padronizada de AgNO3 0,05 mol.l-
1
sobre o extrato filtrado, homogenizar e deixar em repouso por 15’ para
flocular o AgCl;
b) filtrar para erlenmeyer de 125 ml com papel de filtro, lavando o
precipitado com duas porções de 10 ml de solução de HNO3 0,2 mol.l-1;
c) adicionar 0,5 ml de solução de alúmen férrico a 0,830 mol.l-1 e
titular com solução padronizada de KSCN 0,05 mol.l-1 até o aparecimento de
cor rósea e anotar o volume de KSCN gasto (V2).
3.4. APARELHOS E REAGENTES
Para o preparo da solução, os procedimentos abaixo:
13
a) solução de AgNO3 0,05 mol.l-1: dissolver 8,5g de AgNO3 e com-
pletar o volume para 1000 ml com água destilada e deionizada em balão vo-
lumétrico. Padronizar a solução de AgNO3, colocar 50 ml de água destilada
e deionizada, 25 ml de NaCl 0,05 mol.l-1, e 1 ml de solução indicadora de
K2CrO4 a 0,258 mol.l-1, e titular com AgNO3, até o aparecimento da cor
vermelha- clara;
b) solução de NaCl 0,05 mol.l-1: dissolver 2,9226 g de NaCl e com-
pletar o volume para 1000 ml com água destilada e deionizada em balão vo-
lumétrico;
c) solução de KSCN 0,05 mol.l-1: dissolver 5,0 g de KSCN e com-
pletar o volume para 1000 ml com água destilada e deionizada em balão volu-
métrico. Padronizar a solução de KSCN com a solução de AgNO3, já padroniza-
da, usando como indicador 1 ml de solução de alúmen férrico a 0,830 mol.l-1;
d) solução de alúmen férrico a 0,830 mol.l-1: dissolver 40 g de
Fe(NH4)2(SO4)2 e completar o volume para 100 ml com água destilada e
deionizada em balão volumétrico.
3.5. CÁLCULOS
Após a titulação, fazer os cálculos aritméticos de acordo a fórmula abai-
xo:
% Cl- = 0,177 *((V1 * fc1) - (V2 * fc2))
V1 = volume inicial de AgNO3, em ml;
V2 = Volume gasto de KSCN na titulação do AgNO3 residual, em ml;
fc1 = fator de correção da solução de AgNO3;
fc2 = fator de correção da solução de KSCN.
4. MÉTODO DE TITULAÇÃO POTENCIOMÉTRICA
A determinação de cloreto foi baseada em Lacroix, Keeney e Walsh
(1970) e Jeffery et al. (1992).
14
4.1. PRINCÍPIO DO MÉTODO
O procedimento envolve a medição da diferença de potencial entre
dois eletrodos: um indicador, cujo potencial é função da concentração do íon
a ser determinada, e um eletrodo de referência, de potencial constante. O
ponto de equivalência será revelado por uma abrupta modificação do poten-
cial, indicado pelas leituras em milivolt (mV), em peagâmetro, durante a adi-
ção do volume da solução padrão de AgNO3. O volume de AgNO3 consumi-
do na titulação até à modificação abrupta é determinado por um método
prático preconizado por Guenther (1972) e Jeffery et al. (1992), que será
descrito a seguir
4.2. EXTRAÇÃO DO CLORETO
Para a extração do cloreto, proceder do seguinte modo:
a) pesar 1 g de MS em erlenmeyer de 125 ml;
b) adicionar 100 ml de solução de HNO3 0,1 mol.l-1;
c) agitar a mistura em agitador horizontal por 15 minutos;
d) filtrar a mistura em papel de filtro e recolher em frasco com tampa.
4.3. APARELHOS E REAGENTES
Os aparelhos, reagentes e preparo de soluções utilizados são:
a) peagâmetro marca DIGIMED-DMPH-2 utilizado no módulo mili-
volt (mV);
b) eletrodo indicador: um fio de prata com acoplamento no peagâ-
metro;
c) eletrodo de referência: calomelamo saturado com KCl 1 mol.l-1;
d) solução extratora de ácido nítrico a 0,1 mol.L-1: diluir 7,5 ml de
HNO3 concentrado em 1000 ml de água destilada e deionizada;
e) ponte salina de vidro preparada com 3 g de ágar em 100 ml de
água destilada e deionizada mais 40 g de nitrato de potássio;
15
f) solução padrão de nitrato de prata a 0,0282 mol.l-1: preparo idênti-
co àquele descrito para método de Mohr.
O esquema de montagem da aparelhagem é apresentado na Figura 1:
A
C B
H H D F
G
FIGURA 1 - Desenho esquemático da titulação potenciométrica com os
seguintes equipamentos: (A) bureta, (B) ponte salina, (C) eletrodo indicador,
(D) eletrodo de referência, (E) agitador magnético, (F) potenciômetro, (G)
barra magnética e (H) becker.
4.4. MARCHA ANALÍTICA
Para a marcha analítica, proceder do seguinte modo:
a) tomar uma alíquota de 50 ml do extrato (1 g de MS/100 ml da
solução de HNO3 0,1 mol.l-1) e passar para um becker de 50 ml;
16
b) titular com nitrato de prata 0,0282 mol.l-1 utilizando-se de uma
bureta de 10 ml. A torneira deve ser ligada por um fio capilar para que a so-
lução seja titulada diretamente sobre o extrato a determinar. A adição da
solução deve ser lenta e em espaços regulares para que se observe, com cla-
reza, a modificação abrupta; em sguida, deve-se continuar adicionando-se a
solução até que a variação em mV seja praticamente constante.
c) fazer prova em branco, titulando-se 50 ml de solução de HNO3
0,1 mol.l-1 e procedendo-se conforme feito para o extrato.
4.5. CÁLCULOS
Para a determinação do volume gasto de nitrato de prata, utilizar o
método prático, adaptado para a determinação de cloreto em tecido vegetal,
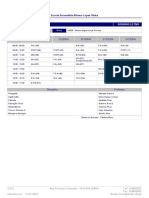
exemplificado na Tabela 1.
Como exemplo, observa-se na Tabela 1, na coluna da derivada se-
gunda, entre os valores de -1275 e 0, que ocorre a mudança abrupta, isto é,
o volume de AgNO3, que reagiu equivalentemente com o cloreto contido na
amostra, é expresso entre aqueles valores. Este volume é calculado pela se-
guinte fórmula:
Veq = V1 + (V2-V1)* D1/(D1+D2), onde:
Veq - Volume equivalente (ml);
V1 - Volume correspondente ao menor valor da derivada segunda (ml);
V2 - Volume correspondente ao maior valor da derivada segunda (ml);
D1 - Menor valor da derivada segunda (mV.ml-2), em valor absoluto;
D2 - Maior valor da derivada segunda (mV.ml-2), em valor absoluto;.
Ex: Veq = 0,04 + (0,08-0,04)* (31875)/(31875+0)
Veq = 0,08 ml.
O volume equivalente obtido de cada amostra é utilizado no cálculo
do cloreto contido na matéria seca pela seguinte fórmula:
% Cl- = 0,2*(Veq (amostra) - Veq (branco)) * fc
Veq (amostra) = volume equivalente de AgNO3 gasto da amostra, em ml;
Veq (branco) = volume equivalente de AgNO3 gasto do branco, em ml;
fc = fator de correção da solução de AgNO3;
17
TABELA 1 - Titulação potenciométrica de extrato foliar de cloreto por so-
lução de nitrato de prata (0,0282 mol.L-1) com eletrodos indicador de fio de
prata e outro calomelano de referência.
sE/sV Volume sDerivada sVolume Derivada
VAgNO3 E sV sE Derivada
médio primeira médio segunda
(ml) (mV) (ml) (mV) primeira
(ml) (mV.ml-1) (ml) (mV.ml-2)
(mV.ml-1)
0 125
0,04 79 1975 0,02
0,04 204 -1275 0,04 -31875
0,04 28 700 0,06
0,08 232 0 0,04 0
0,04 28 700 0,10
0,12 260 -200 0,04 -5000
0,04 20 500 0,14
0,16 280 -150 0,04 -3750
0,04 14 350 0,18
0,20 294 -125 0,04 -3125
0,04 9 225 0,22
0,24 303 -50 0,04 -1250
0,04 7 175 0,26
0,28 310 -75 0,04 -1875
0,04 4 100 0,30
0,32 314 -25 0,04 -625
0,04 3 75 0,34
0,36 317 -25 0,04 625
0,04 4 100 0,38
0,40 321
18
REFERÊNCIAS BIBLIOGRÁFICAS
ADRIANO, D.C.; PRATT, P.F.; HOLTZCLAW, K.M. Comparison of two
simple methods of chlorine analysis in plant materials. Agronomy
Journal, Madison, v.65, n.1, p.133-134, Jan/Feb. 1973.
ASSOCIATION OF OFFICIAL ANALYTICAL CHEMISTRY. Official
methods of analysis of the Association of Official Analytical
Chemists. 11.ed. Washington, 1970. 1015p.
BROYER, T.C.; CARTON, A.B.; JOHNSON, C.M.; STOUT, P.R.
Chlorine: a micronutrient element for higher plants. Plant Physiology,
Lancaster, v.29, n.6, p.526-532, Nov. 1954.
CATANI, R.A.; MORAES, F.R.P.; BERGAMIN, H. A concentração de
cloro em folhas de café. Anais da Escola Superior de Agricultura
“Luiz de Queiroz” - ESALQ, Piracicaba, v.26, p. 97-98, 1969.
EATON, F.M. Chlorine. In: CHAPMAN, H.D. Diagnostic criteria for
plants and soils. California: Divison of Agricultural Sciences, 1966.
p.93-135.
GAINES, T.P.; PARKER, M.B.; GASCHO, G.J. Automated determination
of chlorides in soil and plant tissue by sodium nitrate extration.
Agronomy Journal, Madison, v.76, n.3, p.371-374, May/June 1984.
GILLIAM, J.W. Rapid measurement of chlorine in plant materials. Soil
Science Society of America Proceedings, Madison, v.35, n.3, p.512-
513, May/June 1971.
GOUNY, P. Observaciones sobre el comportamiento del vegetal en
presencia de ions de cloro. Revista de la Potassa, Berna, v.45, n.5, p.1-
14, 1973
19
GUENTHER, W.B. Química quantitativa: medições e equilíbrio. São
Paulo: Edgard Blücher, 1972. 423p.
JEFFERY, G.H.; BASSETT, J.; MENDHAM, J.; DENNEY, R.C. Vogel:
análise química quantitativa. 5.ed. Rio de Janeiro: Guanabara Koogan,
1992. 712p.
JOHNSON, C.M.; STOUT, P.R.; BROYER, T.C.; CARLTON, A.B.
Comparative chlorine requirements of different plant species. Plant and
Soil, The Hague, v.8, p. 337-353, 1957.
KOLTHOFF, I.M.; SANDELL, E.B. Textbook of quantative inorganic
analysis. 3.ed. New York: The MacMillan Company, 1952. 759p.
LACROIX, R.L.; KEENEY, D.R.; WALSH, L.M. Potenciometric titration
of chloride in plant tissue extracts using the chlorine ion electrode.
Commucations in Soil Science and Plant Analysis, Madison, v.1, n.1,
p.1-6, Jan. 1970.
MALAVOLTA, E.; VITTI, G.C.; OLIVEIRA, S.A. Avaliação do estado
nutricional das plantas. Piracicaba: POTAFOS, 1989. 201p
MARSCHENER, H. Mineral nutrition of higher plant. New York:
Academic Press, 1986. 874p.
MENGEL, K.; KIRKBY, E.A. Principales of plant nutrition. 4.ed.
Berna: International Potash Institute, 1987. 687p.
N’GORAN, K. Effets du chlore sur le comportement de quelques clones de
caféiers robusta sur le littoral Ivoirien. In: INTERNATIONAL
SCIENTIFIC COLLOQUIN ON COFFEE, 13, 1989, Paipa (Colômbia).
Paris: Association Scientifique Internacional Du Café, 1990. p.564-572.
20
OHWEILER, O.A. Química analítica quantitativa. Rio de Janeiro:
Livros Técnicos e Científicos, 1974. v.2, 643p.
OHLWEILER, O.A. Química analítica quantitativa. 3.ed. Rio de
Janeiro: Livros Técnicos e Científicos, 1981. 226p.
OHWEILER, O.A. Teoria e prática a análise quantitativa inorgânica.
Brasília: Universidade de Brasília, 1968a. v.2, 536p.
OHWEILER, O.A. Teoria e prática a análise quantitativa inorgânica.
Brasília: Universidade de Brasília, 1968b. v.3, 807p.
RAIJ, B.van. Geoquímica de micronutrientes. In: FERREIRA, M.E.;
CRUZ, M.C.P.(ed.) Micronutrientes na agricultura. Piracicaba:
POTAFOS/CNPq, 1991. p.99-111.
SNOECK, D.; N’GORAN, K.; SNOECK, J. Étude des formes de potassium
sur chimisme foliare des caféiers robusta en Côte d’Ivoire - Influence du
chlore. Café Cacao Thé, Paris, v.30, n.1, p. 37-50, jan./mar. 1986.
TISDALE, S.R.L.; NELSON, W.L.; BEATON, J.D. Soil fertility and
fertilizers. New York: McMillam Publishing, 1986. 754p.
Вам также может понравиться
- Relatório Cloretos em Água PDFДокумент3 страницыRelatório Cloretos em Água PDFalexandroprazeresОценок пока нет
- Síntese e Isomerização Do (Co (NH3) 5ONO3) Cl2Документ14 страницSíntese e Isomerização Do (Co (NH3) 5ONO3) Cl2Lorena Tuane100% (1)
- Determinação de Cloreto de Sódio em Soro FisiológicoДокумент18 страницDeterminação de Cloreto de Sódio em Soro FisiológicoEvelynSchweitzerОценок пока нет
- Corrosão e Proteção dos MateriaisОт EverandCorrosão e Proteção dos MateriaisРейтинг: 5 из 5 звезд5/5 (1)
- Método de MohrДокумент3 страницыMétodo de MohrAndson Rodrigues100% (2)
- Relatório Prática 1. Marcella Di GirolamoДокумент15 страницRelatório Prática 1. Marcella Di GirolamoMarcella Purificacao Di GirolamoОценок пока нет
- Determinação de CLORETOS EM ÁGUASДокумент2 страницыDeterminação de CLORETOS EM ÁGUASdiangiquimicoОценок пока нет
- Síntese e Caracterização Química Do Cloreto de Hexaaminoníquel (Ii)Документ8 страницSíntese e Caracterização Química Do Cloreto de Hexaaminoníquel (Ii)Mariah CorreiaОценок пока нет
- Utilização do lodo gerado na ETA de Alvorada-RS na fabricação de blocos cerâmicosОт EverandUtilização do lodo gerado na ETA de Alvorada-RS na fabricação de blocos cerâmicosОценок пока нет
- Quimica Aplicada Ao Meio AmbienteДокумент5 страницQuimica Aplicada Ao Meio AmbienteVitoria RamosОценок пока нет
- Relatório 4 - Análise Dos Cátions Do Grupo III (Cr3+, Al3+, Fe3+, Zn2+, Mn2+, Fe2+, Co2+, Ni2+) - QAQ (Grupo 03)Документ22 страницыRelatório 4 - Análise Dos Cátions Do Grupo III (Cr3+, Al3+, Fe3+, Zn2+, Mn2+, Fe2+, Co2+, Ni2+) - QAQ (Grupo 03)David Carvalho100% (1)
- Síntese e Caracterização Do Complexo K3Документ7 страницSíntese e Caracterização Do Complexo K3Laís BarbosaОценок пока нет
- Pratica de DQO Por Espectrofotometria PDFДокумент6 страницPratica de DQO Por Espectrofotometria PDFGraziela LealОценок пока нет
- Lista de Exercícios 3Документ2 страницыLista de Exercícios 3MatheusLopes100% (1)
- Síntese Hexa Ureia de CromoДокумент7 страницSíntese Hexa Ureia de CromoClaudia ChavesОценок пока нет
- Físico-Química - Cálculo Estequiométrico (30 Questões)Документ12 страницFísico-Química - Cálculo Estequiométrico (30 Questões)Ciencias PPT100% (3)
- Maria Helena Leibanti Gerhard 2 FinalДокумент9 страницMaria Helena Leibanti Gerhard 2 FinalsborcabrОценок пока нет
- Relatório CloretoДокумент4 страницыRelatório CloretoPriscila MagalhãesОценок пока нет
- Lista de Execícios - Titulação de PrecipitaçãoДокумент3 страницыLista de Execícios - Titulação de PrecipitaçãoOlivia YoungОценок пока нет
- Monitoria QuímicaДокумент6 страницMonitoria QuímicaBrunaОценок пока нет
- Relatório Cloreto de Terc-ButilaДокумент6 страницRelatório Cloreto de Terc-ButilaThais Almeida100% (1)
- Síntese Cloreto de Tec-Butila - GustavoДокумент8 страницSíntese Cloreto de Tec-Butila - GustavoMarcel AmorimОценок пока нет
- Exercicios QuiДокумент31 страницаExercicios Quipaladinox1110% (1)
- Determinação de Íons Cloreto em Uma Amostra de Soro FisiológicoДокумент17 страницDeterminação de Íons Cloreto em Uma Amostra de Soro FisiológicoMari100% (4)
- DETERMINAÇÃO VOLUMÉTRICA DE ÁCIDO ASCÓRBICO EM VITAMINA C MERCK CEBION® - Química - UTFPR - 2010Документ12 страницDETERMINAÇÃO VOLUMÉTRICA DE ÁCIDO ASCÓRBICO EM VITAMINA C MERCK CEBION® - Química - UTFPR - 2010joaomarcosls100% (6)
- Quimica AnaliicaДокумент8 страницQuimica AnaliicaCamila MoreiraОценок пока нет
- Oxigênio DissolvidoДокумент7 страницOxigênio DissolvidoMari100% (1)
- Pratica 11Документ7 страницPratica 11Matheus SigaudОценок пока нет
- Relatório 04 - Volumetria Por PrecipitaçãoДокумент9 страницRelatório 04 - Volumetria Por PrecipitaçãoLucas ManuelОценок пока нет
- Relatorio 9 - Compostos de Cromo, Ferro e Coblato (Lei de Chatelier)Документ17 страницRelatorio 9 - Compostos de Cromo, Ferro e Coblato (Lei de Chatelier)Dowglas MoraesОценок пока нет
- Aula 07 Especifico VestibularДокумент2 страницыAula 07 Especifico VestibularDiogo MoreiraОценок пока нет
- Questoes-Solucoes-2º AnoДокумент8 страницQuestoes-Solucoes-2º AnoJonathan SoaresОценок пока нет
- Roteiro Prtico 2Документ5 страницRoteiro Prtico 2Mariana KattahОценок пока нет
- Relatório de Química - Cloretos em ÁguaДокумент5 страницRelatório de Química - Cloretos em ÁguapaodequeijodasilvasauroОценок пока нет
- Roteiro de Práticas - EditadoДокумент27 страницRoteiro de Práticas - EditadoJéssica VasconcelosОценок пока нет
- Síntese Do Cloreto de Pentaaminclorocobalto (III)Документ12 страницSíntese Do Cloreto de Pentaaminclorocobalto (III)Fabio Aleixo100% (1)
- Química Experimental I Relatorio JakelineДокумент23 страницыQuímica Experimental I Relatorio JakelineJakeline de Souza Bastos100% (3)
- Quest 07 - Revisão - GabДокумент8 страницQuest 07 - Revisão - GabmisaelinacioОценок пока нет
- Resolução de Isômeros Ópticos Oficial 2Документ6 страницResolução de Isômeros Ópticos Oficial 2Leandro Shiroma100% (1)
- ExercíciosДокумент38 страницExercíciosnicoliiiОценок пока нет
- CLORO RESIDUAL LIVREv 05Документ5 страницCLORO RESIDUAL LIVREv 05bispojjosОценок пока нет
- Laboratório de Química IIIДокумент7 страницLaboratório de Química IIIguerraldo manuel cucha cuchaОценок пока нет
- Complexo de CobaltoДокумент16 страницComplexo de CobaltoCezar ManziniОценок пока нет
- Oxidação Do Mentol RelatórioДокумент7 страницOxidação Do Mentol RelatórioStefany Thábian VieiraОценок пока нет
- Relatório grupoIII AnalíticaДокумент19 страницRelatório grupoIII AnalíticaKarllacarvalho -Оценок пока нет
- 2016-Exercícios de OxiДокумент4 страницы2016-Exercícios de OxiAugusto TanamatiОценок пока нет
- Relatório 2 - Acetilacetonato de Ferro III - OkДокумент13 страницRelatório 2 - Acetilacetonato de Ferro III - OkJacyara Flores Arbues Carneiro100% (1)
- Lista 1ºano - Sais e NeutralizaçãoДокумент8 страницLista 1ºano - Sais e NeutralizaçãoganyupeitosОценок пока нет
- Apostila Experimental 1o Ciclo202002Документ7 страницApostila Experimental 1o Ciclo202002LINDAURA VIDALОценок пока нет
- Lista de Exercícios 3 QUI0946Документ1 страницаLista de Exercícios 3 QUI0946Lais VeronezОценок пока нет
- Sinteses de Inorganic A ExpДокумент6 страницSinteses de Inorganic A ExpFláviaDosReisОценок пока нет
- Prática de CloretosДокумент5 страницPrática de CloretosMaria Isabel CabralОценок пока нет
- Roteiro de Inorgânica 1 Modificado 2014.1Документ33 страницыRoteiro de Inorgânica 1 Modificado 2014.1Jéssica VasconcelosОценок пока нет
- Calculo Esteq ExerciciosДокумент42 страницыCalculo Esteq ExercicioslcadmОценок пока нет
- Relatório de MineraçãoДокумент7 страницRelatório de MineraçãogabriellОценок пока нет
- Procedimentos para Ensaio de Abrasao Conforme Norma Din 53.516Документ5 страницProcedimentos para Ensaio de Abrasao Conforme Norma Din 53.516Olavo FagundesОценок пока нет
- L2 - FNS e LajesДокумент8 страницL2 - FNS e LajesJefferson CruzОценок пока нет
- Conferência Prof. Manuel Matos Psicanálise Relacional PDFДокумент17 страницConferência Prof. Manuel Matos Psicanálise Relacional PDFVeraCruzОценок пока нет
- Proposta 2 Modelo de Plano de Aula para Avaliação 2019-1Документ4 страницыProposta 2 Modelo de Plano de Aula para Avaliação 2019-1Izabel BorgesОценок пока нет
- Manual LGPD - EscolasДокумент19 страницManual LGPD - EscolasJacqueline RodriguesОценок пока нет
- A Pré-História AmericanaДокумент4 страницыA Pré-História AmericanaDaniel Torres Pereira SaraivaОценок пока нет
- Projeto Escolinha de FutebolДокумент5 страницProjeto Escolinha de FutebolPaulo Vitor82% (11)
- Magia de Druida LVL 0Документ2 страницыMagia de Druida LVL 0Leonardo Vinicius de GasperinОценок пока нет
- Plenitude - Divaldo FrancoДокумент105 страницPlenitude - Divaldo FrancoCarlosОценок пока нет
- DescartesДокумент8 страницDescartesVitor Moroni BarrozoОценок пока нет
- Máscara - Trabalho Final Com As 3 Etapas para Postar No Link.Документ4 страницыMáscara - Trabalho Final Com As 3 Etapas para Postar No Link.kaiqueaugusto481Оценок пока нет
- CS14 PDFДокумент1 страницаCS14 PDFAl. Afonso Miguel Lucas Ferreira (AEM)Оценок пока нет
- Capítulo 1 - Forças, Potência e MicropolíticaДокумент13 страницCapítulo 1 - Forças, Potência e MicropolíticaPaulo ToledoОценок пока нет
- Código de Ética Do Profissional Da Química - 221104 - 185045Документ4 страницыCódigo de Ética Do Profissional Da Química - 221104 - 185045rodolfo racaneleОценок пока нет
- Captura de Tela 2024-02-26 À(s) 20.11.45Документ14 страницCaptura de Tela 2024-02-26 À(s) 20.11.458gtrzxmzzxОценок пока нет
- FICHA - DE - INSCRIÇÃO - Infraero - CBA - 2 02.2022Документ2 страницыFICHA - DE - INSCRIÇÃO - Infraero - CBA - 2 02.2022Marcelo 2195Оценок пока нет
- Universidade Estácio de SáДокумент10 страницUniversidade Estácio de SáAdrielly WanzelerОценок пока нет
- 10 Montagem Completa Interna e DivididaДокумент55 страниц10 Montagem Completa Interna e DivididaworldinforcellОценок пока нет
- Teste 5 Global 2019 Mat. Máximo Porto Editora 5º AnoДокумент9 страницTeste 5 Global 2019 Mat. Máximo Porto Editora 5º AnoGuida Dos ReisОценок пока нет
- Classes GramaticaisДокумент4 страницыClasses GramaticaisvitorОценок пока нет
- Manual NFe DestinadaДокумент10 страницManual NFe DestinadaMárcio SantosОценок пока нет
- Você É A Minha Luz - Linda EvangelistaДокумент35 страницVocê É A Minha Luz - Linda EvangelistaAna Paula SoaresОценок пока нет
- Artigo KatianeДокумент21 страницаArtigo KatianeFisioterapeutas HCMMОценок пока нет
- Relatorio IPP CensoPopulacaoRua 2022Документ21 страницаRelatorio IPP CensoPopulacaoRua 2022Lucas Santiago MattosОценок пока нет
- 9 - Projetos Alexandre-BДокумент1 страница9 - Projetos Alexandre-BIgor Muniz OliveiraОценок пока нет
- VIDA & CARREIRA - Eu ComigoДокумент5 страницVIDA & CARREIRA - Eu ComigoJennifer AmaralОценок пока нет
- Linguagem e Ludicidade Na InfânciaДокумент85 страницLinguagem e Ludicidade Na InfânciaMurilo SilvaОценок пока нет
- Ficha de Anaminese Micropigmentação: Cadastro Da (O) ClienteДокумент3 страницыFicha de Anaminese Micropigmentação: Cadastro Da (O) ClienteKassia PontesОценок пока нет
- DISSERTAÇÃO - Teoria Econômica Do CrimeДокумент227 страницDISSERTAÇÃO - Teoria Econômica Do CrimeLuiz Carlos Gomes JuniorОценок пока нет