Академический Документы
Профессиональный Документы
Культура Документы
Sustitución electrofilica aromática: Nitración de la anilina para obtener p-nitroacetanilida
Загружено:
michel0 оценок0% нашли этот документ полезным (0 голосов)
22 просмотров6 страницEste documento describe la síntesis de p-nitroacetanilida mediante la nitración de acetanilida. La anilina no puede nitrarse directamente debido a su reactividad, por lo que primero se protege el grupo amino convirtiéndolo en acetanilida. Luego, la acetanilida se nitra usando una mezcla de ácidos sulfúrico y nítrico concentrados en un baño de hielo, obteniéndose p-nitroacetanilida con un rendimiento del 145% y un punto de fusión de 145°C.
Исходное описание:
informe amilina
Оригинальное название
informe amilina
Авторское право
© © All Rights Reserved
Доступные форматы
DOCX, PDF, TXT или читайте онлайн в Scribd
Поделиться этим документом
Поделиться или встроить документ
Этот документ был вам полезен?
Это неприемлемый материал?
Пожаловаться на этот документEste documento describe la síntesis de p-nitroacetanilida mediante la nitración de acetanilida. La anilina no puede nitrarse directamente debido a su reactividad, por lo que primero se protege el grupo amino convirtiéndolo en acetanilida. Luego, la acetanilida se nitra usando una mezcla de ácidos sulfúrico y nítrico concentrados en un baño de hielo, obteniéndose p-nitroacetanilida con un rendimiento del 145% y un punto de fusión de 145°C.
Авторское право:
© All Rights Reserved
Доступные форматы
Скачайте в формате DOCX, PDF, TXT или читайте онлайн в Scribd
0 оценок0% нашли этот документ полезным (0 голосов)
22 просмотров6 страницSustitución electrofilica aromática: Nitración de la anilina para obtener p-nitroacetanilida
Загружено:
michelEste documento describe la síntesis de p-nitroacetanilida mediante la nitración de acetanilida. La anilina no puede nitrarse directamente debido a su reactividad, por lo que primero se protege el grupo amino convirtiéndolo en acetanilida. Luego, la acetanilida se nitra usando una mezcla de ácidos sulfúrico y nítrico concentrados en un baño de hielo, obteniéndose p-nitroacetanilida con un rendimiento del 145% y un punto de fusión de 145°C.
Авторское право:
© All Rights Reserved
Доступные форматы
Скачайте в формате DOCX, PDF, TXT или читайте онлайн в Scribd
Вы находитесь на странице: 1из 6
Sustitución electrofilica Aromática: Nitración la
Anilina.
Michel Mijares
Laboratorio de Química Orgánica II. Facultad Experimental de Ciencias y Tecnología.
Universidad de Carabobo. Naguanagua, Venezuela.
Revisado por: Prof. Maria Tapizquent.
Resumen:
Se realizó la síntesis de la p-nitroacetalinida mediante un proceso de
sustitución electrofilica aromática sobre la acetanilida, a partir de la anilina.
La nitración aromática se llevó a cabo, por la sustitución de un átomo de
hidrogeno sobre un grupo aromático del grupo nitro obteniéndose nitro
derivados, la anilina no se puede nitrar de forma directa debido a la
reactividad de la anilina (inherente a la presencia del grupo amino –NH2). por
lo que en la práctica se procedió a la protección del grupo amino,
seguidamente se realizó la reacción de la nitración y finalmente se eliminó el
grupo protector obteniéndose un rendimiento de la p-nitroacetanilida de con
punto de fusión de 145.
Introducción electrónica) debido a la capacidad
que tiene el par de electrones del
La reacción de nitración del anillo nitrógeno para deslocalizarse a
aromático es uno de los recursos través del sistema pi (efecto +R).
más Utilizados para introducir un Por esta razón la anilina
nuevo grupo funcional en el mismo. experimenta reacciones de
Se trata de un proceso de sustitución electrofílica con mucha
sustitución electrofílica aromática facilidad pudiendo dar lugar a
y, como tal, su regioquímica. productos de polisustitución en las
Depende de los sustituyentes en el posiciones orto y para, por lo que
anillo aromático. En nuestro caso el no se puede llevar a cabo la
anillo aromático de la anilina (1) reacción de nitración de la anilina
está muy activado (rico en densidad sin un paso de protección del grupo
amino. Además, debido al carácter
básico de este grupo tendría lugar
una reacción ácido-base con los
reactivos que seUtilizan en la
nitración Transformando la anilina
en una amida (ej: acetanilida, (2) el
grupo amino queda protegido. Así
se evita que tengan lugar reacciones [1]
de tipo ácido-base y se disminuye la
MATERIALES Y MÉTODOS.
reactividad del sistema. La razón es
que en las amidas hay una Inicialmente se procedió a preparar
estructura resonante resultante de la
una solución de acetanilida Se
deslocalización del par de
añadió en un matraz 2,5 ml de la
electrones del nitrógeno en el doble
anilina y el anhídrido acético y se
enlace C=O de la amida, haciendo mantuvo la mezcla de reacción
al par de electrones menos agitando a temperatura ambiente
accesible al anillo aromático. Una durante 10 minutos. Transcurrido
ventaja adicional de la formación este tiempo el matraz, ya frío la
de amidas es que el mayor tamaño
mezcla de reacción, se diluyo con
del grupo amida favorece la
100 mL de agua. El producto se
sustitución en la posición 4 frente a separó mediante extracción (fig. 1)
la 2, por estar esta última más y fue de pureza Suficiente para ser
impedida a continuación el utilizado en el laboratorio. (fig2)
mecanismo de reacción que se lleva
a cabo para obtener el producto
deseado.
(1) (2) (3) (4)
Fig. 1 montaje de extracción.
Pesar 2,5 g de acetanilida en un matraz de 50 mL provisto de imán. Se colocó
el matraz en un baño de hielo y mientras se agita se añadio 5 mL de ácido
sulfúrico concentrado en porciones de 1 mL y durante un tiempo aproximado
de un minuto en baño de hielo. Con cuidado se mezcló 2 mL de ácido
sulfúrico concentrado y 2,7 mL de nítrico concentrado Seguidamente se
procedió se vertio este contenido en el matraz
estaba en baño de hielo.
se mezcló 2 mL de ácido sulfúrico concentrado y 2,7 mL de nítrico
concentrado Seguidamente se procediose virtio el contenido en el matr
Вам также может понравиться
- Sintesis en Varias EtapasДокумент5 страницSintesis en Varias EtapasKATHERINE LISET ORTIZ PATERNINA ESTUDIANTE ACTIVOОценок пока нет
- Informe de Sear Nitracion AnilinaДокумент8 страницInforme de Sear Nitracion AnilinaSacha OrdazОценок пока нет
- Nitracion AcetanlidaДокумент8 страницNitracion AcetanlidaMaria Claudia MartinezОценок пока нет
- Nitracion de AcetanilidaДокумент4 страницыNitracion de AcetanilidaLuis SuárezОценок пока нет
- Acetilación de La Anilina y Bromación de La AcetanilidaДокумент6 страницAcetilación de La Anilina y Bromación de La AcetanilidaISABELLA RIOS MONTOYAОценок пока нет
- Informe de EntropiaДокумент7 страницInforme de EntropiaMaria Claudia MartinezОценок пока нет
- Acetilación de La Anilina. Informe 4 DefinitivoДокумент2 страницыAcetilación de La Anilina. Informe 4 DefinitivoSHARON OSSA CABALLERO100% (1)
- Pract-2 Obtencion de AcetanilidaДокумент9 страницPract-2 Obtencion de AcetanilidaManuela RamirezОценок пока нет
- Sintesis Del 2,4 DinitroclobencenofinalДокумент8 страницSintesis Del 2,4 DinitroclobencenofinalJeferson Lopez RomeroОценок пока нет
- Nitración de AcetanilidaДокумент5 страницNitración de AcetanilidaKatherine Gomez RamirezОценок пока нет
- PRACTICA P NitroanilinaДокумент8 страницPRACTICA P NitroanilinaLuis Ferráez LindemannОценок пока нет
- Informe 10Документ8 страницInforme 10LiziQuimisPonceОценок пока нет
- Laboratorio Organica 2Документ7 страницLaboratorio Organica 2ljsilva11Оценок пока нет
- Practica No 3 - Sintesis de Un Alqueno y Sus PropiedadesДокумент14 страницPractica No 3 - Sintesis de Un Alqueno y Sus PropiedadesAstrid López CanoОценок пока нет
- Informe Sintesis de WilliamsonДокумент8 страницInforme Sintesis de WilliamsonIvonne QuirogaОценок пока нет
- Practica 1-Obtencion de P-NitroanilinaДокумент10 страницPractica 1-Obtencion de P-Nitroanilinassmrn100% (1)
- OBTENCIÓN DE AMARILLO MARTIUS ColumnasДокумент6 страницOBTENCIÓN DE AMARILLO MARTIUS ColumnasAngel FerrariОценок пока нет
- Acetilacion de AnilinaДокумент4 страницыAcetilacion de AnilinaAngie GomezОценок пока нет
- Reporte Orgánica 8Документ2 страницыReporte Orgánica 8Cir Alejandro AlmazánОценок пока нет
- SÍNTESIS DE ÉSTERES POR REACCIÓN DE WILLIAMSONДокумент14 страницSÍNTESIS DE ÉSTERES POR REACCIÓN DE WILLIAMSONMaría Fernanda Carmona MartínezОценок пока нет
- Investigación Previa Practica No.3Документ12 страницInvestigación Previa Practica No.3Alvarado Fernández Juan CarlosОценок пока нет
- Informe de Laboratorio Practica 2Документ6 страницInforme de Laboratorio Practica 2jeffersonОценок пока нет
- Sintesis Nitroacetanilida - JULIO 2017Документ6 страницSintesis Nitroacetanilida - JULIO 2017Leonela Herrera DuqueОценок пока нет
- Síntesis y aplicación del colorante azoico rojo paranitronilinaДокумент4 страницыSíntesis y aplicación del colorante azoico rojo paranitronilinaVALERIA ALEJANDRA VILLEGAS ALVAREZОценок пока нет
- Laboratorio Obtencion Del Acido PicricoДокумент8 страницLaboratorio Obtencion Del Acido PicricoMachuruti MAОценок пока нет
- SÍNTESIS AMARILLO MARTIUS SUSTITUCIÓN ELECTROFÍLICA 1-NAFTOLДокумент5 страницSÍNTESIS AMARILLO MARTIUS SUSTITUCIÓN ELECTROFÍLICA 1-NAFTOLDiaz AndresОценок пока нет
- Informe SINTESIS de LA AnilinaДокумент8 страницInforme SINTESIS de LA AnilinamichelОценок пока нет
- Informe 2 Organica IIДокумент3 страницыInforme 2 Organica IILUIS JAVIER RAMIRO SANCHEZОценок пока нет
- Preparacion de AcetanilidaДокумент6 страницPreparacion de AcetanilidaJUAN JOSE ZAPATA PUENTESОценок пока нет
- Reporte de Práctica 5 - OBTENCIÓN DE ACETANILIDAДокумент6 страницReporte de Práctica 5 - OBTENCIÓN DE ACETANILIDAMarkОценок пока нет
- AcetalimidaДокумент10 страницAcetalimidaJuan Esteban Serna OsunaОценок пока нет
- PRACTICA #12.docx OrganicaДокумент4 страницыPRACTICA #12.docx Organicaruben100% (2)
- Formación y Acoplamiento de Sales de DiazonioДокумент6 страницFormación y Acoplamiento de Sales de Diazonioalmuchis12Оценок пока нет
- P07 P-Nitroanilina PDFДокумент3 страницыP07 P-Nitroanilina PDFSandra GameroОценок пока нет
- Practica No 2Документ9 страницPractica No 2AshleyGómez0% (1)
- Practica 1 AmarilloДокумент6 страницPractica 1 AmarilloAlma LopezОценок пока нет
- Síntesis Del M-NitrobenzaldehídoДокумент7 страницSíntesis Del M-NitrobenzaldehídoKathyPazmiñoViteriОценок пока нет
- Acetilacion de La AnilinaДокумент3 страницыAcetilacion de La AnilinaMiguel Synyster Fontalvo Garcerant100% (1)
- Sintesis de La NitroacetanilinaДокумент3 страницыSintesis de La Nitroacetanilinagaiselramos240Оценок пока нет
- Informe 3 Síntesis de BenzalanilinaДокумент6 страницInforme 3 Síntesis de BenzalanilinaNatalia Aroz OrtizОценок пока нет
- Reporte Practica 1 P-NitroacetanilidaДокумент8 страницReporte Practica 1 P-NitroacetanilidamonomioОценок пока нет
- Laboratorio 8 NitrobencenoДокумент13 страницLaboratorio 8 NitrobencenoEuge963Оценок пока нет
- Practica 5 - Organica IVДокумент9 страницPractica 5 - Organica IVAntonio SuárezОценок пока нет
- SÍNTESIS DE Para-NitroanilinaДокумент9 страницSÍNTESIS DE Para-NitroanilinaTowerОценок пока нет
- Nitrobenceno Instructivo Julio 2019Документ10 страницNitrobenceno Instructivo Julio 2019july 507Оценок пока нет
- AnilinaДокумент2 страницыAnilinaMishel MijaresОценок пока нет
- Práctica 5 Nitración Del Benzoato de MetiloДокумент3 страницыPráctica 5 Nitración Del Benzoato de MetiloAralee EspinozaОценок пока нет
- Preparación de AcetanilidaДокумент6 страницPreparación de AcetanilidaGonzalo RestrepoОценок пока нет
- Sustitución Electrofílica Aromática en La Síntesis de P-BromoacetanilidaДокумент7 страницSustitución Electrofílica Aromática en La Síntesis de P-BromoacetanilidaVALERIA ALEJANDRA VILLEGAS ALVAREZОценок пока нет
- PREVIO NUMERO 4 SÍNTESIS DE p-NITROANILINA EN TRES ETAPASДокумент8 страницPREVIO NUMERO 4 SÍNTESIS DE p-NITROANILINA EN TRES ETAPASJose Antonio Martinez MorenoОценок пока нет
- Nitración Del Ácido SalicílicoДокумент6 страницNitración Del Ácido SalicílicowendyОценок пока нет
- Cuestionario de La Práctica 9Документ2 страницыCuestionario de La Práctica 9Athenas A.PОценок пока нет
- Reporte P-Nitroacetanilida PBB y LMCДокумент2 страницыReporte P-Nitroacetanilida PBB y LMCluisedo -Оценок пока нет
- 2011 TP 3 LipidosДокумент3 страницы2011 TP 3 LipidosMarcela V. PellegriniОценок пока нет
- ProteínasДокумент1 страницаProteínasmichelОценок пока нет
- RabanoДокумент20 страницRabanomichelОценок пока нет
- Informe Enzima RabanoДокумент2 страницыInforme Enzima RabanomichelОценок пока нет
- Cuantificacion de La Actividad de AmilaДокумент11 страницCuantificacion de La Actividad de AmilamichelОценок пока нет
- 2003-2 - La EstrucДокумент9 страниц2003-2 - La EstrucHobeth BautistaОценок пока нет
- Extraccion e Identificacion de Lipidos PDFДокумент13 страницExtraccion e Identificacion de Lipidos PDFSofia SantanaОценок пока нет
- FORMA IVA 99030 Declaracion Y Pago Del Impuesto Al Valor AgregadoДокумент2 страницыFORMA IVA 99030 Declaracion Y Pago Del Impuesto Al Valor AgregadoMarcelОценок пока нет
- Carbohidratos Azucares ModificadaДокумент10 страницCarbohidratos Azucares ModificadamichelОценок пока нет
- 2011 TP 3 LipidosДокумент3 страницы2011 TP 3 LipidosMarcela V. PellegriniОценок пока нет
- Cuantificacion de La Actividad de AmilaДокумент11 страницCuantificacion de La Actividad de AmilamichelОценок пока нет
- Almdon EnzimaДокумент76 страницAlmdon EnzimaMelany Krystel Morales ZuñigaОценок пока нет
- Constante de velocidad y estado de transición en reacciones químicasДокумент25 страницConstante de velocidad y estado de transición en reacciones químicasmichelОценок пока нет
- 2003-2 - La EstrucДокумент9 страниц2003-2 - La EstrucHobeth BautistaОценок пока нет
- Carbohidratos Azucares ModificadaДокумент10 страницCarbohidratos Azucares ModificadamichelОценок пока нет
- Extracción y análisis de ADN bacterianoДокумент49 страницExtracción y análisis de ADN bacterianoElisramon SuarezduranОценок пока нет
- 2003-2 - La EstrucДокумент9 страниц2003-2 - La EstrucHobeth BautistaОценок пока нет
- DestilacionДокумент6 страницDestilacionmichelОценок пока нет
- RdotaДокумент1 страницаRdotamichelОценок пока нет
- Informe ModeloДокумент7 страницInforme ModelomichelОценок пока нет
- Colorantes y Tintes VegetalesДокумент28 страницColorantes y Tintes Vegetalesjuliob412100% (2)
- DestilacionДокумент6 страницDestilacionmichelОценок пока нет
- InformeДокумент4 страницыInformemichelОценок пока нет
- Informe 2Документ8 страницInforme 2Mishel MijaresОценок пока нет
- DestilacionДокумент6 страницDestilacionmichelОценок пока нет
- Informe ModeloДокумент7 страницInforme ModelomichelОценок пока нет
- Carta Canje de Cheques de GerenciaДокумент1 страницаCarta Canje de Cheques de Gerenciamichel100% (1)
- Informe ModeloДокумент7 страницInforme ModelomichelОценок пока нет
- InformeДокумент11 страницInformemichelОценок пока нет
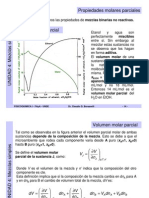
- Propiedades Molares ParcialesДокумент13 страницPropiedades Molares ParcialesCDAMNUОценок пока нет
- Caracterización de diodos mediante simulación en LTSpiceДокумент5 страницCaracterización de diodos mediante simulación en LTSpiceNational physicsОценок пока нет
- Solidworks Composer CWДокумент4 страницыSolidworks Composer CWJosephRomeraloОценок пока нет
- Jitorres MAESTRO16.2017Документ164 страницыJitorres MAESTRO16.2017Berserkher 21Оценок пока нет
- Semana 5 Clase 1Документ27 страницSemana 5 Clase 1dantevictor_g100% (1)
- La Pasta en El HormigonДокумент4 страницыLa Pasta en El Hormigonceci salgueroОценок пока нет
- Descarga El Resumen de El ErmitanoДокумент1 страницаDescarga El Resumen de El ErmitanoNicole van WeezelОценок пока нет
- Unidad 1 de WordДокумент12 страницUnidad 1 de WordSantiago Gomez TijaroОценок пока нет
- 1 Tesalonicenses Alumno - Eduardo B. CoriaДокумент15 страниц1 Tesalonicenses Alumno - Eduardo B. CoriaClecioAlvesОценок пока нет
- No AdmitiodsДокумент501 страницаNo Admitiodsgwionx0% (1)
- Alien Primal's TreasureДокумент244 страницыAlien Primal's TreasureTammy Sanchez100% (1)
- Bar RestaurantДокумент88 страницBar Restaurantrosa alejandra gamez perezОценок пока нет
- Sesión 01 - Mat - Competencia Resuele Problemas de Gestión de Datos e Incertidumbre - 2023Документ11 страницSesión 01 - Mat - Competencia Resuele Problemas de Gestión de Datos e Incertidumbre - 2023Yuliana Diaz Lozada100% (1)
- Taller Lead TimeДокумент4 страницыTaller Lead TimeXimena AlbarracinОценок пока нет
- Semana 13Документ40 страницSemana 13Murrieta Salvatierra RenzoОценок пока нет
- Sistema Solar CompletoДокумент25 страницSistema Solar CompletoSabrina Teran100% (1)
- Trifolio AmhonДокумент2 страницыTrifolio Amhonfantomas1959Оценок пока нет
- AATCC Test Method 61 2009.en - EsДокумент5 страницAATCC Test Method 61 2009.en - EsJhon EdissonОценок пока нет
- Hombres Llamados A Asumir Tareas Del Hogar y Fomentar Equidad en La FamiliaДокумент2 страницыHombres Llamados A Asumir Tareas Del Hogar y Fomentar Equidad en La FamiliaMaría Fidelia Monterrey EspinozaОценок пока нет
- Formulario de informe final de desempeño docente por asignatura (2016Документ3 страницыFormulario de informe final de desempeño docente por asignatura (2016Yessica SolizОценок пока нет
- La Importancia Del Pensamiento CríticoДокумент22 страницыLa Importancia Del Pensamiento CríticoCinthia ReyesОценок пока нет
- Informe Proyecto Entrenador Grupo BДокумент28 страницInforme Proyecto Entrenador Grupo Bfelipe gonzalezОценок пока нет
- TripticoДокумент3 страницыTripticoVanAynderGraysОценок пока нет
- Administración sostenibleДокумент11 страницAdministración sostenibleTenma MagdowellОценок пока нет
- Coseriu El Llamado Lat N VulgarДокумент83 страницыCoseriu El Llamado Lat N VulgarIgnacio Andrés Pardo VásquezОценок пока нет
- Ley de Personas Con DiscapacidadДокумент25 страницLey de Personas Con DiscapacidadNicolás Oliva LealОценок пока нет
- Bitacora de Ppe Estudiante 9Документ17 страницBitacora de Ppe Estudiante 9Ivonne Lara FrancoОценок пока нет
- El Tema y Los Subtemas para Tercero de SecundariaДокумент14 страницEl Tema y Los Subtemas para Tercero de SecundariaAnonymous XpOHZlfFОценок пока нет
- Manual Del Sistema de Captura de Los ResultadosДокумент21 страницаManual Del Sistema de Captura de Los ResultadosPlutogrxyОценок пока нет
- Organización Política y Social ToltecasДокумент3 страницыOrganización Política y Social ToltecasArthur Zecua Pres44% (9)
- Hacer Una Copia de Respaldo de Los Drivers Con DriverMaxДокумент9 страницHacer Una Copia de Respaldo de Los Drivers Con DriverMaxAlemBert López ChОценок пока нет