Академический Документы
Профессиональный Документы
Культура Документы
Monografía Demencia
Загружено:
Willy TorresИсходное описание:
Оригинальное название
Авторское право
Доступные форматы
Поделиться этим документом
Поделиться или встроить документ
Этот документ был вам полезен?
Это неприемлемый материал?
Пожаловаться на этот документАвторское право:
Доступные форматы
Monografía Demencia
Загружено:
Willy TorresАвторское право:
Доступные форматы
MAESTRÍA EN NEUROPSICOLOGÍA
TEMA: MONOGRAFIA, DEMENCIA ALZHEIMER Y CUERPOS DE LEWY
MODULO: PRACTICA NEUROPSICOLÓGICA
MAESTRO: RENE ARMANDO HERRERA DOMINGUEZ
ELABORADO POR:
WILLIAM IGNACIO TORRES PALMA
FECHA: 11 DE JULIO DEL 2019
Introducción
En su concepto actual, la demencia puede definirse como un síndrome
adquirido, de naturaleza orgánica, caracterizado por un deterioro permanente de la
memoria y de otras funciones intelectuales, frecuentemente acompañado de otras
manifestaciones psicopatológicas y del comportamiento, que ocurre sin alteración
del nivel de la conciencia, afectando al funcionamiento social y/o laboral del sujeto
afectado. La demencia es un síndrome clínico de etiología múltiple, por lo general
de curso crónico, pero no necesariamente irreversible ni progresivo.
En esta última década se han producido grandes avances en la genética
molecular, identificándose un gran número de genes determinantes, cuya
mutación permite diagnosticar una enfermedad y de genes de susceptibilidad,
cuyos polimorfismos actúan como marcadores de riesgo genético. Asimismo, se
han dilucidado algunos de los mecanismos implicados en la patogenia de múltiples
enfermedades neurodegenerativas, que cursan con deterioro cognitivo y demencia
(Fonatn, 2012).
Los modernos estudios de neuropatología incluyen las variantes de la
biología molecular, por lo cual, se pueden relacionar los cambios anatomo
patológicos con la presencia de un substrato bioquímico anor- mal originado en un
defecto genético. De acuerdo a la descripción y los hallazgos de neuropatología es
muy difícil establecer una demencia de localización cortical y otra subcortical, de
tal manera que esta diferenciación es fundamentalmente clínica apoyada por los
estudios de MRI (Fonatn, 2012).
Para clasificar una demencia es necesario, en primer lugar, establecer si
existe alguna enfermedad sistémica que la justifique, si puede ser atribuida a
patología cerebrovascular o si, por el contrario, es producida por un proceso
neurológico de carácter lentamente progresivo y de naturaleza degenerativa.
A pesar de la heterogeneidad individual y etiológica del síndrome de
demencia, se han identificado dos patrones clínicos que, aunque controvertidos en
los últimos años, resultan útiles desde un punto de vista clínico, ya que facilitan un
acercamiento sistemático al diagnóstico diferencial (Fonatn, 2012).
El primer patrón incluye las demencias corticales como la enfermedad de
Alzheimer. Se caracteriza por la afectación fundamental del lenguaje, la memoria
(principalmente memoria explícita), praxias, gnosias y razonamiento abstracto.
El otro patrón lo forman las demencias subcorticales (incluyen trastornos
como la enfermedad de Parkinson, enfermedad de Huntington, parálisis
supranuclear progresiva, etc.) y se distinguen fundamentalmente por síntomas
clínicos que implican afectación de los ganglios basales, de ciertos núcleos
talámicos y del tronco cerebral (Cacabelos, 2001).
Desde una perspectiva de la anatomía funcional, el núcleo estriado, el globo
pálido, el tálamo anterior y medial y la sustancia negra mesencefálica están
interconectados con regiones de la corteza prefrontal en una serie de circuitos que
tienen implicaciones comportamentales. Déficit cognitivo similares pueden resultar
de lesiones en cualquier localización de estos circuitos o reflejar disfunción de
éstos, ya sea a nivel cortical o subcortical, como ocurre en la demencia
frontotemporal. Por tanto, se puede establecer una tercera categoría los procesos
mixtos corticales-subcorticales, como la demencia por cuerpos de Lewy,
degeneración corticobasal, algunas demencias vasculares y por virus lentos, que
típicamente producen síntomas atribuibles a disfunción de estructuras corticales y
subcorticales (Cacabelos, 2001).
Como se ha mencionada anteriormente hay una gran diversidad de
etiología relacionada con la demencia, sin embargo, este documento se centrará
en el tipo de Alzheimer y la demencia por cuerpos de Lewy.
Enfermedad de Alzheimer
La enfermedad de Alzheimer es una demencia degenerativa primaria de
inicio insidioso y curso progresivo que se caracteriza clínicamente por la pérdida
de memoria y otras funciones cognoscitivas, así como por una serie de síntomas
no cognoscitivos, entre los que destacan los de tipo depresivo o psicótico, y los
trastornos del comportamiento, y desde el punto de vista anatomopatológico, por
la presencia de una serie de lesiones a nivel cerebral - acúmulo de proteína beta-
amiloide autoagregante con formación de placas neuríticas extraneuronales;
alteración de la proteína tau del citoesqueleto neuronal, que da lugar a los ovillos
neurofibrilares, astrogliosis, y pérdida de sinapsis y muerte neuronal en regiones
cerebrales selectivas que, en su conjunto, son patognomónicas. (INTNAC. 2018).
La EA es la causa más frecuente de síndrome demencial en el anciano. Al
periodo de tiempo en que ya ha comenzado la afectación cerebral, pero sin que se
hayan producido repercusiones funcionales se le denomina “fase silente” o
“preclínica” de la enfermedad. Se desconoce la duración de la fase preclínica; es
posible que la afectación neuronal comience décadas antes de que aparezcan los
primeros síntomas. Con la aparición de los primeros síntomas se inicia la “fase
clínica” de la enfermedad, aunque en un principio los síntomas todavía no son tan
importantes como para poder diagnosticar un síndrome demencial. Más tarde, en
un momento dado de la evolución, la afectación es tan grave que se considera que
se ha instaurado una demencia; a partir de entonces se habla de “fase demencial”
de la enfermedad. Como media, el tiempo que transcurre desde que aparecen los
primeros síntomas hasta que puede realizarse un diagnóstico de demencia es de
2,5 años. El tiempo medio estimado desde el comienzo de la enfermedad hasta la
muerte del sujeto es de 5-10 años. Contamos por lo tanto con tres tipos de
síntomas: neuropsicológicos, psiquiátricos y neurológicos. (INTNAC. 2018).
Entre las características neuropsicológicas encontramos deterioro
progresivo de la memoria y del lenguaje, declive en capacidades visoespaciales y
motoras, y alteraciones en las funciones ejecutivas tales como la capacidad de
abstracción y de juicio. El trastorno de la memoria se caracteriza por alteración de
la capacidad de nuevo aprendizaje y de reproducción de nuevos contenidos.
Asimismo, la memoria de reconocimiento está alterada, y se beneficia poco de
pistas o claves. Por último, la memoria remota está menos alterada que la
reciente, pero también se afecta conforme la enfermedad progresa. Muy
relacionada con la pérdida de memoria, aparece típicamente una desorientación,
en principio temporal y posteriormente topográfica y personal (INTNAC. 2018).
La alteración del lenguaje se caracteriza por afasia nominal, pérdida de
fluencia, tendencia a la repetición y deterioro progresivo de la comprensión verbal.
La capacidad de repetición se conserva hasta una fase avanzada, y con
frecuencia se manifiestan trastornos de repetición como ecolalia y palilalia. Los
trastornos motores incluyen una gama amplia de trastornos, desde la dispraxia –
visoespacial, ideomotora, motora – hasta la abulia cognitiva. Aunque difíciles de
valorar, la capacidad de reconocer objetos y caras (agnosia y prosopagnosia) está
típicamente disminuida (Jurado, Mataró & Pueyo, 2013).
La capacidad de planificación, de juicio y de pensamiento abstracto y otras
funciones mediadas por el lóbulo frontal también se ven afectadas de forma
progresiva en la enfermedad. Como resultado del declive cognoscitivo, se produce
un deterioro en el funcionamiento personal y social, tanto en actividades básicas
de autocuidado (AVD) como en actividades instrumentales (AIVD), y una
dependencia creciente. Los síntomas psiquiátricos son también típicos de la EA
(Jurado, Mataró & Pueyo, 2013).
Se ha descrito una amplia gama de fenómenos psicopatológicos, con una
frecuencia de presentación alta (50-83%), aunque variable a lo largo de la
enfermedad. Al comienzo de la enfermedad son típicos los cambios de
personalidad, por lo general apatía o disminución de intereses previos junto con
una acentuación de rasgos premórbidos, que puede aparecer en el 70% de los
casos. Los síntomas depresivos son frecuentes, especialmente en los estadios
iniciales y medios de la enfermedad, aunque existen discrepancias notables sobre
su prevalencia, oscilando desde el 25 al 85 %. Los trastornos del contenido del
pensamiento alcanzan el 30%, mientras que la presencia de alucinaciones se sitúa
en el 15%. En conjunto, otros síntomas psiquiátricos, como ansiedad, etc. pueden
alcanzar un 20%. Los trastornos conductuales, como la agresividad (20%) o la
deambulación incontrolada (70%) también son frecuentes, así como los trastornos
del sueño (20%), del apetito (30%) y del impulso sexual (10%) (Jurado, Mataró &
Pueyo, 2013).
Finalmente, los síntomas neurológicos solo aparecen en la última fase de la
EA. Típicamente consiste en rigidez generalizada, incapacidad para la marcha y la
deglución, incontinencia, y aparición de reflejos primitivos (prensión, succión).
Pueden aparecer mioclonías, y el 15% de los pacientes tiene crisis epilépticas.
También se manifiestan ocasionalmente síntomas del síndrome de Kluver-Bucy,
como hiperoralidad. Las causas más frecuentes de muerte son la aspiración, y la
sepsis por infección respiratoria o urinaria (Rodríguez, Gutiérrez & Fernandos,
2014).
Dentro de la enfermedad de Alzheimer se establecen dos características
que permiten agrupar a los pacientes para facilitar su estudio: la edad de
comienzo (mayor o menor a 65 años) y la presencia o no de agregación familiar
(existe agregación familiar si dos o más familiares de primer grado han padecido o
padecen enfermedad de Alzheimer) (Rodríguez, Gutiérrez & Fernandos, 2014).
La forma más frecuente de la enfermedad de Alzheimer es la de inicio
tardío sin agregación familiar, seguida de la de inicio tardío con agregación
familiar. Ambas representan el 98% de todos los casos de EA. Dentro de los casos
de inicio precoz se encuentra a su vez formas con o sin agregación familiar,
ambas muy raras.
La heterogeneidad clínica – por ejemplo, en edad de inicio, ritmo de
progresión de la enfermedad, tipo de deterioro cognoscitivo y de síntomas
psiquiátricos es el mayor obstáculo para el diagnóstico de la enfermedad de
Alzheimer. El diagnóstico de la EA exige la presencia de un cuadro clínico similar
al descrito y la confirmación anatomopatológica de la enfermedad (Jurado, Mataró
& Pueyo, 2013).
Con el diagnóstico clínico y la exclusión de otras causas de demencia se
consigue una fiabilidad diagnóstica confirmada por la autopsia del 85%-90%. En la
actualidad existen tres criterios de diagnóstico ampliamente reconocidos: los de la
clasificación internacional CIE-10, los del DSM-IV-TR y los criterios NINCDS-
ADRDA12.
Demencia con cuerpos de Lewy
La Demencia con cuerpos de Lewy (DCL) es una entidad clínico-patológica
descrita recientemente. Sus principales características clínicas son el deterioro
mental, parkinsonismo de intensidad variable, rasgos psicóticos como las
alucinaciones visuales (AV), y fluctuaciones cognitivas que afectan especialmente
a la atención y concentración (Rodríguez, Gutiérrez & Fernandos, 2014).
Hasta la aparición en 1996 de los criterios diagnósticos del Taller
Internacional del Consorcio para la Demencia con Cuerpos de Lewy, los casos de
DCL solían ser erróneamente clasificados como enfermedad de Alzheimer (EA),
enfermedad de Parkinson (EP) o la superposición de ambas (Rodríguez, Gutiérrez
& Fernandos, 2014).
Aún hoy la DCL es infradiagnosticada clínicamente. Constituye más del
10% de todos los casos de demencia que llegan a la necropsia, pero los estudios
de muestras clínicas informan que sólo alrededor de un 5% tienen el síndrome de
DCL.
No hay datos epidemiológicos fiables, pues no hay estudios poblacionales
de esta entidad, pero en las series anatomopatológicas recientes la DCL podría
constituir del 10% al 36% de las demencias, sólo sobrepasada por la EA, a la que
frecuentemente se asocia. La edad de comienzo de la DCL suele ser entre los 70
y los 80 años, como ocurre con otras demencias degenerativas (Romero &
Carrión, 2014).
Algunos estudios longitudinales registran un curso evolutivo más rápido y
un peor pronóstico que el de la EA, con una duración de la enfermedad menor
para la DCL, mientras que otros estudios no encuentran diferencias significativas
en este aspecto. En casi todas las series predomina el sexo masculino.
Aunque la mayor parte de la DCL es esporádica, hay unas cuantas familias
en las que DCL y EP están determinadas genéticamente por anormalidades en el
gen de la α-sinucleína, la proteína que se cree que está más implicada en la
formación de los cuerpos de Lewy. El gen puede tener una mutación, o presentar
secuencias de repetición (duplicación o triplicación). (Romero & Carrión, 2014).
La presentación en tales familias puede ser tanto de EP como de DCL,
aportando una fuerte evidencia de que estos dos trastornos comparten una base
común. Las familias con una duplicación del gen solo tienen EP, sugiriendo que
hay un efecto "dosis-dependiente", o sea que se requiere una mayor
sobreproducción de α-sinucleína para desarrollar una histopatología cortical
extensa que produzca demencia. El hallazgo histológico definitorio de la DCL es
la presencia en las neuronas corticales de los denominados cuerpos de Lewy
(CL), inclusiones citoplasmáticas eosinófilas y redondeadas cuyo principal
componente es la a-sinucleína, además de ubiquitina y proteínas de
neurofilamento. Aparecen también abundantes placas de amiloide (como las de la
enfermedad de Alzheimer), y escasos ovillos neurofibrilares. (Romero & Carrión,
2014).
Los CL fueron descritos por primera vez Forster y Lewy in 1912 en el tronco
cerebral de pacientes con la entonces llamada parálisis agitans (la EP). Más tarde,
Hassler describió los CL corticales en la EP, pero no fue hasta 1961 en que
Okazaki discutió acerca de su posible papel en asociación con demencia (Romero
& Carrión, 2014).
Los CL corticales son difíciles de detectar microscópicamente con las
técnicas convencionales de hematoxilina-eosina, razón por la cual sólo se
publicaron unos pocos casos antes de los años 80 .El desarrollo de métodos de
tinción inmunocitoquímica con anticuerpos, primero frente a la ubicuitina y más
recientemente frente a la α-sinucleína, son los que han facilitado la visualización
cortical de los CL, estimulando con ello la investigación dentro del espectro de los
diferentes trastornos con CL (p.e. la EP con y sin demencia, y la DCL). (Romero &
Carrión, 2014).
Los CL clásicos, definitorios de la EP, se localizan en las neuronas
monoaminérgicas de la sustancia negra y en otros núcleos del tronco cerebral y
diencéfalo. Tienen un centro denso eosinófilo, hialino, a veces laminado, y un halo
más claro.
Los CL corticales, en cambio, tienen un contenido proteico fibrilar y lipídico
muy similar al de los CL clásicos pero totalmente homogéneo, con propiedades
histoquímicas como las del halo de aquellos, y su inmunorreactividad es algo
diferente. Se distribuyen especialmente por el sistema límbico, áreas de
asociación del neocórtex, diencéfalo y tronco encefálico.
Tan solo alrededor del 10-20% de los casos de DCL son "puros", es decir,
sin otra histopatología acompañante - estos pacientes son probablemente más
jóvenes y más parkinsonianos. Pero los casos puros de DCL pueden tener un
"pleno" de síntomas de DCL, lo que sugiere que la histopatología de cuerpos de
Lewy por sí sola es causa suficiente para la formación de los síntomas.
Otro 10-20% de casos presenta suficiente patología de placas y ovillos
(estadios de Braak V y VI) como para ser acreedor de un diagnóstico
histopatológico concomitante de EA. Estos pacientes tienen muchas más
posibilidades de parecer clínicamente una EA, con índices bajos de las tres
características centrales (AV, fluctuación y parkinsonismo) mediante las cuales los
clínicos tratan de identificar a la DCL. Probablemente, esta es la razón principal
del infradiagnóstico de la DCL referido anteriormente.
La mayoría de los casos de DCL tiene alguna histopatología del tipo
Alzheimer, habitualmente placas de amiloide neocorticales e hipocámpicas. La
mayor parte de estos casos tendrá las características clínicas típicas de la DCL.
Además de todo esto, se tiene que considerar la contribución de la
histopatología vascular que podemos encontrar en hasta un 30% de casos de
DCL. Esto puede modificar de nuevo el cuadro clínico, ya sea en términos de
forma de comienzo y progresión, o de presencia de signos y síntomas focales.
Los estudios de neuroimagen demuestran en comparación con la EA, la
atrofia del lóbulo temporal es menos pronunciada en la DCL, mientras que la
atrofia cerebral difusa (con su correspondiente dilatación ventricular ex vacuo) y
las intensidades periventriculares y de la sustancia blanca tampoco diferencian la
DLB de la EA o de la Demencia Vascular (DV). Los estudios de neuroimagen
funcional con SPECT y PET han mostrado una hipoactividad parietotemporal
similar en la EA y en la DCL, mientras que la hipoactividad occipital es más
pronunciada en la DCL.
La función dopaminérgina nigroestriatal puede visualizarse mediante
trazadores específicos para los transportadores presinápticos de la dopamina
(p.e., mediante el carboximetoxi-yodofenil-tropano [CIT]-SPECT o PET). Estudios
recientes que han utilizado este método han encontrado una función
dopaminérgica gravemente deteriorada en la DCL, anormalidad que comparte con
la EP pero no con la EA. Estos hallazgos sugieren que el CIT-SPECT podría ser
especialmente útil en el futuro en el diagnóstico diferencial entere EA y DCL
(Romero & Carrión, 2014).
Inicialmente esta demencia suele ser diagnosticada como EA o DV pero,
posteriormente y ante la presencia de síntomas parkinsonianos, el clínico la
clasifica como DCL. En otros casos, los pacientes presentan inicialmente síntomas
clásicos de la Enfermedad de Parkinson (EP) y más tarde desarrollan la demencia;
solo una minoría de pacientes presenta inicialmente los síntomas de ambos
trastornos (Romero & Carrión, 2014).
Inicialmente esta demencia suele ser diagnosticada como EA o DV pero,
posteriormente y ante la presencia de síntomas parkinsonianos, el clínico la
clasifica como DCL (Romero & Carrión, 2014).
En otros casos, los pacientes presentan inicialmente síntomas clásicos de
la Enfermedad de Parkinson (EP) y más tarde desarrollan la demencia; solo una
minoría de pacientes presenta inicialmente los síntomas de ambos trastornos.
Criterios del Taller Internacional del Consorcio para la DCL
Criterio Esencial: Demencia de curso progresivo, en la que la alteración de
la memoria puede no ser evidente en las fases iniciales. Destacan las alteraciones
de la atención y de las funciones frontosubcorticales y visuoespaciales.
Dos de las siguientes características definen un diagnóstico de demencia
con cuerpos de Lewy probable, y la presencia de una sola de ellas indica el
diagnóstico de demencia con cuerpos de Lewy posible:
• Fluctuación de la capacidad cognoscitiva con variaciones importantes
de la atención y del estado de alerta.
• Alucinaciones visuales recurrentes bien formadas y detalladas
• Signos motores espontáneos de parkinsonismo.
Características que apoyan el diagnóstico:
• Caídas repetidas
• Síncopes
• Pérdidas de consciencia transitorias
• Sensibilidad marcada a los neurolépticos
• Delirios sistematizados
• Alucinaciones no visuales
El diagnóstico de demencia con cuerpos de Lewy es menos probable en
presencia de:
• Enfermedad vascular cerebral, con signos neurológicos focales o
lesiones vasculares en técnicas de neuroimagen.
• Evidencia de otra enfermedad neurológica o sistémica que pudiese
justificar el cuadro clínico.
Sus rasgos clínicos más importantes vienen descritos en los criterios del
Taller Internacional del Consorcio para la Demencia con Cuerpos de Lewy, que se
describen en la tabla adjunta.
Son también frecuentes la atención lábil, la lentitud del pensamiento, la
hipersomnia diurna, los estados de ausencia, los defectos ejecutivos y,
especialmente, los defectos visuoespaciales y visuoconstructivos. A menudo el
"insight" está preservado, a diferencia de los casos de EA.
Las fluctuaciones del rendimiento cognitivo se presentan de un día para otro
o incluso en el mismo día, y son frecuentes los cuadros confusionales de origen
desconocido, no atribuibles a factores externos ni médicos definidos.
Los signos parkinsonianos son, quizá, el rasgo más característico de la
DCL. En algunos casos preceden a la demencia, de forma sutil o notoria, y los
pacientes son diagnosticados durante meses o años de EP, con respuesta escasa
y transitoria a la L-Dopa. Predomina la rigidez, que aparece precozmente en más
de la mitad de los casos, pero son también frecuentes la bradicinesia, la amimia,
los trastornos de la postura, marcha y reflejos posturales y, en menor medida, la
hipofonía y el temblor. Estos rasgos pueden darse también en la EA, pero son más
leves y tardíos y a veces asociados a CL corticales (Vaamonde, Flores, Ibañez,
Gudin & Hérnandez, 2005).
Las diferencias entre el parkinsonismo de la DCL y de la EP son escasas: el
carácter simétrico, escaso temblor y poca respuesta al tratamiento con L-Dopa. Se
aconseja no utilizar el diagnóstico de DCL cuando el parkinsonismo precede a la
demencia en más de un año, calificándose estos casos de enfermedad de
Parkinson con demencia (Vaamonde, Flores, Ibañez, Gudin & Hérnandez, 2005).
El rasgo psicótico más claro es la presencia de AV, típicamente complejas y
muy elaboradas, y de presentación precoz. A veces las alucinaciones se
acompañan de delirios, especialmente del tipo persecutorio, muy establecidos,
elaborados y de fuerte contenido, a diferencia de los pobremente formados de la
EA (Vaamonde, Flores, Ibañez, Gudin & Hérnandez, 2005).
Los defectos en la percepción visual (distorsiones de tamaño, forma,
movimiento o color), en combinación con defectos generales como escasa luz
externa, confusión y deterioro cognitivo, juegan un papel clave en el desarrollo de
las alucinaciones visuales, las identificaciones erróneas delirantes, las agnosias
visuales y las incapacidades visuoconstructivas características de la DCL
(Vaamonde, Flores, Ibañez, Gudin & Hérnandez, 2005).
La mezcla de características clínicas y su orden de aparición en el curso de
la enfermedad pueden variar de paciente a paciente, dependiendo de dónde estén
localizadas predominantemente las lesiones neuropatológicas. Por ejemplo, los
pacientes con signos extrapiramidales precoces y prominentes muestran cambios
nigroestriatales prominentes, mientras que aquellos con alucinaciones y deterioro
cognoscitivo tempranos tienen una pronunciada participación cortical o del sistema
límbico (Vaamonde, Flores, Ibañez, Gudin & Hérnandez, 2005).
De la misma manera, los pacientes con DCL con inestabilidad postural y
caídas muy frecuentes presentan lesiones neuropatológicas de la enfermedad en
médula espinal y ganglios simpáticos y parasimpáticos. La duración media de la
enfermedad es de 5 ó 6 años (con un rango de 2 a 20 años), y el ritmo de
progresión viene a ser de unos 4 ó 5 puntos al año en el MMSE (Mini Mental State
Examination) de Folstein (Vaamonde, Flores, Ibañez, Gudin & Hérnandez, 2005).
En comparación con controles sanos, la función cognoscitiva de los
pacientes con DCL está deteriorada en todas las áreas cognitivas, con gran
variabilidad. En comparación con la EA, los pacientes con DCL pueden mostrar un
deterioro menos grave de la memoria, pero más discapacidad visuoperceptiva,
visuoespacial (como en los pacientes con EP), y constructiva (Romero & Carrión,
2014).
Los pacientes con DCL (al igual que los que padecen EA) sufren una clara
afectación de la memoria semántica. Los pacientes con DCL en particular tienen
problemas cuando tienen que extraer el significado de imágenes, lo que muy
probablemente se debe a una combinación de deterioros semántico y
visuoperceptivo (Romero & Carrión, 2014).
No existe un patrón neuropsicológico único de deterioro cognitivo que
pueda diferenciar claramente a la DCL de la EA en un paciente, y tanto las
fluctuaciones de la atención como los síntomas neuropsiquiátricos o los signos
extrapiramidales pueden interferir con los tests neuropsicológicos (Romero &
Carrión, 2014).
Aunque se puede afirmar que, las fluctuaciones cognitivas en la D-CL son
parecidas al delirium aunque sin factores precipitantes identificables. Estas
fluctuaciones pueden manifestarse de distintas maneras: períodos de confusión-
lucidez, disminución marcada del arousal o largos períodos de somnolencia diurna
(Romero & Carrión, 2014).
Estas variaciones pueden observarse de minuto a minuto o de semana en
semana. A pesar de que las fluctuaciones cognitivas hayan sido consideradas
como uno de los criterios básicos para el diagnóstico de D-CL, no todos los
pacientes las presentan y pueden observarse en alguna de sus formas en otras
demencias, por lo que es importante realizar una entrevista detallada y una
adecuada observación durante la evaluación. Ferman y Boeve (2007, en Romero
& Carrión, 2014). identifican cuatro rasgos distintivos de las fluctuaciones en la
DCL:
1. Somnolencia durante el día y letargo; 2. Siestas durante el día de dos o
más horas; 3. Mirar al vacío durante largos períodos; y 4. Episodios de ideas
desorganizadas, poco claras o ilógicas. La presencia de tres o cuatro rasgos tiene
un valor predictivo positivo del 83% para el diagnóstico clínico de la D-CL respecto
al diagnóstico de EA (Ferman y Boeve, 2007, en Romero & Carrion, 2014).
Existe una gran complejidad en cuanto al correcto diagnóstico del cuadro,
ya que el diagnóstico tiene implicaciones terapéuticas y pronósticos importantes.
Por ello es fundamental realizar un diagnóstico diferencial apropiado. El
diagnóstico diferencial de este cuadro clínico es muy complejo debido al
solapamiento entre DCL y Enfermedad de Alzheimer; existe una gran proporción
de pacientes que cumple criterios clínicos tanto de una como de otra, pero
fundamentalmente las dificultades en el diagnóstico aparecen en los primeros
estadios de la enfermedad (Blanc, 2013, en Romero & Carrión, 2014).
Referencias
Rodríguez, L., Gutiérrez J., & Fernando R. (2014). Demencias y enfermedad de
Alzheimer en America latina y el Caribe. Revista Cubana de Salud Pública,
3, 20-34.
Cacabelos R. (2001). Enfermedad de Alzheimer: presente terapéutico y retos
futuros. Revista Colombiana de Psiauiatría, 3(30), 2015-238.
Fontan, L. (2012). La Enfermedad de Alzheimer: elementos para el diagnóstico y
manejo clínico en el consultorio. Biomedicina, 7(4), 34-41.
Instituto Nacional de Trastornos Neurológicos y Accidentes Cerebrovasculares.
(2018). La esperanza en la investigación. Maryland: Novarts
Romero C. & Carrión L. (2014). Demencias por cuerpo de Lewy: un síndrome
clínico difícil de identificar. Revista Iberoamericana de Psicosomática, 110,
11-17.
Jurado A., Mataró, M., & Pueyo, R. (2013). Neuropsicología de las enfermedades
neurodegenerativas. España: Editorial Síntesis.
Vaamonde-Gamo J, Flores -Barragán JM, Ibáñez R, Gudín M, Hernández A.
(2005). DaT-SCAN SPECT en el diagnóstico diferencial entre demencia por
cuerpos de Lewy y enfermedad de Alzheimer. Revista de Neurología. 41
(5), 257-279.
Вам также может понравиться
- Neuropatia Diabetica - PPTX FinalДокумент61 страницаNeuropatia Diabetica - PPTX FinalYenii López100% (1)
- Peabody. Manual PDFДокумент101 страницаPeabody. Manual PDFWilly Torres100% (1)
- Lesión Medular IncompletaДокумент42 страницыLesión Medular IncompletaLiliana Araya Olmos67% (6)
- Demencia Senil Caso ClinicoДокумент27 страницDemencia Senil Caso ClinicoEduardo Dávila60% (5)
- Neuropsicología InvolutivaДокумент11 страницNeuropsicología InvolutivaRene Crespo0% (1)
- Caso Clinico Alzheimer PDFДокумент9 страницCaso Clinico Alzheimer PDFLaura DanielaОценок пока нет
- Historia NeurologicaДокумент10 страницHistoria Neurologicareynaldo100% (2)
- Sindromes ProtuberancialesДокумент2 страницыSindromes ProtuberancialesAlfredo Luis Arana Maquera100% (2)
- Trastorno Psicotico Debido A Otra Afeccion MedicaДокумент3 страницыTrastorno Psicotico Debido A Otra Afeccion MedicaBessy Toledo100% (1)
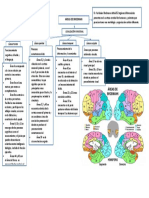
- Areas-de-Brodmann Del Cerebro EsquemaДокумент1 страницаAreas-de-Brodmann Del Cerebro EsquemaHeyner50% (2)
- Prueba 5 Derechos y DeberesДокумент3 страницыPrueba 5 Derechos y DeberesDany Galindo Sánchez78% (32)
- Demencia PDFДокумент3 страницыDemencia PDFAngel Martin100% (1)
- Demencia - MonografíaДокумент49 страницDemencia - Monografíacris07088475% (4)
- Expo Dermato Queratosis Seborreica 2Документ13 страницExpo Dermato Queratosis Seborreica 2Monikita Castro ArteagaОценок пока нет
- Envejecimiento Normal - Patologico (Neuropsicologia II)Документ49 страницEnvejecimiento Normal - Patologico (Neuropsicologia II)alejandra100% (7)
- Sindrome de La Arteria Cerebral MediaДокумент10 страницSindrome de La Arteria Cerebral MediaJesus Chaves0% (1)
- Sindromes LobaresДокумент35 страницSindromes LobaresEdgar Camilo Villa Martinez100% (2)
- Síndrome PrefrontalДокумент13 страницSíndrome PrefrontalSaddayОценок пока нет
- Farmacología de Los Tranquilizantes Mayores o NeurolépticosДокумент4 страницыFarmacología de Los Tranquilizantes Mayores o NeurolépticosJose David Gonzaga Muñoz100% (5)
- Síndromes HemisféricosДокумент37 страницSíndromes HemisféricosEmilio Sarao100% (3)
- Psicopatologia de La InteligenciaДокумент11 страницPsicopatologia de La InteligenciaRosa Montaño Del Alcázar83% (6)
- ANORMALIDADES DE LA VOLUNTAD, CONCIENCIA y CONCIENCIA DEL YOДокумент35 страницANORMALIDADES DE LA VOLUNTAD, CONCIENCIA y CONCIENCIA DEL YOsol100% (1)
- Resmen Manual de Semiologia PsiquiatricaДокумент22 страницыResmen Manual de Semiologia PsiquiatricaKaren RoseroОценок пока нет
- Qué Es Labilidad EmocionalДокумент11 страницQué Es Labilidad EmocionalCarol IsabelОценок пока нет
- Evaluacion Del InsightДокумент1 страницаEvaluacion Del InsightCristhian CanoОценок пока нет
- Updrs (Unified Parkinson's Disease Rating Scale)Документ16 страницUpdrs (Unified Parkinson's Disease Rating Scale)Gabriel Fco Aranda CastilloОценок пока нет
- De MenciaДокумент37 страницDe MenciaLeidy Johana Muñoz ChavezОценок пока нет
- Síndrome Centromedular: Nayma Lera RodríguezДокумент11 страницSíndrome Centromedular: Nayma Lera RodríguezEDGAR ULISES ROMERO VAZQUEZОценок пока нет
- Retraso Mental Informe EscritoДокумент20 страницRetraso Mental Informe EscritoThina Aranibar D.100% (1)
- Hemisección de La Médula EspinalДокумент12 страницHemisección de La Médula Espinalamanda50% (2)
- Trastornos NeurocognitivosДокумент21 страницаTrastornos NeurocognitivosPatrick Luis Rengifo Vargas100% (1)
- Historia Clinica PsiquiatricaДокумент9 страницHistoria Clinica PsiquiatricaNikol Natalia100% (1)
- Test-Escala de Depresión Geriátrica de Yesavage (30 Items) PDFДокумент1 страницаTest-Escala de Depresión Geriátrica de Yesavage (30 Items) PDFMaria Clara Ronqui100% (1)
- Síndrome de AntonДокумент6 страницSíndrome de AntonAnonymous dw49hZmОценок пока нет
- DemenciaДокумент12 страницDemenciayosladis ramirezОценок пока нет
- Síndrome Orgánico CerebralДокумент5 страницSíndrome Orgánico Cerebraljulio100% (1)
- Deterioro CognitivoДокумент12 страницDeterioro CognitivoCesar Augusto Perez Aguilar100% (2)
- Alteraciones de La AfectividadДокумент4 страницыAlteraciones de La AfectividadLilibeth ZambranoОценок пока нет
- Escala de Coma de GlasgowДокумент3 страницыEscala de Coma de GlasgowJohana Alejandra García LunaОценок пока нет
- Escala de Valoracion Sociofamiliar GijónДокумент1 страницаEscala de Valoracion Sociofamiliar GijónJuan Francisco Herrera AlarcónОценок пока нет
- Escala Unificada ParkinsonДокумент8 страницEscala Unificada ParkinsonMiliОценок пока нет
- Esquizofrenia Paranoide SintomasДокумент40 страницEsquizofrenia Paranoide SintomasMariaCambierОценок пока нет
- Valoración Geriátrica IntegralДокумент17 страницValoración Geriátrica Integraldaniel gonzalo moreira montesdeoca100% (1)
- Qué Es La PsicosisДокумент5 страницQué Es La Psicosisandrea alvarez del villar villegas100% (2)
- Areas de BrodmanДокумент5 страницAreas de BrodmanPia Torres0% (1)
- Sensopercepción PsiquiatriaДокумент21 страницаSensopercepción PsiquiatriaSalud Mental Universidad CatolicaОценок пока нет
- Capítulo 5 - La Conducta de Enfermedad - 2c Rodríguez-MarínДокумент13 страницCapítulo 5 - La Conducta de Enfermedad - 2c Rodríguez-Maríningrit100% (3)
- Diferencias Entre Deterioro y PseudodeterioroДокумент4 страницыDiferencias Entre Deterioro y PseudodeterioroDavid GomezОценок пока нет
- Examen Mental C.E.P.BДокумент3 страницыExamen Mental C.E.P.BJadith Jesus Ezaine GutierrezОценок пока нет
- Sindromes LobaresДокумент11 страницSindromes LobaresNepcis 02100% (1)
- Examen NeurologicoДокумент36 страницExamen NeurologicoJennifer CruzОценок пока нет
- Trastorno Neurocognitivo MayorДокумент11 страницTrastorno Neurocognitivo MayorBenjamin Onfray100% (1)
- Los 8 Tipos de Discapacidad AuditivaДокумент10 страницLos 8 Tipos de Discapacidad AuditivaismariОценок пока нет
- Conciencia, Orientación y AtenciónДокумент34 страницыConciencia, Orientación y AtenciónMiguel Lopez100% (1)
- EXAMEN MENTAL COMPLETOdocxДокумент40 страницEXAMEN MENTAL COMPLETOdocxFrancis Abdala100% (4)
- Escala Funcional ElaДокумент6 страницEscala Funcional ElaElena Olmo Valderrama100% (1)
- Análisis Película "El Paciente"Документ5 страницAnálisis Película "El Paciente"Luisa ArroyoОценок пока нет
- Síndrome de Deterioro de Funciones MentalesДокумент7 страницSíndrome de Deterioro de Funciones MentalesRuth Cobo RosalesОценок пока нет
- La LisencefaliaДокумент2 страницыLa LisencefaliaMi CrecerОценок пока нет
- Síndromes PsicopatológicosДокумент6 страницSíndromes PsicopatológicosgadricaОценок пока нет
- Definicion de Sustrato Encefalico y Alteraciones en La Conciencia y OrientacionДокумент3 страницыDefinicion de Sustrato Encefalico y Alteraciones en La Conciencia y Orientacionmilagroscastrogonzal100% (1)
- 20 Demencia ClasificacionesДокумент29 страниц20 Demencia ClasificacionesDaniela AndreottiОценок пока нет
- Protocolo Regreso A Clases 22-23 26 - AgostoДокумент13 страницProtocolo Regreso A Clases 22-23 26 - AgostoWilly TorresОценок пока нет
- 2018 Tesis Chaparro Castañeda Paula AndreaДокумент128 страниц2018 Tesis Chaparro Castañeda Paula AndreaWilly TorresОценок пока нет
- Adobe Scan 27 Feb. 2022Документ1 страницаAdobe Scan 27 Feb. 2022Willy TorresОценок пока нет
- Desempeno en Memoria de Trabajo e Indicadores CompДокумент20 страницDesempeno en Memoria de Trabajo e Indicadores CompWilly TorresОценок пока нет
- Dietra Paleo FitfightersДокумент15 страницDietra Paleo FitfightersWilly TorresОценок пока нет
- Ejemplo Informe Final CAMДокумент2 страницыEjemplo Informe Final CAMWilly TorresОценок пока нет
- Etapas de Desarrollo CognitivoДокумент3 страницыEtapas de Desarrollo CognitivoWilly TorresОценок пока нет
- Áreas de BrodmannДокумент5 страницÁreas de BrodmannWilly TorresОценок пока нет
- DemenciasДокумент17 страницDemenciasWilly TorresОценок пока нет
- Cuestionario Sindromes NeuropsicológicosДокумент16 страницCuestionario Sindromes NeuropsicológicosWilly TorresОценок пока нет
- Conoce El ABC CPV PDFДокумент14 страницConoce El ABC CPV PDFWilly TorresОценок пока нет
- 2 Instrumento Maestro de ApoyoДокумент9 страниц2 Instrumento Maestro de ApoyoWilly Torres100% (1)
- Cuadro Comparativo Piaget Vigostky y SternДокумент3 страницыCuadro Comparativo Piaget Vigostky y SternZullyZamboni100% (2)
- Fase 1 Presentación de La Propuesta - Mapa ConceptualДокумент2 страницыFase 1 Presentación de La Propuesta - Mapa Conceptualandrea clavijoОценок пока нет
- Anual: Mara Yasmina Norabuena CrisoloДокумент41 страницаAnual: Mara Yasmina Norabuena CrisoloJhonatan FigueroaОценок пока нет
- Guia Primer Periodo Grado Decimo 2020Документ13 страницGuia Primer Periodo Grado Decimo 2020hero store loricaОценок пока нет
- DIA 3 SESION DE APRENDIZAJE Elaboramos La Receta de Un Plato TípicoДокумент6 страницDIA 3 SESION DE APRENDIZAJE Elaboramos La Receta de Un Plato TípicoVICTOR JOSE GARCIA GARCIA80% (5)
- Epistemologia de Las Ciencias de La Educacion y La Pedagogia - Rolando BarralДокумент31 страницаEpistemologia de Las Ciencias de La Educacion y La Pedagogia - Rolando BarralPaul VirúОценок пока нет
- Resumen Manual de ConvivenciaДокумент70 страницResumen Manual de ConvivenciaLaura Santana UrielОценок пока нет
- Mapa de ManifestaciónДокумент2 страницыMapa de ManifestaciónAnahata Poder divinoОценок пока нет
- Enseñanza y Aprendizaje de Solidos Geométricos Desde La Perspectiva de La DiscapacidadДокумент86 страницEnseñanza y Aprendizaje de Solidos Geométricos Desde La Perspectiva de La DiscapacidadMartha RamirezОценок пока нет
- Cuadro Comparativo Principales TeoriasДокумент10 страницCuadro Comparativo Principales TeoriasMargarita Gonzalez DavilaОценок пока нет
- Actividad 30 Junio - 5 AñosДокумент6 страницActividad 30 Junio - 5 AñosNora Violeta Saldaña SalazarОценок пока нет
- Aprendizajes Fundamentales TecnologíaДокумент2 страницыAprendizajes Fundamentales TecnologíaWendoly AltamiranoОценок пока нет
- Bruno DiazДокумент5 страницBruno DiazBalin MathuzОценок пока нет
- 1750 8586 2 PBДокумент20 страниц1750 8586 2 PBkimberli espinozaОценок пока нет
- Clases de Métodos y Técnicas de InvestigaciónДокумент3 страницыClases de Métodos y Técnicas de InvestigaciónNayra MuñozОценок пока нет
- Ser CatequistaДокумент2 страницыSer CatequistaWilliam F. TorresОценок пока нет
- Fasciculo3 Orientaciones para DocentesДокумент12 страницFasciculo3 Orientaciones para DocentesKenyerth Thomas Peña VargasОценок пока нет
- Infografía Psicología EducativaДокумент3 страницыInfografía Psicología EducativaEdna PatiñoОценок пока нет
- 3ero Unidad 1 ElementalДокумент14 страниц3ero Unidad 1 ElementalRudi SantosОценок пока нет
- SiProfe Didactica MatematicasДокумент223 страницыSiProfe Didactica Matematicasmariella1250% (2)
- Evaluación Diagnóstica Ept 2ºДокумент4 страницыEvaluación Diagnóstica Ept 2ºHancy Castillo GonzalesОценок пока нет
- Informe de Seguimiento Pedagógico Trimestral Del Alumno: - Datos de IdentificaciónДокумент3 страницыInforme de Seguimiento Pedagógico Trimestral Del Alumno: - Datos de IdentificaciónL Vane FloresОценок пока нет
- Jefe de Desarrollo de SistemasДокумент4 страницыJefe de Desarrollo de SistemasEver Ibiza Berrios AguilarОценок пока нет
- CORREO No. 0855. JURIDICO - PROGRAMA SEGURO ESCOLAR CONTRA ACCIDENTES, PARA EL PERIODO CORRESPONDIENTE AL CICLO ESCOLAR 2023-2024.Документ1 страницаCORREO No. 0855. JURIDICO - PROGRAMA SEGURO ESCOLAR CONTRA ACCIDENTES, PARA EL PERIODO CORRESPONDIENTE AL CICLO ESCOLAR 2023-2024.15EJN0057I J018Оценок пока нет
- Monografia Alzeimer Alzheimer FinalДокумент18 страницMonografia Alzeimer Alzheimer FinalAdolfo Ferruzo BaldeonОценок пока нет
- Proyecto Estructuras de PapelДокумент3 страницыProyecto Estructuras de PapelNancy BertucciОценок пока нет
- Catalogo Iluminacion 2009 2010 LowДокумент110 страницCatalogo Iluminacion 2009 2010 LowCésar FriendОценок пока нет
- Syllabus Del Curso Cálculo IntegralДокумент14 страницSyllabus Del Curso Cálculo IntegralSandra Constanza DavidОценок пока нет