Академический Документы
Профессиональный Документы
Культура Документы
Espectroscopía
Загружено:
reynaHdez0 оценок0% нашли этот документ полезным (0 голосов)
51 просмотров5 страницEspectroscopía
Авторское право
© © All Rights Reserved
Доступные форматы
DOCX, PDF, TXT или читайте онлайн в Scribd
Поделиться этим документом
Поделиться или встроить документ
Этот документ был вам полезен?
Это неприемлемый материал?
Пожаловаться на этот документEspectroscopía
Авторское право:
© All Rights Reserved
Доступные форматы
Скачайте в формате DOCX, PDF, TXT или читайте онлайн в Scribd
0 оценок0% нашли этот документ полезным (0 голосов)
51 просмотров5 страницEspectroscopía
Загружено:
reynaHdezEspectroscopía
Авторское право:
© All Rights Reserved
Доступные форматы
Скачайте в формате DOCX, PDF, TXT или читайте онлайн в Scribd
Вы находитесь на странице: 1из 5
“Espectroscopía”.
La espectroscopía es una técnica de análisis que se basa en la absorción de radiación por
parte de las moléculas. Aunque existen muchos tipos de espectroscopia, las más utilizadas
en química orgánica se agrupan en cuatro categorías:
Espectroscopía de resonancia magnética nuclear (RMN).
Espectroscopía de infrarrojo.
Espectroscopia de ultravioleta.
Espectrometría de masas.
Espectroscopía Infrarroja (IR).
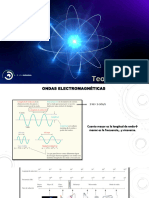
La región del infrarrojo del espectro corresponde a frecuencias que van desde 8 x 10-5 cm
a 8 x 10-2 cm. Los aparatos de Infrarrojo trabajan a la mitad de esta región que corresponde
a energías que van desde 1.1 hasta 11 kcal/mol. Los fotones que transporta la radiación
infrarroja no tienen energía suficiente para provocar transiciones electrónicas, pero si
pueden conseguir vibraciones de los enlaces covalentes de las moléculas orgánicas. La
energía necesaria para provocar una transición vibracional depende del tipo de átomos y
del tipo de enlace que los mantiene unidos.
Los átomos no se encuentran estáticos dentro de una molécula, sino que están en
movimiento constante unos respecto a otros, vibrando en torno a los enlaces que los unen
a frecuencias constantes. A medida que los átomos se acercan unos a otros las fuerzas de
repulsión aumentan y conforme se separan las interacciones de atracción disminuyen. Este
movimiento de alargamiento y compresión alternantes (tensión) se parece al de dos esferas
sujetas por un muelle.
Tipos de Vibraciones:
Podemos imaginar la vibración de dos átomos enlazados, H y Cl, como dos pesas unidas
por un muelle que se estira y se contrae a una frecuencia υ. Según este modelo, la
frecuencia de vibración de los dos átomos depende tanto de la fuerza del enlace como de
sus pesos atómicos. De hecho, se ha demostrado que cumple la ley de Hooke, que explica
el movimiento de un muelle.
Cuando dos átomos de masa atómica diferente están unidos por un enlace, el átomo ligero
se aleja más que el de mayor masa. La absorción de energía infrarroja da por resultado un
aumento en la frecuencia de vibración. Por ejemplo, en el grupo metileno (-CH2-) del
propano (CH3CH2CH3) los dos enlaces C-H del metileno pueden alargarse o contraerse de
manera simétrica o no simétrica:
Tensión simétrica. Los dos átomos exteriores se alejan y se acercan al
centro de forma simultánea.
Tensión asimétrica. Uno de los átomos se acerca al
centro mientras el otro se aleja. Además del estiramiento y comprensión
del enlace hay otros modos vibracionales como el que provoca un cambio
en el ángulo de enlace (flexión). Esta flexión del enlace modifica las
posiciones relativas de dos átomos unidos a un tercero. Según sea el movimiento de dos
átomos respecto a un tercero siempre que haya cambio del ángulo de enlace pueden existir
hasta cuatro modos vibracionales de flexión: Si la flexión tiene lugar manteniendo los tres
átomos implicados en un mismo plano:
Flexión simétrica en el plano (“scissors”): En este modo de vibración el
ángulo de enlace aumenta y disminuye porque los dos átomos de los
extremos se acercan o se alejan entre ellos. Este acercamiento-alejamiento
se da en el mismo plano formado por los tres átomos. Este tipo de
movimiento se asemeja la de las tijeras cuando se abren y se cierran.
Flexión asimétrica en el plano (“rock”): En esta vibración el ángulo de
enlace aumenta y disminuye porque el átomo central se acerca a uno de
los dos extremos y por tanto se aleja del otro, manteniéndose siempre los
tres átomos en el mismo plano, Su denominación rock viene de la similitud
entre este movimiento vibracional y el movimiento de una pareja bailando
rock-and-roll.
Flexión simétrica fuera del plano (“twist”): el ángulo de enlace aumenta y
disminuye porque los dos átomos de los extremos se acercan o se alejan entre
ellos. Este acercamiento-alejamiento se da fuera del plano formado por los
tres átomos.
Flexión asimétrica fuera del plano (“wag”): el ángulo de enlace aumenta y
disminuye porque el átomo central se acerca a uno de los dos extremos y por
tanto se aleja del otro. Este movimiento del átomo central se da fuera del
plano formado por los tres átomos implicados.
Tensión de respiración. Es aquella en la cual todos los dobles enlaces del anillo aromático
se alargan y se acortan simultáneamente, (el movimiento es parecido al de la caja toráxica).
Aunque se acaba de explicar el movimiento vibracional de los enlaces por comparación con
el movimiento de un muelle hay que tener en cuenta que la similitud no es del todo exacta.
En un muelle las dos masas pueden vibrar a cualquier frecuencia y amplitud mientras que
las vibraciones de las moléculas están cuantizadas, es decir, los átomos pueden vibrar sólo
a frecuencias específicas conocidas como estados de vibración.
Absorciones características de los grupos funcionales.
Las bandas de absorción características de casi todos los grupos funcionales se encuentran
entre 4.000 y 800 cm-1. Los espectros de infrarrojo se representan como gráficas de
absorbancia frente a número de onda.
-1
El espectro de IR va de 4000-600 cm y se puede dividir en varias zonas.
4000-3500: No tiene mucha utilidad. Solamente aparecen los sobretonos de bandas
muy intensas. Si hay una banda fundamental o frecuencia doble aparece un
sobretono a una frecuencia triple o bien el segundo sobretono.
3500-2700: Aparecen las tensiones de enlace A-H, donde A es C, O, N, es decir
cualquier heteroátomo.
2700-1800: Aparecen las tensiones de los enlaces C≡C, C≡N; -C=C=C-
1800-1500: Tensiones de los dobles enlaces C=C, C=O, C=N.
1500-900: Zona dactiroscópica. Es una zona muy compleja y es difícil hacer
correlaciones. Aparecen las tensiones de C-C, C-O y C-N. También aparecen las
flexiones en el plano.
900-600: Aparecen las flexiones fuera del plano. Estas bandas no tienen tampoco
mucha utilidad excepto en los anillos aromáticos y se usa para localizas los
sustituyentes en los carbonos del anillo.
La espectroscopia infrarroja se emplea fundamentalmente en Química Orgánica como
método para la asignación funcional. La siguiente tabla muestra una lista de las bandas de
absorción características para los grupos funcionales más comunes.
Espectroscopía de Resonancia Magnética Nuclear (RMN).
La espectroscopía de resonancia magnética nuclear (RMN) es una de las técnicas de
elucidación estructural más útil de que dispone el químico orgánico. La técnica proporciona
información sobre la estructura molecular a base de examinar las propiedades magnéticas
de átomos específicos de las moléculas. La capacidad de “mirar” los núcleos de hidrogeno
(protones) ha sido de particular interés.
Hoy en día son asequibles a la mayoría de químicos instrumentos capaces de llevar a cabo
espectros de protón (1H) rutinarios. Los espectros de RMN de algunos otros núcleos
también son factibles. Los recientes avances en la tecnología de la instrumentación han
tenido como consecuencia una disponibilidad mayor de los espectros de RMN de 13C. La
combinación de espectros de RMN de 1H y 13C constituye una herramienta poderosa para
investigar los principales átomos que forman las moléculas orgánicas.
La espectroscopia de RMN fue desarrollada a finales de los años cuarenta para estudiar
los núcleos atómicos. En 1951, los químicos descubrieron que la espectroscopia de
resonancia magnética nuclear podía ser utilizada para determinar las estructuras de los
compuestos orgánicos. Esta técnica espectroscópica puede utilizarse sólo para estudiar
núcleos atómicos con un número impar de protones o neutrones (o de ambos). Esta
situación se da en los átomos de 1H, 13C, 19F y 31P. Este tipo de núcleos son
magnéticamente activos, es decir poseen espín, igual que los electrones, ya que los núcleos
poseen carga positiva y poseen un movimiento de rotación sobre un eje que hace que se
comporten como si fueran pequeños imanes.
En ausencia de campo magnético, los espines nucleares se orientan al azar. Sin embargo,
cuando una muestra se coloca en un campo magnético, tal y como se muestra en la
siguiente figura, los núcleos con espín positivo se orientan en la misma dirección del campo,
en un estado de mínima energía denominado estado de espín α, mientras que los núcleos
con espín negativo se orientan en dirección opuesta a la del campo magnético, en un estado
de mayor energía denominado estado de espín β.
Existen más núcleos en el estado de espín α que en el β pero
aunque la diferencia de población no es enorme sí que es
suficiente para establecer las bases de la espectroscopia de
RMN.
La diferencia de energía entre los dos estados de espín α y β,
depende de la fuerza del campo magnético aplicado H0.
Cuanto mayor sea el campo magnético, mayor diferencia
energética habrá entre los dos estados de espín. En la
siguiente gráfica se representa el aumento de la diferencia
energética entre los estados de espín con el aumento de la
fuerza del campo magnético.
Desplazamiento químico.
Dependiendo del entorno químico local,
los diferentes protones en una molécula
resuenan a frecuencias ligeramente
diferentes. Dado que tanto este
desplazamiento como la frecuencia de
resonancia fundamental son
directamente proporcionales a la fuerza
del campo magnético, el desplazamiento
de frecuencia se convierte en un campo
independiente de valor adimensional
conocido como desplazamiento químico.
El desplazamiento químico se reporta
como una medida relativa de algunas
frecuencias de resonancia de referencia.
(Para los núcleos 1 H, 13 C, y 29 Si, se usa como referencia el tetrametilsilano o TMS.)
Esta diferencia entre la frecuencia de la señal y la frecuencia de la referencia se divide por
la frecuencia de la señal de referencia para obtener el desplazamiento químico.
Bibliografía.
1. Tema 5. Espectroscopía y estructura.
https://www.liceoagb.es/quimiorg/docencia/textos/TEMA5.pdf
2. TEMA 10. Espectroscopia de Resonancia Magnética Nuclear.
http://www.sinorg.uji.es/Docencia/FUNDQO/TEMA10FQO.pdf
3. Stanley H. Pine. James B. Hendrickson. Donald J. Cram. George S. Hammond.
Química Orgánica. 4ta Ed. (2da Ed. en español). Mc. Graw Hill.
Вам также может понравиться
- Espectrofotometria Infrarojo PDFДокумент17 страницEspectrofotometria Infrarojo PDFJosh GiusseppeОценок пока нет
- Uso Combinado de Los Métodos Físicos de Análisis en La Determinación de Estructuras OrgánicasДокумент18 страницUso Combinado de Los Métodos Físicos de Análisis en La Determinación de Estructuras Orgánicasesteffany aguirreОценок пока нет
- Tema 5, Espectroscopía InfrarrojaДокумент7 страницTema 5, Espectroscopía InfrarrojaIan Kenneth Maciel Sandoval BarragánОценок пока нет
- Espectroscopia Infrarroja PDFДокумент19 страницEspectroscopia Infrarroja PDFDamián LMОценок пока нет
- Trabajo Espectros VibracionalesrotacionalesДокумент8 страницTrabajo Espectros VibracionalesrotacionalesALVARO ALEXIS CHOQUEJAHUA TINEOОценок пока нет
- Radiaciones EspañolДокумент14 страницRadiaciones EspañolRoberto Vieiro PérezОценок пока нет
- Espectroscopia InfrarrojoДокумент9 страницEspectroscopia InfrarrojoJonathan Correa OsorioОценок пока нет
- Lectura 1Документ88 страницLectura 1jean pierre villanueva de la cruzОценок пока нет
- Exposición QuímicaДокумент7 страницExposición QuímicaDayana SierraОценок пока нет
- Espectroscopia de InfrarrojoДокумент9 страницEspectroscopia de InfrarrojoEsteban MedinaОценок пока нет
- Resonancia Magnética NuclearДокумент8 страницResonancia Magnética NuclearerosОценок пока нет
- Espectroscopia InfrarrojaДокумент7 страницEspectroscopia InfrarrojaSilvia VázquezОценок пока нет
- Apuntes de InfrarrojoДокумент38 страницApuntes de InfrarrojoLudving MillanОценок пока нет
- Ensayo de ElectromagnetismoДокумент3 страницыEnsayo de ElectromagnetismoJesik Paolita MartinezОценок пока нет
- Unidad 1Документ14 страницUnidad 1Reynaldo SorucoОценок пока нет
- Teoría de DALTON.: Rayos CatódicosДокумент8 страницTeoría de DALTON.: Rayos Catódicosvictor MarceloОценок пока нет
- Selector de Velocidades MagnetismoДокумент8 страницSelector de Velocidades MagnetismoAnonymous vKQ099100% (3)
- RMN1Документ52 страницыRMN1InaliesОценок пока нет
- Problema de Polarizacion Rayos XДокумент4 страницыProblema de Polarizacion Rayos XEdgardo Olmedo SotomayorОценок пока нет
- Ondas electromagnéticas: frecuencia, longitud de onda y amplitudДокумент9 страницOndas electromagnéticas: frecuencia, longitud de onda y amplitudOmar RamirezОценок пока нет
- VibracionesДокумент63 страницыVibracionesStefania Herenandez MotaОценок пока нет
- Guía de QuímicaДокумент52 страницыGuía de QuímicaIrais OrtizОценок пока нет
- Química General T7-14Документ49 страницQuímica General T7-14Ilian GilОценок пока нет
- Cap. 6. Estructura Electrónica Átomos. Química I. UTNДокумент78 страницCap. 6. Estructura Electrónica Átomos. Química I. UTNJavierОценок пока нет
- Espectroscopia InfrarrojaДокумент35 страницEspectroscopia InfrarrojaLucía M. Mamani CusiatauОценок пока нет
- Informe 5. en ProgresoДокумент18 страницInforme 5. en ProgresoJESUS DAVID BOLA‹O JIMENEZОценок пока нет
- Resonancia Magnetica NuclearДокумент7 страницResonancia Magnetica Nucleareli lopezОценок пока нет
- TEMA7 Metodos EspectroscopicosДокумент11 страницTEMA7 Metodos EspectroscopicosBlanca Zamora ReynosoОценок пока нет
- ATOMOДокумент12 страницATOMOCecy pnfОценок пока нет
- AnalisisДокумент10 страницAnalisisKatia Michelle ArmentaОценок пока нет
- Resonancia ManeticaДокумент14 страницResonancia ManeticaDenisseIreneVillachicaОценок пока нет
- 10 - Resonancia MagneticaДокумент27 страниц10 - Resonancia MagneticaAntonio Gonzales0% (1)
- Espectroscopía InfrarrojaДокумент16 страницEspectroscopía InfrarrojaLaboratorioОценок пока нет
- Oscilador Anarmónico y Vibraciones AnarmónicasДокумент10 страницOscilador Anarmónico y Vibraciones AnarmónicasDanita GmmОценок пока нет
- Apuntes de Infrarrojo1Документ38 страницApuntes de Infrarrojo1Emmanuel Max EspОценок пока нет
- Resumen Equipo 2Документ6 страницResumen Equipo 2Dariana Castro AlarcónОценок пока нет
- Ondas ElectromagneticasДокумент8 страницOndas ElectromagneticasJenni CastilloОценок пока нет
- Tarea de Fisica Casi TerminadaДокумент12 страницTarea de Fisica Casi TerminadaRené De La RosaОценок пока нет
- Manual de Buenas Prácticas en LaboratoriosДокумент54 страницыManual de Buenas Prácticas en LaboratoriosNatalia MaldonadoОценок пока нет
- Espect Rosco PiaДокумент7 страницEspect Rosco PiaXavyer Nukly RidirОценок пока нет
- Relación Carga Masa Del ElectrónДокумент5 страницRelación Carga Masa Del ElectrónNeider BlancoОценок пока нет
- Oscilador ArmónicoДокумент9 страницOscilador ArmónicoLizeth parraОценок пока нет
- Analisis Examen 2 InformacionДокумент25 страницAnalisis Examen 2 InformacionCristina CarrilloОценок пока нет
- Principios Fisicos de La Resonancia Magnetica Original PDFДокумент19 страницPrincipios Fisicos de La Resonancia Magnetica Original PDFMiraldaperezОценок пока нет
- Tema 4. Quimica I - 2018Документ28 страницTema 4. Quimica I - 2018Alex TorresОценок пока нет
- Modelo de DebyeДокумент5 страницModelo de DebyeSyd BarrettОценок пока нет
- EspectrofotometriaДокумент33 страницыEspectrofotometrialuceroОценок пока нет
- Análisis Instrumental - ESPECTROFOTOMETRÍAДокумент75 страницAnálisis Instrumental - ESPECTROFOTOMETRÍAHeacker Hacker HackerОценок пока нет
- ESPECTROSCOPÍA INFRARROJO ModificadoДокумент68 страницESPECTROSCOPÍA INFRARROJO ModificadoAaron QuispeОценок пока нет
- 3-Teoría Cuántica-VfinalДокумент48 страниц3-Teoría Cuántica-VfinaljuanixgenoОценок пока нет
- La Física de La RMДокумент15 страницLa Física de La RMMicaela AlvinoОценок пока нет
- Tema 1.el Atomo Mecano-CuánticoДокумент9 страницTema 1.el Atomo Mecano-CuánticojavierОценок пока нет
- Curso de Resonancia Magnética Bioimagenes FAARDITДокумент9 страницCurso de Resonancia Magnética Bioimagenes FAARDITCesar LopezОценок пока нет
- 5.instrumentos de ObservaciónДокумент13 страниц5.instrumentos de ObservaciónMatias JuarezОценок пока нет
- Resonancia Nuclear MagnéticaДокумент39 страницResonancia Nuclear MagnéticaJuan Gallardo GarcíaОценок пока нет
- Principios Físicos de La Resonancia Magnética NuclearДокумент19 страницPrincipios Físicos de La Resonancia Magnética NuclearDolores100% (1)
- La PersonalidadДокумент28 страницLa PersonalidadreynaHdezОценок пока нет
- Etica Profesional.Документ7 страницEtica Profesional.reynaHdezОценок пока нет
- DesecaciónДокумент4 страницыDesecaciónreynaHdezОценок пока нет
- Señales Químicas Entre CélulasДокумент9 страницSeñales Químicas Entre CélulasreynaHdezОценок пока нет
- Administración Del Cambio.Документ9 страницAdministración Del Cambio.reynaHdezОценок пока нет
- Pared CelularДокумент11 страницPared CelularreynaHdezОценок пока нет
- Aislamiento de Hongos y Levaduras.Документ3 страницыAislamiento de Hongos y Levaduras.reynaHdezОценок пока нет
- El EnsayoДокумент7 страницEl EnsayoreynaHdezОценок пока нет
- Aislamiento de Hongos y Levaduras.Документ3 страницыAislamiento de Hongos y Levaduras.reynaHdezОценок пока нет
- Cuestionario de Sistema Nervioso y Músculo EsqueléticoДокумент8 страницCuestionario de Sistema Nervioso y Músculo EsqueléticoreynaHdezОценок пока нет
- Botella de LeydenДокумент2 страницыBotella de LeydenreynaHdezОценок пока нет
- ElectroimanДокумент1 страницаElectroimanreynaHdezОценок пока нет
- La Rotación ÓpticaДокумент5 страницLa Rotación ÓpticareynaHdezОценок пока нет
- Muerte CelularДокумент5 страницMuerte CelularreynaHdezОценок пока нет
- Alimentos LightДокумент5 страницAlimentos LightreynaHdezОценок пока нет
- Antecedentes de Los Alimentos Light.Документ23 страницыAntecedentes de Los Alimentos Light.reynaHdezОценок пока нет
- Realidades de Los Alimentos Light.Документ14 страницRealidades de Los Alimentos Light.reynaHdezОценок пока нет
- Instituciones Encargadas de La AlimentaciónДокумент7 страницInstituciones Encargadas de La AlimentaciónreynaHdezОценок пока нет
- Capitulo 2. - Uso Del Método Científico.Документ2 страницыCapitulo 2. - Uso Del Método Científico.reynaHdezОценок пока нет
- Calor de disolución del carbonato de sodioДокумент4 страницыCalor de disolución del carbonato de sodioreynaHdezОценок пока нет
- Antecedentes de Los Alimentos Light.Документ23 страницыAntecedentes de Los Alimentos Light.reynaHdezОценок пока нет
- Maximilien François Marie Isidore de RobespierreДокумент1 страницаMaximilien François Marie Isidore de RobespierrereynaHdezОценок пока нет
- Historia de Los LightДокумент23 страницыHistoria de Los LightreynaHdezОценок пока нет
- Muestreo de Aguas ResidualesДокумент6 страницMuestreo de Aguas ResidualesreynaHdezОценок пока нет
- Instituciones Encargadas de La AlimentaciónДокумент7 страницInstituciones Encargadas de La AlimentaciónreynaHdezОценок пока нет
- Sistemas Económicos ContemporáneosДокумент3 страницыSistemas Económicos ContemporáneosreynaHdezОценок пока нет
- Muestreo de Aguas ResidualesДокумент6 страницMuestreo de Aguas ResidualesreynaHdezОценок пока нет
- Alimentos LightДокумент5 страницAlimentos LightreynaHdezОценок пока нет
- Antecedentes de Los Alimentos Light.Документ23 страницыAntecedentes de Los Alimentos Light.reynaHdezОценок пока нет
- PDF 14 Probabilidad 4Документ14 страницPDF 14 Probabilidad 4Wilinton Rodriguez QuiñonezОценок пока нет
- Montecristi TesisДокумент58 страницMontecristi TesisCristobal Argenis CruzОценок пока нет
- 10 razones para escribir según Roland BarthesДокумент1 страница10 razones para escribir según Roland BarthesLuGarcíaОценок пока нет
- More Than HoneyДокумент11 страницMore Than HoneyCarlosОценок пока нет
- Catalogo KairosДокумент21 страницаCatalogo KairosNora StephensОценок пока нет
- ACTIVIDAD FINAL - Análisis de Mis Habilidades ComunicativasДокумент7 страницACTIVIDAD FINAL - Análisis de Mis Habilidades ComunicativasCARLOS ALBERTO CHIRINOS MUNDACAОценок пока нет
- Ejemplos de Tension InterfacialДокумент21 страницаEjemplos de Tension InterfacialcomolapascuanohayОценок пока нет
- BRIK Intervención Familiar Sistémica. Mesa RedondaДокумент8 страницBRIK Intervención Familiar Sistémica. Mesa RedondaLagusОценок пока нет
- GalvanometroДокумент4 страницыGalvanometroAniel Moreno100% (1)
- I Guia Ii Parcial Ingenieria Economica Adolfo EspinalДокумент8 страницI Guia Ii Parcial Ingenieria Economica Adolfo Espinaladolfo espinalОценок пока нет
- Proyecto Informatica Forense PNPДокумент18 страницProyecto Informatica Forense PNPPedro Cruz0% (2)
- Unidad 2 - 1 Macroprocesos ComercialДокумент28 страницUnidad 2 - 1 Macroprocesos ComercialEdgar Magne JiménezОценок пока нет
- Humano vs. HumanoДокумент6 страницHumano vs. HumanoEliezerОценок пока нет
- Walter Benjamin y el arte en la era de la reproducciónДокумент4 страницыWalter Benjamin y el arte en la era de la reproducciónreinasilvinaОценок пока нет
- Entrega de Simbolos InstitucionalesДокумент2 страницыEntrega de Simbolos Institucionalesmaria camila saldarriaga zapataОценок пока нет
- Robot manipulador multifuncional reprogramableДокумент1 страницаRobot manipulador multifuncional reprogramableJorge RodriguezОценок пока нет
- Guia Rp3 Mat2110Документ77 страницGuia Rp3 Mat2110rafael0% (1)
- ActaReuniones - Mecatronica - Diseño CORREGIDASДокумент38 страницActaReuniones - Mecatronica - Diseño CORREGIDASHECTOR COCHISE TERAN HERRERAОценок пока нет
- Repetir A La MadreДокумент31 страницаRepetir A La MadreLuis Jorge ValenzuelaОценок пока нет
- Política SanitariaДокумент5 страницPolítica SanitariaSalvador Diaz RomeroОценок пока нет
- Proceso de ServicioДокумент41 страницаProceso de ServicioJudith MataОценок пока нет
- RamosNaravez MarthaLeticia M2S1AI1Документ6 страницRamosNaravez MarthaLeticia M2S1AI1Martha Leticia Ramos NarvaezОценок пока нет
- C-BOCI Inventario Obsesion Complusión (Clark y Beck, 2002)Документ13 страницC-BOCI Inventario Obsesion Complusión (Clark y Beck, 2002)MargaritaОценок пока нет
- Claves Fundamentales en Terapia de ParejaДокумент6 страницClaves Fundamentales en Terapia de ParejaAngel Eduardo Caceres ReyesОценок пока нет
- Eyal WeizmanДокумент9 страницEyal WeizmanYelitza Xiomara Altamirano EstebanОценок пока нет
- Articles-34377 Programa PDFДокумент268 страницArticles-34377 Programa PDFWalkiria ChilensisОценок пока нет
- Actividad Semana 5-6 CivicaДокумент1 страницаActividad Semana 5-6 CivicaAlfredo Rodriguez0% (1)
- Evolución Del AradoДокумент5 страницEvolución Del AradoAndy BarrazaОценок пока нет
- Suma DE POLINOMIOSДокумент14 страницSuma DE POLINOMIOSAlson GarciaОценок пока нет
- Analisis de Pelicula Enemy 02Документ5 страницAnalisis de Pelicula Enemy 02treseisОценок пока нет