Академический Документы
Профессиональный Документы
Культура Документы
Hidrometalurgia (2019 II)
Загружено:
Jenisser Avalos VasquezАвторское право
Доступные форматы
Поделиться этим документом
Поделиться или встроить документ
Этот документ был вам полезен?
Это неприемлемый материал?
Пожаловаться на этот документАвторское право:
Доступные форматы
Hidrometalurgia (2019 II)
Загружено:
Jenisser Avalos VasquezАвторское право:
Доступные форматы
METALURGIA EXTRACTIVA I: HIDROMETALURGIA
HIDROMETALURGIA
DEFINICIÓN:
Estudia la extracción y/o refinación de los metales de sus menas (minerales,
concentrados, calcinas, etc.), por medio de soluciones acuosas como agentes
de disolución.
ETAPAS DEL PROCESO GENERAL HIDROMETALÚRGICO:
Alimentación
1º Preparación
Reactivos
2º Lixiviación
Residuos
Separación S/L
Sólidos de lixiv.
3º Purificación
Residuos
Separación S/L
Sólidos de purif.
5º
Recup. Metales Regeneración
4º Recuperación
Secundarios Soluc. Lixiv.
Metal Sub productos Relaves
ING. A. CORTIJO G. – DPTO. IMM – UNT. Pág. 1
METALURGIA EXTRACTIVA I: HIDROMETALURGIA
1º. Preparación de la alimentación:
Física: Secado, trituración, molienda, concentración, etc.
Química: tostación (sulfuros a óxidos, sulfatos a cloruros).
2º. Producción de la solución cargada con el metal(es):
Lixiviación: Disolución de metales presentes en la alimentación.
3º. Purificación de la solución:
Eliminación de impurezas de la solución cargada.
4º. Producción del metal:
Precipitación del metal o metales de la solución.
5º. Regeneración de la solución:
Recuperación del reactivo principal para su reciclo a lixiviación.
VENTAJAS Y DESVENTAJAS DEL PROCESO HIDROMETALÚRGICO:
Ventajas:
Menor contaminación ambiental. Fácil control y automatización. Menor
costo de energía. Se pueden trabajar minerales de baja ley y desperdicios
de minas.
Desventajas:
Tasa de producción relativamente baja, esto implica que el tamaño de la
planta sea muy grande. Manejo de grandes cantidades de soluciones.
Reactivos caros.
ING. A. CORTIJO G. – DPTO. IMM – UNT. Pág. 2
METALURGIA EXTRACTIVA I: HIDROMETALURGIA
DIAGRAMA DE FLUJO DEL PROCESO HIDROMETALURGICO
DEL ZINC.
𝑯𝟐 𝑺𝑶𝟒
ING. A. CORTIJO G. – DPTO. IMM – UNT. Pág. 3
METALURGIA EXTRACTIVA I: HIDROMETALURGIA
LIXIVIACION
a) DEFINICIÓN:
Proceso de extracción de un constituyente soluble de un sólido por medio de
un disolvente. Puede ser parcial o total:
Parcial: Ejemplo la disolución ácida de calcopirita con sulfato férrico a
condiciones estándar (25ºC, 1 atm):
𝑪𝒖𝑭𝒆𝑺𝟐 + 𝟐𝑭𝒆𝟐 (𝑺𝑶𝟒 )𝟑 = 𝑪𝒖𝑺𝑶𝟒 + 𝟓𝑭𝒆𝑺𝑶𝟒 + 𝟐𝑺𝟎
Total: Ejemplo la disolución ácida de calcopirita a elevadas temperaturas
y presiones:
𝟐𝑪𝒖𝑭𝒆𝑺𝟐 + 𝟏𝟕/𝟒 𝑶𝟐 + 𝑯𝟐 𝑺𝑶𝟒 = 𝟐𝑪𝒖𝑺𝑶𝟒 + 𝑭𝒆𝟐 (𝑺𝑶𝟒 )𝟑 + 𝑯𝟐 𝑶
b) MATERIAS PRIMAS:
Metales nativos: 𝐴𝑢, 𝐴𝑔, 𝐶𝑢, etc.
Metales de deshechos: Escorias, lodos, polvos, etc.
Productos de cementación.
Minerales oxidados: Óxidos, carbonatos, hidróxidos y silicatos.
Calcinas (sulfuros tostados).
Minerales sulfurados de 𝐶𝑢, 𝑍𝑛, 𝑃𝑏, 𝑁𝑖, 𝐶𝑜, 𝑆𝑏, etc.
c) AGENTES DE LIXIVIACIÓN:
Agua: Para lixiviar calcinas de sulfatos o cloruros.
Ácidos: 𝐻2 𝑆𝑂4 , 𝐻𝑁𝑂3 , 𝐻𝐶𝑙.
Bases: 𝑁𝑎𝑂𝐻, 𝑁𝐻4 𝑂𝐻.
Sales en solución acuosa: 𝐹𝑒2 (𝑆𝑂4 )3 , 𝑁𝑎2 𝐶𝑂3 , 𝑁𝑎𝐶𝑙, 𝑁𝑎𝐶𝑁, 𝑁𝑎2 𝑆,
𝑁𝑎2 𝑆2 𝑂3 (tiosulfato de sodio), 𝐶𝑙2 (acuoso), (𝑁𝐻4 )2 𝑆2 𝑂8 , 𝑁𝑎2 𝑆2 𝑂8 , 𝐾2 𝑆2 𝑂8 .
Ejemplo : Lixiviación de 𝑍𝑛𝑆 con persulfato de amonio en presencia de
𝐻2 𝑆𝑂4:
𝒁𝒏𝑺 + (𝑵𝑯𝟒 )𝟐 𝑺𝟐 𝑶𝟖 = 𝒁𝒏𝑺𝑶𝟒 + (𝑵𝑯𝟒 )𝟐 𝑺𝑶𝟒 + 𝑺𝟎
ING. A. CORTIJO G. – DPTO. IMM – UNT. Pág. 4
METALURGIA EXTRACTIVA I: HIDROMETALURGIA
d) REQUERIMIENTOS DEL REACTIVO DE LIXIVIACIÓN:
a) Debe ser selectivo para disolver al metal o metales deseados, sin reaccionar
con los compuestos no deseados (o reaccionar muy lentamente).
b) No debe ser muy corrosivo.
c) No debe ser muy costoso o debe ser fácilmente recuperable.
d) Debe tener suficiente solubilidad para lograr velocidad de reacción
adecuada.
La selectividad depende de la concentración del agente lixiviante, la
temperatura y el tiempo de contacto. Los tres factores incrementan la lixiviación
o disolución del metal e impurezas, por lo tanto se deben identificar los
óptimos para una extracción máxima y un nivel mínimo de impurezas.
TERMODINAMICA DE LA LIXIVIACION
Los diagramas de POURBAIX o diagramas 𝑬𝒉 – 𝒑𝑯 predicen la posibilidad
termodinámica del proceso de lixiviación. De estas gráficas se pueden determinar:
Las condiciones necesarias para descomponer un mineral y lixiviar un metal
selectivamente.
Las condiciones necesarias para remover el metal de la solución lixiviada,
precipitándolo en alguna forma sólida.
𝒑𝑯 : mide el comportamiento ácido o básico del sistema.
𝑬𝒉 : mide el estado de oxidación o reducción del sistema.
Un alto valor del 𝑬𝒉 (medido en voltios) indica que el sistema es esencialmente
oxidante o tiene tendencia hacia un estado oxidado.
Un bajo valor del 𝑬𝒉 indica que el sistema es esencialmente reductor o tiene
tendencia hacia un estado reducido.
ING. A. CORTIJO G. – DPTO. IMM – UNT. Pág. 5
METALURGIA EXTRACTIVA I: HIDROMETALURGIA
Para aumentar el 𝑬𝒉 se adiciona un oxidante al sistema.
Para disminuir el 𝑬𝒉 se adiciona un reductor al sistema.
Los oxidantes más comunes son el oxígeno, cloro y peróxido de hidrógeno
Los reductores más comunes son los sulfuros metálicos o los metales
elementales.
1. DISOLUCIÓN DE UNA SAL:
Muchas sales metálicas son fácilmente solubles en agua. Por ejemplo, el sulfato
de cobre puede disolverse en agua para producir una solución de alrededor de
80 g/litro a temperatura ambiente:
𝑯𝟐 𝑶
𝑪𝒖𝑺𝑶𝟒 ⇔ 𝑪𝒖𝟐+ (𝒂𝒄) + 𝑺𝑶𝟐−
𝟒 (𝒂𝒄)
Los límites de este tipo de disolución son la disponibilidad de minerales que
sean sales y la solubilidad de estas sales en agua. Otros tipos de sales
importantes en hidrometalurgia incluyen: sulfatos, cianuros, cloruros, nitratos,
cromatos, percloratos, molibdatos, cloratos, etc.
2. LIXIVIACIÓN ÁCIDA DE ÓXIDOS METÁLICOS:
Los metales son frecuentemente hallados en la naturaleza en forma de óxidos.
Muchos de estos minerales oxidados se pueden lixiviar fácilmente con
soluciones acuosas ácidas:
𝒁𝒏𝑶 (𝒔) + 𝑯𝟐 𝑺𝑶𝟒 = 𝒁𝒏𝑺𝑶𝟒 (𝒂𝒄) + 𝑯𝟐 𝑶
𝑪𝒖𝑶 (𝒔) + 𝑯𝟐 𝑺𝑶𝟒 = 𝑪𝒖𝑺𝑶𝟒 (𝒂𝒄) + 𝑯𝟐 𝑶
𝑭𝒆𝑶 (𝒔) + 𝑯𝟐 𝑺𝑶𝟒 = 𝑭𝒆𝑺𝑶𝟒 (𝒂𝒄) + 𝑯𝟐 𝑶
3. LIXIVIACIÓN BÁSICA DE ÓXIDOS METÁLICOS:
La lixiviación básica ha sido practicada por más de 100 años en la industria del
aluminio. El proceso Bayer usa altas temperaturas y soluciones lixiviantes
fuertemente básicas para disolver al aluminio de los minerales de bauxita. El
ING. A. CORTIJO G. – DPTO. IMM – UNT. Pág. 6
METALURGIA EXTRACTIVA I: HIDROMETALURGIA
zinc también es altamente soluble en soluciones básicas y este comportamiento
ha sido aplicado para lixiviar al zinc desde minerales oxidados:
𝑨𝒍𝟐 𝑶𝟑 (𝒔) + 𝟐𝑶𝑯− + 𝟑𝑯𝟐 𝑶 = 𝟐𝑨𝒍(𝑶𝑯)−
𝟒
𝒁𝒏𝑶 (𝒔) + 𝟐𝑶𝑯− = 𝒁𝒏𝑶𝟐−
𝟐 + 𝑯𝟐 𝑶
𝑪𝒖𝑶(𝒔) + 𝟐𝑶𝑯− = 𝑪𝒖𝑶𝟐−
𝟐 + 𝑯𝟐 𝑶
4. LIXIVIACIÓN CON FORMACIÓN DE IONES COMPLEJOS:
Los iones complejos son formados cuando los metales interactúan con ligandos
que están presentes en la solución. Los ligandos típicamente aumentan la
solubilidad de los metales, mejorando así la lixiviación. Los ligandos más
comunes incluyen al cloro, cianuro, amoniaco y tiosulfato.
Ejemplos de complejos formados con estos ligandos:
𝑪𝒍− ∶ 𝑪𝒖𝑪𝑳− − 𝟐−
𝟐 , 𝑨𝒈𝑪𝑳𝟐 , 𝑷𝒃𝑪𝒍𝟒
𝑪𝑵− ∶ 𝑨𝒖(𝑪𝑵)− − −
𝟐 , 𝑪𝒖(𝑪𝑵)𝟐 , 𝑨𝒈(𝑪𝑵)𝟐
+ 𝟐+ 𝟐+
𝑵𝑯𝟑 ∶ 𝑪𝒖(𝑵𝑯𝟑)𝟐+ 𝟐+
𝟒 , 𝑪𝒖(𝑵𝑯𝟑 )𝟐 , 𝒁𝒏(𝑵𝑯𝟑 )𝟒 , 𝑵𝒊(𝑵𝑯𝟑 )𝟔 , 𝑪𝒐(𝑵𝑯𝟑 )𝟔
𝑺𝟐 𝑶𝟐− 𝟑−
𝟑 ∶ 𝑨𝒈(𝑺𝟐 𝑶𝟑 )𝟐 , 𝑨𝒖(𝑺𝟐 𝑶𝟑)𝟑−
𝟐
5. LIXIVIACIÓN CON OXIDACIÓN:
Muchos minerales se encuentran en la naturaleza conteniendo metales en su
estado reducido. Para lixiviar al metal, el mineral requiere una oxidación con un
agente oxidante. Los oxidantes comunes en hidrometalurgia incluyen al
oxígeno, cloro, ácido nítrico, peróxido de hidrogeno, clorato y el ión férrico
(𝐹𝑒 3+). Algunas reacciones comunes de oxidación son las siguientes:
Proceso de lixiviación a presión del 𝒁𝒏𝑺:
𝒁𝒏𝑺 + 𝟎. 𝟓𝑶𝟐 + 𝟐𝑯+ = 𝒁𝒏𝟐+ + 𝑯𝟐 𝑶 + 𝑺
Proceso de oxidación de la pirita:
𝑭𝒆𝑺𝟐 + 𝟑. 𝟕𝟓𝑶𝟐 + 𝟎. 𝟓𝑯𝟐 𝑶 = 𝑭𝒆𝟑+ + 𝟐𝑺𝑶𝟐−
𝟒 + 𝑯+
Cianuración de oro y plata:
𝟐𝑨𝒖 + 𝟒𝑵𝒂𝑪𝑵 + 𝟎. 𝟓 𝑶𝟐 + 𝑯𝟐 𝑶 = 𝟐𝑵𝒂𝑨𝒖(𝑪𝑵)𝟐 + 𝟐𝑵𝒂𝑶𝑯
𝟐𝑨𝒈 + 𝟒𝑵𝒂𝑪𝑵 + 𝟎. 𝟓𝑶𝟐 + 𝑯𝟐 𝑶 = 𝟐𝑵𝒂𝑨𝒈(𝑪𝑵)𝟐 + 𝟐𝑵𝒂𝑶𝑯
ING. A. CORTIJO G. – DPTO. IMM – UNT. Pág. 7
METALURGIA EXTRACTIVA I: HIDROMETALURGIA
LIXIVIACION DE CALCINAS DE ZINC
LIXIVIACIÓN ÁCIDA DEL 𝒁𝒏𝑶:
𝒁𝒏𝑶 (𝒔) + 𝟐𝑯+ = 𝒁𝒏𝟐+ + + 𝑯𝟐 𝑶 … … . . 𝒓𝒆𝒂𝒄𝒄𝒊ó𝒏 𝒊ó𝒏𝒊𝒄𝒂
𝒁𝒏𝑶 (𝒔) + 𝑯𝟐 𝑺𝑶𝟒 = 𝒁𝒏𝑺𝑶𝟒 (𝒂𝒄) + 𝑯𝟐 𝑶 … … . . 𝒓𝒆𝒂𝒄𝒄𝒊ó𝒏 𝒎𝒐𝒍𝒆𝒄𝒖𝒍𝒂𝒓
𝑭𝒆𝑶 (𝒔) + 𝑯𝟐 𝑺𝑶𝟒 = 𝑭𝒆𝑺𝑶𝟒 (𝒂𝒄) + 𝑯𝟐 𝑶
∆𝑮𝒓 = ∆𝑮𝟎𝒓 + 𝟐. 𝟑𝟎𝟑𝑹𝑻𝒍𝒐𝒈 𝑲′ … … … 𝒊𝒔𝒐𝒕𝒆𝒓𝒎𝒂 𝒅𝒆 𝑽𝒂𝒏, 𝒕 𝑯𝒐𝒇𝒇
𝐼𝑛𝑐𝑙𝑢𝑦𝑒𝑛𝑑𝑜 𝑐𝑜𝑛𝑑𝑖𝑐𝑖𝑜𝑛𝑒𝑠 𝑑𝑒 𝑒𝑞𝑢𝑖𝑙𝑖𝑏𝑟𝑖𝑜 𝑦 𝒑𝑯 = − 𝒍𝒐𝒈 𝒂𝑯+ ∶
∆𝑮𝒓 = 𝟐. 𝟑𝟎𝟑𝑹𝑻𝒍𝒐𝒈(𝑲′ ⁄𝑲𝒆) = 𝟐. 𝟑𝟎𝟑𝑹𝑻𝒍𝒐𝒈(𝒑𝑯𝒔𝒐𝒍 ⁄𝒑𝑯𝒆𝒒 )
𝒑𝑯𝒔𝒐𝒍 = 𝒑𝑯𝒆𝒒 , ∆𝑮𝒓 = 𝟎 , ↔ , 𝑬𝑸𝑼𝑰𝑳𝑰𝑩𝑹𝑰𝑶
𝒑𝑯𝒔𝒐𝒍 > 𝒑𝑯𝒆𝒒 , ∆𝑮𝒓 > 0 , ← , 𝑵𝑶 𝑶𝑪𝑼𝑹𝑹𝑬 𝑳𝑰𝑿𝑰𝑽𝑰𝑨𝑪𝑰𝑶𝑵
𝒑𝑯𝒔𝒐𝒍 < 𝒑𝑯𝒆𝒒 , ∆𝑮𝒓 < 0 , → , 𝑶𝑪𝑼𝑹𝑹𝑬 𝑳𝑰𝑿𝑰𝑽𝑰𝑨𝑪𝑰𝑶𝑵 𝑫𝑬𝑳 𝒁𝒏𝑶
Condiciones: 𝒑𝑯𝒔𝒐𝒍 < 𝟓. 𝟓 , 𝑻 = 𝟐𝟓𝟎 𝑪 , 𝑷 = 𝟏 𝒂𝒕𝒎.
PRECIPITACIÓN DEL HIERRO COMO Fe(OH)3 :
a) Oxidación del ion 𝑭𝒆𝟐+ a 𝑭𝒆𝟑+, usando 𝑴𝒏𝑶𝟐:
𝑹𝑨: 𝟐𝑭𝒆𝟐+ = 𝟐𝑭𝒆𝟑+ + 𝟐𝒆− 𝑬𝟎𝒂 = 𝟎. 𝟕𝟕 𝒗
𝑹𝑪: 𝑴𝒏𝑶𝟐 + 𝟒𝑯+ + 𝟐𝒆− = 𝑴𝒏𝟐+ + + 𝟐𝑯𝟐 𝑶 𝑬𝟎𝒄 = 𝟏. 𝟐𝟑 𝒗
-----------------------------------------------------------------------------------------------------------
𝑹𝑻: 𝟐𝑭𝒆𝟐+ + 𝑴𝒏𝑶𝟐 + 𝟒𝑯+ = 𝑴𝒏𝟐+ + 𝟐𝑭𝒆𝟑+ + 𝟐𝑯𝟐 𝑶
𝟐𝑭𝒆𝑺𝑶𝟒 + 𝑴𝒏𝑶𝟐 + 𝟐 𝑯𝟐 𝑺𝑶𝟒 = 𝑴𝒏𝑺𝑶𝟒 + 𝑭𝒆𝟐 (𝑺𝑶𝟒 )𝟑 + 𝟐𝑯𝟐 𝑶
∆𝑮𝒓 = −𝒛 𝑭 ∆𝑬𝒓
𝟐. 𝟑𝟎𝟑𝑹𝑻 𝒂𝒑𝒓𝒐𝒅
∆𝑬𝒓 = ∆𝑬𝟎𝒓 − 𝐥𝐨𝐠 ( )
𝒛𝑭 𝒂𝒓𝒆𝒂𝒄
𝐷𝑜𝑛𝑑𝑒: 𝑹 = 𝟖. 𝟑𝟏𝟒 𝑱⁄𝒎𝒐𝒍.oK 𝑻 = 𝟐𝟓𝟎 𝑪 = 𝟐𝟗𝟖𝟎 𝑲 ∆𝑬𝟎𝒓 = 𝑬𝟎𝒄 − 𝑬𝟎𝒂
𝑭 = 𝟗𝟔𝟒𝟖𝟕 𝑱⁄𝒎𝒐𝒍. 0K .
𝐸𝑛𝑡𝑜𝑛𝑐𝑒𝑠:
𝟎. 𝟎𝟓𝟗𝟏 𝒂𝒑𝒓𝒐𝒅
∆𝑬𝒓 = ∆𝑬𝟎𝒓 − 𝐥𝐨𝐠 ( )
𝒛 𝒂𝒓𝒆𝒂𝒄
ING. A. CORTIJO G. – DPTO. IMM – UNT. Pág. 8
METALURGIA EXTRACTIVA I: HIDROMETALURGIA
∆𝑬𝒓 = 𝟎 , ∆𝑮𝒓 = 𝟎 , ↔, 𝑬𝑸𝑼𝑰𝑳𝑰𝑩𝑹𝑰𝑶
∆𝑬𝒓 < 𝟎 , ∆𝑮𝒓 > 𝟎 . ← , 𝑵𝑶 𝑶𝑪𝑼𝑹𝑹𝑬 𝑳𝑨 𝑶𝑿𝑰𝑫𝑨𝑪𝑰𝑶𝑵
∆𝑬𝒓 > 𝟎 , ∆𝑮𝒓 < 𝟎 , →, 𝑺𝑰 𝑶𝑪𝑼𝑹𝑹𝑬 𝑳𝑨 𝑶𝑿𝑰𝑫𝑨𝑪𝑰𝑶𝑵
La condición termodinámica de la oxidación radica en la diferencia de los
potenciales de equilibrio: El agente oxidante debe tener un potencial mucho más
positivo que el metal a oxidar , con una diferencia mayor a 0.2 voltios para
soportar la oxidación del metal ⇒ ∆𝑬𝒓 > 0 𝑦 ∆𝑮𝒓 < 0
b) Precipitación del 𝑭𝒆(𝑶𝑯)𝟑 por aumento del 𝒑𝑯:
𝟐 [ 𝑭𝒆𝟑+ + 𝟑𝑯𝟐 𝑶 = 𝑭𝒆(𝑶𝑯)𝟑 + 𝟑𝑯+]
𝟑 [ 𝒁𝒏𝑶 + 𝟐𝑯+ = 𝒁𝒏𝟐+ + 𝑯𝟐 𝑶 ]
--------------------------------------------------------------------
𝟐𝑭𝒆𝟑+ + 𝟑𝒁𝒏𝑶 + 𝟑𝑯𝟐 𝑶 = 𝟑𝒁𝒏𝟐+ + 𝟐𝑭𝒆(𝑶𝑯)𝟑 𝑹. 𝒊ó𝒏𝒊𝒄𝒂
𝑭𝒆𝟐 (𝑺𝑶𝟒 )𝟑 + 𝟑𝒁𝒏𝑶 + 𝟑𝑯𝟐 𝑶 = 𝟑𝒁𝒏𝑺𝑶𝟒 + 𝟐𝑭𝒆(𝑶𝑯)𝟑 𝑹. 𝒎𝒐𝒍𝒆𝒄𝒖𝒍𝒂𝒓
𝒑𝑯𝒔𝒐𝒍 > 𝒑𝑯𝒆𝒒 , ∆𝑮𝒓 < 𝟎 , → , 𝑷𝑹𝑬𝑪𝑰𝑷𝑰𝑻𝑨 𝑬𝑳 𝑭𝒆(𝑶𝑯)𝟑
𝑪𝒐𝒏𝒅𝒊𝒄𝒊𝒐𝒏𝒆𝒔: 𝒑𝑯𝒔𝒐𝒍 > 𝟏. 𝟓 , 𝑻 = 𝟐𝟓𝟎 𝑪 , 𝑷 = 𝟏 𝒂𝒕𝒎.
POR LO TANTO: La lixiviación ácida de calcinas de zinc se debe realizar en las
siguientes condiciones:
𝟏. 𝟓 < 𝒑𝑯 < 𝟓. 𝟓 𝑻 = 𝟐𝟓𝟎 𝑪 𝑷 = 𝟏 𝒂𝒕𝒎.
ELIMINACIÓN DE ARSÉNICO Y ANTIMONIO:
El Hidróxido férrico precipitado arrastra consigo todo el As, Sb y Ge, en forma de
arseniatos básicos absorbidos en los flóculos de hidróxido:
𝟒𝑭𝒆(𝑶𝑯)𝟑 + 𝑯𝟑 𝑨𝒔𝑶𝟑 = 𝑭𝒆𝟒 𝑶𝟓 (𝑶𝑯)𝟓 . 𝑨𝒔 + 𝟓𝑯𝟐 𝑶
𝟒𝑭𝒆(𝑶𝑯)𝟑 + 𝑯𝟑 𝑺𝒃𝑶𝟑 = 𝑭𝒆𝟒 𝑶𝟓 (𝑶𝑯)𝟓 . 𝑺𝒃 + 𝟓𝑯𝟐 𝑶
ING. A. CORTIJO G. – DPTO. IMM – UNT. Pág. 9
METALURGIA EXTRACTIVA I: HIDROMETALURGIA
DIAGRAMA DE POURBAIX, 𝒁𝒏 − 𝑯𝟐 𝑶, 𝟐𝟓𝟎 𝑪, [𝒊𝒐𝒏] = 𝟏𝑴
ING. A. CORTIJO G. – DPTO. IMM – UNT. Pág. 10
METALURGIA EXTRACTIVA I: HIDROMETALURGIA
DIAGRAMA DE POURBAIX, 𝑭𝒆 − 𝑯𝟐 𝑶, 𝟐𝟓𝟎 𝑪, [𝒊𝒐𝒏] = 𝟏𝑴
𝑨 ∶ 𝑭𝒆𝟐+ (𝒂𝒄) 𝑫 ∶ 𝑭𝒆(𝑶𝑯)𝟐
𝑩 ∶ 𝑭𝒆𝟑+ (𝒂𝒄) 𝑬 ∶ 𝑭𝒆
𝑪 ∶ 𝑭𝒆(𝑶𝑯)𝟑
ING. A. CORTIJO G. – DPTO. IMM – UNT. Pág. 11
METALURGIA EXTRACTIVA I: HIDROMETALURGIA
DIAGRAMA DE POURBAIX 𝒁𝒏 − 𝑭𝒆 − 𝑯𝟐 𝑶, 𝟐𝟓°𝑪, [𝒊𝒐𝒏] = 𝟏𝑴
𝑭𝒆𝟑+ 𝑭𝒆(𝑶𝑯)𝟑
𝒁𝒏𝑶
𝒁𝒏𝑶𝟐−
𝟐
1 -
𝑶𝟐 (𝒈)
0.77 𝑯𝟐 𝑶(𝒍)
𝑬, 𝒗
𝑭𝒆𝟐+
0 𝒁𝒏𝟐+
𝑯𝟐 𝑶(𝒍)
- 0.44 𝑯𝟐 (𝒈) 𝑭𝒆(𝑶𝑯)𝟐
- 0.76
-1 -
𝑭𝒆
𝒁𝒏
0 1.5 5.5 9 15 18
𝒑𝑯
ING. A. CORTIJO G. – DPTO. IMM – UNT. Pág. 12
METALURGIA EXTRACTIVA I: HIDROMETALURGIA
DIAGRAMA DE FLUJO DEL PROCESO DE LIXIVIACION ACIDA DE
CALCINAS DE ZINC
ING. A. CORTIJO G. – DPTO. IMM – UNT. Pág. 13
METALURGIA EXTRACTIVA I: HIDROMETALURGIA
DIAGRAMA DE POURBAIX, 𝑪𝒖 – 𝑯𝟐 𝑶, 𝟐𝟓𝟎 𝑪, [𝒊𝒐𝒏] = 𝟏𝑴
ING. A. CORTIJO G. – DPTO. IMM – UNT. Pág. 14
METALURGIA EXTRACTIVA I: HIDROMETALURGIA
LIXIVIACIÓN ACIDA DEL COBRE:
𝑹𝑪 ∶ 𝟏⁄𝟐 𝑶𝟐 + 𝟐𝑯+ + 𝟐 𝒆− = 𝑯𝟐 𝑶 𝑬𝟎𝒄 = 1.229 𝑣.
𝑹𝑨 ∶ 𝑪𝒖 = 𝑪𝒖𝟐+ + 𝟐 𝒆− 𝑬𝟎𝒂 = 0.337 𝑣.
---------------------------------------------------------------------------------------------------
𝑹𝑻 ∶ 𝑪𝒖 + 𝟏⁄𝟐 𝑶𝟐 + 𝟐𝑯+ = 𝑪𝒖𝟐+ + 𝑯𝟐 𝑶 ∆𝑬𝟎𝒓 = 𝑬𝟎𝒄 − 𝑬𝟎𝒂
𝟎. 𝟎𝟓𝟗𝟏 𝒂𝒑𝒓𝒐𝒅
∆𝑬𝒓 = ∆𝑬𝟎𝒓 − 𝐥𝐨𝐠 ( )
𝒛 𝒂𝒓𝒆𝒂𝒄
∆𝑮𝒓 = −𝒛 𝑭 ∆𝑬𝒓
∆𝑬𝒓 = 𝟎 , ∆𝑮𝒓 = 𝟎 , ↔, 𝑬𝑸𝑼𝑰𝑳𝑰𝑩𝑹𝑰𝑶
∆𝑬𝒓 < 𝟎 , ∆𝑮𝒓 > 𝟎 . ← , 𝑵𝑶 𝑶𝑪𝑼𝑹𝑹𝑬 𝑳𝑨 𝑳𝑰𝑿𝑰𝑽𝑰𝑨𝑪𝑰𝑶𝑵
∆𝑬𝒓 > 𝟎 , ∆𝑮𝒓 < 𝟎 , →, 𝑺𝑰 𝑶𝑪𝑼𝑹𝑹𝑬 𝑳𝑨 𝑳𝑰𝑿𝑰𝑽𝑰𝑨𝑪𝑰𝑶𝑵
La condición termodinámica de la lixiviación radica en la diferencia de los
potenciales de equilibrio: El agente oxidante debe tener un potencial mucho más
positivo que el metal a lixiviar, con una diferencia mayor a 0.2 voltios para
soportar la oxidación del metal ⇒ ∆𝑬𝒓 > 0 𝑦 ∆𝑮𝒓 < 0
A condiciones estándar:
𝑻 = 𝟐𝟓𝟎 𝑪 𝝅 = 𝟏 𝒂𝒕𝒎. [𝒊ó𝒏] = 𝟏 𝑴 𝒑𝑯 < 𝟐. 𝟓
𝟎. 𝟎𝟓𝟗𝟏 [𝑪𝒖𝟐+]
∆𝑬𝒓 = ∆𝑬𝟎𝒓 − 𝐥𝐨𝐠 ( 𝟏⁄𝟐 )
𝒛 𝑷 [𝑯+]𝟐
𝑶𝟐
0
𝟎. 𝟎𝟓𝟗𝟏 𝟏
∆𝑬𝒓 = ∆𝑬𝟎𝒓 − 𝐥𝐨𝐠 ( )
𝒛 𝟏
∆𝑬𝒓 = ∆𝑬𝟎𝒓 = 𝑬𝟎𝒄 − 𝑬𝟎𝒂 = 𝟏. 𝟐𝟐𝟗 − 𝟎. 𝟑𝟑𝟕 = 𝟎. 𝟖𝟗𝟐 𝒗 > 𝟎
∆𝑮𝒓 = −𝒛 𝑭 ∆𝑬𝟎𝒓 = −(𝟐)(𝟗𝟔𝟒𝟖𝟕 𝑱⁄𝒎𝒐𝒍. 𝒗)(𝟎. 𝟖𝟗𝟐 𝒗) = −𝟏𝟕𝟐𝟏𝟑𝟐. 𝟖𝟏 𝑱⁄𝒎𝒐𝒍 < 𝟎
Por lo tanto si ocurre la lixiviación del cobre a condiciones estándar y en forma
espontánea.
ING. A. CORTIJO G. – DPTO. IMM – UNT. Pág. 15
METALURGIA EXTRACTIVA I: HIDROMETALURGIA
CIANURACION
Se define como la lixiviación de metales preciosos con soluciones de cianuro. Se ha
podido establecer que la disolución de los metales por cianuración, está regida por
los principios electroquímicos de la corrosión.
CIANURACIÓN DEL ORO:
Reacción de ELSNER:
𝟐𝑨𝒖 + 𝟒𝑵𝒂𝑪𝑵 + 𝟎. 𝟓𝑶𝟐 + 𝑯𝟐 𝑶 = 𝟐𝑵𝒂𝑨𝒖(𝑪𝑵)𝟐 + 𝟐𝑵𝒂𝑶𝑯
Reacciones de BODLAENDER:
𝟐𝑨𝒖 + 𝟒𝑵𝒂𝑪𝑵 + 𝑶𝟐 + 𝟐𝑯𝟐 𝑶 = 𝟐𝑵𝒂𝑨𝒖(𝑪𝑵)𝟐 + 𝟐𝑵𝒂𝑶𝑯 + 𝑯𝟐 𝑶𝟐
𝟐𝑨𝒖 + 𝟒𝑵𝒂𝑪𝑵 + 𝑯𝟐 𝑶𝟐 = 𝟐𝑵𝒂𝑨𝒖(𝑪𝑵)𝟐 + 𝟐𝑵𝒂𝑶𝑯
Sumando obtenemos la reacción de ELSNER:
𝟒𝑨𝒖 + 𝟖𝑵𝒂𝑪𝑵 + 𝑶𝟐 + 𝟐 𝑯𝟐 𝑶 = 𝟒𝑵𝒂𝑨𝒖(𝑪𝑵)𝟐 + 𝟒𝑵𝒂𝑶𝑯
TERMODINÁMICA:
RA: 𝟐 𝑨𝒖 + 𝟒𝑪𝑵− = 𝟐𝑨𝒖(𝑪𝑵)−
𝟐 + 𝟐𝒆
−
𝑬𝟎𝒂 = -0.477 v
RC: 𝟎. 𝟓𝑶𝟐 + 𝑯𝟐 𝑶 + 𝟐𝒆− = 𝟐𝑶𝑯− 𝑬𝟎𝒄 = 0.4 v
------------------------------------------------------------------------------------------------------
RT: 𝟐𝑨𝒖 + 𝟒𝑪𝑵− + 𝟎. 𝟓𝑶𝟐 + 𝑯𝟐 𝑶 = 𝟐𝑨𝒖(𝑪𝑵)−
𝟐 + 𝟐𝑶𝑯
−
𝟐𝑨𝒖 + 𝟒𝑵𝒂𝑪𝑵 + 𝟎. 𝟓𝑶𝟐 + 𝑯𝟐 𝑶 = 𝟐𝑵𝒂𝑨𝒖(𝑪𝑵)𝟐 + 𝟐𝑵𝒂𝑶𝑯
𝟎. 𝟎𝟓𝟗𝟏 𝒂𝒑𝒓𝒐𝒅
∆𝑬𝒓 = ∆𝑬𝟎𝒓 − 𝐥𝐨𝐠 ( )
𝒛 𝒂𝒓𝒆𝒂𝒄
∆𝑮𝒓 = −𝒛 𝑭 ∆𝑬𝒓
∆𝑬𝒓 > 𝟎, ∆𝑮𝒓 < 𝟎 , → , 𝑺𝑰 𝑶𝑪𝑼𝑹𝑹𝑬 𝑳𝑨 𝑪𝑰𝑨𝑵𝑼𝑹𝑨𝑪𝑰𝑶𝑵
Condiciones: 𝒑𝑯 > 𝟏𝟎 𝑻 = 𝟐𝟓𝟎 𝑪 𝑷 = 𝟏 𝒂𝒕𝒎.
ING. A. CORTIJO G. – DPTO. IMM – UNT. Pág. 16
METALURGIA EXTRACTIVA I: HIDROMETALURGIA
DIAGRAMA DE POURBAIX, 𝑨𝒖– 𝑪𝑵– 𝑯𝟐 𝑶, 𝟐𝟓𝟎 𝑪, [𝒊𝒐𝒏] = 𝟏𝟎−𝟐 𝑴
𝑯𝑪𝑵 𝑪𝑵−
ING. A. CORTIJO G. – DPTO. IMM – UNT. Pág. 17
METALURGIA EXTRACTIVA I: HIDROMETALURGIA
CINÉTICA:
ZONA CATÓDICA
𝑶𝟐 + 𝟐𝑯𝟐 𝑶 + 𝟐𝒆− → 𝑯𝟐 𝑶𝟐 + 𝟐𝑶𝑯− 𝐴1 𝑶𝟐 𝒅𝒊𝒔𝒖𝒆𝒍𝒕𝒐
A1
𝒆− FASE ACUOSA
𝑨𝒖 → 𝑨𝒖+ + 𝒆− A2
𝑨𝒖+ + 𝟐𝑪𝑵− → 𝑨𝒖(𝑪𝑵)−
𝟐 𝐴2 𝑪𝑵−
ZONA ANÓDICA 𝜹
𝑐𝑎𝑝𝑎 𝑙í𝑚𝑖𝑡𝑒
RC: 𝑶𝟐 + 𝟐𝑯𝟐 𝑶 + 𝟐𝒆− → 𝑯𝟐 𝑶𝟐 + 𝟐𝑶𝑯−
RA: 𝟐 [𝑨𝒖 + 𝟐𝑪𝑵− → 𝑨𝒖(𝑪𝑵)− −
𝟐 + 𝒆 ]
------------------------------------------------------------------------------------------------
RT: 𝟐𝑨𝒖 + 𝟒𝑪𝑵− + 𝑶𝟐 + 𝟐𝑯𝟐 𝑶 → 𝟐𝑨𝒖(𝑪𝑵)−
𝟐 + 𝟐𝑶𝑯
−
+ 𝑯𝟐 𝑶𝟐
Adicionando 𝑵𝒂+ :
𝟐𝑨𝒖 + 𝟒𝑵𝒂𝑪𝑵 + 𝑶𝟐 + 𝟐𝑯𝟐 𝑶 → 𝟐𝑵𝒂𝑨𝒖(𝑪𝑵)𝟐 + 𝟐𝑵𝒂𝑶𝑯 + 𝑯𝟐 𝑶𝟐
De la estequiometria:
−𝒓𝑨𝒖 −𝒓𝑪𝑵− −𝒓𝑶𝟐
= =
𝟐 𝟒 𝟏
−𝒓𝑪𝑵−
⇒ − 𝒓𝑨𝒖 = = 𝟐(− 𝒓𝑶𝟐 ) 0
𝟐
𝒅[𝑶𝟐 ] 𝓓𝑶𝟐 𝑨𝟏
Pero: −𝒓𝑶𝟐 = − = {[𝑶𝟐 ] − [𝑶𝟐 ]𝒊 } 𝟏𝒓𝒂. 𝒍𝒆𝒚 𝒅𝒆 𝑭𝑰𝑪𝑲
𝒅𝒕 𝜹
0
𝒅[𝑪𝑵−] 𝓓𝑪𝑵− 𝑨𝟐
−𝒓𝑪𝑵− = − = {[𝑪𝑵−] − [𝑪𝑵−]𝒊 }
𝒅𝒕 𝜹
𝟐 𝓓𝑶𝟐 𝑨𝟏
⇒ − 𝒓𝑨𝒖 = 𝟐(− 𝒓𝑶𝟐 ) = [𝑶𝟐 ] − − − − − − − (𝟏)
𝜹
−𝒓𝑪𝑵− 𝓓𝑪𝑵− 𝑨𝟐
− 𝒓𝑨𝒖 = = [𝑪𝑵−] − − − − − − − (𝟐)
𝟐 𝟐𝜹
Pero: 𝑨 = 𝑨𝟏 + 𝑨𝟐 , á𝑟𝑒𝑎 𝑡𝑜𝑡𝑎𝑙 𝑑𝑒 𝑙𝑎 𝑠𝑢𝑝𝑒𝑟𝑓𝑖𝑐𝑖𝑒 𝑑𝑒𝑙 𝑚𝑒𝑡𝑎𝑙 𝑒𝑛
𝑐𝑜𝑛𝑡𝑎𝑐𝑡𝑜 𝑐𝑜𝑛 𝑙𝑎 𝑠𝑜𝑙𝑢𝑐𝑖ó𝑛.
⇒ 𝑨𝟏 = 𝑨 − 𝑨𝟐
Reemplazando en la ecuación (1):
𝟐 𝓓𝑶𝟐 (𝑨 − 𝑨𝟐 )
− 𝒓𝑨𝒖 = [𝑶𝟐 ] − − − − − − − (𝟑)
𝜹
De la ecuación (2):
𝟐𝜹(−𝒓𝑨𝒖 )
𝑨𝟐 =
𝓓𝑪𝑵− [𝑪𝑵−]
ING. A. CORTIJO G. – DPTO. IMM – UNT. Pág. 18
METALURGIA EXTRACTIVA I: HIDROMETALURGIA
Reemplazando en la ecuación (3):
𝟐𝓓𝑶𝟐 [𝑶𝟐 ] 𝟐𝜹(−𝒓𝑨𝒖 )
−𝒓𝑨𝒖 = (𝑨 − )
𝜹 𝓓𝑪𝑵− [𝑪𝑵−]
𝟐𝓓𝑶𝟐 𝑨 [𝑶𝟐 ] 𝟒𝓓𝑶𝟐 [𝑶𝟐 ](−𝒓𝑨𝒖 )
−𝒓𝑨𝒖 = − , 𝒆𝒄𝒖𝒂𝒄𝒊ó𝒏 𝒄𝒊𝒏é𝒕𝒊𝒄𝒂 𝒒𝒖𝒆
𝜹 𝓓𝑪𝑵− [𝑪𝑵−]
𝒊𝒏𝒄𝒍𝒖𝒚𝒆 𝒆𝒍 á𝒓𝒆𝒂 𝒕𝒐𝒕𝒂𝒍 𝒅𝒆 𝒓𝒆𝒂𝒄𝒄𝒊ó𝒏.
Despejando (−𝒓𝑨𝒖 ) ∶
𝟒𝓓𝑶𝟐 [𝑶𝟐 ](−𝒓𝑨𝒖 ) 𝟐𝓓𝑶𝟐 𝑨 [𝑶𝟐 ]
−𝒓𝑨𝒖 + =
𝓓𝑪𝑵− [𝑪𝑵−] 𝜹
𝟒𝓓𝑶𝟐 [𝑶𝟐 ] 𝟐𝓓𝑶𝟐 𝑨 [𝑶𝟐 ]
−𝒓𝑨𝒖 (𝟏 + ) =
𝓓𝑪𝑵− [𝑪𝑵−] 𝜹
𝓓𝑪𝑵− [𝑪𝑵−] + 𝟒𝓓𝑶𝟐 [𝑶𝟐 ] 𝟐𝓓𝑶𝟐 𝑨 [𝑶𝟐 ]
−𝒓𝑨𝒖 ( −
) =
𝓓𝑪𝑵− [𝑪𝑵 ] 𝜹
𝟐𝑨𝓓𝑪𝑵− 𝓓𝑶𝟐 [𝑪𝑵−][𝑶𝟐 ]
−𝒓𝑨𝒖 =
𝜹(𝓓𝑪𝑵− [𝑪𝑵−] + 𝟒𝓓𝑶𝟐 [𝑶𝟐 ])
Para bajas concentraciones de [𝑪𝑵−] , se descarta el primer término del
denominador:
𝑨𝓓𝑪𝑵−
−𝒓𝑨𝒖 = ( ) [𝑪𝑵−] = 𝑲 [𝑪𝑵−]
𝟐𝜹
La velocidad de disolución del oro depende de la concentración del [𝑪𝑵−], o
velocidad de reacción del cianuro.
Para altas concentraciones de [𝑪𝑵−], el segundo término del denominador se
descarta:
𝟐𝑨𝓓𝑶𝟐
−𝒓𝑨𝒖 = ( ) [𝑶𝟐 ] = 𝑲 [𝑶𝟐 ]
𝜹
La velocidad de disolución del oro depende de la concentración del [𝑶𝟐 ] o
velocidad de reacción del oxígeno.
La velocidad de disolución del oro (−𝒓𝑨𝒖 ) alcanza su valor óptimo cuando la
velocidad de reacción del cianuro en el ánodo es igual a la velocidad de reacción
del oxígeno en el cátodo:
⇒
𝑨𝓓𝑪𝑵− 𝟐𝑨𝓓𝑶𝟐
( ) [𝑪𝑵−] = ( ) [𝑶𝟐 ]
𝟐𝜹 𝜹
𝓓𝑪𝑵− [𝑪𝑵− ] = 𝟒𝓓𝑶𝟐 [𝑶𝟐 ]
ING. A. CORTIJO G. – DPTO. IMM – UNT. Pág. 19
METALURGIA EXTRACTIVA I: HIDROMETALURGIA
[𝑪𝑵−] 𝓓𝑶𝟐
= 𝟒
[𝑶𝟐 ] 𝓓𝑪𝑵−
A condiciones estándar: 𝑻 = 𝟐𝟓𝟎 𝑪 𝝅 = 𝟏 𝒂𝒕𝒎.
𝓓𝑶𝟐 = 2.7 𝑥 10−5 𝑐𝑚2 ⁄𝑠𝑒𝑔
𝓓𝑪𝑵− = 1.83 𝑥 10−5 𝑐𝑚2 ⁄𝑠𝑒𝑔
⇒
[𝑪𝑵−] 𝟐. 𝟕𝒙𝟏𝟎−𝟓
= 𝟒 ( ) ≅ 𝟔
[𝑶𝟐 ] 𝟏. 𝟖𝟑𝒙𝟏𝟎−𝟓
Pero:
𝑶𝟐 (𝒈) → 𝑶𝟐 (𝒂𝒄)
𝑲 = [𝑶𝟐 ]𝒂𝒄⁄𝑷𝑶𝟐 (𝒈) = 𝟑𝟗 𝒑𝒑𝒎⁄𝒂𝒕𝒎 ; 𝒄𝒐𝒏𝒔𝒕𝒂𝒏𝒕𝒆 𝒅𝒆
𝒅𝒊𝒔𝒐𝒍𝒖𝒄𝒊ó𝒏 𝒅𝒆𝒍 𝒐𝒙í𝒈𝒆𝒏𝒐 𝒆𝒏 𝒂𝒈𝒖𝒂.
[𝑶𝟐 ]𝒂𝒄 = 𝑲 𝑷𝑶𝟐 (𝒈)
= (𝟑𝟗 𝒑𝒑𝒎⁄𝒂𝒕𝒎)(𝟎. 𝟐𝟏 𝒙 𝟏 𝒂𝒕𝒎)
= 𝟖. 𝟐 𝒑𝒑𝒎 = 𝟖. 𝟐 𝒎𝒈 𝑶𝟐⁄𝒍𝒕
= 𝟎. 𝟐𝟔𝒙𝟏𝟎−𝟑 𝒎𝒐𝒍 𝑶𝟐 ⁄𝒍𝒕
⇒
[𝑪𝑵−]𝒂𝒄 = 𝟔 [𝑶𝟐 ]𝒂𝒄 = 𝟔 ( 𝟎. 𝟐𝟔𝒙𝟏𝟎−𝟑 𝒎𝒐𝒍 𝑶𝟐 ⁄𝒍𝒕 )
= 𝟏. 𝟔𝟐𝒙𝟏𝟎−𝟑 𝒎𝒐𝒍 𝑪𝑵−⁄𝒍𝒕
Cambiando a % peso de NaCN:
𝑵𝒂𝑪𝑵 → 𝑵𝒂+ + 𝑪𝑵−
𝟏. 𝟔𝟐𝒙𝟏𝟎−𝟑𝒎𝒐𝒍 𝑪𝑵− 𝟒𝟗 𝒈 𝑵𝒂𝑪𝑵 𝟏 𝒎𝒐𝒍 𝑵𝒂𝑪𝑵
𝒑𝒆𝒔𝒐 𝑵𝒂𝑪𝑵 = ( )( )( )
𝒍𝒕. 𝒔𝒐𝒍 𝟏 𝒎𝒐𝒍 𝑵𝒂𝑪𝑵 𝟏 𝒎𝒐𝒍 𝑪𝑵−
= 𝟕𝟗. 𝟑𝟖𝒙𝟏𝟎−𝟑 𝒈 𝑵𝒂𝑪𝑵⁄𝒍𝒕. 𝒔𝒐𝒍
Sea: 𝜌 = 1 𝑔⁄𝑐𝑚3 , 𝑑𝑒𝑛𝑠𝑖𝑑𝑎𝑑 𝑑𝑒 𝑙𝑎 𝑠𝑜𝑙𝑢𝑐𝑖ó𝑛
⇒
𝟕𝟗. 𝟑𝟖𝒙𝟏𝟎−𝟑 𝒈 𝑵𝒂 𝑪𝑵 𝟏 𝒍𝒕. 𝒔𝒐𝒍
% 𝑵𝒂𝑪𝑵 = ( )( ) 𝒙 𝟏𝟎𝟎 = 𝟕𝟗. 𝟑𝟖𝒙𝟏𝟎−𝟒
𝒍𝒕. 𝒔𝒐𝒍 𝟏𝟎𝟎𝟎 𝒈
% 𝑵𝒂𝑪𝑵 ≅ 𝟎. 𝟎𝟎𝟖 % ≅ 𝟎. 𝟎𝟏 %
Es decir la velocidad máxima de disolución del oro, bajo condiciones ideales de
agitación y aireación debería tener lugar en soluciones con 0.008 % de 𝑁𝑎𝐶𝑁.
En la práctica la mayoría de plantas usan soluciones conteniendo menos de 0.05
% de 𝑁𝑎𝐶𝑁. El promedio general está entre 0.02 a 0.03 % de 𝑁𝑎𝐶𝑁 (esto no
aplica para minerales sulfurados).
ING. A. CORTIJO G. – DPTO. IMM – UNT. Pág. 20
METALURGIA EXTRACTIVA I: HIDROMETALURGIA
TRATAMIENTO DE SOLUCIONES DE LIXIVIACION
Precipitación selectiva de los valores metálicos en solución para purificar la
solución lixiviada o recuperar los metales de interés, empleando métodos
químicos o electroquímicos.
1. METODOS QUIMICOS:
a) PRECIPITACIÓN DE SULFUROS METÁLICOS:
- El ácido sulfhídrico puede precipitar una serie de iones metálicos mediante
un ajuste adecuado del pH de la solución:
H2S(g) = H2S(ac) = 2H+ + S2-
[𝑯+]𝟐 [𝑺𝟐−]
𝑲𝑫 = , 𝒄𝒐𝒏𝒔𝒕𝒂𝒏𝒕𝒆 𝒅𝒆 𝒅𝒊𝒔𝒐𝒄𝒊𝒂𝒄𝒊ó𝒏 𝒅𝒆𝒍 𝑯𝟐 𝑺 (𝒂𝒄)
[𝑯𝟐 𝑺]𝒂𝒄
𝑲𝑫 [𝑯𝟐 𝑺]𝒂𝒄
[𝑺𝟐−] =
[𝑯+ ]𝟐
- A condiciones estándar: 𝑇 = 25°𝐶 𝑃 = 1 𝑎𝑡𝑚.
𝑲𝑫 = 𝟏. 𝟔𝟗 𝒙 𝟏𝟎−𝟐𝟏
[𝑯𝟐 𝑺]𝒂𝒄 = 𝟎. 𝟎𝟗 𝒎𝒐𝒍⁄𝒍𝒕 , 𝒄𝒐𝒏𝒄𝒆𝒏𝒕𝒓𝒂𝒄𝒊ó𝒏 𝒅𝒆 𝒔𝒂𝒕𝒖𝒓𝒂𝒄𝒊ó𝒏 𝒅𝒆 𝑯𝟐 𝑺 𝒆𝒏 𝒂𝒈𝒖𝒂
⇒
(𝟏. 𝟔𝟗𝒙𝟏𝟎−𝟐𝟏)(𝟎. 𝟎𝟗) 𝟏. 𝟓𝟐𝒙𝟏𝟎−𝟐𝟐
[𝑺𝟐−] = =
[𝑯+ ]𝟐 [𝑯+ ]𝟐
𝐥𝐨𝐠[𝑺𝟐−] = 𝐥𝐨𝐠(𝟏. 𝟓𝟐𝒙𝟏𝟎−𝟐𝟐 ) − 𝟐 𝐥𝐨𝐠[𝑯+]
Pero: 𝒑𝑯 = − 𝐥𝐨𝐠[𝑯+]
𝐥𝐨𝐠[𝑺𝟐−] = 𝐥𝐨𝐠(𝟏. 𝟓𝟐𝒙𝟏𝟎−𝟐𝟐 ) + 𝟐𝒑𝑯 ……… (1) Tabla N° 18.1
- Para cualquier sulfuro metálico:
MmSn = m Mz+ + n S2-
𝑲𝒑𝒔 = [𝑴𝒛+]𝒎 [𝑺𝟐−]𝒏 ……… (2) Tabla N° 18.2
- Relacionando ecuaciones (1) y (2): es posible determinar la tendencia
termodinámica de un sulfuro metálico a precipitar a un pH dado:
∆𝑮𝑻 = ∆𝑮𝟎𝑻 + 𝑹𝑻 𝐥𝐧 𝑲𝒑𝒊
Donde:
𝑲𝒑𝒊 ∶ 𝑝𝑟𝑜𝑑𝑢𝑐𝑡𝑜 𝑖ó𝑛𝑖𝑐𝑜 (𝑐𝑡𝑒. 𝑑𝑒𝑙 𝑛𝑜 𝑒𝑞𝑢𝑖𝑙𝑖𝑏𝑟𝑖𝑜)
𝑲𝒑𝒔 ∶ 𝑝𝑟𝑜𝑑𝑢𝑐𝑡𝑜 𝑑𝑒 𝑠𝑜𝑙𝑢𝑏𝑖𝑙𝑖𝑑𝑎𝑑 (𝑐𝑡𝑒. 𝑑𝑒 𝑒𝑞𝑢𝑖𝑙𝑖𝑏𝑟𝑖𝑜)
ING. A. CORTIJO G. – DPTO. IMM – UNT. Pág. 21
METALURGIA EXTRACTIVA I: HIDROMETALURGIA
Entonces:
𝑺𝒊 𝑲𝒑𝒊 = 𝑲𝒑𝒔 , ∆𝑮𝑻 = 𝟎 , ⇄ , Equilibrio: La solución está saturada y
el sistema está en equilibrio con una composición constante.
𝑺𝒊 𝑲𝒑𝒊 < 𝑲𝒑𝒔 , ∆𝑮𝑻 < 0 , → , No ocurre precipitación del sulfuro: La
solución está insaturada y se puede disolver más sólido hasta alcanzar el
equilibrio.
𝑺𝒊 𝑲𝒑𝒊 > 𝑲𝒑𝒔 , ∆𝑮𝑻 > 0 , ← , Si ocurre precipitación del sulfuro: La
solución está sobresaturada y el sólido se precipitará hasta alcanzar el
equilibrio.
En el esquema anterior se observa que “si en el instante de la mezcla el 𝑲𝒑𝒊 > 𝑲𝒑𝒔 ,
habrá precipitación”, con lo que se reducen las concentraciones iónicas en solución
hasta que el 𝑲𝒑𝒊 alcance su valor de equilibrio.
- Gráfica para la precipitación de sulfuros metálicos:
De la ecuación (2):
𝑲𝒑𝒔 = [𝑴𝒛+]𝒎 [𝑺𝟐−]𝒏
𝑲𝒑𝒔
[𝑴𝒛+]𝒎 =
[𝑺𝟐−]𝒏
𝒍𝒐𝒈𝑲𝒑𝒔 𝒏 𝐥𝐨𝐠[𝑺𝟐−]
𝐥𝐨𝐠[𝑴𝒛+] = −
𝒎 𝒎
𝒀 = 𝒂 + 𝒎𝑿
0
-1 -
-2 - CuI CuII NiII MnII
𝐥𝐨𝐠[𝑴𝒛+]
-3 -
-4
-60 -45 -30 -15 0
𝐥𝐨𝐠[𝑺𝟐−]
Los sulfuros metálicos precipitan a la derecha de las rectas. Para Y = 0 , se lee los
Kps en las abscisas.
ING. A. CORTIJO G. – DPTO. IMM – UNT. Pág. 22
METALURGIA EXTRACTIVA I: HIDROMETALURGIA
b) PRECIPITACIÓN DE HIDRÓXIDOS METÁLICOS (POR CAMBIO DE PH):
- Para cualquier hidróxido metálico:
𝑴(𝑶𝑯)𝒏 = 𝑴𝒛+ + 𝒏 𝑶𝑯−
𝑲𝒑𝒔 = [𝑴𝒛+] [𝑶𝑯− ]𝒏 ……… TABLA N° 4.3
Con los datos de 𝐾𝑝𝑠 es posible determinar la tendencia termodinámica de un
hidróxido metálico a precipitar a un pH dado o calcular el pH al cual la
hidrólisis (precipitación) no puede ocurrir:
∆𝑮𝑻 = ∆𝑮𝟎𝑻 + 𝑹𝑻 𝐥𝐧 𝑲𝒑𝒊
𝒂𝒑𝒓𝒐𝒅.
∆𝑮𝑻 = ∆𝑮𝟎𝑻 + 𝑹𝑻 𝐥𝐧 (𝒂 )
𝒓𝒆𝒂𝒄𝒕.
Donde: 𝒑𝑯 = − 𝐥𝐨𝐠 𝒂𝑯+ = − 𝐥𝐨𝐠[𝑯+ ]
𝒑𝑶𝑯 = − 𝐥𝐨𝐠 𝒂𝑶𝑯− = − 𝐥𝐨𝐠[𝑶𝑯− ]
⇒
𝑺𝒊 𝒑𝑯 = 𝒑𝑯𝒆𝒒. , ∆𝑮𝑻 = 𝟎 , ⇄ , 𝑬𝑸𝑼𝑰𝑳𝑰𝑩𝑹𝑰𝑶 (𝑠𝑜𝑙𝑢𝑐𝑖ó𝑛 𝑠𝑎𝑡𝑢𝑟𝑎𝑑𝑎 𝑑𝑒 𝑖ó𝑛 𝑚𝑒𝑡á𝑙𝑖𝑐𝑜)
𝑺𝒊 𝒑𝑯 < 𝒑𝑯𝒆𝒒. , ∆𝑮𝑻 < 0 , → , 𝑵𝑶 𝑶𝑪𝑼𝑹𝑹𝑬 𝑷𝑷𝑻𝑪𝑰𝑶𝑵. 𝑫𝑬𝑳 𝑯𝑰𝑫𝑹𝑶𝑿𝑰𝑫𝑶
(𝑠𝑜𝑙𝑢𝑐𝑖ó𝑛 𝑖𝑛𝑠𝑎𝑡𝑢𝑟𝑎𝑑𝑎 𝑑𝑒 𝑖ó𝑛 𝑚𝑒𝑡á𝑙𝑖𝑐𝑜)
𝑺𝒊 𝒑𝑯 > 𝒑𝑯𝒆𝒒. , ∆𝑮𝑻 > 0 , ← , 𝑺𝑰 𝑶𝑪𝑼𝑹𝑹𝑬 𝑷𝑷𝑻𝑪𝑰𝑶𝑵. 𝑫𝑬𝑳 𝑯𝑰𝑫𝑹𝑶𝑿𝑰𝑫𝑶
(𝑠𝑜𝑙𝑢𝑐𝑖ó𝑛 𝑠𝑜𝑏𝑟𝑒𝑠𝑎𝑡𝑢𝑟𝑎𝑑𝑎 𝑑𝑒 𝑖ó𝑛 𝑚𝑒𝑡á𝑙𝑖𝑐𝑜)
- Gráfica para la precipitación de hidróxidos metálicos:
𝑲𝒑𝒔 = [𝑴𝒛+] [𝑶𝑯− ]𝒏
𝑲𝒑𝒔
[𝑴𝒛+] =
[𝑶𝑯−]𝒏
𝐥𝐨𝐠[𝑴𝒛+] = 𝐥𝐨𝐠 𝑲𝒑𝒔 − 𝒏 𝐥𝐨𝐠[𝑶𝑯− ]
Pero: 𝑲𝒘 = [𝑯+ ] [𝑶𝑯−] = 𝟏𝟎−𝟏𝟒 , 𝒄𝒐𝒏𝒔𝒕𝒂𝒏𝒕𝒆 𝒅𝒆 𝒅𝒊𝒔𝒐𝒄𝒊𝒂𝒄𝒊ó𝒏 𝒅𝒆𝒍 𝒂𝒈𝒖𝒂
𝑲𝒘
[𝑶𝑯−] =
[𝑯+ ]
𝑲
⇒ 𝐥𝐨𝐠[𝑴𝒛+] = 𝐥𝐨𝐠 𝑲𝒑𝒔 − 𝒏 𝐥𝐨𝐠 ([𝑯𝒘+ ])
𝐥𝐨𝐠[𝑴𝒛+] = 𝐥𝐨𝐠 𝑲𝒑𝒔 − 𝒏 𝐥𝐨𝐠 𝑲𝒘 + 𝒏 𝐥𝐨𝐠[𝑯+ ]
𝐥𝐨𝐠[𝑴𝒛+] = 𝐥𝐨𝐠 𝑲𝒑𝒔 − 𝒏 𝐥𝐨𝐠 𝑲𝒘 − 𝒏 𝒑𝑯
𝐘 = 𝐚 + 𝐦𝐗
ING. A. CORTIJO G. – DPTO. IMM – UNT. Pág. 23
METALURGIA EXTRACTIVA I: HIDROMETALURGIA
-2 0 2 4 6 8 10 12 14
0
-1
𝒍𝒐𝒈 [𝑴𝒛+] -2
𝑭𝑰𝑰𝑰
𝒆 𝒁𝒏𝑰𝑰 𝑴𝒏𝑰𝑰
-3
-4
-2 0 2 4 6 8 10 12 14
pH
La precipitación del hidróxido metálico ocurre a la derecha de las líneas.
c) PRECIPITACIÓN DE CARBONATOS:
- El CO2 (g) se disuelve en agua formando el ácido débil H2CO3(ac):
𝑪𝑶𝟐 (𝒈) = 𝑯𝟐 𝑪𝑶𝟑 (𝒂𝒄) = 𝑪𝑶𝟐−
𝟑 + 𝟐𝑯+
[𝑪𝑶𝟐− + 𝟐
𝟑 ] [𝑯 ]
𝑲𝑫 = , 𝒄𝒐𝒏𝒔𝒕𝒂𝒏𝒕𝒆 𝒅𝒆 𝒅𝒊𝒔𝒐𝒄𝒊𝒂𝒄𝒊ó𝒏 𝒅𝒆𝒍 𝑯𝟐 𝑪𝑶𝟑 (𝒂𝒄) 𝒆𝒏 𝒂𝒈𝒖𝒂
[𝑯𝟐 𝑪𝑶𝟑 ]𝒂𝒄
𝑲𝑫[𝑯𝟐 𝑪𝑶𝟑 ]𝒂𝒄
[𝑪𝑶𝟐−
𝟑 ] =
[𝑯+]𝟐
- A condiciones estándar: 𝑇 = 250 𝐶 , 𝑃𝐶𝑂2 (𝑔) = 1 𝑎𝑡𝑚
𝑲𝑫 = 𝟐. 𝟎𝟖 𝒙 𝟏𝟎−𝟏𝟕
[𝑯𝟐 𝑪𝑶𝟑 ]𝒂𝒄 = 𝟎. 𝟑𝟒 𝑴 , 𝒄𝒐𝒏𝒄𝒆𝒏𝒕𝒓𝒂𝒄𝒊ó𝒏 𝒅𝒆 𝒔𝒂𝒕𝒖𝒓𝒂𝒄𝒊ó𝒏 𝒅𝒆𝒍 𝑯𝟐 𝑪𝑶𝟑 𝒆𝒏 𝒂𝒈𝒖𝒂.
⇒
(𝟐. 𝟎𝟖𝒙𝟏𝟎−𝟏𝟕)(𝟎. 𝟎𝟑𝟒) 𝟕. 𝟎𝟕𝟐𝒙𝟏𝟎−𝟏𝟗
[𝑪𝑶𝟐−
𝟑 ] = =
[𝑯+]𝟐 [𝑯+]𝟐
𝒍𝒐𝒈 [𝑪𝑶𝟐−
𝟑 ] = 𝒍𝒐𝒈 (𝟕. 𝟎𝟕𝟐𝒙𝟏𝟎
−𝟏𝟗 )
+ 𝟐𝒑𝑯 ……… (1)
- Para cualquier carbonato metálico:
𝑴𝒎 (𝑪𝑶𝟑)𝒏 = 𝒎 𝑴𝒛+ + 𝒏 𝑪𝑶𝟐−
𝟑
𝒏
𝑲𝒑𝒔 = [𝑴𝒛+]𝒎 [𝑪𝑶𝟐−
𝟑 ] TABLA N° 4.4 ………. (2)
ING. A. CORTIJO G. – DPTO. IMM – UNT. Pág. 24
METALURGIA EXTRACTIVA I: HIDROMETALURGIA
Relacionando ecuaciones (1) y (2) es posible determinar la tendencia termodinámica
de un carbonato metálico a precipitar a un pH dado:
∆𝑮𝑻 = ∆𝑮𝟎𝑻 + 𝑹𝑻 𝐥𝐧 𝑲𝒑𝒊
Donde: 𝑲𝒑𝒊 : 𝑝𝑟𝑜𝑑𝑢𝑐𝑡𝑜 𝑖ó𝑛𝑖𝑐𝑜 (𝑐𝑜𝑛𝑠𝑡𝑎𝑛𝑡𝑒 𝑑𝑒𝑙 𝑛𝑜 𝑒𝑞𝑢𝑖𝑙𝑖𝑏𝑟𝑖𝑜)
𝑲𝒑𝒔 : 𝑝𝑟𝑜𝑑𝑢𝑐𝑡𝑜 𝑑𝑒 𝑠𝑜𝑙𝑢𝑏𝑖𝑙𝑖𝑑𝑎𝑑 (𝑐𝑜𝑛𝑠𝑡𝑎𝑛𝑡𝑒 𝑑𝑒 𝑒𝑞𝑢𝑖𝑙𝑖𝑏𝑟𝑖𝑜)
⟹
𝑺𝒊 𝑲𝒑𝒊 = 𝑲𝒑𝒔 , ∆𝑮𝑻 = 𝟎 , ⇄ 𝑬𝑸𝑼𝑰𝑳𝑰𝑩𝑹𝑰𝑶
𝑺𝒊 𝑲𝒑𝒊 < 𝑲𝒑𝒔 , ∆𝑮𝑻 < 𝟎 , → 𝑵𝑶 𝑶𝑪𝑼𝑹𝑹𝑬 𝑷𝑷𝑻𝑪𝑰𝑶𝑵. 𝑫𝑬𝑳 𝑪𝑨𝑹𝑩𝑶𝑵𝑨𝑻𝑶
𝑺𝒊 𝑲𝒑𝒊 > 𝑲𝒑𝒔 , ∆𝑮𝑻 > 𝟎 , ← 𝑺𝑰 𝑶𝑪𝑼𝑹𝑹𝑬 𝑷𝑷𝑻𝑪𝑰𝑶𝑵. 𝑫𝑬𝑳 𝑪𝑨𝑹𝑩𝑶𝑵𝑨𝑻𝑶
- Gráfica para la precipitación de carbonatos metálicos:
𝒏
𝑲𝒑𝒔 = [𝑴𝒛+]𝒎 [𝑪𝑶𝟐−
𝟑 ]
𝑲𝒑𝒔
[𝑴𝒛+]𝒎 =
[𝑪𝑶𝟐−
𝟑 ]
𝒏
𝒛+ ]
𝒍𝒐𝒈 𝑲𝒑𝒔 𝒏𝒍𝒐𝒈 [𝑪𝑶𝟐−
𝟑 ]
𝒍𝒐𝒈 [𝑴 = −
𝒎 𝒎
𝒀 = 𝒂 + 𝒎𝑿
-20 -15 -10 -5 0 5 10 15
0
-1 si ppta. PbCO3
𝒍𝒐𝒈 [𝑴𝒛+] -2 no ppta.
𝑷𝒃𝑰𝑰
-3
-4
-20 -15 -10 -5 0 5 10 15
𝒍𝒐𝒈 [𝑪𝑶𝟐−
𝟑 ]
La precipitación del carbonato metálico se efectúa a la derecha de las rectas.
ING. A. CORTIJO G. – DPTO. IMM – UNT. Pág. 25
METALURGIA EXTRACTIVA I: HIDROMETALURGIA
2. MÉTODOS ELECTROQUÍMICOS:
d) CEMENTACIÓN:
Es la precipitación de un ión metálico de una solución acuosa por la adición de
un metal sólido más activo que el metal a precipitar, formándose una celda de
corrosión galvánica.
La condición termodinámica del proceso radica en la diferencia de los
potenciales de equilibrio. Para reducir un ión metálico en solución es
necesario que el potencial del agente reductor sea más negativo que el
potencial del sistema metálico a reducir.
LADO CATODICO E0 , voltios
𝑨𝒖𝟑+/𝑨𝒖 1.45
𝑷𝒕𝟐+⁄𝑷𝒕 1.20
𝑪𝒖𝟐+⁄𝑪𝒖 0.34
𝑯+ ⁄𝑯𝟐 0.00 “Potenciales estándar
𝑵𝒊𝟐+⁄𝑵𝒊 - 0.25 de reducción”.
𝑪𝒐𝟐+⁄𝑪𝒐 - 0.28
𝑪𝒅𝟐+⁄𝑪𝒅 - 0.402
𝑭𝒆𝟐+⁄𝑭𝒆 - 0.44
𝒁𝒏𝟐+⁄𝒁𝒏 - 0.763
LADO ANODICO
Ejemplo:
Cementación de Cu2+ sobre chatarra de Fe:
R.C: 𝑪𝒖𝟐+ + 𝟐𝒆− = 𝑪𝒖 𝐸𝑐0 = 0.344 𝑉
R.A: 𝑭𝒆 = 𝑭𝒆𝟐+ + 𝟐𝒆− 𝐸𝑎0 = −0.44
--------------------------------------------------------------------------------------------
R.T: 𝑪𝒖𝟐+ + 𝑭𝒆 = 𝑪𝒖 + 𝑭𝒆𝟐+ ∆𝐸0 = 𝐸𝑐0 − 𝐸𝑎0
𝑹𝑻
𝑬𝒄 = 𝑬𝟎𝑪𝒖 + 𝐥𝐧 𝒂𝑪𝒖𝟐+
𝒛𝑭
𝑹𝑻
𝑬𝒂 = 𝑬𝟎𝑭𝒆 + 𝐥𝐧 𝒂𝑭𝒆𝟐+
𝒛𝑭
∆𝑬𝒓 = 𝑬𝒄 − 𝑬𝒂 (Convenio Americano)
ING. A. CORTIJO G. – DPTO. IMM – UNT. Pág. 26
METALURGIA EXTRACTIVA I: HIDROMETALURGIA
⇒
𝑹𝑻 𝒂 𝟐+
∆𝑬𝒓 = ∆𝑬𝟎𝒓 − 𝐥𝐧 ( 𝑭𝒆 )
𝒛𝑭 𝒂𝑪𝒖𝟐+
𝟎. 𝟎𝟓𝟗𝟏 𝒂𝒑𝒓𝒐𝒅
∆𝑬𝒓 = ∆𝑬𝟎𝒓 − 𝐥𝐨𝐠 ( )
𝒛 𝒂𝒓𝒆𝒂𝒄
𝟎. 𝟎𝟓𝟗𝟏 [𝑭𝒆𝟐+]
∆𝑬𝒓 = ∆𝑬𝟎𝒓 − 𝐥𝐨𝐠 ( )
𝒛 [𝑪𝒖𝟐+]
∆𝑮𝒓 = −𝒛 𝑭 ∆𝑬𝒓
∆𝑬𝒓 = 𝟎 , ∆𝑮𝒓 = 𝟎 , ⇄ 𝑬𝑸𝑼𝑰𝑳𝑰𝑩𝑹𝑰𝑶
∆𝑬𝒓 > 𝟎 , ∆𝑮𝒓 < 𝟎 , → 𝑺𝑰 𝑶𝑪𝑼𝑹𝑹𝑬 𝑪𝑬𝑴𝑬𝑵𝑻𝑨𝑪𝑰𝑶𝑵
∆𝑬𝒓 < 𝟎 , ∆𝑮𝒓 > 𝟎 , ← 𝑵𝑶 𝑶𝑪𝑼𝑹𝑹𝑬 𝑪𝑬𝑴𝑬𝑵𝑻𝑨𝑪𝑰𝑶𝑵
- A condiciones estándar: P = 1 atm T = 250C (2980K) [ión] = 1M
𝟎. 𝟎𝟓𝟗𝟏 𝟏
∆𝑬𝒓 = ∆𝑬𝟎𝒓 − 𝐥𝐨𝐠 ( )
𝒛 𝟏
0
∆𝑬𝒓 = ∆𝑬𝟎𝒓 = 𝑬𝟎𝒄 − 𝑬𝟎𝒂 = 0.34 − (−044) = 𝟎. 𝟕𝟖 𝑽 > 0
∆𝑮𝒓 = −𝒛 𝑭 ∆𝑬𝒓 = −(2)(96487 𝐽⁄𝑚𝑜𝑙. 𝑉 )(0.78 𝑉 ) = −𝟏𝟓𝟎𝟓𝟐𝟎 𝑱⁄𝒎𝒐𝒍 < 0
Por lo tanto si ocurre la cementación a condiciones estándar.
e) PRECIPITACIÓN CON GASES:
R.C: 𝑴𝒛+ + 𝒛𝒆− = 𝑴 𝑬𝟎𝒄 = 𝑬𝟎𝑴𝒛+ ⁄𝑴
𝒛
R.A: 𝑯𝟐 (𝒈) = 𝒛 𝑯+ + 𝒛𝒆− 𝑬𝟎𝒂 = 𝑬𝟎 𝑯+⁄𝑯𝟐 (𝒈)
𝟐
-------------------------------------------------------------------------------------------------------
𝒛
R.T: 𝑴𝒛+ + 𝑯𝟐 (𝒈) = 𝑴 + 𝒛𝑯+
𝟐
𝟎. 𝟎𝟓𝟗𝟏 [𝑯+]𝒛
∆𝑬𝒓 = ∆𝑬𝟎𝒓 − 𝒍𝒐𝒈 ( 𝒛⁄𝟐 )
𝒛 𝑷𝑯𝟐 [𝑴𝒛+]
∆𝑮𝒓 = −𝒛 𝑭 ∆𝑬𝒓
∆𝑬𝒓 = 𝟎 , ∆𝑮𝒓 = 𝟎 , ⇄ 𝑬𝑸𝑼𝑰𝑳𝑰𝑩𝑹𝑰𝑶
∆𝑬𝒓 > 𝟎 , ∆𝑮𝒓 < 𝟎 , → 𝑺𝑰 𝑷𝑹𝑬𝑪𝑰𝑷𝑰𝑻𝑨 𝑪𝑶𝑵 𝑯𝟐 (𝒈)
∆𝑬𝒓 < 𝟎 , ∆𝑮𝒓 > 𝟎 , ← 𝑵𝑶 𝑷𝑹𝑬𝑪𝑰𝑷𝑰𝑻𝑨 𝑪𝑶𝑵 𝑯𝟐 (𝒈)
ING. A. CORTIJO G. – DPTO. IMM – UNT. Pág. 27
METALURGIA EXTRACTIVA I: HIDROMETALURGIA
- En el equilibrio:
∆𝑬𝒓 = 𝑬𝒄 − 𝑬𝒂 = 𝟎
⇒ 𝑬𝒄 = 𝑬𝒂
0
𝟎. 𝟎𝟓𝟗𝟏 𝟎. 𝟎𝟓𝟗𝟏 [𝑯+ ]𝒛
𝑬𝟎𝑴𝒛+ ⁄𝑴 + 𝒛+ 𝟎
𝒍𝒐𝒈 [𝑴 ] = 𝑬𝑯+⁄𝑯𝟐 + 𝒍𝒐𝒈 ( 𝒛⁄𝟐 )
𝒛 𝒛 𝑷𝑯𝟐
Pero: 𝒑𝑯 = −𝒍𝒐𝒈 [𝑯+]
Entonces:
𝟎. 𝟎𝟓𝟗𝟏
𝑬𝟎𝑴𝒛+ ⁄𝑴 + 𝒍𝒐𝒈 [𝑴𝒛+] = −𝟎. 𝟎𝟓𝟗𝟏 𝒑𝑯 − 𝟎. 𝟎𝟐𝟗𝟔 𝒍𝒐𝒈 𝑷𝑯𝟐 (𝒈)
𝒛
Para una presión dada del H2(g) el equilibrio entre [𝑴𝒛+] 𝑦 [𝑯+] se puede
expresar en términos del pH para una actividad específica del ión metálico en
solución.
- Gráfica E vs pH:
𝒍𝒐𝒈 [𝑴𝒛+]
-6 -5 -4 -3 -2 -1 0
-
0.2
0 Mz+ + ze = M
E, v z/2 H2(g) = zH+ + ze
- 0.2
-0.4
0 𝒑𝑯𝒆𝒒 14
Es decir para precipitar al ión metálico en solución con gas hidrógeno depende del
pH de la solución en la cual se insufla el gas. Este tiene que ser mayor que el pH de
equilibrio para que se cumpla: ∆𝑬𝒓 > 𝟎 ⇒ ∆𝑮𝒓 < 𝟎
ING. A. CORTIJO G. – DPTO. IMM – UNT. Pág. 28
Вам также может понравиться
- Hidrometalurgia: procesos de lixiviaciónДокумент23 страницыHidrometalurgia: procesos de lixiviaciónANTONI KEYVI MENDOZA GUTIERREZОценок пока нет
- LixiviacionДокумент24 страницыLixiviacionAndres ContrerasОценок пока нет
- Procesos de Concentracion de SolucionesДокумент33 страницыProcesos de Concentracion de SolucionesDarioОценок пока нет
- Unidad I Hidrometalurgia AglomeraciónДокумент60 страницUnidad I Hidrometalurgia AglomeraciónAlex RodríguezОценок пока нет
- Purificación LixiviadaДокумент13 страницPurificación LixiviadamarianaОценок пока нет
- Concentración o Purificación de La Solución ObtenidaДокумент36 страницConcentración o Purificación de La Solución ObtenidaZeballos CarlosОценок пока нет
- 14lixiviación Espesamiento - FiltradoДокумент49 страниц14lixiviación Espesamiento - FiltradoGINA LINO RODRÍGUEZОценок пока нет
- Tema 4A LixiviacionДокумент13 страницTema 4A LixiviacionAle Calixto HermosillaОценок пока нет
- Cuestionario Concentrado de MineralesДокумент11 страницCuestionario Concentrado de MineralesCarlos Anco YucraОценок пока нет
- Disolucion y DisgregaciónДокумент26 страницDisolucion y DisgregaciónSelenita PS67% (3)
- Analisis Generalidades de Volumetría Redox - EstudiantesДокумент6 страницAnalisis Generalidades de Volumetría Redox - EstudiantesMaritza DiazОценок пока нет
- Tarea DomiciliariaДокумент13 страницTarea DomiciliariaJesus Gelder Zarate CastroОценок пока нет
- Purificacion y ConcentracionДокумент31 страницаPurificacion y ConcentracionAmaral Coaguila100% (1)
- Uap HidrometalurgiaДокумент55 страницUap HidrometalurgiaFrankin Alex Quispe VeraОценок пока нет
- Presentación Flotacion OXIDOSДокумент28 страницPresentación Flotacion OXIDOSluis miguel saavedraОценок пока нет
- Clase 1 Metales No FerrososДокумент33 страницыClase 1 Metales No FerrososAnthony Quispe CarbajalОценок пока нет
- Procesos de extracción de cobre por hidrometalurgiaДокумент23 страницыProcesos de extracción de cobre por hidrometalurgiaJazmina PintoОценок пока нет
- Agentes Lixiviantes PDFДокумент32 страницыAgentes Lixiviantes PDFAlba Limon ManzanoОценок пока нет
- Trabajo Hidrometalurgia RREДокумент26 страницTrabajo Hidrometalurgia RREJose Ignacio Salas B.Оценок пока нет
- Informe Lixiviación.Документ31 страницаInforme Lixiviación.Braulio Ceballos Santander100% (1)
- LixiivacionДокумент32 страницыLixiivacionFRANCISCO SEPULVEDAОценок пока нет
- Soluciones de lixiviación de metalesДокумент96 страницSoluciones de lixiviación de metalesartaxlateОценок пока нет
- Hidrometalurgia: procesos de lixiviación de mineralesДокумент21 страницаHidrometalurgia: procesos de lixiviación de mineralessara richardsОценок пока нет
- Resultados de La Practica 4 de Quimica AnaliticaДокумент6 страницResultados de La Practica 4 de Quimica AnaliticaGabriela Ramirez100% (1)
- Termodinamica y HidrometalurgiaДокумент55 страницTermodinamica y Hidrometalurgiafrank100% (3)
- LIXIVIACION (Modo de Compatibilidad) PDFДокумент54 страницыLIXIVIACION (Modo de Compatibilidad) PDFViviana SanabriaОценок пока нет
- LixiviacionДокумент9 страницLixiviacionMalthus DiОценок пока нет
- HIDROMETALURGIAДокумент17 страницHIDROMETALURGIAKevin QFОценок пока нет
- Lixiviacion de CalcopiritaДокумент12 страницLixiviacion de CalcopiritaWilliy126Оценок пока нет
- SESIÓN #1 Hidrometalurgia Definición, Ventajas y DesventajasДокумент26 страницSESIÓN #1 Hidrometalurgia Definición, Ventajas y DesventajasLourdesОценок пока нет
- Corrosión metalesДокумент7 страницCorrosión metalesRicardo AvilaОценок пока нет
- PhemmДокумент197 страницPhemmisabel mancillaОценок пока нет
- Uap HidrometalurgiaДокумент55 страницUap Hidrometalurgialuis renzo mamani allasiОценок пока нет
- DETERMINACIÓN DE METALES PESADOS MEDIANTE REACTIVOS QUELANTESДокумент4 страницыDETERMINACIÓN DE METALES PESADOS MEDIANTE REACTIVOS QUELANTESDamОценок пока нет
- HIDROMETALURGIAДокумент16 страницHIDROMETALURGIAJimmy ChuquicondoОценок пока нет
- Hidrometalurgia del cobre en Chile: operaciones metalúrgicas de extracción vía húmedaДокумент105 страницHidrometalurgia del cobre en Chile: operaciones metalúrgicas de extracción vía húmedaFelipe Andres Santiago DiazОценок пока нет
- AAI OPHI01 Guia 1 HidrometalurgiaДокумент12 страницAAI OPHI01 Guia 1 HidrometalurgiaAlmacén AndrewОценок пока нет
- Clase #3 Coagulacion y FloculacionДокумент57 страницClase #3 Coagulacion y Floculacionmiluska garciaОценок пока нет
- Tratamiento de SolucionesДокумент96 страницTratamiento de SolucionesCristian Serrano ArayaОценок пока нет
- Reactivos para La Lixiviacion Del CobreДокумент22 страницыReactivos para La Lixiviacion Del CobreHANZ LEONОценок пока нет
- Adsorción en Carbon ActivadoДокумент11 страницAdsorción en Carbon Activadojlls21Оценок пока нет
- Curso Lixiviacion en Pilas Ucn 2014 FinalДокумент95 страницCurso Lixiviacion en Pilas Ucn 2014 FinalPatricio Pasten CruzОценок пока нет
- Tipos de LIXIVIACIÓN InformeДокумент3 страницыTipos de LIXIVIACIÓN InformealexОценок пока нет
- Clase - 27 08 2019Документ15 страницClase - 27 08 2019Bart FrienderОценок пока нет
- Curso de Hidrometalurgia Del Au, Ag y CuДокумент31 страницаCurso de Hidrometalurgia Del Au, Ag y Cunickel de la cruz fortuna100% (12)
- Curso Concentración Minerales CuestionarioДокумент6 страницCurso Concentración Minerales CuestionarioPablo LauraОценок пока нет
- Tratamiento de Materia Inorganica en Aguas ResidualesДокумент41 страницаTratamiento de Materia Inorganica en Aguas ResidualesJenn Rizzo100% (1)
- Informe de Laboratorio Cationes Del Grupo 4Документ16 страницInforme de Laboratorio Cationes Del Grupo 4Kevin CelisОценок пока нет
- Lixiviación Básica y ÁcidaДокумент9 страницLixiviación Básica y Ácidacathy_ariesОценок пока нет
- Resumen Extracción y DespojoДокумент29 страницResumen Extracción y DespojoJimmy RedsОценок пока нет
- Elementos Grupo IAДокумент34 страницыElementos Grupo IAMelissa VasquezОценок пока нет
- Cationes Grupo 2Документ23 страницыCationes Grupo 2jhoniОценок пока нет
- 3 - LixiviaciónДокумент22 страницы3 - LixiviaciónMichel MancillaОценок пока нет
- Metal Ext II Cuestionario 3 VELÁSQUEZ NAYSMARYS.Документ13 страницMetal Ext II Cuestionario 3 VELÁSQUEZ NAYSMARYS.Ricardo RondonОценок пока нет
- Clase 3 BiometalurgiaДокумент32 страницыClase 3 BiometalurgiaronaldОценок пока нет
- (PEP I) 2. Lixiviacion y Diagramas de Pourbaix (Clase 02 04 2019)Документ39 страниц(PEP I) 2. Lixiviacion y Diagramas de Pourbaix (Clase 02 04 2019)Bart FrienderОценок пока нет
- Desintoxicación Con Cilantro - Basado En Las Enseñanzas De Frank Suarez: El Camino Hacia Una Vida Libre De ToxinasОт EverandDesintoxicación Con Cilantro - Basado En Las Enseñanzas De Frank Suarez: El Camino Hacia Una Vida Libre De ToxinasОценок пока нет
- Historia ReferenciasДокумент2 страницыHistoria ReferenciasJenisser Avalos VasquezОценок пока нет
- Clasificación en HúmedoДокумент28 страницClasificación en HúmedoLuis Rodriguez GonzalesОценок пока нет
- S12 Superamos Dificultades en El Juego y Nos Adaptamos A Los CambiosДокумент2 страницыS12 Superamos Dificultades en El Juego y Nos Adaptamos A Los CambiosJenisser Avalos VasquezОценок пока нет
- Problemática Ambiental Por La Quema de Caña de AzúcarДокумент2 страницыProblemática Ambiental Por La Quema de Caña de AzúcarJenisser Avalos VasquezОценок пока нет
- Conminución energíaДокумент37 страницConminución energíaJheraly M. Velasquez Mauricio67% (3)
- Vida Util EconómicaДокумент6 страницVida Util EconómicaJenisser Avalos VasquezОценок пока нет
- FundamentosДокумент6 страницFundamentosJenisser Avalos VasquezОценок пока нет
- Informe Del Laboratorio de Metalurgia FisicaДокумент2 страницыInforme Del Laboratorio de Metalurgia FisicaJenisser Avalos VasquezОценок пока нет
- Obtencion de Gal FinalДокумент44 страницыObtencion de Gal FinalJenisser Avalos VasquezОценок пока нет
- 2015 Obtencion de Un Polimero BiodegradableДокумент53 страницы2015 Obtencion de Un Polimero BiodegradableJenisser Avalos VasquezОценок пока нет
- Azucar RbiaДокумент18 страницAzucar RbiaJenisser Avalos VasquezОценок пока нет
- Ejercicio D2 WankaДокумент4 страницыEjercicio D2 WankaJenisser Avalos VasquezОценок пока нет
- Informe Del Laboratorio de Metalurgia FisicaДокумент2 страницыInforme Del Laboratorio de Metalurgia FisicaJenisser Avalos VasquezОценок пока нет
- Azucar de PanelaДокумент7 страницAzucar de PanelaJenisser Avalos VasquezОценок пока нет
- ALUMINIO CaratulaДокумент1 страницаALUMINIO CaratulaJenisser Avalos VasquezОценок пока нет
- Bomba, Aeroenfriador y Tanque de PropanoДокумент1 страницаBomba, Aeroenfriador y Tanque de PropanoJenisser Avalos VasquezОценок пока нет
- Procesos Leblanc y SolvayДокумент14 страницProcesos Leblanc y SolvayGersonGarcíaSánchezОценок пока нет
- Impacto AmbientalДокумент3 страницыImpacto AmbientalJenisser Avalos VasquezОценок пока нет
- Una Revisión de Las Propiedades Físico TraduccionДокумент24 страницыUna Revisión de Las Propiedades Físico TraduccionJenisser Avalos VasquezОценок пока нет
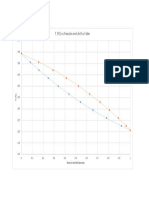
- T (ºC) Vs Fracción Mol de B A 3 AtmДокумент1 страницаT (ºC) Vs Fracción Mol de B A 3 AtmJenisser Avalos VasquezОценок пока нет
- 4 Pulpas y DiluciónДокумент9 страниц4 Pulpas y DiluciónjimenaОценок пока нет
- Horario ViiДокумент3 страницыHorario ViiJenisser Avalos VasquezОценок пока нет
- Cinética 111Документ25 страницCinética 111Jenisser Avalos VasquezОценок пока нет
- 12 11-ArevaloДокумент2 страницы12 11-ArevaloJenisser Avalos Vasquez100% (1)
- 1ra. Practica PII 2018Документ1 страница1ra. Practica PII 2018Diana De La CruzОценок пока нет
- 9 7y9 8Документ3 страницы9 7y9 8Jenisser Avalos VasquezОценок пока нет
- 1.carátula Iinforme PII-I-2018Документ1 страница1.carátula Iinforme PII-I-2018Jenisser Avalos VasquezОценок пока нет
- 1.guia Expo. Pii-2018Документ1 страница1.guia Expo. Pii-2018Jenisser Avalos VasquezОценок пока нет
- 1.carátula Iinforme PII-I-2018Документ1 страница1.carátula Iinforme PII-I-2018Jenisser Avalos VasquezОценок пока нет
- Comparación de Mediciónes Analógicas y DigitalesДокумент26 страницComparación de Mediciónes Analógicas y DigitalesCarlos UsuaОценок пока нет
- Planetas JovianosДокумент3 страницыPlanetas JovianosFernando Victor Quineche LinoОценок пока нет
- Origen de Los Ciclos BiogeoquimicosДокумент5 страницOrigen de Los Ciclos BiogeoquimicosDeygor VJОценок пока нет
- Linea Del Tiempo de Acontecimientos Importantes en La Hidrometalurgia EliasДокумент3 страницыLinea Del Tiempo de Acontecimientos Importantes en La Hidrometalurgia EliasElias OrtegaОценок пока нет
- Análisis de Señales AleatoriasДокумент35 страницAnálisis de Señales AleatoriasMauricio MillánОценок пока нет
- 05 Uso de GIMP Orientado Retoque de Imagenes Digitales. NivelДокумент43 страницы05 Uso de GIMP Orientado Retoque de Imagenes Digitales. NivelMartin GuerreroОценок пока нет
- Constante de Enfriamiento Del AguaДокумент4 страницыConstante de Enfriamiento Del AguaIván Cruz PacaraОценок пока нет
- Granulometria de SedimentosДокумент9 страницGranulometria de SedimentosGuillermo Andree Fernandez CruzОценок пока нет
- Funciones Químicas Inorgánicas Guía 1 PDFДокумент7 страницFunciones Químicas Inorgánicas Guía 1 PDFvalentinaОценок пока нет
- Beacon SpanishДокумент1 страницаBeacon SpanishJuan CarlosОценок пока нет
- Módulo de Cáculos EstequeométricosДокумент2 страницыMódulo de Cáculos EstequeométricosPablo Jesús ArreguiОценок пока нет
- Cap (03) - 3 Tablas de Vapor Con EESДокумент32 страницыCap (03) - 3 Tablas de Vapor Con EESTeofilo Donaires Flores100% (2)
- Determinacion de MineralesДокумент40 страницDeterminacion de MineralesLuis Ignacio VillaneОценок пока нет
- Eficiencia de un sistema de pistón para fluidos compresibles e incompresiblesДокумент13 страницEficiencia de un sistema de pistón para fluidos compresibles e incompresiblesGvillermo OviedoОценок пока нет
- La Mecanica de Rocas en Mineria SubterraneaДокумент14 страницLa Mecanica de Rocas en Mineria SubterraneaJunior Vasquez100% (1)
- Calculos Tuberías de Gas en Baja PresiónДокумент4 страницыCalculos Tuberías de Gas en Baja PresiónArmando SoteroОценок пока нет
- Protocolo Emergencia - Corte de EnergíaДокумент2 страницыProtocolo Emergencia - Corte de EnergíamglorenaОценок пока нет
- Practica 3 Lab TermoДокумент7 страницPractica 3 Lab TermoMarcoCarreónОценок пока нет
- Ejercicios de Una Dimensión (Resumen) - 1Документ3 страницыEjercicios de Una Dimensión (Resumen) - 1Daniel Osorio RОценок пока нет
- Frenos-Abs Con AnalisisДокумент16 страницFrenos-Abs Con AnalisisPepe RodríguezОценок пока нет
- Invernadero Con Botellas de PlasticoДокумент25 страницInvernadero Con Botellas de PlasticoCrisamu MoradarОценок пока нет
- An El Vazquez MartinezДокумент58 страницAn El Vazquez MartinezvidriosОценок пока нет
- Marco TeoricoДокумент2 страницыMarco Teoricojefferson timbilaОценок пока нет
- Pregunta Sins Tru Prueba 1Документ25 страницPregunta Sins Tru Prueba 1Carlos Alberto Andrade NaranjoОценок пока нет
- Construcción de Curvas de ValoraciónДокумент38 страницConstrucción de Curvas de ValoraciónAngel HernandezОценок пока нет
- Marco Teórico Satisfaccion LaboralДокумент3 страницыMarco Teórico Satisfaccion LaboralClauОценок пока нет
- Esfuerzos Caracteristicos PDFДокумент49 страницEsfuerzos Caracteristicos PDFGenaro LabrinОценок пока нет