Академический Документы
Профессиональный Документы
Культура Документы
Delo Piloto Prueba ICFES
Загружено:
Carlos Andrés Cantillo JiménezОригинальное название
Авторское право
Доступные форматы
Поделиться этим документом
Поделиться или встроить документ
Этот документ был вам полезен?
Это неприемлемый материал?
Пожаловаться на этот документАвторское право:
Доступные форматы
Delo Piloto Prueba ICFES
Загружено:
Carlos Andrés Cantillo JiménezАвторское право:
Доступные форматы
Simulacro 1: Prueba Saber
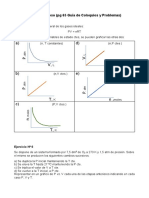
CONTESTAR LAS PREGUNTAS DE ACUERDO CON LA SIGUIENTE 2. De acuerdo con la información de la gráfica, es
LECTURA: CONVERTIDOR CATALÍTICO: correcto afirmar que las emisiones de
Los vehículos modernos están equipados con A. hidrocarburos disminuyen en un 60%
convertidores catalíticos donde se tratan los gases de empleando un catalizador de 3 vías (ciclo
escape del motor antes de dejarlos libres en la abierto)
atmósfera. Cuando el HC (hidrocarburo), CO B. monóxido de carbono disminuye
(monóxido de carbono) y NOx (óxidos de nitrógeno, x = en un 40% empleando un
3, 5) son calentados en presencia de oxígeno a 500 0C, catalizador de 3 vías (ciclo cerrado)
no hay prácticamente ninguna reacción química entre C. hidrocarburos, monóxido de
estos gases. Sin embargo cuando ellos pasan por un carbono y óxido de nitrógeno
catalizador, ocurre una reacción química y estos gases disminuyen en un 100%
son convertidos en compuestos inofensivos de CO 2, empleando un catalizador de
El convertidor utiliza dos tipos de catalizadores, uno de ciclo cerrado
oxidación y otro de reducción. El catalizador de D. de óxido de nitrógeno disminuyen en
reducción es la primera etapa del convertidor más del 80% empleando un
catalítico. Utiliza platino y rodio para disminuir las convertidor catalítico abierto.
emisiones de NOx. Cuando una molécula de monóxido
o dióxido de nitrógeno entra en contacto con el
3. La combustión es una reacción química entre el
combustible y el oxígeno del aire. Por ejemplo la
catalizador, éste atrapa el átomo de nitrógeno y libera
combustión del propano, C3H8, se describe en la
el oxígeno, posteriormente el átomo de nitrógeno se
siguiente ecuación química,
une con otro átomo de nitrógeno y se libera. El
catalizador de oxidación es la segunda etapa del C3H8(g) + 5 O2(g) –> 3CO2(g) + 4H2O(l)
convertidor catalítico. Este catalizador de platino y De acuerdo con la ecuación, para quemar
paladio toma los hidrocarburos (HC) y monóxido de completamente 5 moles de C3H8 se requieren
carbono (CO) que salen del motor y los hace reaccionar A. 5 moles de oxígeno
con el oxígeno que también vienen del motor
B. 10 moles de oxígeno
generando dióxido de carbono (CO2).
C. 20 moles de oxígeno
D. 25 moles de oxígeno
CONTESTA LAS PREGUNTAS DE ACUERDO CON LA
SIGUIENTE INFORMACIÓN
El agua es una sustancia polar que presenta varias
propiedades como la capacidad de disolver una gran
cantidad de sustancias, por lo que se denomina el
“solvente universal”. Todo cuerpo de agua (río, lago,
mar) es una solución formada por agua y una gran
variedad de sustancias disueltas que se pueden separar
mediante procesos físicos y químicos. Otro ejemplo de
solución es el suero fisiológico (agua pura con 1% de
sal). En muchas reacciones químicas se emplean
soluciones para que la reacción se lleve a cabo de
forma más eficaz (mejorar el rendimiento). Por
ejemplo, para la obtención de ciertas sales, se emplean
soluciones de ácidos e hidróxidos o bases de diferentes
concentraciones. La concentración de una solución se
puede expresar empleando unidades físicas y unidades
químicas.
4. La concentración de una solución es una medida de
la cantidad de soluto presente en cierta cantidad de
1. Dentro del convertidor catalítico, la función del solvente (o de solución). Si se quiere preparar 1 litro
catalizador es de solución fisiológica, es correcto afirmar que la
A. evitar las reacciones químicas masa de NaCl que se necesita es
B. facilitar las reacciones químicas A. 5 g B. 10 g C.
C. detener las reacciones entre CO y el O2
15 D. 20
D. hacer más lenta la reacción entre el CO y el O2
Simulacro 1: Prueba Saber
D. la densidad del solvente y la masa del
5. De acuerdo con el texto es correcto afirmar que soluto.
A. al preparar la solución ocurre un cambio
químico
B. al preparar una solución se obtienen
SOLUCIÓN
nuevas sustancias
C. los componentes de una solución
conservan sus propiedades
D. una solución es una mezcla heterogénea
6. Bajo ciertas condiciones una solución del ácido A y
una solución de la base B se hacen reaccionar para
obtener Al2(CO2)3. De acuerdo con lo anterior, es
correcto afirmar que el ácido A y la base B son
respectivamente
A. H2SO4 y Al2O3
B. HCl y Al(OH)3
C. Al2O3 y HNO3
D. H2CO2 y Al(OH)3
7. Un recipiente tiene la siguiente etiqueta
De acuerdo con la etiqueta, el 10 %v/v indica que hay
A. 10 ml de CH3COOH por cada 100 ml de
solución
B. 10 moles de CH3COOH por cada 300 ml de
solución
C. 10 ml de CH3COOH por cada 300 ml de
solución
D. 10 g de CH3COOH por cada 300 ml de
solución
Acido Acético CH3COOH
10%v/v 300 ml
8. La masa molar (o molecular) del K3PO4 es 215
g/mol. Si se requiere preparar 2 litros de una
solución 1,5 M , los gramos de K3PO4 necesarios son
A. 215 B. 430 C.
500 D. 645
9. Las unidades químicas de concentración dependen
del tipo de sustancias que forman la solución,
mientras que las unidades físicas son
independientes de la naturaleza de las sustancias
que la forman. De acuerdo con lo anterior, para
preparar una solución al 20 %m/v es necesario
tener en cuenta
A. la masa del soluto y el volumen de la
solución
B. únicamente la masa molar del soluto y el
volumen del solvente
C. la masa del soluto y la masa del solvente
Вам также может понравиться
- Misión Vision IcbfДокумент2 страницыMisión Vision IcbfCarlos Andrés Cantillo Jiménez100% (1)
- Plan de Gestión Del Riesgo, Desastres y ContingenciaДокумент24 страницыPlan de Gestión Del Riesgo, Desastres y ContingenciaCarlos Andrés Cantillo JiménezОценок пока нет
- VisionДокумент4 страницыVisionCarlos Andrés Cantillo JiménezОценок пока нет
- Salud Mental SaludableДокумент18 страницSalud Mental SaludableCarlos Andrés Cantillo JiménezОценок пока нет
- Pautas de CrianzaДокумент14 страницPautas de CrianzaCarlos Andrés Cantillo JiménezОценок пока нет
- Educación Sexual en La Primera InfanciaДокумент23 страницыEducación Sexual en La Primera InfanciaCarlos Andrés Cantillo JiménezОценок пока нет
- Efectos Negativos Del Uso de Aparatos Tecnológicos y Redes SocialesДокумент18 страницEfectos Negativos Del Uso de Aparatos Tecnológicos y Redes SocialesCarlos Andrés Cantillo Jiménez100% (1)
- Formato Elaboración Plan de Emergencias CZ YariguiesДокумент22 страницыFormato Elaboración Plan de Emergencias CZ YariguiesCarlos Andrés Cantillo JiménezОценок пока нет
- Cartilla Bienestarina 2014Документ63 страницыCartilla Bienestarina 2014Diana Carolina Vásquez Osorio100% (1)
- Cuidados y Aceptacion de Ser Padres y MadresДокумент21 страницаCuidados y Aceptacion de Ser Padres y MadresCarlos Andrés Cantillo JiménezОценок пока нет
- Proceso de Desarrollo en Niños DISCAPACIDADДокумент32 страницыProceso de Desarrollo en Niños DISCAPACIDADCarlos Andrés Cantillo JiménezОценок пока нет
- Cartilla de Educacion Sexual para Niños de PreescolarДокумент72 страницыCartilla de Educacion Sexual para Niños de Preescolarensaranzazu96% (187)
- Riesgo LocativoДокумент13 страницRiesgo LocativoCarlos Andrés Cantillo JiménezОценок пока нет
- El Desarrollo Del Niño en Situacion de DiscapacidadДокумент18 страницEl Desarrollo Del Niño en Situacion de DiscapacidadCarlos Andrés Cantillo JiménezОценок пока нет
- Desarrollo de Los NiñosДокумент17 страницDesarrollo de Los NiñosCarlos Andrés Cantillo JiménezОценок пока нет
- Aplicación A Los Modelos en PsicologíaДокумент11 страницAplicación A Los Modelos en PsicologíaCarlos Andrés Cantillo JiménezОценок пока нет
- Test Mini MentalДокумент1 страницаTest Mini MentalClaudia Toro50% (4)
- Ensayo de Ética en PsicologíaДокумент5 страницEnsayo de Ética en PsicologíaCarlos Andrés Cantillo JiménezОценок пока нет
- Encuesta Salud Mental Colombia 2015 Tomo IДокумент348 страницEncuesta Salud Mental Colombia 2015 Tomo IAnastasiaPalacioОценок пока нет
- Diapositiva Modelos en PsicopatologíaДокумент35 страницDiapositiva Modelos en PsicopatologíaCarlos Andrés Cantillo JiménezОценок пока нет
- Aplicación A Los Modelos en PsicologíaДокумент11 страницAplicación A Los Modelos en PsicologíaCarlos Andrés Cantillo JiménezОценок пока нет
- Cartilla Bienestarina 2014Документ63 страницыCartilla Bienestarina 2014Diana Carolina Vásquez Osorio100% (1)
- Analisis Pelicula, Mi Obra Maestra - Carlos Cantillo JiménezДокумент1 страницаAnalisis Pelicula, Mi Obra Maestra - Carlos Cantillo JiménezCarlos Andrés Cantillo JiménezОценок пока нет
- La red social: proposiciones generalesДокумент18 страницLa red social: proposiciones generalesCarlos Andrés Cantillo JiménezОценок пока нет
- Actividad de Preguntas Modelo Sistemico de La Psi ClínicaДокумент9 страницActividad de Preguntas Modelo Sistemico de La Psi ClínicaCarlos Andrés Cantillo JiménezОценок пока нет
- Familiograma, Trabajo para Clase de Salud FamiliarДокумент7 страницFamiliograma, Trabajo para Clase de Salud FamiliarCarlos Andrés Cantillo JiménezОценок пока нет
- Modelos en PsicopatologíaДокумент6 страницModelos en PsicopatologíaCarlos Andrés Cantillo JiménezОценок пока нет
- Angela Her Na DezДокумент13 страницAngela Her Na DezMonica Giraldo TabaresОценок пока нет
- Cuadro Comparativo Conductismo y NeoconductismoДокумент13 страницCuadro Comparativo Conductismo y Neoconductismoalex74540350% (6)
- Cuadro Comparativo Entre El Conductismo y El Neoconductism Terapias de Segunda GeneraciónДокумент13 страницCuadro Comparativo Entre El Conductismo y El Neoconductism Terapias de Segunda GeneraciónCarlos Andrés Cantillo Jiménez100% (1)
- Sbmb010322-Qu-t02-Estudio Del Átomo (Átomo Actual)Документ25 страницSbmb010322-Qu-t02-Estudio Del Átomo (Átomo Actual)Jorge GuarnízОценок пока нет
- Protocolo de PinturaДокумент6 страницProtocolo de PinturaHenry GonzalezОценок пока нет
- Informe 1Документ5 страницInforme 1Jhan Carlos PajueloОценок пока нет
- Space Materials PDFДокумент448 страницSpace Materials PDFQuispe Inga Americo GiuseppeОценок пока нет
- Calentamiento Global PDFДокумент12 страницCalentamiento Global PDFDavid De La CruzОценок пока нет
- Reacciones Químicas QMC 100l Sem 02 2020Документ43 страницыReacciones Químicas QMC 100l Sem 02 2020Victor Quecaña GutierrezОценок пока нет
- La Importancia de Los Procesos de Cristalización y Evaporación en La Industria AlimentariaДокумент11 страницLa Importancia de Los Procesos de Cristalización y Evaporación en La Industria AlimentariaZayuri MnDzz VicОценок пока нет
- Determinación de Actividad Enzimática A-AmilasaДокумент4 страницыDeterminación de Actividad Enzimática A-AmilasaCamilo MartinezОценок пока нет
- Temario Ciencias Naturales Grado NovenoДокумент3 страницыTemario Ciencias Naturales Grado NovenoAlonsoОценок пока нет
- Sólidos 12Документ28 страницSólidos 12Alexis Allcca PomaОценок пока нет
- 04 - Ejercicios Resueltos de GASESДокумент8 страниц04 - Ejercicios Resueltos de GASESlil10394Оценок пока нет
- Trabajo de Flujo Estacionario TermodinamicaДокумент13 страницTrabajo de Flujo Estacionario TermodinamicaRomario MartinzОценок пока нет
- Diseño de Los Intercambiadores de Calor-Ariza, Arrieta, Castellar, MarquezДокумент12 страницDiseño de Los Intercambiadores de Calor-Ariza, Arrieta, Castellar, MarquezMARIA PAULINA MARTINEZ ARROYAVEОценок пока нет
- Balance de Calor Con ReacciónДокумент2 страницыBalance de Calor Con ReacciónMedardo DominguezОценок пока нет
- Gases Utilizados en Corte PlasmaДокумент7 страницGases Utilizados en Corte PlasmaJhonatan Paolo Sosa PauliniОценок пока нет
- Laboratorio de bioquímica: concentraciones y pHДокумент41 страницаLaboratorio de bioquímica: concentraciones y pHAnaОценок пока нет
- Equilibrio líquido-vapor clase miércolesДокумент4 страницыEquilibrio líquido-vapor clase miércolesZyanya TapiaОценок пока нет
- Guía # 7 C.nat 9°Документ3 страницыGuía # 7 C.nat 9°Marlet MercadoОценок пока нет
- Ley de HenryДокумент9 страницLey de HenryRoberto SalazarОценок пока нет
- Actividad Enzimatica Lab BiologiaДокумент13 страницActividad Enzimatica Lab BiologiaJazminОценок пока нет
- ReglaTecnico - Evaluacion y Control-TERMICAДокумент56 страницReglaTecnico - Evaluacion y Control-TERMICAMirando lo buenoОценок пока нет
- Laboratorio 2Документ4 страницыLaboratorio 2paula rinconОценок пока нет
- 2022 Calor y EntalpiaДокумент20 страниц2022 Calor y EntalpiaMauricio DiazОценок пока нет
- Métodos PotenciométricosДокумент2 страницыMétodos PotenciométricosLuisJuliánMercadoОценок пока нет
- InformeДокумент24 страницыInformealexandraОценок пока нет
- Gases IdealesДокумент4 страницыGases IdealesYenifer Flach LeiriaОценок пока нет
- CatalisisДокумент54 страницыCatalisisLuciano Matías SalasОценок пока нет
- 11 Acidos Carboxilicos2009Документ17 страниц11 Acidos Carboxilicos2009Ignacio DuranОценок пока нет
- Gases Ideales (Ley de Boyle)Документ8 страницGases Ideales (Ley de Boyle)Roberto Silva100% (1)
- Evaluación de Sistemas de Generación EléctricaДокумент3 страницыEvaluación de Sistemas de Generación EléctricaCristian Aguilar QuintanillaОценок пока нет