Академический Документы
Профессиональный Документы
Культура Документы
Pemanfaatan Kulit Cempedak Sebagai Bahan Baku Pembuatan Bioetanol Dengan Proses Fermentasi Menggunakan Saccharomyces Cereviseae
Загружено:
DianSafitriAndazi 27Исходное описание:
Оригинальное название
Авторское право
Доступные форматы
Поделиться этим документом
Поделиться или встроить документ
Этот документ был вам полезен?
Это неприемлемый материал?
Пожаловаться на этот документАвторское право:
Доступные форматы
Pemanfaatan Kulit Cempedak Sebagai Bahan Baku Pembuatan Bioetanol Dengan Proses Fermentasi Menggunakan Saccharomyces Cereviseae
Загружено:
DianSafitriAndazi 27Авторское право:
Доступные форматы
Konversi, Volume 4 No.
2, Oktober 2015, 52 – 60 e- ISSN: 2541-3481
PEMANFAATAN KULIT CEMPEDAK SEBAGAI BAHAN BAKU
PEMBUATAN BIOETANOL DENGAN PROSES FERMENTASI
MENGGUNAKAN SACCHAROMYCES CEREVISEAE
Gusti Safriana Safitrie H, Erisa Maya Safitri, Meilana Dharma Putra*
Program Studi Teknik Kimia Universitas Lambung Mangkurat
Jl. A. Yani Km. 36, Banjarbaru, Kalimantan Selatan 70714
*E-mail corresponding author: aan_mpr@yahoo.com
ARTICLE INFO ABSTRACT
Article history: Along with prevention efforts of fossil fuel crisis in the future and the
Received: 25-09-2015 implementation of government programs on energy policy, it is
Received in revised form: 15-10- necessary to research on renewable energy such as bioethanol. The
2015 raw material for bioethanol production usually contain high enough
Accepted: 20-10-2015 carbohydrates and carbohydrate of jackfruit is 28.6 g/100 g jackfruit.
Published: 22-10-2015 This study aims to determine the effect of the process of acid
Keywords: hydrolysis treatment against the degradation of lignin in the skin
Acid hydrolysis treatment fibers of jackfruit, determine the optimum weight of jackfruit skin to
Jackfruit the process of acid hydrolysis treatment, know the optimum pH and
Bioethanol right nutrient to produce the highest ethanol content. Jackfruit skin
was cut, roasted and refined to powder and then analyzed the
structure of the morphology using SEM and crystallity using XRD
methods. The powder is added with solution of H2SO4 (2% v/v) and 90
mL of distilled water and hydrolyzed at 100°C for 1 hour with a
variety of heavy of jackfruit skin (%w/v) as follows: 2.5%; 5%; 7.5%
and 10%. Hydrolyzate with the highest glucose levels do variations in
pH, which is 4; 4,5 and 5 sterilized using an autoclave for 15 minutes.
The hydrolyzate is added starter that has been activated and
Saccharomyces cerevisiae then fermented in orbital shaker at 120 rpm
for 4 days. The fermentation process is repeated by adjusting pH 4.5
at hydrolyzate and add a variety of nutrients, namely 0.1 g urea; 0.1 g
NPK; and 0.05 g urea+0.05 g NPK. The content of bioethanol tested
with GC method. Based on XRD, the characteristic of peak of
cellulose of jackfruit fiber skin is increased. Crystallinity Index before
hydrolysis 20.39% and 24.59% after hydrolysis. From the analysis by
the Luff-Schoorl method obtained the highest total sugar content with
weight of jackfruit skin of 7.5% (w/ v) is 15.25% (v/v). While the
results of the analysis by GC method to variations in pH and nutrient
is obtained a highest content of bioethanol is 0.810% (v/v) at pH 4.5
and 0.731% (v/v) with the addition of 0.05 g urea+ 0.05 g NPK.
Abstrak-Seiring dengan upaya pencegahan krisis bahan bakar fosil dimasa mendatang dan pelaksanaan
program pemerintah tentang kebijakan energi maka diperlukan penelitian mengenai energi terbarukan,
salah satunya bioetanol. Bahan baku pembuatan bioetanol biasanya mengandung karbohidrat yang cukup
tinggi dan cempedak mengandung karbohidrat sebesar 28,6 g/100 g buah cempedak. Penelitian ini
bertujuan untuk mengetahui pengaruh proses acid hydrolysis treatment terhadap pendegradasian lignin
pada serat kulit cempedak, mengetahui berat kulit cempedak optimum pada proses acid hydrolysis
treatment, mengetahui pH optimum dan nutrient yang tepat untuk menghasilkan kadar etanol tertinggi.
Kulit cempedak dipotong, dioven dan dihaluskan sampai berbentuk serbuk kemudian dianalisa struktur
morfologinya menggunakan metode SEM dan kristanilitasnya menggunakan metode XRD. Serbuk
tersebut ditambahkan dengan larutan H2SO4 (2% v/v) dan akuades 90 mL kemudian dihidrolisis pada
suhu 100oC selama 1 jam dengan variasi berat kulit cempedak (%w/v) yaitu: 2,5%; 5%; 7,5% dan 10%.
Hidrolisat dengan kadar glukosa tertinggi dilakukan variasi pH, yaitu 4; 4,5 dan 5 selanjutnya disterilisasi
menggunakan autoclave selama 15 menit. Hidrolisat ditambahkan starter yang sudah diaktivasi dan
Saccharomyces cerevisiae kemudian difermentasi pada orbital shaker dengan kecepatan 120 rpm selama
Available online at ppjp.ulm.ac.id/journal/index.php/konversi
DOI: 10.20527/k.v4i2.267 52
Konversi, Volume 4 No. 2, Oktober 2015, 52 – 60 e- ISSN: 2541-3481
4 hari. Proses fermentasi diulang kembali dengan mengatur pH 4,5 pada hidrolisat dan menambahkan
variasi nutrient yaitu 0,1 g urea; 0,1 g NPK; dan 0,05 g urea+0,05 g NPK. Kadar bioetanol diujikan
dengan metode GC. Berdasarkan XRD, karakteristik peak selulosa pada serat kulit cempedak mengalami
peningkatan. Crystallinity Index sebelum hidrolisis 20,39%, setelah hidrolisis 24,59%. Dari hasil analisa
dengan metode Luff-Schoorl diperoleh kadar gula total tertinggi dengan berat kulit cempedak 7,5% (w/v)
sebesar 15,25% (v/v). Sedangkan hasil analisa dengan metode GC untuk variasi pH dan nutrient diperoleh
kadar bioetanol tertinggi sebesar 0,810%(v/v) pada pH 4,5 dan 0,731% (v/v) dengan penambahan 0,05 g
urea+0,05 g NPK.
Kata kunci: Acid hydrolysis treatment, cempedak, bioetanol.
PENDAHULUAN Saccharomyces cereviseae. Mengingat di
Bioetanol merupakan bioenergi alternatif Kalimantan Selatan ini juga menghasilkan
yang dapat membantu mengurangi ketergantungan cempedak, salah satunya didaerah Terantang Kab.
masyarakat terhadap bahan bakar minyak. Barito Kuala yang menghasilkan ± 360 kg setiap
Bioetanol menghasilkan emisi gas buang yang panen. Oleh karena itu penelitian ini
ramah lingkungan dan mampu meningkatkan nilai memungkinkan untuk diterapkan di Kalimantan
oktan. Salah satu bahan baku pembuatan bioetanol Selatan.
yaitu kulit cempedak. Cempedak (Artocarpus Buah cempedak dan nangka memiliki sifat
Chempeden) merupakan salah satu jenis tanaman fisik dan kimiawi yang mirip. Sifat fisik maupun
yang banyak ditanam di daerah tropis. Cempedak kimiawi kulit nangka diduga hampir sama dengan
atau biasa disebut tiwadak oleh masyarakat banjar buahnya, kandungan serat kasar pada kulit nangka
merupakan salah satu buah khas di Kalimantan sekitar 1,94% sementara daging buahnya adalah
Selatan. Buah cempedak banyak dimanfaatkan 1,58% (Karim dan Sutjahjo, 2013). Kulit nangka
sebagai bahan makanan, tetapi kulitnya masih mengandung karbohidrat yang terdiri dari glukosa,
belum banyak dimanfaatkan fruktosa, sukrosa, pati, serat dan pectin dengan
Pembuatan bioetanol menggunakan proses jumlah mencapai 15,87% dan protein 1,30%.
fermentasi telah banyak dilakukan. Aktivitas Menurut Jansen dan Coronel (1992) setiap 100
penguraian gula (karbohidrat) menjadi senyawa gram berat kering daging buah nangka
etanol dengan melepaskan CO2 disebut fermentasi mengandung protein 3,5-7,0%, lemak 0,5-2,0%,
etanol, fermentasi ini dilakukan dalam kondisi karbohidrat 84,0-87,0%, serat 5,0-6,0%, dan unsur
anaerob atau tanpa adanya oksigen dan umumnya abu 2,0-4,0%. Menurut Achyadi dan Afiana
menggunakan mikroba Saccharomyces cereviseae (2004), kadar serat cempedak yang didapatkan dari
(Putra dkk, 2011). Berdasarkan penelitian hasil kimia pada penelitian pendahuluan adalah
terdahulu yang dilakukan oleh Jura dan Sari (2013) 2,31%. Pada Tabel 2.1 dapat dilihat perbandingan
pembuatan bioetanol dari kulit ari nangka zat gizi antara nangka masak, nangka muda dan
menggunakan ragi tape dengan proses penyaringan cempedak.
filtrat kulit ari nangka yang sudah diblender
sebagai campuran starter untuk proses fermentasi Tabel 1. Komposisi zat gizi nangka dan cempedak per
dengan variasi waktu 4, 6, dan 8 hari menghasilkan 100 gram
Nangka Nangka
kadar etanol terbesar, yaitu 19,5% pada waktu Zat gizi
masak muda
Cempedak
fermentasi selama 6 hari. Pada dasarnya kulit Energi (kkal) 106 51 116
nangka dan kulit cempedak memiliki karakteristik Protein (g) 1,2 2,0 3,0
yang hampir sama. Jika kulit nangka dapat Lemak (g) 0,3 0,4 0,4
Karbohidrat (g) 27,6 11,3 28,6
menghasilkan bioetanol maka kulit cempedak Kalsium (mg) 20 45 20
kemungkinan juga dapat menghasilkan bioetanol. Fosfor (mg) 19 29 30
Maka dari itu, penelitian ini dapat dilakukan untuk Zat besi (mg) 0,9 0,5 1,5
mengetahui hal tersebut. Vit A (SI) 330 25 200
Vit B1 (mg) 0,07 0,07 0,7
Berdasarkan uraian diatas, pada penelitian ini Vit C (mg) 7 9 15
akan mempelajari pengaruh proses hidrolisis Air (g) 70,0 85,4 67,0
terhadap kristalinitas serat kulit cempedak, Sumber: Direktorat Gizi Departemen Kesehatan RI
pengaruh berat kulit cempedak (%w/v) terhadap (1992)
kadar glukosa yang dihasilkan untuk dikonversi
menjadi bioetanol serta menggunakan variasi pH Saccharomyces cerevisiae merupakan
dan nutrient untuk mengetahui kadar etanol mikroorganisme unggul yang digunakan dalam
terbesar yang dihasilkan menggunakan proses proses fermentasi etanol. Dalam melakukan proses
fermentasi dengan bantuan mikroba fermentasi, S.cerevisiae dipengaruhi oleh faktor
Available online at ppjp.ulm.ac.id/journal/index.php/konversi
DOI: 10.20527/k.v4i2.267 53
Konversi, Volume 4 No. 2, Oktober 2015, 52 – 60 e- ISSN: 2541-3481
tumbuh yang meliputi pH pertumbuhan antara 2,0-
8,6 dengan pH optimum antara 4,5-5,0. Laju Selanjutnya apabila etanol telah melewati rentang
fermentasi gula oleh S.cerevisiae relative intensif waktu fermentasinya maka akan terjadi proses
pada pH 3,5-6,0. Saccharomyces cerevisiae dapat fermentasi lanjutan berupa fermentasi asam asetat
memfermentasi glukosa, sukrosa, galaktosa serta dimana mula-mula terjadi pemecahan gula
rafinosa. Saccharomyces cerevisiae merupakan top sederhana menjadi etanol, selanjutnya etanol
yeast tumbuh cepat dan sangat aktif menjadi asam asetat.
memfermentasi pada suhu 20 oC. S. cerevisiae Nutrient yang diperlukan Saccharomyces
dapat toleran terhadap alkohol yang cukup tinggi cerevisiae bisa berasal dari kedua jenis pupuk yang
(12-18% v/v), tahan terhadap kadar gula yang sering digunakan, yaitu pupuk urea dan NPK. Urea
tinggi dan tetap aktif melakukan fermentasi pada merupakan jenis pupuk dengan butiran kecil
suhu 4-32 oC (Wiratmaja dkk, 2011). hingga halus dan berwarna putih. Pupuk urea
Ada dua cara yang digunakan untuk hidrolisis memiliki kandungan unsur hara nitrogen cukup
gukosa yaitu dalam suasana asam dan secara tinggi yaitu 46%. Sedangkan, NPK merupakan
enzimatis. Acid hydrolysis treatment atau yang yang disukai petani karena termasuk pupuk
disebut proses hidrolisis asam merupakan majemuk yang memiliki lebih dari satu unsur
hidrolisis glukosa dalam suasana asam tunggal pupuk. Salah satu pupuk NPK yang
menggunakan katalis asam, asam berfungsi berasal dari Norwegia, yaitu pupuk Mutiara
sebagai katalisator dengan mengaktifkan air. Asam memiliki kandungan 16% N, 16% P, dan 16% K
akan memecah molekul karbohidrat secara acak (Lingga, 1992).
dan menghasilkan gula yang merupakan gula Etanol yang berasal dari makhluk hidup
pereduksi. Mekanisme kerja katalis asam dalam disebut bioetanol, dengan kata lain berbahan
proses hidrolisis molekul pati bersifat acak nabati. Bahan-bahan yang mengandung pati,
(Judoamidjojo dkk, 1992). bergula dan berselulosa dapat menjadi bahan baku
Katalisator asam yang biasa digunakan pembuatan etanol (Hidayat, 2009). Proses
adalah asam klorida, asam nitrat dan asam sulfat. pengolahan bahan berpati untuk menghasilkan
Dalam skala industri, asam yang digunakan adalah bioetanol dilakukan dengan proses urutan, yaitu :
H2SO4 dan HCl. Pada kecepatan reaksi, bukan 1. Proses hidrolisis, yakni proses konversi pati
jenis asamnya yang berpengaruh melainkan menjadi glukosa.
konsentrasi ion H+ (Lubis, 2012). Pada hidrolisis 2. Proses fermentasi untuk mengkonversi glukosa
asam, asam yang paling banyak dimanfaatkan dan (gula) menjadi etanol dan CO2.
diteliti adalah H2SO4 (Taherzadeh dan Karimi, 3. Proses destilasi untuk memisahkan etanol,
2007). Menurut penelitian yang dilakukan destilasi merupakan pemisahan komponen
(Osvaldo dan Faizal, 2012) konsentrasi H2SO4 2% berdasarkan titik didihnya.
merupakan titik optimum penggunaan H2SO4 yang Penelitian ini bertujuan untuk mengetahui
menghasilkan kadar etanol terbesar karena pengaruh proses acid hydrolysis treatment
kenaikan kadar etanol tidak begitu signifikan jika terhadap kristalinitas serat kulit cempedak,
menggunakan konsentrasi H2SO4 2,5%. Maka dari mengetahui berat kulit cempedak (%w/v) optimum
itu, penggunaan konsentrasi H2SO4 2% dianggap pada proses acid hydrolysis treatment untuk
sebagai yang terbaik untuk selanjutnya menjadi mendapatkan kadar glukosa yang tinggi,
variabel tetap dan digunakan untuk mengetahui mengetahui pH optimum pada proses fermentasi
variabel penelitian yang lainnya. untuk mendapatkan kadar etanol yang tinggi serta
Fermentasi alkohol atau alkoholisasi adalah mengetahui nutrient yang tepat pada proses
proses perubahan gula menjadi alkohol dan CO2 fermentasi untuk mendapatkan kadar etanol yang
oleh mikroba, terutama oleh khamir tinggi.
Saccharomyces cerevisiae. Karbohidrat akan
dipecah dahulu menjadi gula sederhana yaitu METODE PENELITIAN
dengan hidrolisis pati menjadi unit-unit glukosa Alat dan Bahan
(Idral dkk, 2012). Perubahan gula pereduksi Alat-alat yang digunakan dalam penelitian ini
menjadi etanol dilakukan oleh enzyme invertrase, adalah labu leher tiga, stirrer, kondensor, botol
yaitu enzim kompleks yang terkandung dalam ragi. semprot, neraca analitik, gelas ukur, gelas beker,
Reaksinya adalah sebagai berikut: gelas arloji, hot plate, corong, termometer,
erlenmeyer, pengaduk gelas, pH-meter, pipet tetes,
C6H12O6 2C2H5OH + 2CO2 + 2 oven, sudip, orbital shaker dan autoclave. Bahan-
ATP bahan yang diperlukan dalam penelitian ini adalah
Glukosa Etanol karbondioksida kulit cempedak, Saccharomyces cerevisiae,
(Energi=118 Kj/mol) aquadest, kertas saring, asam sulfat (H2SO4), asam
klorida (HCl) 0,1 M, natrium hidroksida (NaOH)
Available online at ppjp.ulm.ac.id/journal/index.php/konversi
DOI: 10.20527/k.v4i2.267 54
Konversi, Volume 4 No. 2, Oktober 2015, 52 – 60 e- ISSN: 2541-3481
0,1 M, KH2PO4, ammonium sulfat ((NH4)2SO4), fermentasi dengan variasi nutrient. Larutan filtrat
MgSO4.7H2O, yeast extract, malt extract, pepton, sebanyak 90 mL ditambahkan 3 variasi nutrient
alumunium foil, yeast agar extract, urea dan NPK. yaitu 0,1 g urea; 0,1 g NPK; dan 0,05 g urea + 0,05
g NPK. pH larutan diatur dan ditambahkan 10 mL
Persiapan Bahan Baku starter. Erlenmeyer ditutup rapat kemudian
Kulit cempedak dikupas dari kulit arinya, diletakkan pada orbital shaker dengan kecepatan
dipotong kecil dan dicuci bersih. Kulit cempedak 120 rpm dan temperatur 30oC. Proses penambahan
yang sudah dibersihkan ditimbang dengan variasi starter ini dilakukan dalam laminar flow dan
berat sampel 2,5%; 5%; 7,5%, 10% (w/v) gram, fermentasi berlangsung selama 4 hari.
dioven sampai kering.
Karakterisasi dan Analisis Sampel
Acid Hydrolysis Treatment a. SEM (Scanning Electron Microscope), sebagai
Kulit cempedak yang sudah diblender uji pendahuluan untuk mengetahui struktur
ditambahkan aquadest sebanyak 90 mL, kemudian morfologi kulit cempedak sebelum
dilakukan acid hydrolysis treatment dengan labu pretreatment yang dilakukan di Laboratorium
leher tiga dan stirrer menggunakan katalis H2SO4 Pengujian Bahan Teknik Mesin Universitas
dengan konsentrasi 2% dan suhu 100 oC selama 1 Brawijaya, Malang.
jam. Larutan yang didapat kemudian disaring, hasil b. XRD (X-Ray Diffraction), sebagai uji untuk
filtrasi dianalisis dengan metode Luff-Schoorl mengetahui struktur kristal dari kulit cempedak
untuk dihitung kadar glukosa. sebelum dan sesudah pretreatment yang
dilakukan di Laboratorium Energi-LPPM
Pembuatan Starter Institut Teknologi Sepuluh November,
Media cair disiapkan dengan komposisi Surabaya.
glukosa 1 g; yeast extract 1 g; malt extract 0,3 g; c. Analisis kandungan glukosa dengan
pepton 0,3 g; KH2PO4 0,1 g; MgSO4.7H2O 0,01 g; menggunakan metode Luff-schoorl (SNI01-
dan (NH4)2SO4 0,1 g yang dilarutkan pada 100 mL 2891-1992) yang dilakukan di Laboratorium
aquadest. Medium cair ini disterilisasi dengan Fakultas MIPA Universitas Lambung
autoclave selama 20 menit. Saccharomyces Mangkurat, Banjarbaru.
cerevisiae diambil sebanyak 3 ose dicampurkan d. Analisis kandungan bioetanol, dengan
dalam 100 mL media cair dan dimasukan kedalam menggunakan metode Gas Chromathography
erlenmeyer 250 mL, kemudian diaktivasi pada (GC) yang dilakukan di Laboratorium Terpadu
suhu kamar selama 44 jam dengan orbital shaker LPPT Universitas Gadjah Mada, Yogyakarta.
kecepatan 120 rpm. Pembuatan starter ini
dilakukan dalam laminar flow. HASIL DAN PEMBAHASAN
Karakterisasi Serat Kulit Cempedak
Proses Fermentasi Serat kulit cempedak dikarakterisasi dengan
pH larutan filtrat hasil hidrolisis diatur menggunakan analisis SEM (Scanning Electron
dengan 3 variasi pH yaitu pH 4; pH 4,5; dan pH 5. Microscope) dan XRD (X-Ray Diffraction).
Larutan filtrat sebanyak 90 mL dengan 3 variasi Analisis SEM digunakan untuk mengetahui
pH ditambahkan 10 mL starter. Erlenmeyer struktur morfologi dari serat kulit cempedak. Hasil
ditutup rapat kemudian diletakkan pada orbital analisis SEM pada serat kulit cempedak sebelum
shaker dengan kecepatan 120 rpm dan temperatur dan sesudah proses hidrolisis disajikan pada
30oC. Proses penambahan starter ini dilakukan Gambar 1.
dalam laminar flow dan fermentasi berlangsung
selama 4 hari.
Larutan filtrat dari variasi pH yang
menghasilkan kadar etanol tertinggi dilakukan
Available online at ppjp.ulm.ac.id/journal/index.php/konversi
DOI: 10.20527/k.v4i2.267 55
Konversi, Volume 4 No. 2, Oktober 2015, 52 – 60 e- ISSN: 2541-3481
a) b)
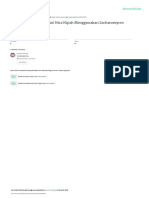
Gambar 1 SEM image dari serat kulit cempedak dengan perbesaran 1000x
(a) Sebelum hidrolisis dan (b) Sesudah hidrolisis
Berdasarkan Gambar 1 menunjukkan (selulosa I), 22,4° (selulosa II) (Sun dan Cheng,
bahwa terjadi perubahan morfologi pada kulit 2002). Karakteristik kulit cempedak sebelum dan
cempedak yang sudah mengalami proses sesudah hidrolisis dengan metode analisa XRD dapat
hidrolisis. Pada gambar a terlihat bahwa dilihat pada Tabel 2.
struktur morfolgi kulit cempedak masih
berbentuk mulus atau tidak pecah namun ketika Tabel 2 Karakteristik Kulit Cempedak Sebelum dan
sudah mengalami proses hidrolisis terjadi Sesudah Hidrolisis dengan Metode Analisa XRD
perubahan struktur morfologi yang ditandai
Karakteristik Peak
dengan adanya serat yang robek. Hal ini Sampel Amorph CrI(%)
dikarenakan serat masih terikat kuat oleh lignin, Kristal (22,4°)
(18,7°)
hemiselulosa dan komponen lain yang Sebelum
304 242 20,39%
mengikat selulosa (Sundari dkk, 2012). Adanya Hidrolisis
Sesudah Hidrolisis 138 183 24,59%
serat yang masih terikat oleh hemiselulosa dan
lignin sehingga diperlukan proses hidrolisis
untuk merusak struktur lignin dan
hemiselulosa. Hidrolisis pada penelitian ini
dilakukan dengan hidrolisis asam menggunakan
larutan H2SO4 2%, karena proses hidrolisis
dengan kondisi tersebut sebagian besar
hemiselulosa dan selulosa dapat terkonversi
menjadi gula. Selain itu, menurut Osvaldo dan
Faizal (2012) konsentrasi asam sulfat 2%
dianggap sebagai yang terbaik untuk
selanjutnya menjadi variabel tetap dan
digunakan untuk mengetahui variabel
penelitian yang lainnya. Serta larutan H2SO4
2%, digunakan dengan tujuan untuk
menghilangkan dan merusak kandungan
komponen-komponen yang mengikat selulosa
seperti lignin dan hemiselulosa (Zhou dkk, Gambar 2 X-Ray diffraction kulit cempedak sebelum
2009). hidrolisis dan sesudah hidrolisis
Analisa XRD (X-Ray Diffraction),
dilakukan untuk mengetahui struktur kristal Perubahan struktur kulit cempedak sebelum dan
selulosa dan mengetahui Crystallinity Index sesudah hidrolisis karena terjadi perubahan komponen
(CrI) kulit cempedak sebelum dan sesudah amorph (Hemiselulosa dan Lignin) pada kulit
proses hidrolisis. Kulit cempedak mengandung cempedak menjadi kristal (selulosa), pada Tabel 2
serat selulosa di dalam struktur penyusunnya, dapat dilihat kenaikan derajat kristalinitas dari kulit
(memiliki) karakteristik peak 2Ɵ = 18,7° cempedak sebelum dihidrolisis dan sesudah hidrolisis.
Available online at ppjp.ulm.ac.id/journal/index.php/konversi
DOI: 10.20527/k.v4i2.267 56
Konversi, Volume 4 No. 2, Oktober 2015, 52 – 60 e- ISSN: 2541-3481
Untuk crystallinity index kulit cempedak (%v/v) yang diperoleh. Kadar gula mengalami
sebelum hidrolisis adalah 20,39% dan setelah kenaikan seiring dengan penambahan berat kulit
dihidrolisis asam adalah 24,59%. Dari nilai cempedak, namun mengalami penurunan pada berat
crystallinity index yang didapat, terjadi kulit cempedak 10% (v/v). Menurut Osvaldo dan
kenaikan crystallinity index pada kulit Faizal (2012) salah satu faktor yang mempengaruhi
cempedak yang dihidrolisis sebesar 4,2%. hidrolisis adalah kandungan karbohidrat bahan baku.
Kenaikan crystalinity index dikarenakan Apabila kandungan karbohidrat bahan baku sedikit
hilangnya kandungan lignin dan hemiselulosa maka gula yang terbentuk juga sedikit. Namun, jika
setelah proses hidrolisis. Hidrolisis asam pada kandungan karbohidrat terlalu tinggi akan
kulit cempedak dapat membuka kandungan mengakibatkan meningkatnya kekentalan campuran
lignin dari kulit cempedak, karena H2SO4 2% sehingga frekuensi tumbukan antara molekul
dapat merestrukturisasi amorphous cellulose karbohidrat dan molekul air semakin berkurang,
menjadi crystalline cellulose (Zhou dkk, 2009). akibatnya reaksi pembentukkan gula akan berkurang.
Penurunan kadar gula pada penggunaan berat kulit
Pengaruh Berat Kulit Cempedak (%w/v) cempedak 10% (w/v) dikarenakan pada proses
dalam Proses Hidrolisis Terhadap Kadar hidrolisis telah mencapai titik optimumnya sehingga
Glukosa yang Dihasilkan cenderung akan menurun apabila berat kulit
Proses hidrolisis pada penelitian ini cempedak yang digunakan lebih banyak dibanding
menggunakan larutan H2SO4 dengan berat kulit cempedak optimumnya. Berdasarkan kadar
konsentrasi 2% (v/v) dengan waktu hidrolisis gula yang dihasilkan dari proses hidrolisis dengan
selama 1 jam. Kadar gula yang dihasilkan dapat variasi berat kulit cempedak (%w/v) dapat diambil
dihubungkan dengan berat kulit cempedak kesimpulan bahwa berat kulit cempedak optimal pada
(%w/v) pada proses hidrolisis dengan grafik proses hidrolisis untuk penelitian ini adalah 7,5%
pada Gambar 3. (w/v) yaitu sebesar 15,25% (v/v).
Proses selanjutnya setelah hidrolisis adalah
16 fermentasi. Pada proses fermentasi menggunakan
hidrolisat hasil hidrolisis dengan berat kulit cempedak
Kadar Gula Total (%)
14
12 7,5% (w/v). Berat kulit cempedak 7,5% (w/v) dipilih
10 untuk mengalami proses fermentasi karena
8 menghasilkan kadar gula yang optimum dan nilai
6 yang diperoleh masih berada dalam range. Disisi lain,
4 konsentrasi gula yang optimum untuk menghasilkan
2 etanol mempunyai range 14-18%, karena aktivitas
0 khamir akan terganggu apabila konsentrasi gula
2,5 5 7,5 10 terlalu tinggi (Budiyanto, 2002).
Berat Kulit Cempedak (%w/v)
Pengaruh pH terhadap Kadar Etanol dari Hasil
Gambar 3 Hubungan Variasi Berat Kulit cempedak Fermentasi
(%w/v) dengan kadar gula pada acid hydrolysis Larutan hidrolisat yang diperoleh dari variasi
treatment dengan t=1 jam dan konsentrasi H2SO4 2%
berat cempedak 7,5% digunakan untuk fermentasi
(v/v)
menggunakan Saccharomyces cerevisiae. Kadar
Berdasarkan Gambar 3 dapat dilihat etanol, nilai cell growth dan ethanol productivity
bahwa berat kulit cempedak (%w/v) yang dapat dilihat pada Tabel 3.
digunakan berbanding lurus dengan kadar gula
Tabel 3 Kadar Etanol, Nilai Cell Growth dan Ethanol Productivity (Variasi pH)
Ethanol
Berat Kulit Cempedak Cell growth
No. pH Kadar etanol (%) Productivity
(%w/v) (h-1)
(g l-1 h-1)
1 4 0,673 0,0114 0,0070
2 7,5 4,5 0,810 0,0144 0,0084
3 5 0,488 0,0072 0,0051
Berdasarkan Tabel 3, dapat disimpulkan 4,5 dan diperkuat hasil percobaan Elevri dan Putra
bahwa kadar etanol tertinggi terdapat pada hasil (2006) yang menyatakan bahwa produksi etanol oleh
fermentasi pH 4,5 dengan kadar etanol sebesar Saccharomyces cerevisiae paling maksimal dapat
0,810% (v/v). Menurut Saroso (1998) pH dicapai pada pH 4,5. Range kadar etanol yang
optimum untuk pertumbuhan khamir adalah 4- diperoleh sebesar 0,488% - 0,810% (v/v), nilai yang
Available online at ppjp.ulm.ac.id/journal/index.php/konversi
DOI: 10.20527/k.v4i2.267 57
Konversi, Volume 4 No. 2, Oktober 2015, 52 – 60 e- ISSN: 2541-3481
tidak terlalu tinggi ini kemungkinan disebabkan dapat berkembang biak pH 5 sehingga mengurangi
karena oksidasi bioetanol menjadi asetaldehid produksi bioetanol, terlihat nilai ethanol productivity
dan selanjutnya dioksidasi menjadi asam asetat menurun menjadi 0,0051 g l-1 h-1. Penurunan kadar
yang akan mengakibatkan media fermentasi etanol ini dikarenakan fermentasi kulit cempedak
semakin asam (Sebayang, 2009). Pada telah mencapai titik optimumnya pada pH 4,5 dan
penelitian ini terjadi perubahan pH akhir hasil kadar etanol akan cenderung menurun apabila telah
fermentasi yang terukur untuk pH 4; 4,5 dan 5 mencapai kadar etanol optimum yang dihasilkan pada
secara berturut-turut berubah menjadi pH 3,4; proses fermentasi. Berdasarkan kadar etanol yang
3,5 dan 3,6. Penurunan nilai pH menunjukkan dihasilkan dari proses fermentasi dengan variasi pH
bahwa kemungkinan proses fermentasi dapat diambil kesimpulan bahwa pH optimal pada
berlangsung secara aerob karena adanya proses fermentasi kulit cempedak untuk penelitian ini
oksigen, sehingga terbentuk senyawa asam adalah pH 4,5 ditunjukkan dengan nilai cell growth
organik yang berpengaruh pada penurunan pH dan ethanol productivity tertinggi diantara variasi pH
(Arnata dan Anggreni, 2013). Selain itu, lainnya yaitu secara berturut-turut sebesar 0,0144/h-1
kemungkinan hal ini juga dipengaruhi oleh dan 0,0084 g l-1 h-1.
produksi gas CO2 yang merupakan hasil
samping proses fermentasi. Menurut Pengaruh Nutrient terhadap Kadar Etanol dari
Kartohardjono dkk (2009) bahwa gas CO2 Hasil Fermentasi
sering disebut sebagai gas asam karena gas CO2 pH optimum yang diperoleh dari variasi pH
memiliki sifat asam. Oleh karena itu gas CO2 yaitu 4,5, hidrolisat dengan pH tersebut digunakan
berperan terhadap nilai pH. Pada pH 5 kadar kembali untuk fermentasi dengan variasi nutrient.
etanol menurun menjadi 0,488% (v/v), Kadar etanol, nilai cell growth dan ethanol
ditunjukan dengan penurunan nilai cell growth productivity pada variasi nutrient dapat dilihat pada
menjadi 0,0072 h-1. Hal ini menunjukkan Tabel 4.
bahwa bakteri Saccharomyces cerevisiae tidak
Tabel 4 Kadar Etanol, Nilai Cell Growth dan Ethanol Productivity (Variasi Nutrient)
Berat Kulit Nutrient Kadar
Ethanol Productivity
No. Cempedak pH Urea NPK etanol Cell Growth (h-1)
(g l-1 h-1)
(%w/v) (g) (g) (%v/v)
1 0,1 - 0,57 0,0084 0,0059
2 7,5 4,5 - 0,1 0 -0,003 0
3 0,05 0,05 0,731 0,0095 0,0076
Berdasarkan data pada Tabel 4, kadar bersifat racun tersebut antara lain Na+, K+, Ca2+ dan
etanol tertinggi dihasilkan dengan penambahan Mg2+. Sedangkan pada penambahan 0,1 g urea dan
nutrient 0,05 g NPK + 0,05 g urea yaitu 0,05 g NPK + 0,05 g urea menghasilkan kadar etanol
0,731% (v/v). Sedangkan kadar etanol terendah berturut-turut 0,57% (v/v) dan 0,731% (v/v). Kadar
dihasilkan dengan penambahan nutrient 0,1 g etanol yang diperoleh dengan penambahan nutrient
NPK yaitu 0% (v/v). Pada penambahan 0,1 g lebih kecil dibandingkan dengan tanpa penambahan
NPK tidak terbentuk etanol. Penambahan NPK nutrient. Hal ini disebabkan adanya kelebihan nutrient
pada proses fermentasi ini akan memperbanyak yang kemungkinan akan menjadi racun bagi mikroba
kandungan ion logam Ca2+ dan Mg2+, kelebihan itu sendiri. Kelebihan nutrient akan menyebabkan
ion logam tersebut kemungkinan akan pertumbuhan mikroba diawal fermentasi besar, namun
menyebabkan keracunan bagi mikroba semakin lama proses fermentasi mikroba akan mati
sehingga fermentasi tidak terjadi. Fermentasi sehingga banyak gula yang tidak terfermentasi.
tidak terjadi ditandai dengan meningkatnya pH Jumlah nutrisi yang dibutuhkan selama proses
yang awalnya mempunyai pH 4,5 menjadi 5,2. fermentasi berlangsung berbeda-beda tergantung dari
Selain itu, memiliki nilai cell growth -0,003 h-1 jenis bahan baku bioetanol yang digunakan serta
yang menandakan bahwa mikroba tidak jumlah ragi yang digunakan. Hal ini dikarenakan pada
berkembangbiak atau mati. Nilai cell growth bahan baku yang digunakan telah terdapat nutrisi
mempengaruhi nilai ethanol productivity yang dibutuhkan untuk pertumbuhan mikroorganisme
karena mikroba tidak berkembangbiak maka fermentasi (Hastuti dkk, 2015). Hal ini membuktikan
nilai ethanol productivitynya 0 g l-1 h-1. bahwa pada kulit cempedak itu sendiri sudah terdapat
Menurut Jenie dan Rahayu (1993) adanya nutrisi yang diperlukan Saccharomyces cerevisiae
kelebihan ion logam pada proses fermentasi untuk berkembangbiak. Tidak optimalnya proses
akan menyebabkan keracunan bagi mikroba fermentasi ini ditandai dengan meningkatnya pH yang
pada konsentrasi tertentu, ion-ion logam yang awalnya memiliki pH 4,5 menjadi 6 dan 5,4 berturut-
Available online at ppjp.ulm.ac.id/journal/index.php/konversi
DOI: 10.20527/k.v4i2.267 58
Konversi, Volume 4 No. 2, Oktober 2015, 52 – 60 e- ISSN: 2541-3481
turut untuk penambahan 0,1 g urea dan 0,1 g DINA, R. N. 2008. Laporan Tugas Akhir Bioetanol
NPK. pH yang terukur mengalami peningkatan, dari Jerami. Surakarta: Universitas Sebelas Maret.
hal ini menyebabkan rendahnya nilai cell ELEVRI, P. A. DAN PUTRA, S. R. 2006. Produksi
growth. Nilai cell growth untuk penambahan etanol menggunakan Saccharomyces cerevisiae
0,1 g urea dan 0,1 g NPK berturut-turut adalah yang diamobilisasi dengan agar batang. Akta
0,0084 h-1 dan 0,0095 h-1. Rendahnya nilai cell Kimindo, 1, 105-114.
growth menyebabkan nilai ethanol productivity FITRIANI, BAHRI, S. DAN NURHAENI 2013.
juga rendah. Nilai ethanol productivity untuk Produksi Bioetanol Tongkol Jagung (Zea Mays)
penambahan 0,1 g urea dan 0,1 g NPK berturut- dari Hasil Proses Delignifikasi. Online Jurnal of
turut adalah 0,0059 g l-1 h-1 dan 0,0076 g l-1 h-1. Natural Science, 2, 66-74.
GROGGINS, P. H. 1958. Unit processes in organic
KESIMPULAN synthesis.
Berdasarkan penelitian yang telah HASTUTI, E. D., PRIHASTANTI, E. DAN
dilakukan maka dapat disimpulkan bahwa HARYANTI, S. 2015. Efektifitas Penambahan
proses hidrolisis asam mengakibatkan Ragi Dan Pupuk Terhadap Kadar Alkohol
kandungan komponen-komponen yang Bioetanol Dengan Bahan Baku Jambu Citra.
mengikat selulosa seperti lignin dan Buletin Anatomi dan Fisiologi, 23, 92-99.
hemiselulosa dalam kulit cempedak menjadi HIDAYAT, R. 2009. Pemanfaatan Tandan Kosong
berkurang yang ditandai dengan kenaikan nilai Kelapa Sawit Menjadi Bioetanol Sebagai Bahan
crystallinity index. Pada penelitian ini nilai Bakar Masa Depan Yang Ramah Lingkungan.
crystallinity index sebelum proses hidrolisis IDRAL, D. D., SALIM, M. DAN MARDIAH, E.
sebesar 20,39% dan sesudah proses hidrolisis 2012. Pembuatan Bioetanol Dari Ampas Sagu
sebesar 24,59%. Dengan Proses Hidrolisis Asam Dan
Dari penelitian ini juga diketahui bahwa Menggunakan Saccharomyces cerevisiae. Jurnal
berat sampel optimum yang menghasilkan kimia Unand, 1.
kadar gula total tertinggi pada proses hidrolisis IRANMAHBOOB, J., NADIM, F. DAN MONEMI,
asam dalam penelitian ini yaitu 7,5% (w/v), S. 2002. Optimizing Acid -Hydrolisis: A Critical
dengan kadar gula sebesar 15,25% (v/v). Step For Production Of Etanol From Mixed Wood
Sementara itu pH optimum yang menghasilkan Chips. Biomass And Bioenergy, 22, 401-404.
kadar etanol tertinggi pada proses fermentasi JANSEN, P. C. M. V., E.W.M. DAN CORONEL, R.
dalam penelitian ini yaitu pH 4,5 dimana E. Artocarpus integer (Thumb) Merr. Edible Fruits
fermentasi menghasilkan kadar etanol sebesar and Nuts. PROSEA Bogor Indonesia, 1992
0,810% (v/v) serta nutrient optimum yang Bogor.
menghasilkan kadar etanol tertinggi pada JENIE, B. S. L. DAN RAHAYU, W. P. 1993.
proses fermentasi dalam penelitian ini yaitu Penanganan Limbah Industri Pangan, Yogyakara,
0,05 g urea + 0,05 g NPK; dimana fermentasi Kanisius.
menghasilkan kadar etanol sebesar 0,731% JOEH, T. 1998. Steam Exploson of Cotton Gin Waste
(v/v). for Fuel Ethanol Production. Jurnal Kimia.
JUDOAMIDJOJO, M., DARWIS, A. A. DAN SAI'D,
DAFTAR PUSTAKA E. G. 1992. Teknologi fermentasi, Rajawali Pers.
ACHYADI, N. DAN AFIANA, H. 2004. JURA, M. R. DAN SARI, I. P. Pembuatan Etanol
Pengaruh Konsentrasi Bahan Pengisi dan Dari Sari Kulit Ari Buah Nangka. Prosiding
Konsentrasi SukrosaTerhadap Karakteristik Seminar Nasional Sains dan Matematika II, 2013
Fruit Leather Cempedak (Actocarpus Sulawesi Tengah.
champeden lour). Fakultas Teknik KARIM, A. DAN SUTJAHJO, D. H. 2013. Uji
Universitas Pasundan. Bandung. Kinerja Mesin 4 Langkah Berbahan Bakar
ARNATA, I. W. DAN ANGGRENI, A. D. Bioethanol Dari Limbah Kulit Jerami Nangka
2013. Rekayasa Bioproses Produksi Sebagai Campuran Premium. Jurnal Teknik
Bioetanol dari Ubi Kayu dengan Teknik Mesin, 1.
Ko-Kultur Ragi Tape dan Saccharomyces KARTOHARDJONO, S., ANGGARA, A., SUBIHI,
cerevisiae. Jurnal Argointek. S. DAN YULIUSMAN, Y. 2009. Absorbsi Co2
BUDIYANTO, M. A. K. 2002. Mikrobiologi Dari Campurannya Dengan Ch4 Atau N2 Melalui
Terapan. Universitas Muhammadiyah, Kontaktor Membran Serat Berongga
Malang, 272. Menggunakan Pelarut Air. MAKARA, 11, pp. 97-
DESROIR, N. 1988. Unit Processing Organic 102.
Synthesis. Ed. KHAIRUNNISA DAN FATIMAH 2012. Konversi
dan Karakterisasi Limbah Serat Kelapa Sawit
(fiber cake) dengan Acid Hydrolisis Via
Available online at ppjp.ulm.ac.id/journal/index.php/konversi
DOI: 10.20527/k.v4i2.267 59
Konversi, Volume 4 No. 2, Oktober 2015, 52 – 60 e- ISSN: 2541-3481
Hydrothermal Treatment Sebagai Bahan Dari Limbah Rumput Laut Eucheuma Cottonii.
Baku Bioetanol, Banjarbaru, Universitas Jurnal Energi Dan Manufaktur, 5
Lambung Mangkurat. REDJEKI, S. 2012. Kinetika Reaksi Fermentasi VCO
LINGGA, P. 1992. Petunjuk penggunaan Secara Curah. Monograf Fermentasi VCO 1.
pupuk, Niaga Swadaya. SAROSO, H. 1998. Pemanfaatan Kulit Pisang dengan
LUBIS, M. R. 2012. Hidrolisis Pati Sukun Cara Fermentasi Untuk Pembuatan Alkohol.
dengan Katalisator H2SO4 untuk Pembuatan Majalah Bistek Edisi, 6.
Perekat. Rekayasa Kimia dan Lingkungan, SEBAYANG, F. 2009. Pembuatan Etanol dari Molase
9, 62-67. Secara Fermentasi Menggunakan Sel
MONICK, J. A. 1968. Alcohols; their Saccharomyces cerevisiae yang Terimobilisasi
chemistry, properties and manufacture. pada Kalsium Alginat.
MUSSATO, I. S. dan Roberto, I. C. 2004. SUN, Y. DAN CHENG, J. 2002. Hydrolysis of
Alternatives For Detoxification Of Diluete- lignocellulosic materials for ethanol production: a
Acid lignocellulosic Hydrolizates For Use review. Bioresource technology, 83, 1-11.
In Fermentative Process A Review. SUNDARI, DANANG DAN AYU 2012. Isolation
Bioresource Technology, 93, 1-10. and Characterization of Cellulose Nanofiber from
MUTHOHAR, A. 2012. Pemanfaatan Limbah the Aquatic Weed Waterhyacinth-Eichhomia
Kulit/Jerami Nangka (Artocarpus Crassipes. Carbohydrate Polymers, 87, 1701-
Heterophyllus) Sebagai Bahan Bakar 1705.
Alternatif (Bioethanol). Surabaya: TAHERZADEH, M. J. DAN KARIMI, K. 2007.
Universitas Negeri Surabaya. Process For Ethanol from Lignocellulosic
OSVALDO, Z. DAN FAIZAL, M. 2012. Materials 1: Acid-Based Hydrolysis Processes.
Pengaruh Konsentrasi Asam dan Waktu Bioresource Technology, 2.
pada Proses Hidrolisis dan Fermentasi WIRATMAJA, I. G., Kusuma, I. G. B. W. dan
Pembuatan Bioetanol dari Alang-Alang. Winaya, I. N. S. 2011. Pembuatan Etanol Generasi
Jurnal Teknik Kimia, 18. Kedua Dengan Memanfaatkan Limbah Rumput
PERRY, R. H., GREEN, D. W. DAN Laut Eucheuma Cottonii Sebagai Bahan Baku.
MALONEY, J. 1999. Perry chemicals jurnal ilmiah teknik mesin, 5, 75-84.
engineering handbook. McGrawhill, ZHOU, W., LI, H. DAN WANG, X. 2009. The
Section, 26. Structure Characterization of Cellulose
PRESCOTT, S. C. DAN DUNN, C. G. 1949. Xanthogenate Derived from The Straw of
Industrial microbiology. Industrial Eichhorniacrassipes. Bioresource Technology,
microbiology. 100, 5366-5369.
PUTRA, I. N. W., KUSUMA, I. W. DAN
WINAYA, I. N. S. 2011. Proses Treatment
Dengan Menggunakan NaOCl Dan H2SO4
Untuk Mempercepat Pembuatan Bioetanol
Available online at ppjp.ulm.ac.id/journal/index.php/konversi
DOI: 10.20527/k.v4i2.267 60
Вам также может понравиться
- Amana Top Load Washer Service ManualДокумент66 страницAmana Top Load Washer Service ManualSamurai Appliance Repair Man86% (51)
- 6 - 370 Handover Checklist Template 100420Документ4 страницы6 - 370 Handover Checklist Template 100420laxave8817100% (3)
- 2012 Melinda Chua Methodologies For The Extraction and Analysis of Konjac Glucomannan FromДокумент9 страниц2012 Melinda Chua Methodologies For The Extraction and Analysis of Konjac Glucomannan FromShofwatun Nida100% (1)
- Drop and Hardness Tests of GreasesДокумент17 страницDrop and Hardness Tests of GreasesJohn Mace VidamoОценок пока нет
- Produksi Bioetanol Dari Alkali-Pretreatment Jerami Padi Dengan Proses Simultaneous SacharificationДокумент7 страницProduksi Bioetanol Dari Alkali-Pretreatment Jerami Padi Dengan Proses Simultaneous SacharificationMiftahul Wijayanti DindaОценок пока нет
- BioRes 07 2 1540 Ding HO Compar Pretreat Strat Coconut Husk Sugars 2491 PDFДокумент8 страницBioRes 07 2 1540 Ding HO Compar Pretreat Strat Coconut Husk Sugars 2491 PDFNatasha Mgt JoharОценок пока нет
- PPI UK Inggris - Pratiwi Eka PutriДокумент2 страницыPPI UK Inggris - Pratiwi Eka PutripratiwiОценок пока нет
- Jurnal - Sayu Nila WidayantiДокумент6 страницJurnal - Sayu Nila WidayantiNila WidayantiОценок пока нет
- Bioprocess Technology To Produce Bioethanol From Cassava by Co-CultureДокумент7 страницBioprocess Technology To Produce Bioethanol From Cassava by Co-Cultureyan_kadirОценок пока нет
- Optimalisasi Penerapan Bioteknologi Dalam Produksi Bioetanol Dari Sagu (Metroxylon SP.)Документ8 страницOptimalisasi Penerapan Bioteknologi Dalam Produksi Bioetanol Dari Sagu (Metroxylon SP.)Fazryaja 8Оценок пока нет
- 15 PDFДокумент7 страниц15 PDFPradeep PereraОценок пока нет
- Potential of Taiwan Sorghum Spirits Lees For The Production of BioethanolДокумент21 страницаPotential of Taiwan Sorghum Spirits Lees For The Production of Bioethanolrichardson sitohangОценок пока нет
- Endraiyani Et Al-2017-Journal of Food Processing and PreservationДокумент6 страницEndraiyani Et Al-2017-Journal of Food Processing and PreservationAndres Felipe CaballeroОценок пока нет
- Bietanol Kulit Pisang PDFДокумент15 страницBietanol Kulit Pisang PDFRomauli NataliaОценок пока нет
- Production of Ethanol From MolassesДокумент5 страницProduction of Ethanol From MolassesKrishna PotluriОценок пока нет
- Biocatalysis and Agricultural Biotechnology: SciencedirectДокумент8 страницBiocatalysis and Agricultural Biotechnology: SciencedirectAyush SinghОценок пока нет
- Biorefinery Sequential Extraction of Alginate by Conventional and Hydrothermal Fucoidan From The Brown Alga, Sargassum CristaefoliumДокумент10 страницBiorefinery Sequential Extraction of Alginate by Conventional and Hydrothermal Fucoidan From The Brown Alga, Sargassum Cristaefoliumsugiono sugionoОценок пока нет
- Pengaruh Berbagai Pengolahan Kulit Singkong Terhadap Kecernaan Bahan Kering Dan Bahan Organik Secara in Vitro, Protein Kasar Dan Asam SianidaДокумент8 страницPengaruh Berbagai Pengolahan Kulit Singkong Terhadap Kecernaan Bahan Kering Dan Bahan Organik Secara in Vitro, Protein Kasar Dan Asam Sianidayulianabiwan biwanОценок пока нет
- GroundДокумент9 страницGroundgodfrey omariОценок пока нет
- Pembuatan Bioetanol Dari Nira Nipah Menggunakan SacharomycesДокумент4 страницыPembuatan Bioetanol Dari Nira Nipah Menggunakan SacharomycesOciKhairaniОценок пока нет
- Variations of Peroxidase Activity in Cocoa (Theobroma Cacao L.) PDFДокумент4 страницыVariations of Peroxidase Activity in Cocoa (Theobroma Cacao L.) PDFFadli Ryan ArikundoОценок пока нет
- tmp50B7 TMPДокумент11 страницtmp50B7 TMPFrontiersОценок пока нет
- Acid Hydrolysis of Sugarcane Bagasse For Lactic Acid ProductionДокумент8 страницAcid Hydrolysis of Sugarcane Bagasse For Lactic Acid ProductionAndressaGonçalvesОценок пока нет
- 3AsianJBiolLifeSci 6 3 408Документ5 страниц3AsianJBiolLifeSci 6 3 408AngelicGamer PlaysОценок пока нет
- The PH Effect On Lactose Uptake Rate by Kefir Cells, During Whey FermentationДокумент3 страницыThe PH Effect On Lactose Uptake Rate by Kefir Cells, During Whey FermentationIoannis KapageridisОценок пока нет
- Ind 23218981Документ4 страницыInd 23218981stilbeneОценок пока нет
- Solid and Liquid Pineapple Waste Utilization For Lactic Acid Fermentation USING Lactobacillus DelbrueckiiДокумент3 страницыSolid and Liquid Pineapple Waste Utilization For Lactic Acid Fermentation USING Lactobacillus Delbrueckiipatrica_23velezОценок пока нет
- Bioethanol Production From Cassava (Manihot Esculenta) Peel Using Yeast Isolated From Durian (Durio Zhibetinus)Документ8 страницBioethanol Production From Cassava (Manihot Esculenta) Peel Using Yeast Isolated From Durian (Durio Zhibetinus)Chinwuba Samuel EbukaОценок пока нет
- Sativa) Melalui Hidrolisis Asan Dan FermentasiДокумент4 страницыSativa) Melalui Hidrolisis Asan Dan FermentasiRizaaaОценок пока нет
- Microbial Diversity and Proximate Composition of Tapai, A Sabah's Fermented BeverageДокумент6 страницMicrobial Diversity and Proximate Composition of Tapai, A Sabah's Fermented BeverageNURUL SHAEERA BINTI SULAIMAN -Оценок пока нет
- Improved Upstream Processing For Detoxification and Recovery of XylitolДокумент5 страницImproved Upstream Processing For Detoxification and Recovery of XylitolMARIA CAMILA MU�OZ COMETAОценок пока нет
- 7710 24863 2 PBДокумент6 страниц7710 24863 2 PBAdi TamaОценок пока нет
- Production of Biofuel (Bioethanol) From Vigna Radiata BiomassДокумент5 страницProduction of Biofuel (Bioethanol) From Vigna Radiata BiomassR.A.Septya Wulan SariОценок пока нет
- Final Defense PPT BackupДокумент26 страницFinal Defense PPT BackupmayheartОценок пока нет
- FTIR and SEM Analysis of Thermo Chemical Fractionated Sugarcane BagasseДокумент7 страницFTIR and SEM Analysis of Thermo Chemical Fractionated Sugarcane BagasseLuis LopezОценок пока нет
- Pengaruh Variasi Penambahan Ragi Tape Dan NPK Terhadap Konsentrasi Bioetanol Hasil Fermentasi Jerami PadiДокумент6 страницPengaruh Variasi Penambahan Ragi Tape Dan NPK Terhadap Konsentrasi Bioetanol Hasil Fermentasi Jerami PadiArin pashadiera mellinaОценок пока нет
- Pengaruh Berbagai Pengolahan Kulit Singkong Terhadap Kecernaan Bahan Kering Dan Bahan Organik Secara in Vitro, Protein Kasar Dan Asam SianidaДокумент9 страницPengaruh Berbagai Pengolahan Kulit Singkong Terhadap Kecernaan Bahan Kering Dan Bahan Organik Secara in Vitro, Protein Kasar Dan Asam SianidaKon CisОценок пока нет
- Acid Hydrolysis of Sugarcane Bagasse For Lactic Acid ProductionДокумент8 страницAcid Hydrolysis of Sugarcane Bagasse For Lactic Acid Productiondh2vuihocОценок пока нет
- Antioxidant Properties of Cocoa Pods and Shells PDFДокумент8 страницAntioxidant Properties of Cocoa Pods and Shells PDFTài ColeОценок пока нет
- 12-6-11 Tofu CarrageenanДокумент7 страниц12-6-11 Tofu Carrageenanmigil66256Оценок пока нет
- Bioethanol Production From Alkaline-Pretreated Sugarcane BagasseДокумент7 страницBioethanol Production From Alkaline-Pretreated Sugarcane BagasseCuartos Amueblados JennyJohnnyОценок пока нет
- Bioethanol Production From Sugarcane Bagasse Using Fermentation ProcessДокумент7 страницBioethanol Production From Sugarcane Bagasse Using Fermentation ProcessM Syafiq SamadОценок пока нет
- Physical Microbial and Chemical Qualities of DangkДокумент8 страницPhysical Microbial and Chemical Qualities of DangkkarlinОценок пока нет
- Enzymatic Saccharification of Pretreated Rice Straw by Cellulases From Aspergillus Niger BK01Документ10 страницEnzymatic Saccharification of Pretreated Rice Straw by Cellulases From Aspergillus Niger BK01Putri AllinyaОценок пока нет
- Edible: Karakteristik Kimia, Fisika Dan Sensoris Pempek Lenjer Kering Dengan Konsentrasi CaclДокумент5 страницEdible: Karakteristik Kimia, Fisika Dan Sensoris Pempek Lenjer Kering Dengan Konsentrasi CaclfatonahОценок пока нет
- °c/15psi) - Under This Condition, The Cellulose Content of Wheat Straw Was Increased byДокумент9 страниц°c/15psi) - Under This Condition, The Cellulose Content of Wheat Straw Was Increased byHet ThankiОценок пока нет
- Study of Sulfite Pretreatment To Prepare Bamboo For Enzymatic Hydrolysis and Ethanol Fermentation - SpringerLinkДокумент9 страницStudy of Sulfite Pretreatment To Prepare Bamboo For Enzymatic Hydrolysis and Ethanol Fermentation - SpringerLinkdesamek647Оценок пока нет
- 7 PBДокумент7 страниц7 PBat6315763Оценок пока нет
- Research Article: Influence of Fenugreek Flour (Addition On The Technofunctional Properties of Dark Wheat FlourДокумент9 страницResearch Article: Influence of Fenugreek Flour (Addition On The Technofunctional Properties of Dark Wheat FlourDanaОценок пока нет
- Penentuan Nilai Kalor Serta Pengaruh Asam Klorida (HCL) Terhadap Kadar Bioetanol Bonggol Pisang (Musa Paradisiacal)Документ10 страницPenentuan Nilai Kalor Serta Pengaruh Asam Klorida (HCL) Terhadap Kadar Bioetanol Bonggol Pisang (Musa Paradisiacal)Aditya FernandoОценок пока нет
- Appl. Environ. Microbiol. 2008 Dumbrepatil 333 5Документ3 страницыAppl. Environ. Microbiol. 2008 Dumbrepatil 333 5DHENADAОценок пока нет
- Jurnal Nipah 1Документ5 страницJurnal Nipah 1Loice Pernando TariganОценок пока нет
- Wang2007 OPAДокумент5 страницWang2007 OPAMarianela RodriguezОценок пока нет
- Food Chemistry: Sujung Hu, Byung-Yong Kim, Moo-Yeol BaikДокумент6 страницFood Chemistry: Sujung Hu, Byung-Yong Kim, Moo-Yeol Baikaledrop1Оценок пока нет
- Bioetanol Por TrichodermaДокумент7 страницBioetanol Por TrichodermaJeah Gogh GoahhОценок пока нет
- Uso de Enzimas Fibrolíticas Na Ensilagem de Cana de AçúcarДокумент7 страницUso de Enzimas Fibrolíticas Na Ensilagem de Cana de Açúcarmacampana1Оценок пока нет
- 19.physicochemical Properties of Defatted RambutanДокумент6 страниц19.physicochemical Properties of Defatted RambutangramdagpinОценок пока нет
- Propiedades Físicas y Químicas de La Gelatina de Piel Wami TilapiaДокумент4 страницыPropiedades Físicas y Químicas de La Gelatina de Piel Wami TilapiaThalia VelásquezОценок пока нет
- Bio Etanol - Ampas Sagu - H2SO4Документ9 страницBio Etanol - Ampas Sagu - H2SO4paramatamaОценок пока нет
- Characterization of Alcohol Resistant Yeast Saccharomyces Cerevisiae Isolated From ToddyДокумент7 страницCharacterization of Alcohol Resistant Yeast Saccharomyces Cerevisiae Isolated From ToddyfikerykОценок пока нет
- Fruit Leather Inggris 5 DoneДокумент3 страницыFruit Leather Inggris 5 DonefitriОценок пока нет
- Jam Processing - Effect of Pectin Replacement by Locust Bean Gum On Its CharacteristicsДокумент12 страницJam Processing - Effect of Pectin Replacement by Locust Bean Gum On Its CharacteristicsThảo PhạmОценок пока нет
- Design and Development of Dual-Band Multi-Stage RF Energy Harvesting Circuit For Low Power ApplicationsДокумент5 страницDesign and Development of Dual-Band Multi-Stage RF Energy Harvesting Circuit For Low Power ApplicationsAnkushJollyОценок пока нет
- How Air Compressor WorksДокумент3 страницыHow Air Compressor WorksPinak ParkhiОценок пока нет
- Dynamics of Fixed Marine Structures N. D. P. Barltrop A. J. AdamsДокумент3 страницыDynamics of Fixed Marine Structures N. D. P. Barltrop A. J. AdamsEri KaОценок пока нет
- Energy Efficient Roadway Lighting Opportunities and BenefitsДокумент15 страницEnergy Efficient Roadway Lighting Opportunities and BenefitsHesham AlzarooniОценок пока нет
- 144S... - PCB Series: Signal Conditioned Precision Pressure TransducersДокумент4 страницы144S... - PCB Series: Signal Conditioned Precision Pressure TransducersAnish KumarОценок пока нет
- Transition To Turbopropeller-Powered AirplanesДокумент14 страницTransition To Turbopropeller-Powered AirplanesAditya Sinha100% (1)
- Boiler Design ReviewДокумент4 страницыBoiler Design ReviewKR PAОценок пока нет
- Difference Between: Turbocharger Vs SuperchargerДокумент14 страницDifference Between: Turbocharger Vs SuperchargerMohammad Al QadomeОценок пока нет
- Manual de P'lata Venezolana PDFДокумент66 страницManual de P'lata Venezolana PDFYovanny GuararimaОценок пока нет
- For ELECTRICAL TESTING LABORATORIES - The NABL (PDFDrive)Документ122 страницыFor ELECTRICAL TESTING LABORATORIES - The NABL (PDFDrive)Mani Dhamodharan100% (1)
- Samba™PLC+HMI Installation Guide: General DescriptionДокумент12 страницSamba™PLC+HMI Installation Guide: General DescriptionDragisa DjukicОценок пока нет
- Data SheetДокумент2 страницыData SheetFarid AfifiОценок пока нет
- Chapter25 PDFДокумент8 страницChapter25 PDFElizabeth DouglasОценок пока нет
- Qatar: Business OpportunitiesДокумент18 страницQatar: Business OpportunitiessanОценок пока нет
- NT7 Practical Guide For Using CFW-09 and CFW-11 Inverters and Weg Motors With Long Motor Cables-R01 PDFДокумент2 страницыNT7 Practical Guide For Using CFW-09 and CFW-11 Inverters and Weg Motors With Long Motor Cables-R01 PDFfelipeОценок пока нет
- chp20 PDFДокумент108 страницchp20 PDFSalman BoghaniОценок пока нет
- Semiconductor Materials Too GoodДокумент5 страницSemiconductor Materials Too GoodHemanth JОценок пока нет
- May Monthly Report GasperДокумент14 страницMay Monthly Report GasperOWTCОценок пока нет
- Del Cos 3000Документ12 страницDel Cos 3000aryluck77Оценок пока нет
- Propane Workshop PPTДокумент71 страницаPropane Workshop PPTch.kashifpervez100% (1)
- 2016 Zapata Hincapie John Alexander ThesisДокумент84 страницы2016 Zapata Hincapie John Alexander ThesisbetelgueseОценок пока нет
- Laporan Praktik Mesin ListrikДокумент4 страницыLaporan Praktik Mesin ListrikFatimah azzahraОценок пока нет
- General Knowledge For General PaperДокумент14 страницGeneral Knowledge For General PaperLilian LimОценок пока нет
- IBM x3650 M4 With Two 130W 4-Core CPUs and 900W Power SupplyДокумент2 страницыIBM x3650 M4 With Two 130W 4-Core CPUs and 900W Power Supplyvaradarajan_radhakriОценок пока нет
- Shibaura Diesel Engine S773L - Tier4 XXДокумент28 страницShibaura Diesel Engine S773L - Tier4 XXMihai PopaОценок пока нет
- Digital Multifunction Instrument: ApplicationДокумент7 страницDigital Multifunction Instrument: ApplicationNihar RoyОценок пока нет
- WRE - 412 - Lec01 - Introduction To Hydraulic StructuresДокумент40 страницWRE - 412 - Lec01 - Introduction To Hydraulic StructuresAzwad Abeer100% (1)