Академический Документы
Профессиональный Документы
Культура Документы
Gc-Po-10 Reesterilización de Dispositivos Médicos
Загружено:
Bantejido Sembramos VidaИсходное описание:
Оригинальное название
Авторское право
Доступные форматы
Поделиться этим документом
Поделиться или встроить документ
Этот документ был вам полезен?
Это неприемлемый материал?
Пожаловаться на этот документАвторское право:
Доступные форматы
Gc-Po-10 Reesterilización de Dispositivos Médicos
Загружено:
Bantejido Sembramos VidaАвторское право:
Доступные форматы
GESTIÓN DE CALIDAD INTEGRAL Código: GC-PO-10
Versión: 02
PROTOCOLO DE REESTERILIZACIÓN
DE DISPOSITIVOS MÉDICOS Fecha: 11/10/2019
1. DEFINICIÓN
Esta protocolo establece los requisitos y condiciones de reesterilización de los
dispositivos médicos de la Clínica Cardiovascular Corazón Joven acorde con la
Política de Seguridad del paciente.
2. OBJETIVO
Definir los lineamientos de reesterilización de los dispositivos médicos de la
Clínica Cardiovascular Corazón Joven de una manera segura que permita la
disminución de riesgos de infecciones, reacciones pirógenas, reacciones
alérgicas y/o reacciones tóxicas frente al paciente, alteraciones de las
propiedades técnicas o funcionales del producto y promoviendo la relación
costo efectividad.
3. ALCANCE
La Política de Reesterilización de Dispositivos Médicos debe ser aplicada en
forma integral por todos los procesos asistenciales, el subproceso de seguridad
del paciente y los procesos de apoyo que intervienen en la cadena de manejo
del dispositivo médico.
4. DESARROLLO DE LA POLÍTICA
4.1. CONCEPTUALIZACIÓN DE TÉRMINOS
Dispositivo Médico: Cualquier instrumento, aparato, máquina, software,
equipo biomédico u otro artículo similar o relacionado, utilizado sólo o en
combinación, incluyendo sus componentes, partes, accesorios y programas
informáticos que intervengan en su correcta aplicación, propuesta por el
fabricante para su uso en:
a) Diagnóstico, prevención, supervisión, tratamiento o alivio de una enfermedad.
b) Diagnóstico, prevención, supervisión, tratamiento, alivio o compensación de
una lesión o de una deficiencia.
c) Investigación, sustitución, modificación o soporte de la estructura anatómica o
de un proceso fisiológico.
d) Diagnóstico del embarazo y control de la concepción;
e) Cuidado durante el embarazo, el nacimiento o después del mismo, incluyendo
el cuidado del recién nacido.
f) Productos para desinfección y/o esterilización de dispositivos médicos.
Dispositivo Médico Reutilizable: Corresponde al dispositivo médico que
puede reutilizarse por recomendación del fabricante.
GESTIÓN DE CALIDAD INTEGRAL Código: GC-PO-10
Versión: 02
PROTOCOLO DE REESTERILIZACIÓN
DE DISPOSITIVOS MÉDICOS Fecha: 11/10/2019
Dispositivo Médico Abierto pero No Usado: Son dispositivos descartables
cuya esterilidad ha sido rota o comprometida o cuyo empaque estéril fue abierto
pero el dispositivo no fue usado. Estos dispositivos son los únicos que dentro de
la política serán objeto de reesterilización.
Esterilización: Consiste en la destrucción total de cualquier forma de vida
microbiana, incluyendo las formas esporuladas, mediante procedimientos físicos o
químicos que preserven y garanticen la esterilización. (Hasta un nivel aceptable
de 10 a la -6 para dispositivos médicos).
Reesterilización: Consiste en volver a esterilizar un producto que no ha sido
usado pero cuya esterilidad ha caducado y/o el empaque ha sido abierto.
Reprocesamiento: Se define como la secuencia de procedimientos que
permiten volver a utilizar un dispositivo médico de manera segura en un
paciente. Incluye la limpieza, desinfección, acondicionamiento, empaquetado,
etiquetado y esterilización del dispositivo garantizando que el proceso no
reduzca la eficacia para la cual se utiliza el dispositivo ni genere riesgos de
infecciones o complicaciones para el usuario. En este caso el dispositivo no ha
tenido contacto con el paciente y el procedimiento busca reestablecer las
condiciones de esterilidad del producto sin alterar sus propiedades
fisicoquímicas. Aplica para los dispositivos médicos abiertos pero no usados
donde de acuerdo a la ficha técnica provista por el fabricante es posible realizar
el reprocesamiento.
4.2. LINEAMIENTOS LEGALES
Ley 9 de 1979. Código sanitario Nacional. Capítulo3. Salud Ocupacional.
Ley 100 de 1993. Sistema de Seguridad Social en Salud.
Decreto 2092 de 1986. Dispositivos generales y definiciones INVIMA.
Resolución 486 de 2003. Departamento de control de calidad de la Secretaría
de Salud.
Resolución 02183 de Julio 9 de 2004. Establece el manual de Buenas
Prácticas de Esterilización para Prestadores de servicios de Salud.
Decreto 4725 del 2005 se reglamenta el régimen de registros sanitarios
permiso de comercialización y vigilancia sanitaria de los dispositivos médicos
para usos humano.
Resolución 2434 del 2006 por el cual se reglamenta la importación de equipos
biomédicos repotenciados clases IIb y III.
Decreto 1011 de 2006 se establece el Sistema Obligatorio de Garantía de
Calidad de la Atención en Salud del Sistema de Seguridad Social en Salud.
JOINT COMMISSION INTERNATIONAL – Estándares de Acreditación para
hospitales – Tercera Edición. Estándar : PCI 7.1
GESTIÓN DE CALIDAD INTEGRAL Código: GC-PO-10
Versión: 02
PROTOCOLO DE REESTERILIZACIÓN
DE DISPOSITIVOS MÉDICOS Fecha: 11/10/2019
Resolución 2003 del 2014; Se definen los procedimientos y condiciones de
inscripción de los Prestadores de Servicios de Salud y de Habilitación de
Servicios de Salud.
Circular ACHC 2014-003 26 de Enero de 2015
4.3. LINEAMIENTOS GENERALES
La Clínica Cardiovascular Corazón Joven, establece los siguientes
lineamientos para la reesterilización de dispositivos médicos:
1. Solo serán reesterilizados aquellos dispositivos médicos cuya pérdida de
condiciones de esterilidad se haya presentado por un fallo en la apertura del
mismo pero que por ningún motivo haya tenido alteración de la asepsia por
manipulación o contacto con superficies de trabajo contaminadas como
mesas, pisos, paredes, entre otras.
2. Todo dispositivo médico cuya ficha técnica no indique la posibilidad de
reúso debe ser desechado posterior a su utilización. Por consiguiente, solo
se reutilizan dispositivos médicos cuando la recomendación del fabricante
así lo indica.
3. Solo se realiza reesterilización de dispositivos médicos cuando el
dispositivo no haya sido utilizado, no tenga evidencia de contaminación y
cuya pérdida de condiciones de esterilidad se haya presentado por apertura
del kit del que hace parte y se puedan optimizar sus componentes y/o si es
un dispositivo que se puede fraccionar para optimizar su utilización.
4. Se acoge el proceso estandarizado y validado de
esterilización de la Central de Esterilización con sus
diferentes fases de acuerdo a los siguientes procedimientos:
Procedimiento de armado y empaque de material.
Procedimiento de esterilización, código.
Procedimiento de almacenaje y entrega.
5. Para garantizar el control del dispositivo médico reesterilizado se generará
su ficha técnica especificando el método de esterilización recomendado por
el fabricante, aplicable en la Fundación (método de vapor, óxido de etileno
y/o peróxido de hidrógeno) y la información emitida por el fabricante y/o
distribuidor en relación con las condiciones de embalaje, almacenamiento y
conservación.
6. El dispositivo médico a reesterilizar deberá ser enviado a la Central de
Esterilización con el inserto o manual del fabricante y con el concepto
GESTIÓN DE CALIDAD INTEGRAL Código: GC-PO-10
Versión: 02
PROTOCOLO DE REESTERILIZACIÓN
DE DISPOSITIVOS MÉDICOS Fecha: 11/10/2019
emitido por el mismo con el fin de determinar el método de esterilización
adecuado y las condiciones descritas en el numeral anterior.
7. Cada dispositivo médico que se someta a reesterilización debe contar con
un registro físico o sistematizado en donde se lleve control de la
observación relacionada con las características del dispositivo, es decir, que
se realizará vigilancia para evaluar si el producto mantiene las
especificaciones adecuadas para su uso (ejemplo: color, textura, forma,
entre otros) durante los procedimientos de reesterilización indicados por el
fabricante).
8. Se anexa a la presente política el formato de ficha técnica de reesterilización.
5. BIBLIOGRAFIA
ECCLESTON, Robert C. A model regulatory program for medical devices: An
international guide. 2002. PAHO/WHO.
CHENG Michael, A guide for the development of medical device regulations. 2001.
PAHO/WHO.
MINISTERIO DE PROTECCIÓN SOCIAL- REPUBLICA DE COLOMBIA. Decreto
4725 del 2005. Dispositivos Médicos.
W.W.W. Wfhss.com/htm/dtuc/sbasics 01 es.htm.
ROJAS Gonzalez, Alba Sofía. GOMEZ, Hoyos Patricia. Manual de Buenas
Practicas en Esterilización para prestadores de servicios de salud. Ministerio de
Protección Social. OPS/OMS. 2004.
Resolución 2003 del 2014; Se definen los procedimientos y condiciones de
inscripción de los Prestadores de Servicios de Salud y de Habilitación de
Servicios de Salud.
GESTIÓN DE CALIDAD INTEGRAL Código: GC-PO-10
Versión: 02
PROTOCOLO DE REESTERILIZACIÓN
DE DISPOSITIVOS MÉDICOS Fecha: 11/10/2019
CONTROL DE CAMBIOS
Cambio Descripción del Fecha del
Versión Responsable
realizado cambio cambio
Elaboración del Coordinador de
Todo 18/01/2019 01
documento esterilización
Andrés Medina
Actualización del
Todo 11/10/2019 02 (Coordinador de
documento
esterilización)
CONTROL DE EMISIÓN DEL DOCUMENTO
Elaboró/ María Carolina Sandi Yolima
Andrés Medina Revisó Aprobó
Modificó Vieda Rincón
Coordinador de Coordinadora
Cargo Cargo Cargo Gerente
esterilización de Calidad
Fecha 11/10/2019 Fecha 11/10/2019 Fecha 11/10/2019
Вам также может понравиться
- PM Gco Ma 03 Manual de Uso y Reuso de Dispositivos OdontologicosДокумент27 страницPM Gco Ma 03 Manual de Uso y Reuso de Dispositivos OdontologicossaludОценок пока нет
- Politica Uso Reuso Dispositivos Medicos CiameДокумент52 страницыPolitica Uso Reuso Dispositivos Medicos CiamemedilabbecerrilОценок пока нет
- GC-S4D1-V4Politica Uso Reuso Dispositivos MedicosДокумент30 страницGC-S4D1-V4Politica Uso Reuso Dispositivos MedicosAdriana PerdomoОценок пока нет
- Pbu-16 Procedimiento de No Reuso de Dispositivos Médicos e InsumosДокумент4 страницыPbu-16 Procedimiento de No Reuso de Dispositivos Médicos e InsumosDiego VillamizarОценок пока нет
- Politicas de Reuso IntitucionalДокумент15 страницPoliticas de Reuso IntitucionalGloria Adela Rodriguez CardenasОценок пока нет
- Manual de Uso y Rehuso para Dispositivos Medicos en El Laboratorio ClinicoДокумент2 страницыManual de Uso y Rehuso para Dispositivos Medicos en El Laboratorio ClinicoKatherine PeñaОценок пока нет
- Reuso y Reprocesamiento de Dispositivos MédicosДокумент16 страницReuso y Reprocesamiento de Dispositivos MédicosJessica MontealegreОценок пока нет
- Manual Uso y ReusoДокумент14 страницManual Uso y Reusoyari valverdesОценок пока нет
- Preparación, transporte y almacenamiento de biocidas y productos fitosanitarios. SEAG0110От EverandPreparación, transporte y almacenamiento de biocidas y productos fitosanitarios. SEAG0110Оценок пока нет
- R MPS 4002 2007 PDFДокумент18 страницR MPS 4002 2007 PDFdenis guevara pinillaОценок пока нет
- Curso DT HabilitacionДокумент46 страницCurso DT Habilitacionluc1902Оценок пока нет
- Manual de Mantenimiento de Equipos Biomedicos KinesisДокумент13 страницManual de Mantenimiento de Equipos Biomedicos KinesisBiomed JasОценок пока нет
- Protocolo de Calibracion de Equipos Biomedicos de Optometria OficialДокумент56 страницProtocolo de Calibracion de Equipos Biomedicos de Optometria OficialEDUARDO GONZALEZ100% (2)
- Marcoteorico REUSOДокумент68 страницMarcoteorico REUSOmaria eugeniaОценок пока нет
- Manual de Uso y Rehuso para Dispositivos Medicos en El Laboratorio ClinicoДокумент8 страницManual de Uso y Rehuso para Dispositivos Medicos en El Laboratorio Clinicojuanjo1071100% (2)
- Resolucion 2183 de 2004Документ137 страницResolucion 2183 de 2004RustbelStithMontillaОценок пока нет
- Taller Insumos y Dispositivos MedicosДокумент19 страницTaller Insumos y Dispositivos MedicosJose RicoОценок пока нет
- Fase 1Документ10 страницFase 1Diana UbaqueОценок пока нет
- Resolucion 4002 2007Документ11 страницResolucion 4002 2007Diana Carolina Vasquez VelezОценок пока нет
- Presentación Universidad Ecci FinalДокумент79 страницPresentación Universidad Ecci FinalSantiago González GualterosОценок пока нет
- Resolución 4002 de 2007 - Manual de Almacenamiento de Disp. MédicosДокумент13 страницResolución 4002 de 2007 - Manual de Almacenamiento de Disp. MédicosMedicina y Tecnología SASОценок пока нет
- Resolucion 4002 2007Документ14 страницResolucion 4002 2007Diani C VeraОценок пока нет
- Resolución 4002 - 02 Noviembre de 2017Документ21 страницаResolución 4002 - 02 Noviembre de 2017Omar RodriguezОценок пока нет
- Coche Paro FinalДокумент11 страницCoche Paro FinalLolit Cristin CorreaОценок пока нет
- Servocuna Principiosy PartesДокумент7 страницServocuna Principiosy PartesJuan SepúlvedaОценок пока нет
- Acta 04 Mayo 2014 Dispositivos MedicosДокумент18 страницActa 04 Mayo 2014 Dispositivos MedicosLorena CadavidОценок пока нет
- Manual de Uso y Reuso Revis - IVДокумент42 страницыManual de Uso y Reuso Revis - IVDanna RincónОценок пока нет
- 156 03 Instructivo Subcomite de Reuso Ins SM 03 01 PDFДокумент4 страницы156 03 Instructivo Subcomite de Reuso Ins SM 03 01 PDFAnonymous MnaMZQWwCОценок пока нет
- Instructivo Externo: Versión (4.0)Документ47 страницInstructivo Externo: Versión (4.0)alexandraОценок пока нет
- Politica Reuso de DispositivosДокумент4 страницыPolitica Reuso de Dispositivosalexander cuellarОценок пока нет
- Cartilla Diligenciamiento Formularios - INVIMAДокумент76 страницCartilla Diligenciamiento Formularios - INVIMALau PrietoОценок пока нет
- Resumen Decreto4725Документ13 страницResumen Decreto4725Diego PeñuelaОценок пока нет
- Ley 26906 Regimen de Trazabilidad y Verificación de Aptitud Tecnica de Los Productos Medicos Activos de Salud en UsoДокумент4 страницыLey 26906 Regimen de Trazabilidad y Verificación de Aptitud Tecnica de Los Productos Medicos Activos de Salud en Usojuanpila777Оценок пока нет
- M-Eo-09-Ma Manual de Uso y Reuso de Dispositivos MedicosДокумент11 страницM-Eo-09-Ma Manual de Uso y Reuso de Dispositivos MedicosrocioОценок пока нет
- Abece Mediciones Equipos BiomedicosДокумент7 страницAbece Mediciones Equipos BiomedicosHarley Jhoan Orjuela BallesterosОценок пока нет
- Plan MantenimientoДокумент30 страницPlan MantenimientoTomas DuranОценок пока нет
- Manual de Uso y Reuso de Dispositivos MedicosДокумент29 страницManual de Uso y Reuso de Dispositivos MedicosMichelle Carolina BeleñoОценок пока нет
- 2183 Buenas Prasticas EsterilizacionДокумент99 страниц2183 Buenas Prasticas EsterilizacionElder Antonio Caliz De HoyosОценок пока нет
- Tec No Vigi LanciaДокумент24 страницыTec No Vigi Lanciacalidad.kuanОценок пока нет
- Resolucion 2183 de 2004 PDFДокумент175 страницResolucion 2183 de 2004 PDFCamiloAlejandroMontenegroОценок пока нет
- Decreto Número 4725 de 2005Документ35 страницDecreto Número 4725 de 2005Oscar RealpeОценок пока нет
- Seguridad e Higiene en un obrador de panadería y bollería. INAF0108От EverandSeguridad e Higiene en un obrador de panadería y bollería. INAF0108Оценок пока нет
- Publicacion 163Документ19 страницPublicacion 163Gabriel OrdoñezОценок пока нет
- Uso y Reuso de Dispositivos MedicosДокумент8 страницUso y Reuso de Dispositivos MedicosChristian Camilo GBОценок пока нет
- Que en El Artículo 10 Del Decreto 4725 de 2005Документ4 страницыQue en El Artículo 10 Del Decreto 4725 de 2005Julieth SamperОценок пока нет
- C2 Nom-059-Ssa1-2015 - ZarmДокумент6 страницC2 Nom-059-Ssa1-2015 - Zarmzyanzy rojasОценок пока нет
- Cuadro Comparativo Farmacia HospitalariaДокумент3 страницыCuadro Comparativo Farmacia Hospitalariayuli paolaОценок пока нет
- Recomendaciones Manejo y Aplicación de Pruebas de Laboratorio en El Punto de Atención Del PacienteДокумент5 страницRecomendaciones Manejo y Aplicación de Pruebas de Laboratorio en El Punto de Atención Del PacienteGABRIELA VANEGAS CAYCEDOОценок пока нет
- ES-PLI-GP001L07 Política de ComprasДокумент13 страницES-PLI-GP001L07 Política de Compraszalua chicreОценок пока нет
- ACTA ORDINARIA No. 7 SEDMRDIV - DEF PDFДокумент28 страницACTA ORDINARIA No. 7 SEDMRDIV - DEF PDFStefany FlorezОценок пока нет
- ANMAT - Regulacion Productos MedicosДокумент71 страницаANMAT - Regulacion Productos MedicosMaximilianoGabrielColazo50% (2)
- Metrologia Biomédica 2019-1Документ206 страницMetrologia Biomédica 2019-1juan veraОценок пока нет
- Manual de Uso y Reuso de Dspositivos MedicosДокумент31 страницаManual de Uso y Reuso de Dspositivos MedicosLilian PallaresОценок пока нет
- Manual de Reuso de Dispositivos Medicos 2014Документ59 страницManual de Reuso de Dispositivos Medicos 2014Carmen Harleny Moreno Perea100% (4)
- Manual de Uso y ReusoДокумент8 страницManual de Uso y ReusoLuis Miguel TrianaОценок пока нет
- Ing Biomedica. Diana Carolina Bahamón Chavarro PDFДокумент21 страницаIng Biomedica. Diana Carolina Bahamón Chavarro PDFEdwaar MoralesОценок пока нет
- Reuso en Odontologia PDFДокумент48 страницReuso en Odontologia PDFCONSULTORIO ODONTOLOGICO OPSОценок пока нет
- Manual de Insumos OdontologicosДокумент33 страницыManual de Insumos OdontologicosEster Calle Calle100% (1)
- Aplicación de normas y condiciones higiénico-sanitarias en restauración. HOTR0308От EverandAplicación de normas y condiciones higiénico-sanitarias en restauración. HOTR0308Оценок пока нет
- English DayДокумент2 страницыEnglish DayBantejido Sembramos VidaОценок пока нет
- Presentacion Portafolio Servicio Crece OK CorporalДокумент47 страницPresentacion Portafolio Servicio Crece OK CorporalBantejido Sembramos VidaОценок пока нет
- Fo-Ga-13 Registro de Lavado de Tanques y FumigacionДокумент1 страницаFo-Ga-13 Registro de Lavado de Tanques y FumigacionBantejido Sembramos VidaОценок пока нет
- Registro de Limpieza Del Tanque de Almacenamiento de AguaДокумент1 страницаRegistro de Limpieza Del Tanque de Almacenamiento de AguaBantejido Sembramos VidaОценок пока нет
- Fo-Ga-12 Rotacion de DesinfectantesДокумент1 страницаFo-Ga-12 Rotacion de DesinfectantesBantejido Sembramos VidaОценок пока нет
- Presentacion Portafolio Servicio CreceДокумент46 страницPresentacion Portafolio Servicio CreceBantejido Sembramos VidaОценок пока нет
- Importancia de La Fisioterapia Desde La Salud OcupacionalДокумент5 страницImportancia de La Fisioterapia Desde La Salud OcupacionalBantejido Sembramos VidaОценок пока нет
- Fo-Ga-11registro de Ingreso VisitantesДокумент1 страницаFo-Ga-11registro de Ingreso VisitantesBantejido Sembramos VidaОценок пока нет
- Fo-Ga-05control de Limpieza y Uso de Equipo BiomedicoДокумент1 страницаFo-Ga-05control de Limpieza y Uso de Equipo BiomedicoBantejido Sembramos VidaОценок пока нет
- Fo-Ga-03mantenimiento Preventivo de Equipos BiomedicosДокумент8 страницFo-Ga-03mantenimiento Preventivo de Equipos BiomedicosBantejido Sembramos VidaОценок пока нет
- Fo-Ga-10-T Recepcion Tecnico Administrativa v1Документ1 страницаFo-Ga-10-T Recepcion Tecnico Administrativa v1Bantejido Sembramos VidaОценок пока нет
- Fo-Ga-09-T Gestión para El Control Condiciones de Almacenamiento de Medicamentos y DispositivosДокумент1 страницаFo-Ga-09-T Gestión para El Control Condiciones de Almacenamiento de Medicamentos y DispositivosBantejido Sembramos VidaОценок пока нет
- Fo-Ga-06evaluación y Selección de ProveedoresДокумент1 страницаFo-Ga-06evaluación y Selección de ProveedoresBantejido Sembramos VidaОценок пока нет
- Fo-Ga-01 Cuadro de Control de Aseo y Desinfección de ÁreasДокумент2 страницыFo-Ga-01 Cuadro de Control de Aseo y Desinfección de ÁreasBantejido Sembramos VidaОценок пока нет
- Inspeccion PeligrosДокумент3 страницыInspeccion PeligrosdanielОценок пока нет
- Fo-Ga-07verificacion de Funcionamiento de Equipo BiomedicoДокумент1 страницаFo-Ga-07verificacion de Funcionamiento de Equipo BiomedicoBantejido Sembramos VidaОценок пока нет
- Fo-Ga-04 Cronograma de Mantenimiento de ApoyoДокумент1 страницаFo-Ga-04 Cronograma de Mantenimiento de ApoyoBantejido Sembramos VidaОценок пока нет
- Fo-Ga-08-T Solicitud y Recepcion de PedidosДокумент1 страницаFo-Ga-08-T Solicitud y Recepcion de PedidosBantejido Sembramos VidaОценок пока нет
- Politica de Seguridad y Salud en El TrabajoДокумент2 страницыPolitica de Seguridad y Salud en El TrabajoBantejido Sembramos VidaОценок пока нет
- Fo-Ga-02 Hoja de Vida de Equipo BiomedicoДокумент2 страницыFo-Ga-02 Hoja de Vida de Equipo BiomedicoBantejido Sembramos VidaОценок пока нет
- ST Fo 12 Cronograma de Actividades Hse 2015 2016Документ2 страницыST Fo 12 Cronograma de Actividades Hse 2015 2016angela maria loaizaОценок пока нет
- ST Fo 43 Seguimiento Examenes Medicos Laborales v1Документ11 страницST Fo 43 Seguimiento Examenes Medicos Laborales v1Bantejido Sembramos VidaОценок пока нет
- ST FO 21 Formato Etiquetado de Residuos QuimicosДокумент1 страницаST FO 21 Formato Etiquetado de Residuos QuimicosBantejido Sembramos VidaОценок пока нет
- ST FO 17 Entrega de EPPДокумент1 страницаST FO 17 Entrega de EPPBantejido Sembramos VidaОценок пока нет
- Manual Sigi 3 1Документ40 страницManual Sigi 3 1Bantejido Sembramos VidaОценок пока нет
- Programa Inspecciones PlaneadasДокумент35 страницPrograma Inspecciones PlaneadasBantejido Sembramos VidaОценок пока нет
- Politicas SST Higiene Seguridad IndrustrialДокумент10 страницPoliticas SST Higiene Seguridad IndrustrialBantejido Sembramos VidaОценок пока нет
- Formato Lista de Chequeo para EPPДокумент1 страницаFormato Lista de Chequeo para EPPBantejido Sembramos VidaОценок пока нет
- Manipulación de Sustancias QuímicasДокумент11 страницManipulación de Sustancias QuímicasBantejido Sembramos VidaОценок пока нет
- Politica de Seguridad y Salud en El TrabajoДокумент2 страницыPolitica de Seguridad y Salud en El TrabajoBantejido Sembramos VidaОценок пока нет
- Universidad Tecnologica de SantiagoДокумент14 страницUniversidad Tecnologica de SantiagoReynaldo RodriguezОценок пока нет
- Consentimiento InformadoДокумент3 страницыConsentimiento InformadoAngie Paola Marin GonzalezОценок пока нет
- Formulario Tamizaje, Declaración Covid y Ficha Sintomatología SSTДокумент4 страницыFormulario Tamizaje, Declaración Covid y Ficha Sintomatología SSTHugo GuglierminoОценок пока нет
- Fisioterapia en Neonatología: La Importancia Del Abordaje Temprano en El Recién Nacido de RiesgoДокумент3 страницыFisioterapia en Neonatología: La Importancia Del Abordaje Temprano en El Recién Nacido de RiesgoAry Gonzalez DominguezОценок пока нет
- Módulo 2 - TB - PBДокумент28 страницMódulo 2 - TB - PBJosé Luis Nogales AsteteОценок пока нет
- Programa Institucional Higiene ManosДокумент120 страницPrograma Institucional Higiene ManosRawLeoifyОценок пока нет
- Vacuna CovidДокумент1 страницаVacuna CovidJaime LunaОценок пока нет
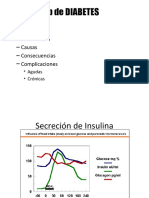
- FP de Diabetes: - Concepto - Clasificación - Causas - Consecuencias - ComplicacionesДокумент25 страницFP de Diabetes: - Concepto - Clasificación - Causas - Consecuencias - ComplicacionesSelene VilchesОценок пока нет
- Mural 08 - Flores Coriñaupa JhoaoДокумент1 страницаMural 08 - Flores Coriñaupa JhoaoJhoao Jacks Flores CoriñaupaОценок пока нет
- Formato #02 - Declaración Jurada de Salud - Ficha de Sintomatología V3.Документ2 страницыFormato #02 - Declaración Jurada de Salud - Ficha de Sintomatología V3.Adailton Umasi PilaОценок пока нет
- Síndrome de Abstinencia NeonatalДокумент8 страницSíndrome de Abstinencia NeonatalDiego PerezОценок пока нет
- Enfermedades Mas Comunes en La Poblacion PanameñaДокумент10 страницEnfermedades Mas Comunes en La Poblacion PanameñaKimberly VergaraОценок пока нет
- COFEPRISДокумент3 страницыCOFEPRISBryan Escamilla TrejoОценок пока нет
- Anestesia GeneralДокумент4 страницыAnestesia GeneralGuidoWalterVargasApazaОценок пока нет
- Protocolo 2°11 - Cirugia IIДокумент3 страницыProtocolo 2°11 - Cirugia IIKelvin Alvarez ToledoОценок пока нет
- Prueba de Trabajo de Parto Induccion y ConduccionДокумент17 страницPrueba de Trabajo de Parto Induccion y ConduccionRosene BarazarteОценок пока нет
- Primeros Auxilios en Casos de Envenenamiento o IntoxicaciónДокумент5 страницPrimeros Auxilios en Casos de Envenenamiento o IntoxicaciónMaryuri ArnalОценок пока нет
- Informe Final Simulacion de Sistemas Hospital YanahuaraДокумент46 страницInforme Final Simulacion de Sistemas Hospital YanahuaraAEPCОценок пока нет
- Dermatologia y OzonoterapiaДокумент71 страницаDermatologia y OzonoterapiaDra María OzonoterapiaОценок пока нет
- Capsulitis AdhesivaДокумент13 страницCapsulitis AdhesivaNico BrantesОценок пока нет
- Mortalidad y Medidas de MortalidadДокумент7 страницMortalidad y Medidas de Mortalidadmirgue2014100% (1)
- CicatrizaciónДокумент50 страницCicatrizaciónJulian Rios MurilloОценок пока нет
- SX HellpДокумент60 страницSX Hellpsthela74_ezОценок пока нет
- Periodoncia y EscorbutoДокумент23 страницыPeriodoncia y EscorbutorolandoОценок пока нет
- Curso de Vida AdolescenciaДокумент45 страницCurso de Vida AdolescenciaFabian Rodriguez MendezОценок пока нет
- Derechos Sexuales Reproductivos - EdissonДокумент1 страницаDerechos Sexuales Reproductivos - EdissonLAURA RAMOSОценок пока нет
- MEMORIA DESCRIPTIVA Del ResidenteДокумент6 страницMEMORIA DESCRIPTIVA Del ResidenteWaldirt Adilson Espinoza SánchezОценок пока нет
- Guía de TerminosДокумент1 страницаGuía de TerminosINVERSIONES FRINOVERОценок пока нет
- HOw To ReembolsosДокумент2 страницыHOw To ReembolsosFernando ContrerasОценок пока нет
- Obstetricia - Bienestar FetalДокумент4 страницыObstetricia - Bienestar FetalKiara LunaОценок пока нет