Академический Документы
Профессиональный Документы
Культура Документы
Ejercicios Gases
Загружено:
Carlos MoscosoАвторское право
Доступные форматы
Поделиться этим документом
Поделиться или встроить документ
Этот документ был вам полезен?
Это неприемлемый материал?
Пожаловаться на этот документАвторское право:
Доступные форматы
Ejercicios Gases
Загружено:
Carlos MoscosoАвторское право:
Доступные форматы
1. Un tanque de 20.0 L contiene 0.225 kg de helio a 18.0 °C.
La masa molar del helio es de
4.00 g>mol. a) ¿Cuántos moles de helio hay en el tanque? b) Calcule la presión en el tanque
en Pa y atm.
2. Helio gaseoso con un volumen de 2.60 L, a 1.30 atm de presión y una temperatura de
41.0 °C, se calienta hasta duplicar la presión y el volumen. a) Calcule la temperatura final.
b) ¿Cuántos gramos de helio hay? La masa molar del helio es de 4.00 g>mol.
3. Un tanque cilíndrico tiene un pistón ajustado que permite cambiar el volumen del
tanque. El tanque contiene originalmente 0.110 m3 de aire a 3.40 atm de presión. Se tira
lentamente del pistón hasta aumentar el volumen del aire a 0.390 m3. Si la temperatura
permanece constante, ¿qué valor final tiene la presión?
4. Un tanque de 3.00 L contiene aire a 3.00 atm y 20.0 °C. El tanque se sella y enfría hasta
que la presión es de 1.00 atm. a) ¿Qué temperatura tiene ahora el gas en grados Celsius?
Suponga que el volumen del tanque es constante. b) Si la temperatura se mantiene en el
valor determinado en el inciso a) y el gas se comprime, ¿qué volumen tendrá cuando la
presión vuelva a ser de 3.00 atm?
5. Una molécula orgánica grande tiene una masa de 1.41 310221 kg. Calcule la masa
molar de este compuesto.
6. Suponga que usted hereda de su tío (un químico excéntrico) 3.00 moles de oro cuando
este metal se cotiza a $14.75 por gramo. Consulte la tabla periódica en el Apéndice D y la
tabla 14.1. a) ¿Cuál es el valor del oro aproximando al dólar más cercano? b) Si usted tiene
su oro en forma de pepita, ¿cuál será el diámetro de ésta?
7. Las bombas de vacío modernas alcanzan fácilmente presiones del orden de 10213 atm
en el laboratorio. a) Auna presión 9.00 3 10214 atm y una temperatura ordinaria de 300 K,
¿cuántas moléculas hay en un volumen de 1.00 cm3? b) ¿Cuántas moléculas estarían
presentes a la misma temperatura pero a un presión de 1.00 atm?
8. Un matraz contiene una mezcla de los gases neón (Ne), criptón (Kr) y radón (Rn).
Compare a) las energías cinéticas medias de los tres tipos de átomos; b) la rapidez eficaz de
sus moléculas. (Sugerencia: la tabla periódica del Apéndice D da la masa molar (en g>mol)
de todos los elementos, bajo el símbolo químico correspondiente.)
9. Difusión gaseosa del uranio. a) A menudo se utiliza un proceso llamado difusión
gaseosa para separar isótopos de uranio, es decir, átomos del elemento que tienen diferentes
masas, como 235U y 238U. El único compuesto de uranio que es gaseoso a temperaturas
ordinarias es el hexafluoruro de uranio, UF6. Especule cómo las moléculas de 235UF6 y
238UF6 podrían separarse por difusión molecular. b) Las masas molares de 235UF6 y
238UF6 son 0.349 kg>mol y 0.352 kg>mol, respectivamente. Si el hexafluoruro de uranio
actúa como gas ideal, determine la razón entre las rapideces eficaces de las moléculas de
235UF6 y 238UF6 suponiendo que la temperatura es uniforme.
10. Las ideas de valor medio y eficaz se pueden aplicar a cualquier distribución. Un grupo
de 150 estudiantes obtuvo los siguientes puntajes en un examen de 100 puntos
a) Calcule el puntaje medio del grupo. b) Calcule el puntaje eficaz del
grupo. (ver libro guia)
11. ¿Cuánto calor se requiere para aumentar la temperatura de 2.50 moles de un gas
diatómico ideal en 30.0 K cerca de la temperatura ambiente si el gas se mantiene a volumen
constante? b) ¿Cuál es la respuesta a la pregunta del inciso a) si el gas es monoatómico en
vez de diatómico? Recipientes perfectamente rígidos contienen cada uno n moles de gas
ideal: uno de ellos es hidrógeno (H2) y el otro es neón (Ne). Si se requieren 100 J de calor
para aumentar la temperatura del hidrógeno en 2.50 °C, ¿en cuántos grados elevará la
misma cantidad de calor la temperatura del neón?12. a) Calcule la capacidad calorífica
específica a volumen constante del nitrógeno gaseoso (N2) y compárela con la del agua
líquida. La masa molar del N2 es 28.0 g>mol. b) Se calienta 1.00 kg de agua, con volumen
constante de 1.00 L, de 20.0 °C a 30.0 °C en una tetera. Con la misma cantidad de calor,
¿cuántos kilogramos de aire a 20.0 °C se podrían calentar a 30.0 °C? ¿Qué volumen (en
litros) ocuparía ese aire a 20.0 °C y 1.00 atm de presión? Suponga, para simplificar, que el
aire es 100% N2.13. Deduzca la ecuación (18.33) a partir de la ecuación (18.32).14.
Demuestre que f (v), dada por la ecuación (18.33), es máxima con P 5 kT. Use este
resultado para obtener la ecuación (18.34).15. Para dióxido de carbono diatómico gaseoso
(CO2, masa molar 5 44.0 g>mol) a T 5 300 K, calcule a) la rapidez más probable vmp; b)
la rapidez media vmed; c) la rapidez eficaz vrms.16. Aproximaciones sucesivas y la
ecuación de Van der Waals. En la ecuación del gas ideal, el número de moles por volumen
n>V es igual a p>RT. En la ecuación de Van der Waals, despejar n>V en términos de p y T
es un tanto más complicado. a) Demuestre que la ecuación de Van der Waals puede
escribirse como
b) Los parámetros de Van der Waals para el sulfuro de hidrógeno gaseoso
(H2S) son y b 5 4.29 3 1025 m3>mol. Determine el número de moles por volumen de H2S
gaseoso a 127 °C y una presión absoluta de 9.80 3 105 Pa como sigue: i) Calcule una
primera aproximación usando la ecuación del gas ideal n>V 5 p>RT.
ii) Sustituya esta aproximación en el miembro derecho de la ecuación del inciso a). El
resultado es una aproximación mejorada de n>V. iii) Sustituya la nueva aproximación en el
miembro derecho de la ecuación del inciso a). El resultado es una aproximación todavía
mejor de n>V. iv) Repita el paso iii) hasta que aproximaciones sucesivas coincidan con el
nivel de precisión deseado (en este caso, tres cifras significativas). c) Compare su resultado
final del inciso b) con el valor de p>RT obtenido usando la ecuación del gas ideal. ¿Qué
resultado da un valor mayor de n>V? ¿Por qué?
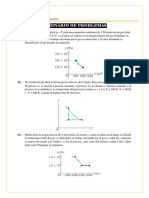
SOLUCIÓN TALLER
1)
Вам также может понравиться
- Máquinas de Calor, Segunda Ley de La Termodinámica y EntropiaДокумент9 страницMáquinas de Calor, Segunda Ley de La Termodinámica y EntropiaAlexis GarciaОценок пока нет
- Problemas Resueltos TermodinamicaДокумент15 страницProblemas Resueltos TermodinamicaAndrea PaolaОценок пока нет
- Temperatura y Diltacion Térmica PDFДокумент2 страницыTemperatura y Diltacion Térmica PDFMisael Orellano0% (2)
- Termodinámica de gases ideales y primera leyДокумент9 страницTermodinámica de gases ideales y primera leymarioОценок пока нет
- Ejercicio 29 PDFДокумент4 страницыEjercicio 29 PDFirvinОценок пока нет
- Hoja de Problemas #04Документ4 страницыHoja de Problemas #04Paul Quiroz AliagaОценок пока нет
- Cómo varía el volumen del aire al calentarloДокумент4 страницыCómo varía el volumen del aire al calentarloDAREN ATENCIAОценок пока нет
- Entropía y segunda ley de la termodinámicaДокумент6 страницEntropía y segunda ley de la termodinámicaRafael Quispe Velasquez0% (1)
- G3 BF1 003 U4 T2...Документ17 страницG3 BF1 003 U4 T2...Gaby PachecoОценок пока нет
- Un Gas en Un Cilindro Se Mantiene A Presión Constante de 2Документ1 страницаUn Gas en Un Cilindro Se Mantiene A Presión Constante de 2kevin alvarezОценок пока нет
- Ejemplos TermodinámicaДокумент13 страницEjemplos TermodinámicaGoku SayainОценок пока нет
- Química Analítica I: Dra. Norma Rodríguez LagunaДокумент65 страницQuímica Analítica I: Dra. Norma Rodríguez LagunaYazОценок пока нет
- Introducción A La Física Moderna PDFДокумент2 страницыIntroducción A La Física Moderna PDFiva nОценок пока нет
- Ejercicios 2da UnidadДокумент14 страницEjercicios 2da UnidadBrayan Gilberto López Conde100% (1)
- Taller 4 Termodinamica - 2019Документ5 страницTaller 4 Termodinamica - 2019Vane Gomez0% (2)
- Taller Primera Ley de La TermodinámicaДокумент3 страницыTaller Primera Ley de La TermodinámicaMaria Mercado0% (1)
- Taller 6Документ6 страницTaller 6William QuinchiaОценок пока нет
- Lista de Ejercicios 5 (F2) 22... SoluДокумент4 страницыLista de Ejercicios 5 (F2) 22... Soluyerald vega floresОценок пока нет
- Ex 2Документ6 страницEx 2wilson cortesОценок пока нет
- Problemas de física II: flujo, presión y difusiónДокумент2 страницыProblemas de física II: flujo, presión y difusiónEsteban Riveros RodriguezОценок пока нет
- Guiadefisica2 130617154642 Phpapp02Документ8 страницGuiadefisica2 130617154642 Phpapp02Ricky P RendonОценок пока нет
- EjerciciosДокумент2 страницыEjerciciosJane BerrioОценок пока нет
- Ejercicios Resueltos de Termodinamica PDFДокумент21 страницаEjercicios Resueltos de Termodinamica PDFMarco SánchezОценок пока нет
- Fisica IIIДокумент7 страницFisica IIIRonaldo Sarabia100% (1)
- Actividad 1. ElasticidadДокумент7 страницActividad 1. ElasticidadLina Tobias100% (1)
- Expansión térmica y transferencia de calorДокумент7 страницExpansión térmica y transferencia de calorJose Luis Claros ChoqueОценок пока нет
- Cálculos de conversión entre escalas de temperatura Celsius, Fahrenheit y KelvinДокумент5 страницCálculos de conversión entre escalas de temperatura Celsius, Fahrenheit y KelvinYarielis OramaОценок пока нет
- Guia TermoДокумент4 страницыGuia TermoMarcelo EstebanОценок пока нет
- Expansión Térmica y CalorimetriaДокумент1 страницаExpansión Térmica y CalorimetriaAnggie Maricel Acero Omana0% (1)
- Calores específicos molares de gases idealesДокумент19 страницCalores específicos molares de gases idealesIrak AGОценок пока нет
- Taller de Gases IdealesДокумент3 страницыTaller de Gases Idealespaula7acevedoОценок пока нет
- AA1 - UNIDAD 3 - Bryan YungaДокумент5 страницAA1 - UNIDAD 3 - Bryan YungaBryan YungaОценок пока нет
- Universidad Nacional de Chimborazo Trabajo FisicaДокумент6 страницUniversidad Nacional de Chimborazo Trabajo FisicaJohn Mejia Gallegos33% (3)
- Parcial Termodinamica 3... 2019 PDFДокумент12 страницParcial Termodinamica 3... 2019 PDFcristianОценок пока нет
- Bernoulli G 15Документ5 страницBernoulli G 15juan diego pertuz0% (1)
- Practica N01 Operaciones II 1Документ1 страницаPractica N01 Operaciones II 1DanielCarrascoОценок пока нет
- 1Документ9 страниц1Robert WilliamsОценок пока нет
- Practica de OndasДокумент4 страницыPractica de OndasRonny TavarezОценок пока нет
- Capitulo Iii Segundo Principio de La Termodinamica: Problemas de Maquina TérmicasДокумент14 страницCapitulo Iii Segundo Principio de La Termodinamica: Problemas de Maquina TérmicasCamilo Alcon100% (1)
- Ejercicios Propuestos - Actividad 4 - Fisica 2 - TemperaturaДокумент1 страницаEjercicios Propuestos - Actividad 4 - Fisica 2 - TemperaturaAles DiesroОценок пока нет
- Cap 9 13 35 40 41 42 55 64Документ6 страницCap 9 13 35 40 41 42 55 64WoldreidОценок пока нет
- Taller 3BДокумент4 страницыTaller 3BJULIAN DAVID NUNEZ GONZALEZОценок пока нет
- Universidad de La CostaДокумент2 страницыUniversidad de La CostaHarles Manuel Salazar Guerra0% (1)
- Parcial 3 Corte FisicaДокумент3 страницыParcial 3 Corte FisicaNixon Jeovanny RodriguezОценок пока нет
- Ejercicio 2 Física General Primera Ley de La TermodinámicaДокумент2 страницыEjercicio 2 Física General Primera Ley de La TermodinámicaBerzeck LopezОценок пока нет
- Transferencia de CalorДокумент11 страницTransferencia de CalorMaria JuliaОценок пока нет
- CAP - 4 1era Ley de La TermodinamicaДокумент4 страницыCAP - 4 1era Ley de La TermodinamicaSteven B-Roen100% (1)
- Problemas 1Документ4 страницыProblemas 1Nadal Vallespir FrauОценок пока нет
- Actividad 4.3 - Procesos TermodinámicosДокумент9 страницActividad 4.3 - Procesos TermodinámicosÁngel Ayala GonzalezОценок пока нет
- Problemas de RefrigeraciónДокумент4 страницыProblemas de RefrigeraciónJuan Pablo RosalesОценок пока нет
- Preguntas TermodinamicaДокумент8 страницPreguntas TermodinamicaAndrea Stephanie SanchezОценок пока нет
- Propiedades térmicas de gasesДокумент7 страницPropiedades térmicas de gasesCarlos Israel JimenezОценок пока нет
- Laboratorio Conductividad TermicaДокумент21 страницаLaboratorio Conductividad TermicaMateo RuizОценок пока нет
- Solucion Taller 3 PDFДокумент4 страницыSolucion Taller 3 PDFMarlonОценок пока нет
- Taller 1 Física 3Документ2 страницыTaller 1 Física 3Andres Barrero100% (1)
- Trabajo Practico PotencialДокумент2 страницыTrabajo Practico Potencialnazarena guerraОценок пока нет
- Fisica 2.unidad 3.Документ54 страницыFisica 2.unidad 3.Katelin TurmeroОценок пока нет
- Taller 1 de Fisica IiiДокумент17 страницTaller 1 de Fisica IiiAndreyGomez50% (2)
- Propiedades Térmicas de La Materia - ProblemasДокумент3 страницыPropiedades Térmicas de La Materia - Problemasnorma rojasОценок пока нет
- Problemas de Física 1 Semana 6Документ3 страницыProblemas de Física 1 Semana 6ALONSO CONDORI CORNEJOОценок пока нет
- Tallaer 4 TermoДокумент7 страницTallaer 4 TermoKeith Caicedo0% (1)
- Propuesta de Grado Paula Yepes y Mateo CartagenaДокумент8 страницPropuesta de Grado Paula Yepes y Mateo CartagenaCarlos MoscosoОценок пока нет
- Laboratorio de HidráulicaДокумент13 страницLaboratorio de HidráulicaCarlos MoscosoОценок пока нет
- Trabajo de DocumentaciónДокумент8 страницTrabajo de DocumentaciónCarlos MoscosoОценок пока нет
- Las Oscilaciones Caóticas y Las Tragedias de La InfraestructuraДокумент2 страницыLas Oscilaciones Caóticas y Las Tragedias de La InfraestructuraCarlos MoscosoОценок пока нет
- Trabajo Física Principio de ArquímedesДокумент7 страницTrabajo Física Principio de ArquímedesCarlos MoscosoОценок пока нет
- Taller de HIDRODINÁMICA 2Документ13 страницTaller de HIDRODINÁMICA 2Carlos MoscosoОценок пока нет
- Trabajo Física Principio de ArquímedesДокумент7 страницTrabajo Física Principio de ArquímedesCarlos MoscosoОценок пока нет
- Taller de HIDRODINÁMICAДокумент11 страницTaller de HIDRODINÁMICACarlos MoscosoОценок пока нет
- Laboratorio de HidráulicaДокумент13 страницLaboratorio de HidráulicaCarlos MoscosoОценок пока нет
- Ensayo Atentado A Las Torres Gemelas y Su Relación Con El Calor y La TemperaturaДокумент4 страницыEnsayo Atentado A Las Torres Gemelas y Su Relación Con El Calor y La TemperaturaCarlos MoscosoОценок пока нет
- Taller de HIDRODINÁMICAДокумент11 страницTaller de HIDRODINÁMICACarlos MoscosoОценок пока нет
- Guia Cap19 y 20Документ5 страницGuia Cap19 y 20victrexОценок пока нет
- Fuentes de Energia - 2023Документ5 страницFuentes de Energia - 2023lauraОценок пока нет
- Santana análisis Formación Agua NuevaДокумент131 страницаSantana análisis Formación Agua NuevaRamón F. Zapata SánchezОценок пока нет
- Servicios Auxiliares en La FermentaciónДокумент33 страницыServicios Auxiliares en La FermentaciónDANIELA PAOLA DIAZ PAJAROОценок пока нет
- Hoja de Datos de Seguridad Aceite RefrigeranteДокумент7 страницHoja de Datos de Seguridad Aceite RefrigeranteSST ClimatizaОценок пока нет
- Guía N°4 de Aprendizaje Física Grado 10°Документ10 страницGuía N°4 de Aprendizaje Física Grado 10°Andres BallestaОценок пока нет
- Tres Versiones Clásicas Sobre La Creación. Rosemary RadfordДокумент24 страницыTres Versiones Clásicas Sobre La Creación. Rosemary RadfordJaime Goyes AcostaОценок пока нет
- 1° Grado - Actividad Del Dia 30 de MayoxДокумент34 страницы1° Grado - Actividad Del Dia 30 de Mayoxadela porras liviaОценок пока нет
- Práctica - Oscar Trillo CuevasДокумент3 страницыPráctica - Oscar Trillo CuevasOscar Tr.Оценок пока нет
- Dia 1 Sem 28 - 1°. V°b°Документ2 страницыDia 1 Sem 28 - 1°. V°b°MinnieОценок пока нет
- Modelo Prueba (Algunas de Alternativa Múltiple y Términos Pareados)Документ3 страницыModelo Prueba (Algunas de Alternativa Múltiple y Términos Pareados)dannaeh gomez cortesОценок пока нет
- Biodeversidad en La Región de CajamarcaДокумент8 страницBiodeversidad en La Región de CajamarcaMily MarinОценок пока нет
- 6 PDFДокумент20 страниц6 PDFhgcu0% (2)
- Parametros GeotecnicosДокумент20 страницParametros GeotecnicosFabianSanchezKikeОценок пока нет
- ICA-1a QuimboДокумент92 страницыICA-1a QuimboMariela Méndez CОценок пока нет
- EstequiometríaДокумент11 страницEstequiometríaSteven Aleman100% (1)
- Planta de Cogeneración Eléctrica San CarlosДокумент19 страницPlanta de Cogeneración Eléctrica San CarlosJosé AlavaОценок пока нет
- Tarjetas Navideñas con Papel RecicladoДокумент19 страницTarjetas Navideñas con Papel RecicladoAnderson Joao MoranОценок пока нет
- INFORME Final Lab 03Документ6 страницINFORME Final Lab 03cristian Apaza palaciosОценок пока нет
- 2024 Almanaque MeteorologicoДокумент136 страниц2024 Almanaque MeteorologicoyarlindaОценок пока нет
- 1 Analisis DimensionalДокумент4 страницы1 Analisis Dimensionaljuan lunaОценок пока нет
- El Planeta 3.3.3.la TierraДокумент15 страницEl Planeta 3.3.3.la TierraSandraОценок пока нет
- Transmisión calor ejerciciosДокумент8 страницTransmisión calor ejercicioscedu126Оценок пока нет
- Fase 2 - Revisar El Aprovechamiento y Valorización de Residuos Sólidos ConvencionalesДокумент8 страницFase 2 - Revisar El Aprovechamiento y Valorización de Residuos Sólidos Convencionaleshenry fernandezОценок пока нет
- Act 2 GHCДокумент17 страницAct 2 GHCJosé Miguel Salazar Malave0% (1)
- Diferencias entre enfoques analítico y experimental de transferencia de calorДокумент4 страницыDiferencias entre enfoques analítico y experimental de transferencia de caloryair suarezОценок пока нет