Академический Документы
Профессиональный Документы
Культура Документы
Propiedades Coligativas
Загружено:
tatialinaОригинальное название
Авторское право
Доступные форматы
Поделиться этим документом
Поделиться или встроить документ
Этот документ был вам полезен?
Это неприемлемый материал?
Пожаловаться на этот документАвторское право:
Доступные форматы
Propiedades Coligativas
Загружено:
tatialinaАвторское право:
Доступные форматы
Propiedades coligativas
Las propiedades coligativas son sustancias que dependen del nmero de partculas que tiene la solucin. Numero de partculas se refiere a la cantidad de soluto que tenga, un ejemplo puede ser azcar con agua, el soluto es el agua y el agua el disolvente. (Acurdate de que las soluciones son soluto+solvente) Hay algunos conceptos que tienes que entender antes de conocer los 4 tipos de las propiedades coligativas. Uno de ellos es la presion de vapor, la cual es la presin que ejercen los gases de un liquido, no todos los lquidos tiene una misma presin de vapor. Otro concepto es la ebullicin, cuando algo ebull la presin de vapor (Acurdate que es la presin de vapor) del liquido de la solucin se iguala a la presin atmosfrica que es el ambiente en donde vivimos. Otro concepto es la evaporacin ocurre a temperatura ambiente, por ejemplo cuando uno deja el alcohol destapado y se va evaporando poco a poco a temperatura ambiente. Otros dos ms: Solutos voltiles, sus interacciones moleculares son deviles. Soluto voltil, sus interacciones moleculares son mas fuertes.
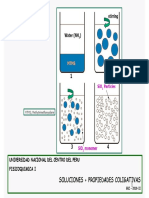
Ahora los 4 tipos de propiedades coligativas: 1) Descenso de la presin de vapor: como te dije antes la presin de vapor es la fuerza que ejercen los gases de un liquido, cada liquido tiene distintas presiones de vapor. Algunos tiene presiones de vapor ms altas y otros ms bajas. Para lograr que la presion de vapor disminuya hay que agregar soluto al lquido, y este tiene que ser no voltil para que las partculas del lquido no se muevan tanto. Como ves en la imagen las que tiene soluto no voltil que es esas pelotas rojas atrapan a las partculas celestes del agua. Pv= P x disolvente Esa formula la hizo Ralt, te la tienes que aprender nomas no aras ejercicios.
2) Aumento del punto de ebullicin: recordando que es la ebullicin, la presin de vapor se iguala a la atmosfrica, para eso tenemos que agregar un soluto que retarde tarde el punto de ebullicin y que despus ebulla a mas temperatura
Te = Ke m
Esa frmula solo te la aprendes de memoria. 3) Descenso del punto de congelacin: ocurre cuando la presin de vapor del liquido iguala a la presin de vapor del slido. El punto de congelacin de el agua pro ejemplo es 0 grados Celsius y si le agregamos sal ser a -4 grados Celsius, entonces esto quiere decir que tenemos que echar a la solucin un slido que retarde la congelacin a menor temperatura. 4) Presin osmtica: es aplicable a sistemas biolgicos. La presin osmtica es la fuerza que se opone al movimiento del agua, esta presin la ejerce el soluto. (Esta no la entiendo muy bien por eso solo aprndete de memoria esto.) Su frmula: = m R t
Ah estn todas, Camila es solo aprenderse de memoria esto enserio. No hay anda que entender.
Acido-Base
A) Acido: algo es asido cuando su escala de PH es del 1 al 6,9. Son electrolitos lo que significa que conducen la electricidad. Son cidos y corrosivos a veces. B) Bases: tambin llamados alcalinos jabonosas, conducen la electricidad.
Ejemplos por si preguntan en la prueba:
Teorias:
1) Arrenius:
ACIDOS: liberaran H que es hidrogeno, en agua H + CL si son mezclados con agua. Yo lo entiendo como que siempre ser al principio una H, es fcil. BASE: al mezclarse con agua liberaran OH que son hidroxilos. LiOH= Li + OH, siempre al final siempre es oh as que es fcil.
2) Brosted y locury: ACIDOS: liberan H BASES: Aceptan H
3) Lewis: ACIDOS: Aceptan un par de electrones BASES: liberan un par de electrones.
Вам также может понравиться
- Métodos de Separación de MezclasДокумент6 страницMétodos de Separación de MezclasEle Tejeiro GОценок пока нет
- Propiedades ColigativasДокумент25 страницPropiedades ColigativasJhoelVM vargasОценок пока нет
- Final Química General e Inorgánica 14-07-15Документ2 страницыFinal Química General e Inorgánica 14-07-15melОценок пока нет
- Clasificación de Las Reacciones QuímicasДокумент5 страницClasificación de Las Reacciones QuímicasPaula OlmosОценок пока нет
- Energía de Ionización, Afinidad Electrónica y ElectronegatividadДокумент12 страницEnergía de Ionización, Afinidad Electrónica y ElectronegatividadMariaPaulaGomezGuerreroОценок пока нет
- Oosmosis en El Huevo-Epistemologia R PDFДокумент24 страницыOosmosis en El Huevo-Epistemologia R PDFEver BlancoОценок пока нет
- Átomo y Sus ParticulasДокумент41 страницаÁtomo y Sus ParticulasKaryVelázquezОценок пока нет
- UnMundoFeliz MapasConceptualesДокумент19 страницUnMundoFeliz MapasConceptualesTinkyWinky100% (1)
- Práctica Densidades de MetalesДокумент4 страницыPráctica Densidades de MetalesFernandoОценок пока нет
- Soluciones Propiedades ColigativasДокумент75 страницSoluciones Propiedades ColigativasXiomara ACОценок пока нет
- Info Leyes Ponderales y EstequiometriaДокумент22 страницыInfo Leyes Ponderales y EstequiometriaJose Manuel Godoy LabarcaОценок пока нет
- Métodos VolumétricosДокумент287 страницMétodos VolumétricosMariОценок пока нет
- EstequiometriaДокумент7 страницEstequiometriaLeonelОценок пока нет
- Modelo Atómico de ThomsonДокумент6 страницModelo Atómico de ThomsonSantiago Mancheno100% (1)
- Laboratorio de Ósmosis - Virtual2 PDFДокумент7 страницLaboratorio de Ósmosis - Virtual2 PDFana maria villotaОценок пока нет
- Tipos de Enlaces QuímicosДокумент7 страницTipos de Enlaces QuímicosJessica De Jesus AlvaradoОценок пока нет
- Cuestionario de Laboratorio N°4Документ3 страницыCuestionario de Laboratorio N°4jjjbsОценок пока нет
- Soluciones QuimicasДокумент13 страницSoluciones QuimicasRaul FarfanОценок пока нет
- 2.1 La Reacción y La Ecuación QuímicaДокумент77 страниц2.1 La Reacción y La Ecuación QuímicaOctavio DaNoobОценок пока нет
- ANALÍTICA CLASES Química Analítica2007 IER SEMESTREДокумент68 страницANALÍTICA CLASES Química Analítica2007 IER SEMESTREEMMAZELОценок пока нет
- LABORATORIO DE SOLUCIONES ACUOSAS FinalДокумент6 страницLABORATORIO DE SOLUCIONES ACUOSAS FinalKAREN ANDREA BANOL RICOОценок пока нет
- Mezcla HeterogéneaДокумент17 страницMezcla HeterogéneaXiomara Ramirez FloresОценок пока нет
- MolaridadДокумент9 страницMolaridadEduardo KlintworthОценок пока нет
- Tarea Metodos de Separacion de MezclasДокумент2 страницыTarea Metodos de Separacion de MezclasMayerlis Gomez100% (1)
- Estequiometría de DisolucionesДокумент47 страницEstequiometría de DisolucionesAllen50% (2)
- Reglamento de Obras e Instalaciones Electricas-20!04!2011Документ6 страницReglamento de Obras e Instalaciones Electricas-20!04!2011gabrielОценок пока нет
- 2 Soluciones 6 PDFДокумент106 страниц2 Soluciones 6 PDFsebastian CarbajalОценок пока нет
- Soluciones QuímicasДокумент20 страницSoluciones QuímicasDavis LiveОценок пока нет
- Guía 1Документ20 страницGuía 1erikavasquez100% (1)
- Guia de Quimica Inorganica y Organica Labo - 3Документ63 страницыGuia de Quimica Inorganica y Organica Labo - 3Frank Alexander AtuncarОценок пока нет
- Introducción (Practica 2.6) ElectroquimicaДокумент7 страницIntroducción (Practica 2.6) ElectroquimicaMangelVillanuevaОценок пока нет
- Postulados de La RelatividadДокумент3 страницыPostulados de La RelatividadMario RodrigezОценок пока нет
- Clasificación de La MateriaДокумент4 страницыClasificación de La MateriaLux FernándezОценок пока нет
- Análisis PotenciometricoДокумент4 страницыAnálisis PotenciometricoMarianne Lugo BermanОценок пока нет
- Ej PHДокумент3 страницыEj PHRicardo OlguinОценок пока нет
- FUERZAS IntermolecularesДокумент14 страницFUERZAS IntermolecularesJavier Cerda InfanteОценок пока нет
- 5A Nomenclatura e Isomeria EstreucturalДокумент14 страниц5A Nomenclatura e Isomeria EstreucturallujulОценок пока нет
- La Materia VivienteДокумент3 страницыLa Materia VivienteeliotmonsterОценок пока нет
- Mary WollstonecraftДокумент1 страницаMary WollstonecraftnachitronОценок пока нет
- Regla de FasesДокумент22 страницыRegla de FasesSTEPHANY1214100% (1)
- Punto de Fusion y EbullicionДокумент14 страницPunto de Fusion y Ebullicionjeampol100% (1)
- Aminas UsosДокумент3 страницыAminas UsosAngela NuñezОценок пока нет
- Laboratorio 1Документ12 страницLaboratorio 1Edgar EspinozaОценок пока нет
- 1propiedades de Los Elementos Del Grupo 13 Al 16 de La TBPДокумент6 страниц1propiedades de Los Elementos Del Grupo 13 Al 16 de La TBPjorgeОценок пока нет
- AzeotroposДокумент5 страницAzeotroposIrene CuevasОценок пока нет
- Practica N°4 FermentacionДокумент11 страницPractica N°4 FermentacionALEXANDER ARCIAОценок пока нет
- Informe 6Документ6 страницInforme 6Döniel Boanerges Herrera Rayo50% (2)
- Celdas VoltaicasДокумент6 страницCeldas VoltaicasUvexclearОценок пока нет
- Aminoacidos Proteinas y Enzimas - Timberlake PDFДокумент36 страницAminoacidos Proteinas y Enzimas - Timberlake PDFgustavoОценок пока нет
- Sulfato de CobreДокумент17 страницSulfato de CobreArce Cruz MarcosОценок пока нет
- Examen Diagnostico Diagrama de Fases.Документ10 страницExamen Diagnostico Diagrama de Fases.Angel DoroteoОценок пока нет
- Ejercicio de Tabla PeriodicaДокумент2 страницыEjercicio de Tabla PeriodicaReymundo SeguraОценок пока нет
- Reflexionary Responder 1Документ2 страницыReflexionary Responder 1Angelica Ortiz100% (1)
- Fenomenos SuperficialesДокумент30 страницFenomenos SuperficialesFabián R ContrerasОценок пока нет
- Experimento 09 F. IntermolecularesДокумент8 страницExperimento 09 F. IntermolecularesAndrea G. ChОценок пока нет
- Intensidad de Corriente EléctricaДокумент17 страницIntensidad de Corriente EléctricaerickОценок пока нет
- Reporte #3 - Determinación Potenciométrica Del PHДокумент7 страницReporte #3 - Determinación Potenciométrica Del PHAlberto Palomares MuñozОценок пока нет
- Formación y Contaminación de PrecipitadosДокумент3 страницыFormación y Contaminación de PrecipitadosRoceli Acosta100% (1)
- Propiedades ColigativasДокумент8 страницPropiedades ColigativasKaren Santander RojasОценок пока нет
- INFORME Soluciones Propiedades ColigativasДокумент15 страницINFORME Soluciones Propiedades ColigativasAlexander Macedo0% (1)
- 5546iuxДокумент7 страниц5546iuxKaylam Salazar LópezОценок пока нет
- Titulaciones ComplejometricasДокумент6 страницTitulaciones Complejometricasmattyurrutia17Оценок пока нет
- Electromagnetismo - Acceso A La UniversidadДокумент333 страницыElectromagnetismo - Acceso A La UniversidadDiego Montero0% (1)
- UNIDAD 1. Cuadros SinopticosДокумент8 страницUNIDAD 1. Cuadros SinopticosHector Saul Hernandez NogueraОценок пока нет
- Ficha #2 - ArtefactosДокумент23 страницыFicha #2 - ArtefactosrafaeladaripizzornoОценок пока нет
- Guia Estados de La Materia 10°-2020Документ7 страницGuia Estados de La Materia 10°-2020Jennifer SantanaОценок пока нет
- Ciclos de GasДокумент32 страницыCiclos de Gasjuan Ahumada disponibleLJ6PM10PMОценок пока нет
- Informe No. 2 Quimica 1Документ5 страницInforme No. 2 Quimica 1Ángel OrozcoОценок пока нет
- Documento 2. Ecuaciones para UltrafiltracionДокумент8 страницDocumento 2. Ecuaciones para UltrafiltracionGuillermo duran becerraОценок пока нет
- Capítulo 1 Tipos y Propiedades de SuelosДокумент45 страницCapítulo 1 Tipos y Propiedades de SuelosShadyacОценок пока нет
- Sensor de Oxigeno Principios de FuncionamientoДокумент6 страницSensor de Oxigeno Principios de FuncionamientoING. Miguel Angel Sanchez MonzonОценок пока нет
- MSDS Aceite Hydra 68 LubraxДокумент9 страницMSDS Aceite Hydra 68 LubraxNaJo CasBarОценок пока нет
- Taller en ClasesДокумент2 страницыTaller en ClasesLuis Santiago Castro JaimesОценок пока нет
- Actividad de Puntos Evaluables - Escenario 2 - SEGUNDO BLOQUE-CIENCIAS BASICAS - FUNDAMENTOS DE QUIMICA - (GRUPO2) PDFДокумент6 страницActividad de Puntos Evaluables - Escenario 2 - SEGUNDO BLOQUE-CIENCIAS BASICAS - FUNDAMENTOS DE QUIMICA - (GRUPO2) PDFAndrés Cruz Herrera0% (1)
- PHD Thesis Atkinson-Miller RNOVELLA PDFДокумент347 страницPHD Thesis Atkinson-Miller RNOVELLA PDFalejandro_roldán_61Оценок пока нет
- Voltage Inducido en Una Espira GiratoriaДокумент16 страницVoltage Inducido en Una Espira Giratoriaandres atencioОценок пока нет
- Solucionario 1 - 28 Cap 12 Libro de FinnДокумент61 страницаSolucionario 1 - 28 Cap 12 Libro de FinnCesar Idvorsky Gutiérrez Cachique67% (3)
- Intercambio de Oxígeno y Dióxido de CarbonoДокумент3 страницыIntercambio de Oxígeno y Dióxido de CarbonoCarlos Beltran CОценок пока нет
- Aplicacion de La Mecanica de FluidosДокумент8 страницAplicacion de La Mecanica de Fluidosmijael cahuaya100% (1)
- Sol Tema 1Документ19 страницSol Tema 1leire100% (1)
- Análisis CacaoДокумент21 страницаAnálisis CacaoPaulandrea MoraОценок пока нет
- S 7.1metalurgia FísicaДокумент79 страницS 7.1metalurgia FísicaVictor LaosОценок пока нет
- Tablas RMN 13CДокумент5 страницTablas RMN 13CFernandoОценок пока нет
- Análisis InstrumentalДокумент7 страницAnálisis InstrumentalLuz CortésОценок пока нет
- Tratamiento Terciario de Aguas ResidualesДокумент9 страницTratamiento Terciario de Aguas ResidualesVictor Santa cruzОценок пока нет
- 1) ¿Por Qué El Motor Monofásico Asincrónico No Puede Arrancar Solo (No Tiene Cupla deДокумент25 страниц1) ¿Por Qué El Motor Monofásico Asincrónico No Puede Arrancar Solo (No Tiene Cupla deLaila KronebergerОценок пока нет
- Absorcion Via Oral PDFДокумент1 страницаAbsorcion Via Oral PDFLinda Carol Ruiz García0% (1)
- Propiedades Magnéticas de Los MaterialesДокумент18 страницPropiedades Magnéticas de Los MaterialesTatianaValentinaOrdoñezОценок пока нет
- LowryДокумент4 страницыLowryJonhy Garcia100% (1)
- Practica 9.solucionesДокумент3 страницыPractica 9.solucionesAlonzo Silva Santisteban PiedraОценок пока нет